Электрохимия, 2019, T. 55, № 8, стр. 948-960
Исследование влияния подложки из стеклоуглерода и активированной графитовой фольги на электрохимическое поведение композитных покрытий на основе полианилина и его N-замещенных производных
В. В. Абаляева a, *, Г. В. Николаева a, Е. Н. Кабачков a, О. Н. Ефимов a
a Учреждение Российской академии наук Институт проблем химической физики РАН
142432 Московская обл., Черноголовка, просп. академика Н.Н. Семенова, 1, Россия
* E-mail: avva@icp.ac.ru
Поступила в редакцию 08.10.2018
После доработки 23.11.2018
Принята к публикации 12.03.2019
Аннотация
Получены гибридные полимерные наноматериалы на основе полианилина (ПАни) и его N-замещенного поли-3,6-дианилин-2,5-дихлор-1,4-бензохинона (ПДАДХБ) в сочетании с оксидом графена (ОГ). Исследованы электрохимические свойства электродов, представляющих собой композитное полимерное покрытие на основе ПАни или ПДАДХБ (в сочетании с ОГ) на подложке из стеклоуглерода (СУ) и активированной графитовой фольги (АГФ). Показано, что на подложке из АГФ формируется структура электропроводящего нанокомпозитного материала с электрохимической емкостью, превышающей 1000 Ф/г, и стабильностью емкостных характеристик при значительном расширении интервала потенциалов в протонном (1 М H2SO4) электролите.
Список сокращений: ПАни – полианилин, Ан – анилин, ДАДХБ – мономер дианилиндихлорбензохинон, ПДАДХБ – полимер полидианилиндихлорбензохинон, ОГ – оксид графена, МК – муравьиная кислота, СУ – стеклоуглерод, АГФ – активированная графитовая фольга, ЭС – электрохимический синтез, ХС – химический синтез, АС – анилин сульфат, КЭ – композитный электрод.
Пять композитных электродов (КЭ) под номерами 1–5 описаны подробно в экспериментальной части.
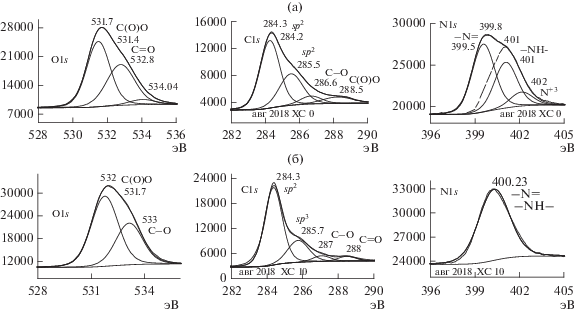
Обозначения для спектров РФЭС: ПАни-АГФ(ХС0) – КЭ ПАни-АГФ, полученный химическим синтезом ПАни и нанесенный на АГФ до всех испытаний, ПАни-АГФ(ХС10) – этот же КЭ, прошедщий все испытания, т.е. после ЦВА 10 и соответствующего зарядно-разрядного исследования.
1. ВВЕДЕНИЕ
Известно, что оксид графена оказывает значительное влияние на скорость и ход окислительной полимеризации анилинов (Ан) и производных анилина [1]. Практически сразу после открытия графена [2] выяснилось, что графеноподобные материалы – оксид графена и восстановленный оксид графена являются новыми типами углеродных электродных материалов в силу своих уникальных свойств: высокой площади поверхности [3], высокой проводимости для восстановленного оксида графена и доступности материалов [4]. Исследование возможных областей применения графеновых материалов привело к разработке био- и электрокаталитических устройств [5, 6], солнечных [7] и литий-ионных [8] батарей, электрохромных устройств [9] и т.д. Наиболее часто восстановленный оксид графена получают восстановлением оксида графена с использованием гидразина в качестве восстановителя [10].
В последнее время большой интерес стали вызывать углеродные материалы на основе терморасширенного графита (ТРГ). В НПО “Унихимтек” на основе фундаментальных исследований в области химии и физики интеркалированных соединений графита удалось реализовать полный технологический цикл переработки природного графита от его очистки до производства широкой номенклатуры углеродных материалов в виде фольги под товарным знаком Графлекс®. Благодаря высокой термостойкости, теплопроводности и хорошим прочностным свойствам графитовая фольга находит широкое применение в технике (теплозащитные материалы, сальниковые уплотнения и др.). Графитовая фольга обладает хорошей электропроводностью, низкой плотностью 1 г/см3, развитой поверхностью и однородной пористой структурой, образованной щелевидными мезопорами с характеристическим радиусом около 20 Å, и может быть использована в качестве подложки для модифицированных электродов [11]. В настоящей работе мы использовали графитовую фольгу в качестве подложки (токоотвода) для приготовления электродов, покрытых ПАни, и N-замещенным полианилина – ПДАДХБ. ЭС ПАни на СУ и АГФ был осуществлен путем окислительной электрополимеризации мономеров Ан и ДАДХБ для того, чтобы сравнить возможности получения электроактивных полимерных материалов двумя методами – химическим и электрохимическим синтезами.
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для создания композитных образцов была осуществлена электрохимическая и химическая полимеризации исследуемых полимеров на основе Ан и ДАДХБ на поверхности СУ и АГФ. Для приготовления рабочего графитового электрода использовали пластину ГФ толщиной 0.6 мм, которую подвергали анодной обработке в 0.1% (NH4)2SO4 при 3 В и 0.3 А в течение 1–5 мин. При этом поверхность ГФ становилась шероховатой. Полученную активированную графитовую фольгу (АГФ) промывали дистиллированной водой, сушили до постоянного веса и наносили на обе поверхности (СУ и АГФ) раствор исследуемого образца в МК. Электрохимический синтез (ЭС) ПАни проводили на поверхности подложки из 0.2 М раствора сульфата анилина в 1 М H2SO4 (АС). Все варианты подложек были тщательно высушены и взвешены до и после нанесения исследуемого материала для последующего расчета электрохимической емкости. ЭС ПАни на СУ и АГФ был осуществлен для того, чтобы показать возможности обеих подложек в сохранении активности композитного электрода при работе с ними в разных интервалах потенциалов. Были получены и изучены следующие композитные электроды:
1. КЭ1: ПАни–СУ получен путем ЭС ПАни на СУ.
2. КЭ2: ПАни–АГФ (ЭС) получен путем ЭС ПАни на АГФ.
3. КЭ3: ПАни–АГФ (ХС) получен путем предварительного химического синтеза ПАни и нанесения на поверхность АГФ покрытия ПАни из раствора в МК.
4. КЭ4: ДАДХБ–АГФ (ЭС). ДАДХБ – N-замещенный аналог ПАни, в котором два Ан фрагмента разделены молекулой хлоранила (ХА) (схема 1 ). Синтез этого мономера ДАДХБ(3) проводился по реакции алкилирования Ан (1) хлоранилом (2) в растворе диоксана при 15°С [12] с последующим нанесением этого мономера на поверхность АГФ и полимеризацией на поверхности при циклировании электрода в потенциодинамическом режиме.
Схема 1.
5. КЭ5: ПДАДХБ–ОГ–АГФ (ХС). Нанокомпозиты на основе полимеров ДАДХБ и ОГ получали в условиях окислительной полимеризации ДАДХБ в гетерофазной системе в присутствии ОГ [12]. Навеску ОГ (15 мас. % от массы мономера) обрабатывали ультразвуком 1.5 ч при охлаждении в 0.25 М растворе H2SO4. Затем добавляли необходимое количество мономера и снова обрабатывали ультразвуком 30 мин для его равномерного распределения в реакционном объеме. После вводили необходимое количество окислителя – персульфата аммония, отношение окислитель : мономер равно 1.25. Реакцию проводили в течение 4 ч при постоянной ультразвуковой обработке и охлаждении. Затем суспензию отфильтровывали, промывали сначала раствором 0.1 М H2SO4, затем водой, не допуская фильтрации досуха. Помещали влажную массу в 0.5 М раствор NH3 на 1 сут, после чего суспензию фильтровали и промывали водой (не досуха) до нейтральной реакции фильтрата. Конечный продукт представлял собой пасту. Перед нанесением покрытия на углеродную подложку пасту растворяли в муравьиной кислоте с образованием раствора ярко зеленого цвета [12]. Раствор хорошо впитывался поверхностью АГФ. Пропитку заканчивали, не допуская образования на поверхности свободной пленки. Затем электрод сушили до постоянного веса и по разности веса до и после пропитки определяли массу нанесенного материала.
ИК-фурье-спектры снимали на ИК-фурье-спектрометре Perkin Elmer Spectrum 100, оснащенном приставкой многократного нарушенного полного внутреннего отражения с германиевой призмой в диапазоне 4000–675 см–1. Сухие образцы помещали на призму приставки и фиксировали с помощью механического прижимного устройства.
РФЭС-спектры были сняты как спектры высокого разрешения С1s, O1s и N1s. Прибор – электронный спектрометр для химического анализа Specs PHOIBOS 150 MCD, рентгеновская трубка с магниевым анодом (MgKα-излучение 1253.6 эВ). При съемке спектров вакуум в камере спектрометра не превышал 3 × 10–9 мбар. Мощность источника составляла 225 Вт. Спектры регистрировались в режиме постоянной энергии пропускания (10 эВ для отдельных линий). Спектры отдельных линий записывались с шагом 0.05 эВ.
ЭС проводили в потенциодинамическом режиме из 0.2 М АС в 1 М H2SO4. Электрохимические исследования проводили в потенциодинамическом или в гальваностатическом режиме в интервале потенциалов –0.7…+1.3 В (относительно Ag/AgCl; все потенциалы в работе приведены относительно этого электрода сравнения) в трехкамерной стеклянной электрохимической ячейке (используемый объем электролита 15 мл) при комнатной температуре на потенциостате PS-7 (фирма Элинс, Россия). Рабочим электродом служила пластина АГФ или СУ размером 1 × 5 см, подготовленная для ЭС или с нанесенным нанокомпозитным покрытием (размер покрытия 1 × 1 см). Вспомогательным электродом служила СУ-пластина размером 1 × 5 см. Удельную электрохимическую емкость (Ф/г) рассчитывали по формуле Cm = it/ΔV, где i – удельная плотность тока (А/г), рассчитанная из веса композитной пленки на электроде; t – время разряда (с); ΔV – область потенциалов (В), в которой происходит разряд. При необходимости, например в ЭС, расчет вели также на единицу площади поверхности СS (Ф/см2).
3. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
3.1. КЭ1: ПАни–СУ. ЭС ПАни на СУ проводился в потенциодинамическом режиме из 0.2 М АС в 1 М H2SO4 в течение 40 циклов со скоростью 20 мВ/с в интервале потенциалов –200…+700 мВ. Общая цикловольтамперограмма (ЦВА) ЭС приведена на рис. 1а (ЦВА1). Для исследований электрод с синтезированным ПАни был извлечен из реакционного раствора, промыт дистиллированной водой и помещен в ячейку с 1 М H2SO4 (ЦВА2); Еа – Ек = 137 мВ. В этом электролите была исследована реакция композитного электрода ПАни–СУ на изменение интервала циклирования с расширением его в катодную и анодную стороны. На рис. 1б приведены ЦВА циклирования такого электрода с расширением интервала циклирования до –0.3, –0.4, –0.5 и –0.6 В. Зарядно-разрядные кривые, снятые после каждого из перечисленных интервалов циклирования показывают одинаковые времена разряда, из чего становится понятным, что количественных изменений при расчете СS практически не наблюдается. Во всех измеренных катодных интервалах СS = = 0.68 Ф/см2. Также постоянным для всех катодных интервалов остается катодный пик при 70 мВ, а анодный пик при увеличении катодного предела постоянно смещается в анодную сторону от 200 мВ при катодном пределе –200 до 225 мВ при катодном пределе –600 мВ. При увеличении катодного потенциала успевает восстановиться большее количество хиноидных фрагментов, и для их последующего окисления требуется большее количество времени, что и выражается в небольшом сдвиге анодного потенциала. На рис. 1в приведены ЦВА циклирования обсуждаемого электрода с расширением интервала циклирования в анодную сторону до 1100 мВ (ЦВА11).
Рис. 1.
(а) ЦВА 1 ЭС ПАни из 0.2 М АС на СУ; ЦВА2 после ЭС в 1 М H2SO4; (б) ЦВА ПАни–СУ в 1 М H2SO4 при разных катодных потенциалах; (в) ЦВА ПАни–СУ в 1 М H2SO4 при разных анодных потенциалах; (г) начальная и конечная (после всех испытаний) ЦВА ПАни–СУ, 1 М H2SO4 Ag/AgCl, 20 мВ/c.
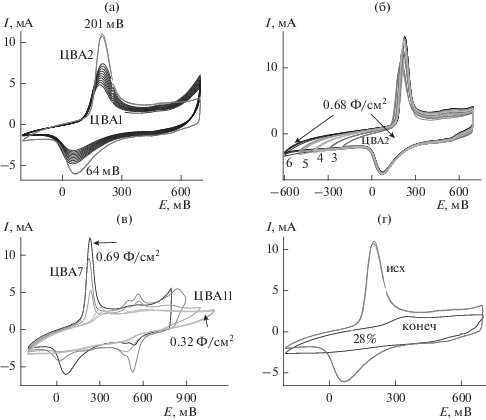
При этом сдвиг в анодном направлении на каждые 100 мВ значительно изменяет вид ЦВА для ПАни, и его электронная пара пиков перехода лейкоэмеральдин-эмеральдин практически сразу же после первых анодных продвижений исчезает вовсе. После каждого интервала циклирования были проведены зарядно-разрядные исследования для расчета СS. При зарядно-разрядных испытаниях резкое изменение времени разряда наблюдалось до 1 В, далее фарадеевская составляющая практически исчезает совсем из величины СS. И можно видеть, что емкость электрода уменьшилась более чем в два раза от 0.69 до 0.32 Ф/см2. Дальнейшее дополнительное восстановление системы с возвращением потенциала циклирования в катодную сторону не исправляет сложившуюся ситуацию.
3.2. КЭ2: ПАни–АГФ(ЭС). ЭС ПАни на АГФ проводился аналогично описанному ЭС для ПАни на СУ, но проходил значительно активнее. Ход такого ЭС показан на рис. 2а, из которого видно, что за 30 циклов ЭС на 1 см2 АГФ (сравнивая площади ЦВА рис. 1а и 2а) получено значительно большее количество полимера (ЦВА1, 2, 3 по 10 циклов каждая), чем за 40 циклов на 1 см2 СУ. Для исследований электрод с синтезированным ПАни был извлечен из реакционного раствора, промыт дистиллированной водой и помещен в ячейку с 1 М H2SO4 (ЦВА4); Еа – Ек = 340 мВ. В этом же электролите была исследована реакция КЭ Пани–СУ, описанная в предыдущем разделе, на изменение интервала циклирования с расширением его в катодную и анодную стороны. Для композитного электрода ПАни–АГФ после каждого интервала циклирования были проведены зарядно-разрядные испытания и рассчитана СS. Увеличения катодного потенциала до –400 мВ сохраняет пару – интенсивность и расположение фарадеевских пиков 1–1 '. Исходя из времени разряда (рис. 2в, разрядные кривые группы К), продвижение катодного потенциала до –400 мВ увеличивает значение СS от 0.76 до 0.84 Ф/см2, т.е. почти на 9%. Совсем другая картина наблюдается при заходе циклирования в анодную область после 700 мВ. Даже небольшое анодное увеличение на 100 мВ понижает высоту пиков 1–1 ' с одновременным появлением и резким ростом интенсивности второй пары пиков 2–2 '. При дальнейшем увеличении анодного потенциала происходит полное исчезновение первой пары пиков 1–1 ' и активный рост интенсивности второй пары пиков 2–2 '. Зарядно-разрядные кривые также можно разделить на две основные группы. Первая группа (рис. 2в, группа К) характеризует поведение композитного электрода, работающего в основной части циклирования (–200…+700 мВ) и с удалением в катодную область до –400 мВ. Вторая (рис. 2в, группа А), отличная от первой, характеризует зарядно-разрядные процессы композитного материала, вынужденного работать в интервалах после +800 мВ, т.е в той области, где обычный ПАни переокисляется и фактически (как это произошло с ПАни–СУ) теряет значительную часть своей СS. Расчет СS показывает, что во всем исследуемом интервале потенциалов изменения значений СS незначительны, и, несмотря на изменение вида ЦВА от –400 до +1100 мВ, значение СS от одной границы до другой изменяется всего на 9% от 0.88 Ф/см2 (максимум) до 0.8 Ф/см2 (в минимуме). Следует заметить, что дальнейшее продвижение циклирования в анодном направлении после 1100 мВ вызывало резкое уменьшение площади ЦВА и, соответственно, снижение значения С. Поэтому изучение этого интервала потенциалов (после 1100 мВ) в данной работе не проводилось. Последнее сравнение двух ЦВА (рис. 2г) – начальной (ЦВА4) и последней (ЦВА10) (после всех испытаний) в исходном интервале потенциалов (–200…+700 мВ) показывает потерю СS всего 5%.
Рис. 2.
(а) ЭС ПАни из АС (ЦВА1, 2, 3 – 10, 20, 30 циклов); ЦВА 4 – в 1 М H2SO4; (б) ЦВА4–6 – циклирование до катодных потенциалов –0.2, –0.3, –0.4 В; ЦВА7–10 – циклирование до анодных +0.8, +0.9, +1.1 В; (в) зарядно-разрядные кривые ПАни–АГФ: К – с заходом в катодную область, А – с заходом в анодную область; (г) сравнительные ЦВА начала и конца испытаний ПАни–АГФ.

3.3. КЭ3: ПАни–АГФ(ХС). Композит ПАни–АГФ (ХС) получали путем предварительного ХС ПАни и нанесения на поверхность АГФ покрытия из раствора полученного полимера в МК. Так как на поверхность АГФ нанесен уже готовый полимер, исследования начались с первых циклов. На рис. 3а показано поведение покрытия при постепенном увеличении катодного потенциала от –200 до –400 мВ. Практически все ЦВА повторяют друг друга за исключением первой ЦВА, показывающей один необратимый катодный пик ‒167 мВ, который в дальнейшем нигде не повторяется и относится, скорее всего, к необратимому восстановлению окисной группы самой подложки. Также все зарядно-разрядные кривые этой катодной серии (вкладка к рис. 3а) практически сливаются в одинаковые кривые заряда и разряда, показывая при этом практически для всех ЦВА одно и то же значение СS: 1172 Ф/г или 0.42 Ф/см2. Совсем другую картину можно наблюдать визуально при изменении границ циклирования в анодную сторону. Финальная картина изменения ЦВА при анодном увеличении границы циклирования показана на рис. 3б и соответствующий этому циклированию ход зарядно-разрядных кривых на рис. 3в. Здесь так же, как и в случае ЭС ПАни на АГФ, все зарядно-разрядные кривые делятся на две группы – катодную и анодную. При переходе (рис. 3д) от ЦВА1 (до +0.8 В) к ЦВА2 (до +0.9 В) наблюдается резкое уменьшение пары пиков А–А' и столь же резкое начало роста новой пары пиков В–В'. ЦВА3 (до +1 В) и все последующие ЦВА в анодном направлении уже практически не содержат пары пиков А–А'. К тому же в полимере при переходе от пары А–А' к паре В–В' значительно уменьшилось значение Еа‒Ек от 180 до 98 мВ, т.е. система становится более обратимой. В отличие от катодной, практически одинаковой для всех интервалов СS, при анодных испытаниях СS заметно зависела от анодного потенциала. После всех анодных исследований полимер сохранил (рис. 3г) почти 90% своей первоначальной СS. На рис. 3д подробно приведено изменение вида ЦВА в зависимости от интервала циклирования и также показаны значения СS, соответствующие меняющимся интервалам циклирования. На основании этих расчетов видно, что максимальным значением СS обладает полимер, находящийся в стадии перехода от пары пиков А–А' к паре В–В' (рис. 3д (ЦВА2)), т.е. когда обе эти формы присутствуют, или полимер находится в стадии перестройки.
Рис. 3.
(а) ЦВА ПАни–АГФ (ХС) с заходом в катодную область; вкладка – зарядно-разрядные кривые; (б) ЦВА ПАни–АГФ с заходом в анодную область; (в) зарядно-разрядные кривые ПАни–АГФ после соответствующих ЦВА; (г) ЦВА и Суд ПАни–АГФ (ХС) в начале (ЦВА1) и в конце испытаний (ЦВА8); (д) вид ЦВА в отдельно взятом интервале циклирования и рассчитанные для каждого интервала значения С.

РФЭС-спектры двух образцов – только что нанесенного ПАни-АГФ(ХС0) (рис. 4а) и прошедшего все испытания (ЦВА во всех интервалах и зарядно-разрядные циклы) – ПАни–АГФ(ХС10) (рис. 4б) приведены на рис. 4. Обычно N1s-спектр ПАни может быть разложен на три составляющих его кривые – относящиеся к хиноидной структуре, бензоидной структуре и положительно заряженному азоту или протонированному амину [13]. На рис. 4а (исходный образец, прошедший только ЦВА 1) в спектре N1s два главных пика 399.5–399.8 и 401 эВ относятся соответственно к хиноидному иминному и бензоидному аминному атомам азота. Третий пик 402 эВ относится к протонированному азоту. На рис. 3б видно, какое количество форм проходит ПАни в зависимости от условий циклирования (интервала потенциалов) и регулярных зарядно-разрядных исследований.
К концу всех испытаний полимерное покрытие электрода имеет РФЭС-спектр, показанный на рис. 4б. На этом спектре полностью отсутствуют все пики обозначенных трех форм N, которые присутствовали в полимере ПАни, нанесенном на АГФ до всех вариантов циклирования. Значение энергии связи 400.23 эВ является промежуточным значением между энергиями связи иминной и аминной форм N, но как можно заключить из литературных источников [14], такой пик более относится к аминной форме. Как уже отмечалось выше, система после всех катодно-анодных циклирований с нехарактерными для классического ПАни значениями Еа и Ек (рис. 3г, ЦВА8), стала достаточно устойчивой и более равновесной, практически сохраняя на всем протяжении испытаний величину Сm 1200–1300 Ф/г, а также за время испытаний потеряв лишь около 10% максимального значения С. В спектре O1s можно заметить, что после всех испытаний электрода количество связей С=О уменьшилось с 77% для ЦВА1 до 65% для ЦВА8. Пики связей С(О)ОН и С–ОН 531.4 и 531.7 эВ, наоборот, выросли. Уменьшение количества более окисленных форм в процессе испытаний может быть связано с акцепторной способностью [15] поверхности АГФ, на которой образуются донорно-акцепторные связи sp2 поверхности АГФ со структурами ПАни, обладающими донорными свойствами. В основе поверхностных структур АГФ лежат sp2-элементы, но как видно из спектров С1s, наблюдается и некоторое количество sp3-структур, которые могут присутствовать на поверхности АГФ в виде пыли или сажи, образующейся, возможно, при анодировании образца исходной графлексовой фольги. Их количество, как следует из спектров С1s ряда ЦВА8, значительно снижается к концу испытаний.
3.4. КЭ4: ДАДХБ–АГФ. В отличие от анилина мономер ДАДХБ при полимеризации в порах ГФ может обладать расклинивающим эффектом из-за присутствия объемных заместителей у атомов азота, что облегчает доступ электролита в электродный материал. Плохо растворяющийся в водных растворах органических и неорганических кислот ДАДХБ удалось растворить в ДМСО, из которого проводили пропитку поверхности АГФ для дальнейшей электрополимеризации. После всего цикла необходимых операций (пропитки, высушивания и взвешивания) было получено покрытие, пригодное для исследования. На первом же цикле в 1 М H2SO4 (ЦВА1 на рис. 5а) были зафиксированы нехарактерные для данного типа электродов два острых пика: 110 и 52 мВ. В процессе дальнейшего циклирования с изменением интервалов циклирования в анодную и катодную области эти два пика постепенно снижают свою интенсивность. Возможно, эти пики связаны с небольшими количествами ДМСО, которые могут остаться при просушке полимера, нанесенного на АГФ и удаляются из полимера при длительном циклировании в 1 М H2SO4. И в сравнительной конечной ЦВА13, повторяющей ЦВА1 (рис. 5в), этих пиков не видно совсем. Таким образом, при циклировании мономера ДАДХБ, нанесенного из ДМСО на АГФ, происходит полимеризация ДАДХБ. На первом цикле цикле (рис. 5а, ЦВА1) фактически снята ЦВА мономера, СS (по расчетам зарядно-разрядных испытаний) которого составляет 412 Ф/г. При дальнейшем циклировании как в анодном, так и в катодном интервале начинается активный рост пиков окисления-восстановления в районе Еа = 532 и Ек = 468 мВ, что может указывать на рост полимера.
Рис. 5.
(а) циклирование пленки ПДАДХБ из ДМСО на АГФ с заходом в катодную и анодную области; (б) зарядно-разрядные кривые ПДАДХБ–АГФ из ДМСО; (в) начальная и конечная ЦВА циклирования мономера ДАДХБ в 1 М H2SO4.

Рассчитанные из гальваностатических кривых заряда–разряда значения электрохимической емкости приведены на рис. 5а и 5б. Эти кривые, как и в случае покрытия ПАни на поверхности АГФ, также делятся на две группы (но уже не столь явно, как для ПАни) – катодную и анодную. Катодная группа зарядно-разрядных кривых, снимаемая каждый раз после очередного циклирования электрода с заходом в катодную область до –400 мВ, показывает прямолинейный зарядно-разрядный процесс без изгиба кривых. В то же время анодная группа в районе потенциалов +500 мВ (где и происходит основной окислительно-восстановительный процесс в полимере) показывает на месте изгиба кривых некоторое замедление скоростей окисления и восстановления. Таким образом, циклирование мономера ДАДХБ на поверхности АГФ приводит к его полимеризации с образованием ПДАДХБ. Отметим, что разность Еа – Ек = = 64 мВ (рис. 5в), указывает на равновесный фарадеевский процесс, протекающий на поверхности электрода.
3.5. КЭ5: ПДАДХБ–ОГ–АГФ. В этом случае для нанесения химически синтезированного ПДАДХБ на АГФ использовали влажную суспензию полимера, полученную в присутствии 15 вес. % ОГ. После растворения суспензии в МК полученный раствор хорошо впитывался поверхностью АГФ. На ЦВА подготовленного КЭ присутствует основная окислительно-восстановительная пара В (Еа 594 мВ и Ек 432 мВ) (рис. 6а), которая растет в последующих циклах. Происхождение пика А неясно, и при циклировании он исчезает.
Рис. 6.
(а) ЦВА композитного электрода ПДАДХБ–ОГ–АГФ в разных интервалах циклирования; (б) зарядно-разрядные кривые для разных интервалов циклирования композитного электрода ПДАДХБ–ОГ–АГФ; (в) начальная и конечная ЦВА композитного электрода ПДАДХБ–ОГ–АГФ.

После каждого интервала циклирований были сняты зарядно-разрядные кривые, из которых можно было рассчитать СS и Сm. Расчеты этих величин показали, что в интервале циклирования КЭ величины электрохимических емкостей остаются приблизительно одинаковыми в разных интервалах циклирования на протяжении от –600 до +1300 мВ. Разница между величинами емкости составляет 5%. Как следует из рис. 6в, после всех электрохимических испытаний конечная ЦВА этого электрода полностью воспроизводит по площади начальную ЦВА, т.е. в процессе всех испытаний КЭ сохранил свои емкостные характеристики на 100% в разных интервалах потенциалов.
4. ИК-СПЕКТРЫ ОТДЕЛЬНЫХ КОМПОЗИТНЫХ МАТЕРИАЛОВ
Полимерное покрытие, которое образуется на АГФ, очень прочно связано с подложкой. Это обусловлено впитыванием пропиточного раствора в поры АГФ, и только небольшая часть покрытия может находится в виде пленки на поверхности АГФ.
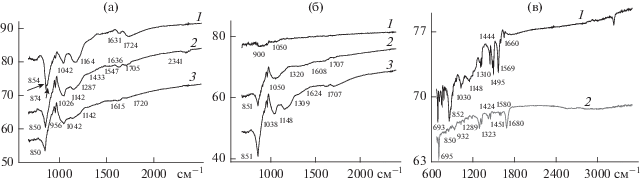
Поэтому ИК-спектры поверхности электродов могут быть обусловлены не только строением полимера, но отражать связи, которые полимер образует с АГФ, например в результате взаимодействия с кислородсодержащими группами на АГФ и π-стекинга ароматических систем полимера и АГФ. Полимеры, которые образуются или осаждаются на поверхности АГФ, вступают в π–π-взаимодействие своими хиноиминными звеньями с поверхностью АГФ. При этом происходит значительное снижение интенсивности характеристических пиков, а их полосы сдвигаются в длинноволновую область. На рис. 7а приведены ИК-спектры электрохимически синтезированного ПАни (раздел 3.2) на поверхности АГФ (спектр 1), проциклированного (спектр 2) с заходом в катодную область (рис. 2б, ЦВА4–7) и этого же образца (спектр 3), проциклированного с заходом в анодную область (рис. 2б, ЦВА8–11). В области 850–874 см–1 расположены полосы, характеризующие внеплоскостные С–Н-колебания ароматического кольца и деформацию хиноидного кольца [16, 17]. При анодном и катодном циклировании (спектры 2 и 3) интенсивность этих полос усиливается, что, возможно, связано с окислительно-восстановительными процессами в самом полимере и перераспределением бензоидно-хиноидных фрагментов. Полоса 1142–1164 см–1 характеризует наличие иминовых звеньев в хиноидных фрагментах [18]. Эта полоса максимально активна при ЭС ПАни (спектр 1), но в процессе различных циклирований ее интенсивность снижается (спектры 2, 3). Также с этим обстоятельством можно связать снижение интенсивности полосы 1724 см–1, которую можно отнести к наличию на поверхности АГФ кислородсодержащих групп. В процессе электрохимического циклировавния возможно образование внутренних водородных связей между СО- и NH-группами [19]. Во всех трех образцах имеются активные полосы в районе 1028–1042 см–1, которые являются характерными полосами сульфатных групп [20]. На рис. 7б приведены ИК-спектры АГФ (спектр 1) образца соскоба с поверхности АГФ после осаждения химически синтезированного ПАни из раствора МК на АГФ (спектр 2) и соскоба с такого электрода после всех проведенных циклирований и зарядно-разрядных исследований (спектр 3). АГФ после анодирования, которое проходит в H2SO4, показывает небольшой пик в районе 1030 см–1. Поверхность композитного электрода после процессов исследований (спектр 3) отличается от исходной значительно большей интенсивностью пика 851 см–1, также активным пиком 1148 см–1, содержащим в себе несколько полос в области 1100–1300 см–1, которые по данным [21] представляют иминные группы и хиноидные состояния ПАни, т.е нахождение полимера практически в окисленном состоянии после всех испытаний. Это может быть связано с более низкой степенью сопряжения в новом полимере либо из-за присутствия олигомерных структур, либо из-за адсорбции на поверхности АГФ не чистого полимера (при ЭС), а его раствора в МК. По данным некоторых исследователей, полоса 1148 см–1 соответствует структуре ПАни N=Q=N [22]. На рис. 7в приведены два ИК-спектра (спектр 1) ПДАДХБ–ОГ (до всех испытаний) и (спектр 2) ПДАДХБ–ОГ, осажденного на АГФ из МК и прошедшего все электрохимические испытания. Сопоставление ИК-спектров этих образцов ПДАДХБ–ОГ и ПДАДХБ–ОГ (покрытия на АГФ) показало наличие полос валентных колебаний С–С-связей хиноидного и бензоидного колец в области 1580 и 1490 см–1, соответственно – более активных в чистом образце (спектр 1) и менее активных в покрытии на АГФ (спектр 2). Полоса в области 1675 см–1 характеризует хиноидную структуру хлоранила [23] и взаимодействие хиноидных звеньев ХА фрагментов полимеров как с ОГ, так и с поверхностью АГФ [19]. Причем, такое взаимодействие в композитном материале значительно убедительнее в виде полосы 1690 см–1. Деформация хиноидного фрагмента, которая характеризуется в спектре 1 пиком 852 см–1 на поверхности АГФ, практически исчезает. Но связь С–Cl в ХА-фрагменте проявляется пиком 693 см–1 [19] и в чистом материале (спектр 1) и в композите, осажденном на АГФ (спектр 2).
5. ЗАКЛЮЧЕНИЕ
Обнаружено принципиальное различие в электрохимическом поведении покрытий из Пани и N-замещенных Пани – ПДАДХБ при нанесении на гладкую поверхность СУ и шероховатую пористую поверхность АГФ (табл. 1). В результате анодной активации графитовой фольги образуются поверхностные поры с кислородсодержащими группами, поверхность АГФ становится полярной и хорошо впитывает растворы мономеров и полимеров в муравьиной кислоте. При циклировании в потенциодинамическом режиме наблюдается полимеризация мономеров с частичным восстановлением кислородсодержащих групп АГФ.
Таблица 1.
Результаты электрохимического исследования пяти КЭ
| Электрод | Интервал исследуемых потенциалов | С, Ф/г | С, Ф/см2 | А/см2 | % сохранения электрохимических характеристик в процессе всего исследования |
|---|---|---|---|---|---|
| КЭ1 ПАни–СУ(ЭС) |
–0.2…+0.9 | 0.68–0.28 | 0.5–1 | 23 | |
| КЭ2 ПАни–АГФ (ЭС) |
–0.4…+1.1 | 1.46–1.55 | 2–3 | 95 | |
| КЭ3 ПАни–АГФ (ХС) |
–0.4…+1.2 | 1100–1350 | 0.47–0.52 | 2–3 | 90 |
| КЭ4 ДАДХБ–АГФ(ЭС) |
–0.4…+1.2 | 0.32–0.39 | 2–3 | Мономер → полимер 130 |
|
| КЭ5 ПДАДХБ–ОГ(ХС) |
–0.6…+1.3 | 360–400 | 0.39 | 2–3 | 100 |
Наиболее высокую емкость 1100–1350 Ф/г и хорошую стабильность при циклировании показал электрод КЭ3 ПАни–АГФ (ХС), полученный пропиткой АГФ из раствора химически синтезированного ПАни в муравьиной кислоте.
Следует отметить высокую обратимость электродных процессов для электродов КЭ4 ДАДХБ–АГФ(ЭС) и КЭ5 ПДАДХБ–ОГ(ХС), для которых значение Ea – Eк составляло соответственно 80 и 64 мВ, в то время как показатели этих значений для полианилиновых электродов КЭ 1 и 2 составляли 300 и 107 мВ, что может быть связано с плотной упаковкой полимерных цепей. Присутствие объемных заместителей в N-положении для ПДАДХБ препятствует такой упаковке. В то же время разрыхление полимерного покрытия улучшает ионный транспорт. Важную роль может играть и тесный контакт одиночных цепей ПДАДХБ с графитовой матрицей для транспорта электронов. В целом многофазное строение нанокомпозитного покрытия стабилизирует пористую структуру поверхностного электродного слоя.
АГФ представляет собой новый перспективный материал для создания электродов для суперконденсаторов на основе доступной промышленной графитовой фольги. Такие электроды не требуют внесения токопроводящих добавок и инертных связующих. Низкая плотность ГФ (около 1 г/см3) создает дополнительные преимущества перед металлическими токоотводами. Наконец достигается более широкий интервал потенциалов заряда–разряда. Наряду с электроактивными полимерами АГФ можно использовать в качестве подложки, которая включает неорганические материалы, такие как оксид ванадия, сложные оксиды и др. для катодов суперконденсаторов и литий-ионных аккумуляторов.
Дальнейшие исследования электродных материалов на основе АГФ в сочетании с электроактивными полимерами позволят расширить и уточнить представления о взаимодействии компонентов электродов и механизме электрополимеризации в порах графеноподобных материалов, к которым предположительно можно отнести и АГФ.
Таким образом, имеется широкий выбор достоинств изученных КЭ, которые могут быть использованы в разрабатываемом изделии в зависимости от поставленной цели.
Список литературы
Chen, W. and Mu, Sh., The electrocatalytic oxidative polymerizations of aniline and aniline derivatives by grapheme, Electrochim. Acta, 2011, vol. 56, p. 2284.
Novoselov, K.S., Geim, A.K., Morozov, S.V., Jiang, D., Zhang, Y., Dubonos, S.V., Grigorieva, I.V., and Firsov, A.A., Electric Field Effect in Atomically Thin Carbon Films, Science, 2004, vol. 306, p. 666.
Peigney, A., Laurent, C., Flahaut, E., Bacsa, R.R., and Rousset, A., Specific surface area of carbon nanotubes and bundles of carbon nanotubes, Carbon, 2001, vol. 39, p. 507.
Geim, A.K. and Novoselov, K.S., The rise of grapheme, Nat. Mater. 2007, vol. 6, p. 183.
Hong, W.J., Bai, H., Xu, Y.X., Yao, Z.Y., Gu, Z.Z., and Shi, G.Q., Preparation of Gold Nanoparticle Graphene Composites with Controlled Weight Contents and Their Application in Biosensors, J. Phys. Chem. C, 2010, vol. 114, p. 1822.
Wang, L., Tian, C.G., Wang, H., Ma, Y.G., Wang, B.L., and Mass, H.G., Production of Graphene via an in situ Self-Generating Template Route and Its Promoted Activity as Electrocatalytic Support for Methanol Electroxidization, J. Phys. Chem. C., 2010, vol. 114, p. 8727.
Hong, W.J., Xu, Y.X., Lu, G.W., Li, C., and Shi, G.Q., Transparent graphene/PEDOT–PSS composite films as counter electrodes of dye-sensitized solar cells, Electrochem. Commun. 2008, vol. 10, p. 1555.
Choi, D.W., Wang, D.H., Viswanathan, V.V., Bae, I.T., Wang,W., Nie, Z.M., Zhang, J.G., Graff, G.L., Liu, J., Yang, Z.G., and Duong, T., Li-ion batteries from LiFePO4 cathode and anatase/graphene composite anode for stationary energy storage, Electrochem. Commun., 2010, vol. 12, p. 378.
Zhao, L., Zhao, L., Xu, Y.X., Qiu, T.F., Zhi, L.J., and Shi, G.Q., Polyaniline electrochromic devices with transparent graphene electrodes, Electrochim. Acta, 2009, vol. 55, p. 491.
Gilje, S., Han, S., Wang, M.S., Wang, K.L., and Kaner, R.B., A Chemical Route to Graphene for Device Applications, Nano Lett., 2007, vol. 7, p. 3394.
Shornikova, O.N., Kogan, E.V., Sorokina, N.E., and Avdeev, V.V. The Specific Surface Area and Porous Structure of Graphite Materials Russian J. Phys. Chem. A. 2009. vol. 83, no. 6. p. 1022. [Шорникова, О.Н., Коган, Е.В., Сорокина, Н.Е., Авдеев, В.В. // Журн. Физ. Химии. 2009, Т. 83. № 6. С. 1161].
Abalyaeva, V.V., Nikolaeva, G.V., Kabachkov, E.N., Kiseleva, S.G., Orlov, A.V., Efimov, O.N., and Karpacheva, G.P., Obtainment and Comparative Study of Electrochemical Behavior of Composite Electrodes Based on Polyaniline and Its N-Substituted Derivatives, Polymer Science, Series B, 2018, vol. 60, no. 6, p. 777. [Абаляева, В.В., Николаева, Г.В., Кабачков, Е.Н., Киселева, С.Г, Орлов А.В., Ефимов, О.Н, Карпачева, Г.П. Высокомолек. Соед., Сер. Б, 2018, Т. 60. № 6. С. 511.]https://doi.org/10.1134/S1560090418060015
Gu, H., Su, X., and Loh, K.P., Electrochemical Impedance Sensing of DNA Hybridization on Conducting Polymer Film-Modified Diamond, J. Phys. Chem. B, 2005, vol. 109, p. 13611.
Patil, D.S., Pawar, S.A., Devan, R.S., Mal, S.S., Gang, M.G., Ma, Y.R., Hong, C.K, Kim, J.H., and Patil, P.S., Polyaniline based electrodes for electrochemical supercapacitor: Synergistic effect of silver, activated carbon and polyaniline, J. Electroanalyt. Chem., 2014, vol. 724, p. 21.
Zhaoa, B., Liua, P., Jianga, Y., Taob, H., Songa, J., Fanga, T., and Xua, W., Supercapacitor performances of thermally reduced graphene oxide, J. Power Sources, 2012, vol. 198, p. 423.
Kieffel, Ya., Travers, J.P., Ermolieff, A., and Rouchon, D., Effect of chemical degradation one electrical properties, J. Appl. Polym. Science, 2002, vol. 86, p. 395.
Lindfors, T., Kvarnström, C., and Ivaska, A., Raman and UV–vis spectroscopic study of polyaniline membranes containin gabulky cationic additive, J. Electroanalyt. Chem., 2002, vol. 518, is. 2, p. 131.
Dhibar, S., Sahoo, S., and Das, C.K., Copper chloride-doped polyaniline/multiwalled carbon nanotubes nanocomposites: Superior electrode material fo rsupercapacitor applications, Polymer composites, 2013, vol. 34, is. 4, p. 517.
Refat, M.S., Ibrahim, O.B., Al-Didamony, H., El-Noir, K.M.A., and El-Zayat, L., Spectroscopic and thermal studies on the charge transfer complexes formed between morpholine as donor with p-chloranil and 7,7′,8,8′-tetracyanoquinodimethane, J. Saudi Chem. Soc., 2012, vol. 16, p. 227.
Qiu-Feng, L., Huang, M.-R., and Li, X.-G., Synthesis and Heavy-Metal-Ion Sorption of Pure Sulfophenylenediamine Copolymer Nanoparticles with Intrinsic Conductivity and Stability, Eur. J., 2007, vol. 13, p. 6009.
Trchova, M., Moravkova, Z., Blaha, M., and Stejskal, J., Raman spectroscopy of polyaniline and oligoaniline thin films, Electrochim. Acta, 2014, vol. 122, p. 28.
Wang, Y., Wu, X., Zhang, W., Li, J., Luo, Ch., and Wang, Q., Fabrication and enhanced electromagnetic wave absorption properties of sandwich-likegrapheme @ NiO @ PANI decorated with Ag particles, Synth. Met., 2017, vol. 229, p. 82.
Trchova, M. and Stejskal, Ja., Polyaniline: The infrared spectroscopy of conducting polymer nanotubes, Pure Appl. Chem., 2011, vol. 83, p. 1803.
Дополнительные материалы отсутствуют.