Электрохимия, 2020, T. 56, № 11, стр. 1042-1056
Модификации сепараторов для Li–S-аккумуляторов с улучшенными электрохимическими характеристиками
Д. Ян a, С. Сион a, Ю. Жу a, Ю. Чен a, Л. Фу a, Й. Жан a, Ю. Ву a, *
a Нанкинский технологический университет
211816 Нанкин, КНР
* E-mail: wuyp@njtech.edu.cn
Поступила в редакцию 04.05.2019
После доработки 16.05.2019
Принята к публикации 14.09.2019
Аннотация
Литий-серные (Li–S) аккумуляторы принято рассматривать, как одну из перспективных вторичных систем для запасания энергии следующего поколения. Однако их практическое применение ограничивается такими запутанными проблемами, как электрически изолирующая природа серы, челночный перенос и образование литиевых дендритов. Легкий и недорогой способ решения трех вышеприведенных проблем, имеющий большие преимущества перед другими и существенно улучшающий эксплуатационные характеристики Li–S-аккумуляторов – это модифицирование сепараторов. В настоящей работе мы даем обзор недавних успехов в создании сепараторов для Li–S-аккумуляторов, включая различные покрытия, углеродистые материалы, полимеры и неорганические материалы, и разработку многоцелевых гелевых сепараторов для усовершенствования работы Li–S-аккумуляторов. Также обсуждаются значение и пути развития функциональных сепараторов для дальнейшей коммерциализации Li–S-аккумуляторов.
ВВЕДЕНИЕ
По мере того, как проблема загрязнения окружающей среды становится все острее, обостряется и стремление человечества к чистой энергии [1–3]. В то же время ключом к решению проблемы является поиск соответствующих систем для запасания энергии. Чересчур низкая теоретическая емкость катодов из оксидов переходных металлов обычных литий-ионных аккумуляторов едва ли позволит им удовлетворить все растущие требования человечества к материалам [4, 5]. Литий-серные (Li–S) аккумуляторы принято рассматривать как одну из перспективных вторичных систем для запасания энергии следующего поколения из-за их высокой теоретической емкости (1675 мА ч г–1) и удельной энергии (2600 Вт ч кг–1) [6–8]. А сочетание таких характеристик, как безопасность, большие природные запасы и низкая стоимость элементной серы, позволяет считать Li–S-аккумуляторы идеальной альтернативой литий-ионным аккумуляторам на будущее [9–12]. Однако у них существуют критичные проблемы, такие как недостаток электронной проводимости серы, челночный перенос и образование литиевых дендритов, которые ограничивают их разработку [13, 14]. Среди этих проблем одна из наиболее критичных – челночный перенос полисульфидов, который постепенно приводит к потере активного материала и коррозии литиевых анодов и, таким образом, к падению емкости Li–S-аккумулятора [15].
Для решения вышеперечисленных проблем использовали разные способы; наиболее широко применяемый метод – это организация строения материала S-катода. Для улучшения характеристик Li–S-аккумуляторов испробовали множество материалов, таких как углеродистые материалы [16–21], проводящие полимеры [22–27], оксиды и сульфиды металлов [28–31]. Однако, следует отметить, что такая организация строения материала часто требует сложных синтезов и трудных процедур, что неизбежно увеличивает затраты времени и цену, затрудняя коммерциализацию Li–S-аккумулятора.
Не так давно был найден еще один перспективный способ оптимизации работы Li–S-аккумулятора: модифицирование сепаратора, благодаря тому, что этот путь прямой и эффективный [32, 33]. Дополнительно, по сравнению с устройством катода, часто сопровождаемым расходом запасенной серы, это модифицирование сепаратора дает возможность большего запасания серы в катоде. В настоящем обзоре мы суммируем успехи в модифицировании сепараторов для Li‒S-аккумулятора при сохранении хорошей циклируемости. Бóльшая часть таких модификаций основана на использовании коммерческих полиолефиновых сепараторов и других материалов, таких как углеродистые материалы [34–38], полимеры [39–42], неорганические материалы [43–45] и их композиты [46, 47] – все они использовались с целью усовершенствовать эти полиолефиновые сепараторы. Кроме того, для улучшения работы Li–S-аккумуляторов применяются функциональные гелевые полимерные сепараторы [48–55]. Благодаря успешному развитию модифицирования сепараторов в последние годы, достигнуты значительные успехи в улучшении работы Li–S-аккумуляторов. С учетом уникальных преимуществ этого направления, модифицирование сепараторов может стать мощным методом для дальнейшего продвижения коммерциализации Li–S-аккумулятора.
МОДИФИЦИРОВАНИЕ КОММЕРЧЕСКИХ СЕПАРАТОРОВ
Модифицирование коммерческих сепараторов – это наиболее перспективный путь для реализации высокопроизводительных Li–S-аккумуляторов ввиду его простоты и эффективности. Для создания коммерческого сепаратора применяются различные материалы, они демонстрируют большие преимущества в улучшении эксплуатационных характеристик Li–S-аккумулятора. В табл. 1 сведены воедино недавние успехи в модифицировании коммерческих сепараторов для Li‒S-аккумулятора; детали будут обсуждаться далее.
Таблица 1.
Сводка результатов модифицирования коммерческих сепараторов для Li–S-аккумулятора
| Класс материала | Модификаторы | Содержание серы, мг cм–2 | Число циклов и скорость (1 C = 1675 мA г–1) | Емкость, мА ч г–1 | Ссылка |
|---|---|---|---|---|---|
| Углеродистые материалы | Углеродные нанотрубки | 2 | 300 (1 C) | 621 | [37] |
| Углерод Super P | 1.1–1.3 | 200 (0.2 C) | 828 | [35] | |
| Оксид графена | 1–1.5 | 100 (0.1 C) | 708 | [38] | |
| Углеродные сферы | 3 | 100 (0.2 C) | 730 | [56] | |
| Неорганические материалы | Al2O3 | 1.6 | 50 (0.2 C) | 593.4 | [43] |
| SiO2 | 1.2–1.4 | 200 (0.2 C) | 603.5 | [44] | |
| SnO2 | 1 | 500 (0.2 C) | 423.2 | [45] | |
| MoS2 | – | 600 (0.5 C) | 401 | [57] | |
| Co9S8 | 2 | 1000 (1 C) | 530 | [58] | |
| Полимеры | Нафион | 0.53 | 500 (1 C) | 468.6 | [40] |
| Полиакриловая кислота | 1.2 | 600 (0.5 C) | 311 | [42] | |
| Поли (p-стиролсульфонат) натрия | 1.8–2.2 | 20 (0.2 C) | 600–700 | [41] | |
| Композиты | Полиэтилен оксид/Нафион/Super P | 0.98 | 300 (1 C) | 770 | [46] |
| Al2O3/оксид графена | 0.75 | 100 (0.2 C) | 804.4 | [47] | |
| Полимер с металлокаркасной структурой/углеродные нанотрубки | 2 | 300 (0.2 C) | 1183 | [59] |
Сепараторы, модифицированные углеродистыми материалами
Изолирующая природа серы – вот основное препятствие, ограничивавшее развитие Li–S-аккумуляторов на его ранней стадии. Углеродистые материалы обычно имеют хорошую электронную проводимость. Применяемые в качестве модификатора сепараторов, углеродистые материалы способствуют электронному переносу и реактивируют соединения серы в процессе заряда–разряда, что может повысить эффективность использования серы. Кроме того, углеродистые материалы могут сыграть роль барьера и физически блокировать челночный перенос полисульфидов. Поэтому углеродистые материалы сделались наиболее популярными при модифицировании сепараторов Li–S-аккумулятора.
Углеродные нанотрубки обладают большой удельной площадью поверхности и множеством каналов электронного переноса, что делает их хорошим “хозяином” для соединений серы при применении в Li–S-аккумуляторах [60–62]. Сепаратор, модифицированный многостенными углеродными нанотрубками, был изготовлен для Li–S-аккумулятора с высокими эксплуатационными характеристиками (рис. 1a и 1б) [37]. Многостенные углеродные нанотрубки были диспергированы под действием ультразвука в изопропиловом спирте и отфильтрованы под вакуумом на поверхность сепаратора Celgard 2500. Эти нанотрубки равномерно прилипли к сепаратору Celgard 2500. Исследование композитного сепаратора, подвергнутого циклированию: большое количество серы оказалось равномерно распределено по поверхности многостенных углеродных нанотрубок, и это показывает, что многостенные углеродные нанотрубки предоставляют множество мест для протекания реакций с участием соединений серы и могут реактивировать промежуточные соединения. Li–S-аккумулятор с катодом из чистой серы и с сепаратором, покрытым многостенными углеродными нанотрубками, имеет высокую начальную емкость 1324 мА ч г–1 при скорости заряда–разряда (0.2 C) и хорошую циклируемость в течение 300 циклов при скорости 1 C. По сравнению с ним Li–S-аккумулятор с обычным сепаратором показал низкую емкость при различных плотностях тока, и это показывает, что многостенные углеродные нанотрубки эффективно улучшают эксплуатационные характеристики Li–S-аккумуляторов. Углерод Super P с высокой проводимостью тоже используется в Li‒S-аккумуляторах (рис. 1в и 1г) [35]. Свойства Super P похожи на свойства многостенных углеродных нанотрубок; он тоже улучшает эксплуатационные характеристики Li–S-аккумуляторов при различных плотностях тока. Li–S-аккумулятор с углеродом Super P способен сохранять свою емкость на 86% в течение месяца, в то время как Li–S-аккумулятор с обычным сепаратором сохраняет лишь 49% своей первоначальной емкости. Это показывает, что углерод Super P может существенно снизить саморазряд Li–S-аккумулятора благодаря предотвращению челночного переноса.
Рис. 1.
Сепараторы для Li–S-аккумулятора, модифицированные углеродистыми материалами: (a) схема механизма функционирования сепаратора в Li–S-аккумуляторе, покрытого многостеннымих углеродными нанотрубками, и (б) морфология поверхности слоя многостенных углеродных нанотрубок после циклирования и соответствующая “карта”, полученная методом энергорассеивающей рентгеновской спектроскопии [37] (воспроизводится с разрешения © 2014, American Chemical Society); (в) схема механизма функционирования сепаратора в Li–S-аккумуляторе, покрытого Super P, и (г) морфология поверхности слоя Super P после циклирования и соответствующая “карта”, полученная методом энергорассеивающей рентгеновской спектроскопии [35] (воспроизводится с разрешения © 2014, Wiley-VCH Verlag GmbH & Co. KGaA); (д) схема механизма функционирования сепаратора в Li–S-аккумуляторе, покрытого графеном, и (е) анализ методом рентгеновской фотоэлектронной спектроскопии оксида графена, диспергированного в воде и органическом растворителе [38] (воспроизводится с разрешения © 2015, American Chemical Society); (ж) схема механизма подавления диффузии полисульфидов в сепараторе, покрытом полыми углеродными сферами, (з) процесс приготовления полых углеродных сфер и (и, к) соответствующие SEM-микрофотографии полученных полых углеродных сфер [56] (воспроизводится с разрешения © 2018, Royal Society of Chemistry).

Как типичный двумерный (2D) материал с разнообразными хорошими свойствами, графен широко используется для модифицирования сепараторов Li–S-аккумуляторов [63, 64]. В Li–S-аккумуляторе применяли и сепаратор, модифицированный оксидом графена, Он был приготовлен осаждением оксида графена, полученного по методу Хаммерса (Hummers), с помощью фильтрования на сепаратор Celgard 2400 (рис. 1д и 1е) [38]. Свежеприготовленный оксид графена содержит множество кислородных функциональных групп и дает возможность приготовить сепаратор с избирательной проницаемостью, который позволяет переносить ионы лития, но блокирует перенос анионов полисульфидов. Такой Li–S-аккумулятор с избирательно проницаемым сепаратором демонстрирует улучшение кулоновской эффективности до 95–98% при скорости 0.1 C, в сравнении с 67–75% у аккумулятора с обычным сепаратором. Помимо этого, сепаратор, модифицированный оксидом графена, снижает потери в циклируемости с 0.49 до 0.23% за цикл при скорости заряда–разряда 0.1 C. Такой избирательно проницаемый сепаратор может создавать как физические, так и химические препятствия для полисульфидов. У Li–S-аккумулятора с сепаратором, модифицированным оксидом графена, гораздо меньшнй саморазряд; его напряжение разомкнутой цепи остается постоянным выше 2.3 В в течение 30 ч, в то время как напряжение разомкнутой цепи аккумуляторов с изначальным сепаратором резко спадает ниже 2.2 В уже после 5 ч. Оксид графена используют для модифицирования сепаратора и при конструировании катода и в то же время для изучения положительных эффектов, оказываемых оксидом графена [65]. Полученные результаты показывают, что количество полисульфидов в сепараторе, покрытом оксидом графена, и в растворе электролита после циклирования намного меньше, чем в случае немодифицированного сепаратора; это указывает на то, что оксид графена является хорошей защитой от полисульфидов. Li–S-аккумулятор с сепаратором, покрытом оксидом графена, и S-катодом демонстрирует высокую емкость 1550 мАч г–1, от которой сохраняется 835 мА ч г–1 после 50 циклов.
Для модифицирования сепаратора Li–S-аккумулятора с успехом используется также пористый активированный уголь, потому что он эффективно блокирует полисульфиды [66, 67]. Впервые был изготовлен сепаратор, модифицированный полыми углеродными сферами, с целью улучшить работу Li–S-аккумулятора (рис. 1ж–1к) [56]. Эти полые углеродные сферы были синтезированы методом травления с шаблоном с использованием диангидрида 3,4,9,10-перилентетракарбоновой кислоты в качестве источника углерода. Затем полые углеродные сферы диспергировали и намазывали на сепаратор Celgard 2400 с поливинилидендифторидом в качестве связующего. Такая однородная сеть углеродных сфер физически и химически затрудняет диффузию полисульфидов и способствует переносу электрона в катоде. Полая структура этих сфер также помогает приспособиться к большим изменениям объема активных материалов при циклировании аккумулятора. Li–S-аккумулятор с катодом из сажи и серы и сепаратором, модифицированным полыми углеродными сферами, демонстрирует гораздо лучшую циклируемость при скоростях заряда–разряда 0.5 и 1 C в течение 500 циклов, чем аккумуляторы с обычными сепараторами. Даже при большом содержании серы (3.0 мг см–2) Li–S-аккумулятор имеет весьма высокую емкость 1087 мА ч г–1, которая все еще сохраняется на уровне 730 мА ч г–1 после 100 циклов при скорости 0.2 C.
Сепараторы, модифицированные полимерами
Челночный перенос – это самая “коварная” проблема, с которой сталкиваются разработчики Li–S-аккумулятора, потому что она порождает различные побочные эффекты. Углеродистые материалы обычно не полярны, и потому им трудно полностью предотвратить диффузию больших количеств полисульфидов. Полимеры с гибкой структурой обычно хорошо справляются с формированием пленок. Полимеры со специфическими функциональными группами (–SO3H, ‒COOH и –OH) могут послужить основой для тонкой ион-селективной пленки на поверхности коммерческого сепаратора, которая будет химически адсорбировать полисульфид или исключит его диффузию и таким образом сильно ограничит челночный перенос.
Нафион – типичная протонообменная мембрана, широко используемая в топливных элементах [68, 69]. Нафион впервые использовали в Li–S-аккумуляторе в литированном состоянии, и он внес существенные улучшения в его работу [70]. Результаты ИК-спектроскопии с преобразованием Фурье доказывают успешное литирование нафионовой мембраны после ее погружения на некоторое время в 1 M раствор LiOH. Такая литированная нафионовая мембрана демонстрирует высокое число переноса иона лития (0.986), и это показывает, что практически только ионы лития могут проходить через эту мембрану. Li–S-аккумулятор с подобным сепаратором имеет улучшенные эксплуатационные характеристики по сравнению с аккумулятором с обычным сепаратором Celgard 2400. Однако, из-за слабой проводимости нафионовой мембраны по иону лития ее емкость резко спадает на последующих циклах. Сообщалось о покрытии сепаратора Celgard 2400 для Li–S-аккумулятора из раствора нафиона (рис. 2a) [40]. Li–S-аккумулятор с более тонким слоем нафиона обладает лучшей циклируемостью. Тонкая ион-селективная мембрана эффективно препятствует диффузии полисульфида, а также не дает побочных эффектов по отношению к переносу иона лития. Li–S-аккумулятор с сепаратором, покрытым нафионом, показал более слабый спад емкости (0.08% при скорости 1 C) по сравнению с аккумулятором с обычным сепаратором (0.13%). И хотя Li–S-аккумулятор с ион-селективным сепаратором показывает лучшую циклируемость, по способности работать при высоких скоростях заряда–разряда он все же уступает аккумуляторам с обычным сепаратором, из-за неизбежного повышения сопротивления переноса заряда, которое вносит слой нафиона. С этим недостатком можно справиться, контролируя количество нафиона, осаждаемое на коммерческие сепараторы. Сообщалось о приготовлении сепаратора для Li–S-аккумулятора, покрытого слоем литированного нафиона [39]. При небольших плотностях тока такой Li–S-аккумулятор имеет те же эксплуатационные характеристики, что и аккумуляторы с исходными сепараторами; но все же при высоких плотностях тока он работает хуже, чем аккумуляторы с обычным сепаратором.
Рис. 2.
Модифицирование сепараторов Li–S-аккумуляторов полимерами: (a) схема механизма функционирования сепаратора, покрытого нафионом, в Li–S-аккумуляторе [40] (воспроизводится с разрешения © 2014, Royal Society of Chemistry); (б) схема механизма функционирования сепаратора, модифицированного катионообменным слоем, в Li‒S-аккумуляторе [41] (воспроизводится с разрешения © 2015, Royal Society of Chemistry); (в) процесс полимеризации мономера акриловой кислоты при нанесении на сепаратор и механизм функционирования такого сепаратора в Li‒S-аккумуляторе [42] (воспроизводится с разрешения © 2018, Elsevier).
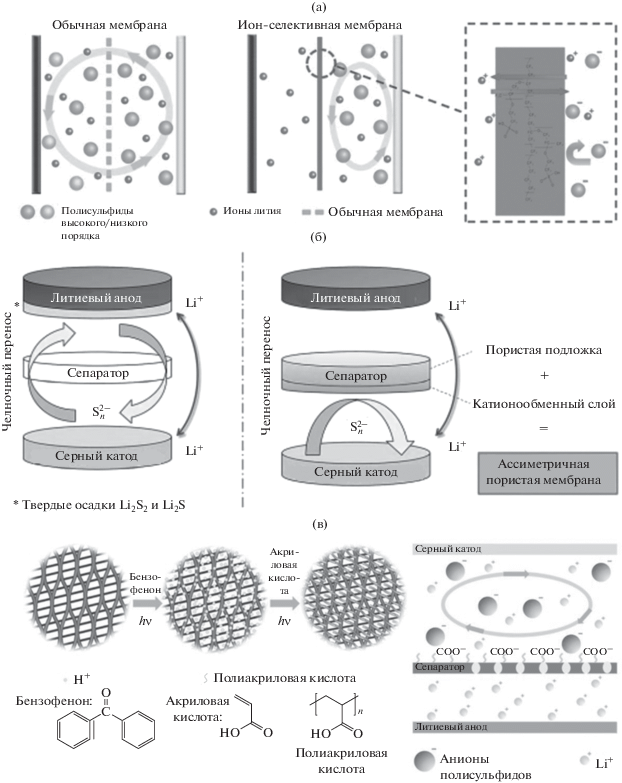
Ввиду слабой ионной проводимости нафиона, исследователи постоянно обращались к поискам других ион-селективных полимеров для высокопроизводительных Li–S-аккумуляторов. Новый катионообменный функциональный сепаратор был приготовлен методом плазменной “привитой” сополимеризации (рис. 2б) [41]. Поддерживающей подложкой служил полипропиленовый сепаратор. Натриевая соль стиролсульфокислоты была “привита” к одной стороне полипропиленового сепаратора методом плазменной сополимеризации. Полученный композитный сепаратор погружали в раствор Li2CO3 на ночь для того, чтобы получить литированный ион-селективный сепаратор. Нужный результат этих двух стадий подтверждали методами сканирующей электронной микроскопии и ИК-спектроскопии с преобразованием Фурье. Испытание на диффузию полисульфидов показало, что приготовленный ион-селективный сепаратор эффективно блокирует диффузию полисульфидов. Li–S-аккумулятор с таким ион-селективным сепаратором демонстрирует более высокую кулоновскую эффективность и лучшую циклируемость, чем Li–S-аккумулятор с немодифицированным сепаратором.
Полиакриловая кислота содержит функциональные группы, которые, как группы в нафионе, способны блокировать диффузию полисульфидных анионов. Утверждается [71], что полиакриловая кислота сильно улучшает свойства катода. Если нанести тонкую мембрану из полиакриловой кислоты на поверхность катода, то работа Li–S-аккумулятора улучшается. Поэтому полиакриловая кислота используется для модифицирования сепараторов Li–S-аккумуляторов с целью повышения их эксплуатационных характеристик (рис. 2в) [42]. Полиакриловую кислоту “прививают” к материалу сепаратора Celgard 2325 методом фотополимеризации с использованием бензофенона в качестве инициатора полимеризации. Различные времена облучения (5, 10 и 15 мин) оказывают разное влияние на работу Li–S-аккумулятора. Наилучшие характеристики Li–S-аккумулятора с сепаратором, модифицированным полиакриловой кислотой, получаются после 10-минутного ее облучения. Например, спад емкости после 600 циклов при скорости заряда–разряда 0.5 C составил всего 0.074% за цикл. Анализ показывает, что причиной такой хорошей циклируемости является физическое препятствование диффузии и электростатическое отталкивание полисульфида со стороны карбоксильных функциональных групп в полиакриловой кислоте.
Сепараторы, модифицированные неорганическими материалами
Полимеры со специфическими функциональными группами, действительно, могут подавлять челночный перенос. Однако такая плотная полимерная пленка неизбежно уменьшает ионную проводимость модифицированного сепаратора. Неорганические материалы, такие как оксиды металлов и неметаллов и сульфиды металлов, могут быть легко диспергированы и использованы для модифицирования коммерческих сепараторов. Такой пористый модифицирующий слой повышает поглощение электролита сепаратором и гарантирует ионную проводимость. Что еще важнее, этот неорганический модифицирующий слой может физически и химически взаимодействовать с полисульфидами и ограничивать челночный перенос. Хорошая сопротивляемость неорганических материалов высокой температуре также может повышать устойчивость сепараторов с покрытием к деформации при повышении температуры.
Al2O3 демонстрирует ряд уникальных преимуществ при модифицировании коммерческих сепараторов для Li–S-аккумулятора (рис. 3a–3в) [43]. Al2O3 наносили на сепаратор Celgard 2320 с использованием поливинилидендифторида в качестве связующего. Однородный слой Al2O3 способен физически предотвратить диффузию полисульфидов и в то же время не препятствует свободной диффузии ионов лития. Кроме того, анализ сепараторов после циклирования показывает, что соединения серы равномерно осаждаются на поверхность Al2O3, что доказывает способность модифицирующего слоя химически блокировать диффузию полисульфидов. Li–S-аккумулятор с сепаратором, покрытым Al2O3, имеет начальную емкость 967 мА ч г–1 при 0.2 C и сохраняет высокую обратимую емкость 593.4 мА ч г–1 после 50 циклов, что намного лучше, чем у аккумуляторов с исходным сепаратором. Похожий керамический сепаратор с SiO2 также применялся в Li‒S-аккумуляторе (рис. 3г–3е) [44]. Сепаратор, модифицированный SiO2, готовили, погружая сепаратор Celgard 2075 в реакционный раствор SiO2. Повышенная скорость потребления электролита способствует “гладкому” переносу иона лития. Тест на диффузию и адсорбцию полисульфидов показал, что SiO2 эффективно адсорбирует полисульфид и подавляет челночный перенос. Li–S-аккумулятор с сепаратором, модифицированным SiO2, имеет высокую обратимую емкость 603.5 мА ч г–1 при 0.2 C после 200 циклов, а спад ее всего 0.05% за цикл. Такой сепаратор, модифицированный SiO2, также уменьшает усадку в размерах по сравнению с обычным сепаратором, что повышает безопасность аккумуляторов. Подобный же метод с применением SnO2 употреблялся и ранее для модифицирования материалов [45].
Рис. 3.
Сепараторы для Li–S-аккумулятора, модифицированные неорганическими материалами: (a) схема помещения сепаратора, покрытого Al2O3, в Li–S-аккумуляторе и SEM-микрофотография слоя Al2O3 (б) до и (в) после циклирования [43] (воспроизводится с разрешения © 2014, Elsevier); (г) сравнение механизмов функционирования обычного сепаратора и модифицированного Si2O2, в Li–S-аккумуляторе; фото обычного сепаратора и покрытого SiO2 (д) до и (е) после термообработки [44] (воспроизводится с разрешения © 2017, American Chemical Society); (ж) схема механизма функционирования сепаратора, модифицированного MoS2, в Li–S-аккумуляторе [57] (воспроизводится с разрешения © 2017, Wiley-VCH Verlag GmbH & Co. KGaA); (з) схематическое описание процесса приготовления сепаратора, модифицированного Co9S8, и схема механизма его функционирования в Li–S-аккумуляторе [58] (воспроизводится с разрешения © 2018, Royal Society of Chemistry).

Помимо оксидов металлов и неметаллов, в модифицировании сепараторов Li–S-аккумулятора большие преимущества у сульфидов металлов. Модифицирование сепаратора с помощью MoS2 весьма улучшает эксплуатационные характеристики Li–S-аккумулятора (рис. 3ж) [57]. Эксфолиированный MoS2 равномерно распределяют по поверхности сепаратора Celgard методом фильтрования под вакуумом. Многослойный MoS2 может служить барьером для блокировки диффузии полисульфидов. В то же время в полостях и пустотах между нанослоями могут накапливаться большие количества соединений серы, что препятствует образованию изолирующих слоев. К тому же процесс интеркаляции лития приводит к быстрому переносу ионов лития. Li–S-аккумулятор с обширным катодом из серы и сепаратором, модифицированным MoS2, имеет начальную емкость 808 мА ч г–1 и очень слабый спад емкости (0.083% за цикл после 600 циклов), в то время как емкость Li–S-аккумулятора с обычным сепаратором резко спадает до 290 мА ч г–1 за 208 циклов. К тому же Li–S-аккумулятор с сепаратором, модифицированным MoS2, имеет высокую кулоновскую эффективность (>99.5%). В таком аккумуляторе существенно подавлена диффузия полисульфидов. В последнее время для модифицирования сепаратора Li–S-аккумулятора с большим успехом применяют Co9S8 (рис. 3з) [58]. Ансамбли из полых Co9S8-структур с наноразмерными стенками, большой площадью поверхности и выдающейся термостойкостью, полученные гидротермальной реакцией с использованием металлоорганических каркасных структур, наносят на сепараторы. Результаты анализов методами ИК-спектроскопии с преобразованием Фурье и рентгеновской фотоэлектронной спектроскопии показывают, что Co9S8 обладает сильным сродством к полисульфидам, так что слой Co9S8 действует как полярный барьер и сильно подавляет диффузию полисульфидов в результате химического и физического взаимодействий. Li–S-аккумулятор с таким сепаратором, модифицированным Co9S8, показал высокую начальную емкость 1385 мА ч г–1 и обратимую емкость 1190 мА ч г–1 после 200 циклов при плотности тока 0.1 C даже при содержании серы на поверхности до 5.6 мг см–2. Далее, в сочетании с оптимизированным катодом, Li–S-аккумулятор с модифицированным сепаратором дал начальную емкость 986 мА ч г–1 и сохранил ее на 83.2% даже после 1500 циклов, что дает ему шансы на практическое использование.
Сепараторы, модифицированные композитами
С учетом сложности проблем, стоящих перед литий-серным аккумулятором, не приходится надеяться, что какой-либо один компонент сможет решить их все полностью. Поэтому в целях улучшения работы Li–S-аккумулятора рассматривались и сепараторы, модифицированные несколькими компонентами.
В последнее время в Li–S-аккумуляторах применяли различные сепараторы, модифицированные несколькими компонентами [72–75]. Для модифицирования таких сепараторов одновременно использовали нафион, полиэтиленоксид и углерод Super P. Они демонстрируют прекрасный синергический эффект (рис. 4a) [46]. Эти результаты показывают, что углерод Super P может удерживать серу и таким образом блокировать диффузию полисульфидов; также он повышает проводимость катода. Нафион – катионообменная мембрана – может еще больше подавить диффузию полисульфидов, в то время как полиэтиленоксид используется для того, чтобы скомпенсировать потерю проводимости, вызванную нафионом, и интенсифицировать перенос ионов лития. Сочетание влияния этих компонентов сообщает Li–S-аккумулятору с таким композитным сепаратором прекрасную циклируемость (его обратимая емкость равняется 770 мА ч г–1, а скорость ее спада не превышает 1% за 300 циклов). Также он приобрел способность работать при высоких скоростях заряда–разряда (с обратимой емкостью 690 мА ч г–1 даже при скорости 10 C).
Рис. 4.
Композитный сепаратор для Li–S-аккумулятора: (a) схема механизма функционирования пластинчатого сепаратора в Li–S-аккумуляторе [46] (воспроизводится с разрешения © 2015, Elsevier); (б) схематическое описание структуры трехслойного сепаратора Li–S-аккумулятора и механизм его функционирования [47] (воспроизводится с разрешения © 2016, Elsevier).

Был разработан сепаратор состава графен/пористый полипропилен/Al2O3. Он продемонстрировал многообещающее всестороннее улучшение работы аккумулятора (рис. 4б) [47]. Слой графена, обращенный к катоду, является проводящим слоем, он способствует быстрому переносу электрона и уменьшает сопротивление катода, а также служит резервуаром электролита и таким образом способствует быстрому переносу ионов лития. К тому же графен обладает большим запасом объема для того, чтобы, захватывая полисульфид, остановить его диффузию. Слой Al2O3, обращенный к аноду, уменьшает усадку в размерах композитного сепаратора по сравнению с сепаратором, не содержащим Al2O3; это показывает, что Al2O3 улучшает термобезопасность Li–S-аккумулятора. Такой Li–S-аккумулятор с трехслойным сепаратором имеет начальную емкость 1067 мА ч г–1 при плотности тока 0.2 C и сохраняет 75% от нее после 100 циклов.
Для высокопроизводительного Li–S-аккумулятора был разработан пористый полиэтиленовый сепаратор, покрытый металлоорганической структурой, модифицированной Ni, и углеродными нанотрубками [76]. Эта Ni-металлоорганическая структура эффективно препятствует диффузии полисульфида вследствие ее сильного взаимодействия с полисульфидом. В то же время слой углеродных нанотрубок дополнительно физически блокирует диффузию полисульфида. Далее эти углеродные нанотрубки, обладающие хорошей электропроводностью, способствуют превращениям соединений серы и таким образом повышают процент ее использования. Благодаря совместному влиянию Ni-металлоорганической структуры и углеродных нанотрубок, такой Li–S-аккумулятор с сепаратором, покрытым металлооганической структурой, модифицированной Ni, и углеродными нанотрубками имеет лучшую циклируемость, емкость 1183 мА ч г–1 после 300 циклов при скоростиt 0.2 C и высокий процент сохранности емкости (87.1%), в то время, как емкость Li–S-аккумулятора с обычным сепаратором резко падает до 200 мА ч г–1 после 300 циклов.
ГЕЛЬ-ПОЛИМЕРНЫЕ СЕПАРАТОРЫ
Как видно из недавних исследований, модифицирование коммерческих сепараторов сообщает Li–S-аккумулятору существенное улучшение его работы. Тем не менее рост литиевых дендритов, который существенно ограничивает срок службы и снижает безопасность аккумулятора, является еще одной критичной проблемой Li–S-аккумулятора. В вышеописанных примерах модифицирования сепараторов ею обычно пренебрегали.
Гель-полимерные сепараторы, которые также называют гель-полимерными электролитами после поглощения ими жидкого электролита, могут эффективно подавлять рост литиевых дендритов, поскольку гель-полимер плотно прилегает к поверхности литиевого анода и уменьшает свободное пространство для роста дендритов [77–80]. Такое модифицирование также выполняет задачу подавления диффузии полисульфида. Такие гель-полимерные сепараторы постепенно начинают применять в Li–S-аккумуляторах, и они демонстрируют свои преимущества. Таблица 2 суммирует недавний прогресс в разработке гель-полимерных сепараторов для Li–S-аккумулятора; конкретные детали обсуждаются ниже.
Таблица 2.
Сводка свойств гель-полимерных сепараторов для Li–S-аккумулятора
| Состав | Содержание серы, мг см–2 | Число циклов и скорость заряда–разряда (1 C = 1675 мA г–1) | Емкость, мА ч г–1 | Ссылка |
|---|---|---|---|---|
| Поливинилидендифторид/полиметилметакрилат/поливинилидендифторид | 1 | 300 (0.6 C) | 523.1 | [48] |
| Керамика/полиэтиленоксид | 0.64 | 300 (0.5) | 700 | [81] |
| Полиметилметакрилат/полиакрилонитрил | 1.5–1.8 | 500 (0.3 C) | 792 | [82] |
| Полиэтиленоксид/поливинилидендифторид/ZrO2 | 1.7 | 500 (1 C) | 847.2 | [51] |
| Полидопамин/поливинилидендифторид | 1.0–1.3 | 200 (0.1 C) | 868.8 | [52] |
| Лигноцеллюлоза | – | 100 (0.01) | 653.5 | [83] |
| Тетраакрилат пентаэритритола | 1.0–1.2 | 300 (0.5 C) | >400 | [84] |
| Полиметилметакрилат/ацетиленовая сажа | 1.0–1.3 | 200 (1 C) | 550 | [85] |
| Полиэтиленгликоль–пропиленгликоль–полиэтиленгликоль | 1.5 | 1500 (0.5 C) | 460 | [86] |
Гель-полимерные сепараторы на основе поливинилидендифторида, содержащие полиэтилен-оксид и ZrO2, в Li–S-аккумуляторе (рис. 5a–5д), обладают большими преимуществами [51]. Согласно SEM-микрофотографиям, гель-полимерная мембрана имеет плотную однородную структуру, которая эффективно блокирует диффузию полисульфидов. Внедренные в сепаратор полиэтиленоксид и ZrO2 усиливают захват электролита, что способствует переносу ионов лития, благодаря взаимодействию между ионами лития и атомами кислорода полиэтиленоксида и ZrO2. Такой Li–S-аккумулятор способен сохранять обратимую емкость 847.2 мА ч г–1 после 500 циклов при скорости 1 C, а спад емкости равняется всего лишь 0.05%. Кроме того, SEM-микрофотографии проциклированных литиевых анодов показывают, что компактная структура гель-полимерной мембраны эффективно защищает литиевый анод от коррозии в полисульфидной среде.
Рис. 5.
Гель-полимерные сепараторы для Li–S-аккумулятора: (a) схема механизма функционирования гель-полимерного сепаратора на основе поливинилидендифторида с внедренными полиэтиленоксидом и ZrO2 в Li–S-аккумуляторе; морфология поверхности циклированного литиевого анода Li–S-аккумулятора с (б) полиолефиновым сепаратором и (в) гель-полимерным сепаратором; морфология поперечного сечения циклированного литиевого анода Li–S-аккумулятора с (г) полиолефиновым сепаратором и (д) гель-полимерным электролитом [51] (воспроизводится с разрешения © 2017, Royal Society of Chemistry); (е) сравнение рабочего состояния сепаратора Celgard и гель-полимерного сепаратора на основе полидиацетилена–поливинилидендифторида в Li–S-аккумуляторе; морфология поверхности циклированного литиевого анода Li–S-аккумулятора с (ж) полиолефиновым сепаратором и (з) гель-полимерным сепаратором [52] (воспроизводится с разрешения © 2018, Royal Society of Chemistry); (и, к) схема механизма функционирования многофункционального гель-полимерного сепаратора со структурой сэндвича в Li–S-аккумуляторе [86] (воспроизводится с разрешения © 2018, Wiley-VCH Verlag GmbH & Co. KGaA).
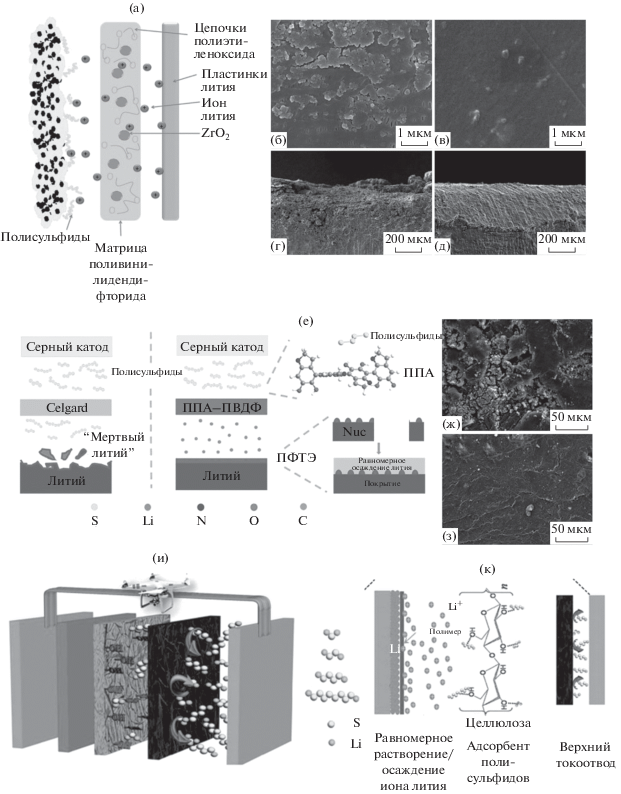
Позднее для улучшения работы Li–S-аккумулятора был создан гель-полимер поливинилидендифторида, модифицированый полидопамином (рис. 5е–5з) [52]. Полидопамин наносят на поливинилидендифторидную мембрану по фазоинверсному методу. Приготовленная таким образом полидопамин-поливинилидендифторидная мембрана эффективно подавляет челночный перенос вследствие сильного взаимодействия между полисульфидом и полидопамином. К тому же эта полидопамин-поливинилидендифторидная мембрана может способствовать процессам растворения/осаждения иона лития, соответственно, из литиевого анода и на него, что способствует образованию устойчивой пленки SEI (промежуточной фазы твердого электролита) и стабилизации литиевого анода. Li–S-аккумулятор с полидопамин-поливинилидендифторидным гель-полимерным сепаратором показал начальную емкость 1215.4 мА ч г–1 при 0.1 C и удерживал обратимую емкость 868.8 мА ч г–1 после 200 циклов, в то время как емкость аккумулятора с жидким электролитом радикально упала до 509.7 мА ч г–1. После циклирования поверхность литиевого анода Li‒S-аккумулятора с полидопамин-поливинилидендифторидной гель-полимерной мембраной сохраняет гладкую плотную структуру, что подтверждает хорошее защитное действие.
Гель-полимерный сепаратор на основе тетраакрилата пентаэритритола, который готовили, используя коммерческий сепаратор в качестве подложки, показал уникальные возможности в Li–S-аккумуляторе [49]. Эту гель-полимерную мембрану готовили непосредственной полимеризацией мономеров тетраакрилата пентаэритритола в перчаточном боксе. Такая гель-полимерная мембрана отличается высокой ионной проводимостью: 11.3 мСм cм–1. Было показано, что такой гель-полимерный сепаратор способствует образованию устойчивой и гибкой пассивирующей пленки на поверхности катода, что эффективно устраняет диффузию полисульфидов и способствует образованию стабильной границы раздела электролит/катод. В сочетании с катодом из чистой серы, Li–S-аккумулятор с гель-полимерным сепаратором дает обратимую емкость 529.7 мА ч г–1 после 400 циклов при 0.5 C с высокой степенью сохранения емкости (81.9%), в то время как емкость Li–S-аккумулятора с жидким электролитом радикально упала до 70.2 мА ч г–1 после 200 циклов. Позднее, в Li–S-аккумуляторе применили аналогичный гель-полимер на основе тетраакрилата пентаэритритола, поперечно сшитого с дивиниладипатом, с использованием пористого полиэтилена в качестве поддерживающей структуры-подложки [84]. Анализ методом рентгеновской фотоэлектронной спектроскопии и ИК-спектроскопии с преобразованием Фурье такого гель-полимерного сепаратора до и после циклирования показал, что сигнал от связи C=O сложного эфира почти исчез после циклирования, что указывает на то, что вследствие сильного взаимодействия между полисульфидом и гель-полимером диффузия полисульфида эффективно подавлена. Li–S-аккумулятор с таким гель-полимерным сепаратором показал повышенную устойчивость по отношению к циклированию и сохранение емкости на 70% после 300 циклов при скорости заряда–разряда 0.5 C. Напротив, аккумулятор с исходным сепаратором с жидким электролитом сохранил только 29% от своей начальной емкости. Результаты фитинга сопротивления и SEM-микрофотографии циклированных литиевых анодов показали, что гель-полимерный сепаратор способствует образованию устойчивой и однородной пленки промежуточной фазы твердого электролита (SEI) на литиевых анодах. Благодаря исключительной гибкости гель-полимера, мягко уплотненный Li–S-аккумулятор, собранный с таким гель-полимерным сепаратором, продемонстрировал хорошее электрохимическое поведение при различных складчатых состояниях, и это указывает на то, что гель-полимерный сепаратор имеет хорошие перспективы применения в гибком Li–S-аккумуляторе.
Композитный гель-полимерный электролит, состоящий из слегка поперечно сшитых слоев полиметилметакрилата и слоев ацетиленовой сажи исполняет в Li–S-аккумуляторе многочисленные функции [85]. Если такой гель-полимер плотно прилегает к литиевому аноду, то слой полиметилметакрилата эффективно подавляет рост литиевых дендритов. Слой ацетиленовой сажи, обращенный к серному катоду, способствует переносу электрона и радикально улучшает способность Li–S-аккумулятора работать при высоких скоростях заряда–разряда. Как и в цитированной выше работе, многофункциональный многокомпонентный гель-полимерный сепаратор сильно улучшает эксплуатационные характеристики Li–S-аккумулятора и намечает хорошие перспективы его практического применения (рис. 5и и 5к) [86]. Сажу и поли(этиленгликоль)-b-поли(пропиленгликоль)-b-поли(этиленгликоль) наносили на целлюлозный нетканый материал, образуя таким образом сэндвич-электролит. Слой сажи, обращенный к катоду, служит проводящей “сеткой”, облегчающей перенос электрона на катоде, и одновременно действует как барьер, физически блокирующий диффузию полисульфида. Целлюлозный нетканый материал, содержащий большое число гидроксильных групп, дополнительно препятствует диффузии полисульфида в результате сильного взаимодействия между полисульфидом и нетканой целлюлозой, что подтверждается методом рентгеновской фотоэлектронной спектроскопии и измерениями энергии адсорбции. Этот гель-полимер поли(этиленгликоль)-b-поли(пропиленгликоль)-b-поли(этиленгликоль) может способствовать равномерному растворению/осаждению иона лития, соответственно, из литиевого анода и на него, что эффективно защищает литий от коррозии. Li–S-аккумулятор с таким многофункциональным гель-полимерным сепаратором имеет начальную емкость 1146 мА ч г–1 при 0.5 C и небольшую скорость спадания емкости: 0.039% за цикл в течение 1500 циклов, что превосходит результаты большинства опубликованных работ.
ЗАКЛЮЧЕНИЕ
Суммирован недавний прогресс в модифицировании сепараторов для Li–S-аккумуляторов, обеспечивающих хорошую циклируемость. По сравнению с созданием сложных катодов, модифицирование сепараторов обладает многочисленными преимуществами, такими как легкость изготовления, низкая стоимость, меньшие затраты времени и легкость масштабирования производства. Это весьма благоприятно для коммерциализации Li–S-аккумулятора. Большинство модификаций основано на коммерческих полиолефиновых сепараторах. Для создания коммерческих сепараторов используются различные материалы – углеродистые материалы, полимеры, неорганические материалы и композиты. Другое перспективное направление усовершенствования Li–S-аккумулятора – это гель-полимерные сепараторы, благодаря их уникальным характеристикам. Прежние работы показали, что модифицирование сепараторов дает следующие преимущества [33, 87, 88]: 1) модифицирующий слой с хорошей электронной проводимостью обеспечивает подходящие реакционные места для активных материалов и реактивирует промежуточные соединения, повышая таким образом степень использования серы; 2) модифицирующие материалы могут взаимодействовать химическим и физическим образом с полисульфидами, подавляя таким образом челночный перенос и восстанавливая потери активных материалов; 3) гель-полимерные сепараторы могут подавлять рост литиевых дендритов и повышать безопасность Li–S-аккумуляторов, благодаря хорошей межфазной совместимости гель-полимера и литиевого анода, что также помогает устранить челночный перенос.
В общем и целом, в последнее время достигнуто важное улучшение поведения Li–S-аккумулятора по мере того, как используется все больше и больше функциональных материалов. Следует отметить, что проблемы Li–S-аккумулятора часто взаимосвязаны. Модифицирование только одного компонента не может решить сложных практических проблем. Для решения различных проблем следует применять многокомпонентное модифицирование и в то же время использовать специфические функции отдельных компонентов. Более того, в сочетании с уникальными преимуществами гель-полимерных сепараторов, способных эффективно подавлять рост литиевых дендритов, использование многофункциональных сепараторов сделается фокусом дальнейших разработок сепараторов для Li–S-аккумуляторов.
Список литературы
Whittingham, M.S., Chem. Rev., 2004, vol. 104, p. 4271.
Fergus, J.W., J. Power Sources, 2010, vol. 195, p. 939.
Scrosati, B. and Garche, J., J. Power Sources, 2010, vol. 195, p. 2419.
Tarascon, J.M. and Armand, M., Nature, 2001, vol. 414, p. 359.
Dunn, B., Kamath, H., and Tarascon, J.M., Science, 2011, vol. 334, p. 928.
Manthiram, A., Fu, Y., Chung, S., Zu, C., and Su, Y., Chem. Rev., 2014, vol. 114, p. 11751.
Manthiram, A., Fu, Y., and Su, Y., Acc. Chem. Res., 2012, vol. 46, p. 1125.
Evers, S. and Nazar, L.F., Acc. Chem. Res., 2012, vol. 46, p. 1125.
Ji, X. and Nazar, L.F., J. Mater. Chem., 2010, vol. 20, p. 9821.
Bruce, P.G., Hardwick, L.J., and Abraham, K.M., MRS Bull., 2011, vol. 36, p. 506.
Song, M.K., Cairns, E.J., and Zhang, Y., Nanoscale, 2013, vol. 5, p. 2186.
Fang, R., Zhao, S., Sun, Z., Wang, D., Cheng, H., and Li, F., Adv. Mater., 2017, vol. 29, p. 1606823.
Zhang, S.S., J. Power Sources, 2013, vol. 231, p. 153.
Yin, Y., Xin, S., Guo, Y., and Wan, L., Angew. Chem. Int. Ed., 2013, vol. 52, p. 13186.
Nazar, L.F., Cuisinier, M., and Pang, Q., MRS Bull., 2014, vol. 39, p. 436.
Ji, X., Lee, K.T., and Nazar, L.F., Nat. Mater., 2009, vol. 8, p. 500.
Zhang, B., Qin, X., Li, G.R., and Gao, X.P., Energy Environ. Sci., 2010, vol. 3, p. 1531.
Guo, J., Xu, Y., and Wang, C., Nano Lett., 2011, vol. 11, p. 4288.
Zheng, G., Yang, Y., Cha, J.J., Hong, S.S., and Cui, Y., Nano Lett., 2011, vol. 11, p. 4462.
Park, M., Yu, J., Kim, K.J., Jeong, G., Kim, J., Jo, Y., Hwang, U., Kang, S., Woo, T., and Kim, Y., Phys. Chem. Chem. Phys., 2012, vol. 14, p. 6796.
Liu, Z., Yuan, X., Zhang, S., Wang, J., Huang, Q., Yu, N., Zhu, Y., Fu, L., Wang, F., Chen, Y., and Wu, Y., NPG Asia Mater., 2019, vol. 11, p. 12.
Liang, X., Liu, Y., Wen, Z., Huang, L., Wang, X. and Zhang, H., J. Power Sources, 2011, vol. 196, p. 6951.
Li, G., Li, G., Ye, S., and Gao, X., Adv. Energy Mater., 2012, vol. 2, p. 1238.
Xiao, L., Cao, Y., Xiao, J., Schwenzer, B., Engelhard, M.H., Saraf, L.V., Nie, Z., Exarhos, G.J., and Liu, J., Adv. Mater., 2012, vol. 24, p. 1176.
Zhang, Y., Bakenov, Z., Zhao, Y., Konarov, A., Doan, T.N.L., Malik, M., Paron, T., and Chen, P., J. Power Sources, 2012, vol. 208, p. 1.
Fu, Y. and Manthiram, A., RSC Adv., 2012, vol. 2, p. 5927.
Zhou, W., Yu, Y., Chen, H., DiSalvo, F.J., and Abruña, H.D., J. Am. Chem. Soc., 2013, vol. 135, p. 16736.
Ma, X.Z., Jin, B., Wang, H.Y., Hou, J.Z., Zhong, X.B., Wang, H.H., and Xin, P.M., J. Electroanal. Chem., 2015, vol. 736, p. 127.
Liang, X., Kwok, C.Y., Lodi-Marzano, F., Pang, Q., Cuisinier, M., Huang, H., Hart, C.J., Houtarde, D., Kaup, K., Sommer, H., Brezesinski, T., Janek, J., and Nazar, L.F., Adv. Energy Mater., 2016, vol. 6, p. 1501636.
Pang, Q., Kundu, D., and Nazar, L.F., Mater. Horiz., 2016, vol. 3, p. 130.
Liu, X., Huang, J., Zhang, Q., and Mai, L., Adv. Mater., 2017, vol. 29, p. 1601759.
Huang, J., Zhang, Q., and Wei, F., Energy Storage Mater., 2015, vol. 1, p. 127.
Deng, N., Kang, W., Liu, Y., Ju, J., Wu, D., Li, L., Hassan, B.S., and Cheng, B., J. Power Sources, 2016, vol. 331, p. 132.
Jeong, T., Moon, Y.H., Chun, H., Kim, H.S., Cho, B.W., and Kim, Y., Chem. Commun., 2013, vol. 49, p. 11107.
Chung, S. and Manthiram, A., Adv. Funct. Mater., 2014, vol. 24, p. 5299.
Yao, H., Yan, K., Li, W., Zheng, G., Kong, D., Seh, Z.W., Narasimhan, V.K., Liang, Z., and Cui, Y., Energy Environ. Sci., 2014, vol. 7, p. 3381.
Chung, S. and Manthiram, A., J. Phys. Chem. Lett., 2014, vol. 5, p. 1978.
Huang, J., Zhuang, T., Zhang, Q., Peng, H., Chen, C., and Wei, F., ACS Nano, 2015, vol. 9, p. 3002.
Bauer, I., Thieme, S., Brückner, J., Althues, H., and Kaskel, S., J. Power Sources, 2014, vol. 251, p. 417.
Huang, J., Zhang, Q., Peng, H., Liu, X., Qian, W., and Wei, F., Energy Environ. Sci., 2014, vol. 7, p. 347.
Conder, J., Urbonaite, S., Streich, D., Novák, P., and Gubler, L., RSC Adv., 2015, vol. 5, p. 79654.
Song, S., Shi, L., Lu, S., Pang, Y., Wang, Y., Zhu, M., Ding, D., and Ding, S., J. Membr. Sci., 2018, vol. 563, p. 277.
Zhang, Z., Lai, Y., Zhang, Z., Zhang, K., and Li, J., Electrochim. Acta, 2014, vol. 129, p. 55.
Li, J., Huang, Y., Zhang, S., Jia, W., Wang, X., Guo, Y., Jia, D., and Wang, L., ACS Appl. Mater. Inter., 2017, vol. 9, p. 7499.
Xiang, Y., Wang, Z., Qiu, W., Guo, Z., Liu, D., Qu, D., Xie, Z., Tang, H., and Li, J., J. Membr. Sci., 2018, vol. 563, p. 380.
Cai, W., Li, G., He, F., Jin, L., Liu, B., and Li, Z., J. Power Sources, 2015, vol. 283, p. 524.
Song, R., Fang, R., Wen, L., Shi, Y., Wang, S., and Li, F., J. Power Sources, 2016, vol. 301, p. 179.
Yang, W., Yang, W., Feng, J., Ma, Z., and Shao, G., Electrochim. Acta, 2016, vol. 210, p. 71.
Liu, M., Zhou, D., He, Y., Fu, Y., Qin, X., Miao, C., Du, H., Li, B., Yang, Q., Lin, Z., Zhao, T.S., and Kang, F., Nano Energy, 2016, vol. 22, p. 278.
Choi, S., Song, J., Wang, C., Park, S., and Wang, G., Chem. Asian J., 2017, vol. 12, p. 1470.
Gao, S., Wang, K., Wang, R., Jiang, M., Han, J., Gu, T., Cheng, S., and Jiang, K., J. Mater. Chem. A, 2017, vol. 5, p. 17889.
Han, D., Liu, S., Liu, Y., Zhang, Z., Li, G., and Gao, X., J. Mater. Chem. A, 2018, vol. 6, p. 18627.
Huang, H., Ding, F., Zhong, H., Li, H., Zhang, W., Liu, X., and Xu, Q., J. Mater. Chem. A, 2018, vol. 6, p. 9539.
Zhang, A., Fang, X., Shen, C., Liu, Y., Seo, I.G., Ma, Y., Chen, L., Cottingham, P., and Zhou, C., Nano Res., 2018, vol. 11, p. 3340.
Chen, D., Wen, K., Lv, W., Wei, Z., and He, W., Phys. Status Solidi RRL., 2018, vol. 12, p. 1800249.
Song, J., Zhang, C., Guo, X., Zhang, J., Luo, L., Liu, H., Wang, F., and Wang, G., J. Mater. Chem. A, 2018, vol. 6, p. 16610.
Ghazi, Z.A., He, X., Khattak, A.M., Khan, N.A., Liang, B., Iqbal, A., Wang, J., Sin, H., Li, L., and Tang, Z., Adv. Mater., 2017, vol. 29, p. 1606817.
He, J., Chen, Y., and Manthiram, A., Energy Environ. Sci., 2018, vol. 11, p. 2560.
Lee, D.H., Ahn, J.H., Park, M., Eftekhari, A., and Kim, D., Electrochim. Acta, 2018, vol. 283, p. 1291.
Yuan, L., Yuan, H., Qiu, X., Chen, L., and Zhu, W., J. Power Sources, 2009, vol. 189, p. 1141.
Chen, J., Zhang, Q., Shi, Y., Qin, L., Cao, Y., Zheng, M., and Dong, Q., Phys. Chem. Chem. Phys., 2012, vol. 14, p. 5376.
Cheng, X., Huang, J., Zhang, Q., Peng, H., Zhao, M., and Wei, F., Nano Energy, 2014, vol. 4, p. 65.
Li, X. and Sun, X., Adv. Funct. Mater., 2018, vol. 28, p. 1801323.
Li, B., Xu, H., Ma, Y., and Yang, S., Nanoscale Horiz., 2018, vol. 4, p. 77.
Jiang, Y., Chen, F., Gao, Y., Wang, Y., Wang, S., Gao, Q., Jiao, Z., Zhao, B., and Chen, Z., J. Power Sources, 2017, vol. 342, p. 929.
Chen, G., Song, X., Wang, S., Wang, Y., Gao, T., Ding, L., and Wang, H., J. Membr. Sci., 2018, vol. 548, p. 247.
Zhang, L., Wang, Y., Niu, Z., and Chen, J., Carbon, 2019, vol. 141, p. 400.
Kreuer, K.D., J. Membr. Sci., 2001, vol. 185, p. 29.
Mauritz, K.A. and Moore, R.B., Chem. Rev., 2004, vol. 104, p. 4535.
Jin, Z., Xie, K., Hong, X., Hu, Z., and Liu, X., J. Power Sources, 2012, vol. 218, p. 163.
Zhang, S.S., Tran, D.T., and Zhang, Z., J. Mater. Chem. A, 2014, vol. 2, p. 18288.
Li, M., Wang, C., Miao, L., Xiang, J., Wang, T., Yuan, K., Chen, J., and Huang, Y., J. Mater. Chem. A, 2018, vol. 6, p. 5862.
Wang, L., He, Y., Shen, L., Lei, D., Ma, J., Ye, H., Shi, K., Li, B., and Kang, F., Nano Energy, 2018, vol. 50, p. 367.
Pang, Y., Wei, J., Wang, Y., and Xia, Y., Adv. Energy Mater., 2018, vol. 8, p. 1702288.
Guan, Y., Wang, A., Liu, S., Li, Q., Wang, W., and Huang, Y., J. Alloy. Compd., 2018, vol. 765, p. 544.
Lee, D.H., Ahn, J.H., Park, M., Eftekhari, A., and Kim, D., Electrochim. Acta, 2018, vol. 283, p. 1291.
Ryou, M., Lee, D.J., Lee, J., Lee, Y.M., Park, J., and Choi, J.W., Adv. Energy Mater., 2012, vol. 2, p. 645.
Luo, W., Zhou, L., Fu, K., Yang, Z., Wan, J., Manno, M., Yao, Y., Zhu, H., Yang, B., and Hu, L., Nano Lett., 2015, vol. 15, p. 6149.
Wu, F., Yuan, Y., Cheng, X., Bai, Y., Li, Y., Wu, C., and Zhang, Q., Energy Storage Mater., 2018, vol. 15, p. 148.
Liu, K., Bai, P., Bazant, M.Z., Wang, C., and Li, J., J. Mater. Chem. A, 2017, vol. 5, p. 4300.
Wang, Q., Wen, Z., Jin, J., Guo, J., Huang, X., Yang, J., and Chen, C., Chem. Commun., 2016, vol. 52, p. 1637.
Liu, M., Jiang, H.R., Ren, Y.X., Zhou, D., Kang, F.Y., and Zhao, T.S., Electrochim. Acta, 2016, vol. 213, p. 871.
Song, A., Huang, Y., Zhong, X., Cao, H., Liu, B., Lin, Y., Wang, M., and Li, X., J. Membr. Sci., 2018, vol. 556, p. 203.
Du, H., Li, S., Qu, H., Lu, B., Wang, X., Chai, J., Zhang, H., Ma, J., Zhang, Z., and Cui, G., J. Membr. Sci., 2018, vol. 550, p. 399.
Yang, D., He, L., Liu, Y., Yan, W., Liang, S., Zhu, Y., Fu, L., Chen, Y., and Wu, Y., J. Mater. Chem. A, 2019. https://doi.org/10.1039/C9TA03123E
Qu, H., Zhang, J., Du, A., Chen, B., Chai, J., Xue, N., Wang, L., Qiao, L., Wang, C., Zang, X., Yang, J., Wang, X., and Cui, G., Adv. Sci., 2018, vol. 5, p. 1700503.
Zhao, Y., Zhang, Y., Gosselink, D., Doan, T.N.L., Sadhu, M., Cheang, H., and Chen, P., Membranes, 2012, vol. 2, p. 553.
Huang, S., Guan, R., Wang, S., Xiao, M., Han, D., Sun, L., and Meng, Y., Prog. Polym. Sci., 2019, vol. 89, p. 19.
Дополнительные материалы отсутствуют.
Инструменты
Электрохимия


