Электрохимия, 2020, T. 56, № 2, стр. 127-132
Твердые электролиты ZrO2–Sc2O3, легированные оксидами Yb2O3 или Y2O3
Е. Е. Ломонова a, Д. А. Агарков b, c, М. А. Борик a, Г. М. Елисеева b, А. В. Кулебякин a, И. Е. Курицына b, Ф. О. Милович d, В. А. Мызина a, В. В. Осико a, А. С. Числов a, d, Н. Ю. Табачкова a, d, *
a Институт общей физики им. А.М. Прохорова РАН
119991 Москва, ул. Вавилова, 38, Россия
b Институт физики твердого тела РАН
142432 Московская обл., Черноголовка, ул. академика Осипьяна, 2, Россия
c Федеральное государственное автономное образовательное учреждение высшего образования
“Московский физико-технический институт (государственный университет)”
117303 Московская обл., Долгопрудный, Институтский пер., 9, Россия
d Национальный исследовательский технологический университет “МИСиС”
119049 Москва, Ленинский просп., 4, Россия
* E-mail: ntabachkova@gmail.com
Поступила в редакцию 03.09.2018
После доработки 14.02.2019
Принята к публикации 10.07.2019
Аннотация
В работе проведено сравнение влияния со-легирующей примеси Y2O3 и Yb2O3 на транспортные характеристики и стабилизацию кубической фазы в твердых растворах на основе ZrO2–Sc2O3. Кристаллы твердых растворов (ZrO2)0.99 –x(Sc2O3)x(Yb2O3)0.01 и (ZrO2)0.99 –x(Sc2O3)x(Y2O3)0.01 (где x = 0.08–0.10) были выращены направленной кристаллизацией расплава в холодном контейнере. Показано, что стабилизация высокотемпературной кубической фазы для кристаллов (ZrO2)0.99 –x(Sc2O3)x(Y2O3)0.01 наблюдается при суммарной концентрации стабилизирующих оксидов 11 мол. %, в то время как в случае кристаллов (ZrO2)0.99 –x(Sc2O3)x(Yb2O3)0.01 это происходит при суммарной концентрации стабилизирующих оксидов 10 мол. %. Установлено, что при содержании оксида скандия (9–10) мол. % высокотемпературная проводимость кристаллов, со-легированных оксидом иттербия выше, чем в случае со-легирования оксидом иттрия. Максимальную проводимость во всем температурном интервале имеют кристаллы (ZrO2)0.9(Sc2O3)0.09(Yb2O3)0.01.
ВВЕДЕНИЕ
Материалы на основе твердых растворов ZrO2–Sc2O3, используемые в твердооксидных топливных элементах (ТОТЭ), вызывают большой интерес, поскольку они обладают наивысшей ионной проводимостью среди твердых электролитов на основе диоксида циркония [1–4]. Применение таких материалов позволяет снизить рабочую температуру топливного элемента до 800°C, что весьма важно для увеличения стабильности, ресурса эксплуатации и надежности электрохимических устройств. Однако, для составов с максимальной проводимостью ZrO2–(9–11) мол. % Sc2O3, существуют проблемы использования их в качестве материалов для электролитических мембран, такие как нестабильность транспортных характеристик при рабочих температурах и наличие при нагреве фазового перехода ромбоэдрической фазы в кубическую. Одним из возможных путей решения данных проблем является стабилизация высокопроводящей кубической фазы путем со-легирования твердых растворов ZrO2–Sc2O3 оксидом иттрия либо оксидами редкоземельных элементов [5–10]. Подбор со-легирующих примесей определяется как получением стабильного в диапазоне температур от комнатной до рабочей (700–1000°С) однофазного кубического твердого раствора, так и сохранением высокой проводимости, характерной для системы ZrO2–Sc2O3.
Влияние ионного радиуса редкоземельных оксидов на кислород-ионную проводимость изучалось во многих работах [11–13]. Показано, что энергия активации, определяющая величину проводимости, в низкотемпературной области (до 600–700°С) складывается из энергии миграции и энергии ассоциации, а в высокотемпературной – определяется энергией миграции. Эти величины зависят от радиуса иона легирующей примеси.
Целью настоящей работы является синтез кристаллов твердых растворов ZrO2–Sc2O3, солегированных оксидами иттрия или иттербия, исследование их транспортных характеристик и сравнение влияния со-легирующей примеси Y2O3 или Yb2O3 на транспортные характеристики и стабилизацию кубической фазы в твердых растворах на основе ZrO2–Sc2O3.
МЕТОДИКА ЭКСПЕРИМЕНТА
Кристаллы твердых растворов (ZrO2)0.99 ‒ x(Sc2O3)x(Yb2O3)0.01 и (ZrO2)0.99 ‒ x(Sc2O3)x(Y2O3)0.01 (где x = 0.08–0.10) были выращены направленной кристаллизацией расплава в холодном контейнере [14].
Химический состав выращенных кристаллов определяли на сканирующем электронном микроскопе JEOL 5910 LV с энергодисперсионной приставкой INCA Energy. При измерениях состава кристаллов в качестве эталонов использовались плавленые оксиды циркония, скандия, иттрия и иттербия. Фазовый анализ проводили рентгенодифрактометрическим методом на дифрактометре Bruker D8 при использовании СuKα излучения, и методом спектроскопии комбинационного рассеяния (КРС). В качестве источника возбуждения использовали лазер с длиной волны 532 нм. Установка для изучения спектров КРС кристаллов в воздушной атмосферее при комнатной температуре и при рабочих температурах до 1000°С была подробно описана в предыдущих работах [15–17].
Плотность определяли методом гидростатического взвешивания на приборе для гидростатического взвешивания фирмы “Сарториус”.
Исследования проводимости кристаллов на основе диоксида циркония проводили в температурном интервале 400–900°С c использованием анализатора частотных характеристик Solartron SI 1260 в частотном интервале 1 Гц–5 МГц с амплитудой переменного токового сигнала 24 мВ. Для измерений были использованы пластины площадью 7 × 7 мм2 и толщиной 0.5 мм. Для формирования токовых контактов на противоположные стороны кристаллов наносили платиновую пасту, которую вжигали при температуре 950°С в течение часа на воздухе. Измерения проводили в режиме нагрева с шагом 50°С и с выдержкой при данной температуре до достижения термического равновесия. Обработку импедансных спектров осуществляли с помощью программы ZView (ver. 2.8). Удельную проводимость кристаллов рассчитывали из данных, полученных при обработке импедансных спектров, с учетом геометрических размеров образцов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В табл. 1 приведены составы твердых растворов, используемые далее обозначения, фазовый состав и плотность кристаллов. Выращенные кристаллы имели форму и размеры, аналогичные кристаллам диоксида циркония, стабилизированного оксидом скандия и/или иттрия, полученным в холодном тигле [18, 19].
Таблица 1.
Фазовый состав, обозначения и плотность выращенных кристаллов
| Состав | Обозначение | Фазовый состав* | Плотность, г/см3 |
|---|---|---|---|
| (ZrO2)0.91(Sc2O3)0.08(Yb2O3)0.01 | 8Sc1YbSZ | t-ZrO2 | 5.924 ± 0.001 |
| (ZrO2)0.91(Sc2O3)0.08(Y2O3)0.01 | 8Sc1YSZ | t-ZrO2 | 5.824 ± 0.001 |
| (ZrO2)0.90(Sc2O3)0.09(Yb2O3)0.01 | 9Sc1YbSZ | c-ZrO2 | 5.863 ± 0.001 |
| (ZrO2)0.90(Sc2O3)0.09(Y2O3)0.01 | 9Sc1YSZ | t-ZrO2 c-ZrO2 |
5.769 ± 0.001 |
| (ZrO2)0.89(Sc2O3)0.10(Yb2O3)0.01 | 10Sc1YbSZ | r-ZrO2 c-ZrO2 |
5.820 ± 0.001 |
| (ZrO2)0.89(Sc2O3)0.10(Y2O3)0.01 | 10Sc1YSZ | c-ZrO2 | 5.744 ± 0.001 |
Кристаллы 8Sc1YbSZ и 8Sc1YSZ были однородные, мутные, без видимых дефектов. При увеличении концентрации Sc2O3 в твердых растворах до 9 мол. % и добавлении 1 мол. % Y2O3, в кристаллах появились прозрачные области. Прозрачные области находились в нижней части кристалла 9Sc1YSZ, соответствующей началу кристаллизации, а полупрозрачные области (мутные) были расположены в верхней части кристалла (конец кристаллизации). В некоторых кристаллах 9Sc1YSZ из центральной части слитка закристаллизованного расплава можно было видеть чередование прозрачных и мутных областей. Прозрачные, без видимых дефектов монокристаллы, дополнительно легированные 1 мол. % Y2O3, были получены только при концентрации 10 мол. % Sc2O3 в твердом растворе.
В отличие от кристаллов 9Sc1YSZ, легирование 1 мол. % Yb2O3 твердого раствора ZrO2–(9 мол. %) Sc2O3 привело к получению прозрачных однородных монокристаллов. При увеличении концентрации Sc2O3 до 10 мол. % в твердых растворах, легированных 1 мол. % Yb2O3, были получены опалесцирующие кристаллы с микротрещинами в объеме слитков.
Фазовый состав кристаллов, дополнительно легированных 1 мол. % Y2O3, менялся от тетрагонального до кубического при увеличении концентрации Sc2O3. Так кристаллы 8Sc1YSZ содержали только тетрагональную модификацию ZrO2. На изображениях микроструктуры, полученных в проходящем свете, на полированных тонких пластинах были видны двойники, которые образуются при охлаждении монокристалла во время кубическо–тетрагонального перехода в соответствии с диаграммой состояния ZrO2–Sc2O3. Из‑за наличия двойников, рассеивающих свет, тетрагональные кристаллы 8Sc1YSZ были мутными, непрозрачными. По данным фазового анализа кристаллы 9Sc1YSZ были двухфазными и содержали области с тетрагональной и кубической структурой. Кристаллы 10Sc1YSZ были однофазными с кубической флюоритовой структурой.
Фазовый состав кристаллов, дополнительно легированных 1 мол. % Yb2O3, также менялся в зависимости от концентрации Sc2O3. Кристаллы 8Sc1YbSZ были тетрагональными, 9Sc1YbSZ – кубическими, а 10Sc1YbSZ содержали две фазы: кубическую и ромбоэдрическую модификации диоксида циркония.
Плотность кристаллов зависит как от вида и концентрации стабилизирующего оксида, так и от фазового состава кристалла. При одинаковой концентрации Sc2O3 в кристаллах плотность кристаллов, со-легированных Yb2O3, выше, чем у кристаллов, дополнительно легированных Y2O3, так как отношение массы к объему у ионов Yb3+ больше, чем у ионов Y3+. При увеличении концентрации Sc2O3 в кристаллах, со-легированных 1 мол. % Yb2O3, плотность кристаллов уменьшается. Наибольшим значением плотности обладали кристаллы, содержащие тетрагональную фазу 8Sc1YbSZ. Плотность кубических кристаллов меньше, чем тетрагональных. Из-за наличия областей ромбоэдрической фазы в 10Sc1YbSZ значение плотности для данных кристаллов меньше, чем для однофазных кубических монокристаллов 9Sc1YbSZ.
В кристаллах, дополнительно легированных 1 мол. % Y2O3, плотность кристаллов также уменьшается с увеличением концентрации Sc2O3, что связано с изменением фазового состава в данных кристаллах от тетрагонального (8Sc1YSZ) до кубического (10Sc1YSZ) твердого раствора на основе диоксида циркония.
Таким образом, стабилизация высокотемпературной кубической фазы для кристаллов ScYSZ наблюдается при суммарной концентрации стабилизирующих оксидов 11 мол. %, в то время как в случае кристаллов Sc1YbSZ это происходит при суммарной концентрации стабилизирующих оксидов 10 мол. %. Несмотря на меньший ионный радиус Yb3+ по сравнению с Y3+, стабилизация кубической фазы в кристаллах, со-легированных Yb2O3, происходит при меньшей концентрации Sc2O3 в твердом растворе, чем в кристаллах, со-легированных Y2O3.
В двойных системах ZrO2–R2O3 уменьшение ионного радиуса снижает температуру перехода из высокотемпературной кубической фазы в низкотемпературную тетрагональную фазу, что будет приводить к сохранению высокотемпературной кубической фазы при комнатной температуре при меньшей концентрации стабилизирующего оксида. Возможно, данная закономерность справедлива и для исследуемых тройных систем.
Исследование фазового состава проводили также методом комбинационного рассеяния света. На рис. 1 приведены спектры КРС исследуемых кристаллов.
Рис. 1.
Спектры КРС кристаллов (ZrO2)0.99 ‒ x(Sc2O3)x(Y2O3)0.1 и (ZrO2)0.99 ‒ x(Sc2O3)x(Yb2O3)0.1: 1 – 8Sc1YSZ, 2 – 8Sc1YbSZ, 3 – 9Sc1YSZ, 4 – 9Sc1YbSZ, 5 – 10Sc1YSZ, 6 – 10Sc1YbSZ.

В спектрах КРС кристаллов 8Sc1YSZ и Sc1YbSZ присутствуют пики, характерные для тетрагональной фазы [20, 21]. В спектрах КРС кристаллов 9Sc1YSZ линии существенно уширены, что обусловлено наличием в данных кристаллах кубической и тетрагональной фазы. Спектры комбинационного рассеяния кристаллов 10Sc1YbSZ содержат линии, соответствующие ромбоэдрической фазе [21], которые также существенно уширены, что может быть вызвано с наличием и кубической фазы в данных кристаллах.
Спектры кристаллов 9Sc1YbSZ и 10Sc1YSZ подобны и содержат кроме линий кубической фазы линию 480 см–1, которую в ряде работ приписывают тетрагональной t"-фазе [22–24]. Эта фаза имеет степень тетрагональности ${c \mathord{\left/ {\vphantom {c {\sqrt {2a} }}} \right. \kern-0em} {\sqrt {2a} }}$ = 1, но принадлежит пространственной группе симметрии P42/nmc из-за смещения ионов кислорода в анионной подрешетке [23]. Спектры КРС, характерные для t‑ZrO2, t"-ZrO2, и с-ZrO2 фаз приведены в работе [25].
Таким образом, структура кристаллов, идентифицированная с помощью рентгенодифракционного анализа как кубическая, по данным КРС является тетрагональной t"-фазой.
На рис. 2 в аррениусовских координатах приведены температурные зависимости удельной проводимости всех исследуемых кристаллов. На рис. 3 в качестве примера приведены импедансные спектры для кристаллов 10Sc1YSZ и 10Sc1YbSZ.
Рис. 2.
Температурные зависимости удельной объемной проводимости кристаллов (ZrO2)0.99 –x(Sc2O3)x(Y2O3)0.1 и (ZrO2)0.99 –x(Sc2O3)x(Yb2O3)0.1: 1 – 8Sc1YbSZ, 2 – 9Sc1YbSZ, 3 – 10Sc1YbSZ, 4 – 8Sc1YSZ, 5 – 9Sc1YSZ, 6 – 10Sc1YSZ.
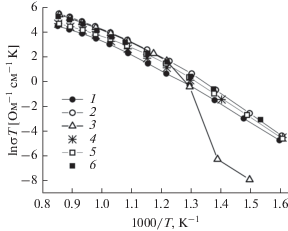
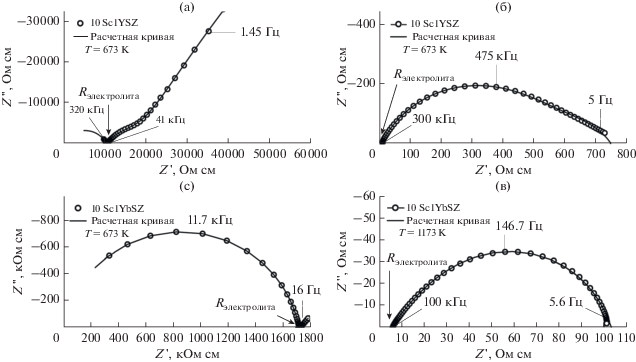
Рис. 3.
Импедансные спектры кристаллов 10Sc1YSZ (а), (б) и 10Sc1YbSZ (в), (г) при температуре 673 и 1173 К.
На графике температурной зависимости удельной электропроводности кристаллов 10Sc1YbSZ в диапазоне температур 450–550°С наблюдается излом, обусловленный фазовым переходом ромбоэдрической фазы в кубическую. Наибольшей проводимостью во всем температурном интервале обладают кристаллы 9Sc1YbSZ, а наименьшей – 8Sc1YbSZ.
На рис. 4 приведена зависимость проводимости кристаллов Sc1YbSZ и Sc1YSZ от содержания Sc2O3. Как следует из рисунка, увеличение содержание Sc2O3 в составе кристаллов, со-легированных оксидами иттрия или иттербия, приводит увеличению проводимости кристаллов. Для кристаллов, со-легированных Yb2O3, концентрационная зависимость имеет максимум при содержании оксида скандия 9 мол. % Sc2O3. В случае со-легирования Y2O3 наблюдается заметное увеличение проводимости только при содержании 10 мол. % Sc2O3. Наблюдаемые концентрационные зависимости проводимости можно объяснить с учетом данных по фазовому составу образцов. Так, для однофазных тетрагональных кристаллов 8Sc1YbSZ и 8Sc1YSZ, а также для кристалла двухфазного 9Sc1YSZ, представляющего собой смесь тетрагональной и кубической фаз, значения проводимости близки и составляют ~0.1 См/см. Аналогичные значения проводимости были получены и для нелегированных тетрагональных кристаллов 8ScSZ и 9ScSZ [26]. Кристаллы 9Sc1YbSZ являются однофазными псевдокубическими (t"-фаза) и имеют максимальную проводимость. При увеличении содержания Sc2O3 до 10 мол. % (кристалл 10Sc1YbSZ) в кристаллах появляются области ромбоэдрической фазы и их проводимость уменьшается. Кристаллы 10Sc1YSZ также являются однофазными псевдокубическими (t"-фаза), однако их проводимость меньше, чем у кристаллов 9Sc1YbSZ, имеющих аналогичную кристаллическую структуру. Такое различие в значениях проводимости может быть связано с большим ионным радиусом Y3+ по сравнению с Yb3+. Введение более крупного иона при гетеровалентном замещении приводит к увеличению напряжений кристаллической решетки, снижающих проводимость. Кроме того, кристаллы 10Sc1YSZ и 9Sc1YbSZ отличаются суммарной концентрацией стабилизирующих оксидов (11 и 10 мол. %, соответственно). Увеличение суммарной концентрацией стабилизирующих оксидов выше некоторого порогового значения, зависящего от вида стабилизирующей примеси, приводит к снижению проводимости вследствие образования кластеров кислородных вакансий и катионов допанта [11].
Рис. 4.
Сравнение ионной проводимости кристаллов при температуре 900°С: 1 – (ZrO2)0.99 –x(Sc2O3)x(Y2O3)0.1, 2 – (ZrO2)0.99 –x(Sc2O3)x(Yb2O3)0.1.

Следует отметить, что величина проводимости кристаллов 9Sc1YbSZ при температуре 900°С (0.214 См/см) сопоставима с аналогичным значением кристаллов 10ScSZ (0.197 См/см) [26]. Однако, в отличие от кристалла 10ScSZ, содержащего ромбоэдрическую фазу, образец 9Sc1YbSZ является однофазным псевдокубическим.
ЗАКЛЮЧЕНИЕ
Проведено сравнительное исследование фазового состава и транспортных характеристик кристаллов твердых растворов (ZrO2)0.99 –x(Sc2O3)x(Yb2O3)0.1 и (ZrO2)0.99 – x(Sc2O3)x(Y2O3)0.1 (где x = 0.08–0.10), полученных направленной кристаллизацией расплава в холодном контейнере.
Показано, что стабилизация псевдокубической (t"-фазы) для кристаллов ScYSZ наблюдается при суммарной концентрации стабилизирующих оксидов 11 мол. %, в то время как в случае кристаллов Sc1YbSZ это происходит при суммарной концентрации стабилизирующих оксидов 10 мол. %.
Установлено, что для всех исследуемых составов проводимость кристаллов увеличивается с увеличением концентрации Sc2O3. Для кристаллов, со-легированных оксидом иттрия или иттербия, максимальная проводимость наблюдается при различном содержании Sc2O3 (10 и 9 мол. %, соответственно). Установлено, что при содержании Sc2O3 9–10 мол. % высокотемпературная проводимость кристаллов, со-легированных Yb2O, выше, чем в случае со-легирования Y2O3. Максимальную проводимость во всем температурном интервале имеют кристаллы 9Sc1YbSZ.
Список литературы
Badwal, S.P.S., Ciacchi, F.T., and Milosevic, D., Scandia–zirconia electrolytes for intermediate temperature solid oxide fuel cell operation, Solid State Ionics, 2000, vol. 136, p. 91.
Kumar, A., Jaiswal, A., Sanbui, M., and Omar, S., Oxygen-Ion Conduction in Scandia-Stabilized Zirconia-Ceria Solid Electrolyte (xSc2O3–1CeO2–(99 – x)ZrO2, 5 ≤ x ≤ 11), J. Am. Ceram. Soc., 2016, p. 1.
Stricker, D.W. and Carlson, W.G., Electrical Conductivity in the ZrO2-Rich Region of Several M2O3–ZrO2 System, J. Am. Ceram. Soc., 1965, vol. 48, p. 286.
Borik, M.A., Bredikhin, S.I., Kulebyakin, A.V., Kuri-tsyna, I.E., Lomonova, E.E., Milovich, F.O., Myzina, V.A., Osiko, V.V., Panov, V.A., Ryabochkina, P.A., Seryakov, S.V., and Tabachkova, N.Yu., Melt growth, structure and properties of (ZrO2)1 –x(Sc2O3)x solid solution crystals (x = 0.035–0.11), J. Crystal Growth, 2016, vol. 443, p. 54.
Yamamura, H., Matsusita, T., Nishino, H., and Kakinuma, K., Co-doping effect on electrical conductivity in the fluorite-type solid-solution systems Zr0.7(Sc1 –xMx)0.3O2 – δ (M = Ca, Mg, Al, Gd, Yb), J. Mater. Sci.: Materials in Electronics, 2002, vol. 13, p. 57.
Lee, D.-S., Kim, W.S., Choi, S.H., Kim, J., Lee, H.-W., and Lee, J.-H. Characterization of ZrO2 co-doped with Sc2O3 and CeO2 electrolyte for application of intermediate temperature SOFCs, Solid State Ionics, 2005, vol. 176, p. 33.
Omar, S., Najib, W.B., Chen, W., and Bonanos, N., Electrical conductivity of 10 mol % Sc2O3–1 mol % M2O3–ZrO2 ceramics, J. Am. Ceram. Soc., 2012, vol. 95, p. 1965.
Chiba, R., Ishii, T., and Yoshimura, F., Temperature dependence of ionic conductivity in (1 – x)ZrO2–(x – y)Sc2O3–yYb2O3 electrolyte material, Solid State Ionics, 1996, vol. 91, p. 249.
Spirin, A. Ivanov, V., Nikonov, A., Lipilin, A., Paranin, S., Khrustov, V., and Spirina A., Scandia-stabilized zirconia doped with yttria: Synthesis, properties, and ageing behavior, Solid State Ionics, 2012, vol. 225, p. 448.
Omar, S. and Bonanos, N., Ionic Conductivity Ageing Behaviour of 10 mol % Sc2O3–1 mol % CeO2–ZrO2 Ceramics, J. Mater. Sci., 2010, vol. 45, p. 6406.
Arachi, Y., Sakai, H., Yamamoto, O., Takeda, Y., and Imanishai, N., Electrical conductivity of the ZrO2–Ln2O3 (Ln-lanthanides) system, Solid State Ionics, 1999, vol. 121, p. 133.
Kilner, J.A. and Brook, R.J., A study of oxygen ion conductivity in doped non-stoichiometric oxides, Solid State Ionics, 1982, vol. 6, p. 237.
Zacate, M.O., Minervini, L., Bradfield, D.J., Grimes, R.W, and Sickafus, K.E., Defect Cluster Formation in M2O3 Doped Cubic ZrO2, Solid State Ionics, 2000, vol. 128, p. 243.
Osiko, V.V., Borik, M.A., and Lomonova E.E., Synthesis of Refractory Materials by Skull Melting Technique, Springer Handbook Crystal Growth, 2010, P B, p. 433.
Agarkov, D.A., Burmistrov, I.N., Tsybrov, F.M., Tartakovskii, I.I., Kharton, V.V., and Bredikhin, S.I., In-situ Raman spectroscopy analysis of the interfaces between Ni-based SOFC anodes and stabilized zirconia electrolyte, Solid State Ionics, 2017, vol. 302, p. 133.
Агарков, Д.А., Бурмистров, И.Н., Цыбров, Ф.М., Тартаковский, И.И., Хартон, В.В., Бредихин, С.И. Кинетика восстановления и морфологические изменения Ni в композиционных анодах ТОТЭ: оценка методом комбинационного рассеяния света. Электрохимия. 2016. Т. 52. С. 673. [Agarkov, D.A., Burmistrov, I.N., Tsybrov, F.M., Tartakovskii, I.I., Kharton, V.V., and Bredikhin, S.I., Kinetics of NiO reduction and morphological changes in composite anodes of solid oxide fuel cells: estimate using Raman scattering technique, Russ. J. Electrochem., 2016, vol. 52, p. 600.]
Agarkov, D.A., Burmistrov, I.N., Tsybrov, F.M., Tartakovskii, I.I., Kharton, V.V., Bredikhin, S.I., and Kveder, V.V., Analysis of Interfacial Processes at the SOFC Electrodes by in-situ Raman Spectroscopy, ECS Trans., 2015, vol. 68(1), p. 2093.
Borik, M.A., Bredikhin, S.I., Bublik, V.T., Kulebyakin, A.V., Kuritsyna, I.E., Lomonova, E.E., V.A., Osiko, V.V., Ryabochkina, P.A., Seryakov, S.V., and Tabachkova, N.Yu., Phase composition, structure and properties of (ZrO2)1 –x–y(Sc2O3)x(Y2O3)y solid solution crystals (x = 0.08–0.11; y = 0.01–0.02) grown by directional crystallization of the melt, J. Crystal Growth, 2017, vol. 457, p. 122.
Borik, M.A., Bredikhin, S.I., Bublik, V.T., Kulebyakin, A.V., Kuritsyna, I.E., Lomonova, E.E., Milovich, Ph.O., Myzina, V.A., Osiko, V.V., Ryabochkina, P.A., and Tabachkova, N.Y., Structure and conductivity of yttria and scandia-doped zirconia crystals grown by skull melting, J. Am. Ceram. Soc., 2017, vol. 100, p. 5536.
Fujimori, H., Yashima, M., Kakihana, M., and Yoshimura, M., Structural Changes of Scandia-Doped Zirconia Solid Solutions: Rietveld Analysis and Raman Scattering, J. Amer. Ceram. Soc., 1998, vol. 81, p. 2885.
Fujimori, H., Yashima, M., Kakihana, M., and Yoshimura M., β-cubic phase transition of scandia-doped zirconia solid solution: Calorimetry, X-ray diffraction, and Raman scattering, J. Applied Physics, 2002, vol. 91, p. 6493.
Yashima, M., Sasaki, S., Kakihana, M., Yamaguchi, Y., Arashi, H., and Yoshimura, M., Oxygen-induced structuralchange of the tetragonal phase around the tetragonal-cubic phase-boundary in ZrO2–YO1.5 Solid-solutions, Acta Crystallogr B Struct Sci., 1994, vol. 50, p. 663.
Yashima, M., Ohtake, K., Kakihana, M., Arashi, H., and Yoshimura, M., Determination of tetragonal-cubic phase boundary of Zr1 –xRxO2 –x/2 (R = Nd, Sm, Y, Er and Yb) by Raman scattering, J. Phys. Chem. Solids, 1996, vol. 57, p. 17.
Lipkin, D.M., Krogstad, J.A., Gao, Y., Johnson, C.A., Nelson, W.A., and Levi, C.G., Phase evolution upon aging of air plasma spray t'-zirconia coatings: I—synchrotron X-ray diffraction. J. Am. Ceram. Soc., 2013, vol. 96, p. 290.
Hemberger, Y., Wichtner, N., Berthold, Ch., and Nickel, K.G., Quantification of Yttria in Stabilized Zirconia by Raman Spectroscopy, Int. J. Appl. Ceram. Technol., 2016, vol. 13, p. 116.
Agarkov, D.A., Borik, M.A., Bublik, V.T., Bredikhin, S.I., Chislov, A.S., Kulebyakin, A.V., Kuritsyna, I.E., Lomonova, E.E., Milovich, F.O., Myzina, V.A., Osiko, V.V., and Tabachkova, N.Yu., Structure and transport properties of melt grown Sc2O3 and CeO2 doped ZrO2 crystals, Solid State Ionics, 2018, vol. 322, p. 24.
Дополнительные материалы отсутствуют.


