Электрохимия, 2020, T. 56, № 2, стр. 119-126
Смешанная ионно-электронная проводимость перовскитоподобных твердых растворов Ba1 – xSrxFe1 – yTiyO3 – δ и BaTi0.5Fe0.5 – zCezO3 – δ
В. А. Колотыгин a, *, А. П. Вискуп b, Е. В. Пивак c, В. В. Хартон a
a ИФТТ РАН
142432 Московская обл., Черноголовка, ул. академика Осипьяна, 2, Россия
b НИИ ФХР БГУ
220006 Минск, ул. Ленинградская, 14, Республика Беларусь
c Факультет материалов и инжиниринга керамики, Университет Авейро
3810-193 Авейро, Португалия
* E-mail: kolotygin@issp.ac.ru
Поступила в редакцию 28.09.2018
После доработки 10.12.2018
Принята к публикации 13.06.2019
Аннотация
В работе были изучены структурные особенности, электронная и ионная проводимость, а также термомеханические свойства перовскитоподобных соединений в системах Ba1 –xSrxFe1 –yTiyO3 – δ и BaTi0.5Fe0.5 –zCezO3 – δ. Показано, что кубическая структура сохраняется при замещении до 50% катионов стронция барием в А-подрешетке (Ва,Sr)(Fe,Ti)O3 – δ, в то время как при дальнейшем допировании кристаллическая решетка переходит в гексагональную модификацию. Введение церия в В-подрешетку в некоторой степени препятствует данному переходу. Замещение железа титаном или церием снижает электронную и ионную проводимость, благодаря уменьшению концентрации позиций в В-подрешетке, доступных для электронного переноса, а также более низкой кислородной нестехиометрии и большей энергией связей Ti–O и Ce–O по сравнению с Fe–O. Как правило, стабилизация кубической структуры способствует более высокой подвижности электронных и особенно ионных носителей заряда. Повышение концентрации бария в перовскитах (Ва,Sr)(Fe,Ti)O3 – δ с кубической структурой улучшает ионную проводимость, но при этом приводит к увеличению длины связи Fe–O и уменьшению степени перекрывания между атомами железа и кислорода, что вызывает снижение электронной проводимости. Коэффициенты термического расширения хорошо коррелируют с ионной проводимостью; минимальный уровень расширения наблюдается для составов с повышенным содержанием бария и гексагональной структурой. Показано, что кислородная проницаемость через плотные мембраны (Ва,Sr)(Fe,Ti)O3 – δ и Ва(Fe,Ti,Се)O3 – δ лимитируется кислородной диффузией в фазе мембраны и кинетикой кислородного обмена на поверхности.
ВВЕДЕНИЕ
Материалы на основе допированных ферритов могут рассматриваться в качестве катодов твердооксидных топливных элементов (ТОТЭ), а также керамических мембран для получения кислорода и парциального окисления метана, благодаря их стабильности в достаточно широком диапазоне р(О2) и сравнительно высокой электронной и ионной проводимости [1–13]. Среди Fe-содержащих оксидов с перовскитоподобными структурами наиболее высокий уровень параметров ионного переноса наблюдался для Sr(Fe,Co)O3 – δ и его производных, однако недостатком данной группы материалов является существенное ухудшение транспортных свойств при восстановлении, связанное с фазовым разложением и процессами упорядочения в кристаллической решетке. Кроме того, эти материалы обладают высокими коэффициентами термического расширения (КТР), что обуславливает механическую деградацию [1–5]. Допирование барием в некоторой степени подавляет упорядочение, сохраняя при этом хорошие транспортные свойства [3–5]. Однако перовскиты (Ba,Sr)(Fe,Co)O3 – δ подвержены низкотемпературному разложению с образованием многокомпонентной системы; при этом высокое содержание бария дестабилизирует материал в присутствии СО2 или паров воды [6–9].
Влияние радиуса А-катионов на кислородную нестехиометрию и ионную проводимость перовскитов в настоящий момент до конца не изучено, в то время как в литературных источниках отмечаются противоречия. Например, в работе [5] наблюдались более высокие кислородные потоки через мембраны Ba0.5Sr0.5Fe0.2Co0.8O3 – δ по сравнению со SrFe0.2Co0.8O3 – δ; с другой стороны, авторы [3] отмечали близкую проницаемость для обоих составов. Если для перовскитов (La,Ba)(Fe,Co)O3 – δ характерна более высокая кислородная нестехиометрия по сравнению с (La,Sr)(Fe,Co)O3 – δ [4], то для оксидов A(Fe,Ti)O3 – δ (А = Ca, Sr) уменьшение радиуса А-катиона приводит к более высокой кислородной нестехиометрии, предположительно обусловленной уменьшением стабильности перовскитной решетки и формированием микродоменов с упорядоченной структурой браунмиллерита [10]. Кроме того, увеличение радиуса катионов А-подрешетки может привести к повышенной подвижности ионов благодаря увеличению свободного пространства в кристаллической решетке [4]. Тем не менее, можно определенно отметить, что стабилизация перовскитной фазы с кубической решеткой способствует более высокой кислород-ионной проводимости.
Настоящая работа посвящена исследованию влияния катионного состава в А- и В-подрешетках перовскитов (Ba,Sr)(Fe,Ti)O3 – δ и Ba(Fe,Ti,Ce)O3 – δ на их структурные особенности, смешанную электронную и ионную проводимость, а также термомеханические свойства. Ожидалось, что высокий ионный радиус Ва2+ [14] позволит стабилизировать кубическую фазу, в то время как допирование титаном расширит диапазон р(О2), при котором ферриты устойчивы, минимизирует процессы упорядочения, снизит уровень термического и химического расширения [10–12, 15, 16]. Для изучения влияния замещения железа церием на структурные, транспортные и механические свойства был выбран модельный состав BaFe0.5Ti0.5O3 – δ.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Порошки и керамика Ba1 –xSrxFe1 –yTiyO3 – δ (х = 0.2; 0.5) и BaTi0.5Fe0.5 –zCezO3 – δ (z = 0.1; 0.3) были получены глицин-нитратным методом. К водному раствору глицина добавлялись стехиометрические количества Ва(NО3)2, Sr(NО3)2, FeС2О4 ∙ 2Н2О, Се(NО3)3 ∙ 6Н2О и TiO2, после чего проводилось перемешивание, выпаривание растворителя и термическое разложение на воздухе при нагреве до 1073 К. Порошки BaFe1 –yTiyO3 – δ (у = 0.2; 0.5) получали по стандартной керамической технологии из ВаС2О4, FеС2О4 ∙ 2Н2О и TiО2. Твердофазный синтез проводился при 1273–1473 К на воздухе с периодическим перетиранием шихты в ступке и перемалыванием в шаровой мельнице. Газоплотную керамику получали путем спекания спрессованных дисков на воздухе при 1483–1703 К в течение 2–10 ч, с последующим медленным охлаждением для достижения равновесия с газовой атмосферой.
Фазовый состав и структура полученных материалов изучались методом рентгенофазового анализа (РФА); примеры рентгенограмм представлены на рис. 1. Исследование материалов включало в себя высокотемпературную дилатометрию на воздухе, измерения полной электропроводности, кислородной проницаемости (КП) и чисел кислород-ионного переноса модифицированным методом Тубандта (МТ). Подробное описание методик экспериментов и схемы измерительных установок можно найти в [10, 13, 16]. Для измерений методами КП и МТ были изготовлены мембраны толщиной 0.60–1.40 мм и диаметром 10–12 мм, в то время как изучение электропроводности и дилатометрический анализ проводились на образцах в форме брусков 2 × 2 × 10 мм. Данные по КП были получены при атмосферном парциальном давлении кислорода на внешней поверхности мембраны (р2 = 0.21 атм); измерения методом МТ были получены при атмосферном давлении кислорода на обоих электродах. Для сравнения транспортных и термомеханических характеристик представлены данные, полученные в предыдущих работах для системы Sr0.97Fe1 –уTiуО3 – δ [10, 16].
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В соответствии с предыдущими работами [10, 16], материалы Sr0.97Fe1 –уTiуО3 – δ являются однофазными перовскитами с кубической решеткой. Эта структура сохраняется при введении как минимум 50% бария (рис. 1а, табл. 1); при избыточном содержании бария происходит образование фазы типа BaFeО2.8 с гексагональной структурой и ВаFe2О4. Составы BaFe1 –yTiyO3 – δ также имеют гексагональную структуру. Стоит отметить, что образование аналогичной фазы наблюдалось при увеличении содержания бария в (Ва,Sr)Со0.8Fe0.2О3 – δ [5]. Гексагональная структура, характерная для BaFeО2.8 [17], образована октаэдрами FeО6 с общими вершинами или ребрами, в то время как пустоты между октаэдрами, которые делятся на два типа с кристаллографической точки зрения, заполнены ионами бария (рис. 2).
Таблица 1.
Параметры решетки, фактор толерантности и свободный объем перовскитов Ba1 –xSrxFe1 –yTiyO3 – δ и BaTi0.5Fe0.5 –zCezO3 – δ. Данные представлены для материалов после спекания и медленного охлаждения на воздухе
| Состав | Пространственная группа | Параметры решетки | Vsf* | t* | |
|---|---|---|---|---|---|
| a, нм | c, нм | ||||
| Ba0.5Sr0.5Fe0.5Ti0.5O3 – δ | $Pm\bar {3}m$ | 0.39557(2) | – | 0.231 | 1.02 |
| BaFe0.5Ti0.5O3 – δ | ${{P{{6}_{3}}} \mathord{\left/ {\vphantom {{P{{6}_{3}}} {mmc}}} \right. \kern-0em} {mmc}}$ | 0.57032(1) | 1.40423(3) | 0.240 | 1.05 |
| BaFe0.8Ti0.2O3 – δ | ${{P{{6}_{3}}} \mathord{\left/ {\vphantom {{P{{6}_{3}}} {mmc}}} \right. \kern-0em} {mmc}}$ | 0.56878(2) | 1.40197(4) | 0.234 | 1.04 |
| BaTi0.5Fe0.4Ce0.1O3 – δ | ${{P{{6}_{3}}} \mathord{\left/ {\vphantom {{P{{6}_{3}}} {mmc}}} \right. \kern-0em} {mmc}}$ | 0.57418(2)** | 1.41162(6)** | ||
| 0.57682(4)** | 1.41348(8)** | ||||
| BaTi0.5Fe0.2Ce0.3O3 – δ | $Pm\bar {3}m$ | 0.41423(1) | – | 0.264 | 1.02 |
| Sr0.97Fe0.4Ti0.6O3 – δ | $Pm\bar {3}m$ | 0.3898(1) | – | 0.244 | 0.98 |
| Sr0.97Fe0.6Ti0.4O3 – δ | $Pm\bar {3}m$ | 0.3897(1) | – | 0.243 | 0.97 |
| Sr0.97Fe0.8Ti0.2O3 – δ | $Pm\bar {3}m$ | 0.3883(1) | – | 0.234 | 0.97 |
Чтобы найти взаимосвязь между составом исследуемых перовскитов, их структурными особенностями и транспортными свойствами, были рассчитаны такие стереологические характеристики, как фактор толерантности t и свободный объем Vsf в кристаллической решетке. В соответствии с работой [18], величина t рассчитывалась по формуле
(1)
$t = {{\left( {{{r}_{{\text{A}}}} + {{r}_{{\text{O}}}}} \right)} \mathord{\left/ {\vphantom {{\left( {{{r}_{{\text{A}}}} + {{r}_{{\text{O}}}}} \right)} {\sqrt 2 \left( {{{r}_{{\text{B}}}} + {{r}_{{\text{O}}}}} \right)}}} \right. \kern-0em} {\sqrt 2 \left( {{{r}_{{\text{B}}}} + {{r}_{{\text{O}}}}} \right)}},$(2)
${{V}_{{{\text{sf}}}}} = \frac{{{{V}_{{{\text{cell}}}}} - {4 \mathord{\left/ {\vphantom {4 3}} \right. \kern-0em} 3}{\pi }\sum\limits_i {{{n}_{i}}r_{i}^{3}} }}{{{{V}_{{{\text{cell}}}}}}}.$Для расчета вышеуказанных параметров рассматривались катионы Ba2+, Sr2+, Fe4+, Ti4+, Ce4+ и О2–, предполагая кислородное содержание равное 3 на формульную единицу, а также координационные числа А- и В-катионов, равные 12 и 6, соответственно. В работах [18, 19] было предположено, что больший свободный объем обеспечивает более высокую кислородную подвижность.
Как следует из табл. 1, замещение стронция барием в Ba1 –xSrxFe1 –yTiyO3 – δ приводит к увеличению параметров решетки и фактора толерантности, в соответствии с большим катионным радиусом Ва2+. При повышенном содержании бария величина t превышает критический уровень, допустимый для стабилизации кубической структуры, вследствие чего происходит образование гексагональной фазы. Поскольку ионный радиус Ti4+ превышает радиус Fe4+, при допировании титаном параметры решетки увеличиваются. Если предположения относительно степени окисления и координации катионов верны для всех составов, то минимальным свободным объемом среди изученных материалов обладает Ba0.5Sr0.5Fe0.5Ti0.5O3 – δ. Более объективная оценка требует точного знания кислородной нестехиометрии, поскольку, помимо влияния на степень окисления катионов, наличие вакансий может приводить к локальным искажениям в кристаллической решетке, влияющим на свободный объем и, как следствие, на ион-проводящие свойства.
При введении 10% церия в BaFe0.5Ti0.5O3 – δ гексагональная структура сохраняется, хотя наблюдается разложение на 2 изоструктурные фазы с различными параметрами решетки (рис. 1в). Согласно [20], для системы BaFe1 –zCezO3 – δ при 0.15 ≤ z ≤ 0.85 характерно образование смеси сложных оксидов, обогащенных церием или железом; разложение объясняется сильным различием радиусов Ce и Fe. Увеличение содержания церия в ВаТi0.5Fe0.5 –zСеzО3 – δ до z = 0.3 способствует образованию кубической структуры (рис. 1г), в соответствии с уменьшением фактора толерантности до 1.02, а также значительно повышает свободный объем.
На дилатометрических кривых (рис. 3) можно наблюдать типичное для ферритов увеличение наклона в высокотемпературной области [2, 15]. Данное поведение особенно ярко выражено для составов с повышенным содержанием железа и связано с интенсивным выходом кислорода их решетки, а также прогрессирующим разупорядочением вакансий в данных условиях. Величины КТР для (Ba,Sr)(Fe,Ti)O3 – δ в высокотемпературном регионе изменяются в пределах (20–29) × 10–6 K–1 (табл. 2); увеличение содержания титана снижает уровень расширения, что особенно характерно для перовскитов с высоким содержанием стронция.
Рис. 3.
Дилатометрические кривые, полученные для керамики Ba1 –xSrxFe1 –yTiyO3 – δ (а) и BaTi0.5Fe0.5 –zCezO3 – δ (б) на воздухе.

Таблица 2.
Коэффициенты термического расширения керамики Ba1 –xSrxFe1 –yTiyO3 – δ и BaTi0.5Fe0.5 –zCezO3 – δ на воздухе
| Состав | T, K | α × 106, K–1 |
|---|---|---|
| Ba0.5Sr0.5Fe0.5Ti0.5O3 – δ | 363–813 | 15.2 ± 0.1 |
| 813–1053 | 22.5 ± 0.1 | |
| BaFe0.5Ti0.5O3 – δ | 363–663 | 13.2 ± 0.3 |
| 663–1073 | 20.8 ± 0.3 | |
| BaFe0.8Ti0.2O3 – δ | 343–723 | 12.1 ± 0.3 |
| 723–1053 | 28.8 ± 0.2 | |
| BaTi0.5Fe0.4Ce0.1O3 – δ | 363–773 | 11.6 ± 0.1 |
| 773–1073 | 14.5 ± 0.1 | |
| BaTi0.5Fe0.2Ce0.3O3 – δ | 363–773 | 11.7 ± 0.1 |
| 773–1073 | 14.4 ± 0.1 | |
| Sr0.97Fe0.4Ti0.6O3 – δ | 303–723 | 11.7 ± 0.2 |
| 723–1073 | 16.6 ± 0.1 | |
| Sr0.97Fe0.8Ti0.2O3 – δ | 303–783 | 13.8 ± 0.1 |
| 783–1043 | 27.0 ± 0.4 |
Очевидно, что кубические перовскиты Sr0.97(Fe,Ti)O3 – δ подвержены более сильному влиянию температуры на концентрацию кислородных вакансий по сравнению с гексагональной фазой Ba(Fe,Ti)O3 – δ, поэтому стабилизация нестехиометрии при добавлении титана оказывает больший эффект на перовскиты с повышенным содержанием стронция. Допирование церием снижает КТР в высокотемпературной области до 14.5 × 10–6 K–1, при этом содержание церия слабо влияет на термомеханические свойства, несмотря на фазовые превращения (рис. 3б).
Образование кислородных вакансий при нагревании косвенно подтверждается наличием максимума на температурной зависимости полной проводимости (рис. 4). Замещение железа церием или титаном подавляет данный эффект, что согласуется с термомеханическим поведением. Проводимость Ba(Fe,Ti)O3 – δ существенно ниже по сравнению со стронций-замещенными аналогами, что может быть обусловлено влиянием параметров решетки на длину связи Fe–O и, как следствие, степень перекрывания атомов кислорода и железа, а также более благоприятными условиями для электронного переноса в кубической решетке. С другой стороны, высокотемпературное уменьшение проводимости менее существенно для материалов с повышенным содержанием бария, что подтверждает предположение о более слабых изменениях в них кислородной нестехиометрии.
Рис. 4.
Температурные зависимости полной удельной электропроводности керамики Ba1 –xSrxFe1 –yTiyO3 – δ (а) и BaTi0.5Fe0.5 –zCezO3 – δ (б) на воздухе. Рядом с кривыми указаны соответствующие энергии активации.
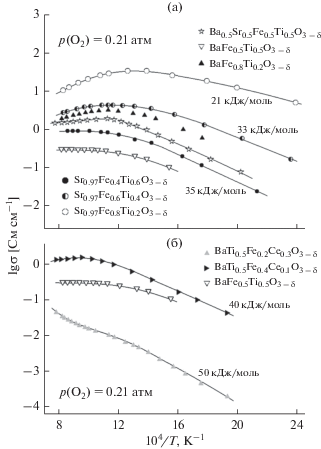
Допирование титаном уменьшает электронную проводимость и увеличивает соответствующую энергию активации (рис. 4, табл. 3). Влияние содержания церия на электропроводность менее очевидно (рис. 4б), вероятно, вследствие структурного перехода; тем не менее, энергия активации в низкотемпературной области увеличивается при добавлении церия. Наблюдаемое поведение предполагает, что на позициях в В-подрешетке, занятых титаном или церием, не могут локализоваться носители заряда из-за постоянной степени окисления Ti4+ и Се4+ в окислительной области. Допирование барием (в интервале сохранения кубической структуры) повышает энергию активации, предположительно благодаря увеличению длины связи Fe–O, что затрудняет электронный перенос.
Таблица 3.
Энергия активации полной удельной электропроводности и кислород-ионной проводимости керамики Ba1 –xSrxFe1 –yTiyO3 – δ и BaTi0.5Fe0.5 –zCezO3 – δ на воздухе
| Состав | Полная проводимость | Кислород-ионная проводимость | ||
|---|---|---|---|---|
| T, K | Ea, кДж/моль | T, K | Ea, кДж/моль | |
| Ba0.5Sr0.5Fe0.5Ti0.5O3 – δ | 483–853 | 37 ± 1 | 1173–1223 | 87 |
| 1113–1173 | 144 | |||
| BaFe0.5Ti0.5O3 – δ | 723–943 | 20 ± 2 | 1023–1233 | 192 ± 30 |
| BaFe0.8Ti0.2O3 – δ | 563–723 | 34 ± 5 | 1023–1223 | 102 ± 7 |
| 723–883 | 17 ± 2 | |||
| BaTi0.5Fe0.4Ce0.1O3 – δ | 523–863 | 40 ± 1 | 1173–1223 | 52 |
| 1113–1173 | 103 | |||
| BaTi0.5Fe0.2Ce0.3O3 – δ | 1033–1293 | 52 ± 4 | ||
| 773–1033 | 37 ± 2 | |||
| 523–773 | 50 ± 1 | |||
| Sr0.97Fe0.4Ti0.6O3 – δ | 473–893 | 35 ± 3 | 1073–1223 | 123 |
| 893–1123 | 11 ± 1 | |||
| Sr0.97Fe0.6Ti0.4O3 – δ | 333–763 | 33 ± 3 | 1123–1223 | 97 ± 21 |
| Sr0.97Fe0.8Ti0.2O3 – δ | 293–723 | 21 ± 1 | 1123–1223 | 76 ± 21 |
Отсутствие пропорциональности между кислородными потоками через мембраны Ba1 ‒ xSrxFe1 –yTiyO3 – δ и BaTi0.5Fe0.5 –zCezO3 – δ и их обратной толщиной (рис. 5) показывает, что кислородная проницаемость определяется как диффузией кислорода в объеме материала, так и кинетикой поверхностного обмена. Последний особенно критичен для Ba0.5Sr0.5Fe0.5Ti0.5O3 – δ при повышенных температурах и более высоком градиенте р(О2) между внешней и внутренней поверхностью мембраны, т.е., в условиях повышенной кислородной нестехиометрии. Стоит отметить, что совместное влияние диффузии и кинетики поверхностного кислородного обмена на проницаемость наблюдалось и для мембран Sr0.97(Fe,Ti,Mg)O3 – δ [16] и Ba(Fe,Ce)O3 – δ [20]. Величины кислород-ионной проводимости, рассчитанные из данных МТ или КП, в соответствии с методикой, приведенной в работе [21], представлены на рис. 6б. Ионная проводимость ниже для системы Ba(Fe,Ti)O3 – δ, что согласуется с предположением относительно влияния кристаллической структуры на ионный перенос. Несмотря на малый свободный объем, для перовскита Ba0.5Sr0.5Fe0.5Ti0.5O3 – δ наблюдалась наибольшая величина ионной проводимости. Из этого следует, что ионный перенос определяется рядом других факторов: концентрацией кислородных вакансий, локальными напряжениями и деформациями в кристаллической решетке, и взаимодействием между дефектами.
Рис. 5.
Зависимости кислородных потоков через плотные мембраны Ba0.5Sr0.5Fe0.5Ti0.5O3 –δ (а) и BaTi0.5Fe0.4Ce0.1O3 – δ (б) с различной толщиной от градиента парциального давления кислорода.
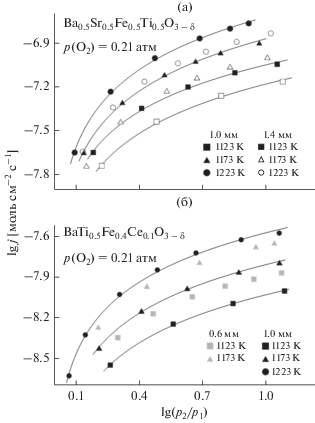
Рис. 6.
Температурные зависимости (а) кислородных потоков через плотные мембраны толщиной 1.00 мм при фиксированном градиенте p(O2) и (б) кислород-ионной проводимости, измеренной или рассчитанной для p(O2) = 0.21 атм. Рядом с кривыми указаны соответствующие энергии активации.

Допирование катионами титана снижает ионную проводимость и повышает соответствующую энергию активации. Известно, что Ti-содержащие соединения характеризуются низкой концентрацией кислородных вакансий, в то время как катионы Ti4+ оказывают блокирующее влияние на соседние кислородные атомы благодаря стабильной октаэдрической координации и большей энергии связи Ti–O [12, 22] . Аналогичное поведение наблюдается при замещении железа катионами Се4+, несмотря на стабилизацию кубической фазы для материала с z = 0.3. При температурах ниже 1173 К происходит небольшое увеличение энергии активации, более выраженное для оксидов с кубической структурой (рис. 6б). Наблюдаемое поведение типично для ферритов с высокой концентрацией кислородных вакансий и может быть обусловлено их упорядочением [5, 13].
Сравнивая значения кислородной проницаемости и кислород-ионной проводимости для изучаемых материалов с соответствующими величинами для ряда других известных ферритов, стоит отметить, что перовскит Ba0.5Sr0.5Fe0.5Ti0.5O3 – δ проявляет достаточно высокие параметры кислородного переноса. В частности, кислородные потоки через мембрану Ba0.5Sr0.5Fe0.5Ti0.5O3 – δ близки к потокам, наблюдаемым для перовскитов (La,Sr)FeO3 – δ; при этом исследуемое соединение, очевидно, в меньшей степени подвержено процессам упорядочения. Однако электронная проводимость исследуемых материалов, как правило, не превышает 10 См/см, что, наряду с высокими значениями КТР, ограничивает применение материалов в качестве катодов ТОТЭ. С другой стороны, можно ожидать, что стабилизация механических свойств путем изготовления композитной керамики позволит рассматривать данные материалы в качестве компонентов мембран для разделения кислорода или парциального окисления углеводородов.
ЗАКЛЮЧЕНИЕ
В работе показано, что умеренное замещение стронция более крупными катионами бария в (Ва,Sr)(Ti,Fe)O3 – δ сохраняет перовскитную структуру, увеличивает объем элементарной ячейки, а также способствует более высокой ионной проводимости. При содержании бария свыше 50% происходит образование гексагональной фазы с ухудшенными транспортными свойствами. Указанный переход можно предотвратить добавлением в В-подрешетку сравнительно крупных катионов Се4+/3+, однако снижение содержания железа приводит к ухудшению электронной и ионной проводимостей. Величины КТР в существенной мере определяются кислородными потерями при повышенных температурах, а также структурными особенностями. Показано отсутствие корреляции между транспортными свойствами и свободным объемом кристаллической решетки.
Список литературы
Teraoka, Y., Zhang, H.M., Furukawa, S., and Yamazoe, N., Oxygen permeation through perovskite-type oxides, Chem. Lett., 1985, vol. 14, p. 1743.
Petric, A., Huang, P., and Tietz, F., Evaluation of La–Sr–Co–Fe–O perovskites for solid oxide fuel cells and gas separation membranes, Solid State Ionics, 2000, vol. 135, p. 719.
Vente, J.F., Haije, W.G., and Rak, Z.S., Performance of functional perovskite membranes for oxygen production, J. Membr. Sci., 2006, vol. 276, p. 178.
Stevenson, J.W., Armstrong, T.R., Carneim, R.D., Pederson, L.R., and Weber, W.J., Electrochemical properties of mixed conducting perovskites La1 –xMxCo1 –yFeyO3 – δ (M = Sr, Ba, Ca), J. Electrochem. Soc., 1996, vol. 143, p. 2722.
Shao, Z., Xiong, G, Tong, J., Dong, H., and Yang, W., Ba effect in doped Sr(Co0.8Fe0.2)O3 – δ on the phase structure and oxygen permeation properties of the dense ceramic membranes, Sep. Purif. Technol., 2001, vol. 25, p. 419.
Švarcová, S., Wiik, K., Tolchard, J., Bouwmeester, H.J.M., and Grande, T., Structural instability of cubic perovskite BaxSr1 –xCo1 –yFeyO3 – δ, Solid State Ionics, 2008, vol. 178, p. 1787.
Ovenstone, J., Jung, J.I., White, J.S., Edwards, D.D., and Misture, S.T., Phase stability of BSCF in low oxygen partial pressures, J. Solid State Chem., 2008, vol. 181, p. 576.
Arnold, M., Gesing, T.M., Martynczuk, J., and Feldhoff, A., Correlation of the formation and the decomposition process of the BSCF perovskite at intermediate temperatures, Chem. Mater., 2008, vol. 20, p. 5851.
Yan, A., Liu, B., Dong, Y., Tian, Z., Wang, D., and Cheng, M., A temperature programmed desorption investigation on the interaction of Ba0.5Sr0.5Co0.8Fe0.2O3 – δ perovskite oxides with CO2 in the absence and presence of H2O and O2, Appl. Catal. B, 2008, vol. 80, p. 24.
Kharton, V.V., Figueiredo, F.M., Kovalevsky, A.V., Viskup, A.P., Naumovich, E.N., Jurado, J.R., and Frade, J.R., Oxygen diffusion and thermal expansion of SrTiO3 – δ- and CaTiO3 – δ-based materials, Defect. Diffus. Forum, 2000, vol. 186, p. 119.
Steinsvik, S., Bugge, R., Glonnes, J., Tafto, J., and Norby, T., The defect structure of SrTi1 –xFexO3 –y (x = 0–0.8) investigated by electrical conductivity measurements and electron energy loss spectoscopy (EELS), J. Phys. Chem. Solids, 1997, vol. 58, p. 969.
Park, C.Y., and Jacobson, A.J., Electrical conductivity and oxygen nonstoichiometry of La0.2Sr0.8Fe0.55Ti0.45O3 – δ, J. Electrochem. Soc., 2005, vol. 152, p. J65.
Kharton, V.V., Shaula, A.L., Viskup, A.P., Avdeev, M., Yaremchenko, A.A., Patrakeev, M.V., Kurbakov, A.I., Naumovich, E.N., and Marques, F.M.B., Perovskite-like system (Sr,La)(Fe,Ga)O3 – δ: structure and ionic transport under oxidizing conditions, Solid State Ionics, 2002, vol. 150, p. 229.
Shannon, R.D., Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides, Acta. Crystal., 1976, vol. A32, p. 751.
Fagg, D.P., Kharton, V.V., Kovalevsky, A.V., Viskup, A.P., Naumovich, E.N., and Frade, J.R., The stability and mixed conductivity in La and Fe doped SrTiO3 in the search for potential SOFC anode materials, J. Eur. Ceram. Soc., 2001, vol. 21, p. 1831.
Kharton, V.V., Viskup, A.P., Kovalevsky, A.V., Figueiredo, F.M., Jurado, J.R., Yaremchenko, A.A., Naumovich, E.N., and Frade, J.R., Surface-limited ionic transport in perovskites Sr0.97(Ti,Fe,Mg)O3 – δ, J. Mater. Chem., 2001, vol. 10, p. 1161.
Gomez, M.I., Lucotti, G., de Moran, J.A., Aymonino, P.J., Pagola, S., Stephens, P., and Carbonio, R.E., Ab Initio Structure Solution of BaFeO2.8 – δ, a New Polytype in the System BaFeOy (2.5 ≤ y ≤ 3.0) Prepared from the Oxidative Thermal Decomposition of BaFe[(CN)5NO] · 3H2O, J. Solid State Chem., 2001, vol. 160, p. 17.
Hayashi, H., Inaba, H., Matsuyama, M., Lan, N.G., Dokiya, M., and Takawa, H., Structural consideration on the ionic conductivity of perovskite-type oxides, Solid State Ionics, 1999, vol. 122, p. 10.
Mogensen, M., Lybye, D., Bonanos, N., Hendriksen, P.V., and Poulsen, F.W., Factors controlling the oxide ion conductivity of fluorite and perovskite structured oxides, Solid State Ionics, 2004, vol. 174, p. 279.
Zhu, X., Cong, Y., and Yang, W., Oxygen permeability and structural stability of BaCe0.15Fe0.85O3 – δ membranes, J. Membr. Sci., 2006, vol. 283, p. 38.
Marozau, I.P., Kharton, V.V., Viskup, A.P., Frade, J.R., and Samakhval, V.V., Electronic conductivity, oxygen permeability and thermal expansion of Sr0.7Ce0.3Mn1 –xAlxO3 – δ, J. Eur. Ceram. Soc., 2006, vol. 26, p. 1371.
Kolotygin, V.A., Tsipis, E.V., Shaula, A.L., Naumovich, E.N., Frade, J.R., Bredikhin, S.I., and Kharton, V.V., Transport, thermomechanical, and electrode properties of perovskite-type (La0.75 –xSr0.25 +x)0.95Mn0.5Cr0.5 –xTixO3 – δ, J. Solid State Electrochem., 2011, vol. 15, p. 313.
Дополнительные материалы отсутствуют.




