Электрохимия, 2022, T. 58, № 10, стр. 697-708
Металл-углеродные композиты на основе карбонизированного меламиноформальдегидного полимера и их электрокаталитические свойства
Н. М. Иванова a, *, З. М. Мулдахметов a, Е. А. Соболева a, Я. А. Висурханова a, Т. С. Животова a
a ТОО “Институт органического синтеза и углехимии Республики Казахстан”
Караганда, Казахстан
* E-mail: nmiva@mail.ru
Поступила в редакцию 27.01.2022
После доработки 04.04.2022
Принята к публикации 10.04.2022
- EDN: ZNPIVU
- DOI: 10.31857/S042485702210005X
Аннотация
Композиты металл/N-допированный углерод (М/C–N) получены с применением меламиноформальдегидного полимера (МФП), как источника C–N-углерода, и соли металла (Cu2+, Ni2+, Co2+) по двум методикам синтеза: 1 – введение соли металла in situ поликонденсации меламина с формальдегидом с дальнейшей термической обработкой при 400, 500 и 700°С, 2 – проведение химического восстановления катионов металла в присутствии карбонизированного МФ-полимера. Методами рентгенофазового анализа и электронной микроскопии проанализированы фазовые составы и морфологические особенности полученных композитов. Их электрокаталитические свойства изучены в процессе электрогидрирования ацетофенона. Установлена более высокая электрокаталитическая активность композитов Cu/C–N, приготовленных по методике 2, благодаря дополнительному восстановлению катионов меди в электрохимической системе. Синтез композитов по методике 1 и их термическая обработка приводят к формированию оксидов металлов и их восстановленных форм, находящихся большей частью внутри углеродной матрицы карбонизированного МФ-полимера.
ВВЕДЕНИЕ
В последние два десятилетия особое внимание уделяется созданию каталитических систем из наночастиц металлов, нанесенных на углеродный носитель, модифицированный гетероатомами, в качестве которых наиболее часто используется азот (C–N-углеродный носитель) [1–4]. Многими исследованиями показано, что введение азота в углеродный материал повышает полярность углеродной матрицы, улучшает взаимодействие наночастиц металла с C–N-носителем, стабилизирует наночастицы металла, что способствует улучшению его адсорбционных, каталитических, электрохимических и др. физико-химических свойств [1–7]. Выделяют два основных способа получения металл-углеродных материалов, допированных азотом [2]: первый – нанесение металла на предварительно приготовленный C–N-углеродный материал, что возможно выполнить различными методами, включая импрегнирование, осаждение, золь-иммобилизацию и др.; второй – одновременное введение металла и азота в углеродный носитель. Второй способ предполагает проведение карбонизации смешанных друг с другом прекурсоров гетероатома, металла и углеродного материала и считается наиболее простым для создания катализаторов типа металл/допированный гетероатомом пористый углерод [3].
Как пример первого способа создания M/C–N-катализаторов можно привести работу [8], в которой описано получение катализаторов из наночастиц Pt, нанесенных на допированный азотом пористый углерод, приготовленный в результате термической обработки сажи (carbon black) и цианамида, проявивших высокую эффективность в реакции восстановления кислорода. Отмечено, что на поверхности допированного азотом углеродного носителя появляются дополнительные активные центры, способствующие равномерному распределению наночастиц платины и уменьшению их размеров (1.90–2.99 нм), что повышает эффективность Pt/C–N-катализаторов. В качестве углеродного материала в этом способе часто используют функционализированные углеродные нанотрубки, графен и другие современные углеродные наноматериалы [9–11].
Ко второму способу получения металл-углеродных допированных азотом композитов относится проведение совместной термической обработки азотсодержащего полимера и прекурсора металла. Подобным образом были приготовлены металл-углеродные нанокомпозиты на основе полиакрилонитрила и соли металла путем их совместного инфракрасного нагрева [12, 13]. Селективные электрокатализаторы восстановления нитробензола в анилин – металлы Fe, Co, Cu на N-допированном углеродном носителе – были приготовлены путем карбонизации полианилина, синтезированного в присутствии активированного угля и прекурсора металла [14]. Авторами было установлено, что в структуре пиролизованного углеродного материала содержатся атомы азота пиридиновой, пиррольной и других конфигураций. По подобной методике были получены также PANI–M–C-катализаторы (M = Fe и/или Co), в которых агрегаты металлов инкапсулированы в оболочку графитизированного углерода [15].
В данной работе приведены результаты исследований по созданию металл-углеродных композитов (Cu/C–N, Ni/C–N, Co/C–N) на основе меламиноформальдегидного полимера (МФП) и нитратов соответствующих металлов по двум выше упомянутым способам. Изучена их электрокаталитическая активность в электрогидрировании ацетофенона (АФ) как модельного соединения.
Следует отметить, что получение N-допированных углеродных материалов на основе МФ-полимера, как источника углерода с большим содержанием азота, и металл-углеродных композитов и их применение описаны в ряде работ [16‒22]. Например, в работе [16] изучен процесс превращения МФ-полимера в N-углерод в виде сферических микросфер с помощью его пиролиза при 400–1000°С в атмосфере аргона. N-допированный пористый углерод был получен также карбонизацией МФ-полимера, сшитого фитиновой кислотой [17], или с добавлением резорцинола и триблок-сополимера (Pluronic F 127) [18], или нанографита [19] и др. Целью этих исследований было получение новых материалов, обладающих химической и термической стойкостью, высокой сорбционной емкостью, электропроводностью, или являющихся эффективными электрокатализаторами в реакции восстановления кислорода, или проявляющих другие практически важные свойства.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для синтеза исходного меламиноформальдегидного полимера была использована методика, разработанная нами для получения полимер-металлических композитов на его основе [23]:
К меламину (0.1 моль или 12.6 г) приливают 32.0 мл (0.4 моль) 34%-ного раствора формалина и 1.0 мл 10%-ного раствора NaOH (до рН 10). Смесь перемешивают при 80°C в течение 20 мин. Образуется прозрачный раствор. Затем приливают 20 мл 4%-ного водного раствора щавелевой кислоты. Перемешивают 15 мин, и постепенно выпадает плотный белый осадок. Осадок фильтруют, промывают дистиллированной водой, сушат при 80°C до постоянной массы и измельчают. Кислоту в ходе синтеза МФП добавляют с целью отверждения и получения химически стойкого полимера, в котором триазиновые фрагменты связаны между собой, главным образом, через метиленовые мостики.
Металл-углеродные композиты были получены сначала вторым из вышеупомянутых способов. Методика 1 – введение соли металла in situ поликонденсации меламина с формальдегидом. При этом, после взаимодействия меламина с формальдегидом в образовавшийся прозрачный раствор добавляют по каплям 20 мл водного раствора соли металла (Cu(NO3)2·3H2O, Ni(NO3)2·6H2O, Co(NO3)2·3H2O) с содержанием металла 3.6 г. Перемешивают смесь 20 мин. Добавляют 5.5 г щавелевой кислоты (H2C2O4·2H2O), растворенной в 30 мл дистиллированной воды и перемешивают 15 мин при 80°C. Выпадает осадок, который фильтруют и промывают дистиллированной водой комнатной температуры. Осадок высушивают при 80°C, тщательно измельчают. Затем металлсодержащий МФП-композит делят на 3 равные части и в корундовых тиглях с закрытой крышкой выдерживают в электропечи (Накал, Россия) при 500, 700 и 900°C в течение 2 ч.
В синтезах металл-углеродных композитов количество щавелевой кислоты было увеличено в соответствии с уравнениями реакций с целью осаждения всего количества введенного металла в виде его оксалата (MC2O4) и образования композитов МФП + MC2O4 с последующей термической обработкой (ТО).
Затем был реализован первый из вышеописанных способов получения металл-углеродных композитов. Методика 2 – проведение химического восстановления катионов металлов из их солей в присутствии МФ-полимера, карбонизированного при 500°С (МФ-сажи). Для этого в 100 мл водно-этанольного раствора (соотношение H2O/спирт равно 1 : 1 по объему) вводят МФ-сажу массой 2.0, 1.0 или 4.0 г и тщательно перемешивают в течение 1 ч. Затем добавляют соль металла (были использованы нитраты металлов) с содержанием металла 2.0 г. Продолжают перемешивание с постепенным поднятием температуры до определенных значений, рекомендуемых для восстановления катионов металлов гидразингидратом: 60°C (Cu2+), 90°C (Ni2+), 90°C (Co2+) [24]. Затем при постоянном перемешивании по каплям добавляют щелочной раствор гидразингидрата (37 мл 64%-ного N2H4∙H2O и 20 мл 12%-ного водного раствора NaOH). После завершения восстановления реакционную смесь фильтруют, промывают дистиллированной водой и этиловым спиртом, нагретыми до 40°C, сушат при 80°C и давлении 0.06 МПа.
Для определения влияния полимерного стабилизатора на формирующиеся ультрадисперсные частицы металлов по этой же методике были получены МФС + М композиты с добавлением в реакционную среду поливинилового спирта (ПВС). Кроме того, с целью уменьшения размера частиц сажи, полученной карбонизацией МФ-полимера при 500°С, была проведена их предварительная ультразвуковая обработка (УЗО) в течение 30 мин, затем были также получены композиты МФС + М + УЗО.
Все синтезированные металл-углеродные композиты были изучены на проявление электрокаталитической активности в электрогидрировании ацетофенона. Условия проведения экспериментов аналогичны описанным в работе [25], в которой представлены результаты исследований электрокаталитических свойств полианилин-медных композитов. Так, эксперименты были выполнены в диафрагменной ячейке в спиртово-водно-щелочном растворе при силе тока 1.5 А и температуре 30°С. Катод – медная пластина (площадью 0.05 дм2), прилегающая ко дну электролизера, на которую наносили порошки металл-углеродных композитов (без закрепления) массой 1 г. Под катодом с внешней стороны электролизера помещался магнит (магнитная индукция создаваемого магнитного поля ~0.05 Тл). Анодом служила платиновая сетка. Начальная концентрация АФ составляла 0.198 моль/л. Нанесенные на катод композиты сначала насыщались водородом. В ходе насыщения водородом осуществлялось электрохимическое восстановление катионов металлов, содержащихся в композитах, которые способны к электрохимическому восстановлению в заданных условиях. Насыщение водородом композита осуществлялось до установления соотношения выделяющихся газов V(H2) : V(O2) = 2 : 1. Затем в католит вносилось органическое вещество, и происходило (или нет) его электрокаталитическое гидрирование на частицах металлов, восстановленных в ходе карбонизации композитов (по методике 1) или в результате химического (по методике 2) или электрохимического восстановления их катионов. Продукты гидрирования экстрагировали из католита хлороформом, полученную вытяжку анализировали с помощью хроматографа “Кристаллюкс-4000М” (Мета-хром, Россия).
Фазовые составы синтезированных металл-углеродных композитов после ТО и после электрохимических экспериментов определяли на дифрактометрах ДРОН-2 (Буревестник, Россия) и D8 ADVANCE ECO (Bruker, Германия) с использованием CuKα-излучения в диапазоне углов (2θ) 15°–90°. Их морфологические особенности были изучены с помощью растрового сканирующего электронного микроскопа TESCAN MIRA 3 LMU (TESCAN, Чехия), элементный анализ некоторых образцов был проведен методом энергодисперсионной рентгеновской спектроскопии (ЭДС) с помощью прибора X-Act – 10 mm2 SDD Detector (Oxford Instruments Inc.). Термогравиметрические исследования (ТГА) проводили на дериватографе Q-1500D (MOM, Венгрия). Удельную площадь поверхности полимерных образцов определяли методом БЭТ (Брунауэра, Эммета и Теллера) по изотермам адсорбции–десорбции азота на приборе Sorbi MS (МЕТА, Россия).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
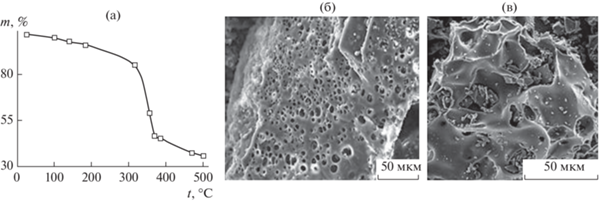
Согласно ТГА-исследованиям (рис. 1а), проведенным в кислородной атмосфере, наибольшие потери массы МФ-полимера происходят в области температур 300–380°С, затем потери замедляются и к 500°С достигают почти 65%. Из полимера удаляются формальдегид, метанол, аминогруппы; триазиновые кольца соединяются между собой, и образуются продукты конденсации меламина (мелем, мелам и др.) [14].
Удельная площадь поверхности образца МФП (500°С) (рис. 1в) составляет 13.2 ± 0.8 м2/г, при ультразвуковой обработке (при частоте 22 кГц в течение 60 мин) она незначительно увеличивается: 23.5 ± 0.6 м2/г. Исходный МФ-полимер, синтезированный по описанной выше методике, имеет довольно плотное и, в то же время, пористое строение (рис. 1б).
Согласно рентгенофазовым анализам (РФА), составы композитов МФП + M(NO3)2 (M = Cu2+, Ni2+, Co2+), синтезированных методом in situ (по методике 1) и после синтезов содержащих оксалаты металлов, после ТО имеют некоторые отличия, определяемые температурой ТО. Фазовые составы медьсодержащих композитов МФП + + Cu(NO3)2, выдержанные при 400 и 500°С, представлены кристаллическими фазами оксидов меди(I, II) и углеродной сажей, количество которой с повышением температуры ТО уменьшается (рис. 2, 1а–3а). При термолизе этого композита при 700°С, во-первых, появляются кристаллические фазы меди, восстановленной продуктами распада МФ-полимера, во-вторых, увеличивается содержание оксида Cu2O (рис. 2, 3а).
Рис. 2.
Рентгенограммы композита МФП + Cu(NO3)2, термически обработанного при 400 (1), 500 (2) и 700°С (3), до (а) и после (б) электрогидрирования АФ.

В этих же композитах после насыщения водородом в электрохимической ячейке и электрогидрирования АФ (рис. 2б) снижается содержание CuO, повышается количество Cu2O и появляются кристаллические фазы меди, как результат электрохимического восстановления из ее оксидов. В составе МФП-композита, обработанного при 700°С, заметно возрастает содержание восстановленной меди и снижается количество оксида CuO (рис. 2, 3б).
Термическая обработка композитов МФП + + Ni(NO3)2 и МФП + Co(NO3)2 при 400 и 500°C сопровождается образованием оксидов металлов (NiO, Co3O4); при 700°C в составе этих композитов помимо оксидов появляются кристаллические фазы восстановленных металлов (рис. 3), образующихся под действием продуктов распада полимера.
Практически такой же фазовый состав Ni-содержащего композита сохраняется после электрохимических экспериментов, в составе Co-содержащего композита появляются кристаллические фазы гидроксида кобальта (β-Co(OH)2) при снижении содержания его оксидов.
Микроснимки композита МФП + Cu(NO3)2 (500°C) (а) после ТО (рис. 4а) показывают, что медно-оксидные образования имеются как на поверхности частиц МФП-сажи, так и в приповерхностном слое. Кроме того, имеются отдельные агломераты из округлых частиц, образованных мелкими чешуйками из CuO или Cu2O. Результаты ЭДС-анализов для этого композита подтвердили высокое содержание азота и углерода в нем (рис. 4а), при этом на многослойной карте исследованного участка было видно, что вся его поверхность покрыта слоем углерода. Морфологическое строение композита МФП + Ni(NO3)2 (500°C) (рис. 4б) подобно строению Cu-содержащего композита – часть формирующихся кристаллитов оксида никеля NiO расположена в матрице карбонизированного полимера, имеются также отдельные агломераты из частиц NiO или никеля, покрытых его оксидом.
Композиты МФП + M(NO3)2, синтезированные по методике 1, были проверены на проявление электрокаталитической активности в процессе электрогидрирования ацетофенона (C6H5‒CO‒CH3). Полученные результаты собраны в табл. 1, в которой приведены такие характеристики исследуемых процессов, как объем поглощенного водорода $({{V}_{{{{{\text{H}}}_{{\text{2}}}}}}})$ при насыщении им композитов, продолжительность насыщения водородом (τ), средняя скорость гидрирования (W) за период прохождения процесса α = 25% и степень превращения АФ, или его конверсия (α). Для сравнения приведены также данные по электрохимическому восстановлению АФ на Cu-катоде в условиях, указанных в Экспериментальной части. Согласно этим данным, электрогидрирование АФ осуществляется с малой степенью превращения и с образованием, в основном, димерных продуктов – пинаконов (ПК). Здесь же приведены результаты хроматографических анализов.
Таблица 1.
Результаты электрокаталитического гидрирования ацетофенона на композитах МФП + М(NO3)2, полученных методом in situ
| МФП-композиты | Электрохимическое восстановление | Электрокаталитическое гидрирование АФ | Состав продуктов, % | ||||
|---|---|---|---|---|---|---|---|
| τ, мин | ${{V}_{{{{{\text{H}}}_{2}}}}}$, мл | W, мл Н2/мин (α = 0.25) | α, % | МФК | АФ | ПК | |
| Cu-катод | 0 | 0.0 | 2.0 | 28.1 | 4.4 | 49.9 | 45.7 |
| МФП + Cu(NO3)2 (400oC) | 20 | 51.8 | 2.3 | 43.2 | 42.1 | 50.2 | 6.8 |
| МФП + Cu(NO3)2 (500oC) | 20 | 42.8 | 1.9 | 41.9 | 43.0 | 29.9 | 24.6 |
| МФП + Cu(NO3)2 (700oC) | 20 | 142.4 | 4.6 | 54.1 | 61.6 | 32.9 | 4.8 |
| МФП + Ni(NO3)2 | 0 | 0.0 | 0.0 | 0.0 | – | – | – |
| МФП + Co(NO3)2 (700oC) | 30 | 12.5 | 5.2 | 100.0 | 97.5 | 2.5 | – |
Выполненными экспериментами установлено отсутствие электрокаталитической активности у всех трех Ni-содержащих и двух Co-содержащих композитов МФП, что подтверждает ранее сделанные выводы о неспособности катионов никеля к электрохимическому восстановлению в аналогичных условиях [26]. К тому же, в полученных по этой методике МФП-композитах поверхность сформированных при ТО частиц восстановленных металлов частично закрыта продуктами карбонизации полимера, или оксидами этих металлов. Насыщение водородом композитов МФП + + Cu(NO3)2 сопровождается электрохимическим восстановлением катионов меди из ее оксидов (что следует из значений ${{V}_{{{{{\text{H}}}_{{\text{2}}}}}}}$ в табл. 1) и образованием меди в нуль-валентном состоянии (рис. 2). Образец с ТО при 700°С, в котором восстановление катионов меди прошло более полно, проявил более высокую активность. В продуктах гидрирования снизилось содержание пинаконов и повысились выходы метилфенилкарбинола (МФК). Однако лучшие характеристики исследуемого процесса получены при применении композита МФП + Co(NO3)2 (700°C): скорость гидрирования повысилась до 5.2 мл H2/мин, конверсия АФ достигла максимального значения, что обусловлено присутствием частиц термически восстановленного кобальта в этом композите с доступной каталитической поверхностью.
Согласно РФ-анализам композитов МФС + М, полученных по методике 2, в их составах имеются кристаллические фазы химически восстановленных металлов, небольшие примеси оксида меди (CuO), гидроксида никеля (Ni(OH)2) и существенно с большим содержанием гидроксида кобальта (β-Co(OH)2) (рис. 5, 1а–3а). Средние размеры частиц для основной фазы (111) металлов, вычисленные по формуле Шеррера с помощью программного обеспечения дифрактометра D8 ADVANCE ECO, составляют ~30 нм для Cu, 18 нм для Ni и 44 нм для Co. Следует отметить, что кристаллические фазы восстановленного в заданных условиях кобальта соответствуют кристаллической модификации β-Co с кубической гранецентрированной решеткой (fcc-Co), которая является менее стабильной, чем α-модификация с гексагональной плотноупакованной решеткой (hcp-Co) [27].
Рис. 5.
Рентгенограммы композитов МФС(1) + M(1) (M = Cu (1), Ni (2), Co (3)) после синтезов (а) и после электрогидрирования АФ (б).

Микроскопические исследования синтезированных композитов МФС(1) + М(1) показали, что на поверхности довольно крупных частиц МФ-сажи расположены агломерированные металлсодержащие частицы, образующие кристаллы различной формы. Так, в медьсодержащем композите присутствуют кристаллоподобные образования без определенной формы, а также можно разглядеть тонкие медные пластинки, концентрирующиеся в клубки для формирования, по-видимому, более крупных кристаллических структур (рис. 6а). На микроснимках композита МФС + Ni (рис. 6б) хорошо видны скопления округлых образований с острыми выступами, состоящих из отдельных зерен и остроконечных пластинок никеля. Размеры таких колючих клубков составляют ~100–600 нм. На поверхности частиц МФ-сажи присутствуют также плотно прилегающие к ней металлические полусферы диаметром 200–500 нм. На втором микроснимке хорошо просматривается структура МФ-сажи, образующейся из МФ-полимера в ходе ТО при 500°С.
Подобные полусферы образуются также на частицах сажи в Co-содержащем композите (рис. 6в). ЭДС-анализы на участке такой полусферы показали наличие следующих химических элементов (по убыванию их содержания): Co, C, O, N и в незначительном количестве Na. На первых двух микроснимках этого композита (рис. 6в), выполненных с применением детектора отраженных электронов (backscattered electrons, BSE), наиболее светлые участки – это частицы кобальта. Можно предположить, что полусферы на поверхности сажи – это также частицы кобальта, вырастающие в месте локализации N- атомов в структуре сажи. В этом же композите присутствуют пластинчатые кристаллиты с неровными краями, принадлежащие, по-видимому, гидроксиду кобальта (β-Co(OH)2), кристаллические фазы которого были также обнаружены РФ-анализами (рис. 5, 3).
Металлоуглеродные композиты МФС + М, полученные в результате восстановления катионов металлов в присутствии частиц сажи, образующейся в ходе ТО МФ-полимера при 500°С (методика 2), также были изучены на проявление электрокаталитической активности в электрогидрировании АФ. Результаты представлены в табл. 2.
Таблица 2.
Результаты электрокаталитического гидрирования ацетофенона на композитах МФС(500°С) + М (M = Cu, Ni, Co)
| МФС-композиты | Содержание M в 1 г композита, г | Электрохимическое восстановление | Электрокаталитическое гидрирование АФ | Состав продуктов, % | ||||
|---|---|---|---|---|---|---|---|---|
| τ, мин | ${{V}_{{{{{\text{H}}}_{2}}}}}$, мл | W, мл Н2/мин (α = 0.25) | α, % | МФК | АФ | ПК | ||
| Cu-катод | – | 0 | 0.0 | 2.0 | 28.1 | 4.4 | 49.9 | 45.7 |
| Cu | 1.000 | 10 | 13.3 | 7.6 | 95.9 | 94.5 | 2.4 | 3.1 |
| МФС(1) + Cu(1) | 0.506 | 20 | 43.2 | 8.2 | 95.0 | 96.7 | 0.8 | 2.2 |
| МФС(1) + Cu(1) + УЗО | 0.494 | 10 | 3.1 | 7.9 | 96.4 | 96.1 | 1.7 | 2.2 |
| МФС(1) + Cu(1) + ПВС | 0.529 | 10 | 12.6 | 6.6 | 97.8 | 97.0 | 0.7 | 2.3 |
| МФС(2) + Cu(1) | 0.314 | 20 | 40.5 | 8.0 | 98.2 | 95.1 | 4.4 | 0.5 |
| МФС(3) + Cu(1) | 0.233 | 20 | 42.3 | 7.8 | 97.3 | 96.6 | 1.2 | 0.7 |
| МФС(1) + Cu(2) | 0.678 | 10 | 25.6 | 7.4 | 98.1 | 98.0 | 2.0 | – |
| Ni | 1.000 | 0 | 0.0 | 5.7 | 95.9 | 98.3 | 1.7 | – |
| МФС(1) + Ni(1) | 0.508 | 0 | 0.0 | 4.5 | 94.6 | 96.8 | 3.2 | – |
| МФС(1) + Ni(1) + УЗО | 0.480 | 0 | 0.0 | 3.5 | 84.2 | 92.1 | 7.4 | 0.5 |
| МФС(1) + Ni(1) + ПВС | 0.474 | 0 | 0.0 | 2.8 | 84.9 | 94.3 | 5.7 | – |
| МФС(2) + Ni(1) | 0.341 | 0 | 0.0 | 0.0 | 0.0 | – | – | – |
| МФС(1) + Co(1) | 0.446 | 30 | 12.7 | 3.9 | 80.1 | 85.8 | 13.4 | 0.8 |
| МФС(1) + Co(1) + УЗО | 0.457 | 20 | 21.8 | 4.8 | 85.7 | 92.4 | 7.6 | – |
| МФС(1) + Co(1) + ПВС | 0.388 | 0 | 0.0 | 2.3 | 87.3 | 90.0 | 10.0 | – |
| МФС(2) + Co(1) | 0.309 | 10 | 4.2 | 2.6 | 75.7 | 78.8 | 20.3 | 0.9 |
Из данных табл. 2 следует, что поглощение водорода при нанесении порошковых МФС-композитов на Cu-катод осуществляется почти всеми медьсодержащими композитами, что указывает на прохождение дополнительного восстановления катионов меди в электрохимической ячейке. Небольшие объемы водорода поглощаются также Co-содержащими композитами, но, как следует из рентгенограммы этого композита (рис. 5, 3в), повышение содержания восстановленного кобальта после электрохимических экспериментов не наблюдается. По-видимому, этот водород расходуется на побочные процессы, осуществляемые с этим композитом в щелочной среде. Дополнительного электрохимического восстановления катионов никеля также не происходит. Более того, добавление ПВС-стабилизатора в ходе синтезов снижает его активность, а при увеличении содержания МФ-сажи в композите МФС(2) + Ni(1) он становится каталитически неактивным. Можно предположить, что продукты карбонизации МФ-полимера при 500оС, в структуре которых имеются C=N-связи, довольно сильно взаимодействуют с никелем и его оксидом, и при повышении их содержания они закрывают поверхность никеля.
Согласно данным табл. 2, все полученные МФС-композиты проявили электрокаталитическую активность в исследуемом процессе. Наиболее интенсивно электрогидрирование АФ проходит в присутствии композитов МФС + Cu. На примере этих же композитов установлено, что увеличение содержания МФ-сажи в них приводит к некоторому снижению скорости гидрирования АФ и почти не влияет на степень превращения АФ с образованием МФК. Электрокаталитическое гидрирование АФ на Ni- и Co-содержащих МФС-композитах осуществляется медленнее и с незначительно меньшей степенью превращения АФ, чем на Cu-содержащих композитах. Однако, по хроматографическим данным (табл. 2), выходы МФК остаются высокими при практически полном отсутствии побочных димерных продуктов. Предварительная ультразвуковая обработка МФ-сажи оказала благоприятное влияние только в электрогидрировании АФ с применением МФС-композита с кобальтом и его гидроксидом.
Сравнение медь- и никельсодержащих N-углеродных композитов по их электрокаталитической активности в исследуемом процессе с частицами этих металлов, синтезированных в одних и тех же условиях и без углеродного носителя, является неоднозначным. Композиты МФС + Cu демонстрируют лучшую активность, чем частицы Cu, несмотря на меньшее содержание меди в 1 г композитов, наносимых на катод (табл. 1). Композиты МФС + Ni заметно менее активны, чем частицы Ni. Другими словами, электрокаталитическая активность металл-углеродных композитов в заданных условиях электрогидрирования АФ определяется как способом их получения, так и природой металла, его взаимодействием с углеродным носителем и его способностью к электрохимическому восстановлению.
ЗАКЛЮЧЕНИЕ
Таким образом, выполненными исследованиями установлена более высокая электрокаталитическая активность Cu-углеродных и наличие такой активности у Ni-углеродных допированных азотом композитов, приготовленных методом химического восстановления катионов металлов в присутствии МФ-сажи (по методике 2), чем у M/C–N-композитов этих металлов, полученных методом in situ (по методике 1). Электрокаталитическая активность Co-углеродного композита (с термической обработкой при 700°С), наоборот, немного выше, чем у полученных методом in situ. Показано, что композиты Cu/C–N проявляют лучшую активность в электрогидрировании АФ, чем Ni/C–N- и Co/C–N-композиты, благодаря способности катионов меди к электрохимическому восстановлению в заданных условиях. Сделано предположение о более сильном взаимодействии никеля и его оксида, а также кобальта и его оксидов с продуктами карбонизации меламиноформальдегидного полимера, что также влияет на электрокаталитические свойства формирующихся Ni/C–N- и Co/C–N-композитов. В целом, проведенными исследованиями показана возможность применения металл/N-допированных углеродных композитов, полученных на основе карбонизированного МФ-полимера, в качестве электрокатализаторов в электрогидрировании органических соединений. Их эффективность определяется методикой приготовления, природой и свойствами вводимого металла.
Список литературы
Mabena, L.F., Ray, S.S., Mhlanga, S.D., and Coville, N.J., Nitrogen-doped carbon nanotubes as a metal catalyst support, Appl. Nanosci., 2011, vol. 1, p. 67.
He, L., Weniger, F., Neumann, H., and Beller, M., Synthesis, characterization, and application of metal nanoparticles supported on nitrogen-doped carbon: catalysis beyond electrochemistry, Angew. Chem. Int. Ed., 2016, vol. 55, p. 2.
Rangraz, Ya., Heravi, V.V., and Elhampour, A., Recent advances on heteroatom-doped porous carbon/metal materials: fascinating heterogeneous catalysts for organic transformations, Chem. Rec., 2021, vol. 21, p. 1.
Thakur, A.K., Kurtyka, K., Majumder, M., Yang, X., Ta, H.Q., Bachmatiuk, A., Liu, L., Tizebicka, B., and Rummeli, M.H., Recent advances in boron- and nitrogen-doped carbon-based materials and their various applications, Adv. Mater. Interfaces, 2022, article number: 2101964, 27 p.
Shen, W.Z. and Fan, W.B., Nitrogen-containing porous carbons: synthesis and application, J. Mater. Chem. A, 2013, vol. 1, p. 999.
Majeed, S., Zhao, J., Zhang, L., Anjum, S., Liu, Zh., and Xu, G., Synthesis and electrochemical applications of nitrogen-doped carbon nanomaterials, Nanotechnol. Rev., 2013, vol. 2, p. 615.
Wei, Q., Tong, X., Zhang, G., Qiao, J., Gong, Q., and Sun, Sh., Nitrogen-doped carbon nanotube and graphene materials for oxygen reduction reactions, Catalysts, 2015, vol. 5, p. 1574.
Tachibana, N., Yukawa, Y., Morikawa, K., Kawaguchi, M., and Shimanoe, K., Pt nanoparticles supported on nitrogen-doped porous carbon as efficient oxygen reduction catalysts synthesized via a sample alcohol reduction method, SN Appl. Sci., 2021, vol. 3, p. 338.
Zhu, Q.-L. and Xu, Q., Immobilization of ultrafine metal nanoparticles to high-surface-area materials and their catalytic applications, Chem., 2016, vol. 1, p. 220.
Wu, G., Santandreu, A., Kellogg, W., Gupta, Sh., Ogoke, O., Zhang, H., Wang, H.-L., and Dai, L., Carbon nanocomposite catalysts for oxygen reduction and evolution reaction: From nitrogen doping to transition-metal addition, Nano Energy, 2016, vol. 29, p. 83.
Sundaram, R.M., Sekiguchi, A., Sekiya, M., Yamada, T., and Hata, K., Copper/carbon nanotube composites: research trends and outlook, R. Soc. open sci., 2018, vol. 5, article number: 180814.
Кожитов, Л.В., Козлов, В.В., Костиков, А.В., Попкова, А.В. Новые металлоуглеродные нанокомпозиты и углеродный нанокристаллический материал с перспективными свойствами для развития электроники. Материалы электрон. техники. 2012. № 3. С. 59. [Kozhitov, L.V., Kozlov, V.V., Kostikov, A.V., and Popkova, А.V., New metal-carbon nanocomposites and carbon nanocrystalline material with promising properties for the development of electronics, Materialy elektronnoy tekhniki (in Russian), 2012, no. 3, p. 59.]
Муратов, Д.Г., Якушко, Е.В., Кожитов, Л.В., Попкова, А.В., Пушкарев, М.А. Формирование нанокомпозитов Ni/C на основе полиакрилонитрила под действием ИК-излучения. Материалы электрон. техники. 2013. № 1. С. 61. [Muratov, D.G., Yakushko, E.V., Kozhitov, L.V., Popkova, A.V., and Pushkarev, M.A., Formation of Ni/C nanocomposites based on polyacrylonitrile under the influence of IR radiation, Materialy elektronnoy tekhniki (in Russian), 2013, no. 1, p. 61.]
Daems, N., Wouters, J., Van Goethem, C., Baert, K., Poleunis, C., Declorte, A., Hubin, A., Vankelecom, I.F.J., and Pescarmona, P.P., Selective reduction of nitrobenzene to aniline over electrocatalysts based on nitrogen-doped carbons containing non-noble metals, Appl. Catalysis B: Environmental, 2018, vol. 226, p. 509.
Wu, G., More, K.L., Johnston, Ch.M., and Zelenay, P., High-performance electrocatalysts for oxygen reduction derived from polyaniline, iron and cobalt, Science, 2011, vol. 332, p. 443.
Friedel, B. and Weber, S.G., Preparation of monodisperse, submicrometer carbon spheres by pyrolysis of melamine-formaldehyde resin, Small, 2006, vol. 2, p. 859.
Xiong, W., Kang, J.H., and Jung, Y., Preparation of nitrogen-doped porous carbon from melamine-formaldehyde resins crosslinked by phytic acid, Int. J. Electrochem. Sci., 2018, vol. 13, p. 852.
Yu, J., Guo, M., Muhammad, F., Wang, A., Yu, G., Ma, H., and Zhu, G., Simple fabrication of an ordered nitrogen-doped mesoporous carbon with resorcinol-melamine-formaldehyde resin, Microporous and Mesoporous Mater., 2014, vol. 190, p. 117.
Pretschuh, C., Schwarzinger, C., Abdala, A.A., and Vukusic, S., Characterization of conductive nanographite melamine composites, Open J. Composite Mater., 2014, vol. 4, p. 61.
Tiwari, D., Goel, Ch., Bhunia, H., and Bajpai, P., Melamine-formaldehyde derived porous carbons for adsorption of CO2 capture, J. Environmental Management, 2017, vol. 197, p. 415.
Zhong, H., Zhang, H., Liu, S., Deng, Ch., and Wang, M., Nitrogen-enriched carbon from melamine resins with superior oxygen reduction reaction activity, ChemCusChem., 2013, vol. 6, p. 807.
Balla, P.K., Kumar, B.V.N., Ganesan, K., Shaik, E.B., and Rao, K.R., Nano casting fabrication of porous N-doped carbon using melamine-formaldehyde resins, AIP Conf. Proc., 2018, vol. 1992, article number: 040016.
Visurkhanova, Ya.A., Ivanova, N.M., Tusupbekova, G.K., and Izbastenova, D.S., Synthesis and the characteristic melamine formaldehyde composites, Adv. Mater. Res., 2014, vol. 1040, p. 393.
Помогайло, А.Д., Розенберг, А.С., Уфлянд, И.Е. Наночастицы металлов в полимерах. М.: Химия, 2000. 672 с. [Pomogailo, A.D., Rozenberg, A.D., and Uflyand, I.E., Metal Nanoparticles in Polymers (in Russian), M.: Khimiya, 2000. 672 p.]
Иванова, Н.М., Соболева, Е.А., Висурханова, Я.А., Кирилюс, И.В. Электрокаталитическая активность полианилин-медных композитов в электрогидрировании п-нитроанилина. Электрохимия. 2015. Т. 51. С. 197. [Ivanova, N.M., Soboleva, E.A., Visurkhanova, Ya.A., and Kirilyus, I.V., Electrocatalytic activity of polyaniline-copper composites in electrohydrogenation of p-nitroaniline, Russ. J. Electrochem., 2015, vol. 51, p. 166.]
Visurkhanova, Ya.A., Soboleva, E.A., Ivanova, N.M., and Muldakhmetov, Z.M., Thermal and electrochemical reduction of nickel(II) ferrite under the influence of polymer stabilizers, Bull. Karaganda Univer. Chem. Series, 2020, № 2(98), p. 42.
Manjunatha, M., Srinivas Reddy, G., Mallikarjunaiah, K.J., Ramakrishna, Damle, and Ramesh, K.P., Determination of phase composition of cobalt nanoparticles using 59Co internal field nuclear magnetic resonance, J. Supercond. Nov. Magn., 2019, vol. 32, p. 3201.
Дополнительные материалы отсутствуют.
Инструменты
Электрохимия