Электрохимия, 2022, T. 58, № 11, стр. 746-755
Новый электрохимически активный и стабильный электрод на основе молибдата празеодима для симметричных ТОТЭ
Н. В. Лысков a, *, А. И. Котова b, Д. И. Петухов b, С. Я. Истомин b, Г. Н. Мазо b
a ФГБУН Институт проблем химической физики РАН
142432 Московская обл., Черноголовка, просп. академика Семенова, 1, Россия
b Московский государственный университет имени М.В. Ломоносова, Химический факультет
ГСП-1119992 Ленинские горы, 1, стр. 3, Москва, Россия
* E-mail: lyskov@icp.ac.ru
Поступила в редакцию 27.01.2022
После доработки 29.04.2022
Принята к публикации 29.04.2022
- EDN: HLQIKJ
- DOI: 10.31857/S0424857022110093
Аннотация
Исследована электрохимическая активность нового электродного материала на основе Pr5Mo3O16 + δ (РМО) в составе симметричных твердооксидных топливных элементов (С-ТОТЭ) электролит-поддерживающей конструкции. Показано, что модельный С-ТОТЭ состава РМО/Ce0.9Gd0.1O1.95(GDC)/Zr0.84Y0.16O1.92(YSZ)/GDC/PMO продемонстрировал максимальную удельную мощность 28 мВт/см2 при 900°С. Для улучшения мощностных характеристик С-ТОТЭ была проведена модификация буферного пористого слоя GDC методом инфильтрации Pr6O11. Установлено, что введение электроактивной добавки Pr6O11 в буферный слой GDC обеспечило трехкратное повышение удельной мощности топливной ячейки, максимум которой составил 90 мВт/см2 при 900°С. Проведенные ресурсные испытания модельного С-ТОТЭ состава РМО/GDC + Pr6O11/YSZ/GDC + Pr6O11/PMO в течение 10 ч при нагрузке 0.7 В показали, что существенной деградации мощностных характеристик топливной ячейки не наблюдается. Полученные результаты свидетельствуют о перспективности нового электродного материала на основе РМО для создания С-ТОТЭ.
ВВЕДЕНИЕ
В настоящее время одним из активно развивающихся направлений в области разработки электрохимических генераторов энергии на основе твердооксидных топливных элементов (ТОТЭ) является создание так называемых симметричных ТОТЭ (С-ТОТЭ) [1–3]. Их отличительной особенностью является использование в качестве электродов одного и того же по химическому составу материала, который одновременно выполняет анодную и катодную электрохимические функции. Переход от традиционных ТОТЭ к симметричным должен способствовать снижению энергозатрат при их изготовлении за счет уменьшения числа стадий термообработки. Кроме того, в этом случае обеспечивается высокая толерантность к качеству углеводородного топлива: проблема отравления анода серой и углеродом решается путем их окисления при кратковременной подаче на анод катодных газов (деполяризация) [1, 4, 5]. При выборе электродного материала для С-ТОТЭ необходимо учитывать, что он должен обладать термической и фазовой стабильностью как в окислительной, так и в восстановительной атмосферах, а также обеспечивать высокую скорость протекания анодной и катодной электрохимических реакций. Кроме того, его высокотемпературная электропроводность в широком интервале парциальных давлений кислорода должна быть не ниже 1 См см–1, а коэффициент термического расширения (КТР) сопоставим с КТР материала твердого электролита [3].
Перечень материалов, подходящих по своим физико-химическим свойствам на роль электродного материала С-ТОТЭ, ограничен. В литературе, главным образом, рассматриваются сложные оксиды d-металлов со структурой перовскита или производными от нее [1–3]. Преимуществами оксидов со структурой перовскита в качестве электродных материалов ТОТЭ является их высокая электропроводность, термодинамическая устойчивость и каталитическая активность в электродных реакциях [6–10]. Необходимо отметить, что основной недостаток таких материалов заключается в их высокой химической активности по отношению к реакции со смежными компонентами ТОТЭ, а именно c электролитами на основе Zr0.84Y0.16O1.92 (YSZ) и Ce0.9Gd0.1O1.95 (GDC) [11–16]. Этот недостаток, главным образом, связан с присутствием в их составе крупных и, следовательно, оснóвных катионов таких как Sr2+ и Ba2+. Поэтому актуальной является задача поиска электродных материалов на основе оксидов с отличной от перовскита кристаллической структурой. Таких электродных материалов С-ТОТЭ всего лишь несколько: кермет Ni0.7Co0.3O–Ce0.8Sm0.2O1.9 [17], LiNi0.8Co0.15Al0.05O2 [18], а также Fe0.5Mg0.25Ti0.25Nb0.9Mo0.1O4 – δ (FMTMN) со структурой α-PbO2 [19].
С нашей точки, зрения наиболее перспективными объектами поиска новых электродных материалов С-ТОТЭ являются молибденсодержащие оксиды, кристаллизующиеся в структурных типах перовскита и флюорита. Это связано с тем, что в этих фазах катионы молибдена легко меняют степень окисления при варьировании парциального давления кислорода с сохранением кристаллической структуры. Вместе с тем в их структурах достаточно легко образуются кислородные вакансии, что обеспечивает возможность быстрого кислород-ионного транспорта, наличие которого способствует повышению эффективности протекания реакции восстановления кислорода на катоде ТОТЭ. Если рассматривать поведение молибденсодержащих оксидов в восстановительной атмосфере, то частичное восстановление катионов молибдена (Мо6+ → Mo5+) приводит к появлению в качестве носителей заряда электронов. Этот процесс можно выразить следующим квазихимическим уравнением:
(1)
${\text{O}}_{{\text{O}}}^{x} + 2{\text{Mo}}_{{{\text{Mo}}}}^{x} \to 2{\text{Mo}}_{{{\text{Mo}}}}^{'} + {\text{V}}_{{\text{O}}}^{{ \bullet \bullet }} + {1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}{{{\text{O}}}_{2}}\,\,({\text{г}}),$Относительно недавно в качестве потенциальных кандидатов на роль электродных материалов для ТОТЭ стали рассматриваться молибденсодержащие оксиды редкоземельных элементов (РЗЭ) с флюоритоподобной структурой состава R5Mo3O16 + δ, где R = РЗЭ [20–23]. Их кристаллическая структура и некоторые высокотемпературные свойства были изучены ранее [21–24]. Исследование высокотемпературных свойств оксида Pr5Mo3O16 + δ (РМО) [20, 21] с точки зрения его использования в качестве электродного материала показало, что КТР данного материала как на воздухе, так и в восстановительных условиях [21] сопоставим с КТР традиционно используемых в ТОТЭ твердых электролитов со структурой флюорита на основе YSZ и GDC. Вместе с тем РМО проявляет химическую устойчивость по отношению к YSZ (до 950°С) и GDC (до 1000°С), а его электропроводность в восстановительной атмосфере составляет 1.2 См/см при 800°С [21]. Исследование электрохимической активности электродного материала на основе РМО, нанесенного на поверхность твердого электролита GDC, показало, что величины поляризационного сопротивления (Rp) электрода РМО при 800°С на воздухе и в восстановительной атмосфере составляют 8.8 и 4.8 Ом см2 соответственно [20]. При этом величину Rp удается снизить на порядок до 0.6 Ом см2 при переходе от однофазного электрода РМО к композиту РМО–xPr6O11 (x = 50 мас. % Pr6O11). Однако возможности практического использования электродного материала на основе РМО в составе С-ТОТЭ в настоящий момент не исследованы. В связи с этим целью настоящей работы являлось его изучение в качестве электродного материала С-ТОТЭ.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез однофазного порошка PMO был осуществлен твердофазным методом на воздухе [20]. В качестве исходных веществ использовали оксиды Pr6O11 (Sigma-Aldrich, 99.9%) и MoO3 (Sigma-Aldrich, 99.97%), взятые в стехиометрических количествах. Оксид празеодима предварительно отжигали при температуре 350°С в течение 10 ч на воздухе для удаления сорбированных на поверхности примесей диоксида углерода и воды. Смесь исходных веществ гомогенизировали в планетарной мельнице (Fritzch Pulverisette 6, Германия) с добавкой гептана в течение 30 мин (скорость вращения 600 об./мин). Далее полученный порошок сушили на воздухе до полного удаления гептана, прессовали в таблетки и подвергали ступенчатому нагреву на воздухе: при температуре 600°С в течение 30 ч, затем при 1000°С в течение 58 ч. Фазовый состав полученного соединения контролировали методом рентгенофазового анализа (РФА) с помощью дифрактометра Huber G670 c детектором Image Plate (излучение CuKα1, интервал 2Θ 3°–100°, время съемки 30 мин). Обработку рентгенографических данных осуществляли с помощью программы STOE WinXpow (Ver. 1.04).
Для исследования электрохимических характеристик РМО в качестве электродного материала С-ТОТЭ были приготовлены модельные симметричные топливные ячейки электролит-поддерживающей конструкции следующего состава РМО/GDC/YSZ/GDC/PMO. Катионный состав использованных твердых электролитов GDC и YSZ соответствовал составу, указанному во Введении. На первом этапе их изготовления были получены газоплотные керамические мембраны YSZ толщиной 450–500 мкм и диаметром 24 мм. В качестве исходного реактива был использован коммерческий однофазный порошок YSZ (размер частиц – 0.5 ± 0.2 мкм, Ningbo SOFCMAN Energy Technology Co., Ltd., Китай), спекание которого проводили при температуре 1400°С в течение 10 ч на воздухе. Согласно результатам гидростатического взвешивания, их относительная плотность составила ~95% от рентгенографической. Далее на поверхности полученных мембран YSZ формировали буферный электролитный слой GDC. Для этого была приготовлена суспензия, состоящая из порошков GDC (размер частиц 0.5–3 мкм, Ningbo SOFCMAN Energy Technology Co., Ltd., Китай) и рисового крахмала (размер частиц 3–5 мкм, Deffner & Johann GmbH, Германия), взятых в соотношении 80 и 20 мас. % соответственно, и органического связующего (α-терпинеол) [25]. Массовое соотношение смеси порошков и α-терпинеола составляло 2 : 1. Нанесение суспензии осуществляли методом трафаретной печати с использованием тканевых сеток VS-Monoprint PES HT TW 77/55 (Verseidag-Techfab GmbH, Германия). Процедуру нанесения на каждую сторону мембраны YSZ повторяли 2 раза. После каждого нанесения образец сушили при 130°С в течение 1 ч. Припекание нанесенного слоя GDC осуществляли при температуре 1300°С в течение 6 ч на воздухе. Также были приготовлены образцы с буферным пористым слоем GDC, модифицированным путем введения электрокаталитически активной добавки Pr6O11. Детальное описание процедуры инфильтрационного введения раствора нитрата празеодима(III) и дальнейшей его термообработки приведено в работе [25]. Содержание введенного Pr6O11 в буферный пористый слой GDC составляло около 30 мас. % относительно массы пористого слоя. После формирования буферного слоя GDC на заключительном этапе изготовления симметричных топливных ячеек осуществляли процедуру нанесения электродного слоя РМО. Для этого была приготовлена электродная паста, состоящая из синтезированного порошка РМО и органического связующего (Heraeus V006, Германия), взятых в массовом соотношении 1 : 1, которую наносили методом трафаретной печати по методике, аналогичной описанной выше. Процедуру нанесения электродного материала повторяли 2 раза. После этого образцы сушили при 130°С в течение 1 ч и отжигали при температуре 900°С в течение 4 ч на воздухе. Площадь электрода составляла около 2 см2.
Для анализа микроструктуры полученных образцов был использован метод растровой электронной микроскопии (РЭМ). Исследования скола образцов проводили с помощью электронного микроскопа LEO Supra 50VP (Германия). Катионный состав границы электрод/электролит исследовали на электронном микроскопе TM4000Plus (Hitachi, Япония) с помощью метода рентгеноспектрального микроанализа (РСМА). Для этого был использован многоканальный энергодисперсионный спектрометр INCA Energy 350Х-Мах 80 (Oxford Instruments, Великобритания). Пористость и толщина электродных слоев оценивалась на основании анализа микрофотографий поперечных сколов образцов с помощью программы Image J.
Электрохимическое тестирование модельных С-ТОТЭ проводили в керамической измерительной ячейке ProbostatTM (NorECs AS, Норвегия) в диапазоне температур 800–900°С. В качестве токоподводов была использована платиновая проволока, а токосъемными контактами служила платиновая сетка, плотно прижатая к электродам. Температуру образца измеряли с помощью Pt–Pt/Rh термопары, расположенной вблизи образца. В качестве топлива использовалась увлажненная (3 об. % H2O) аргоно-водородная смесь (50 : 50 об. %), окислителем служила аргоно-кислородная смесь (80 : 20 об. %). Скорость подачи реагентов контролировалась с помощью регуляторов расхода газов Bronkhorst (Нидерланды) и составляла 90 мл/мин. Измерение вольт-амперных характеристик (ВАХ) осуществляли с помощью потенциостата-гальваностата Autolab PGSTAT302N, оснащенного модулем измерения импеданса FRA 32M (Нидерланды), в режиме развертки напряжения в диапазоне от 1000 до 100 мВ со скоростью сканирования 20 мВ/с. Импедансные измерения топливных ячеек и контрольного образца твердого электролита YSZ с нанесенными платиновыми электродами проводили в режиме ЭДС разомкнутой цепи в диапазоне частот от 0.1 до 1 × 106 Гц с амплитудой сигнала 10 мВ в диапазоне температур 800–900°С.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
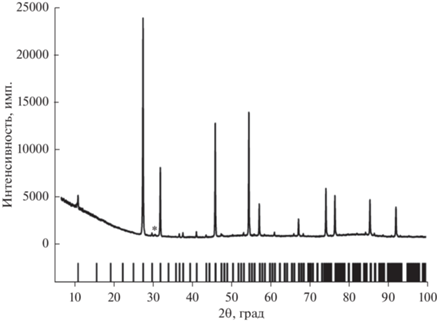
На рис. 1 представлена рентгенограмма образца РМО, синтезированного твердофазным методом на воздухе. Согласно данным РФА, полученный образец РМО является практически однофазным (максимальная интенсивность рефлекса неидентифицированной примесной фазы $ \ll {\kern 1pt} 1\% $). Рефлексы, относящиеся к фазе PMO, были проиндицированы в кубической сингонии с пространственной группой Pn-3n с параметром элементарной ячейки a = 11.0968(1) Å, что соответствует литературным данным: 11.1007(3) Å [24] и a = 11.0897(1) Å [26]. Разброс значений параметра элементарной ячейки, по-видимому, обусловлен отличающимся содержанием кислорода в образцах Pr5Mo3O16 + δ, полученных в различных экспериментальных условиях.
Рис. 1.
Рентгенограмма синтезированного порошка Pr5Mo3O16 + δ (вертикальными штрихами внизу рисунка показано расчетное положение рефлексов фазы РМО, звездочка – положение рефлекса неидентифицированной примесной фазы).
Микроструктура электродного материала и способ организации границы электрод/электролит являются одними из ключевых факторов, определяющих эффективность работы ТОТЭ. Наличие пористой структуры электрода и доступность реагентов к реакционным центрам, расположенным на границе электрод/электролит, способствует высокой скорости протекания электрохимических реакций.
На рис. 2 приведено РЭМ-изображение границы электрод PMO/буферный слой GDC/электролит YSZ модельного С-ТОТЭ состава РМО/GDC/YSZ/GDC/PMO. Электродный и буферный слои имеют развитую поверхность и характеризуются однородным распределением частиц и пор по размеру. При этом поры формируют связанную сетку каналов, обеспечивающих хорошую газовую доступность по всей толщине слоя. Следует отметить хорошую адгезию как буферного слоя GDC к поверхности твердоэлектролитной мембраны YSZ, так и электродного слоя PMO к буферному GDC. Толщина электродного слоя РМО составила ~20 мкм, а буферного слоя GDC ~8 мкм.
Рис. 2.
РЭМ-изображение поперечного сечения границы электрод PMO/буферный слой GDC/электролит YSZ модельного С-ТОТЭ состава РМО/GDC/YSZ/GDC/PMO.

На рис. 3 приведены обобщенные данные по вольт-амперным и мощностным характеристикам модельного С-ТОТЭ состава РМО/GDC/ YSZ/GDC/PMO в зависимости от рабочей температуры. Величина максимума удельной мощности симметричной топливной ячейки при повышении температуры от 800 до 900°С увеличивалась от 13 до 28 мВт/см2.
Рис. 3.
Вольт-амперные (закрытые символы) и мощностные (открытые символы) характеристики модельного С‑ТОТЭ состава РМО/GDC/YSZ/GDC/PMO при варьировании рабочей температуры (погрешность измерения температуры ±3°С).

Для оценки омического и поляризационного вкладов в общее сопротивление топливной ячейки она была исследована методом импедансной спектроскопии в режиме ЭДС разомкнутой цепи. На рис. 4 представлены импедансные спектры образца С-ТОТЭ состава РМО/GDC/YSZ/GDC/PMO при варьировании рабочей температуры от 800 до 900°С. Величину омического сопротивления (RОм) образца рассчитывали из аппроксимации импедансного спектра на действительную ось сопротивлений в высокочастотном пределе. Данная величина определяется преимущественно сопротивлением материала твердого электролита. Суммарную величину поляризационных потерь на электродах (Rη) рассчитывали исходя из разницы между низко- и высокочастотной отсечками импедансного спектра на действительную ось сопротивлений. Полученные расчетные величины RОм и Rη с учетом нормировки на площадь электрода обобщены в табл. 1. Из приведенных данных видно, что основной вклад в мощностные потери топливной ячейки приходится, преимущественно, на омическое сопротивление.
Рис. 4.
Импедансные спектры С-ТОТЭ состава РМО/GDC/YSZ/GDC/PMO, измеренные в режиме ЭДС разомкнутой цепи, при варьировании рабочей температуры (погрешность измерения температуры ±3°С).

Таблица 1.
Расчетные величины омического (RОм) и поляризационного (Rη) сопротивлений С-ТОТЭ состава РМО/GDC/YSZ/GDC/PMO при варьировании рабочей температуры от 800 до 900°С
| T, °С | RОм, Ом см2 | Rη, Ом см2 |
|---|---|---|
| 900 | 13.3 | 3.4 |
| 850 | 17.6 | 5.4 |
| 800 | 23.4 | 11.9 |
В последнее время для увеличения удельных мощностных характеристик ТОТЭ, помимо снижения омического сопротивления за счет уменьшения толщины слоя электролита и перехода к электрод-поддерживающим конструкциям, весьма популярными становятся подходы, направленные на повышение электрохимической активности электрода за счет использования метода инфильтрационного введения частиц электроактивной добавки Pr6O11 в предварительно созданную пористую структуру. Для формирования последней могут быть использованы материалы твердого электролита или катода [25, 27–29]. Выбор оксида празеодима обусловлен его высокой эффективностью в окислительно-восстановительных реакциях. Также немаловажным фактом является отсутствие взаимодействия между Pr6O11 и твердыми электролитами YSZ [30] и GDC [25] при температурах до 1000°С. В этой связи был приготовлен модифицированный образец С-ТОТЭ, у которого в буферный пористый слой GDC путем инфильтрации была введена электрокаталитически активная добавка Pr6O11 (РМО/GDC + Pr6O11/YSZ/GDC + Pr6O11/PMO).
На рис. 5 и 6а приведено РЭМ-изображение границы электрод PMO/буферный слой GDC, модифицированный Pr6O11/электролит YSZ. В этом случае подслой GDC также имеет развитую поверхность. Согласно данным рентгеноспектрального микроанализа (рис. 6б, 6в) видно, что фаза электроактивной добавки Pr6O11 покрывает внутренний объем пор в слое GDC, при этом субмикронные частицы Pr6O11 образуют на поверхности GDC связанную структуру, которая должна обеспечивать образование новых электроактивных центров, участвующих в окислительно-восстановительных реакциях.
Рис. 5.
РЭМ-изображение поперечного сечения границы электрод PMO/буферный слой GDC, модифицированный инфильтрацией Pr6O11/электролит YSZ модельного С-ТОТЭ состава РМО/GDC + + Pr6O11/YSZ/GDC + Pr6O11/PMO.

Рис. 6.
(а) РЭМ-изображение поперечного сечения границы электрод PMO/буферный слой GDC, модифицированный инфильтрацией Pr6O11/электролит YSZ модельного С-ТОТЭ состава РМО/GDC + + Pr6O11/YSZ/GDC + Pr6O11/PMO; (б) карта распределения празеодима (красные области) по поверхности поперечного сечения границы электрод/электролит; (в) карта распределения церия (синие области) по поверхности поперечного сечения границы электрод/электролит.

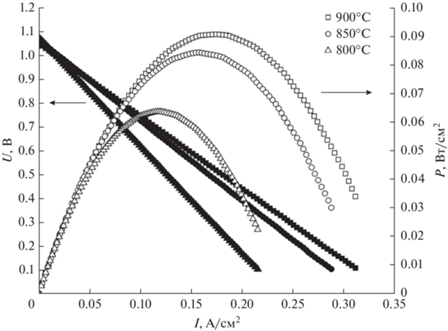
На рис. 7 представлены вольт-амперные и мощностные характеристики модельного С‑ТОТЭ состава РМО/GDC + Pr6O11/YSZ/GDC + + Pr6O11/PMO в зависимости от рабочей температуры. Величина максимума удельной мощности симметричной топливной ячейки при повышении температуры от 700 до 900°С увеличивалась от 30 до 90 мВт/см2. Сравнение мощностных характеристик исследованных модельных С-ТОТЭ показывает, что введение электроактивной добавки Pr6O11 в буферный слой GDC обеспечивает трехкратное повышение максимума удельной мощности топливной ячейки.
Рис. 7.
Вольт-амперные (закрытые символы) и мощностные (открытые символы) характеристики модельного С‑ТОТЭ состава РМО/GDC + Pr6O11/YSZ/GDC + Pr6O11/PMO при варьировании рабочей температуры (погрешность измерения температуры ±3°С).
Исследование модельного С-ТОТЭ состава РМО/GDC + Pr6O11/YSZ/GDC + Pr6O11/PMO методом импедансной спектроскопии (рис. 8) показало, что введение электроактивной добавки Pr6O11 способствует снижению не только величины поляризационных потерь на электродах, но и уменьшает вклад омических потерь. Расчетные величины RОм и Rη модельного С-ТОТЭ состава РМО/GDC + Pr6O11/YSZ/GDC + Pr6O11/PMO приведены в табл. 2. Для понимания причин значимого снижения омических потерь проведем сопоставление удельной ионной проводимости используемого твердого электролита YSZ, определенной из данных импедансных измерений симметричной ячейки Pt/YSZ/Pt (рис. 9), с величинами проводимости, рассчитанными из величин RОм в экспериментах по исследованию мощностных характеристик топливных ячеек РМО/GDC/YSZ/GDC/PMO (ячейка 1) и РМО/GDC + Pr6O11/YSZ/GDC + Pr6O11/PMO (ячейка 2). В случае ячейки 2, где диффузионные пути движения ионов кислорода ограничены фактически толщиной слоя YSZ (т. к. буферные слои GDC, покрытые слоем электрокатализатора, выступают в роли электродов), величина проводимости, рассчитанная из величины RОм, сопоставима с удельной электропроводностью твердого электролита YSZ. В случае же ячейки 1, где электролитная мембрана представляет собой совокупность слоев GDC/YSZ/GDC, его величина проводимости примерно в 6 раз меньше по сравнению с проводимостью твердоэлектролитной мембраны ячейки 2. По всей видимости, в данном случае определяющую роль играет не омическое сопротивление YSZ, а совокупный вклад сопротивления пористого буферного слоя GDC и межфазного сопротивления границы GDC/YSZ, которые увеличивают протяженность диффузионных путей миграции ионов кислорода и способствуют повышению омического сопротивления топливной ячейки в случае РМО/GDC/YSZ/GDC/PMO. Несмотря на повышение удельных мощностных характеристик топливной ячейки и снижение ее общего сопротивления, в том числе омической и поляризационной составляющих, соотношение между RОм и Rη остается на уровне 3 : 1. На основании этого можно сделать вывод, что, как и в предыдущем случае, омическое сопротивление вносит основной вклад в мощностные потери топливной ячейки. Таким образом, последующее усовершенствование С-ТОТЭ с использованием РМО в качестве электродного материала может быть связано с переходом от электролит- к электрод-поддерживающей конструкции.
Рис. 8.
Импедансные спектры С-ТОТЭ состава РМО/GDC + Pr6O11/YSZ/GDC + Pr6O11/PMO, измеренные в режиме ЭДС разомкнутой цепи, при варьировании рабочей температуры (погрешность измерения температуры ±3°С).

Таблица 2.
Расчетные величины омического (RОм) и поляризационного (Rη) сопротивлений С-ТОТЭ состава РМО/GDC + Pr6O11/YSZ/GDC + Pr6O11/PMO при варьировании рабочей температуры от 800 до 900°С
| T, °С | RОм, Ом см2 | Rη, Ом см2 |
|---|---|---|
| 900 | 2.17 | 0.67 |
| 850 | 2.33 | 0.89 |
| 800 | 3.19 | 1.19 |
Рис. 9.
Сравнение проводимости твердого электролита YSZ с величинами проводимости, рассчитанными из величины RОм для топливных ячеек РМО/GDC/YSZ/GDC/PMO (ячейка 1) и РМО/GDC + + Pr6O11/YSZ/GDC + Pr6O11/PMO (ячейка 2).

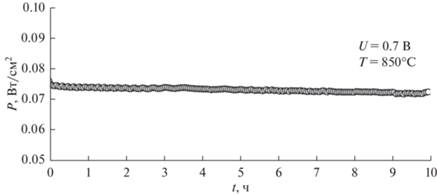
Для проверки временной стабильности электрохимических характеристик С-ТОТЭ состава РМО/GDC + Pr6O11/YSZ/GDC + Pr6O11/PMO были проведены его ресурсные испытания при температуре 850°С в течение 10 ч в условиях работы под нагрузкой в потенциостатическом режиме при напряжении 0.7 В. На рис. 10 приведена зависимость удельной мощности топливной ячейки от времени. Из рисунка видно, что резкого падения мощностных характеристик топливной ячейки под нагрузкой в период проведения эксперимента не происходит. Величина снижения удельной мощности топливной ячейки в условиях воздействия нагрузочного напряжения 0.7 В в течение 10 ч непрерывной работы составила ~2.7%.
ЗАКЛЮЧЕНИЕ
Исследование электрохимических характеристик модельного С-ТОТЭ электролит-поддерживающей конструкции РМО/GDC/YSZ/GDC/PMO с новым электродным материалом на основе молибдата празеодима PMO, кристаллизующегося во флюоритоподобной структуре, показало достижение максимума удельной мощности 28 мВт/см2 при 900°С. Модификация буферного пористого слоя GDC методом инфильтрации Pr6O11 помогла существенно повысить максимальную удельную мощность до 90 мВт/см2 при 900°С. Проведенные ресурсные испытания образца С-ТОТЭ состава РМО/GDC + + Pr6O11/YSZ/GDC + Pr6O11/PMO в течение 10 ч при напряжении 0.7 В показали, что существенной деградации мощностных характеристик топливной ячейки под нагрузкой в период проведения испытаний не наблюдается. Таким образом, полученные результаты свидетельствуют о перспективности предложенного электродного материала на основе РМО и разработанных подходов для создания С-ТОТЭ с электродными материалами, которые не имеют перовскитоподобной структуры. Дальнейшее улучшение мощностных характеристик наиболее вероятно может быть достигнуто при переходе к композитным электродам PMO–Pr6O11.
Список литературы
Истомин, С.Я., Лысков, Н.В., Мазо, Г.Н., Антипов, Е.В. Электродные материалы на основе сложных оксидов d-металлов для симметричных твердооксидных топливных элементов. Успехи химии. 2021. Т. 90. С. 644. [Istomin, S.Ya., Lyskov, N.V., Mazo, G.N., and Antipov, E.V., Electrode materials based on complex d-metal oxides for symmetrical solid oxide fuel cells, Russ. Chem. Rev., 2021, vol. 90, p. 644.]
Su, C., Wang, W., Liu, M., Tadé, M.O., and Shao, Z., Progress and prospects in symmetrical solid oxide fuel cells with two identical electrodes, Adv. Energy Mater., 2015, vol. 5, p. 1500188.
Ruiz-Morales, J.C., Marrero-López, D., Canales-Vázquez, J., and Irvine, J.T., Symmetric and reversible solid oxide fuel cells, RSC Adv., 2011, vol. 1, p. 1403.
Cowin, P.I., Petit, C.T., Lan, R., Irvine, J.T., and Tao, S., Recent progress in the development of anode materials for solid oxide fuel cells, Adv. Energy Mater., 2011, vol. 1, p. 14.
Ge, X.M., Chan, S.H., Liu, Q.L., and Sun, Q., Solid oxide fuel cell anode materials for direct hydrocarbon utilization, Adv. Energy Mater., 2012, vol. 2, p. 1156.
Ishihara, T., Perovskite oxide for solid oxide fuel cells. N.Y.: Springer Science & Business Media, 2009. 302 p.
Tilley, R.J.D., Perovskites: structure – property relationships. Chichester, West Sussex, United Kingdom: Wiley, 2016. 327 p.
Sadykov, V.A., Muzykantov, V.S., Yeremeev, N.F., Pelipenko, V.V., Sadovskaya, E.M., Bobin, A.S., Fedorova, Yu.E., Amanbaeva, D.G., and Smirnova, A.L., Solid oxide fuel cell cathodes: importance of chemical composition and morphology, Catal. Sustain. Energy, 2015, vol. 2, p. 57.
Shu, L., Sunarso, J., Hashim, S.S., Mao, J., Zhou, W., and Liang, F., Advanced perovskite anodes for solid oxide fuel cells: A review, Int. J. Hydrogen Energy, 2019, vol. 44, p. 31275.
Истомин, С.Я., Антипов, Е.В. Катодные материалы на основе перовскитоподобных оксидов переходных металлов для среднетемпературных твердооксидных топливных элементов. Успехи химии. 2013. Т. 82. С. 686. [Istomin, S.Ya. and Antipov, E.V., Cathode materials based on perovskite-like transition metal oxides for intermediate temperature solid oxide fuel cells, Russ. Chem. Rev., 2013, vol. 82, p. 686.]
Kostogloudis, G.Ch., Tsiniarakis, G., and Ftikos, Ch., Chemical reactivity of perovskite oxide SOFC cathodes and yttria stabilized zirconia, Solid State Ionics, 2000, vol. 135, p. 529.
Zhang, L., Chen, G., Dai, R., Lv, X., Yang, D., and Geng, Sh., A review of the chemical compatibility between oxide electrodes and electrolytes in solid oxide fuel cells, J. Power Sources, 2021, vol. 492, p. 229630.
Van Roosmalen, J.A.M. and Cordfunke, E.H.P., Chemical reactivity and interdiffusion of (La,Sr)MnO3 and (Zr,Y)O2, solid oxide fuel cell cathode and electrolyte materials, Solid State Ionics, 1992, vol. 52, p. 303.
Yokokawa, H., Sakai, N., Kawada, T., and Dokiya, M., Thermodynamic Analysis of Reaction Profiles Between LaMO3 (M = Ni, Co, Mn) and ZrO2, Solid State Ionics, 1991, vol. 138, p. 2719.
Dos Santos-Gomez, L., Leon-Reina, L., Porras-Vazquez, J.M., Losilla, E.R., and Marrero-Lopez, D., Chemical stability and compatibility of double perovskite anode materials for SOFC, Solid State Ionics, 2013, vol. 239, p. 1.
Marrero-Lopez, D., Pena-Martínez, J., Ruiz-Morales, J.C., Gabas, M. P., Nunez, M.A. Aranda, G., and Ramos-Barrado, J.R., Redox behaviour, chemical compatibility and electrochemical performance of Sr2MgMoO6 – δ as SOFC anode, Solid State Ionics, 2010, vol. 180, p. 1672.
Chen, Y., Cheng, Z., Yang, Y., Yu, W., Tian, D., Lu, X., Ding, Y., and Lin, B., Improved performance of symmetrical solid oxide fuel cells with redox-reversible cermet electrodes, Mater. Lett., 2017, vol. 188, p. 413.
Chen, G., Sun, W., Luo, Y., Liu, H., Geng, S., Yu, K., and Liu, G., Investigation of layered Ni0.8Co0.15Al0.05LiO2 in electrode for low-temperature solid oxide fuel cells, Int. J. Hydrogen Energy, 2018, vol. 43, p. 417.
Ni, C., Feng, J., Cui, J., Zhou, J., and Ni, J., An n-type oxide Fe0.5Mg0.25Ti0.25Nb0.9Mo0.1O4 – δ for both cathode and anode of a solid oxide fuel cell, J. Electrochem. Soc., 2017, vol. 164, p. F283.
Лысков, Н.В., Котова, А.И., Истомин, С.Я., Мазо, Г.Н., Антипов, Е.В. Электрохимические свойства электродных материалов на основе Pr5Mo3O16 + δ. Электрохимия. 2020. Т. 56. С. 100. [Lyskov, N.V., Kotova, A.I., Istomin, S.Ya., Mazo, G.N., and Antipov, E.V., Electrochemical properties of electrode materials based on Pr5Mo3O16 + δ, Russ. J. Electrochem., 2020, vol. 56, p. 93.]
Истомин, С.Я., Котова, А.И., Лысков, Н.В., Мазо, Г.Н., Антипов, Е.В. Pr5Mo3O16 + δ – новый анодный материал для твердооксидных топливных элементов. Журн. неорган. химии. 2018. Т. 63. С. 1274. [Istomin, S.Ya., Kotova, A.I., Lyskov, N.V., Mazo, G.N., and Antipov, E.V., Pr5Mo3O16 + δ: A new anode material for solid oxide fuel cells, Russ. J. Inorg. Chem., 2018, vol. 63, p. 1291.]
Антипин, А.М., Алексеева, О.А., Сорокина, Н.И., Кускова, А.Н., Артемов, В.В., Мурзин, В.Ю., Харитонова, Е.П., Орлова, Е.А., Воронкова, В.И. Cтроение соединения Pr5Mo3O16 + δ, обладающего смешанной электронно-ионной проводимостью. Кристаллография. 2015. Т. 60. С. 704. [Antipin, A.M., Alekseeva, O.A., Sorokina, N.I., Kuskova, A.N., Artemov, V.V., Murzin, V.Y., Kharitonova, E.P., Orlova, E.A., and Voronkova, V.I., Structure of compound Pr5Mo3O16 + δ exhibiting mixed electronic-ionic conductivity, Crystallogr. Rep., 2015, vol. 60, p. 640.]
Voronkova, V.I., Leonidov, I.A., Kharitonova, E.P., Belov, D.A., Patrakeev, M.V., Leonidova, O.N., and Kozhevnikov, V.L., Oxygen ion and electron conductivity in fluorite-like molybdates Nd5Mo3O16 and Pr5Mo3O16, J. Alloys Compd., 2014, vol. 615, p. 395.
Tsai, M., Greenblatt, M., and McCarroll, W.H., Oxide ion conductivity in Ln5Mo3O16 +x (Ln = La, Pr, Nd, Sm, Gd; x = 0.5), Chem. Mater., 1989, vol. 1, p. 253.
Лысков, Н.В., Галин, М.З., Напольский, К.С., Росляков, И.В., Мазо, Г.Н. Повышение электрохимической активности границы Pr1.95La0.05CuO4/ пористый слой Ce0.9Gd0.1O1.95 при инфильтрационном введении Pr6O11. Электрохимия. 2021. Т. 57. С. 670. [Lyskov, N.V., Galin, M.Z., Napol’skii, K.S., Roslyakov, I.V., and Mazo, G.N., Increasing the electrochemical activity of the interface Pr1.95La0.05CuO4/ porous Ce0.9Gd0.1O1.95 layer by infiltrating Pr6O11, Russ. J. Electrochem., 2021, vol. 57, p. 670.]
Martinez-Lope, M.J., Alonso, J.A., Sheptyakov, D., and Pomyakushin, V., Preparation and structural study from neutron diffraction data of Pr5Mo3O16, J. Solid State Chem., 2010, vol. 183, p. 2974.
Ding, D., Li, X., Lai, S.Y., Gerdes, K., and Liu, M., Enhancing SOFC cathode performance by surface modification through infiltration, Energy Environ. Sci., 2014, vol. 7, p. 552.
Nicollet, C., Flura, A., Vibhu, V., Rougier, A., Bassat, J.M., and Grenier, J.C., An innovative efficient oxygen electrode for SOFC: Pr6O11 infiltrated into Gd-doped ceria backbone, Int. J. Hydrogen Energy, 2016, vol. 41, p. 15538.
Connor, P.A., Yue, X., Savaniu, C.D., Price, R., Triantafyllou, G., Cassidy, M., Kerherve, G., Payne, D.J., Maher, R.C., Cohen, L.F., Tomov, R.I., Glowacki, B.A., Kumar, R.V., and Irvine, J.T.S., Tailoring SOFC electrode microstructures for improved performance, Adv. Energy Mater., 2018, vol. 8, p. 1800120.
Taguchi, H., Chiba, R., Komatsu, T., Orui, H., Watanabe, K., and Hayashi, K., LNF SOFC cathodes with active layer using Pr6O11 or Pr-doped CeO2, J. Power Sources, 2013, vol. 241, p. 768.
Дополнительные материалы отсутствуют.