Журнал эволюционной биохимии и физиологии, 2020, T. 56, № 2, стр. 158-161
СРАВНИТЕЛЬНЫЙ АНАЛИЗ МЕХАНИЗМА КАТАЛИЗА МНОГОЯДЕРНЫХ СИНИХ ОКСИДАЗ: КВАНТОВО-ХИМИЧЕСКОЕ ИССЛЕДОВАНИЕ ПЕРОКСИДНОГО ИНТЕРМЕДИАТА ЦЕРУЛОПЛАЗМИНА
И. В. Крауклис 1, Ю. В. Чижов 1, В. Е. Стефанов 1, *, К. А. Мошков 1
1 Санкт-Петербургский государственный университет
Санкт-Петербург, Россия
* E-mail: V.Stefanov@spbu.ru
Поступила в редакцию 20.12.2018
После доработки 20.09.2019
Принята к публикации 21.10.2019
Многоядерные синие медьсодержащие оксидазы (MCO) – обширное семейство ферментов, встречающихся в клетках архей, прокариотов и эукариотов. Несмотря на огромные “эволюционные расстояния” между отдельными представителями этого семейства, все они характеризуются высококонсервативным набором Сu-центров, которые обеспечивают окисление разнообразных субстратов, сопровождаемое 4-х электронным восстановлением молекулы кислорода до воды. Сu-центры в этих белках принято подразделять на три типа. Центр типа 1 (T1Cu) содержит один ион меди, связанный (в подавляющем большинстве случаев) с двумя остатками гистидина, одним остатком цистеина и одним остатком метионина. Центр типа 2 (Т2Cu) также содержит единственный ион меди, лигандами которого служат два остатка гистидина. Центр типа 3 (Т3Cu) – биядерный центр, включающий два иона меди, каждый из которых связан с тремя остатками гистидина. Этот центр сближен с Т2Cu, образуя триядерный комплекс Т3Cu + Т2Cu.
В ходе каталитического акта происходит перенос электронов от восстановленной молекулы субстрата вначале на центр Т1Cu, а затем на триядерный центр Т3Cu + Т2Cu. Эта реакция осуществляется в две двухэлектронные стадии. На первой из них во взаимодействии О2 с полностью восстановленной формой фермента формируется так называемый пероксидный интермедиат (ПИ). На второй стадии происходит восстановительное расщепление связи О–О с формированием так называемого нативного интермедиата (НИ). В нем один атом О связан с двумя ионами Cu центра Т3Cu, а второй атом О в составе гидроксильной группы ОН связан с ионом Cu центра Т2Cu [1]. НИ изучен достаточно подробно [2, 3], чего нельзя сказать о ПИ. Следует отметить, что все опубликованные до настоящего времени работы касались наиболее простых многоядерных синих оксидаз – лакказ (Lc), CotA, Fet3 и др. В настоящей работе проведено квантово-химическое исследование интермедиата ПИ гораздо более сложной оксидазы – церулоплазмина (ЦП, КФ 1.16.3.1, Fe(II):кислород оксидоредуктаза) плазмы крови человека [4].
Моделирование геометрии триядерного медного центра ЦП проводилось неограниченным по спину методом теории функционала плотности с функционалом CAM-B3LYP, учитывающим поправки на дальнодействие. В качестве базисного набора при оптимизации геометрии использовался базис def2SVP с улучшенной параметризацией. Особенностью проведения квантово-химических расчетов промежуточной ПИ структуры являлось использование подхода «нарушенной симметрии» (the broken symmetry approach, BS [5]), при этом отдельно проверялась стабильность волновой функции основного состояния. Электронные спектры поглощения рассчитывались в рамках нестационарной теории функционала плотности (TDDFT) с гибридным обменно-корреляционным функционалом B3LYP и базисом def2SVP. Для оценки зарядового распределения и электронной конфигурации атомов применялся NBO-подход. Все расчеты проводились посредством квантово-химического пакета Gaussian 16 (Revision A.03, M.J. Frisch, G.W. Trucks, H.B. Schlegel et al., Gaussian, Inc., Wallingford CT, 2016.), установленного на Huawai-кластере Вычислительного Центра СПбГУ http://www.cc.spbu.ru/.
Особенности моделирования электронной структуры. Рассматриваемый нами триядерный медный центр Т3Cu + Т2Cu содержит три иона меди, которые могут находиться в восстановленном, Cu(I), или окисленном, Cu(II), состоянии. Состояние Cu(I) характеризуется замкнутой электронной оболочкой 3d10, в то время как состояние Cu(II) подразумевает конфигурацию 3d 9 и наличие одного неспаренного электрона. В полностью восстановленной форме (Fully Reduced, FR) триядерного центра все три иона находятся в состоянии Cu(I). Эта форма хорошо описывается в рамках ограниченного по спину однодетерминантного подхода. Однако промежуточные структуры ПИ и НИ содержат несколько ионов Cu(II) с локализованными на них электронами, между которыми может возникать сильное спин-обменное взаимодействие. Поэтому описание электронной структуры таких комплексов требует разделения электронной плотности для α- и β-электронов, что реализуется в неограниченном по спину методе функционала плотности.
Кроме того, для таких систем с успехом применяется так называемый подход “нарушенной симметрии”. Он обеспечивает в расчетах более низкую энергию для основного синглетного состояния (BS), которое в таких молекулярных системах часто бывает спин-загрязненным более высокими спиновыми состояниями. Также BS-подход успешно используется для определения константы обменного взаимодействия J в молекулярных системах, имеющих возможные магнитные обменные взаимодействия.
Константа обменного взаимодействия J может быть рассчитана через синглет (S)-триплетное (T) расщепление, которое в простейшем случае, – для двух неспаренных электронов, выражается формулой [6]:
Здесь J – константа обменного взаимодействия (параметр Гейзенберга в гамильтониане вида $\hat {H} = - ~J{{\hat {S}}_{1}}{{\hat {S}}_{2}}$). Если J < 0, то это означает, что синглетное состояние системы ниже триплетного, и указывает на антиферромагнитный характер связывания между магнитными центрами. Если J > 0, то триплетное состояние располагается ниже синглетного, что указывает на ферромагнитный характер спин-обменного взаимодействия.Экспериментально установлено, что в триядерном медном центре МСО наблюдается сильное антиферромагнитное связывание между медными центрами Cu(II) [3]. Поэтому мы использовали BS-подход для определения геометрии нижнего синглетного состояния и оценки константы спинового взаимодействия изучаемых структур.
Моделирование структуры пероксидного интермедиата обнаружило, что реакция восстановления O2 до Н2О начинается с захвата полностью восстановленным триядерным центром T3Cu(I) + T2Cu(I) молекулярного кислорода, который находится в триплетном состоянии [3]. Затем происходит передача двух электронов от двух ионов меди на молекулярный кислород с образованием пероксида (О2)2–. В качестве исходной для моделирования пероксидного интермедиата бралась геометрия триядерного медного центра из рентгеноструктурных данных для ЦП [4], где молекула О2 была связана внутри медного кластера, а молекула Н2О была выбрана в качестве лиганда на T2Cu центре.
Квантово-химические исследования модельных ПИ структур многоядерных медьсодержащих оксидаз (Lc, Fet3p, CotA) показали [2, 3], что из двух возможных ПИ структур с боковой µ-η2:η2-О$_{2}^{{2 - }}$ и мостиковой µ3-1,2,2-${\text{O}}_{2}^{{2 - }}$ геометрией спектроскопически значимой оказалась вторая структура. Это подтвердилось спектроскопическим исследованием пероксидного аддукта (РА) от T1HgLc, кристаллографическим исследованием РА от CotA и квантово-химическими QM/MM расчетами ПИ и PA [3].
Поскольку в случае ЦП нам не удалось найти в литературе экспериментальных данных в пользу того или иного зарядового распределения на ионах меди триядерного центра, то были проведены uCAM-B3LYP/def2SVP расчеты ПИ-структуры в синглетном состоянии c тремя возможными вариантами распределения зарядов: Сu65(II)–Cu66(I)–Cu67(II), Сu65(I)–Cu66(II)–Cu67(II), Сu65(II)–Cu66(II)–Cu67(I). Здесь и далее номер при атоме меди соответствует нумерации работы [4]. При оптимизации геометрии этих структур фиксировались ионы меди и учитывалось дисперсионное взаимодействие в рамках эмпирической поправки GD3. В результате была получена только одна мостиковая µ3-1,2,2-О$_{2}^{{2 - }}$ структура c зарядовым распределением на ионах меди Сu65(II)–Cu66(I)–Cu67(II), геометрия которой представлена в табл. 1а. Однако анализ геометрии показал, что расстояние между атомами кислорода R(O–O) = 1.31 Å, что соответствует анионной ${\text{O}}_{2}^{{1 - }}$ (R(O–O) = 1.34 Å), а не пероксидной ${\text{O}}_{2}^{{2 - }}$ форме молекулярного кислорода (R(O–O) = 1.42 Å). Поэтому дальнейшие расчеты ПИ проводились в рамках BS-метода с “загрязненной” синглетной волновой функцией. В результате полной оптимизации геометрии в состоянии с нарушенной спиновой симметрией (MS = 0, 〈S2〉 ≈ 1) была получена мостиковая µ3-1,2,2-${\text{O}}_{2}^{{2 - }}$ структура пероксидного интермедиата ПИ (см. рис. 1а, табл. 1b). Расстояние между атомами кислорода в этом случае оказалось равным R(O–O) = 1.392 Å, что значительно лучше соответствует пероксидной форме молекулы О2. По всей видимости, часть электронной плотности в связанном состоянии молекулы O2 перераспределяется по всей структуре ПИ. В таблице для сравнения также представлены некоторые расстояния модельной ПИ структуры из работы [2] и рентгеноструктурные данные для Т3Cu + Т2Cu центра ЦП [4].
Таблица 1.
Геометрия пероксидного интермедиата ПИ. В скобках указаны гистидиновые остатки ЦП и вода (W)
| Atom A | Atom B | Distance, Å (a) | Distance, Å (b) | Distance, Å [3] | Distance, Å [4] |
|---|---|---|---|---|---|
| Cu 65 | N 32 (His163) | 2.122 | 2.126 | 2.14 | |
| N 48 (His980) | 2.013 | 2.073 | 1.97 | ||
| N 56 (His1020) | 1.971 | 1.990 | 2.02 | ||
| Cu 66 | 4.971 | 4.115 | 4.197 | 4.97 | |
| Cu 67 | 4.018 | 3.661 | 3.714 | 4.02 | |
| O 68 | 1.973 | 1.980 | 1.943 | 2.64 | |
| O 69 | 1.936 | 2.029 | 2.033 | 2.77 | |
| О 68 | О 69 | 1.309 | 1.392 | 1.435 | 1.08 |
| Cu 66 | N 16 (His103) | 2.031 | 2.101 | 1.90 | |
| N 24 (His161) | 2.004 | 2.016 | 2.09 | ||
| N 64 (His1022) | 1.987 | 2.034 | 2.20 | ||
| Cu 67 | 4.086 | 3.598 | 4.063 | 4.09 | |
| O 68 | 3.023 | 2.185 | 2.199 | 2.36 | |
| O 69 | 3.737 | 2.912 | 3.173 | 2.58 | |
| Cu 67 | N 8 (His101) | 1.961 | 2.005 | 1.87 | |
| N 40 (His978) | 1.982 | 2.011 | 2.00 | ||
| O 69 | 2.221 | 1.935 | 1.973 | 2.25 | |
| O 118 (W148) | 2.195 | 2.052 | 2.070 | 2.98 |
(a) uCAM-B3LYP/def2SVP + GD3, частичная оптимизация (зафиксированы ионы меди Cu 65,66,67);
(b) uCAM-B3LYP/def2SVP + GD3, полная оптимизация, метод “нарушенной симметрии”;
[4] рентгеноструктурные данные.
Рис. 1.
Геометрическая (a) и электронная структура (b) пероксидного интермедиата, полученная методом “нарушенной симметрии” в рамках uCAM-B3LYP/def2SVP расчета: E(BS) = –8931.165970 a.u., 〈S2〉 = 0.9693, µ = 4.959 D.
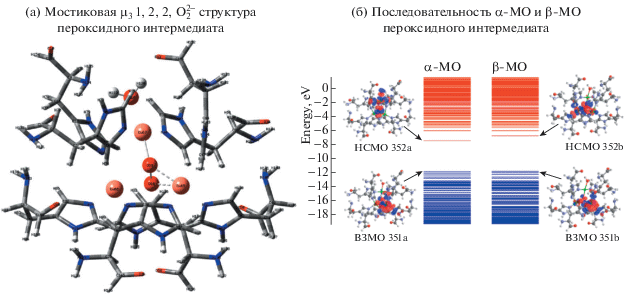
Электронная структура ПИ характеризуется появлением в энергетической щели вакантных орбиталей α-НСМО (352а) и β-НСМО (352b) с энергиями –7.464 эВ и –6.814 эВ, которые представляют собой две магнитные орбитали, участвующие в обменном взаимодействии (см. рис. 1b). Обе эти орбитали содержат значительные вклады $\pi _{\sigma }^{*}$(${\text{O}}_{2}^{{2 - }}$)-орбитали и 3d–АО Cu67(II) и Сu65(II) соответственно. Более высокие НСМО локализованы преимущественно на группах C=O гистидиновых остатков и имеют энергию от –6.02 эВ и выше. Высшие занятые МО локализованы преимущественно на ионах Cu66(I) и имеют характер 3d AO; они лежат в узкой области от –11.9 эВ до –12.8 эВ. Энергетическая щель для α-МО составляет Δα = 5.930 эВ и для β‑МО – Δβ = 5.868 эВ.
Электронный спектр поглощения ПИ. Характерной спектральной особенностью ПИ ЦП является полоса при 350 нм (f = 0.023). Два малоинтенсивных пика с энергиями при 345.6 нм (f = 0.010) и 352.4 нм (f = 0.011) обусловлены одноэлектронными переходами на вакантные α-НСМО (352а) и β‑НСМО (352b). Донорными орбиталями выступают дважды занятые $\pi _{\sigma }^{*}$(${\text{O}}_{2}^{{2 - }}$)-орбитали, взаимодействующие с 3d-орбиталями ионов Cu67(II) и Сu65(II). Вторая полоса при 490 нм (f = 0.066) образована несколькими состояниями с переносом заряда с π-His остатков и 3d–АО Cu67(II) и Сu65(II) на $\pi _{\sigma }^{*}$(${\text{O}}_{2}^{{2 - }}$)-орбитали. Третья широкая полоса 670 нм (f = 0.072) обусловлена многочисленными переходами преимущественно c металлических 3d-орбиталей ионов Cu66(I) на α-НСМО (352а) и β-НСМО (352b). Мы не обнаружили в литературе экспериментальные спектры поглощения ПИ ЦП, однако наши расчеты хорошо согласуются с качественным описанием экспериментального спектра поглощения ПИ T1HgLc [3], основанном на анализе последовательности НСМО и ВЗМО. В частности, авторы связывают первую высокоэнергетическую полосу 31 000–27 500 см–1 (290–365 нм) с ${\text{O}}_{2}^{{2 - }}$($\pi _{\sigma }^{*}$) → Cu(II) ПЗ-переходами на α-НСМО на T2 Cu(II) и β-НСМО на Т3 Cu(II).
Оценка константы обменного взаимодействия. Согласно формуле (1), константа обменного взаимодействия в нашем случае оказалась равной J = = ‒99.21 см–1. Отрицательное значение J указывает на антиферромагнитный характер спин-обменного взаимодействия между магнитными центрами Cu65(II) и Cu67(II) в пероксидном интермедиате ЦП, что согласуется с аналогичными данными для других медьсодержащих оксидаз (–2J > 200 см–1) [3].
Список литературы
Мошков К.А., Зайцев В.Н., Гришина Т.В., Стефанов В.Е. Многоядерные синие медьпротеиды: эволюционный дизайн. Ж. эвол. биохим. и физиол. 50(3): 169–181. 2014. [Moshkov K.A., Zaitsev V.N. Grishina T.V., Stefanov V.E. Multinuclear blue copper-proteins: The evolutionary design. J. Evol. Biochem. Physiol. 50(3): 169–181. 2014 (in Russ)].
Solomon E.I., Augustine A.J., Yoon J. O2 Reduction to H2O by the multicopper oxidases. Dalton Trans. 30: 3921–3932. 2008. https://doi.org/10.1039/b800799c
Yoon J., Solomon E.I. Electronic structure of the peroxy intermediate and its correlation to the native intermediate in the multicopper oxidases: insights into the reductive cleavage of the O–O bond. J. Am. Chem. Soc. 129(43): 13127–13136. 2007. https://doi.org/10.1021/ja073947a
Bento I., Peixoto C., Zaisev V.N., Lindley P.F. Ceruloplasmin revisited: Structural and functional roles of various metal cation-binding sites. Acta Cryst. D63: 240–248. 2007.
Case D.A., Noodleman L., Li J. Metal-ligand interaction in chemistry, physics and biology. Edited by N. Russo and D. Salagub, NATO Science Series, Series C: Mathematical and Physical Sciences. 546: 20. 1998.
Shoji M., Koizumi K., Kitagawa Y., Kawakami T., Yamanaka S., Okumura M., Yamaguchi K. A general algorithm for calculation of Heisenberg exchange integrals J in multispin systems. Chem. Phys. Letters 432: 343–347. 2006.
Дополнительные материалы отсутствуют.
Инструменты
Журнал эволюционной биохимии и физиологии


