Известия РАН. Физика атмосферы и океана, 2023, T. 59, № 1, стр. 61-70
Модельная оценка закисленности атмосферных осадков за счет антропогенных соединений серы в ХХ веке
Р. Д. Гизатуллин a, А. В. Елисеев a, b, c, d, *
a Казанский (Приволжский) федеральный университет
420097 Казань, ул. Товарищеская, 5, Россия
b Московский государственный университет имени М.В. Ломоносова
119991 Москва, Ленинские горы, 1 стр. 2, Россия
c Институт физики атмосферы им. А.М. Обухова РАН
119017 Москва, Пыжевский пер., 3, Россия
d Московский центр фундаментальной и прикладной математики
119991 Москва, Ленинские горы, 1 стр. 1, Россия
* E-mail: eliseev.alexey.v@mail.ru
Поступила в редакцию 04.08.2022
После доработки 22.08.2022
Принята к публикации 12.10.2022
- EDN: DMKUYF
- DOI: 10.31857/S0002351523010030
Аннотация
Проведен анализ кислотности осадков по расчетам со схемой серного цикла атмосферы ChAP-1.0 (Chemistry and Aerosol Processes), разработанной для моделей Земной системы промежуточной сложности (МЗСПС), при задании среднемесячных антропогенных эмиссий диоксида серы в атмосферу в 1850–2000 гг. по данным проекта CMIP5 (Coupled Models Intercomparison Project, phase 5), а полей метеорологических переменных – по многолетним средним (с учетом годового хода) данным реанализа ERA-Interim для 1979–2015 гг. Выявлено, что значимая кислотность осадков (минимальное $pH$ гидрометеоров) характерна для регионов с высокой интенсивностью антропогенных эмиссий соединений серы в атмосферу – Европы, юго-восточной Азии, востока Северной Америки, юга Африки и запада Южной Америки. В этих регионах в последние десятилетия ХХ века типичные значения $pH$ осадков составляют от 2.5 до 3.5, что хорошо согласуется с имеющимися данными измерений. Максимальная кислотность осадков (минимальное значение $pH$ гидрометеоров, близкое к 2) из-за антропогенных соединений серы отмечена на востоке средиземноморского региона. Перенос в примесей атмосфере приводит к тому, что в последние десятилетия ХХ века регионы с $pH < 3.5$ охватывают практически всю Евразию. Влияние этого переноса также заметно и в других регионах средних широт – на юге Северной Америки и на западе Южной Америки. В целом, использование схема ChAP целесообразно для МЗСПС, но после доработки с учетом влияния осадков разного типа на влажное осаждение соединений серы из атмосферы и учета влияния орографии на перенос примесей в атмосфере.
1. ВВЕДЕНИЕ
Одной из составляющих антропогенного воздействия на Земную систему являются эмиссии соединений серы в атмосферу. Основной вклад в эти эмиссии обусловлен выбросами диоксида серы [1–3]. В атмосфере этот газ окисляется до сульфатных аэрозолей (отметим также, что часть антропогенных сульфатов являются первичными аэрозолями), которые затем выводятся из атмосферы влажным и сухим осаждением. Влажное осаждение (вымывание атмосферными гидрометеорами), в свою очередь, приводит к формированию кислых осадков.
Такие осадки сами по себе являются нежелательным природным явлением. В частности, они приводят к увеличению кислотности водных объектов суши (озер, рек, и т.д.) [4–7], закислению почв с деградацией растительности [8, 9] и коррозии стальных конструкций [3]. Отметим, что увеличение кислотности водных объектов суши и закисление почв может происходить также и при сухом осаждении сульфатов и диоксида серы за счет их поглощения речной или озерной водой или влагой почвы с последующим включением в цепочку жидкофазных реакций серного цикла [3, 8].
Традиционно характеристикой кислотности осадков является $pH$. В соответствии с определением Международного союза теоретической и прикладной химии (The International Union of Pure and Applied Chemistry, IUPAC) эта величина определяется через активность свободных ионов водорода в осадках ${{a}_{{{{{\text{H}}}^{ + }}}}}$ [10]:
(1)
$pH = - \mathop {\log }\nolimits_{10} {\kern 1pt} {{a}_{{{{{\text{H}}}^{ + }}}}} = - \mathop {\log }\nolimits_{10} {\kern 1pt} \frac{{{{m}_{{{{{\text{H}}}^{ + }}}}}{{\gamma }_{{{{{\text{H}}}^{ + }}}}}}}{{{{m}_{ \star }}}},$(2)
$p{{H}_{F}} = - \mathop {\log }\nolimits_{10} \left( {{{m}_{{{{{\text{H}}}^{ + }}}}}{\text{/}}{{m}_{ \star }}} \right).$Измерения кислотности осадков достаточно редки. Это связано, в частности, с затруднениями выделения различных химических веществ, влияющих на кислотность осадков [6, 11]. Систематически измерения проводятся на нескольких десятках измерительных станций над сушей (см. рис. 15 из [6]). Типичные значения $pH$ составляют от 3 до 6, а в ряде регионов – даже от 2 до 3 [6].
Тем не менее, кислотность осадков может служить и дополнительным инструментом для верификации моделей химических процессов в атмосфере. В данной работе такая верификация проводится для схемы вычисления соединений серы в тропосфере ChAP-1.0 (Chemistry and Aerosol Processes), разработанной авторами данной статьи.
2 СХЕМА ВЫЧИСЛЕНИЯ СОДЕРЖАНИЯ СОЕДИНЕНИЙ СЕРЫ В АТМОСФЕРЕ
Подробное описание схемы ChAP-1.0 приведено в [12]. Она разработана для моделей Земной системы промежуточной сложности (МЗСПС) [13] и позволяет вычислять характеристики цикла серы в тропосфере. Основными предположениями схемы являются:
• вертикальные профили соединений Х серы в тропосферы экспоненциальны [2, 14, 15] с масштабом высоты ${{H}_{X}}$; для диоксида серы ${{H}_{{{\text{S}}{{{\text{O}}}_{2}}}}} = 1.2{\kern 1pt} {\text{ км}}{\kern 1pt} $, для сульфатов ${{H}_{{{\text{S}}{{{\text{O}}}_{2}}}}} = 1.8{\kern 1pt} {\text{км}}{\kern 1pt} $;
• нестационарные слагаемые в уравнениях баланса не учитываются (это связано с типичной формулировкой МЗСПС);
• все химические реакции подчиняются кинетике первого порядка [1–3]; газофазные реакции окисления ${\text{S}}{{{\text{O}}}_{2}}$ не учитываются; константы скорости гетерофазного (внутриоблачного) окисления зависят от температуры нижней тропосферы и от доли покрытия модельной ячейки облаками;
• влажное осаждение учитывается только для сульфатов, сухое осаждение – и для ${\text{S}}{{{\text{O}}}_{2}}$, и для ${\text{S}}{{{\text{O}}}_{4}}$; интенсивность обоих процессов пропорциональна содержанию соответствующего вещества в атмосфере; для влажного осаждения константа пропорциональности зависит от температуры нижней тропосферы и от количества осадков.
• современная версия схемы ChAP-1.0 учитывает только антропогенную часть атмосферного цикла серы (это исключает, например, формирование диоксида серы из диметилсульфида и карбонил-сульфида).
Расчеты со схемой были выполнены при задании среднемесячных антропогенных эмиссий диоксида серы в атмосферу в 1850–2000 гг. (в виде временных срезов с шагом по времени 10 лет) по данным CMIP5 (Coupled Models Intercomparison Project, phase 5) [16], а полей метеорологических переменных (температура, осадки, ветер, количество облаков) – по многолетним средним (с учетом годового хода) данным реанализа ERA-Interim [17] для 1979–2015 гг. Неучет межгодовой и более долгопериодной изменчивости приводит к исключению обратной связи между климатом и серным циклом атмосферы. Однако этот подход подобен использованному при подготовке полей интенсивности антропогенных и естественных эмиссий соединений серы в проекте CMIP5 [16], в связи с чем он используется и в данной работе. Все вычисления проводились на вычислительной сетке с шагом 4.5° по широте и 6.0° по долготе, что соответствует сетке модели Земной системы Института физики атмосферы им. А.М. Обухова Российской Академии наук [18, 19].
Отметим, что в данных CMIP5 доступно также полное содержание сульфатов на единицу площади (также полученное без учета обратных связей при межгодовых и более долгопериодных изменений климата), что позволяет провести верификацию схемы ChAP [12].
3 ВЫЧИСЛЕНИЕ $pH$ ОСАДКОВ
Т.к. в использованной версии ChAP $pH$ осадков не вычисляется, то в данной работе использована следующая схема вычисления данной переменной.
При интенсивности влажного осаждения сульфат-ионов ${{D}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}{\text{,wet}}}}}$ соответствующий молярный поток серы на поверхность
(3)
${{M}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}} = \frac{{{{D}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}{\text{,wet}}}}}}}{{{{\mu }_{{\text{S}}}}}},$(4)
${{\left[ {{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{4}}} \right]}_{{\text{T}}}}{{ = 10}^{{ - 3}}} \times \frac{{{{M}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}}}{{{{\mu }_{{\text{S}}}}P}}.$При попадании в воду серная кислота участвует в цепочке реакций
(5)
$\begin{gathered} {{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}} \rightleftharpoons {{{\text{H}}}^{ + }} + {\text{HSO}}_{{\text{4}}}^{ - }, \hfill \\ {\text{HSO}}_{{\text{4}}}^{ - } \rightleftharpoons {{{\text{H}}}^{ + }} + {\text{SO}}_{{\text{4}}}^{{{\text{2}} - }}. \hfill \\ \end{gathered} $Как правило, основную роль первая реакция цепи (5) c константой диссоциации ${{K}_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}} = 1 \times $ $ \times {{10}^{3}}\;{\kern 1pt} {\text{моль/л}}{\kern 1pt} $ [3]. Как следствие,
(6)
$\left[ {{{{\text{H}}}^{ + }}} \right]\left[ {{\text{HS}}{{{\text{O}}}_{{\text{4}}}}^{ - }} \right] = {{K}_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}\left[ {{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}} \right],$(7)
$\left[ {{\text{HSO}}_{4}^{ - }} \right] + \left[ {{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}} \right] = {{\left[ {{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}} \right]}_{{\text{T}}}}.$(8)
$\begin{gathered} \left[ {{{{\text{H}}}^{ + }}} \right]\left[ {{\text{HSO}}_{4}^{ - }} \right] = \\ = {{K}_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}{{\left[ {{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}} \right]}_{{\text{T}}}} - {{K}_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}\left[ {{\text{HSO}}_{4}^{ - }} \right]. \\ \end{gathered} $Поскольку в пренебрежении второй реакцией цепи (5) из уравнения первой реакции той же цепи следует, что
то(10)
${{\left[ {{{{\text{H}}}^{ + }}} \right]}^{2}} + {{K}_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}\left[ {{{{\text{H}}}^{ + }}} \right] - {{K}_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}{{\left[ {{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}} \right]}_{{\text{T}}}} = 0.$Единственным положительным корнем последнего уравнения служит
(11)
${{\left[ {{{{\text{H}}}^{ + }}} \right]}_{S}}\, = \,\frac{{\sqrt {K_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}^{2}\, + \,4{{K}_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}{{{\left[ {{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}} \right]}}_{{\text{T}}}}} - {{K}_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}}}{2}. = $(12)
$ = \frac{{{{K}_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}}}{2}\left( {\sqrt {1 + 4{{{\left[ {{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}} \right]}}_{{\text{T}}}}{\text{/}}{{K}_{{{{{\text{H}}}_{{\text{2}}}}{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}} - 1} \right).$Ввиду самодиссоциации воды, приводящей к фоновому значению $p{{H}_{0}} = 7$ [3], к решению (12) добавлялось соответствующее значение концентрации ионов водорода ${{\left[ {{{{\text{H}}}^{ + }}} \right]}_{0}}$, так что полная концентрация
(13)
$\left[ {{{{\text{H}}}^{ + }}} \right] = {{\left[ {{{{\text{H}}}^{ + }}} \right]}_{S}} + {{\left[ {{{{\text{H}}}^{ + }}} \right]}_{0}}.$Кислотность осадков $pH$ далее вычислялась по формуле (2).
Постановка численных экспериментов в данной работе с заданием метеорологических полей в виде средних многолетних значений исключает влияние изменений климата на характеристики закисленности осадков. Основным эффектом такого влияния является зависимость эффективности выведения сульфатов из атмосферы от типа осадков, так что на единицу массы выпадающей влаги интенсивность выведения уменьшается от крупномасштабных жидких осадков к конвективным и, далее, к крупномасштабным твердым осадкам [20, 21]. Для простейшего учета данного эффекта, наряду с базовыми расчетами, проведены расчеты с исключением осадков в месяцы с $\frac{1}{2}\left( {{{T}_{{850}}} + {{T}_{{1000}}}} \right) < 0^\circ {\text{C}}$, где ${{T}_{{850}}}$ и ${{T}_{{1000}}}$ – температура на изобарических уровнях 850 и 1000 гПа соответственно. При этом исключаются осадки в виде снега. Следует отметить, что такой подход не противоречит балансу массы серы в атмосфере, воспроизводимому ChAP – при этом просто в регионах и в месяцы с твердыми осадками соединения серы выводятся из атмосферы за счет сухого осаждения, и время жизни соединений серы в атмосфере увеличивается. Однако и в этом случае при откалиброванном в [12] значении коэффициента для сухого выведения ${\text{S}}{{{\text{O}}}_{{\text{4}}}}$ не превышает 1 мес. Таким образом, на сезонном масштабе времени (который и анализируется в данной статье, см. ниже) баланс массы серы в атмосфере не нарушается.
4 РЕЗУЛЬТАТЫ
4.1. Содержание в тропосфере и интенсивность осаждения ${\text{S}}{{{\text{O}}}_{{\text{2}}}}$ и ${\text{S}}{{{\text{O}}}_{{\text{4}}}}$
Результаты расчетов содержания ${\text{S}}{{{\text{O}}}_{{\text{2}}}}$ и ${\text{S}}{{{\text{O}}}_{{\text{4}}}}$ в тропоcфере, а также интенсивность их осаждения подробно представлены в [12]. Однако в данной работе целесообразно кратко их воспроизвести для полноты и удобства интерпретации результатов оценки закисленности осадков.
Подобно результатам расчетов с другими моделями, глобально около половины эмиссий ${\text{S}}{{{\text{O}}}_{{\text{2}}}}$ в атмосферу превращается в сульфаты, а вторая половина осаждается на поверхность Земли. Содержание антропогенного диоксида серы в атмосфере увеличивается от нулевого (по построению) значения в 1850 г. до $ \approx {\kern 1pt} 0.2\;{\kern 1pt} {\text{ТгS}}{\kern 1pt} $ в 1970–1990 гг., а затем уменьшается до $0.16\;{\kern 1pt} {\text{ТгS}}{\kern 1pt} $ к 2000 г. При этом масса антропогенных сульфатов в атмосфере увеличивается от нулевого в 1850 г. $ \approx 0.4\;{\kern 1pt} {\text{ТгS}}$ в 1970–1990 гг., а затем уменьшается до $0.32\;{\kern 1pt} {\text{ТгS}}$ к 2000 г. Эти значения в целом соответствуют оценкам CMIP5. Для сульфатов в модели основную роль (около 85%) играет влажное осаждение, что в целом согласуется с оценками по другим схемам серного цикла атмосферы [22]. Время нахождения диоксида серы (сульфатов) в атмосфере в ChAP близко к 1 сут., а сульфатов – к 5 сут., что также согласуется с результатами расчетов с другими схемами цикла серы в атмосфере (см. [23] и табл. 5.5 из [24]). Глобальная интенсивность влажного и сухого осаждения антропогенных соединений серы из атмосферы на поверхность Земли (с примерно равным друг другу вкладом этих типов осаждения в полное осаждение ${\text{S}}{{{\text{O}}}_{{\text{X}}}}$) хорошо согласуется с данными ACCMIP (Atmospheric Chemistry and Climate Model Intercomparison Project) [25], в котором также не учитывалось влияние межгодовых и более долгопериодных изменений климата на воспроизведение содержания химических веществ в атмосфере.
Региональные значения содержания и антропогенного ${\text{S}}{{{\text{O}}}_{{\text{2}}}}$, и антропогенного ${\text{S}}{{{\text{O}}}_{{\text{4}}}}$ характеризуются максимумами в регионах максимального загрязнения. Для последних десятилетий ХХ века это Европа, юго-восточная Азия и восток Северной Америки. Здесь содержание антропогенных диоксида серы и сульфатов (соответственно ${{B}_{{{\text{S}}{{{\text{O}}}_{{\text{2}}}}}}}$ и ${{B}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}$) на единицу площади, как правило, $ \geqslant {\kern 1pt} 2\;{\kern 1pt} {\text{мгS }}{{{\text{м}}}^{{ - 2}}}$, а для последней переменной оно даже превышает $5\;{\kern 1pt} {\text{мгS }}{{{\text{м}}}^{{ - 2}}}$ (рис. 3 и 5–7 из [12]). Кроме того, вторичные максимумы ${{B}_{{{\text{S}}{{{\text{O}}}_{{\text{2}}}}}}}$ и ${{B}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}$ отмечены на юге Африки и в регионах на западе Южной Америки. При этом сезонный ход ${{B}_{{{\text{S}}{{{\text{O}}}_{{\text{2}}}}}}}$ в регионах антропогенного загрязнения атмосферы соединениями серы не очень выражен, что в целом согласуется с данными CMIP5. Однако по расчетам с ChAP ${{B}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}$ в этих же регионах зимой значительно больше, чем летом, что отличается от соответствующих данных CMIP5. Следует отметить, что даже без учета естественных эмиссий соединений серы в атмосферу схема достаточно хорошо воспроизводит по крайней мере среднегодовые значения ${{B}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}$ в указанных выше регионах антропогенного загрязнения атмосферы соединениями серы по сравнению с данными реанализа CAMS (Copernicus Atmospheric Monitoring System) [26].
Географическое распределение годового полного осаждения антропогенных соединений серы в целом подобно географическому распределению антропогенных эмиссий этого элемента.
Для последних десятилетий ХХ века полная интенсивность осаждения (сумма интенсивностей влажного и сухого осаждения) соединений серы ${{D}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}$ в регионах соответствующего антропогенного загрязнения атмосферы в Северном полушарии превышает $2\;{\kern 1pt} {\text{МгS }}{{{\text{м}}}^{{ - 2}}}{\text{ го}}{{{\text{д}}}^{{ - 1}}}$ (рис. 1). Пространственное распределение годовой ${{D}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}$ в схеме ChAP над континентами подобно полученному в проекте ACCMIP. Тем не менее, по сравнению с данными ACCMIP схема ChAP завышает интенсивность влажного осаждения и занижает – сухого. Однако в Европе согласие для влажного осаждения заметно улучшается при использовании данных EMEP MSC-W (Meteorological Synthesizing Centre–West of the European Monitoring and Evaluation Programme) [27] и по расчетам с моделями MOGUNTIA [28], IMAGES [29] и GISS [22].
Рис. 1.
Влажное осаждение ${\text{S}}{{{\text{O}}}_{{\text{X}}}}$ (МгS м$^{{ - 2}}$ год$^{{ - 1}}$) для 2000 г. по расчетам со схемой ChAP (а; учитывается только влажное осаждение ${\text{S}}{{{\text{O}}}_{{\text{4}}}}$) и по результатам проекта ACCMIP [25] (б).

4.2 Кислотность осадков
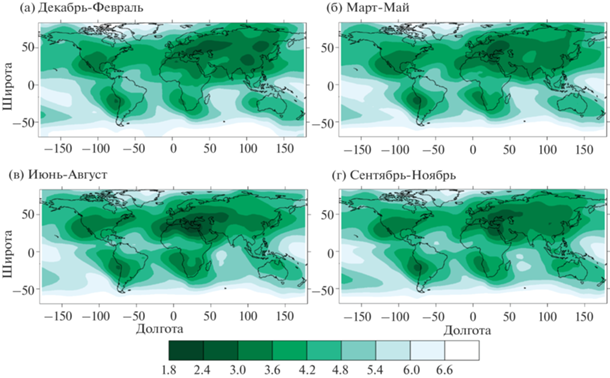
Уже для условий 1850 г. антропогенные эмиссии диоксида серы в атмосферу способны заметно изменить кислотность осадков от фонового значения $p{{H}_{0}} = 7$ (рис. 2). В частности, в разные сезоны $pH$ находится в интервале от 4.2 до 5.4 в регионах наиболее значительного загрязнения соединениями серы, прежде всего над Европой. Наиболее значима кислотность осадков в летний период. Отметим, что последнее отмечается даже с учетом общего занижения ${{B}_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}$ в этот сезон схемой ChAP. Как следствие, эффект закисления осадков соединениями серы для указанного года в реальности может оказаться даже более выраженным, чем в наших расчетах.
Рис. 2.
$pH$ осадков для эмиссий соединений серы в атмосферу, соответствующих 1850 г. в декабре-феврале (а), марте-мае (б), июне-августе (в) и сентябре-ноябре (г).
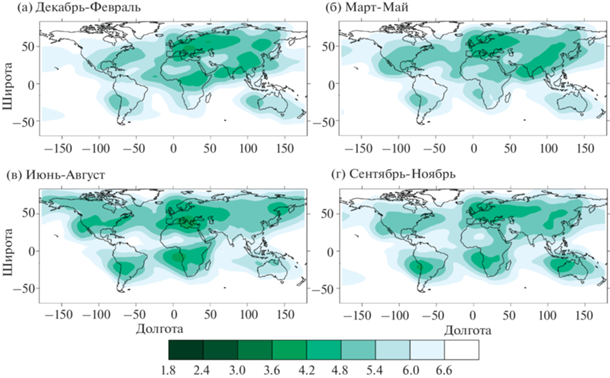
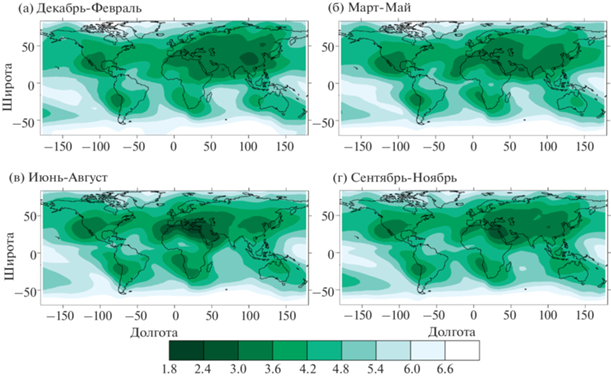
Общее увеличение интенсивности антропогенных эмиссий соединений серы в атмосферу на протяжении XX века приводит и к существенному увеличению закисленности осадков для последних десятилетий этого столетия (рис. 3 и 4). При этом к европейскому региону значительной кислотности осадков добавляются и другие регионы с высокой интенсивностью антропогенных эмиссий соединений серы в атмосферу – юго-восточная Азия, восток Северной Америки, юг Африки и запад Южной Америки.
Для обоих временных срезов в этих регионах типичные значения $pH$ осадков составляют от 2.5. до 3.5. Эти значения хорошо согласуются с приведенными на рис. 15 из [6] для временных интервалов 1986–1995 гг. и 1996–2005 гг. (см. также рис. 20.8 из [1]). Для территории России они также удовлетворительно согласуются с данными прямых наблюдений [30] за исключением регионов Поволжья и Забайкалья, где кислотность осадков в схеме ChAP выше, чем по данным наблюдений. Максимально закисленные осадки (с $pH$ близким к 2) в схемой воспроизводятся на востоке средиземноморского региона летом. Следует отметить, что в этом же регионе отмечено и минимальное значение $pH < 2$ по систематическим наблюдениям для 1986–1995 гг. Это значение не проявляется для более позднего временного интервала 1996–2005 гг. Все это в совокупности указывает на то, что в кислотные осадки в данном регионе около 1990 г. по крайней мере частично связаны с атмосферным переносом сульфатов из Европы. Следует отметить, что данные результат согласуется с [31], где было отмечено, что перенос воздушных масс на Европейскую территорию России из Средиземноморья сопровождается увеличением кислотности осадков.
Атмосферный перенос также приводит к тому, что в последние десятилетия ХХ века регионы с $pH < 3.5$ охватывают большую часть Евразии, юг Северной Америки и запад Южной Америки. В Северном полушарии кислотность осадков летом больше, чем зимой. Это в целом согласуется с отдельными измерениями в ряде регионов [3], [32]. Кроме того, зимой Южного полушария схема также воспроизводит подобную область на юге Африки и над расположенной рядом частью Атлантики. Эти расчеты затруднительно сравнить с данными наблюдений ввиду отсутствия систематических измерений кислотности осадков вне регионов с большой интенсивностью антропогенных эмиссий серы в атмосферу [6].
Следует отметить, что перенос примесей в атмосфере в использованном в данной работе варианте схемы ChAP не учитывает влияние орографии. Последнее может служить одной из причин занижения кислотности осадков в Поволжье и Забайкалье. Первый из этих регионов подвержен преимущественно влиянию европейского региона-источника, но отделен от него Валдайской возвышенностью с высотой до примерно 400 м. Высота горных гряд, отделяющих второй регион – Забайкалье – от соответствующего региона-источника, расположенного в юго-восточной Азии, еще выше и достигает нескольких километров. Таким образом, согласие модельных расчетов с данных прямых наблюдений в этих регионах может быть улучшено при учете влияния орографии на перенос примесей в атмосфере. При этом можно ожидать также улучшения воспроизведения и сезонного хода $pH$ осадков.
Основным различием временных срезов 1900 и 2000 гг. является общее уменьшение кислотности в Европе и, в меньшей степени, в Северной Америке, на юге Африки и в Южной Америке для второго среза относительно первого с увеличением в южной и юго-восточной Азии. Эти тренды обусловлены преимущественно соответствующими трендами антропогенных эмиссий серы в атмосферу в указанных регионах [2]. В регионах Евразии, подверженных загрязнению соединениями серы из европейского региона уменьшение кислотности осадков наиболее значимо проявляется в зимний и весенний периоды. Для других регионов, в которых проявляется уменьшение кислотности осадков, это уменьшение более однородно распределено по календарным сезонам. Относительно однородным по сезонам является и увеличение кислотности осадков от 1900 к 2000 гг. в южной и юго-восточной Азии.
4.3 Чувствительность кислотности осадков к типу осадков
Описанная выше постановка численных экспериментов затрудняет полный анализ чувствительности $pH$ к типу осадков (крупномасштабные жидкие, крупномасштабные твердые, конвективные). Однако простейший анализ можно провести за счет исключения наиболее неэффективного для влажного вымывания типа осадков – снега. Соответствующий анализ был проведен с исключением таких осадков в соответствии с алгоритмом раздела 3. Отметим, однако, что такой подход является весьма грубым. Например, он не учитывает зимние оттепели с возможным выпадением крупномасштабных осадков малой интенсивности (которые в пересчете на единицу массы выпадающей влаги наиболее эффективны для влажного выведения соединений серы в атмосфере [20, 21]) или, наоборот, развития сильных штормов в переходные сезоны с выпадением осадков в виде снега. Адекватный анализ таких эффектов возможен лишь при соответствующем учете типа выпадающих осадков, что в данной работе затруднительно. Тем не менее, используемый в данной работе грубый подход к учету влияния целесообразен, особенно ввиду общего завышения содержания сульфатов в атмосфере схемой ChAP в зимний период.
Поскольку такой подход очевидным образом не должен влиять на $pH$ осадков в летний период, достаточно ограничиться зимним периодом (рис. 5а) и переходными периодами (например, весной; рис. 5б). При этом в обоих случаях в регионах с отрицательными температурами в нижней тропосфере кислотность осадков значительно уменьшается. Это согласуется с обзором [6] результатов измерений $pH$ гидрометеоров.
5. ОБСУЖДЕНИЕ И ВЫВОДЫ
В данной работе проведен анализ кислотности осадков по расчетам со схемой серного цикла атмосферы ChAP-1.0 (Chemistry and Aerosol Processes), разработанной для моделей Земной системы промежуточной сложности. Расчеты со схемой были выполнены при задании среднемесячных антропогенных эмиссий диоксида серы в атмосферу в 1850–2000 гг. (в виде временных срезов с шагом по времени 10 лет) по данным проекта CMIP5 (Coupled Models Intercomparison Project, phase 5), а полей метеорологических переменных – по многолетним средним (с учетом годового хода) данным реанализа ERA-Interim для 1979–2015 гг. Вычисления проводились на сетке с шагом 4.5° по широте и 6.0° по долготе.
Выявлено, что значимая кислотность осадков характерна для регионов с высокой интенсивностью антропогенных эмиссий соединений серы в атмосферу – Европы, юго-восточной Азии, востока Северной Америки, юга Африки и запада Южной Америки. В этих регионах в последние десятилетия ХХ века типичные значения $pH$ осадков составляют от 2.5. до 3.5, что хорошо согласуется с имеющимися данными измерений. Максимальная кислотность осадков (минимальное значение $pH$ гидрометеоров, близкое к 2) из-за антропогенных соединений серы отмечена на востоке средиземноморского региона. В Северном полушарии кислотность осадков летом больше, чем зимой. Перенос примесей в атмосфере приводит к тому, что в последние десятилетия ХХ века регионы с $pH < 3.5$ охватывают практически всю Евразию. Влияние этого переноса также заметно и в других регионах средних широт – на юге Северной Америки и на западе Южной Америки. Тем не менее, ряд отличий пространственного распределения модельных данных от данных прямых измерений, а также соответствующие отличия в сезонном ходе, могут быть связаны с неучетом влияния орографии на перенос примесей в атмосфере в использованном в данной работе варианте схемы ChAP.
Следует отметить, что увеличение размера регионов, подверженных кислым осадкам, по сравнению с размером региона-источника может быть оценен именно как следствие переноса в атмосфере. Если считать, что
• бóльшая часть антропогенных эмиссий серы в атмосферу происходит в форме диоксида серы с последующим его окислением в сульфаты, выведение которых из атмосферы происходит преимущественно влажным осаждением;
• размер регионов – источников диоксида серы пренебрежимо мал по сравнению с размера региона влияния этого источника,
то порядок величины размера региона, подверженного влиянию источника по направлению преобладающей скорости ветра $u$, может быть оценен следующим образом:
(14)
$L = u\left( {{{\tau }_{{{\text{S}}{{{\text{O}}}_{{\text{2}}}}}}} + {{\tau }_{{{\text{S}}{{{\text{O}}}_{{\text{4}}}}}}}} \right),$Отметим также ряд ограничений данной работы.
• В работе не учитываются естественные эмиссии соединений серы – прежде всего диметилсульфида с поверхности океана и выделение диоксида серы и сульфатов из вулканов. Современная интенсивность первого источника оценивается величиной около $28\;{\kern 1pt} {\text{ТгS/год}}{\kern 1pt} $ [33, 34], [35], второго – около $23\;{\kern 1pt} {\text{ТгS/год}}{\kern 1pt} $ (выделение диоксида серы из-за извержений на порядок меньше) [36]. Суммарная интенсивность этих источников сравнима с интенсивностью антропогенных эмиссий ${\text{S}}{{{\text{O}}}_{{\text{2}}}}$ в атмосферу в последние десятилетия ХХ века ($ \approx {\kern 1pt} 54\;{\kern 1pt} {\text{ТгS/год}}{\kern 1pt} $ [37]). Таким образом, их учет может дополнительно увеличить кислотность осадков, в том числе и над континентами. С учетом логарифмической зависимости $pH$ от концентрации ионов водорода в гидрометеорах это увеличение может привести к уменьшению $pH$ на несколько десятых.
• Кислотность осадков также может возрасти при учете влажного осаждения диоксида серы. Однако для большинства современных моделей вклад влажного осаждения ${\text{S}}{{{\text{O}}}_{{\text{2}}}}$ в полное осаждение этого газа не превышает 15% [24], что лишь незначительно изменит вычисленные в данной работе значения $pH$.
• В работе не учитывается влияние на $pH$ осадков оснований других кислот, присутствующих в атмосфере (в том числе азотной кислоты). В связи с последним важно иметь в виду, что после 2000 г. в промышленно развитых регионах (Европа, США, Китай) отмечен рост содержания нитратов в атмосферных осадках [11]. Адекватную оценку этого влияния в данной работе сделать затруднительно. Однако, исходя из общей реалистичности полученных результатов и их удовлетворительного согласия с имеющимися данными наблюдений, можно утверждать, что для пространственно-временного разрешения, использованного в данной работе, учет таких веществ не изменит $pH$ осадков более чем на единицу. Кроме того, период с ростом вклада нитратов в кислотность осадков не учитывается в данной работе, т.к. расчеты заканчиваются в 2000 г.
• Кроме того, в работе не учитывается влияние углекислого газа на кислотность осадков [1, 2, 3]. Будучи хорошо перемешанным в атмосфере, углекислый газ способен уменьшить пространственные различия $pH$ между регионами с сильным и слабым загрязнением атмосферы соединениями серы.
Таким образом, проведенная в данной работе дополнительная верификация схемы ChAP показывает ее реалистичность для моделей Земной системы промежуточной сложности. При этом, однако, целесообразна доработка схемы с учетом влияния осадков разного типа на влажное осаждение соединений серы из атмосферы и учета влияния орографии на перенос примесей в атмосфере.
Авторы выражают благодарность Г.В. Сурковой и анонимным рецензентам за замечания, высказанные к предыдущей версии работы. Часть работы, связанная с разработкой схемы химических процессов в атмосфере, была проведена с использованием УНУ “Самолет-лаборатория ТУ-134 “Оптик” при финансовой поддержке Минобрнауки РФ (соглашение 075-15-2021-934). Часть работы, связанная с анализом пространственных и временных особенностей $pH$ осадков выполнена за счет средств Программы стратегического академического лидерства Казанского (Приволжского) федерального университета (ПРИОРИТЕТ-2030).
Список литературы
Seinfeld J., Pandis S. Atmospheric chemistry and physics: From air pollution to climate change. Hoboken: Wiley. 2006. 1326 p.
Warneck P. Chemistry of the Natural Atmosphere. San Diego: Academic Press. 2000. 927 p.
Суркова Г.В. Химия атмосферы. М.: МГУ. 2002. 210 с.
Моисеенко Т.И., Гашкина Н.А. Зональные особенности закисления озер // Водные ресурсы. 2011. Т. 38. 1. С. 39–55.
Моисеенко Т.И., Гашкина Н.А., Дину М.И. и др. Влияние природных и антропогенных факторов на процессы закисления вод в гумидных регионах // Геохимия. 2017. 1. С. 41–56.
Pye H.O.T., Nenes A., Alexander B. et al. The acidity of atmospheric particles and clouds // Atmos. Chem. Phys. 2020. V. 20. 8. P. 4809–4888.
Tilgner A., Schaefer T., Alexander B. et al. Acidity and the multiphase chemistry of atmospheric aqueous particles and clouds // Atmos. Chem. Phys. 2021. V. 21. 17. P. 13483–13536.
Kuylenstierna J.C.I., Rodhe H., Cinderby S. et al. Acidification in developing countries: Ecosystem sensitivity and the critical load approach on a global scale // Ambio. 2001. V. 30. 1. P. 20–28.
Моисеенко Т.И., Калабин Г.В., Хорошавин В.Ю. Закисление водосборов арктических регионов // Изв. РАН, серия географическая. 2012. 2. С. 49–58.
Buck R.P., Rondinini S., Covington A.K. et al. Measurement of $pH$. Definition, standards, and procedures (IUPAC Recommendations 2002) // Pure Appl. Chem. 2002. V. 74. 11. P. 2169–2200.
Vet R., Artz R.S., Carou S. et al. A global assessment of precipitation chemistry and deposition of sulfur, nitrogen, sea salt, base cations, organic acids, acidity and $pH$, and phosphorus // Atmos. Environ. 2014. V. 93. P. 3–100.
Eliseev A.V., Gizatullin R.D., Timazhev A.V. ChAP 1.0: A stationary tropospheric sulfur cycle for Earth system models of intermediate complexity // Geosci. Model. Dev. 2021. V. 14. 12. P. 7725–7747.
Claussen M., Mysak L., Weaver A. et al. Earth system models of intermediate complexity: closing the gap in the spectrum of climate system models // Clim. Dyn. 2002. V. 18. 7. P. 579–586.
Jaenicke R. Tropospheric aerosols // Aerosol–Cloud–Climate Interactions. Hobbs P. (ed.). San Diego: Academic Press 1993. P. 1–31.
Елисеев А.В., Тимажев А.В., Хименес П.Л. Вертикальный масштаб для профилей водяного пара и соединений серы в нижней тропосфере // Оптика атмосферы и океана. 2022. Т. 35. 7. .
Lamarque J.-F., Bond T.C., Eyring V. et al. Historical (1850–2000) gridded anthropogenic and biomass burning emissions of reactive gases and aerosols: methodology and pplication // Atmos. Chem. Phys. 2010. V. 10. 15. P. 7017–7039.
Dee D.P., Uppala S.M., Simmons A.J. et al. The ERA–Interim reanalysis: configuration and performance of the data assimilation system // Quart. J. R. Met. Soc. 2011. V. 137. 656. P. 553–597.
Мохов И.И., Елисеев А.В. Моделирование глобальных климатических изменений в XX–XXIII веках при новых сценариях антропогенных воздействий RCP // Доклады AH. 2012. Т. 443. 6. С. 732–736.
Мохов И.И., Елисеев А.В., Гурьянов В.В. Модельные оценки глобальных и региональных изменений климата в голоцене // Доклады Aкадемии наук. Науки о Земле. 2020. V. 490. 1. P. 27–32.
Allen R.J., Landuyt W., Rumbold S.T. An increase in aerosol burden and radiative effects in a warmer world // Nature Clim. Change. 2016. V. 6. 3. P. 269–274.
Wang Y., Xia W., Liu X. et al. Disproportionate control on aerosol burden by light rain // Nature Geosci. 2021. V. 14. 2. P. 72–76.
Koch D., Jacob D., Tegen I. et al. Tropospheric sulfur simulation and sulfate direct radiative forcing in the Goddard Institute for Space Studies general circulation model // J. Geophys. Res.: Atmospheres. 1999. V. 104. D19. P. 23799–23822.
Gliß J., Mortier A., Schulz M. et al. Aerocom phase III multi-model evaluation of the aerosol life cycle and optical properties using ground- and space-based remote sensing as well as surface in situ observations // Atmos. Chem. Phys. 2021. V. 21. 1. P. 87–128.
Climate Change 2001: The Scientific Basis. Contribution of Working Group I to the Third Assessment Report of the Intergovernmental Panel on Climate Change. Houghton J.T., Ding Y., Griggs D.J. (eds.). Cambridge/New York: Cambridge University Press. 2001. 881 p.
Lamarque J.-F., Dentener F., McConnell J. et al. Multi-model mean nitrogen and sulfur deposition from the Atmospheric Chemistry and Climate Model Intercomparison Project (ACCMIP): evaluation of historical and projected future changes // Atmos. Chem. Phys. 2013. V. 13. 16. P. 7997–8018.
Inness A., Ades M., Agustí–Panareda A. et al. The CAMS reanalysis of atmospheric composition // Atmos. Chem. Phys. 2019. V. 19. 6. P. 3515–3556.
Simpson D., Benedictow A., Berge H. et al. The EMEP MSC-W chemical transport model – technical description // Atmos. Chem. Phys. 2012. V. 12. 16. P. 7825–7865.
Langner J., Rodhe H. A global three–dimensional model of the tropospheric sulphur cycle // J. Atmos. Chem. 1991. V. 13. 3. P. 225–263.
Pham M., Müller J-F., Brasseur G.P. et al. A three-dimensional study of the tropospheric sulfur cycle // J. Geophys. Res.: Atmospheres. 1995. V. 100. D12. P. 26 061–26 092.
Свистов П.Ф. Антропогенные осадки: происхождение, состав и свойства // Экологическая химия. 2011. Т. 20. 2. С. 105–113.
Суркова Г.В., Еремина И.Д., Мордкович П.А. О влиянии крупномасштабного атмосферного переноса на химический состав и количество атмосферных осадков в центре Европейской территории Рoссии // Метеорология и гидрология. 2010. 4. С. 36–44.
Еремина И.Д., Чубарова Н.Е., Алексеева Л.И. и др. Кислотность и химический состав осадков на территории московского региона в теплый период года // Вестник Московского университета. Серия 5: География. 2014. 5. С. 3–11.
Lana A., Bell T.G., Simó R. et al. An updated climatology of surface dimethlysulfide concentrations and emission fluxes in the global ocean // Glob. Biogeochem. Cycles. 2011. V. 25. 1. P. GB1004.
Galí M., Levasseur M., Devred E. et al. Sea-surface dimethylsulfide (DMS) concentration from satellite data at global and regional scales // Biogeosciences. 2018. V. 15. 11. P. 3497–3519.
Wang W.-L., Song G., Primeau F. et al. Global ocean dimethyl sulfide climatology estimated from observations and an artificial neural network // Biogeosciences. 2020. V. 17. 21. P. 5335–5354.
Carn S.A., Fioletov V.E., McLinden C.A. et al. A decade of global volcanic ${\text{S}}{{{\text{O}}}_{{\text{2}}}}$ emissions measured from space // Sci. Rep. 2017. V. 7. 1. P. 44095.
Lamarque J.-F., Kyle G.P., Meinshausen M. et al. Global and regional evolution of short–lived radiatively–active gases and aerosols in the Representative Concentration Pathways // Clim. Change. 2013. V. 109. 1–2. P. 191–212.
Дополнительные материалы отсутствуют.
Инструменты
Известия РАН. Физика атмосферы и океана