Журнал физической химии, 2019, T. 93, № 1, стр. 154-157
Особенности адсорбции бутена-1 на цеолите H-бетаЭ. А. Волнина, М. А. Кипнис, С. Н. Хаджиев
Э. А. Волнина a, М. А. Кипнис a, *, С. Н. Хаджиев a
a Российская академия наук, Институт нефтехимического синтеза им. А.В. Топчиева
Москва, Россия
* E-mail:
Поступила в редакцию 20.03.2018
Аннотация
Методом проточно-адсорбционной калориметрии исследована адсорбция бутена-1 на цеолите Бета (Н-форма). При пуске бутена-1 (использована смесь 2 об. % бутена-1 в азоте) при комнатной температуре на предварительно прокаленный цеолит (500°С) обнаружен экзоэффект, связанный с адсорбцией и превращениями бутена, в частности, протеканием реакции изомеризации до цис-транс-бутенов-2. При термодесорбции адсорбированного бутена-1 в продуктах зафиксирован ряд углеводородов, что свидетельствует о реакциях олигомеризации в процессе адсорбции. Установлено, что цеолит, предварительно обработанный влажным азотом, адсорбирует воду до содержания 9.2 мас. %; при адсорбции бутена-1 на таком регидратированном цеолите выявлен слабый экзоэффект, связанный, по-видимому, с физической адсорбцией бутена-1. При длительной выдержке регидратированного цеолита в токе смеси бутен/азот на выходе из реактора зафиксирован цис-бутен-2, что свидетельствует о постепенном замещении воды бутеном-1 на активных центрах цеолита.
Реакции легких алкенов на твердокислотных катализаторах, в частности, изомеризация, активно исследуются в настоящее время. Так, в [1, 2] изучена изомеризация н-бутена-1 в изобутен на ряде цеолитов в Н-форме при 400°С, в [3] – олигомеризация пропена и бутена-1 на Н-цеолитах и алюмосиликатах при 230°С, в [4] – скелетная изомеризация бутена-1 в изобутен на ферьерите при 400°С, в [5] – скелетная изомеризация бутена-1 в бутен-2 при комнатной температуре на Pd-содержащих цеолитах Бета и ZSM-5, в [6] – олигомеризация изобутена при 40–100°С на ряде цеолитов.
В [7] установлено, что на характер адсорбции изобутена на цеолите НY, промотированном Ca и La, влияет температура дегидратации цеолита. Снижение температуры дегидратации с 500 до 130°C приводит к изменению характера экзоэффекта, связанного с адсорбцией и превращениями изобутена. Можно полагать, что это связано с присутствием гидроксилов в случае низкой температуры термообработки. Влияние воды на изомеризацию бутена-1 в изобутен на нанесенной гетерополикислоте (H4SiW12O40) отмечено в [8]: добавка воды положительно влияет на конверсию, снижая, по мнению авторов, коксование активных центров.
В настоящей работе изучено влияние воды на адсорбцию бутена-1 на цеолите Н-Бета при комнатной температуре методом проточно-адсорбционной калориметрии, использованным ранее при изучении адсорбции изобутана и изобутена на ряде цеолитов [7, 9].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Характеризация цеолита
Использовали цеолит Бета в аммонийной форме (производитель ОАО “АЗК и ОС”). Для удаления органического темплата из исходного цеолита и перевода его в Н-форму проводили прокаливание при 500°С в течение 2 ч. Элементный анализ выполняли на усовершенствованном волновом рентгенофлуоресцентном спектрометре ARL Perform’x.
Термопрограммированную десорбцию (ТПД) аммиака выполняли на сорбционном анализаторе УСГА-101 (“Унисит”, Россия). Фракцию предварительно таблетированного цеолита размером 0.2–0.5 мм прокаливали в токе осушенного гелия при 550°С, затем охлаждали до 60°С. Адсорбцию аммиака проводили в течение 30 мин при 60°C из потока, содержащего 10% аммиака в азоте. Физически сорбированный аммиак отдували в токе осушенного гелия при 100°С в течение 1 ч. ТПД NH3 проводили в интервале температур от 60 до 700°С в токе осушенного гелия (расход 30 мл/мин) со скоростью нагрева 8 K/мин.
Кривые потери массы образцов исходного и регидратированного цеолита получали с использованием термоанализатора SDTQ600, нагрев со скоростью 8 K/мин до 600°С.
Исследование адсорбции
Схема проточной установки, на которой проведены эксперименты, приведена в [9]. Основные элементы установки: кварцевый реактор с шлифовыми вводами для поступающего газа и термопары, контролирующей температуру слоя образца, электропечь, регуляторы и измерители расхода и давления. В реактор (внутренний диаметр 13 мм), помещенный в электропечь, на вставку из пористого кварца загружали навеску цеолита. Для контроля тепловых эффектов в процессе обработки цеолита использовали одну или две термопары типа КТХА (ПК “Тесей”) с диаметром чехла 1 мм. Спаи термопар размещали на уровне входа и выхода из слоя. Для навески массой 0.6 г высота слоя 14 мм.
Расход газового потока (55–60 нмл/мин) устанавливали с помощью регулятора давления и вентиля тонкой регулировки и измеряли на входе и выходе из реактора измерителями ИРГ-100. Давление на входе в установку и входе в реактор контролировали датчиками давления. Газовая схема установки оснащена двумя трехходовыми вентилями (до и после реактора), позволяющими направлять поток газа в реактор или “в обход”. Кроме того, комбинируя соответствующие повороты вентилей, можно проводить опрессовку реактора, проверяя его герметичность. Для работы с влажным азотом на линии входа в реактор устанавливали шестиходовой кран и сатуратор с водой. Показания температур, расходов, давлений выводили с помощью специальной программы (разработчик А.С. Коротков) на дисплей и записывали в файл.
Для адсорбции бутена использовали смесь 2 об. % С4Н8 в азоте. Использовали 1-бутен, чистотой 99.5% (Linde AG). Смесь готовили по давлению в предварительно отвакуумированном баллоне.
Исследования проводили на предварительно прокаленном цеолите, навеску которого после помещения в реактор дополнительно прокаливали в токе азота при 500°С в течение 1 ч и затем охлаждали до комнатной температуры в токе азота. Для регидратации прокаленного цеолита при комнатной температуре азот перед вводом в реактор пропускали через водный сатуратор. Процесс регидратации контролировали, следя за показаниями термопары в слое образца: адсорбция воды сопровождалась заметным экзоэффектом. По мере насыщения образца водой температура слоя снижалась, приближаясь к исходному значению. При продуве регидратированного образца сухим азотом наблюдался небольшой эндоэффект, свидетельствующий об удалении слабосвязанной воды.
Хроматографический анализ углеводородов выполняли на хроматографе “Хром 5” (колонка 23% SP-1700 Supelco, детектор ПИД).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Физико-химические данные
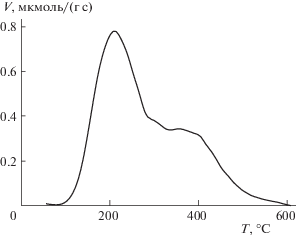
По данным элементного анализа, содержание SiO2, Al2O3 отвечает силикатному модулю 29. В качестве примесей присутствуют оксиды (мас. %):Ca (0.6), Mg (0.4), Fe (0.1), Na (0.08). По данным дериватографии, удаление органики из исходного цеолита протекает в температурном интервале 420–480°С. Цеолит в Н-форме изучали с использованием ТПД аммиака. Соответствующий спектр представлен на рис. 1. Вид кривой термодесорбции свидетельствует о наличии, по крайней мере, двух типов центров, существенно различающихся по энергетике. Общая кислотность 1045 мкмоль аммиака/г (в интервале 55–300°С десорбируется 670 мкмоль аммиака/г, выше 300°С – 375 мкмоль аммиака/г).
По данным дериватографии при прокаливании до 600°С регидратированный цеолит теряет мас. 9.2% .При этом максимум пика потери массы (∼100оС) связан с удалением молекулярно-связанной воды. Исследование потери массы, выполненное с промежуточной остановкой при 120°С (выдержка 20 мин до выхода кривой ДTG на плато) показало, что при последующем нагреве от 120 до 500°С удаляется 0.026 г воды в пересчете на 1 г прокаленного цеолита. Эту потерю массы можно отнести к дегидроксилированию цеолита.
Адсорбционные исследования на прокаленном цеолите
Адсорбция бутена-1 при комнатной температуре на предварительно прокаленном цеолите сопровождается значительным по амплитуде и протяженности экзоэффектом (рис. 2) и образованием цис- и транс-бутенов-2 (рис. 3). Максимальный разогрев наблюдается на выходе из слоя. При этом начальный прирост температуры на выходе из слоя составляет ∼7°С. Быстрый начальный подъем температуры отражает, на наш взгляд, адсорбцию бутена-1, тогда как далее на характер экзоэффекта влияют протекающие реакции. Характерно, что образование изомеров проходит через максимум и постепенно снижается (рис. 3а), но при этом отношение цис/транс-бутенов-2 монотонно растет (рис. 3б), увеличиваясь за 4 ч от 1.8 до 8. После замены смеси на азот в течение 0.5 ч на выходе из реактора детектировали постепенно уменьшающиеся следы изомеров, а следы бутена-1 наблюдали в течение 1.5 ч. Выгруженный образец увеличил массу по сравнению с исходным значением на 0.6 мас. %.
Рис. 2.
Температурный эффект при адсорбции бутена-1 на прокаленном цеолите Бета при комнатной температуре; 1 и 2 – температура на выходе из слоя и входе в слой соответственно. Навеска 0.64 г. Стрелкой отмечен момент пуска смеси 2 об. % бутен-1/N2.
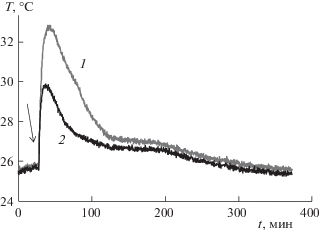
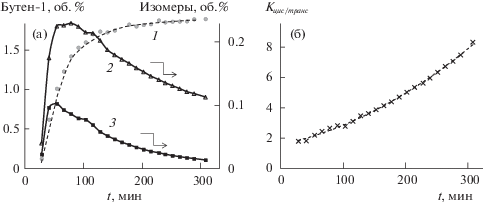
Рис. 3.
Выход углеводородов при адсорбции бутена-1 на прокаленном цеолите Бета при комнатной температуре; а: 1 – бутен-1, 2 – цис-бутен-2, 3 – транс-бутен-2; б – временная зависимость отношения цис/транс-бутенов. Навеска 0.64 г.
При повторении эксперимента с адсорбцией бутена-1 с последующим прогревом образца в токе азота, в процессе нагрева до 200°С наблюдали появление не только бутенов-2, но и изобутана, бутана, пентана, пентенов, метилпентанов. Это позволяет полагать, что наблюдающиеся температурные эффекты при адсорбции бутена-1 (рис. 2) связаны не только с адсорбцией и изомеризацией, но и с олигомеризацией бутена-1 и, возможно, его продуктов. При этом образующиеся продукты, по-видимому, препятствуют протеканию реакций изомеризации, с чем и связано постепенное снижение выхода изомеров (рис. 3а).
Адсорбционные исследования на регидратированном цеолите
Адсорбированная вода существенно влияет на адсорбцию бутена-1: резко уменьшается термический эффект адсорбции (рис. 4а), в газовых продуктах отсутствует транс-бутен-2, а содержание цис-бутена-2 существенно снижается по сравнению с адсорбцией на прокаленном образце (ср. 3а и рис. 4б). Кроме того, при адсорбции бутена-1 на регидратированном образце экзоэффект адсорбции бутена-1 сопровождается последовательно эндоэффектом (интервал 70–130 мин), связанным, по нашему мнению, с частичной десорбцией слабоадсорбированной воды в токе газовой смеси.
Рис. 4.
Влияние воды на термоэффект адсорбции бутена на регидратированном цеолите Бета при комнатной температуре. Стрелками отмечены моменты пуска смеси 2% С4H8/N2 и азота (пунктир). Навеска 0.62 г; а – динамика температуры слоя: 1 и 2 – температура на выходе из слоя и входе в слой соответственно; б – содержание бутенов на выходе из реактора: 1 – бутен-1, 2 – цис-бутен-2.
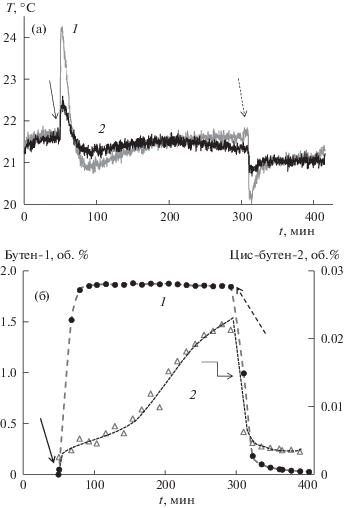
После пуска смеси на выходе из реактора появляется цис-бутен-2 (рис. 4б), содержание которого растет во времени, что свидетельствует о вытеснении адсорбированной воды бутеном. Вместе с тем транс-бутен-2 отсутствует, по-видимому, вследствие того, что на центрах, связанных с его образованием, вода адсорбирована прочнее. Содержание бутена-1 на выходе из реактора быстро выходит на стационар, достигая величины ∼1.85 об. %. Поскольку в исходной смеси содержание бутена-1 составляет 2 об. %, различие в 0.15 об. % можно отнести к адсорбции бутена-1 на цеолите. Так, при смене смеси на азот (∼310 мин) наблюдается заметный эндоэффект, а содержание бутена-1 на выходе из реактора после резкого падения (интервал 290–323 мин) снижается медленно в течение 80 мин.
Таким образом, хотя бутен-1 и вытесняет адсорбированную воду, о чем свидетельствует рост содержания изомера (рис. 3б), но вода, при определенных условиях, может конкурировать с бутеном-1 за активные центры цеолита Н-Бета.
Работа выполнена в рамках Государственного задания ИНХС РАН при финансовой поддержке ФАНО России.
Список литературы
Jo D., Hong S.B. // Chem. Cat. Chem. 2017. V. 9. P. 114.
Jo D., Hong S.B., Camblor M.A. // ACS Catal. 2015. V. 5. P. 2270.
Sarazen M.L., Doskocil E., Iglesia E. // J. Catal. 2016. V. 344. P. 553.
Lee Y., Park M.B., Kim P.S. et al. // ACS Catal. 2013. V. 3. P. 617.
Li Y., Ma C., Yang H. et al. // Chem. Eng. J. 2016. V. 299. P. 1.
Yoon J.W., Chang J.-S., Lee H.-D. et al. // J. Catal. 2007. V. 245. P. 253.
Кипнис М.А., Сухореброва О.А., Герзелиев И.М. и др. // Нефтехимия. 2015. Т. 55. № 2. С. 134–139.
Zhang J., Ohnishi R., Kamiya Y., Okuhara T. // J. Catal. 2008. V. 254. P. 263.
Кипнис М.А., Самохин П.В., Яшина О.В., Сухореброва О.А. // Журн. физ. химии. 2013. Т. 87. С. 868.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии