Журнал физической химии, 2019, T. 93, № 12, стр. 1763-1772
Строение и периодичность свойств металл-органических каркасов
Л. М. Кустов a, b, *, А. И. Куделин a, В. И. Исаева b
a Московский государственный университет им. М.В. Ломоносова,
Химический факультет
119992 Москва, Россия
b Российская академия наук, Институт органической химии им. Н.Д. Зелинского
119991 Москва, Россия
* E-mail: lmk@ioc.ac.ru
Поступила в редакцию 10.05.2019
После доработки 10.05.2019
Принята к публикации 14.05.2019
Аннотация
В обзоре дан анализ структуры металл-органических каркасов в связи с периодичностью их свойств, определяющихся положением элементов, образующих металл-органический каркас в Периодической таблице элементов Д.И. Менделеева. В настоящее время синтезировано 69666 соединений таких координационных полимеров, которые содержат 78 элементов Периодической таблицы и структура которых установлена. Перечислены обстоятельства, затрудняющие адекватный анализ исследованных структур.
Металл-органические каркасные структуры (metal organic frameworks, MOFs), которые представляют лишь часть огромного многообразия координационных полимеров, произвели революцию в современной химии. Ведь еще 20 лет назад не существовало такого термина и этого теперь весьма обширного класса соединений. Это – периодические решетки, построенные из неорганических единиц (как правило, ионы металлов) и органических линкеров, соединяющих неорганические структурные единицы [1–3]. По сути MOF представляет собой органический цеолит (рис. 1). Напомним, что цеолиты были открыты в 18 веке, первые синтетические цеолиты появились в 1950–1960-х годах, и до сих пор их число не превышает 250 [4], при том что на практике используется не более 10 структур. Первая работа по MOF была опубликована в 1989 г., а термин MOF был предложен O. Yaghi в 1995 г. [5, 6]. Начиная с 2000–2002 гг. публикации по этим материалам растут как лавина, и сейчас их уже насчитывается около 70000, хотя возможное число комбинаций неорганических единиц и органических линкеров может быть оценено как 1020, т.е. ограничено только человеческим воображением. Отметим, что металл-органические каркасы могут быть одно-, двух- и трехмерными (пористыми) [1–3], причем их удельная поверхность (условная) может достигать 5000–10000 м2/г, а объем пор – 2–3 см3/г, это на порядок больше, чем соответствующие величины для цеолитов (500–600 м2/г, 0.3–0.4 см3/г). Столь же безграничны и области их применения. Помимо уже хорошо изученных (катализ, адсорбенты, сенсоры, мембраны) исследуются и совершенно нетрадиционные области (нелинейная оптика, хранение запахов, средства доставки лекарств и пр.), которые, впрочем, практически сразу становятся традиционными для этих материалов [7–11].
Рис. 1.
Формирование мезоструктурированной матрицы MOF на основе ионов металлов и полифункциональных органических линкеров в присутствии мицелл ПАВ в качестве темплата [60]; М – ион металла или металлический кластер, L – мультифункциональный органический лиганд, Т – мицеллы (темплат).

СИНТЕЗ И МОДИФИЦИРОВАНИЕ МЕТАЛЛ-ОРГАНИЧЕСКИХ КАРКАСНЫХ СТРУКТУР
Благодаря исключительным текстурным свойствам, а также возможности варьирования геометрии и функциональности пор путем рационального подбора строительных блоков каркаса, MOF представляют собой пример направленного дизайна пористых гибридных материалов. В соответствии с принципами рационального дизайна, характеристики MOF и материалов на их основе можно регулировать с учетом области их конкретного применения. Действительно, в настоящее время потенциальными областями применения MOF являются хранение газов [12–16], гетерогенный катализ [17–20], адсорбция и разделение газов и органических соединений [21–26], направленная доставка лекарств в живом организме [27] и создание сенсорных устройств [28]. Свойства, в частности, каталитическая активность матриц MOF определяется размером и формой пор, а также химическим составом каналов и полостей [29].
Большинство исследований, связанных с MOF, относятся, в основном, к синтезу этих соединений, структурному анализу и определению потенциальных областей применения металл-органических каркасов [30]. В этом контексте разработка доступных, быстрых и экономичных способов синтеза MOF имеет существенное значение не только с фундаментальной точки зрения, но и для дальнейшего масштабирования и практического использования металл-органических каркасов и гибридных материалов на их основе. Это обусловлено тем, что экспресс-методы синтеза наиболее удобны для масштабирования процессов получения MOF. Сокращение времени реакции и температуры позволяет реализовать энергосберегающие процессы и избежать использования сложной аппаратуры [31].
Важная проблема для приготовления гибридных материалов на основе MOF – получение образцов с контролируемой морфологией (размером и формой) кристаллов [32, 33]. К этим материалам, в частности, относятся мембраны в виде тонких пленок и слоев MOF, нанесенных на пористые носители и гибридные МММ (mixed matriх membrane) мембраны, представляющие собой полимерные матрицы, содержащие внедренные наночастицы MOF [34].
Известно, что выбор способа синтеза определяет размер частиц, морфологию, распределение частиц по размерам формируемых образцов MOF [31, 35]. Эти характеристики, в свою очередь, влияют на свойства металл-органических каркасов, имеющих практическое значение. Например, размер частиц MOF определяет диффузию гостевых молекул в этих матрицах, что, в свою очередь, влияет на каталитические, адсорбционные или газоразделительные свойства материалов на их основе.
К настоящему времени разработаны различные подходы к воспроизводимому синтезу металл-органических каркасов. К этим методам относится, в первую очередь, масштабированный гидро(сольво)термальный способ, который наиболее подходит к промышленным условиям производства в масштабе тысяч тонн в год и обычно используется для синтеза цеолитов. В связи с этим гидро(сольво)термальный метод представляет существенный интерес для получения адсорбентов и носителей гетерогенных катализаторов на основе MOF [36]. В последнее время были проведены исследования, связанные с масштабированием сольвотермального синтеза для получения MOF с целью их практического применения [37, 38].
Однако, гидро(сольво)термальный способ синтеза MOF энергоемок и требует специального оборудования [39]. Для преодоления этих ограничений были предложены новые подходы, например, сольвотермальный синтез в несмешивающихся растворителях [32]. Этот метод, предусматривающий проведение реакции синтеза на границе раздела фаз, позволяет контролировать размер кристаллитов MOF в нанодиапазоне.
В настоящее время исследуются альтернативные способы получения металл-органических каркасов: гидро(сольво)термальный синтез в условиях СВЧ-активации (нагрева) реакционной массы [40], электрохимический метод [41], проведение реакции под воздействием ультразвука [42], а также механохимический метод (“solvent-free”) [43]. Последний метод представляет собой пример реализации подходов “зеленой химии”, поскольку в этом случае реакция проводится без растворителя [44, 45].
В [46] отмечается, что синтез в СВЧ-полях постепенно начинает вытеснять “традиционный” сольвотермальный способ синтеза под воздействием тепловой обработки. Так, сольвотермальный способ синтеза MOF требует значительных временных затрат, от 20 ч до 3 сут [47–49]. По сравнению с обычным сольвотермальным методом преимущества СВЧ-метода заключаются в резком снижении времени реакции (до нескольких часов или минут), увеличении выхода целевого продукта и улучшении качества продукта.
Матрицы MOF отличаются улучшенными функциональными характеристиками по сравнению с традиционными носителями, такими как цеолиты и активированные угли [50]. К этим свойствам принадлежат низкая кристаллическая плотность, высокая удельная поверхность, большой объем пор, доступных для адсорбата или субстрата, а также возможность рационального дизайна каркаса путем подбора органических и неорганических строительных блоков (ионов металлов и линкеров) [51, 52].
Отметим, справедливости ради, что большинство матриц MOF являются микропористыми [53], и большинство известных структур разрушается при удалении из пор гостевых молекул растворителя. Размер пор микропористых матриц ограничивает доступ объемных молекул адсорбатов к их внутренней поверхности (поверхности внутри пор). Приготовление материалов MOF с достаточно большими мезопорами расширяет область их практического применения [54]. Следовательно, актуальна разработка матриц мезопористых MOF (мезо-MOF) для улучшения транспорта в их пустотах (полостях и каналах) “гостевых” молекул адсорбатов (адсорбция и разделение), субстратов (катализ) или анализируемых соединений (в сенсорных устройствах).
В отношении структуры пор матрицы мезо-MOF могут иметь поры в виде каналов или в виде полостей [55]. Структура пор в виде одномерных каналов доступна, а во втором случае доступность полостей определяется обрамляющими их микропористыми “окнами”. Этот последний тип мезо-MOF наиболее распространен.
Существуют несколько стратегий приготовления мезопористых MOF с использованием линкеров относительно большого размера, мезоструктурирование или генерирование мезопор в процессе синтеза микропористых матриц MOF, включая приготовление каркасов с иерархической системой пор. С этой целью обычно используются объемные темплаты [56]. Эффективным подходом служит приготовление каркасов со смешанными линкерами, т.е. введение лигандов нескольких видов в одно и то же соединение. Первый подход формирования позволяет значительно увеличить размер полостей и раскрытие пор матриц MOF. Например, в случае микропористого каркаса MOF-74 использование органических линкеров длиной 5 нм привело к формированию чрезвычайно больших пор размером 9.8 нм [57].
Недостаток этого подхода – снижение стабильности кристаллической структуры MOF в процессе удаления “гостевых” молекул растворителя после завершения синтеза такого материала [58]. Вследствие этого второй путь, заключающийся в создании мезопор в матрицах микропористых MOF, включая формирование иерархической системы пор, является перспективной альтернативой. Реализация этого способа предусматривает использование объемных органических темплатов, как правило, ПАВ или триблок-сополимеров, например, pluronic P123 [59]. Например, цетилтриметиламмонийбромид (CTAB) был использован в качестве темплата для формирования мезо-MOF [60]. С применением этого темплата были синтезированы цеолитоподобные имидазолатные каркасы ZIF-95 с размером полостей 2.0–3.0 нм и ZIF-100 с размером полостей 3.56 нм.
В реакционной системе молекулы ПАВ образуют мицеллы, которые являются “мягкими” (soft) темплатами в процессе кристаллизации матриц MOF (рис. 1). Последующее удаление их после завершения синтеза приводит к формированию мезопор, размер которых может целенаправленно изменяться в диапазоне 3.8–31.0 нм.
Иерархически мезоструктурированные металл-органические каркасы L-MOF были синтезированы с использованием блок-сополимеров pluronic (P123 или F127) в качестве структуронаправляющих агентов (SDA). Основой для материалов L-MOF служил микропористый каркас MIL-53(Al). Было найдено, что эти матрицы могут содержать две системы мезопор с размерами около 4.0 нм и 5.4–7.6 нм [61].
Однако, малые молекулярные мицеллы зачастую нестабильны в условиях синтеза большинства материалов MOF, поэтому лишь ограниченное число металл-органических каркасов, как правило, с карбоксилатными линкерами могут быть получены таким способом. В этой связи для синтеза мезопористых материалов MOF применяется также стратегия использования двух темплатов различной природы одновременно. Например, таким способом был приготовлен каркас COK-15 с мезопорами размером 5 нм. В этом случае темплатами служили гетерополикислота (HPW) и ПАВ (СТАБ) [62].
В последние годы было разработано несколько новых методов приготовления мезопористых MOF: гелеобразование [63] и варьирование растворителя в процессе синтеза [64]. Эти методы достаточно эффективны, однако их недостаток – отсутствие контроля формы, положения и распределения мезопор в матрицах MOF. Это обстоятельство препятствует практическому применению мезопористых материалов, приготовленных указанными способами.
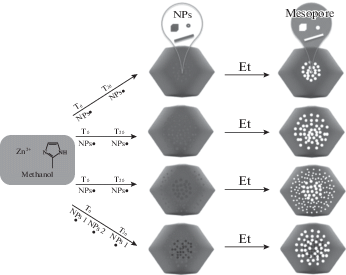
Одна из совершенно новых стратегий создания мезопор в матрицах MOF – инкапсулирование наночастиц металлов с последующим их “вытравливанием” (рис. 2). Этот способ обеспечивает надежный контроль морфологии, иерархической структуры и распределения в пространстве мезопор [65].
Анализ современной литературы указывает на то, что доступные и адаптируемые пути приготовления матриц MOF, имеющих мезопоры с контролируемым размером, формой и распределением в пространстве немногочисленны, несмотря на неуклонно возрастающую потребность в таких материалах.
В настоящее время значительное число исследований относится к введению специфических функций в металл-органические каркасы [66, 67]. Эффективная стратегия создания многоцелевых материалов MOF – введение в них новых органических строительных блоков с разнообразными функциями в процессе синтеза или после его завершения. Это позволяет достаточно точно регулировать физические и химические свойства указанных структур. Полифункциональные или так называемые мультивариантные матрицы MOF (MTV-MOF) с разнообразными функциональными группами в качестве многоцелевых гибридных материалов были разработаны для использования в разнообразных областях. Яги и сотр. разработали серию MTV-MOF, содержащих до восьми различных функций в одной кристаллической фазе [67] (рис. 3).
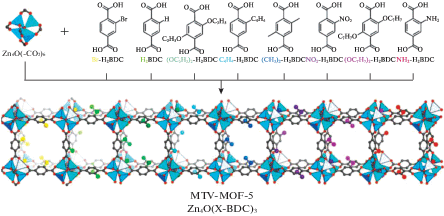
Рис. 3.
Пример синтеза серии мультивариантных материалов MTV-MOF-5 (Zn4O(X-BDC)3) путем конструирования каркаса с линкерами различной природы [67].
Коэн и сотр. применили стратегию пост-синтетического модифицирования предварительно синтезированных каркасов для получения матриц MOF с новыми улучшенными свойствами [68]. За счет использования органических линкеров специфической геометрии и с различными функциональными группами, Жанг (Zhang) и сотр. [69] модифицировали размер и химический состав пор матриц MOF с целью их многообразного применения.
Использование различных органических линкеров для построения одного каркаса MOF может быть достигнуто за счет использования смешанных линкеров или пост-синтетического обмена линкеров [70]. Стратегия замены и комбинации различных органических линкеров в одной структуре доказала свою эффективность для создания матриц мезо-MOF. По этой методологии была приготовлена серия мезопористых матриц MOF с ионами редкоземельных металлов [55].
Недавно был разработан также подход последовательного внедрения новых органических линкеров в предварительно синтезированные каркасы, что позволяет ввести в поры таких матриц MTV-MOF до трех функциональных групп одновременно [71].
Литературные данные по данной тематике указывают на то, что эта область создания и исследования полифункциональных материалов MOF начала развиваться относительно недавно, но весьма перспективна с точки зрения различных областей их применения.
ПЕРИОДИЧНОСТЬ СВОЙСТВ МЕТАЛЛ-ОРГАНИЧЕСКИХ КАРКАСНЫХ СТРУКТУР
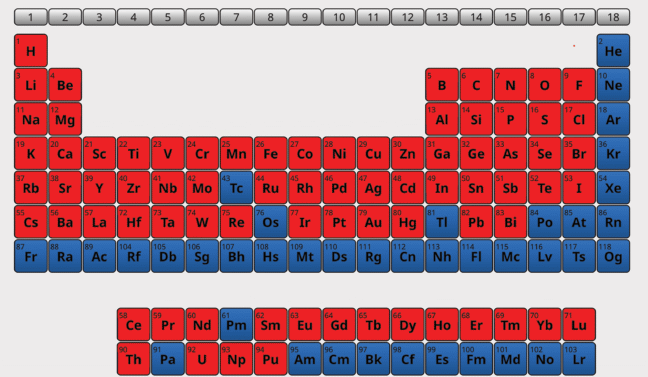
В результате вариативности состава и методологии синтеза MOF стало возможным синтезировать самые разнообразные структуры, и в настоящее время известны каркасы, содержащие 78 элементов из Периодической таблицы Д.И. Менделеева. Эти элементы помечены серым на рис. 4, на котором изображена Периодическая таблица элементов, входящих в состав MOF. Известна и широко используется база структур MOF (СoRE-MOF) [72–75]. Отметим, что наибольшее число структур (более 90% всех описанных материалов) получено с такими элементами как Al, Cr, Eu и другие редкоземельные элементы, Fe, Mg, Ti, Zn, Zr.
Рис. 4.
Элементы Периодической таблицы Д.И. Менделеева, с которыми синтезированы металл-органические каркасы (помечены красным).
Хотя до сих пор не проведено систематического анализа всего многообразия структур MOF, при сравнении групп материалов с одинаковой структурой, но с разными ионами металлов в их составе можно отметить отдельные примеры как периодичности изменения структурных параметров, так и влияния так называемого лантаноидного и актиноидного сжатия на структурные характеристики представителей MOF в полном соответствии с Периодическим законом Д.И. Менделеева и положением элементов в Периодической таблице элементов. Так, имидазоляты кадмия и ртути топологии dia-c [76], полученные из водных растворов ацетатов металлов, имидазола и аммиака, образуют кристаллы, имеющие элементарную ячейку группы Pbca, причем ее объем уменьшается от кадмия к ртути, что можно объяснить лантаноидным сжатием.
Элементарные ячейки имидазолятов железа и марганца топологии mog [77, 78], синтезированных из ферроцена или дикарбонилцикло-пентадиенила железа в случае железа, а также из декакарбонила димарганца в случае марганца, соответственно, имеют симметрию P2_1/c, и их объем уменьшается от марганца к железу, как и атомные радиусы этих элементов.
Можно сравнить структуры каркаса типа MIL-100, содержащие разные элементы – скандий [79], ванадий [80] и марганец [81]. Для этой кубической структуры MIL-100 (Fd-3m) можно показать зависимость размера ячейки от атомного радиуса. Ячейка MIL-100(Sc) имеет длину ребра 75.436 Å, MIL-100(V) – 73.0286 Å, MIL-100(Mn) – 73.2990 Å, в то время как ковалентные радиусы атомов варьируются следующим образом: 1.44, 1.25 и 1.39 Å для скандия, ванадия и марганца, соответственно. Удельные площади поверхности этих материалов подчиняются той же тенденции: наибольшую удельную поверхность имеет MIL-100(V) – 2320 м2 г–1, далее следует MIL-100(Mn) – 1610 м2 г–1, а наименьшая величина наблюдается для MIL-100(Sc) – варьируется от 1000 до 1400 м2 г–1. Это объяснено различной льюисовской кислотностью центров.
2,6-Нафталиндикарбоксилаты циркония и гафния, описанные в работе [82], синтезируют ультразвуковым способом, используя ДМФА в качестве растворителя смеси тетрахлорида металла, 2,6-нафталендикарбоновой и уксусной кислот. Полученные структуры имеют кубическую гранецентрированную ячейку (Fm-3m), причем параметр ячейки для обеих структур имеет одну и ту же величину, что можно объяснить лантаноидным сжатием оболочек гафния. Удельная площадь поверхности закономерно уменьшается от циркониевого MOF (1399 м2/г) к гафниевому (1097 м2/г) вследствие уменьшения льюисовской кислотности металлических центров.
Имеются также интересные данные для одной из наиболее хорошо изученных структур – UiO-66, которая содержала титан [83] (теоретическая работа), цирконий [84] и гафний [85]. На примере подобных терефталатных структур, образованных элементами IVB группы, можно продемонстрировать лантаноидное сжатие оболочек: если параметр кубической решетки F-43m для теоретически описанного UiO-66(Ti) составляет 20.3 Å, то для UiO-66(Zr) и UiO-66(Hf) он имеет одинаковое значение 20.70 Å. Объемный модуль упругости и минимальный модуль сдвига для этих трех веществ имеют близкие значения, но тем не менее можно проследить закономерность: первый уменьшается с увеличением порядкового номера, а второй – растет. Этот феномен объясняется анизотропией механических свойств кубического кристалла и небольшим отличием в конфигурации металлических центров этих веществ. Удельная площадь поверхности падает с увеличением порядкового номера элемента, образующего MOF.
1,3,5-Бензолтрикарбоксилаты (BTC) двухвалентных металлов с кубической структурой, включая производные хрома [86], молибдена [87], железа [88] и рутения [89] изоструктурны подробно изученному каркасу HKUST-1 (MOF-199) и имеют пространственную группу Fm-3m. Изменения параметров решетки демонстрируют периодическую зависимость, а также сходство d-элементов: ребро куба элементарной ячейки для Cr-BTC составляет 26.714 Å, для Fe-BTC – 26.633 Å, для Mo-BTC – 27.179 Å, а для Ru-BTC – 26.634 Å. Таким образом, внутри группы при заполнении d-уровня и роста заряда ядра ячейка сжимается, так же, как и при переходе к другому периоду, причем этот рост совсем небольшой, что показывает сходство элементов.
В случае каркаса CPO-27 с ростом порядкового номера от марганца к кобальту и никелю [90], и далее к железу [91] и меди [92] уменьшается объем элементарной ячейки вследствие уменьшения кристаллографического радиуса иона вместе с увеличением заряда ядра. Согласно правилу Ирвинга–Вильямса, стабильность при замене координационной воды другими лигандами, в том числе газами, например, водородом, увеличивается в том же ряду, что приводит к росту экспериментальных начальных изостерических энергий адсорбции. Удельная площадь поверхности, однако, снижается от марганца к меди.
Сравнение структурных параметров для серии каркасов MIL-96, содержащих элементы одной группы – алюминий [93], галлий [94] и [95], синтезированных из нитратов алюминия, галлия, индия и 1,3,5-бензолтрикарбоновой кислоты сольвотермальным способом также дает картину, полностью согласующуюся с законом периодического изменения свойств. Полученные кристаллы имели гексагональную сингонию и пространственную группу P6_3/mmc, при этом объем элементарной ячейки увеличивается с увеличением атомной массы (номера) образующего каркас металла, равно как и размер кристаллитов. Термический распад структур происходит в интервале от 300 до 580°С.
Аналогичные изменения наблюдаются и для другой структуры – MIL-68 – с теми же элементами: алюминием [96], галлием и индием [97]. Координационные полимеры были приготовлены сольвотермальным методом с использованием солей соответствующих металлов, терефталевой кислоты и DMF в качестве растворителя. Получены игольчатые кристаллиты длиной около 1.25 мкм для MIL-68(Al), 2–5 мкм для MIL-68(Ga) и 20–200 мкм для MIL-68(In) орторомбической сингонии и пространственной группы Cmcm. Объем элементарной ячейки увеличивается с ростом порядкового номера образующего MOF металла. Термостабильность структур приблизительно одинакова. Однако, удельная площадь поверхности с атомным номером не коррелирует: 1051 м2 г–1 для MIL-68(Al), 1117 м2 г–1 для MIL-68(Ga) и 746 м2 г–1 для MIL-68(In).
Еще один пример зависимости структурных параметров решетки и других свойств металл-органических каркасов для ряда катионов IIIа группы получен для производных каркаса типа MIL-122. Гидротермальным способом из нитратов соответствующих металлов получены изоструктурные 1,4,5,8-нафталинтетракарбоксилаты алюминия, галлия и индия типа MIL-122 моноклинной симметрии, пространственная группа P2_1/c [98]. Структура представляет собой бесконечные цепи октаэдрически координированных катионов, соединенных через тетракарбоксилатные лиганды. Объемы элементарных ячеек растут с увеличением атомного номера. При этом с увеличением атомного номера уменьшается размер кристаллитов: 2000–4000 нм для MIL-122(Al), 500–1000 нм для MIL-122(Ga) и 100–200 нм для MIL-122(In). Эти структуры похожи на ранее синтезированные орторомбические MIL-122(Mn) и MIL-122(Zn), но мостиковая молекула H2O заменена на µ2-гидроксогруппу. В то же время термостабильность каркаса от порядкового номера атома металла не зависит: наибольшая термостабильность наблюдается для MIL-122(Ga), наименьшая – для MIL-122(In).
Для серии металл-органических каркасов со щелочными металлами CD-MOF, содержащих калий, рубидий и цезий [99], полученных из растворов, содержащих ионы щелочных металлов, а также гамма-циклодекстрин, в виде высокопористых кристаллов кубической морфологии и пространственной группы I432, длина связи металла с кислородом увеличивается с ростом атомной массы (порядкового номера элемента), хотя объем элементарной ячейки практически не изменяется. Кубический цезий-содержащий CD-MOF-3 неустойчив к процессу активации, а CD-MOF-1, содержащий калий, имеет удельную площадь поверхности по БЭТ, равную 1220 м2 г–1, что несколько больше, чем для CD-MOF-2 с рубидием (1030 м2 г–1). В этом можно увидеть проявление периодических свойств элементов: энергия адсорбции для CD-MOF-1 выше, так как электронные оболочки калия менее диффузны.
1,3,5-Бензолтрикарбоксилаты калия и рубидия получены в работе [100] сольвотермальным способом из нитратов металлов и 1,3,5-бензолтрикарбоновой кислоты в среде ДМФА с добавкой фторида аммония. Эти каркасы кристаллизуются в моноклинной решетке с пространственной группой P2_1/c, причем объем элементарной ячейки увеличивается от калия (955.6 Å3) к рубидию (1007.8 Å3). ИК-спектры и термостабильность этих материалов идентичны.
Работ по металл-органическим каркасам радиоактивных элементов очень немного, однако, и в описанных структурах можно надежно определить тенденции изменения структурных параметров и других свойств каркаса с положением элемента (металла) в Периодической таблице Д.И. Менделеева. Так, дифосфонаты тория и урана [101] были синтезированы гидротермальным способом из тетранитрата тория или гексагидрата нитрата уранила и 1,4-бензол-бис-фосфониевой кислоты с добавкой HF. Полученные изотипические структуры Thbbp-2 и U4bbp имеют триклинную симметрию и кристаллизуются в пространственной группе P-1, однако торий имеет ограниченное восьмигранное окружение из семи атомов кислорода, а уран – ограниченное тригонально-призматическое. Ячейка U4bbp меньше, чем Thbbp-2, что можно объяснить меньшим кристаллическим радиусом атома урана (актиноидное сжатие). В то же время ИК-спектры этих веществ аналогичны.
Огромное число структур MOF синтезировано с использованием лантаноидов. Так, представительная серия лантанид-содержащих MOF семейства UCY [102] cинтезирована из 5-(4-карбоксибензилиденамино)-изофталевой кислоты и нитратов La, Ce, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, получены моноклинные структуры с пространственной симметрией C2/c, металлические центры представлены двухъядерными металлсодержащими структурами. Объем элементарной ячейки уменьшается с первым заполнением f‑уровня, затем, от европия к гольмию, растет. Магнитная восприимчивость увеличивается от гадолиний-содержащего UCY к гольмий-содержащему, достигая 24.09 см3 моль–1 K–1, что связано с уменьшением плотностей состояний в магнитно-изолированной двухъядерной структуре с ростом атомного номера. Отметим, что термостабильность всех полученных MOF одинакова.
В [103] рассматривается тенденция к уменьшению объема тригональной элементарной ячейки структуры MIL-103 (симметрия R32), образованной лантанидами с лантана по гольмий и 1,3,5-бензол-трис-бензойной кислоты (H3BTB), с ростом атомного номера, при этом получается прямолинейная зависимость объема ячейки от атомного номера с коэффициентом корреляции R = = 0.991. Термостабильность этих MOF практически не изменяется при замене иона лантаноида в ячейке, за исключением MIL-103(Ce), разложение которого начинается уже при 320°С (около 400°С для остальных каркасов). Измерения адсорбции дейтерированного ацетонитрила на MIL-103(La), MIL-103(Eu) и MIL-103(Dy) методом ИК-спектроскопии в области колебания связи Ln–N полученных систем показали, что льюисовская кислотность металлических центров увеличивается с уменьшением ионного радиуса, как и предсказывает теория. Удельные площади поверхности всех исследованных MOF составляли примерно одинаковую величину – около 700 м2 г–1.
Бис-фенилдикарбоксилаты тербия, гольмия и эрбия [104] синтезированы из трехзарядных ионов тербия, гольмия и эрбия c 4,4'-бифенилдикарбоновой кислотой сольвотермальным способом. Они кристаллизуются в моноклинной ячейке симметрии C2/c, содержащей металл-кислородные строительные блоки пропеллерной (paddle-wheel) формы и ромбические каналы. Лантаноидное сжатие приводит к уменьшению объема ячейки Ho2bpdc3 по сравнению с Tb2bpdc3, однако, ячейка Er2bpdc3 чуть больше, чем ячейка Ho2bpdc3. Люминесцентные свойства для всех трех MOF практически идентичны: полосы переходов отличаются только интенсивностью.
Изоморфные карбоксифосфонаты лантанидов Ce, Pr, Nd, Sm, Eu, Gd, Tb, а также Y были синтезированы гидротермальным способом из (4-карбоксипиперидил)-N-метиленфосфониевой кислоты и хлорида соответствующего металла с добавлением NaOH для создания необходимого значения pH [105]. Материалы кристаллизуются в моноклинной ячейке пространственной группы P2_1/c, причем в ряду Pr–Nd–Sm–Eu, по мере заполнения f-оболочки происходит уменьшение объема ячейки. При переходе от Eu к Gd ячейка увеличивается, что можно объяснить появлением d-электрона. ИК-спектры веществ схожи, так же как и термическая устойчивость.
Рассмотренные примеры периодичности свойств и зависимости параметров структуры металл-органического каркаса от размера иона металла и его положения в Периодической таблице Д.И. Менделеева, безусловно, не дают полной картины, и полный анализ данных потребует гораздо больших усилий и объема изложения. В то же время, несмотря на изобилие полученных структур (69666 структур, включенных в базу CoreMOF), адекватный анализ затрудняется по меньшей мере тремя обстоятельствами:
1. Однотипные структуры (изоструктурные металл-органические каркасы), содержащие металлы одного периода или одной группы, чаще всего получены разными исследователями и разными методами, иногда с использованием разных растворителей, молекулы которых остаются в порах каркаса, и структурные параметры не всегда можно сравнить.
2. Известно такое свойство металл-органических каркасов как “дыхание” (“breathing”), выражающееся в изменении параметров решетки, объема и диаметра пор и даже иногда пространственной группы при заполнении или удалении гостевых молекул, в качестве которых выступают молекулы растворителя или адсорбированных газов. Степень удаления этих гостевых молекул может отличаться от образца к образцу.
3. Наконец, не всегда возможно по разным причинам синтезировать изоструктурные металл-органические каркасы, содержащие разные металлы даже одного периода или одной группы, не говоря о металлах с принципиально разными свойствами. В таком случае просто недостаточно данных для анализа и адекватного сравнения, поскольку ряды получаются неполными.
Авторы благодарят Российский фонд фундаментальных исследований за финансовую поддержку (код проекта № 19-03-00930).
Список литературы
Eddaoudi M. // Sci. 2002. V. 295. P. 469.
Férey G. // Chem. Soc. Rev. 2008. V. 37. P. 191.
Long J.R., Yaghi O.M. // Chem. Soc. Rev. 2009. V. 38. P. 1213.
http://europe.iza-structure.org/IZA-SC/ftc_table.php
Hoskins B.F., Robson R. // J. Am. Chem. Soc. 1989. V. 111. P. 5962.
Yaghi O.M., Li G., Li H. // Nature. 1995. V. 378. P. 703.
Petit C. // Current Opinion Chem. Eng. 2018. V. 20. P. 132.
García-García P., Müller M., Corma A. // Chem. Sci. 2014. V. 5. P. 2979.
Huang Y.-B., Liang J., Wang X.-S., Cao R. // Chem. Soc. Rev. 2017. V. 46. P. 126.
Mendes P.A.P., Rodrigues A.E., Horcajada P. et al. // Micropor. Mesopor. Mater. 2014. V. 194. P. 146.
Yi F.-Y., Chen D., Wu M.-K. et al. // ChemPlusChem. 2016. V. 81. P. 675.
Li J.-R., Kuppler R.J., Zhou H.-C. // Chem. Soc. Rev. 2009. V. 38. P. 1477.
Zhao X. // Sci. 2004. V. 306. P. 1012.
Latroche M., Surblé S., Serre C. et al. // Angew. Chem. Int. Ed. 2006. V. 45. P. 8227.
Han S., Wei Y., Valente C. et al. // J. Am. Chem. Soc. 2010. V. 132. P. 16358.
Nijem N., Wu H., Canepa P. et al. // Ibid. 2012. V. 134. P. 15201.
Valvekens P., Vermoortele F., De Vos D. // Catal. Sci. Technol. 2013. V. 3. P. 1435.
García-García P., Müller M., Corma A. // Chem. Sci. 2014. V. 5. P. 2979.
Liu J., Chen L., Cui H. et al. // Chem. Soc. Rev. 2014. V. 43. P. 6011.
Gascon J., Corma A., Kapteijn F. et al. // ACS Catal. 2014. V. 4. P. 361.
Sumida K., Rogow D.L., Mason J.A. et al. // Chem. Rev. 2012. V. 112. P. 724.
Dietzel P.D.C., Besikiotis V., Blom R. // J. Mater. Chem. 2009. V. 9. P. 7362.
Исаева В.И., Кустов Л.М., Белецкая И.П. // Журн. орган. химии. 2014. V. 50. P. 1567.
Mendes P.A.P., Rodrigues A.E., Horcajada P. et al. // Micropor. Mesopor. Mater. 2014. V. 194. P. 146.
Nuzhdin A.L., Kovalenko K.A., Dybtsev D.N., Bukhtiyarova G.A. // Mendeleev Commun. 2010. V. 20. P. 57.
Maes M., Schouteden S., Alaerts L. et al. // Phys. Chem. Chem. Phys. 2011. V. 13. P. 5587.
Horcajada P., Serre C., Vallet-Regí M. et al. // Angew. Chem. Int. Ed. 2006. V. 45. P. 5974.
Kreno L.E., Leong K., Farha O.K. et al. // Chem. Rev. 2012. V. 112. P. 1105.
Xu W., Thapa K.B., Ju Q. et al. // Coord. Chem. Rev. 2018. V. 37. P. 199.
Lee Y.-R., Kim J., Ahn W.-S. // Korean J. Chem. Eng. 2013. V. 30. P. 1667.
Stock N., Biswas S. // Chem. Rev. 2012. V. 112. P. 933.
Tanaka D., Henke A., Albrecht K. et al. // Nat. Chem. 2010. V. 2. P. 410.
Choi K.M., Jeong H.M., Park J.H. et al. // ACS Nano. 2014. V. 8. P. 7451.
Shah M., McCarthy M.C., Sachdeva S. et al. // Ind. Eng. Chem. Res. 2012. V. 51. P. 2179.
Huang L. // Micropor. Mesopor. Mater. 2003. V. 58. P. 105.
Yilmaz B., Trukhan N., Müller U. // Chin. J. Catal. 2012. V. 33. P. 3.
Kim J., Kim S.-H., Yang S.-T., Ahn W.-S. // Micropor. Mesopor. Mater. 2012. V. 161. P. 48.
Cho H.-Y., Kim J., Kim S.-N., Ahn W.-S. // Ibid. 2013. V. 169. P. 180.
Tranchemontagne D.J., Hunt J.R., Yaghi O.M. // Tetrahedron. 2008. V. 64. P. 8553.
Klinowski J., Paz F.A.A.P. Silva, Rocha J. // Dalton Trans. 2011. V. 40. P. 321.
Schlesinger M., Schulze S., Hietschold M., Mehring M. // Micropor. Mesopor. Mater. 2010. V. 132. P. 121.
Qiu L.-G., Li Z.-Q., Wu Y. et al. // Chem. Commun. 2008. P. 3642.
Yang H., Orefuwa S., Goudy A. // Micropor. Mesopor. Mater. 2011. V. 143. P. 37.
Pilloni M., Padella F., Ennas G. et al. // Ibid. 2015. V. 213. P. 14.
Tella A.C., Owalude S.O. // J. Mater Sci. 2014. V. 49. P. 5635.
Haque E., Khan N.A., Park J.H., Jhung S.H. // Chem. Eur. J. 2010. V. 16. P. 1046.
Liu J., Tian J., Thallapally P.K., McGrail B.P. // J. Phys. Chem. C. 2012. V. 116. P. 9575.
Caskey S.R., Wong-Foy A.G., Matzger A.J. // J. Am. Chem. Soc. 2008. V. 130. P. 10870.
Dietzel P.D.C., Panella B., Hirscher M. et al. // Chem. Commun. 2006. P. 959.
Rowsell J.L.C., Yaghi O.M. // Micropor. Mesopor. Mater. 2004. V. 73. P. 3.
Yaghi O.M., O’Keeffe M., Ockwig N.W. et al. // Nature. 2003. V. 423. P. 705.
Férey G., Mellot-Draznieks C., Serre C., Millange F. // Acc. Chem. Res. 2005. V. 38. P. 217.
Yi F.-Y., Chen D., Wu M.-K. et al. // ChemPlusChem. 2016. V. 81. P. 675.
Xuan W., Zhu C., Liu Y., Cui Y. // Chem. Soc. Rev. 2012. V. 41. P. 1677.
Fang Q.-R., Makal T.A., Young M.D., Zhou H.-C. // Comm. Inorg. Chem. 2010. V. 31. P. 165.
Guan H.-Y., LeBlanc R.J., Xie S.-Y., Yue Y. // Coord. Chem. Rev. 2018. V. 369. P. 76.
Cho H.S., Deng H., Miyasaka K. et al. // Nature. 2015. V. 527. P. 503.
Cai G., Jiang H.-L. // Angew. Chem. Int. Ed. 2017. V. 56. P. 563.
Xu W., Thapa K.B., Ju Q. et al. // Coord. Chem. Rev. 2018. V. 373. P. 199.
Qiu L.-G., Xu T., Li Z.-Q. et al. // Angew. Chem. Int. Ed. 2008. V. 47. P. 9487.
Do X.-D., Hoang V.-T., Kaliaguine S. // Micropor. Mesopor. Mater. 2011. V. 141. P. 135.
Wee L.H., Wiktor C., Turner S. et al. // J. Am. Chem. Soc. 2012. V. 134. P. 10911.
Li L., Xiang S., Cao S. et al. // Nat. Commun. 2013. P. 4.
Yue Y., Qiao Z.-A., Fulvio P.F. et al. // J. Am. Chem. Soc. 2013. V. 135. P. 9572.
Zhang W., Liu Y., Lu G. et al. // Adv. Mater. 2015. V. 27. P. 2923.
Corma A., García H., Llabrés i Xamena F.X. // Chem. Rev. 2010. V. 110. P. 4606.
Diercks C.S., Kalmutzki M.J., Diercks N.J., Yaghi O.M. // ACS Cent. Sci. 2018. V. 4. P. 1457.
Cohen S.M. // Chem. Rev. 2012. V. 112. P. 970.
Zhang W., Liu Y., Lu G. et al. // Adv. Mater. 2015. V. 27. P. 2923.
Juan-Alcañiz J., Ferrando-Soria J., Luz I. et al. // J. Catal. 2013. V. 307. P. 295.
Chen C.-X., Wei Z.-W., Jiang J.-J. et al. // J. Am. Chem. Soc. 2017. V. 139. P. 6034.
Moghadam P.Z., Li A., Wiggin S.B. et al. // Chem. Mater. 2017. V. 29. P. 2618.
Chung Y.G., Camp J., Haranczyk M. et al. // Ibid. 2014. V. 26. P. 6185.
https://gregchung.github.io/CoRE-MOFs.
Chung Y.G., Camp J., Haranczyk M. et al. // Chem. Mater. 2014. V. 26. P. 6185.
Masciocchi N., Ardizzoia G.A., Brenna S. et al. // Chem. Commun. 2003. P. 2018.
Lehnert R., Seel F. // Z. Anorg. Allg. Chem. 1978. V. 444. P. 91.
Lehnert R., Seel F. // Ibid. 1980. V. 464. P. 187.
Mowat J.P.S., Miller S.R., Slawin A.M.Z. et al. // Micropor. Mesopor. Mater. 2011. V. 142. P. 322.
Lieb A., Leclerc H., Devic T. et al. // Ibid. 2012. V. 157. P. 18.
Reinsch H., Stock N. // CrystEngComm. 2013. V. 15. P. 544.
Bon V., Senkovska I., Weiss M.S., Kaskel S. // Ibid. 2013. V. 15. P. 9572.
Wu H., Yildirim T., Zhou W. // J. Phys. Chem. Lett. 2013. V. 4. P. 925.
Cavka J.H., Jakobsen S., Olsbye U. et al. // J. Am. Chem. Soc. 2008. V. 130. P. 13850.
Jakobsen S., Gianolio D., Wragg D. et al. // Phys. Rev. B. 2012. V. 86. P. 125429.
Leszczyński M.K., Kornowicz A., Prochowicz D. et al. // Inorg. Chem. 2018. V. 57. P. 4803.
Kramer M., Schwarz U., Kaskel S. // J. Mater. Chem. 2006. V. 16. P. 2245.
Xie L., Liu S., Gao C. et al. // Inorg. Chem. 2007. V. 46. P. 7782.
Kozachuk O., Yusenko K., Noei H. et al. // Chem. Commun. 2011. V. 47. P. 8509.
Zhou W., Wu H., Yildirim T. // J. Am. Chem. Soc. 2008. V. 130. P. 15268.
Bloch E.D., Murray L.J., Queen W.L. et al. // Ibid. 2011. V. 133. P. 14814.
Sanz R., Martínez F., Orcajo G. et al. // Dalton Trans. 2013. V. 42. P. 2392.
Loiseau T., Lecroq L., Volkringer C. et al. // J. Am. Chem. Soc. 2006. V. 128. P. 10223.
Volkringer C., Loiseau T., Férey G. et al. // Micropor. Mesopor. Mater. 2007. V. 105. P. 111.
Volkringer C., Loiseau T. // Mater. Res. Bull. 2006. V. 41. P. 948.
Perea-Cachero A., Sánchez-Laínez J., Zornoza B. et al. // Dalton Trans. 2019. V. 48. P. 3392.
Volkringer C., Meddouri M., Loiseau T. et al. // Inorg. Chem. 2008. V. 47. P. 11892.
Volkringer C., Loiseau T., Guillou N. et al. // Solid State Sci. 2009. V. 11. P. 1507.
Forgan R.S., Smaldone R.A., Gassensmith J.J. et al. // J. Am. Chem. Soc. 2012. V. 134. P. 406.
Kim M.K., Jo V., Lee D.W. et al. // CrystEngComm 2010. V. 12. P. 1481.
Adelani P.O., Albrecht-Schmitt T.E. // J. Solid State Chem. 2012. V. 192. P. 377.
Efthymiou C.G., Kyprianidou E.J., Milios C.J. et al. // J. Mater. Chem. A. 2013. V. 1. P. 5061.
Chen M.-S., Chen M., Okamura T. et al. // Micropor. Mesopor. Mater. 2011. V. 139. P. 25.
Guo X., Zhu G., Fang Q. et al. // Inorg. Chem. 2005. V. 44. P. 3850.
Zhang N., Sun Z., Zhu Y. et al. // New J. Chem. 2010. V. 34. P. 2429.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии