Журнал физической химии, 2019, T. 93, № 4, стр. 632-640
Термодинамический подход к обоснованию работы и потенциала разделения многокомпонентной смеси
В. П. Чижков a, В. Н. Бойцов a, *
a Российская академия наук, Институт органической химии им. Н.Д. Зелинского
Москва, Россия
* E-mail: boysoft@list.ru
Поступила в редакцию 09.07.2018
Аннотация
Предложены и обобщены уравнения для расчета термодинамической работы разделения.
Основные положения общей теории разделения рассматриваются в [1–3] на примерах переработки бинарных смесей (например, смеси изотопов урана). На практике, однако, встречаются преимущественно с задачами разделения смесей, состоящих из более чем двух компонентов. В связи с этим большой интерес вызывает развитие обобщенной теории разделения компонентов бинарных и многокомпонентных смесей [4, 5]. Статья [5] носит дискуссионный характер, содержит перечень и критическую оценку работ, направленных на поиск и обоснование универсального разделительного потенциала для многокомпонентных смесей, который стал бы полным аналогом функции ценности (потенциала разделения) Дирака–Пайерлса [1, 4]. Объектом исследования выбран “обобщенный” разделительный потенциал [5]. Обобщенный потенциал рассматривался ранее как перспективный в работах различных авторов [6–9]. Не без основания отмечается [5], что данный потенциал, как и другие упомянутые и описанные в [5] варианты разделительных потенциалов для многокомпонентных смесей, не может выступать в качестве полноценного аналога функции ценности. Открытым остается также вопрос о взаимосвязи предложенного в [5] разделительного потенциала с энтропийным потенциалом разделения многокомпонентной смеси [5–7]. Предположено [5], что на него возможно удастся ответить, применив, например, подход, недавно описанный в [10]. Авторами [5] сделано несколько замечаний по ранее опубликованным работам [11, 12]. В связи с этим считаем необходимым высказать свое мнение, сложившееся на данный момент времени, по существу сделанных замечаний и разъяснить до некоторой степени предлагаемый нами термодинамический подход.
При оценке [1, 6] термодинамического совершенства и энергоэффективности процессов разделения важное значение приобретает определение термодинамической работы разделения и соответствующего разделительного потенциала. Цель наших исследований – наиболее полное термодинамическое обоснование работы разделения компонентов смеси идеальных газов, а также распространение общей теории разделения на распределительные системы фракционирования (жидкостную экстракцию и хроматографию). Отметим, что экстракция и хроматография нашли реальное применение для разделения изотопов урана [13]. В современной органической химии актуальной остается задача разделения пар оптических изомеров на отдельные практически чистые компоненты [14].
ТЕРМОДИНАМИЧЕСКАЯ РАБОТА РАЗДЕЛЕНИЯ СТУПЕНИ КАСКАДА
К фундаментальным понятиям общей теории разделения относится понятие разделительной способности (ценности смеси) [1, 4, 15]. Это понятие имеет большое значение в изотопной технологии [4, 13], так как его использование позволяет оценить удельные затраты на производство продукта [4, 15] и дать сравнительную оценку эффективности процесса разделения [4, 8]. Данное понятие оказалось также практически важным для проведения некоторых расчетов экономического характера [5, 13]. В качестве показателя разделительной способности ступени (элемента) газоразделительного каскада используют функцию
где q, q' и q'' – количества молей исходной бинарной смеси и полученных фракций, x0, x' и x'' – соответствующие концентрации, Φ(x) – функция, которую называют разделительным потенциалом [1, 6, 7]:Физический смысл W изучен недостаточно [7]. Предпринимались ранее [4, 6, 7] попытки объяснения W и Φ(x) с привлечением энтропии и выражений для термодинамических потенциалов по Гиббсу. В [6, 7] функцию W называют полезной работой разделения. Для случая разделения компонентов бинарной смеси и при выделении двух фракций, в соответствии с данными [6, 7], можно написать (j = n = 2):
(2)
$W = \sum\limits_{j = 1}^n {{{q}^{j}}} \sum\limits_{i = 1}^n {x_{i}^{j}} \ln \frac{{x_{i}^{j}}}{{1 - x_{i}^{j}}} - q\sum\limits_{i = 1}^n {x_{i}^{0}} \ln \frac{{x_{i}^{0}}}{{1 - x_{i}^{0}}},$Уравнение для W можно представить также в виде [16]:
Последнее уравнение для W удобно применять при исследовании ступеней многоступенчатой фракционной экстракции [17].
Однократный акт разделения характеризуют обычно коэффициентом разделения α, эффективным коэффициентом разделения β [2] и степенью деления фракций Θ:
(3)
$\begin{gathered} {{B}_{1}}{\text{/}}{{B}_{0}} = (\alpha --\beta ){\text{/}}(\alpha --1) = {{q}_{{\text{B}}}}, \\ {{B}_{2}}{\text{/}}{{B}_{0}} = (\beta --1){\text{/}}(\alpha --1) = {{p}_{{\text{B}}}}, \\ {{A}_{1}}{\text{/}}{{A}_{0}} = (\alpha --\beta ){\text{/}}[\beta (\alpha --1)] = {{q}_{{\text{A}}}}, \\ {{A}_{2}}{\text{/}}{{A}_{0}} = \alpha (\beta --1){\text{/}}[\beta (\alpha --1)] = {{p}_{{\text{A}}}}. \\ \end{gathered} $Используя приведенные уравнения, найдем
Подобные соотношения были получены Дираком, Пайерлсом и Фуксом в ходе выполнения Манхеттенского проекта [15]. Для значений α, близких к единице и заметно отличающихся от единицы [1], установлена [19] связь:
Известна формула Пайерлса и Фукса [4, 15], связывающая Wуд = W/q с изменением молярной величины – энтропии смешения ∆S. По данным [4, 15, 16], для тонкого разделения компонентов смеси идеальных газов можно написать
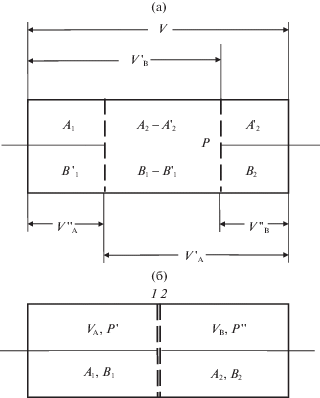
где R – газовая постоянная. Идеальный газ, как известно, теоретическая модель газа, в которой “взаимодействием” частиц газа пренебрегают. Идеальный газ может быть однокомпонентным и многокомпонентным и подчиняется уравнению состояния идеального газа. В смеси идеальных газов поведение каждого из них не зависит от присутствия остальных [12].Гипотетические полупроницаемые мембраны и идеализированные поршни как теоретические модели достаточно широко применяются в термодинамике равновесных процессов [20–22]. В [16] описано разделительное устройство, обеспечивающее неполное равновесное (квазистатическое) разделение компонентов смеси идеальных газов. Это устройство изображено на рис. 1 (положения “а” и “б”). В данном устройстве давление (P) исходной смеси идеальных газов и выделенных фракций (P', P'') в общем случае [16] различаются (P' ≠ P'' ≠ P). Связь между W и термодинамической работой WТ, совершаемой в предложенном устройстве при симметричном разделении (β = α1/2 = γ), по данным [16], можно представить в следующей форме:
Рис. 1.
Устройство для равновесного разделения (смешения) газов с полупроницаемыми поршнями (A0 ≠ B0, β = α1/2). Обозначения см. в [16].
В [16] обоснована связь
Учитывая приведенные выше данные, перейдем к термодинамическому обоснованию работы разделения многокомпонентной смеси. В качестве примера рассмотрим процесс симметричного разделения смеси идеальных газов, содержащей две пары газов AB и CD. На рис. 2 изображено гипотетическое устройство, которое позволяет, по крайней мере, в принципе осуществить равновесное разделение указанных пар. Данное устройство [11] является модификацией системы, изображенной на рис. 1, и представляет собой цилиндрический сосуд объемом V, заполненный смесью идеальных газов A, B, C и D в количествах A0, B0, C0 и D0 молей при общем давлении P. В общем случае A0 ≠ B0 ≠ C0 ≠ D0 (рис. 2). В сосуде установим четыре полупроницаемые перегородки (рис. 2а), каждая из которых имеет форму поршня [20, 22], способного перемещаться бесконечно медленно [22] и без трения. Учитывая [21–23], будем считать, что перегородка 1 проницаема для В, а перегородка 2 – для А. Существенно (и это следует особо подчеркнуть), что обе перегородки 1 и 2 свободно пропускают газы C и D. Одновременно считаем, что перегородка 3 проницаема для D, а перегородка 4 – для С, и обе перегородки 3 и 4 проницаемы для А и В, т.е. свободно пропускают эти газы. Тогда, передвигая перегородки, можно получить при симметричном разделении каждой из пар (${{\beta }_{{{\text{AB}}}}} = \alpha _{{{\text{AB}}}}^{{1/2}} = {{\gamma }_{{{\text{AB}}}}}$, ${{\beta }_{{{\text{CD}}}}} = \alpha _{{{\text{CD}}}}^{{1/2}} = {{\gamma }_{{{\text{CD}}}}}$) картину, показанную на рис. 2б. В конечном положении (как и на рис. 1) перегородки симметрично располагаются относительно центра цилиндра (VA= VB= V/2). Выбор пар и соответствующих перегородок осуществляется по принципу, описанному, например, в [25, 26].
Рис. 2.
Устройство для равновесного разделения (смешения) газов (A0 ≠ B0 ≠ C0 ≠ D0, ${{\beta }_{{{\text{mk}}}}} = \alpha _{{{\text{mk}}}}^{{1/2}}$). Обозначения см. в [11].
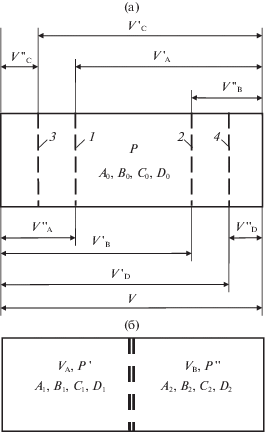
В соответствии с рис. 2, принимаем αСD > αAB. При одновременном выполнении равенств ${{\beta }_{{{\text{AB}}}}} = \alpha _{{{\text{AB}}}}^{{1/2}}$ и ${{\beta }_{{{\text{CD}}}}} = \alpha _{{{\text{CD}}}}^{{1/2}}$ (рис. 2) справедливы соотношения
С учетом принятых обозначений, приведенных рисунков и данных, можно, на наш взгляд, сразу написать (для устройства на рис. 2)
Из данных [11] следует, что в изученном устройстве (рис. 2) давление (P) исходной многокомпонентной смеси идеальных газов и выделенных фракций (P', P'') в общем случае различаются. При A0 = B0 и C0 = D0 имеем ΘAB = ΘCD = 0.5 и P' = P'' = P. В этих условиях вновь выполняются равенства
Эти равенства подтверждают адекватность предложенной модели (рис. 2). Здесь ∆Sсм относится к рассматриваемой многокомпонентной смеси идеальных газов (A0 = B0 и C0 = D0 [10, 11]).В заключение раздела сумму W = WAB + WCD целесообразно представить в следующей обобщенной форме [26]:
ТЕРМОДИНАМИЧЕСКАЯ РАБОТА РАЗДЕЛИТЕЛЬНОГО КАСКАДА
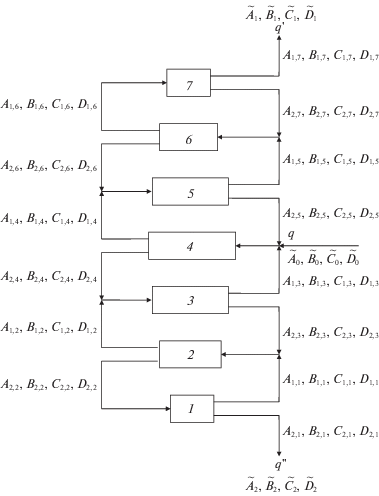
Упрощенная схема каскада изображена на рис. 3. Она включает в себя семь описанных выше ступеней равновесного разделения. Ограничимся случаем разделения эквимолярных смесей идеальных газов. С учетом содержания предыдущего раздела считаем, что каждая ступень каскада работает в режиме симметричного разделения.
Для варианта разделения в каскаде компонентов смеси А(1) и В(2) и при выделении двух фракций можно, в соответствии с данными [6, 7], написать (j = n = 2)
Уравнение для WK можно представить также в виде:
Для расчета термодинамической работы разделения многокомпонентной смеси идеальных газов (A, B, C и D) воспользуемся рассмотренным в предыдущем разделе условием, согласно которому, симметричное разделение на ступенях каскада возможно более чем для одной пары компонентов разделяемой многокомпонентной смеси. Процесс разделения в каскаде охарактеризуем величинами (см. рис. 3):
В узлах каскада (рис. 3) осуществляется несмешивание по нескольким относительным концентрациям для выбранных пар компонентов смеси (т.е. по RAB и RCD [5]). Например, в узле перед ступенью 6 выполняются равенства
В заключение выражаем искреннюю благодарность авторам [5] за интерес, проявленный к нашим работам [10–12]. Приведенные в статье [5] данные и уравнения будут учитываться в наших дальнейших исследованиях.
Список литературы
Розен А.М. Теория разделения изотопов в колоннах. М.: Атомиздат, 1960. 440 с.
Бенедикт М., Пигфорд Т. Химическая технология ядерных материалов. М.: Атомиздат, 1960. 560 с.
Хванг С.-Т., Каммермейер К. Мембранные процессы разделения, М.: Химия, 1981, 463 с.
Изотопы: свойства, получение, применение / Под ред. В.Ю. Баранова. М.: ИздАТ, 2000. 703 с.
Смирнов А.Ю., Сулаберидзе Г.А. // Журн. физ. химии. 2019. Т. 93. № 4. С. 627.
Кузнецов П.Г., Соколов В.А., Седин И.П. // Разделение и анализ углеводородных газов. М.: Изд-во АН СССР, 1963. С. 114.
Нисельсон Л.А., Вигдорович В.Н. // Матер. всесоюзн. совещ. по методам получения особо чистых веществ. М.: НИИТЭХИМ, 1967. С. 48.
Попов В.В., Герасимов А.Д., Филиппов В.П., Первушина В.К. // Методы получения и анализа веществ особой чистоты. М.: Наука, 1970. С. 21.
Чижков В.П., Стерхов Н.В., Забокрицкий М.П. // Журн. физ. химии. 1991. Т. 65. № 7. С. 1729.
Чижков В.П., Бойцов В.Н. // Там же. 2016. Т. 90. № 1. С. 147.
Чижков В.П., Бойцов В.Н. // Там же. 2013. Т. 87. № 3. С. 512.
Чижков В.П., Бойцов В.Н. // Там же. 2015. Т. 89. № 2. С. 316
Ран Ф., Адамантиадес А., Кентон Дж., Браун Ч. Справочник по ядерной энерготехнологии. М.: Энергоатомиздат, 1989. 752 с.
Алленмарк С. Хроматографическое разделение энантиомеров. М.: Мир, 1991. 268 с.
Сулаберидзе Г.А., Борисевич В.Д. // Журн. физ. химии. 2008. Т. 82. № 7. С. 1392.
Чижков В.П., Бойцов В.Н., Демин А.В. // Там же. 2010. Т. 84. № 3. С. 585.
Трейбал Р. Жидкостная экстракция. М.: Химия, 1966, 722 с.
Руководство по газовой хроматографии / Под ред. Э. Лейбница, Х.Г. Штруппе. М.: Мир, 1988. 479 с.
Чижков В.П., Бойцов В.Н. // Журн. физ. химии. 2015. Т. 89. № 4. С. 700.
Еремин Е.И. Основы химической термодинамики. М.: Высшая школа, 1974. 340 с.
Хейвуд Р. Термодинамика равновесных процессов. М.: Мир., 1983. 401 с.
Базаров И.П. Термодинамика. М.: Высшая школа, 1983. 344 с.
Чижков В.П., Бойцов В.Н. // Журн. физ. химии. 2004. Т. 78. № 7. С. 1301.
Чижков В.П., Бойцов В.Н. // Там же. 2008. Т. 82. № 7. С. 1397.
Чижков В.П., Бойцов В.Н. // Там же. 2017. Т. 91. № 6. С. 1066.
Чижков В.П., Бойцов В.Н. // Там же. 2018. Т. 92. № 1. С. 169.
Чижков В.П., Стерхов Н.В. // Там же. 2004. Т. 78. № 10. С. 1874.
Чижков В.П., Бойцов В.Н., Демин А.В. // Там же. 2011. Т. 85. № 3. С. 565.
Чижков В.П., Бойцов В.Н. // Там же. 2017. Т. 91. № 3. С. 549.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии