Журнал физической химии, 2019, T. 93, № 7, стр. 1038-1042
Процессы гидратации и состояние кислородо-водородных групп во фторзамещенных перовскитах на основе Ba4In2Zr2O11
Н. А. Тарасова a, *, А. О. Галишева a, И. Е. Анимица a
a Уральский федеральный университет им. Первого президента России Б.Н. Ельцина
620002 Екатеринбург, Россия
* E-mail: Natalia.Tarasova@urfu.ru
Поступила в редакцию 03.09.2018
После доработки 14.12.2018
Принята к публикации 17.12.2018
Аннотация
Проведен синтез фторзамещенных перовскитов на основе Ba4In2Zr2O11. Доказана способность исследуемых фаз к гидратации. Установлено, что введение фторид-ионов приводит к уменьшению степени гидратации относительно матричного состава. Показано, что допирование не приводит к изменению типа протонсодержащих частиц и, независимо от степени разупорядочения кислородной подрешетки, во фторзамещенных кислороддефицитных перовскитоподобных фазах на основе Ba4In2Zr2O11, Ba2In2O5 и Ba4Ca2Nb2O11 единственной формой кислородно-водородных групп являются энергетически неэквивалентные гидроксо-группы.
Интерес к разработкам твердооксидных топливных элементов ТОТЭ не ослабевает уже в течение длительного времени [1]. Это обусловлено как их высоким КПД, так и возможностью использования различных видов топлива. Кроме того, отсутствие необходимости применения дорогостоящих катализаторов, таких как платина, способствует значительному удешевлению таких устройств. Однако такие недостатки ТОТЭ, как высокие рабочие температуры и разбавление топлива продуктами сгорания, например, вследствие выделения воды в анодной секции, приводят к поиску альтернативных решений.
Так, применение протонпроводящего сложного оксида в качестве материала электролита ТОТЭ имеет ряд неоспоримых достоинств [2–10]: снижение рабочих температур с 900–1000°С до 500–700°С, увеличение КПД за счет 100% использования топлива вследствие выделения воды в катодной секции. Кроме того, достоинствами протонных электролитов являются их более высокие величины электропроводности относительно кислородно-ионных проводников как результат более низких значений энергии активации (∼0.5 эВ для протонов относительно ∼1 эВ для ионов кислорода) [11].
Важно отметить, что для применения материалов с протонной проводимостью в топливных элементах особенно остро стоит проблема химической стабильности сложного оксида к кислотным газам, в частности, к СО2. Ранее было установлено, что введение фторид- и хлорид-ионов в анионную подрешетку кислород-дефицитных сложных оксидов позволяет значительно улучшить химическую стабильность к углекислому газу [12, 13]. Поскольку метод анионного допирования оказался весьма перспективным, то представляется важным исследование процессов гидратации, то есть, механизмов появления протонных дефектов, мест локализации протонов, их концентрации для таких галоген-допированных сложных оксидов.
Ранее особенности процессов гидратации анион-допированных протонных проводников с перовскитоподобной структурой были изучены на примере фторзамещенных составов на основе браунмиллерита Ba2In2O5, вакансии кислорода в котором упорядочены, и двойного перовскита Ba4Ca2Nb2O11, вакансии кислорода в котором разупорядочены [14]. Поскольку круг таких протон-проводящих систем со смешанным анионным окружением еще остается малочисленным, то вопросы о взаимосвязи между величиной степени гидратации, состоянием кислородно-водородных групп и кристаллохимическими особенностями сложнооксидных систем еще остаются до конца не выясненными.
В настоящей работе было осуществлено анионное гетеровалентное допирование F– → O2− протонного проводника Ba4In2Zr2O11, характеризующегося структурой простого (одинарного перовскита) с 1/12 вакантных позиций в кислородной подрешетке и их статистическим расположением [15]. Исследовано влияние концентрации фторид-ионов на процессы гидратации и состояние кислородно-водородных групп, а также проведен сравнительный анализ результатов с полученными ранее данными для фторзамещенных составов Ba2In2O5 – 0.5yFy и Ba4Ca2Nb2O11 – 0.5zFz [14].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Образцы Ba4In2Zr2O11 – 0.5xFx были получены методом твердофазного синтеза из предварительно осушенных BaCO3, In2O3, ZrO2, BaF2. Синтез проводили на воздухе при ступенчатом повышении температуры (800–1300°С) и многократных перетираниях в агатовой ступке в среде этилового спирта. Время отжига на каждой стадии составляло 24 ч.
Рентгенографический анализ был выполнен на дифрактометре Bruker Advance D8 в СuКα-излучении при напряжении на трубке 40 кВ и токе 40 мА. Съемка производилась в интервале 2θ = = 20–80° с шагом 0.05°θ и экспозицией 1 с на точку. Расчеты параметров решетки проводили методом полнопрофильного анализа Ритвельда с помощью программы FullProf Suite.
Термический анализ проводили на приборе NETZSCH STA 409 PC в комплекте с квадрупольным масс-спектрометром QMS 403C Aëolos (NETZSCH), позволяющем одновременно выполнять термогравиметрические измерения (ТГ), дифференциальную сканирующую калориметрию (ДСК) и анализ отходящих газов (масс-спектрометрия МС), в интервале температур 25–1000°С и скоростью нагрева 10 K/мин. Перед измерениями образцы подвергались термической обработке во влажном воздухе (рН2О = 2 × 10–2 атм) путем медленного охлаждения от 1000 до 200°C со скоростью 1 K/мин с целью получения гидратированных форм образцов. Влажность задавали путем барботирования воздуха при комнатной температуре последовательно через дистиллированную воду и насыщенный раствор бромида калия KBr (pH2O = 2 × 10–2 атм).
Для идентификации кислородно-водородных групп использовали метод ИК-спектроскопии. Исследования проводили на ИК-фурье-спектрометре Nicolet 6700 в диапазоне частот от 400 до 4000 см–1 методом диффузного отражения с использованием приставки Smart Diffuse Reflectance.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
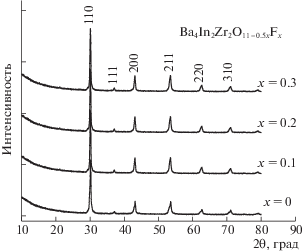
Методом рентгенофазового анализа было установлено, что составы Ba4In2Zr2O11 – 0.5xFx являются однофазными в интервале 0 ≤ x ≤ 0.3 и, как и матричный состав Ba4In2Zr2O11, характеризуются структурой одинарного перовскита (пространственная группа $Pm3m$). Эволюция рентгенограмм с ростом концентрации допанта представлена на рис. 1. Введение фторид-ионов, обладающих меньшим радиусом относительно ионов кислорода (${{r}_{{{{{\text{F}}}^{ - }}}}} = 1.33$ Å, ${{r}_{{{{{\text{O}}}^{{2 - }}}}}} = 1.40$ Å [16]), обусловило уменьшение параметров и объема элементарной ячейки образцов с ростом концентрации фтора, которые для состава с x = 0.3 составили соответственно а = 4.201(2) Å, V = 74.14 Å3. Значения, полученные для матричного состава (а = 4.204(3) Å, V = 74.30 Å3), хорошо согласуются с описанными ранее в литературе [15]. Необходимо отметить, что аналогичное уменьшение объема элементарной ячейки с ростом концентрации допанта было зафиксировано ранее для фторзамещенных составов Ba2In2O5 – 0.5yFy и Ba4Ca2Nb2O11 – 0.5zFz [14].
Для определения возможности поглощения воды из газовой фазы для предварительно гидратированных образцов Ba4In2Zr2O11 – 0.5xFx · nH2О (0 ≤ x ≤ 0.3) были проведены термические и МС-исследования. По убыли массы гидратированных составов была определена степень гидратации. Для удобства сравнения данные приведены в пересчете на число молей воды на формульную единицу сложного оксида (рис. 2). Совместно с ТГ-кривыми представлены результаты ДСК и масс-спектрометрии для состава Ba4In2Zr2O10.85F0.3 · · nH2О. Основная потеря массы наблюдается в температурном интервале 300–500°С, что, согласно результатам масс-спектрометрического анализа, обусловлено выходом H2O. Одновременно на ДСК кривой фиксируется слабо разрешенный эндотермический эффект. Выделения других возможных летучих веществ (СО2, HF) не было обнаружено.
Рис. 2.
Данные термогравиметрии (ТГ) для образцов Ba4In2Zr2O11 – 0.5xFx · nH2O (0 ≤ x ≤ 0.3), а также данные дифференциальной сканирующей калориметрии (ДСК) и масс-спектрометрии для образца Ba4In2Zr2O10.85F0.3 · nH2О.

То есть, исследуемые в работе фторзамещенные перовскиты Ba4In2Zr2O11 – 0.5xFx (0 ≤ x ≤ 0.3) способны к поглощению воды из газовой фазы. Однако рост концентрации допанта приводит к снижению степени гидратации от ∼0.95 моль для недопированного состава до ∼0.50 моль для состава с содержанием допанта x = 0.3. Одной из причин снижения степени гидратации является уменьшение концентрации вакансий кислорода в структуре фторзамещенных образцов с ростом содержания допанта:
(1)
${\text{Ba}}{{{\text{F}}}_{2}}\;\xrightarrow{{{\text{BaO}}}}\;{\text{Ba}}_{{{\text{Ba}}}}^{ \times } + {\text{F}}_{{\text{O}}}^{ \bullet } + {\text{F}}_{i}^{'},$Как известно, для высокотемпературных протонных проводников на основе сложных оксидов, появление во влажной атмосфере протонных дефектов описывается квазихимическим уравнением:
(2)
${\text{V}}_{{\text{O}}}^{{ \bullet \bullet }} + {{{\text{H}}}_{2}}{\text{O}} + {\text{O}}_{{\text{O}}}^{ \times } \Leftrightarrow 2{\text{OH}}_{{\text{O}}}^{ \bullet }.$Поэтому, исходя из номинальной концентрации вакансий кислорода, заданной уровнем допирования, можно было бы ожидать степени гидратации 0.95, 0.90 и 0.85 моль для составов Ba4In2Zr2O10.95F0.1[VО]0.95, Ba4In2Zr2O10.9F0.2[VО]0.9 и Ba4In2Zr2O10.85F0.3[VО]0.85 соответственно. Однако экспериментальные значения степени гидратации, как было показано выше, оказываются меньше. Эти различия тем больше, чем больше концентрация фтора.
Как известно, способность сложного оксида к гидратации обеспечивается не только наличием вакансий кислорода, но и способностью полиэдров с пониженным координационным числом (к.ч. < 6) восстанавливать свое координационное окружение (до к.ч. = 6) при участии ОН–-групп. Можно предположить, что появившиеся в структуре в ходе допирования фторсодержащие полиэдры [InO3F]/[ZrO3F] не способны к трансформации в октаэдры при диссоциативном поглощении воды, то есть, не реализуют смешанное окружение с участием ОН–-групп. Эта причина, вероятно, обуславливает снижение степени гидратации.
Для фторзамещенных составов, характеризующихся как структурой браунмиллерита Ba2In2O5 – 0.5yFy · nH2О, так и структурой двойного перовскита Ba4Ca2Nb2O11 – 0.5zFz · nH2О, рост концентрации допанта также приводит к снижению степени гидратации [14], что позволяет утверждать, что данный эффект является общим для исследуемых кислороддефицитных перовскитоподобных фаз и не зависит от степени разупорядочения вакансий кислорода.
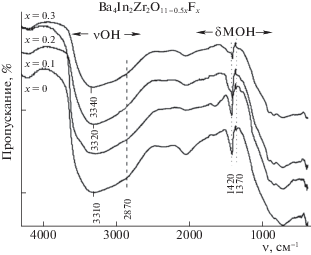
Установление форм кислородно-водородных групп было выполнено с помощью метода ИК-спектроскопии (рис. 3). Анализ области деформационных колебаний позволяет говорить о присутствии в данной области (ниже 2000 см–1) нескольких сигналов, относящихся к колебаниям кислородно-водородных групп. Близкорасположенные полосы с частотами 1420 и 1370 см–1 принадлежат деформационным колебаниям гидроксо-групп, связанных с атомами металла M–OH [17, 18]. Сигналов, относящихся к колебаниям молекулярной воды и катионам гидроксония (∼1600 см–1 и ∼1700 см–1) зарегистрировано не было. Асимметричный вид широкой полосы в области валентных колебаний 2800–3500 см–1 свидетельствует о наложении нескольких сигналов, то есть, о наличии ОН–-групп с различным кристаллографическим положением, и, соответственно, с разной степенью их участия в водородных связях. Четко прослеживается наличие двух полос. Полоса в области 3310–3340 см–1 соответствует ОН–-группам, вовлеченным в слабые водородные связи. Полоса с меньшей частотой ∼2870 см–1 (низкочастотное плечо главной полосы) указывают на наличие ОН–-групп, участвующих в образовании более сильных водородных связей.
Также с ростом концентрации фторид-ионов наблюдается уменьшение интенсивности полосы в области валентных колебаний, что говорит об уменьшении концентрации ОН–-групп в структуре. Данный факт хорошо коррелирует с результатами ТГ-исследований, показавших уменьшение степени гидратации образцов с ростом концентрации допанта.
Кроме того, можно отметить общую тенденцию (рис. 3) − с ростом концентрации допанта наблюдалось смещение сигнала от ОН–-групп, слабо связанных водородными связями (∼3310 см–1), в сторону бóльших частот (∼3320–3340 см–1), что свидетельствует о дополнительном ослаблении водородных связей. Этот факт может быть следствием укорочения длин связей М–ОН в полиэдрах, что хорошо коррелирует с уменьшением параметра решетки с ростом концентрации допанта.
Таким образом, гидратированные фторзамещенные образцы Ba4In2Zr2O11-0.5xFx · nH2О, как и матричный состав Ba4In2Zr2O11 · 0.95H2О, содержат энергетически неравноценные ОН–-группы, что подтверждается наличием двух сигналов в области валентных колебаний. Новых форм кислородно-водородных групп при допировании фтором не появлялось.
Аналогичный вид ИК-спектров был зафиксирован ранее для фторзамещенных фаз Ba4Ca2Nb2O11 – 0.5zFz · nH2О [14], характеризующихся, как и Ba4In2Zr2O11 – 0.5xFx · nH2О, статистическим распределением вакансий кислорода. В ИК-спектрах данных фаз в области валентных колебаний также присутствуют две полосы, отвечающие колебаниям энергетически неэквивалентных ОН–-групп.
В то же время, ИК-спектры индата бария Ba2In2O5 – 0.5yFy · nH2О [14], вакансии кислорода в котором упорядочены, имеют существенные отличия в области валентных колебаний по сравнению со спектрами для составов с разупорядоченными вакансиями кислорода Ba4In2Zr2O11 – 0.5xFx · · nH2О и Ba4Ca2Nb2O11 – 0.5zF · nH2О. В области высоких частот в спектрах Ba2In2O5 – 0.5yFy · nH2О появляется третий сигнал, отвечающий колебаниям изолированных ОН–-групп, т.е. ОН–-групп, вовлеченных в слабые водородные связи. Данный факт позволяет сделать вывод о том, что состояние анионной подрешетки кислород-дефицитных перовскитов, а именно, степень разупорядочения вакансий кислорода, оказывает влияние на степень вовлеченности ОН–-групп в водородные связи.
Таким образом, в работе осуществлен синтез фторзамещенных перовскитов Ba4In2Zr2O11 – 0.5xFx (0 ≤ x ≤ 0.3), рентгенографически подтверждена их однофазность. Установлено, что введение фторид-ионов приводит к уменьшению параметров кристаллической решетки. Доказана способность исследуемых фаз к диссоциативному поглощению воды из газовой фазы, сопровождающаяся появлением в структуре ОН–-групп, концентрация которых уменьшается с ростом концентрации допанта. Показано, что независимо от степени разупорядочения кислородной подрешетки, во фторзамещенных кислороддефицитных перовскитоподобных фазах на основе Ba4In2Zr2O11, Ba2In2O5 и Ba4Ca2Nb2O11 единственной формой кислородно-водородных групп являются энергетически неэквивалентные гидроксо-группы.
Исследование выполнено за счет гранта Российского научного фонда (проект № 18-73-00006).
Список литературы
Tatsumi Ishihara. Perovskite Oxide for Solid Oxide Fuel Cells. Fuel Cells and Hydrogen Energy, 2009.
Iwahara H., Asakura Y., Katahira K., Tanaka M. // Solid State Ionics. 2004. V. 168. P. 299.
Tao S., Irvine J.T.S. // Advanced Materials. 2006. V. 18. P. 1581.
Fabbri E., Bi L., Pergolesi D., Traversa E. // Advanced Materials. 2012. V. 24. P. 195.
Colomban Ph., Zaafrani O., Slodczyk A. // Membranes. 2012. V. 2. P. 493.
Kochetova N., Animitsa I., Medvedev D. et al. // RSC Advances. 2016. V. 6. P. 73222.
Medvedev D.A., Lyagaeva J.G., Gorbova E.V. et al. // Progress in Materials Science. 2016. V. 75. P. 38.
Marrony M., Dailly J. // ECS Transactions. 2017. V. 78. P. 3349.
Dubois A., Ricote S., Braun R.J. // ECS Transactions. 2017. V. 78. P. 1963.
Shin E., Shin M., Lee H., Park J.-S. // Ceramics International. 2018. V. 44. P. 8423.
Duan C., Tong, J., Shang M. et al. // Science. 2015. V. 349. I. 6254. P. 1321.
Wang Y., Wang H., Liu T. et al. // Electrochem. Commun. 2013. V. 28. P. 87.
Tarasova N., Animitsa I. // J. Alloys and Compounds. 2018. V. 739. P. 353.
Tarasova N.A., Animitsa I.E., Belova K.G. // Bulletin of the Russian Academy of Sciences: Physics. 2017. V. 81. P. 632.
Animitsa I.E., Dogodaeva E.N., Nokhrin S.S. et al. // Russ. J. Electrochemistry. 2010. V. 46. P. 734.
Shannon R.D. // Acta Crystallographica. 1976. V. A32. P. 155.
Юхневич Г.В. Инфракрасная спектроскопия воды. М.: Наука, 1973. 205 с.
Карякин А.В., Кривенцова Г.А. Состояние воды в органических и неорганических соединениях. М.: Наука, 1973. 176 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии