Журнал физической химии, 2020, T. 94, № 11, стр. 1723-1726
Кинетическая модель сопряженных метаболических циклов: орнитинового и лимонной кислоты
Ю. А. Ершов a, К. Д. Лукин b, Т. К. Слонская c, *, М. А. Хачатурян c
a Московский государственный технический университет имени Н.Э. Баумана
Москва, Россия
b Минский филиал РЭУ имени Г.В. Плеханова
Минск, Республика Беларусь
c Первый Московский государственный медицинский университет имени И.М. Сеченова
Москва, Россия
* E-mail: tslonskaya@mail.ru
Поступила в редакцию 27.12.2019
После доработки 27.12.2019
Принята к публикации 21.01.2020
Аннотация
На основе кинетического графа и модели биокинетики сопряженных метаболических циклов лимонной кислоты и орнитинового цикла подобраны константы биохимических реакций и решена система из восьми обыкновенных дифференциальных уравнений. Построены зависимости количества метаболитов и продуктов от времени.
Существование сопряженных метаболических циклов в организме экспериментально доказано [1]. Изучена кинетика биохимических реакций отдельных стадий метаболических путей [2]. Кинетика сопряженных метаболических циклов изучена недостаточно из-за большого числа параметров, влияющих на протекание биохимических процессов. Воссоздать подобные процессы in vitro для изучения и анализа практически невозможно, поэтому актуальным, а иногда и единственным, остается подход с использованием математического моделирования.
Сложные связи между орнитиновым циклом и циклом лимонной кислоты (рис. 1), с точки зрения химической кинетики, предложено описывать с помощью кинетического графа [2] и моделировать с помощью системы обыкновенных дифференциальных уравнений.
В [3] приводится система обыкновенных дифференциальных уравнений (I), а также формулируются задачи, связанные с этой системой.
(2)
$d{{x}_{1}}{\text{/}}dt = {{k}_{x}}_{{01}}{{x}_{0}} + {{k}_{x}}_{{31}}{{x}_{3}}--{{k}_{x}}_{{12}}{{x}_{1}},$(3)
$d{{x}_{2}}{\text{/}}dt = {{k}_{x}}_{{12}}{{x}_{1}}--{{k}_{x}}_{{23}}{{x}_{2}} + {{k}_{y}}_{{22}}{{y}_{2}}--{{k}_{y}}_{{21}}{{y}_{2}},$(I)
$\begin{gathered} \hfill d{{x}_{3}}{\text{/}}dt = {{k}_{x}}_{{23}}{{x}_{2}}--{{k}_{x}}_{{31}}{{x}_{3}}--{{k}_{x}}_{{3p}}{{x}_{3}},\quad \quad \left( 4 \right) \\ \hfill d{{y}_{{\text{1}}}}{\text{/}}dt = {{k}_{y}}_{{21}}{{x}_{2}}--{{k}_{y}}_{{21}}{{y}_{1}},\quad \quad \;\quad \left( 5 \right) \\ \end{gathered} $(6)
$d{{y}_{2}}{\text{/}}dt = {{k}_{y}}_{{12}}{{y}_{1}}--{{k}_{y}}_{{22}}{{y}_{2}}--{{k}_{y}}_{{2p}}{{y}_{2}},$Настоящая работа посвящена построению кинетических кривых зависимости количества метаболитов и продуктов xi, yi, px, py от времени на основе решения системы дифференциальных уравнений (I), а также проведению регуляризации полученных решений для метаболитов и продуктов на основе базы экспериментальных данных для значений констант скорости реакций. Для достижения поставленной цели:
а) проанализированы неизвестные функции системы (I): x0(t), x1(t), x2(t), y1(t), y2(t), px(t), py(t). Все коэффициенты k c индексами – постоянные величины;
б) подобраны значения концентраций субстратов (табл. 1) и констант для решения системы дифференциальных уравнений (табл. 2).
Таблица 1.
Концентрации субстратов (yi) в метаболических циклах
| yi, М | t = 10 с | t = 360 с | t = 600 с |
|---|---|---|---|
| y1 (аргинин сукцинат) | 9.31 × 10–7 | 2.40 × 10–6 | 2.44 × 10–6 |
| y2 (аргинин) | 3.90 × 10–7 | 8.82 × 10–7 | 9.04 × 10–7 |
| Орнитин | 3.96 × 10–4 | 2.58 × 10–4 | 2.56 × 10–4 |
| Цитрулин | 4.81 × 10–5 | 1.84 × 10–4 | 1.86 × 10–4 |
| Мочевина | 1.20 × 10–5 | 2.20 × 10–3 | 3.77 × 10–3 |
| х2 (сукцинат) | 9.50 × 10–7 | 9.04 × 10–6 | 1.09 × 10–5 |
Таблица 2.
Значения кинетических констант в уравнениях
| ky21, 1/c | ky12, 1/c | ky2p, 1/c | kx23, 1/c |
|---|---|---|---|
| 2.04 × 10–3 | 1.00 × 10–4 | 1.00 × 10–2 | 1.6 × 10–3 |
| kx12, 1/c | kx3p, 1/c | ky22, 1/c | kx31, 1/c |
| 2.0 × 10–1 | 0.9 × 10–3 | 1.5 × 10–3 | 1.3 × 10–3 |
При ${{{v}}_{0}}$ = ${{{v}}_{0}}$(t) уравнение (1) – линейное дифференциальное уравнение первого порядка. Частное решение этого уравнения при начальном условии x0(0) = a:
(II)
${{x}_{0}} = {{{v}}_{0}}{\text{/}}{{k}_{x}}_{{01}}--({{{v}}_{0}}{\text{/}}{{k}_{x}}_{{01}}--a)\exp (--{{k}_{x}}_{{01}}t).$При моделировании рассматривали варианты А и Б.
А. Пусть ky22 = ky21. В этом случае система (I) распадается на три подсистемы: (2), (3*), (4); (5), (6) и (7), (8); при этом
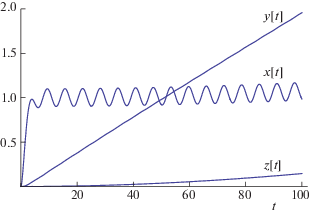
Решаем подсистему (2), (3*), (4), полагая при t = = 0: ${{{v}}_{0}}$ = 0.1, a = 2, xi = y = px = py = 0. Для удобства введены следующие обозначения: x1(t) = x(t), x2(t) = y(t), x3(t) = z(t). Программа для решения этой системы имеет видРешаем подсистему (5), (6). Так как функция x2 найдена в виде интерполяционного многочлена, то, подставив этот многочлен в подсистему (5), (6). Решаем ее так же, как и подсистему (2), (3*), (4). При этом вводим обозначения y1(t) = Y(t), y2(t) = Z(t). Программа для решения этой подсистемы:
Решаем третью подсистему (7), (8). Функции x3[t] и y2[t] найдены выше в виде интерполяционных многочленов:
Б. Снимая ограничение: ky22 ≠ ky21, решаем исходную систему (I) при следующих значениях констант:
При значении kx12 = 2.1 × 10–2 1/c решение этой системы получаем аналогично.
Решение системы (I) существенно зависит от ее первого уравнения. Решение этого уравнения задается формулой (II). При ${{{v}}_{0}}$ = 2 решение первого уравнения принимает вид:
Решение системы для x0 = 2 – еxp(–t):Полученные результаты могут служить базой для количественного прогнозирования при изучении сложных биохимических процессов метаболических циклов в организме человека.
Список литературы
Mogilevskaya E., Demin O., Goryanin I. // J. Biol. Phys. 2006. V. 32. P. 245.
Feng Qi, Xuewen Chen, Beard D.A. // Biochim. Biophys. Acta. 2008. V. 1784(11). P. 1641.
Ершов Ю.А. // Журн. физ. xимии. 2016. Т. 90. № 1. С. 13.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии