Журнал физической химии, 2020, T. 94, № 12, стр. 1842-1848
Новый кислород-дефицитный перовскит La(Al0.5Zn0.5)O2.75: синтез, структура, транспортные свойства
А. В. Егорова a, b, К. Г. Белова a, b, И. Е. Анимица a, b, *
a Уральский федеральный университет им. первого Президента России Б.Н. Ельцина
620002 Екатеринбург, Россия
b Российская академия наук, Уральское отделение, Институт высокотемпературной электрохимии
Екатеринбург, Россия
* E-mail: irina.animitsa@urfu.ru
Поступила в редакцию 03.03.2020
После доработки 25.03.2020
Принята к публикации 14.04.2020
Аннотация
Впервые осуществлен твердофазный синтез кислород-дефицитного перовскита La(Al0.5Zn0.5)O2.75, кристаллизующегося в пр. гр. Pm3m с параметром решетки 3.7932 Å. Катионный состав фазы подтвержден методом химического анализа. Доказано, что алюмоцинкат лантана обладает смешанным типом проводимости в области высоких парциальных давлений кислорода и температур выше 500°C, а при температурах ниже 400°С проявляет доминирующий кислород-ионный транспорт. Введение цинка в В-подрешетку перовскита позволило получить высокоплотную керамику (>95%).
Оксидные соединения, кристаллизующиеся в структуре перовскита АВО3, являются наиболее интенсивно изучаемыми материалами в химии и физике твердого тела [1]. С одной стороны, интерес к перовскитам обусловлен их важными физико-химическими свойствами: среди них известны сегнето- и антисегнетоэлектрики, ферромагнетики, сегнетоэластики [2, 3], перовскиты обнаруживают свойства полупроводников, сверхпроводимость [4], ионную проводимость [5] и каталитические свойства [6]. Возможность сочетания комплекса физико-химических характеристик предопределяет высокую фундаментальную значимость перовскитов, как особого класса неорганических соединений.
C другой стороны, благодаря толерантности перовскитной структуры, существует возможность получения большого круга соединений при реализации разнообразных способов модифицирования структуры. А это делает возможным целенаправленную “подгонку” практически важного свойства и значительно расширяет границы поиска новых соединений с определенными функциональными свойствами.
Для создания новых керамических материалов со структурно-чувствительными свойствами важной задачей является задание определенной дефектности. Особый интерес представляют перовскиты с кислородным дефицитом. Такие соединения способны к облегченному кислород-ионному транспорту и, в зависимости от соотношения ионной и электронной проводимости, могут быть использованы в различных электрохимических устройствах как электролиты, мембранные материалы, катоды и т.д. Основной проблемой использования таких материалов является низкая химическая устойчивость к кислотным газам, в частности, к СО2. Химическая устойчивость напрямую зависит от элементного состава вещества. Так, например, присутствие щелочноземельного компонента в составе перовскитов А+2В+4О3 может привести к образованию соответствующих карбонатов [7–9] и, как следствие, разрушению материала. В связи с этим, в настоящее время одним из перспективных направлений материаловедческого поиска является разработка новых кислород-дефицитных соединений, не содержащих в составе химической формулы щелочно-земельного металла (в зарубежной литературе эта стратегия известна как alkaline earth elements free strategy). Это можно реализовать при модифицировании перовскитов с иными зарядовыми комбинациями элементов А- и В-подрешеток, например, А+3В+3О3.
Традиционно для задания кислородного дефицита в перовскитах используется метод акцепторного допирования. Однако перовскиты А+3В+3О3 имеют, как правило, небольшие области гомогенности относительно допирующих элементов, и это не позволяет достичь высоких концентраций вакансий кислорода. Кроме того, в качестве допантов – двухзарядных элементов, используют щелочноземельные металлы, присутствие которых снижает химическую устойчивость фаз.
Однако, существует другой способ организации кислородного дефицита – это создание многоподрешеточных структур. В частности, введение в В-подрешетку соответствующих разнозарядных катионов в соотношении 1 : 1 может привести к ситуации, когда часть позиций кислорода остается не заполненной. Этот метод успешно реализован для кислород-дефицитных перовскитов, например, составов Ba4(Ca2Nb2)O11, [10–12], Ba4(Ca2Ta2)O11 [13], Sr4(Sr2Nb2)O11 [14], Sr4(Sr2Та2)O11 [15, 16], Ba4Na2W2O11 [17, 18]. Однако для перовскитов A3+B3+O3 в литературе такие методы модифицирования структуры не описаны. И в этой связи, имеется широкое поле для кристаллохимического дизайна новых многоподрешеточных структур на основе A3+B3+O3 и получения новых соединений с улучшенными свойствами.
Например, введение в В-подрешетку перовскитов А3+В3+О3 в качестве 2-х зарядного элемента цинка, La(В0.5Zn0.5)O2.75, приводит не только к частичной занятости кислородной подрешетки, но может улучшить спекаемость образцов и позволит получить высокоплотную керамику.
Среди известных перовскитов состава А3+В3+О3 алюминаты LaAlO3 имеют такие преимущества, как невысокая стоимость сырья, более высокая термодинамическая устойчивость из-за прочности связи Al–O, более широкая T–${{p}_{{{{{\text{O}}}_{2}}}}}$ область ионной проводимости [19]. Поэтому алюминатная система представляет интерес для модифицирования ее структуры и получения новых фаз на ее основе.
В настоящей работе проведен синтез нового кислород-дефицитного перовскита La(Al0.5Zn0.5)O2.75, впервые описана его кристаллическая структура и транспортные свойства.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез образца состава La(Al0.5Zn0.5)O2.75 проводили на воздухе из оксидов лантана (La2O3, 99.99%), алюминия (Al2O3, 99.99%) и цинка (ZnO, 99.99%), взятых в стехиометрических соотношениях. Исходные реагенты перед взятием навесок были предварительно прокалены. Для оксидов алюминия и цинка прокаливание проводили для удаления адсорбционной влаги при 500°С в течение 3 ч. Оксид лантана прокаливали при 1100°С в течение 3 ч для удаления поверхностных основных карбонатов. После прокаливания оксиды охлаждали и взвешивали в бюксах с известной массой. Исходные навески были взяты на аналитических весах с точностью ±0.0001 г, их смешивание проводили в среде этилового спирта в агатовой ступке, затем в шаровой мельнице. Синтез проводили в алундовых тиглях в температурном интервале 700–1400°С с шагом в 100° и выдержками по 24 ч. После каждой стадии отжига образец перетирали в шаровой мельнице в среде этилового спирта.
Фазовый состав полученного образца контролировали методом порошковой рентгеновской дифракции. Съемка рентгенограмм была выполнена при комнатной температуре на дифрактометре Bruker D8 Advance в СuKα-излучении, с шагом 0.05Θ в интервале углов 2Θ = 10°–80° и экспозицией 1 с, напряжение 40 кВ, ток 40 мА. Уточнение кристаллической структуры осуществляли методом полнопрофильного анализа Ритвельда с использованием ПО FULLPROF и графического инструментария к ней – WinPLOTR. Кристаллические фазы идентифицировали по базе данных ICDD–2003.
Элементный состав образца количественно определяли атомно-эмиссионным методом на спектрометре с индуктивно-связанной плазмой “Optima 4300 DV ICP-OES” фирмы “Perkin Elmer” (используемый газ – аргон; расход 25 л/мин; чистота газа 99.996%). Для проведения анализа брали навески образцов массой 0.02–0.05 г, растворяли в концентрированной азотной кислоте (“ос.ч.”), доводили до метки деионизованной водой в мерной колбе). По результатам рассчитывали соотношение по металлическим компонентам в соединении. Погрешность определения содержания не превышала 5 отн. %.
Для определения размера частиц был использован анализатор “Litesizer™ 500” фирмы “Anton Paar”, источник света – полупроводниковый лазер, 40 мВ, с длиной волны 658 нм. Углы измерения 15°, 90°, 175°, температура измерений 23.0°С, точность ±2% (стандарт NIST), повторяемость ±2% (стандарт NIST). Небольшое количество порошка вносили в абсорбционную микрокювету из кварца SUPRASIL (длина волны 200–2500 нм, длина оптического пути 10 мм), кювету с образцом помещали в анализатор. Эксперименты проводили в нескольких параллелях, в водной среде и в ацетоне.
Для проведения электрических измерений полученный образец прессовали в виде таблеток диаметром 10–12 мм и толщиной ~2 мм на ручном прессе при давлении ∼5 МПа. В качестве пластификатора использовали раствор натурального каучука в толуоле. Спекание сформированных брикетов проводили при температуре 1400°С в течение 24 ч. Относительная плотность образцов, измеренная методом гидростатического взвешивания, составила 95–98%. Платиновые электроды в виде мелкодисперсной Pt-пасты, смешанной со спиртовым раствором канифоли, наносили на предварительно отшлифованную поверхность спеченных таблеток. Вжигание электродов проводили на воздухе при 900°С, 2 ч.
Электропроводность измерялась в двухконтактной ячейке методом электрохимического импеданса с использованием измерителя параметров импеданса “Elins Z-1000P” в частотном интервале 100 Гц–1 МГц в режиме охлаждения с 1000°С до 300°С со скоростью 2°С/мин, при измерениях на каждой температуре проводилась выдержка до установления постоянного значения сопротивления. Удельную электропроводность рассчитывали по формуле:
где l – толщина образца, см; S – площадь поверхности поперечного сечения, см2; R – объемное сопротивление образца, Ом, рассчитанное из данных электрохимического импеданса.Для измерения электропроводности образца La(Al0.5Zn0.5)O2.75 в зависимости от парциального давления кислорода использовали установку с электрохимическим насосом и датчиком из стабилизированного ZrO2 (Y2O3), что позволило произвести измерения в интервале парциальных давлений кислорода 0.21–10–20 атм. Измерения проводили в интервале температур 400–900°С, с шагом в 100° и с длительными выдержками для достижения равновесия в системе “образец – газовая фаза” при Т = const и ${{p}_{{{{{\text{O}}}_{2}}}}}$ = const.
Из зависимостей общей электропроводности от ${{p}_{{{{{\text{O}}}_{2}}}}}$ были рассчитаны парциальные проводимости (ионные и электронные составляющие), а также ионные числа переноса. Обработка экспериментальных зависимостей lg σ–lg ${{p}_{{{{{\text{O}}}_{2}}}}}$ проводилась при использовании аппроксимации уравнением вида (Т = const):
(2)
${{\sigma }_{{{\text{общ}}}}} = {{\sigma }_{{{\text{эл}}}}} + {{\sigma }_{{{\text{ион}}}}} = Kp_{{{{{\text{O}}}_{2}}}}^{{1/4}} + {{\sigma }_{{{\text{ион}}}}},$ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Синтез образца проводили согласно следующей твердофазной реакции:
(3)
$\begin{gathered} 1{\text{/}}2{\text{L}}{{{\text{a}}}_{{\text{2}}}}{{{\text{O}}}_{3}} + 1{\text{/}}4{\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{3}} + 1{\text{/}}2{\text{ZnO}} \to \\ \to {\text{La}}({\text{A}}{{{\text{l}}}_{{{\text{0}}{\text{.5}}}}}{\text{Z}}{{{\text{n}}}_{{{\text{0}}{\text{.5}}}}}){{{\text{O}}}_{{2.75}}}. \\ \end{gathered} $(4)
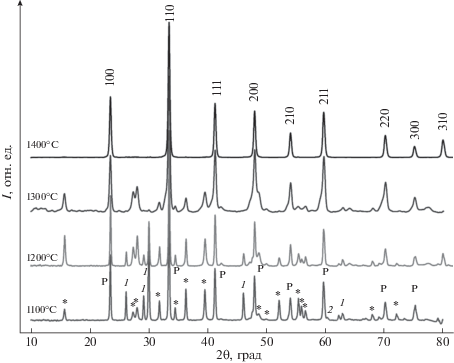
$1{\text{/}}2{\text{LaAl}}{{{\text{O}}}_{3}} + 1{\text{/}}2{\text{LaZn}}{{{\text{O}}}_{{2.5}}} \to {\text{La}}({\text{A}}{{{\text{l}}}_{{{\text{0}}{\text{.5}}}}}{\text{Z}}{{{\text{n}}}_{{{\text{0}}{\text{.5}}}}}){{{\text{O}}}_{{2.75}}}.$Рис. 1.
Эволюция рентгенограмм образца состава 1/2La2O3 · 1/4Al2O3 · 1/2ZnO в интервале температур 1100–1400°С (1 – La2O3, 2 – Al2O3, * – LaZnO2.5, Р – перовскит).
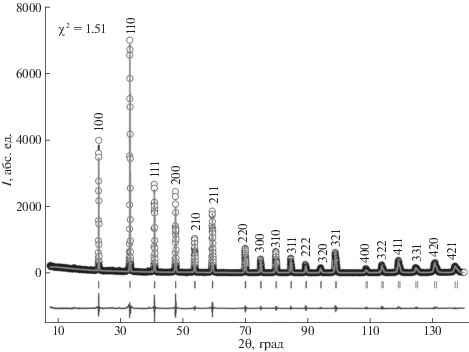
Обработка дифрактограмм (рис. 2) методом Ритвельда показала, что фаза La(Al0.5Zn0.5)O2.75 кристаллизуется в кубической симметрии. Пространственная группа Pm3m, рассчитанный параметр решетки составил 3.79321Å ± 0.00003.
Рис. 2.
Наблюдаемые, рассчитанные и разностные рентгеновские профили, угловые положения рефлексов для фазы La(Al0.5Zn0.5)O2.75 показаны штрихами.
По результатам химического анализа был установлен катионный состав синтезированной фазы (табл. 1). Как видно, катионный состав, в целом, хорошо сохранялся, небольшие отклонения входят в доверительный интервал.
Таблица 1.
Катионный состав перовскита La(Al0.5 Zn0.5)O2.75 по результатам химического анализа (II) в сравнении с теоретическими значениями (I)
| Элемент | Содержание, ат. % | |
|---|---|---|
| I | II | |
| La | 50 | 50.84 ± 0.5 |
| Al | 25 | 24.51 ± 0.2 |
| Zn | 25 | 24.65 ± 0.2 |
Серия измерений, выполненная с помощью анализатора размеров частиц, позволила определить средний диаметр частиц. На зависимостях распределения интенсивности светорассеяния суспензии частиц La(Al0.5Zn0.5)O2.75 по гидродинамическому диаметру наблюдался один основной пик, отвечающий максимуму распределения в области ∼1 мкм. Образец характеризовался достаточно узким распределением. По результатам статистической обработки данных, cреднее значение гидродинамического диаметра частиц составило 1.32 мкм, стандартное отклонение 0.02 мкм (1.51%).
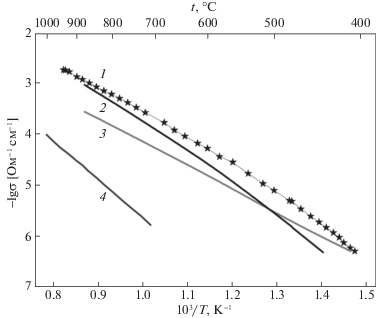
На рис. 3 представлены политермы электропроводности исследуемого образца La(Al0.5Zn0.5)O2.75 в сравнении с данными для алюмината лантана LaAlO3 [20]. Как видно, проводимость La(Al0.5Zn0.5)O2.75 на несколько порядков выше, чем у алюмината лантана LaAlO3, что обусловлено наличием кислородного дефицита в исследуемой фазе.
Рис. 3.
Температурные зависимости общей (1), электронной (2) и кислород-ионной (3) проводимостей La(Al0.5Zn0.5)O2.75 в сравнении с общей проводимостью алюмината лантана LaAlO3 (4) [20].
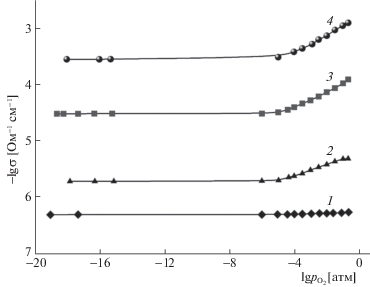
Для последующего разделения общей проводимости алюмоцинката лантана La(Al0.5Zn0.5)O2.75 на парциальные вклады (ионный и электронный), исследовали электропроводность при варьировании парциального давления кислорода в интервале температур 400–900°С. На рис. 4 приведены изотермы проводимости в зависимости от парциального давления кислорода. На изотермах можно выделить две области: область электролитической проводимости, которая выглядит как плато, то есть, область независимости проводимости от давления кислорода, и область при высоких парциальных давлениях кислорода (${{p}_{{{{{\text{O}}}_{2}}}}}$ > > 10–4 атм), для которой наблюдается положительный наклон зависимости. В данной области проявляется вклад электронной проводимости р-типа, возникающей за счет образования дырочных дефектов ${{h}^{ \bullet }}$ в соответствии с уравнением:
(5)
$V_{{\text{O}}}^{ \times } + \frac{1}{2}{{{\text{O}}}_{2}} \leftrightarrow {\text{O}}_{i}^{{''}} + 2{{h}^{ \bullet }},$Рис. 4.
Зависимости общей проводимости La(Al0.5Zn0.5)O2.75 от парциального давления кислорода при 400 (1), 500 (2), 700 (3), 900°С (4).
При снижении температуры наблюдается расширение области независимости проводимости от парциального давления кислорода, и при температурах ниже 400°С образец характеризуется доминирующим ионным типом проводимости во всей исследованной области ${{p}_{{{{{\text{O}}}_{2}}}}}$.
Температурные зависимости рассчитанных парциальных проводимостей − ионной и электронной, представлены на рис. 3, их энергии активации составили 0.93 и 1.20 эВ, соответственно. Как видно, ниже 450°С начинает преобладать ионная проводимость.
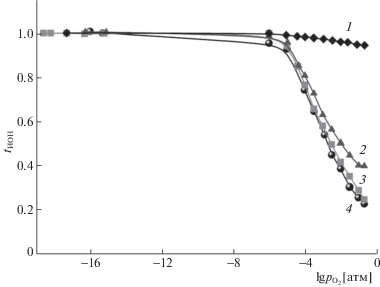
Ионные числа переноса tион были рассчитаны как отношение ионной электропроводности к общей σиoн/σ. На рис. 5 представлены рассчитанные данные tион в зависимости от парциального давления кислорода. Максимальные значения ∼1 достигаются в области низких значений парциальных давлений кислорода. На воздухе (${{p}_{{{{{\text{O}}}_{2}}}}}$ = 0.21 атм) при понижении температуры наблюдается увеличение значений ионных чисел переноса, доминирующий ионный транспорт реализуется ниже 400°С.
Рис. 5.
Зависимости ионных чисел переноса для La(Al0.5Zn0.5)O2.75 от парциального давления кислорода при 400 (1), 500 (2), 700 (3), 900°C (4).
Таким образом, в настоящей работе впервые синтезирован новый кислород-дефицитный перовскит La(Al0.5Zn0.5)O2.75, на основе которого получена высокоплотная керамика (>95%). По результатам РФА установлено, что алюмоцинкат лантана кристаллизуется в кубической симметрии с параметром 3.7932 Å. Фаза La(Al0.5Zn0.5)O2.75 на воздухе обладает смешанным типом проводимости, доминирующий кислород-ионный транспорт реализуется при температурах ниже 400°С (${{p}_{{{{{\text{O}}}_{2}}}}}$ = 0.21 атм), а также при низких ${{p}_{{{{{\text{O}}}_{2}}}}}$ < 10–6 атм.
Работа выполнена при финансовой поддержке госзадания АААА-А20-120061990010-7. Авторы выражают благодарность Н.И. Москаленко за эксперименты по определению элементного состава соединения и И.А. Мальковой за результаты анализа размера частиц.
Список литературы
Vasala S., Karppinen M. // Progress in Solid State Chemistry. 2015. V. 43. P. 1. https://doi.org/10.1016/j.progsolidstchem.2014.08.001
Cross L.E., Newnham R.E. // Ceramics and Civilization. J. Am. Ceram. Soc. 1987. V. 3. P. 289.
Iwanaga D., Inaguma Y., Itoh M. // J. Solid State Chem. 1999. V. 147. P. 291. https://doi.org/10.1006/jssc.1999.8273
Cava R.J., Batlogg B., Krajewski J.J. et al. // Nature. 1988. V. 332. P. 814.https://doi.org/10.1038/332814a0
Li M., Pietrowski M.J., De Souza R.A. et al. // Nat Mater. 2014. V. 13. P. 31.https://doi.org/10.1038/nmat3782
Tanaka H., Misono M. // Curr Opin Solid State Mater Sci. 2001. V. 5. P. 381.https://doi.org/10.1016/S1359-0286(01)00035-3
Matsumoto H., Kawasaki Y., Ito N. et al. // Electrochem. Solid-State Lett. 2007. V. 10. № 4. P. B77–B80. https://doi.org/10.1149/1.2458743
Medvedev D.A., Lyagaeva J.G., Gorbova E.V. et al. // Prog. Mater. Sci. 2016. V. 75. P. 38.https://doi.org/10.1016/j.pmatsci.2015.08.001
Ryu K.H., Haile S.M. // Solid State Ion. 1999. V. 125. P. 355. https://doi.org/10.1016/S0167-2738(99)00196-4
Kochetova N.A., Animitsa I. E., Neiman A.Ya. // Russ. J. Phys. Chem. A. 2009. V. 83. № 2. P. 203. https://doi.org/10.1134/S0036024409020101
Ashok A., Kochetova N., Norby T., Olsen A. // Solid State Ion. 2008. V. 179. P. 1858.https://doi.org/10.1016/j.ssi.2008.05.008
Korona D.V., Neiman A.Ya., Animitsa I.E., Sharafutdinov A.R. // Russ. J. Electrochem. 2009. V. 45. № 5. P. 586. https://doi.org/10.1134/S1023193509050176
Baliteau S., Mauvy F., Fourcade S., Grenier J.C. // Solid State Sci. 2009. V. 11. P. 1572. https://doi.org/10.1002/chin.200946008
Jalarvo N., Haavik C., Kongshaug C. et al. // Solid State Ion. 2009. V. 180. № 20–22. P. 1155.https://doi.org/10.1016/j.ssi.2009.05.021
Animitsa I., Norby T., Marion S. et al. // Ibid. 2001. V. 145. № 1–4. P. 357. https://doi.org/10.1016/S0167-2738(01)00931-6
Animitsa I., Neiman A., Titova S. et al. // Ibid. 2003. V. 156. P. 95. https://doi.org/10.1016/S0167-2738(02)00605-7
Animitsa I., Dogodaeva E., Tarasova N. et al. // Ibid. 2011. V. 185. P. 1.https://doi.org/10.1016/j.ssi.2010.12.013
Hoffmann R., Hoppe R. // Z. Anorg. Allg. Chem. 1989. V. 575. № 1. P. 154.https://doi.org/10.1002/zaac.19895750119
Park J.Y., Choi G.M. // Solid State Ion. 2002. V. 154. P. 535. https://doi.org/10.1016/S0167-2738(02)00510-6
Fabiana M., Arias-Serranob B.I., Yaremchenko A.A. et al. // J. Eur. Ceram. Soc. 2019. V. 39. P. 5298. https://doi.org/10.1016/j.jeurceramsoc.2019.07.038
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


