Журнал физической химии, 2020, T. 94, № 12, стр. 1776-1782
Наноструктурированные пленки Pb(S,O): синтез, механизм осаждения и оптические свойства
Р. Х. Сарыева a, Н. С. Кожевникова a, b, *, Л. Н. Маскаева a, c, В. Ф. Марков a, c, В. И. Воронин d, О. А. Липина b, А. Н. Еняшин b, В. Г. Бамбуров b
a Уральский федеральный университет имени первого Президента России Б.Н. Ельцина
Екатеринбург, Россия
b Российская академия наук, Уральское отделение, Институт химии твердого тела
Екатеринбург, Россия
c Уральский институт ГПС МЧС России
Екатеринбург, Россия
d Российская академия наук, Уральское отделение, Институт физики металлов имени М.Н. Михеева
Екатеринбург, Россия
* E-mail: kozhevnikova@ihim.uran.ru
Поступила в редакцию 03.03.2020
После доработки 25.03.2020
Принята к публикации 14.04.2020
Аннотация
Методом химического осаждения из водных щелочных растворов получены тонкие пленки сульфида свинца Pb(S,O) с содержанием кислорода от 0.2 до 30.7 ат. %, регулируемым различными лигандами. C использованием экспериментальных методов и квантово-химического моделирования продемонстрировано влияние кислорода на механизм формирования и оптические свойства пленок Pb(S,O). Впервые показан гетероструктурный характер синтезированных соединений Pb(S,O) и предложен механизм их формирования в водном растворе.
Тонкопленочный сульфид свинца PbS – базовый полупроводниковый материал для регистрации видимого и инфракрасного излучения в диапазоне 0.4–3.0 мкм [1]. PbS относится к узкозонным полупроводникам AIVBVI с р-типом проводимости и шириной запрещенной зоны Eg = = 0.41–0.42 эВ при комнатной температуре и применяется в транзисторах, инжекционных лазерах, сенсорах для определения ионов свинца в аква- и биосредах, электролюминесцентных батареях, датчиках контроля влажности, температуры и выбросов токсичных газов [2–4]. Высокое значение коэффициента поглощения (∼105 см–1) позволяет использовать PbS для изготовления солнечных элементов [5].
Формирование слоев PbS осуществляется методами термического испарения в вакууме, ионного наслаивания, ультразвукового спрей-пиролиза, химического осаждения из газовой фазы [6–9] и др. Однако наиболее перспективным способом считается химическое осаждение из водных сред [10, 11]. Этот универсальный метод характеризуется простотой организации, высоким качеством и однородностью получаемых покрытий, не требует применения сложного технологического оборудования.
Одним из способов регулирования структурных, оптических, электрических и магнитных свойств PbS является допирование подрешетки Pb различными элементами [12]. Анализ современных литературных данных показал отсутствие работ по влиянию кислорода на структурные, морфологические и оптические свойства PbS. В настоящем исследовании методом химического осаждения из водных растворов предпринята попытка направленного синтеза пленок сульфида свинца с разным содержанием примесного кислорода Pb(S,O), а также предложен механизм их формирования и установлено влияние кислорода на структуру и оптические свойства пленок Pb(S,O).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Пленки Pb(S,O) получали химическим осаждением из водных растворов с использованием ацетата свинца Pb(CH3COO)2 и тиомочевины N2H4CS. Роль лигандов выполняли гидроксид-(OH–) и цитрат-(C6H5O$_{7}^{{3 - }}$) ионы, а также молекулы этилендиамина C2H8N2 (табл. 1). Щелочную среду, способствующую разложению N2H4CS, создавали в зависимости от используемой рецептуры введением в объем реакционной смеси гидроксида натрия NaOH, водного раствора аммиака NH4OH или этилендиамина C2H8N2 (табл. 1). Осаждение пленок Pb(S,O) осуществляли на ситалловые и стеклянные подложки. Синтез проводили в термостате при 298 и 353 K с точностью поддержания температуры ±0.1 K.
Таблица 1.
Характеристики пленок Pb(S,O), полученных из водных щелочных растворов N2H4CS c использованием различных лигандов (d – толщина пленки)
| Система | pH | Элементный анализ, ат. % | d, нм | 〈D〉, нм | ||
|---|---|---|---|---|---|---|
| Pb | S | О | ||||
| Аммиачно-цитратная NH3 + C6H5O$_{7}^{{3 - }}$ (1) | 12.3 | 49.70 | 50.07 | 0.23 | 590 | 290 |
| Этилендиамин-цитратная C2H8N2 + C6H5O$_{7}^{{3 - }}$ (2) | 12.1 | 41.16 | 43.60 | 15.24 | 540 | 114 |
| Гидроксидная NaOH (3) | 13.1 | 41.88 | 44.37 | 13.76 | 390 | 189 |
| Гидроксидно-цитратная NaOH + C6H5O$_{7}^{{3 - }}$ (4) | 12.3 | 33.58 | 34.70 | 30.68 | 270 | 61 |
Кристаллическую структуру и фазовый состав пленок Pb(S,O) изучали на рентгеновском дифрактометре Empyrean с вертикально расположенным гониометром высокого разрешения. Рентгенодифракционные измерения проводили методом Брэгга–Брентано в CuKα1,2-излучении в интервале углов 2θ = 15°–100° с шагом ∆(2θ) = = 0.02° и экспозицией в точке 5 с. Толщину пленок Pb(S,O) оценивали с помощью микроинтерферометра Линника МИИ-4М.
Изучение морфологических характеристик и элементного состава Pb(S,O) проводили на растровом электронном микроскопе JEOL JSM-5900 LV с приставкой для энергодисперсионного анализа. Для исследования оптических свойств пленок Pb(S,O) использовали спектрофотометр Shimadzu UV-3600, съемку спектров светопропускания осуществляли в диапазоне длин волн 200–1850 нм.
Квантово-химические расчеты проводили методом теории функционала электронной плотности (DFT) с использованием остовных псевдопотенциалов типа Трулье–Мартинса и обменно-корреляционным потенциалом в приближении обобщенного градиента по Педью–Бурке–Эрнцерхофу (GGA PBE), как имплементировано в программе SIESTA 4.0 для периодических систем [13]. Валентные состояния соответствовали O2s22p4, S3s23p4, Pb5d106s26p2 с волновыми функциями в базисе двухэкспонентных псевдоорбиталей с введением поляризационных функций. Расчетная схема воспроизводит параметры решеток ГЦК-PbS и α-PbO с погрешностью менее 2% и характеризует эти соединения как прямозонный (L-L) и непрямозонный (Г-М) полупроводники с Eg = 0.47 и 1.29 эВ соответственно.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Образование сульфидной пленки в щелочной среде описывается реакцией
(1)
$\begin{gathered} {\text{PbL}}_{x}^{{2 + k}} + {{{\text{N}}}_{{\text{2}}}}{{{\text{H}}}_{{\text{4}}}}{\text{CS}} + 2{\text{О}}{{{\text{Н}}}^{ - }} = \\ = {\text{PbS}}{\kern 1pt} \downarrow + \;х{{{\text{L}}}^{k}} + {{{\text{H}}}_{{\text{2}}}}{\text{C}}{{{\text{N}}}_{2}} + 2{{{\text{H}}}_{{\text{2}}}}{\text{O}}, \\ \end{gathered} $Связывание свинца в комплексы осуществляется для замедления процесса образования PbS и создания условий зарождения и формирования однородной пленки. Природа лиганда определяет прочность комплексной формы PbL$_{x}^{{2 + k}}$ и влияет на скорость, механизм процесса пленкообразования, фазовый состав и толщину слоя. Реакция (1) протекает в условиях значительных пересыщений ∆. Величину пересыщения ∆ для различных составов растворов при образовании осадка PbS находили как отношение ионного произведения (ПИ) к произведению растворимости (ПР) PbS: ∆ = ПИ/ПР. Для расчета ПИ использовали термодинамический подход, разработанный на кафедре физической и коллоидной химии УрФУ, в основе которого лежит представление о гидролитическом распаде тиомочевины N2H4CS в водных щелочных растворах с образованием слабой сероводородной кислоты [14]. При расчете величины ∆ использовали справочные термодинамические константы устойчивости комплексных ионов свинца, константы ионизации сероводородной кислоты, экспериментально найденные значения константы разложения N2H4CS. Рассчитанные значения ∆ для выбранных систем составляли (1.43–4.04) × 106.
По данным энергодисперсионного анализа пленок Pb(S,O) наиболее близкими к стехиометрическому соотношению основных элементов Pb : S = 0.99 являются пленки, полученные из аммиачно-цитратной системы. В этих пленках содержание кислорода менее 0.5 ат. %. В остальных пленках наблюдается присутствие атомов кислорода в количестве от 13.76 до 30.68 ат. % (табл. 1).
На рис. 1 продемонстрировано разнообразие форм агломератов и частиц, из которых сформированы пленки Pb(S,O). Пленки представляют собой либо скопления крупных агрегатов частиц, сформированных, в свою очередь, из более мелких фракций (гидроксидно-цитратная система), либо образования кристаллитов с четкой огранкой (аммиачно-цитратная и этилендиамин-цитратная системы). Форма и размеры частиц зависят от природы используемого лиганда в реакционной смеси (рис. 1). Толщина пленки уменьшается от 590 до 270 нм при возрастании содержания О от 0 до 30.68 ат. % (табл. 1).
Рис. 1.
Микрофотографии пленок Pb(S,O), полученных из водных щелочных растворов N2H4CS c использованием различных лигандов; 1–4 – соответствуют номерам систем в табл. 1.

На рентгенограммах синтезированных пленок (рис. 2) из-за их малой толщины присутствуют отражения как основной фазы – кубического PbS (В1, пр. гр. Fm-3m), так и дополнительные рефлексы от ситалловой подложки, интенсивности которых определяются пропусканием слоев. Пленки, синтезированные из гидроксидной и аммиачно-цитратной систем, имеют основной максимум интенсивности рентгеновских отражений на угле 2θ = 25.9°, характерном для роста кристаллитов кубического PbS в направлении [111]. Для слоев из гидроксидно-цитратной системы наблюдается преимущественная ориентация кристаллитов в направлении [200]. Равновероятная ориентация кристаллитов вдоль направлений [111] и [200] характерна для пленок, полученных из этилендиамин-цитратной системы, что согласуется с данными электронной микроскопии (рис. 1).
Рис. 2.
Рентгенограммы и рассчитанные значения периода кубической кристаллической решетки пленок Pb(S,O); 1–4 – соответствуют номерам систем в табл. 1.
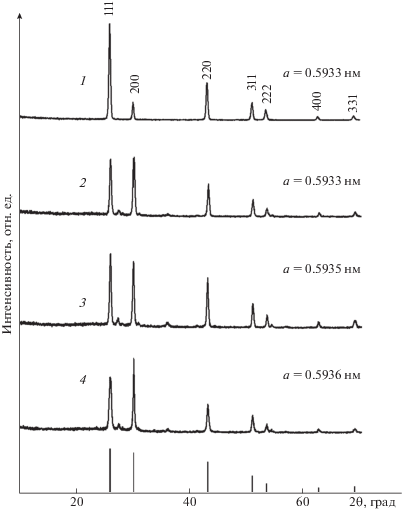
Оценку размеров областей когерентного рассеивания (ОКР) в пленках Pb(S,O) (табл. 1), которая численно равна среднему размеру кристаллитов 〈D〉, проводили по традиционной формуле Шерера 〈D〉 = 0.9λ/β*cos θs = 0 при экстраполяции зависимости приведенного уширения β* на значение вектора рассеяния s = 0. Размер 〈D〉 в сульфидных пленках варьируется от 61 до 290 нм, при этом наибольшая величина 〈D〉 наблюдается для пленок, практически не содержащих кислорода (табл. 1). Рассчитанные значения параметра a кристаллической решетки сульфида свинца в изученных пленках приведены на рис. 2. Наблюдаемые значения параметра a в пленках Pb(S,O) практически совпадают с величиной a для монокристаллического PbS (0.5935 нм).
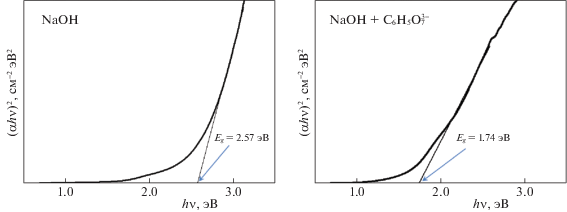
Оптическую ширину запрещенной зоны Eg осажденных пленок Pb(S,O) определяли из соотношения для случая прямых разрешенных переходов
где α – коэффициент поглощения; $h\nu $ – энергия падающих фотонов; C – постоянная, зависящая от показателя преломления, эффективной массы электрона. Величину Eg определяли путем экстраполяции линейного участка зависимости квадрата произведения коэффициента поглощения на энергию фотонов ($\alpha h\nu $)2 от энергии фотонов $h\nu $ на ось абсцисс (рис. 3).Точные значения Eg для пленок Pb(S,O) определить не удается, поскольку использованная область измерений (200–1850 нм) недостаточна для регистрации края полосы поглощения пленки PbS, который, вероятно, находится при длинах волн больше, чем 1850 нм. Можно лишь утверждать, что Eg для PbS в изученных пленках не превышает 0.7 эВ.
В данной работе было обнаружено, что на спектрах оптического поглощения пленок Pb(S,O) с содержанием кислорода от 16.8 до 30.7 ат. % имеются перегибы (рис. 3), свидетельствующие о наличии еще одной фазы, не определяемой методом рентгеновской дифракции. Экспериментальные значения Eg для этой фазы составляют 2.57 и 1.74 эВ соответственно, что существенно превышает значение Eg = 0.41–0.42 эВ для крупнокристаллического PbS. Значительное увеличение Eg невозможно интерпретировать с привлечением квантового ограничения самого PbS, так как такие Eg должны соответствовать наночастицам PbS диаметром 2–2.5 нм [15], что существенно меньше, чем размеры наночастиц ∼60–190 нм (табл. 1) в синтезированных пленках. В связи с этим было предположено, что наблюдаемые увеличения значений Eg до ∼2.6 эВ в пленках Pb(S,O) обусловлены наличием посторонних фаз, в частности, кислородсодержащих, с учетом высокого содержания кислорода, зарегистрированного методом энергодисперсионного анализа (табл. 1).
Рентгеноструктурные методы не обнаружили присутствия сторонней индивидуальной фазы, что свидетельствует либо об аморфности ее решетки, либо о наноразмерности. В условиях химического осаждения, использованных в данной работе, наиболее вероятным соединением является наноразмерный оксид свинца (II) PbO: согласно экспериментальным данным, его кристаллическая форма имеет Eg ∼ 1.9 эВ, а мономолекулярный слой толщиной 0.26 нм имеет Eg ∼ 2.2 эВ в виду квантового ограничения [16]. Это значение Eg по порядку величины уже близко к значениям Eg для кислородсодержащих образцов PbS.
Для определения наиболее вероятного распределения атомов кислорода в структуре соединения Pb(S,O) с привлечением DFT-расчетов рассмотрены два типа соединений Pb(S,O): твердые растворы замещения PbS1 – xOx с x = 0.03–0.5 и разным распределением O и гетероструктуры α-PbO||ГЦК-PbS с разной толщиной компонентов и ориентацией поверхностей и формальным x = = 0.2–0.5. Все соединения оказались метастабильными относительно механической смеси ГЦК-PbS и α-PbO. Однако энергии образования PbS1 – xOx всегда оказывались более высокими (>0.6 эВ/O-атом) в сравнении с PbO||PbS (0.1–0.4 эВ/O-атом). Это обусловлено большим различием в длинах связей Pb–O и Pb–S (2.4 и 3.0 Å) и как следствие сильными напряжениями решетки PbS1 – xOx. Согласно расчетам, напряжение может быть существенно нивелировано выделением атомов O и S в индивидуальные фазы, например, в составе гетероструктур PbO||PbS. Образованию гетероструктур благоприятствует и низкая несоразмерность их интерфейсов, не превышающая 4% уже для случая контакта малых ячеек √2a × × √2a PbS и 2a × 2a PbO.
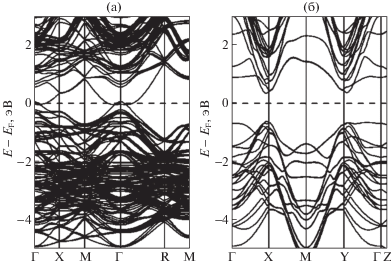
Наличие границ раздела PbO||PbS в образцах Pb(S,O) подтверждается также сравнением теоретического и экспериментального изменения Egдля кристаллического PbS. Модели твердых растворов PbS1 – xOx обладают мéньшими Eg, чем для PbS, и, тем более, для синтезированных пленок согласно данным по оптическому поглощению (рис. 4). Часть Pb6p-состояний из зоны проводимости PbS понижает свою энергию и даже перекрывается с потолком валентной зоны со схлопыванием запрещенной щели в зависимости от содержания и распределения атомов O в PbS1 – xOx. Напротив, все рассмотренные модели гетероструктур PbO||PbS обладают более высокими Eg = = 0.8–1.4 эВ в сравнении с Eg для PbS (рис. 4). Запрещенная щель таких соединений Pb(S,O) может быть отнесена к типу II со слабым доминированием O2p-состояний слоя PbO у потолка широкой валентной зоны и дном зоны проводимости, составленным преимущественно Pb6p-состояниями слоя PbS.
Рис. 4.
Зонная структура разных соединений Pb(S,O): твердого раствора PbS0.75O0.25 (a) и гетероструктуры 1PbO||3PbS (б), расчеты DFT GGA.
Таким образом, теоретические расчеты показывают, что основой наночастиц в пленках Pb(S,O) не могут быть твердые растворы, а сульфидная пленка, содержащая от 15.2 до 30.7 ат. % кислорода, представляет собой материал на основе гетероструктурных соединений PbO||PbS. Дополнительно с учетом данных элементного анализа (табл. 1), можно предполагать, что поверхность PbS частично подвергается процессам окисления с образованием фазы xPbS · PbSO4 (x = = 3.5–11.5), которая также является аморфной и не определяется рентгено-дифракционным методом. Проведенный DFT-расчет свойств сульфата свинца PbSO4 (в модификации англезита) показал, что величина Eg этого соединения составляет 4 эВ, т.е. PbSO4 является полупроводником с широкой Eg и прозрачным соединением в видимой части оптического спектра.
Образование границ PbO||PbS в водном растворе идет, вероятно, по ионному механизму. Этот механизм предполагает образование зародышей твердой фазы и последующее формирование кластеров этой фазы непосредственно на подложке, а адгезия твердой фазы к подложке в общем случае обеспечивается силами Ван-дер-Ваальса [8, 10]. Химический состав образующихся зародышей и кластеров определяется условиями синтеза и в данной системе представляет собой гидратированный оксид свинца (II) PbO · · H2O. В этом случае помимо основной реакции сульфидообразования (1) идут реакции образования зародышей:
(3)
$m{\text{P}}{{{\text{b}}}^{{2 + }}} + 2m{\text{О}}{{{\text{Н}}}^{--}} \to {{({\text{PbO}} \cdot {{{\text{H}}}_{{\text{2}}}}{\text{O}})}_{m}}$(4)
${\text{PbO}} \cdot {{{\text{H}}}_{{\text{2}}}}{{{\text{O}}}_{m}} + {\text{PbO}} \cdot {{{\text{H}}}_{{\text{2}}}}{{{\text{O}}}_{n}} \to {{({\text{PbO}} \cdot {{{\text{H}}}_{{\text{2}}}}{\text{O}})}_{{m + n}}},$(5)
$\begin{gathered} 2{\text{PbO}} \cdot {{{\text{H}}}_{{\text{2}}}}{\text{O}} + {{({\text{N}}{{{\text{H}}}_{{\text{2}}}})}_{2}}{\text{CS}} \to \\ \to 2{\text{PbO}} \cdot {{({\text{N}}{{{\text{H}}}_{2}})}_{2}}{\text{CS}} + 2{{{\text{H}}}_{{\text{2}}}}{\text{O}}, \\ \end{gathered} $(6)
$2{\text{PbO}} \cdot {{({\text{N}}{{{\text{H}}}_{{\text{2}}}})}_{2}}{\text{CS}} \to {\text{PbO}}\,|{\kern 1pt} |\,{\text{PbS}} + {{{\text{H}}}_{{\text{2}}}}{\text{C}}{{{\text{N}}}_{2}} + {{{\text{H}}}_{{\text{2}}}}{\text{O}},$ЗАКЛЮЧЕНИЕ
Таким образом, методом химического осаждения из водных щелочных растворов с использованием различных лигандов для катионов Pb2+ получены сульфидные нанокристаллические пленки Pb(S,O) с разным содержанием кислорода. Показано, что с увеличением содержания кислорода от 0.23 до 30.68 ат. % не только уменьшаются толщина пленки и размер кристаллитов, но и меняется их форма: кристаллы теряют какую-либо четкую огранку. Величина оптической ширины запрещенной зоны при этом возрастает и достигает 2.57 эВ. Квантово-химические расчеты позволили определить распределение атомов кислорода в структуре соединения Pb(S,O) и предположить стадийный механизм формирования пленки. Согласно полученным результатам, выращенные на подложке пленки состава Pb(S,O) представляют собой гетероструктурные соединения PbO||PbS, в которых поверхность оксида PbO непосредственно связана с подложкой, а образование PbS происходит за счет реакции сульфидизации PbO. При этом экспериментально наблюдаемое увеличение оптической ширины запрещенной зоны PbS при введении O должно быть приписано эффекту квантового ограничения, как возникающему исключительно благодаря наноразмерной внутренней организации кристаллической решетки Pb(S,O), а не субмикронным размерам самих наночастиц Pb(S,O) или PbS. Вероятно, поверхность PbS также может подвергаться процессам окисления с образованием фазы xPbS · · PbSO4. Установленные закономерности влияния природы лиганда на элементный состав пленок Pb(S,O) позволят контролировать процесс роста пленки, прогнозировать ее морфологию, кристаллическую структуру и оптические свойства. В дальнейшем с помощью просвечивающей электронной микроскопии и рентгеновской дифракции под скользящим пучком планируется провести детальные исследования кинетики формирования гетероструктур PbO||PbS на подложках с целью уточнения механизмов реакций их образования.
Работа выполнена при финансовой поддержке программы 211 Правительства Российской Федерации № 02.А03.21.0006. Оптические исследования и квантово-химические расчеты выполнены в рамках плановых заданий НИР ИХТТ УрО РАН.
Список литературы
Cheragizade M., Yousefi R., Jamali-Sheini F. et al. // Materials Science in Semiconductor Processing. 2014. V. 26. P. 704. https://doi.org/10.1016/j.mssp.2014.08.026
Smith D.K., Luther J.M., Semonin O.E. et al. // ACS Nano. 2011. V. 5. № 1. P. 183. https://doi.org/10.1021/nn102878u
Park B. // Thin Solid Films. 2014. V. 550. P. 696. https://doi.org/10.1016/j.tsf.2013.11.070
Li J., Tang Y., Yang J. et al. // Sensors and Actuators B: Chemical. 2014. V. 190. P. 549. https://doi.org/10.1016/j.snb.2013.09.046
Patel J., Mighri F., Ajji A. et al. // Applied Physics A. 2014. V. 117. № 4. P. 1791. https://doi.org/10.1007/s00339-014-8659-x
Kumar S., Sharma T.P., Zulfequar M., Husain M. // Physica B: Condensed Matter. 2003. V. 325. P. 8. https://doi.org/10.1016/S0921-4526(02)01272-3
Preetha K.C., Murali K.V., Ragina A.J. et al. // Current Applied Physics. 2012. V. 12. № 1. P. 53. https://doi.org/10.1016/j.cap.2011.04.040
Sarica E., Bilgin V. // Materials Science in Semiconductor Processing. 2017. V. 71. P. 42. https://doi.org/10.1016/j.mssp.2017.07.007
Khan M.D., Hameed S., Haider N. et al. // Materials Science in Semiconductor Processing. 2016. V. 46. P. 39. https://doi.org/10.1016/j.mssp.2016.02.002
Маскаева Л.Н., Марков В.Ф., Сарыева Р.Х., Шемякина А.И. // Журн. прикл. химии. 2015. Т. 88. № 9. С. 1271.
Baruah B.J., Sarma K.C. // J. Materials Science: Materials in Electronics. 2017. V. 28. № 8. P. 5913. https://doi.org/10.1007/s10854-016-6265-8
Du X., Wang Y., Shi R. et al. // J. Eur. Ceram. Soc. 2018. V. 38. № 10. P. 3512. https://doi.org/10.1016/j.jeurceramsoc.2018.03.046
Ordejon P., Artacho E., Soler J.M. // Phys. Rev. B. 1996. V. 53. R10441. https://doi.org/10.1103/PhysRevB.53.R10441
Марков В.Ф., Маскаева Л.Н. //Журн. физ. химии. 2010. Т. 84. № 8. С. 1421.
Segets D., Lucas J.M., Taylor R.N.K. et al. // ACS Nano. 2012. V. 6. № 10. P. 9021. https://doi.org/10.1021/nn303130d
Bakhtatou A., Ersan F. // Phys. Chem. Chem. Phys. 2019. V. 21. P. 3868. https://doi.org/10.1039/C8CP07327A
Елисеев А.А., Лукашин А.В. Функциональные наноматериалы / Под ред. Ю.Д. Третьякова. М.: Физматлит, 2010. 456 с.
Goger S., Hodes G. // J. Phys. Chem. 1994. V. 98. P. 5338. https://doi.org/10.1021/j100071a026
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии