Журнал физической химии, 2020, T. 94, № 12, стр. 1871-1876
Термохимический анализ межфазного взаимодействия в композитах, содержащих нанодисперсные порошки Al и Al2O3
Т. В. Терзиян a, *, А. П. Сафронов a, b, Э. Р. Заляева a, И. В. Бекетов a, b, Н. В. Лакиза a
a Уральский федеральный университет им. первого Президента России Б.Н. Ельцина
620002 Екатеринбург, Россия
b Российская академия наук, Уральское отделение, Институт электрофизики
Екатеринбург, Россия
* E-mail: Tatiana.Terzian@urfu.ru
Поступила в редакцию 03.03.2020
После доработки 25.03.2020
Принята к публикации 14.04.2020
Аннотация
Методом изотермической микрокалориметрии изучено межфазное взаимодействие в композитных пленках на основе электронодонорного (полистирола) и электроноакцепторного (поливинилхлорида) полимеров, содержащих нанодисперсные порошки Al и Al2O3, полученных методом электрического взрыва проволоки. По величинам энтальпии адгезии в композитах, а также энтальпии смачивания дисперсных порошков растворителями различной химической природы установлено, что поверхность Al2O3 в межфазном взаимодействии проявляет преимущественно электроноакцепторные свойства, тогда как поверхность Al и акцепторные, и донорные свойства. Результаты калориметрических исследований согласуются с данными ИК-спектроскопического изучения композитных пленок.
Сочетание нанодисперсных порошков металлов или их оксидов и полимерных матриц позволяет получать уникальные композиционные материалы с ценными физико-химическими свойствами. Как правило, полимерная матрица обеспечивает такие характеристики как низкая плотность, коррозионная стойкость и технологичность, а дисперсный наполнитель функциональность и прочность. Кроме природы самих компонентов, свойства композитного материала определяются межфазным интерфейсом, а именно адгезионным взаимодействием на границе раздела фаз, приводящим к структурированию полимера и формированию граничных слоев. В этой связи, изучение межфазного взаимодействия актуально, как для понимания механизмов структурирования материалов, так и их практического применения.
В течение ряда лет на базе Уральского федерального университета проводятся исследования термодинамики многокомпонентных полимерных систем [1–3], в том числе композитных материалов, где полимерная матрица сочетается с нанопорошками неорганических веществ [4, 5]. Разработан и хорошо апробирован термохимический подход, позволяющий оценить величину энтальпии адгезии и структурные изменения полимера [6]. Круг изучаемых систем был значительно расширен в рамках сотрудничества с Институтом электрофизики УрО РАН, где для получения нанопорошков применяется метод электрического взрыва проволоки (ЭВП) [7–10]. Метод заключается в испарении металлической проволоки высоковольтным электрическим разрядом в заданной атмосфере и последующей конденсацией паров в наночастицы сферической формы. Вариацией параметров реализации метода ЭВП можно получать наночастицы металлов и их оксидов различной дисперсности.
Особый интерес представляет исследование полимерных композитных систем, содержащих ЭВП наночастицы Al и Al2O3. Оксид алюминия характеризуется высокой теплопроводностью, низким коэффициентом теплового расширения, высоким модулем упругости, низкой диэлектрической проницаемостью и относительно низкой ценой по сравнению с другими керамическими наполнителями. В литературе имеется большое число работ, где описано исследование композитов с наночастицами Al2O3 в различных полимерных матрицах. Так, приводятся результаты исследования систем на основе полиэтилена [11], полипропилена [12], полиэтиленгликоля [13], полиимида [14], поливинилбутираля [15], поликарбоната [16], полиметилметакрилата [17] и других полимеров. Наночастицы алюминия также рассматриваются как наполнители для полимеров с целью создания материалов с повышенной теплопроводностью [18], электропроводностью [19], топливных систем [20, 21].
В данной работе были изучены композитные пленки, содержащие ЭВП наночастицы Al и Al2O3 в сочетании с широко используемыми промышленными полимерами – полистиролом (ПС) и поливинилхлоридом (ПВХ). Эти полимеры были выбраны в качестве объектов исследования, не только как имеющие большую практическую значимость, но и как среды с потенциально возможным электронодонорноакцепторным (ЭДА) взаимодействием на границе раздела фаз.
ЭКПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Наполненные полимерные композиты получали на основе промышленных образцов ПС и ПВХ марки С-55. Молекулярные массы полимеров были рассчитаны по данным вискозиметрических измерений [22] растворов в толуоле для ПС и в циклогексаноне для ПВХ, и составили 2.6 × 105 и 5.9 × 105, соответственно. В качестве наполнителей полимерных композитных пленок использовали порошки Al и Al2O3, полученные в лаборатории импульсных процессов Института электрофизики УрО РАН методом электрического взрыва алюминиевой проволоки [7], в инертной среде для металлического порошка или в окислительной среде для его оксида.
Рентгенофазовый анализ (РФА) порошков Al и Al2O3 проводили с помощью дифрактометра D8 ADVANCE (Bruker) с использованием CuKα излучения (λ = 1.5418 Å), графитового монохроматора и сцинтилляционного детектора. При обработке рефлексов использовали метод полнопрофильного анализа Ритвельда, реализованный во встроенном программном обеспечении TOPAS-3. Согласно данным РФА частицы алюминия однофазны – металл с кубической решеткой пространственной группы Fm-3m (PDF 00-004-0787) с периодом a = 4.050(2) Å и областью когерентного рассеяния (ОКР) 123(5) нм. Частицы Al2O3 содержат две фазы: 20 мас. % γ-Al2O3 c кубической решеткой пространственной группы Fd-3m (PDF 00-050-0741) с периодом a = 7.90(2) Å и 80 мас. % δ-Al2O3 с тетрагональной решеткой пространственной группы Р43212 (PDF 00-047-1770) с периодами a = 7.95(2) Å и c = 23.4(6) Å, ОКР = = 22 нм.
На рис. 1 приведены микрофотографии порошков Al и Al2O3, полученные на просвечивающем электронном микроскопе “JEOL JEM 2100”. Частицы порошков имеют сферическую форму, их размер лежит в интервале 50–200 и 10–100 нм, для алюминия и оксида соответственно.
Удельная поверхность порошков была определена объемным вариантом метода БЭТ [23] по низкотемпературной равновесной сорбции азота на вакуумной установке “Micrometrics TriStar 3000” и составила Sуд = 18.1 м2/г для алюминия и Sуд = 50.0 м2/г для оксида алюминия. Сферический размер частиц позволяет использовать известное уравнение [24]: d = 6/(Sудρ), для расчета среднего эффективного размера частиц (d), где ρ – плотность материала, равная 2.7 и 3.6 г/см3 для Al и Al2O3 соответственно. Рассчитанные значения среднего размера составили 123 нм для частиц Al и 33 нм для частиц Al2O3, что согласуется с данными электронной микроскопии и величинами ОКР.
Композитные пленки на основе полимерных матриц и дисперсных порошков получали методом полива из суспензий, диспергированных ультразвуком (УЗ-дезинтегратор “Cole Palrmer CPX 750”) на тефлоновую поверхность с последующим удалением растворителя. В качестве растворителей были выбраны толуол для композитов ПС и тетрагидрафуран для ПВХ. Подробная методика получения композитных пенок описана ранее [4, 5, 25]. Таким образом, были получены четыре системы, отличающиеся природой порошка и полимера: ПС/Al; ПС/Al2O3; ПВХ/Al и ПВХ/Al2O3, где содержание дисперсного порошка варьировалось от 10 до 90 мас. %.
Энтальпия адгезии частиц к матрице в пленочных композитах была исследована методом микрокалориметрии [26] на приборе ДАК-1 с изотермической оболочкой и чувствительностью 90 мВ/мВт. Изотермическая оболочка калориметра термостатирована при 298 ± 0.1 K. Экспериментально измеряли тепловые эффекты растворения наполненных композиций в выбранных растворителях. Для этого в стеклянную тонкостенную калориметрическую ампулу помещали навеску композита ∼0.04–0.08 г, ампулу запаивали и помещали в калориметрическую камеру, содержащую ∼5 мл растворителя. В процессе калориметрического опыта ампулу разбивали внутри камеры и регистрировали тепловой эффект процесса растворения полимерной составляющей. Кроме этого, измеряли тепловые эффекты процесса смачивания порошка и растворения пленки полимера. Абсолютная погрешность калориметрических измерений, по данным электрической калибровки прибора, составляла ±0.02 Дж. Измеряемые тепловые эффекты составляли не менее 0.4 Дж, так что относительная погрешность измерений не превышала 5%.
ИК-спектры композитных пленок были получены в диапазоне волновых чисел 4000–500 см–1 с помощью ИК-фурье-спектрометра Nicolet 6700, оснащенного приставкой НПВО.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Адгезионное взаимодействие в композитных пленках было изучено методом микрокалориметрии в изотермических условиях, и экспериментально измеряемыми величинами были значения энтальпии процессов, входящих в термохимический цикл. Основы термохимического анализа наполненных полимерных систем были заложены в классических работах А.А. Тагер с сотр. [27, 28], где был предложен термохимический цикл расчета энтальпии процесса смешения полимерной матрицы с наполнителем (ΔНm), в ходе которого формируется композиция определенного состава. В данном исследовании был использован вариант термохимического цикла, подробно описанный в работах [4, 6], где экспериментально измеряемыми величинами являются: энтальпия растворения полимера (ΔН1), энтальпия смачивания частиц порошка (ΔН2), и энтальпии растворения композитов, а именно полимерной составляющей композитов, (ΔН3) различного состава в одном и том же растворителе.
На рис. 2 приведены концентрационные зависимости величины ΔН3, для четырех систем, отличающихся природой порошка и полимера. Все экспериментально измеренные тепловые эффекты выражены в Джоулях на грамм навески, использованной в калориметрическом эксперименте.
Рис. 2.
Концентрационные зависимости энтальпии растворения композиций: 1 – ПС/Al, 2 – ПС/Al2O3 в толуоле, 3 – ПВХ/Al, 4 – ПВХ/Al2O3 в циклогексаноне. Т = 298 K. Точки на графике соответствуют экспериментальным измерениям, линии интерполяции приведены для наглядности.
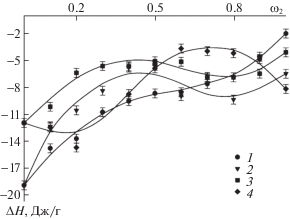
Абсцисса каждой точки соответствует массовому содержанию порошка в композиции, ордината – тепловому эффекту растворения композиции. Точки при ω2 = 1 отвечают теплоте смачивания порошков Al и Al2O3 толуолом и циклогексаноном, т.е. ΔН2, а точки при ω2 = 0 теплоте растворения полимеров, т.е. ΔН1. Растворение полимеров сопровождается большими экзотермическими эффектами. Действительно, оба полимера в условиях калориметрического опыта, т.е. при 298 K, находятся в стеклообразном релаксационном состоянии. Известно [1, 29], что тепловые эффекты растворения стеклообразных полимеров принимают большие отрицательные значения за счет разрушения неравновесной структуры стекла при растворении. На основании экспериментальных данных в соответствии с уравнением термохимического цикла:
(1)
$\Delta {{H}_{m}} = {{\omega }_{1}}\Delta {{H}_{1}} + {{\omega }_{2}}\Delta {{H}_{2}}--\Delta {{H}_{3}},$Зависимости энтальпии смешения от массовой доли порошка представлены на рис. 3.
Рис. 3.
Концентрационные зависимости энтальпии смешения полимера с порошком 1 – ПС/Al, 2 – ПС/Al2O3, 3 – ПВХ/Al, 4 – ПВХ/Al2O3. Точки – рассчитанные значения энтальпии смешения. Кривые – результат аппроксимации уравнением (2).
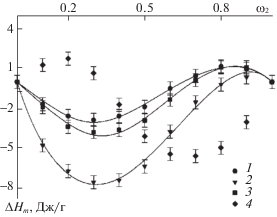
Как видно из рис. 3 концентрационные зависимости энтальпии смешения полимеров с порошками Al и Al2O3 для всех систем имеют сложный знакопеременный характер, и их положение зависит от природы компонентов системы. Для систем ПС/Al, ПС/Al2O3 и ПВХ/Al наблюдаются положительные значения энтальпии смешения в области высокого содержания порошка, и отрицательные в области малого содержания. Такой вид зависимостей согласуется с ранее полученными данными для ряда наполненных полимерных систем в стеклообразном релаксационном состоянии, и хорошо описывается термодинамической моделью, предложенной в работе [6]. Так, в рамках рассматриваемой модели, предполагается формирование адгезионного контакта на границе раздела фаз в наполненной полимерной композиции, которое сопровождается выигрышем энергии. Адгезионные контакты ограничивают подвижность макромолекул, что приводит к увеличению доли метастабильных вакансий в граничном слое полимера и может рассматриваться как усиление неравновесной стеклообразной структуры полимера, что в свою очередь, является энергетически не выгодным. Таким образом, на величину теплового эффекта смешения действуют два фактора противоположной направленности: межфазное адгезионное взаимодействие и структурирование полимера. В этой связи, в рамках модели, величина энтальпии смешения описывается суммой двух слагаемых, каждое из которых определяет вид концентрационной зависимости соответствующего фактора:
(2)
$\begin{gathered} \Delta {{H}_{m}} = \Delta H_{{{\text{адг}}}}^{\infty }\frac{{K(1 - {{\omega }_{2}}){{\omega }_{2}}{{S}_{{{\text{уд}}}}}}}{{K(1 - {{\omega }_{2}}) + {{\omega }_{2}}{{S}_{{{\text{уд}}}}}}} - \\ - \;\frac{{{{\varepsilon }_{{22}}}}}{{{{M}_{{{\text{зв}}}}}}}{{\varphi }_{1}}\gamma \exp \left( { - \frac{{1 - {{\omega }_{2}}}}{{{{\omega }_{2}}{{S}_{{{\text{уд}}}}}}}{{d}_{2}}{{l}_{0}}} \right), \\ \end{gathered} $Как показано в работе [6], уравнение (2) описывает концентрационную знакопеременную зависимость энтальпии смешения, где отрицательные значения ΔНm наблюдаются в области малого содержания наполнителя, а положительные – в области большого. Используя уравнение (2) для систем ПС/Al, ПС/Al2O3 и ПВХ/Al был произведен расчет величины энтальпии адгезии, константы адсорбции, степени увеличения вакансий и толщины адсорбционного слоя методом аппроксимации концентрационных зависимостей энтальпии смешения, приведенных на рис. 2. Рассчитанные значения приведены в табл. 1.
Таблица 1.
Рассчитанные значения параметров* межфазного взаимодействия и изменения стеклообразной структуры полимера для композитных пленок
| Образец | –$\Delta H_{{{\text{адг}}}}^{\infty }$, Дж/м2 | K | γ | l0 , нм |
|---|---|---|---|---|
| ПС/Al | 1.18 | 7.3 | 0.032 | 31 |
| ПС/Al2O3 | 1.27 | 15.7 | 0.033 | 11 |
| ПВХ/Al | 1.32 | 9.9 | 0.036 | 19 |
Из табл. 1 видно, что для всех трех систем, несмотря на значительную разницу в химическом составе, как энтальпия адгезии, так и параметры изменения стеклообразной структуры полимера принимают близкие значения. Большие отрицательные значения энтальпии адгезии свидетельствуют о сильном межфазном взаимодействии. Протяженность граничного слоя, где доля вакансий превышает средние значения для объема полимера, составляет от 10 до 30 нм. Концентрационная зависимость энтальпии смешения компонентов системы ПВХ/Al2O3 также имеет знакопеременный вид, но, отличающийся от трех выше рассмотренных. При низком содержании наполнителя энтальпия принимает положительные значения, и отрицательные при большом содержании. Такой вид зависимости может быть обусловлен адгезионным взаимодействием и структурированием на границе раздела фаз, механизм которого не описывается термодинамической моделью, предложенной в работе [6].
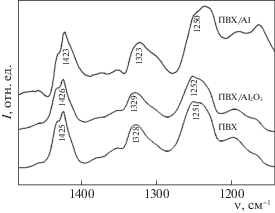
Особое поведение системы ПВХ/Al2O3 также наблюдается в ИК-спектрах композитных пленок. Макромолекулы ПВХ и ПС проявляют себя в ИК-спектрах полосами поглощения, характерными для связей C–C и C–H, в различных функциональных группировках. Для ПВХ обнаруживается интенсивная полоса 609 см–1, отвечающая колебаниям С–Cl, но ее идентификация для композитов затруднена, вследствие интенсивного поглощения порошками Al и Al2O3 в области волновых чисел менее 1000 см–1. Сопоставление спектров индивидуальных полимеров и композитов позволяет установить следующую закономерность: все полосы характерные для полимеров, проявляют себя для композитных пенок, но их положение смещается на величину 2–5 см–1, причем для систем ПС/Al, ПС/Al2O3 и ПВХ/Al в сторону меньших значений, а для системы ПВХ/Al2O3 в сторону больших. Уменьшение частоты ИК-излучения, при которой наблюдаются колебания функциональной группы, может быть связано с уменьшением подвижности звеньев макромолекул, участвующих в формировании адгезионных контактов с поверхностью наночастиц. Уменьшение подвижности макромолекул в системах ПС/Al, ПС/Al2O3 и ПВХ/Al коррелирует с большими отрицательными значениями энтальпии адгезии. Описанную закономерность подтверждают ИК-спектры пленок ПВХ, ПВХ/Al и ПВХ/Al2O3 (рис. 4) в области 1500–1100 см–1, поглощение в которой обусловлено деформационными колебаниями группы СН2.
Для получения дополнительной информации о природе сил формирующих межфазные контакты на поверхности частиц Al и Al2O3 были изменены значения энтальпии смачивания порошков жидкостями, характеризующимися различными видами межмолекулярного взаимодействия. Были измерены значения энтальпии смачивания водой и определена степень гидрофильности поверхности по величине параметра Ребиндера (R):
Кроме этого, использовали полярный растворитель этилацетат, молекулы которого имеют высокое значение дипольного момента, но не образуют водородные связи. Также были использованы растворители с высоким значением донорного (N,N-диметилацетамид) и акцепторного (1,2-дихлорэтан) чисел. Измеренные значения энтальпии смачивания, отнесенные к единице площади поверхности нанопорошка, а также физико-химические константы растворителей приведены в табл. 2.
Таблица 2.
Энтальпии смачивания (ΔНсм) порошков Al и Al2O3 различными жидкостями и физико-химические константы жидкостей
| Образец | $--\Delta {{Н}_{{{\text{см}}\;{\text{Al}}}}}$, Дж/м2 | $--\Delta {{Н}_{{{\text{см}}\;{\text{A}}{{{\text{l}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}}}}}$, Дж/м2 | μ, D | ND | NA |
|---|---|---|---|---|---|
| Этилацетат | 0.27 | 0.25 | 1.81 | 17.1 | – |
| Гексан (С6Н14) | 0.01 | 0.06 | 0.08 | – | – |
| ДМАА | 0.34 | 0.30 | 3.79 | 27.8 | 13.6 |
| Н2О | 0.42 | 0.21 | 1.84 | 18.0 | 54.8 |
| 1,2-Дихлорэтан | 0.44 | 0.18 | 1.75 | – | 23.1* |
Обозначения: μ – дипольный момент, ND – донорное число, NA – акцепторное число. Хлорсодержащие соединения проявляют электроноакцепторную способность [30], связанную с наличием свободных d-орбиталей атомов хлора. В таблице, для примера, приведено значение NA для хлороформа (отмечено звездочкой), так как для использованного в работе 1,2-дихлорэтана таких справочных данных нет.
Известно [31], что поверхность наночастиц металлического алюминия покрыта слоем оксида, который вследствие малой толщины не обнаруживается методом рентгенофазового анализа, но виден на электронных микрофотографиях порошков. Таким образом, если поверхность двух порошков имеет одинаковую химическую природу, то и поверхностное взаимодействие с различными жидкостями можно ожидать одинаковое. В пользу этого свидетельствуют близкие значения энтальпии смачивания порошков этилацетатом, гексаном и диметилацетамидом (ДМАА) приведенные в табл. 2. Существенное различие наблюдается в величинах энтальпии смачивания порошков водой и 1,2-дихлорэтаном, причем для Al тепловые экзотермические эффекты оказались более выраженными, чем для Al2O3. Рассчитанные величины параметра Ребиндера составили 42.0 и 3.5 для Al и Al2O3 соответственно. Хорошая смачиваемость порошка Al водой – известный факт [32], но получить настолько высокое значение параметра Ребиндера для Al оказалось неожиданным. В ряду использованных растворителей, вода и дихлорэтан имеют наибольшие значения акцепторного числа. По-видимому, поверхность наночастиц Al, представляющих собой металлическое ядро и оксидную оболочку, обладает преимущественно электронодонорными свойствами. Такой вывод согласуется с данными работы [33], где установлено, что поверхность Al2O3, модифицированная наночастицами металлического никеля, в отличие от не модифицированной, также обладает электронодонорными свойствами. Акцепторные свойства характерны как для поверхности Al, так и Al2O3, о чем свидетельствуют большие экзоэффекты смачивания электронодонорным ДМАА. В работе [34] указывается на наличие активных центров, проявляющих свойства кислот Льюиса на поверхности оксида алюминия. Именно поверхностный оксидный слой обеспечивает ЭДА связи с ДМАА как для Al2O3, так и для Al.
На границе раздела фаз полимерных композитных пленок также может быть реализовано электронодонорноакцепторное взаимодействие. Матрица полистирола проявляет электронодонорные свойства за счет π-электронов фенильных радикалов. ПВХ, как хлорсодержащий полимер, проявляет электроноакцепторные свойства. Таким образом, каждая из трех систем: ПС/Al, ПС/Al2O3 и ПВХ/Al, состоит как из донорного, так и акцепторного компонента, что обеспечивает межфазное адгезионное взаимодействие. Оба компонента системы ПВХ/Al2O3 проявляют преимущественно акцепторные свойства. Возможно, именно это стало причиной особого поведения системы ПВХ/Al2O3.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (коды проектов 18-08-00178 и 20-48-66044)
Список литературы
Safronov A.P., Adamova L.V. // Polymer. 2002. V. 43. P. 2653. https://doi.org/10.1016/S0032-3861(02)00050-2
Сафронов А.П., Адамова Л.В., Курляндская Г.В. // Высокомолекуляр. соединения. А. 2019. Т. 61. С. 33. https://doi.org/10.1134/S2308112019010152
Терзиян Т.В., Сафронов А.П., Сабирова А.Р. // Журн. физ. химии. 2017. Т. 91. № 7. С. 1155. https://doi.org/10.7868/S0044453717070329
Терзиян Т.В., Сафронов А.П., Петров А.В. и др. // Там же. 2014. Т. 88. № 7–8. С. 1121. https://doi.org/10.7868/S0044453714060351
Kurlyandskaya G.V., Safronov A.P., Terzian T.V. et al. // IEEE Magnetics Letters. 2015. V. 6. P. 38001041. https://doi.org/10.1109/LMAG.2015.2390595
Сафронов А.П., Истомина А.С., Терзиян Т.В. и др. // Высокомолекуляр. соединения. А. 2012. Т. 54. № 3. С. 411.
Котов Ю.А., Бекетов И.В., Саматов О.М. Способ получения сферических ультрадисперсных порошков оксидов активных металлов: Патент РФ № 2033901 // Б. И. 1995. № 12. С. 179.
Багазеев А.В., Котов Ю.А., Медведев А.И. и др. // Российские нанотехнологии. 2010. Т. 5. № 9–10. С. 101.
Kotov Y.A., Beketov I.V., Murzakaev A.M. et al. // Materials Science Forum. Switzerland. Trans Tech Publications. 1996. V. 225-227. P. 913. DOI: 10.4028/www.scientific.net/MSF.225-227.913.
Котов Ю.А., Багазеев А.В., Бекетов И.В. и др. // Журн. технич. физики. 2005. Т. 75. № 10. С. 39.
Liu D., Pallon L.K.H., Pourrahimi A.M. et al. // Eur. Polym. J. 2017. V. 87. P. 255. https://doi.org/10.1016/j.eurpolymj.2016.12.021
Khare P., Verma N. // Polym. Compos. 2017. V. 38. P. E359. https://doi.org/10.1002/pc.23783
Ganapatibhotla L.V.N.R., Maranas J.K. // Macromolecules. 2014. V. 47. P. 3625. https://doi.org/10.1021/ma500072j
Li H., Liu G., Liu B. et al. // Mater. Lett. 2007. V. 61. P. 1507. https://doi.org/10.1016/j.matlet.2006.07.063
Handge U.A., Wolff M.F.H., Abetz V., Heinrich S. // Polymer. 2016. V. 82. P. 337. https://doi.org/10.1016/j.polymer.2015.11.047
Hakimelahi H.R., Hu L., Rupp B.B., Coleman M.R. // Ibid. 2010. V. 51. P. 2494. https://doi.org/10.1016/j.polymer.2010.04.023
Ash B.J., Siegel R.W., Schadler L.S. // Macromolecules. 2004. V. 37. P. 1358. https://doi.org/10.1021/ma0354400
Goyanes S.N., Marconi J.D., König P.G. et al. // Polymer. 2001. V. 42. P. 5267.
Cerveny S., Goyanes S.N., Marzocca A.J., Rubiolo G.H. // Ibid. 1999. V. 40. P. 1495.
DeLisio J.B., Hu X., Wu T. et al. // J. Phys. Chem. B. 2016. V. 120. P. 5534. https://doi.org/10.1021/acs.jpcb.6b01100
Rout A., Pandey P., Oliveira E.F., Autreto P.A. da S. et al. // Polymer. 2019. V. 169. P. 148. https://doi.org/10.1016/j.polymer.2019.02.049
Энциклопедия полимеров / Под ред. В. А. Каргина М.: Советская энциклопедия, 1972. Т. 1–3.
Грег С., Синг К. Адсорбция, удельная поверхность, пористость. М.: Мир, 1984.
Фролов Ю.Г. Курс коллоидной химии. М.: Химия, 1988. 464 с.
Терзиян Т.В., Сафронов А.П., Петров А.В. и др. // Высокомолекуляр. соединения. А. 2014. Т. 56. № 1. С. 69. https://doi.org/10.7868/S2308112014010106
Кальве Э., Прат А. Микрокалориметрия. М.: Изд-во иностр. лит., 1963. 478 с.
Тагер А.А., Юшкова С.М., Бессонов Ю.С. и др. // Высокомолекуляр. соединения. А. 1979. Т. 21. № 5. С. 1051.
Юшкова С.М., Тагер А.А., Бессонов Ю.С. и др. // Там же. 1982. Т. 24. № 7. С. 1373.
Сафронов А.П., Адамова Л.В. // Там же. 2002. Т. 44. № 4. С. 655.
Тагер А.А. Основы учения о растворах электролитов. Екатеринбург: Изд-во Урал. ун-та, 1993.
Котов Ю.А., Бекетов И.В., Медведев А.И., Тимошенкова О.Р. // Рос. нанотехнологии. 2009. Т. 4. № 5–6. С. 126.
Антипина С.А., Змановский С.В., Громов А.А., Коновалов А.С. // Журн. физ. химии. 2017. Т. 91. № 1. С. 58. https://doi.org/10.7868/S0044453717010034
Ланин С.Н., Банных А.А., Ковалева Н.В. // Там же. 2013. Т. 87. № 11. С. 1910. https://doi.org/10.7868/S0044453713100178
Zhang H., Wang J., Zheng H. et al. // J. Phys. Chem. B. 2005. V. 109. P. 2610. https://doi.org/10.1021/jp045838d
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии