Журнал физической химии, 2020, T. 94, № 6, стр. 898-902
Адсорбция газов на поверхности железосодержащего полиакрилонитрила
М. М. Авилова a, *, Е. А. Марьева a, О. В. Попова a, Т. А. Финоченко b
a Ростовский государственный университет путей сообщения
Ростов-на-Дону, Россия
b Южный федеральный университет, Институт управления в экономических, экологических и социальных системах
Таганрог, Россия
* E-mail: m.avir89@yandex.ru
Поступила в редакцию 05.09.2019
После доработки 05.09.2019
Принята к публикации 17.09.2019
Аннотация
Оценена возможность адсорбции газов-загрязнителей (диоксид азота, метан, аммиак, оксид серы(II), сероводород, озон, монооксид углерода, оксид углерода(II), хлор) на поверхности железосодержащего ПАН. Построена модель кластера железосодержащего ПАН. Методом молекулярного моделирования в работе определены термодинамические показатели систем: кластер Fe-ПАН–молекула газа, кластер Fe-ПАН–молекула кислорода, кластер Fe-ПАН–молекула воды, кластер Fe‑ПАН–молекула кислорода–молекула газа, кластер Fe-ПАН–молекула воды–молекула газа и проведено их сравнение. Выявлено влияние кислорода на процесс адсорбции газов-загрязнителей на поверхности кластера железосодержащего ПАН и отсутствие влияния молекул воды, находящихся в непосредственной близости кластера. Установлено, что железосодержащий ПАН обладает способностью адсорбировать хлор и монооксид углерода.
Полиакрилонитрил (ПАН) является газочувствительным материалом, который успешно используется в современных сенсорах газов [1–6]. Для получения материала, обладающего селективной чувствительностью к газам-поллютантам, варьируют концентрации и виды модифицирующих добавок, а также температуру и время термообработки при его формировании [7–12]. В частности, в статье [13] экспериментально установлено, что нанокомпозитные мембраны на основе железосодержащего ПАН обладают газочувствительностью к диоксиду углерода. В указанном исследовании методом электроспиннинга получали мембраны ПАН с добавлением различных концентраций Fe2O3, а именно 1–5 мас. %. Результатами инфракрасной спектроскопии с Фурье-преобразованием подтверждено, что наличие наночастиц Fe2O3 в концентрации 4 мас. % приводит к улучшению характеристик газового датчика диоксида углерода. Согласно результатам, представленным в работе [13], наночастицы Fe2O3, присутствующие внутри или на поверхности волокна, могут приводить к усиленной адсорбции газа, что обусловлено высокой аффинностью между молекулами газа и поверхностными молекулами.
Для обеспечения пожарной безопасности в рабочей зоне предприятий крайне важно своевременное выявление в окружающей среде содержания и концентраций диоксида углерода. Поэтому исследование механизма газочувствительности поверхности нанокомпозита на основе железосодержащего ПАН является актуальным.
В целях объяснения газочувствительности требуется установить причину адсорбции одних газов-загрязнителей и невозможности данного процесса для других газов. Кроме этого, необходимо оценивать влияние газовой среды рабочей зоны на механизм адсорбции газов-загрязнителей на поверхности железосодержащего ПАН.
Вышеуказанные исследования возможно выполнить с помощью метода молекулярного моделирования, который позволяет быстро и корректно изучать сложные системы, исключив лишние ресурсные и финансовые затраты.
Таким образом, целью данной работы является определение возможности адсорбции газов-загрязнителей на поверхности железосодержащего ПАН методами молекулярного моделирования и оценка влияния молекул кислорода и молекул воды на данный процесс.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Модели макромолекул ПАН и их термодинамические показатели получены квантово-химическими расчетами с применением полуэмпирических методов в программе HyperChem. Для дальнейших расчетов использовали программный пакет Gaussian 09 и теорию функционала плотности с использованием базисного набора Попла (6-31G*) [14–17].
Для получения модели кластера железосодержащего ПАН в работе используется программный пакет Сhemoffice 2010, а именно, подпрограмма Chem3D с использованием методов молекулярного моделирования (метода молекулярной механики или метода минимизации потенциальной энергии системы) в модифицированной версии силового поля (ММ2). Применение метода ММ2 и реализация подпрограммы Chem3D позволяют получать и рассчитывать сложные химические системы, содержащие в своем составе переходные металлы [14, 18–20].
Для формирования правильной и максимально приближенной к реальной структуре модели железосодержащего ПАН изучена технология получения соответствующего материала. На основании исследований литературных данных приняли, что для получения газочувствительных материалов необходимо использовать оксид железа(III) при концентрациях от 1–5 мас. % [13]. Отжиг металлсодержащего ПАН проводят при температурах 250–600°С [7, 8, 10]. Согласно [13] оксид железа(III) в полимерных пленках присутствует в виде молекул. Однако следует учитывать, что при полимеризации самого ПАН и формировании его сопряженных цепочек вследствие протекающих химических реакций при соответствующем температурном режиме ИК-отжига образуются газы СО и Н2 [20, 21]:
(1)
${\text{F}}{{{\text{e}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}} + {{{\text{H}}}_{2}} \to 2{\text{FeO}} + 3{{{\text{H}}}_{{\text{2}}}}{\text{O}},$(2)
${\text{F}}{{{\text{e}}}_{{\text{2}}}}{{{\text{O}}}_{{\text{3}}}} + {\text{CO}} \to 2{\text{FeO}} + {\text{C}}{{{\text{O}}}_{{\text{2}}}}\;(500{\kern 1pt} --{\kern 1pt} 600^\circ {\text{С}}).$При получении оптимальной модели кластера железосодержащего ПАН в программном пакете Chem3D варьировали положение молекул оксидов железа как по отношению друг к другу, так и по отношению к сопряженным макромолекулам пентамера ПАН. В результате определена наиболее энергетически выгодная морфология поверхности Fe-ПАН (рис. 1).
После получения модели кластера железосодержащего ПАН исследовали возможность адсорбции газов-загрязнителей на его поверхности. Рассматривали адсорбцию следующих газов: оксида азота(IV), аммиака, оксида серы(II), сероводорода, озона, оксида углерода(IV), оксида углерода(II), хлора, метана. Для определения стерических энергий систем “кластер железосодержащего ПАН–молекула газа” задавали различные позиции молекул газа: (1) – внутри кластера – и (2)–(12) – посередине кластера на расстоянии от поверхности 2–10 Å (рис. 1).
Помимо определения стерической энергии методом ММ2 были определены другие термодинамические характеристики, а именно энергия связи (ΔE), точка энергетического минимума (lmin)).
На следующем этапе оценивали и сравнивали системы, в которых адсорбция газов-загрязнителей происходит при наличии молекул воды и кислорода. Для этого рассматривали системы кластер железосодержащего ПАН–молекула кислорода и кластер железосодержащего ПАН–молекула воды. Далее в указанные системы внедряли молекулы газов-загрязнителей. Наряду с вышеуказанными термодинамическими показателями (Еmin, ΔE, lmin) в системах “кластер железосодержащего ПАН–молекула кислорода/воды–молекула газа” рассчитывали расстояния от газов-загрязнителей до молекул кислорода (воды) (${{L}_{{{{{\text{О}}}_{2}}}}}$, ${{L}_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}}$).
В результате реализации метода ММ2, исходя из полученных термодинамических показателей систем, оценивали энергетическую возможность адсорбции конкретного газа-загрязнителя и устанавливали влияние кислорода и влажности на адсорбцию газов.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
По итогам молекулярного моделирования установлено, что наиболее подходящий вариант расположения оксидов железа – в центральной области внутри кластера ПАН (рис. 1). При этом расстояние между цепочками ПАН составляет 5–6 Å, а расстояние от молекул оксидов железа до цепочек ПАН – 3–4 Å, минимальная стерическая энергия кластера – 2518.82 кДж/моль. Стерическая энергия для системы “кластер железосодержащего ПАН–молекула кислорода” составляет 2512.16 кДж/моль, для системы “кластер железосодержащего ПАН–молекула воды” – 7242.75 кДж/моль.
Исходя из изложенного выше делаем вывод, что молекулы воды, находящиеся в предасорбционном состоянии, не будут оказывать влияния ни на поверхность кластера, ни на адсорбцию других молекул газов (Eмин Fe-ПАН $ \ll $ Eмин Fe-ПАН Н2О). При этом молекула кислорода, напротив, будет оказывать влияние на кластер железосодержащего ПАН (Eмин Fe-ПАН + О2 < Eмин Fe-ПАН).
Ниже приведены результаты молекулярного моделирования при адсорбции газов-загрязнителей на поверхности Fe-ПАН в различных газовых средах (рис. 2–5 и табл. 1).
Рис. 2.
Минимальная стерическая энергия адсорбции молекул газов на кластере железосодержащего ПАН в сухой (Fe-PAN, 1), влажной (Fe-PAN + Н2О, 2) и кислородной среде (Fe-PAN + О2, 3).

Рис. 3.
Энергия связи при адсорбции молекул газов на кластер железосодержащий ПАН систем в сухой (Fe-PAN, 1), влажной (Fe-PAN + Н2О, 2) и кислородной среде (Fe-PAN + О2, 3).

Рис. 4.
Зависимости величины энергии системы от расстояния между молекулой газа и поверхностью кластера в системе кластер железосодержащего ПАН–молекула газа.
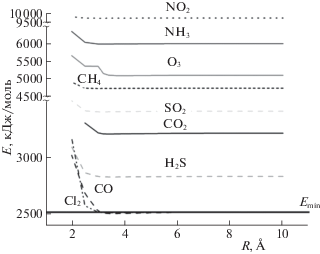
Рис. 5.
Зависимости величины энергии системы от расстояния между молекулой газа: 1 – Cl2, 2 – CO, 3 – H2S, 4 – CO2, 5 – SO2, 6 – CH4, 7 – O3, 8 – NH3, 9 – NO2 и поверхностью кластера для систем кластер Fe-ПАН–молекула кислорода–молекула газа (вверху) и кластер Fe-ПАН–молекула газа (внизу).

Таблица 1.
Длина связей в системах: кластер Fe-ПАН–молекула газа, кластер Fe-ПАН–молекула воды–молекула газа, кластер Fe-ПАН–молекула кислорода–молекула газа
| Газ | lmin, Å | ||
|---|---|---|---|
| Fe-ПАН | Fe-ПАН + Н2О | Fe-ПАН + О2 | |
| Cl2 | 3.5 | 3 | 3.4 |
| CO | 3.5 | 3.2 | 3.4 |
| О3 | 4 | 3.2 | 3.2 |
| NO2 | 3 | 2.5 | 3 |
| H2S | 3.4 | 3.5 | 3 |
| СО2 | 3.4 | 3.2 | 3.2 |
| SO2 | 3 | 3.4 | 3 |
| NH3 | 3.2 | 3.2 | 3.2 |
| CH4 | 3 | 2.5 | 3 |
Анализ расчетов стерических энергий (Емин) систем: кластер Fe-ПАН–молекула газа, кластер Fe-ПАН–молекула кислорода–молекула газа и кластер Fe-ПАН–молекула воды–молекула газа показал, что Fe-ПАН будет обладать обязательной газочувствительностью к хлору и монооксиду углерода (рис. 4 и 5), так как в системах, в которых присутствуют данные газы, энергии систем ниже энергий самих кластеров. Следует отметить, что стерические энергии систем, в которых присутствуют сероводород и диоксид углерода также невысоки, но энергии в таких системах немного выше энергий их кластеров. Можно предположить, что при определенном температурном режиме к молекулам сероводорода и диоксида углерода может также обнаруживаться чувствительность железосодержащего ПАН.
Энергии связи между газами и поверхностью кластера не превышают значений 15 кДж/моль (исключение – молекула NO2). Точки энергетического минимума для адсорбирующихся молекул газов находятся в области от 2.5 Å и выше от кластера (табл. 1). Данные расстояния исключают возможность образования химической связи, но подтверждают наличие межмолекулярного взаимодействия. Следует отметить, что расстояния между молекулами газов-поллютантов и молекулой кислорода/воды (${{L}_{{{{{\text{О}}}_{2}}}}}$, ${{L}_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}}$) также превышают 2 Å, причем в большинстве случаев составляют 3–3.5 Å, что также позволяет говорить о наличии межмолекулярного взаимодействия между указанными компонентами системы.
Таким образом, проведенные методом молекулярного моделирования исследования позволили установить, что во всех рассмотренных системах: кластер Fe-ПАН–молекула газа, кластер Fe-ПАН–молекула кислорода–молекула газа, кластер Fe-ПАН–молекула воды–молекула газа адсорбция хлора и монооксида углерода на поверхности железосодержащего ПАН является энергетически выгодной. Адсорбция сероводорода и монооксида углерода возможна. Учитывая невысокие значения энергии связи, полученные для системы кластер железосодержащий ПАН–молекула газа, можно предположить, что при адсорбции газов между молекулами газов и поверхностью ПАН возникают силы Ван-дер-Ваальса. Таким образом, по результатам проведенных теоретических исследований можно сделать вывод, что железосодержащий ПАН является перспективным материалом, способным адсорбировать хлор и монооксид углерода.
Список литературы
Karbownik I., Fiedot M., Rac O. et al. // Polymer. 2015. V. 75. P. 97.
Wenyu Wang, Yide Zheng, Xin Jin et al. // Nano Energy. 2019. V. 56. P. 588.
Stergios Logothetidis. Flexible organic electronic devices // Materials Science and Engineering: 2008. B. 152. P. 96.
Efimov M.N., Sosenkin V.E., Volfkovich Yu.M. et al. // Electrochemistry Communications. 2018. V. 96. P. 98.
Liang Chen, Yinze Zuo, Yu Zhang, Yanmin Gao // Materials Letters. 2018. V. 215. P. 268.
Savest N., Plamus T., Tarasova E. et al. // J. Electrostatics. 2016. V. 83. P. 63.
Kozlov V.V., Karpacheva G.P., Petrov V.S., Lazovskaya E.V. // Polymer Science Series A. 2001. V. 43. P. 20.
Laffont L., Monthioux M., Serin V. et al. // Carbon. 2004. V. 42. P. 2485.
Yoshida H., Sato N. // J. Phys. Chem. B. 2006. V. 110. P. 4232.
Kozlov V.V., Kozhitov L.V. // Перспективные материалы. 2007. С. 377.
Merdrignac-Conanec O., Bernicot Y., Guyader J. // Sensors and Actuators B: Chemical. 2000. V. 63. № 1–2. P. 86.
Ravindra V. Ghorpade, Dong Won Cho, Sung Chul Hong // Carbon. 2017. V. 121. P. 502.
Yena Kim, Eun-Young Park, Deuk Yong Lee et al. // J. Korean Ceram. Soc. 2007. V. 44. № 4. P. 194.
Avilova M.M., Petrov M.M. // Russ. J. Phys. Chem. B. 2017. V. 11. № 4. P. 618.
Zaporotskova I.V., Kojitov L.V., Anikeev N.A. et al // J. Nano- and Electronic Physics. 2014. V. 6. № 3. P. 03035.
Xinliang Yu, Bing Yi, Zhimin Xie et al. // Chemometrics and Intelligent Laboratory Systems. 2007. V. 87. № 2. P. 247.
Kun Ge, Qichang Yu, Shaohua Chen et al. // Chem. Eng. J. 2019. V. 364. P. 328.
Masataka Nagaoka, Yusuke Ohta, Haruko Hitomi // Coordination Chemistry Reviews. 2007. V. 251. № 21–24. P. 2522.
Jing Zhang, Yu-Xi Liu, Re-Bing Wu et al. // Physics Reports. 2017. V. 679. P. 1.
Gupta A.K., Paliwal D.K., Bajaj P. // J. Appl. Polym. Sci. 1995. V. 58. № 7. P. 1161.
Surianarayanan M., Vijayaraghavan R., Raghavan K.V. // J. Polym. Chem. 1998. № 17. P. 2503.
https://www.chem21.info/info/6736/.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии



