Журнал физической химии, 2021, T. 95, № 4, стр. 558-561
Излучение водных растворов неэлектролитов в миллиметровой области спектра и их диэлектрические свойства
А. К. Лященко a, *, А. Ю. Ефимов a, В. С. Дуняшев a
a Российская академия наук, Институт общей и неорганической химии им. Н.С. Курнакова
119991 Москва, Россия
* E-mail: aklyas@mail.ru
Поступила в редакцию 12.05.2020
После доработки 11.07.2020
Принята к публикации 13.07.2020
Аннотация
С помощью высокочувствительного радиометра на частоте 61.2 ГГц изучены радиояркостные характеристики водных растворов неэлектролитов (формамида, диметилформамида, ацетамида, диметилацетамида) в широкой области концентраций при 298 К. Они сопоставлены с расчетными данными из диэлектрических спектров в миллиметровой (мм) области спектра. Показано хорошее согласие экспериментальных и расчетных радиояркостных параметров в начальной области концентраций, где преобладают гидратационные изменения воды в растворах (за исключением диметилацетамида). Установлено, что собственное излучение растворов растет с увеличением концентрации неэлектролита; влияние количества CH3-групп в молекулах на радиояркостные характеристики неаддитивно вследствие различных эффектов полярных и неполярных групп молекул. Суммарный эффект может быть установлен на основе измерений собственного излучения растворов в мм-области спектра.
Как известно, дистанционный метод СВЧ-радиометрии широко применяется для измерения геофизических параметров поверхностных вод морей и океанов. Увеличение содержания солей в морской воде сильно изменяет ее диэлектрические и другие физико-химические характеристики, имеющие важное значение [1–3]. Наряду с СВЧ-радиометрией, высокочувствительный радиометр мм-диапазона может успешно применяться для исследования характеристик излучения и отражения воды и растворов разного состава в широкой области концентраций. Нами этот метод был применен в лабораторных условиях. Ранее такие исследования проводились только в отношении растворов электролитов [4–7]. В настоящей работе рассмотрены изменения параметров излучения растворов неэлектролитов и их связь с диэлектрическими характеристиками растворов СВЧ- и КВЧ-спектров. В качестве модельных систем выбраны растворы амидов карбоновых кислот гомологического ряда (формамид, ацетамид, диметилформамид и диметилацетамид). Представлялось важным рассмотреть, каким образом радиояркостные контрасты в миллиметровом диапазоне меняются при росте количества СН3-групп в ряду неэлектролитов. Кроме того, водные растворы ацетамида, диметилацетамида и диметилформамида представляют характерный пример воздействия на воду полифункциональных молекул, у которых имеются как полярные, так и неполярные группы. Суммарное влияние полярных и неполярных групп молекул на состояние воды может быть установлено на основе измерений собственного излучения растворов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
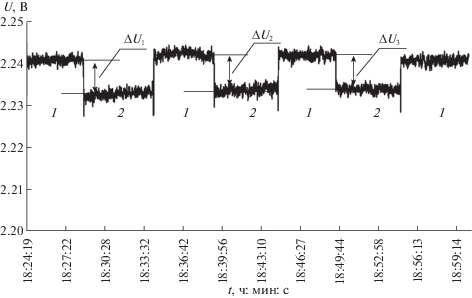
Исследование образцов воды и растворов неэлектролитов проводилось с помощью высокочувствительного радиометра с фиксированной частотой 61.2 ГГц (ИРЭ РАН, Фрязино). Устройство радиометра и методика проведения измерений описаны ранее в работе [7]. Показания от прибора оцифровываются и передаются на ПК, где с помощью специальной программы ведутся запись и дальнейшая обработка сигнала. Запись сигнала осуществляется таким образом, что на результирующем графике по оси абсцисс откладывается время проведения измерений t (часы, минуты, секунды), а по оси ординат – радиофизический отклик U (напряжение на выходе радиометра, вольт). Градуировка шкалы прибора с использованием эталонов подробно описана в [8]. Уровень сигнала от полированной металлической пластины, используемой для калибровки, принимается за нулевой. Таким образом, показания для медной пластины соответствуют минимальному значению, а минимальные показания прибора для воды и растворов неэлектролитов отвечают максимальному эффекту. В качестве примера участок зависимости U от t для парных измерений воды и раствора ацетамида приведен на рис. 1. Парные измерения U раствора и воды проводились с целью повышения точности и достоверности результатов эксперимента. Среднее значение этих величин далее использовалось для расчета ∆U = Uводы– Uраствора. Пересчет величин ∆U в коэффициент излучения χ осуществлялся по уравнению калибровки:
Интенсивность собственного излучения раствора удобнее всего выражать через радиояркостную температуру Tя. Для методики измерений, использованной в данной работе, выполняется соотношение [9]:
где T – термодинамическая температура (данные, приведенные в настоящей работе, относятся к T = 298 K), а R – коэффициент отражения по мощности. Значения ∆U, χ и ∆Тя= Тя (раствор) – Тя (H2O), полученные методом радиометрии, представлены в табл. 1.Таблица 1.
Разность уровней напряжения ∆U, коэффициенты излучения χ и разность радиояркостных температур ∆Тя растворов неэлектролитов, измеренные с помощью радиометра на частоте 61.2 ГГц
| Система | Моляльность, моль/кг H2O |
∆U, мВ | χ | ∆Тя, К |
|---|---|---|---|---|
| H2O | 0 | 0 | 0.506 | 0 |
| H2O/Формамид | 0.62 | 0.7 | 0.513 | 2.1 |
| 1.72 | 0.8 | 0.514 | 2.4 | |
| 2.92 | 1 | 0.516 | 3.0 | |
| 4.18 | 1.5 | 0.521 | 4.5 | |
| 6.17 | 1.6 | 0.522 | 4.8 | |
| 9.79 | 2.1 | 0.527 | 6.2 | |
| H2O/Ацетамид | 1.66 | 2 | 0.526 | 6.0 |
| 2.77 | 3.8 | 0.544 | 11.3 | |
| 3.88 | 4.6 | 0.552 | 13.7 | |
| 5.55 | 7.7 | 0.583 | 22.9 | |
| 8.32 | 9.6 | 0.602 | 28.6 | |
| 11.09 | 12.1 | 0.627 | 36.1 | |
| 13.88 | 14.1 | 0.647 | 42.0 | |
| H2O/Диметил- ацетамид |
0.39 | 4 | 0.546 | 6.3 |
| 1.48 | 4.6 | 0.552 | 13.7 | |
| 4.56 | 11.4 | 0.620 | 34.0 | |
| 6.17 | 15.3 | 0.659 | 45.6 | |
| 7.71 | 15.9 | 0.665 | 47.4 | |
| H2O/Диметил- формамид |
0.88 | 8 | 0.586 | 6.55 |
| 2.41 | 9.7 | 0.603 | 28.9 | |
| 3.88 | 11.5 | 0.621 | 34.3 | |
| 4.99 | 12.8 | 0.634 | 38.1 |
МЕТОДИКА РАСЧЕТОВ
Оптические и диэлектрические свойства веществ тесно связаны между собой. Коэффициент отражения по мощности R связан с комплексной диэлектрической проницаемостью ε* по уравнению Френеля [4, 10]:
Из величины R, используя соотношение (1), можно получить величины χ = 1 – R, Тя и ∆Тя.
Комплексная диэлектрическая проницаемость ε* определяется с помощью экспериментально измеряемых диэлектрической проницаемости ε'(ν) и диэлектрических потерь ε''(ν):
Растворы неэлектролитов являются непроводящими системами, поэтому, в отличие от растворов электролитов, диэлектрические потери ε'' определяются только переориентацией дипольных молекул. Диэлектрические данные ε' и ε'' в диапазоне частот 7–25 ГГц для водных растворов ацетамида [11, 12], формамида [13–15], диметилацетамида [13, 16], диметилформамида [13, 17, 18], были аппроксимированы функциями вида:
Параметры α, εs, ε∞, τd, зависят от состава раствора.
Далее полученные модели диэлектрических спектров были использованы для расчетов ε' и ε'' на частоте 61.2 ГГц. По приведенным выше формулам были получены R, χ и Тя. Параметры ε', ε'', χ и ∆Tя для рассматриваемых систем, рассчитанные из данных диэлектрических экспериментов, приведены в табл. 2.
Таблица 2.
Диэлектрические и радиояркостные характеристики растворов на частоте 61.2 ГГц, полученные экстраполяцией диэлектрических данных в диапазоне частот 7–25 ГГц
| Система | Моляль-ность, моль/кг H2O | ε' | ε'' | χ | ∆Тя, К |
|---|---|---|---|---|---|
| H2O | 0 | 11.63 | 21.05 | 0.506* | 0 |
| H2O/Формамид | 0.62 | 11.26 | 20.70 | 0.507 | 0.3 |
| 1.72 | 11.16 | 20.18 | 0.512 | 1.8 | |
| 2.92 | 10.98 | 20.20 | 0.511 | 1.5 | |
| 4.18 | 10.94 | 19.88 | 0.514 | 2.4 | |
| 6.17 | 10.69 | 19.21 | 0.520 | 4.2 | |
| 9.79 | 10.34 | 18.52 | 0.527 | 6.2 | |
| H2O/Ацетамид | 1.72 | 9.98 | 18.15 | 0.530 | 7.1 |
| 2.92 | 9.29 | 16.46 | 0.548 | 12.5 | |
| 6.17 | 8.72 | 12.96 | 0.591 | 25.3 | |
| 9.79 | 7.93 | 10.43 | 0.630 | 36.9 | |
| 13.88 | 7.00 | 7.77 | 0.680 | 51.9 | |
| H2O/Диметил- ацетамид |
0.39 | 11.15 | 19.54 | 0.517 | 3.3 |
| 1.48 | 9.27 | 14.92 | 0.566 | 17.9 | |
| 4.56 | 7.18 | 8.42 | 0.667 | 48.0 | |
| 6.17 | 6.52 | 6.54 | 0.708 | 60.2 | |
| 7.71 | 6.25 | 5.42 | 0.735 | 68.2 | |
| H2O/Диметил- формамид |
0.88 | 9.80 | 17.72 | 0.535 | 8.6 |
| 2.41 | 7.59 | 12.74 | 0.594 | 26.2 | |
| 3.88 | 6.69 | 9.67 | 0.645 | 41.4 | |
| 4.99 | 6.85 | 9.22 | 0.653 | 43.8 |
* – значение взято из [5].
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Как видно из табл. 1, собственное излучение растворов неэлектролитов растет при переходе от воды к раствору. С ростом концентрации неэлектролита растут коэффициенты излучения χ и полученные в эксперименте разности радиояркостных температур ∆Тя= Тя (раствор) – Тя (H2O). Это также следует из расчетных данных (табл. 2). Таким образом, для всех изученных систем характерны однознаковые изменения радиояркостных параметров при переходе от воды к раствору. Это отличает их от растворов электролитов, где разнознаковые изменения могут быть связаны с наличием ионных потерь [4, 5]. В ряду неэлектролитов наблюдаются отличия гидрофобной и гидрофильной гидратации, причем с ростом количества неполярных групп в растворенной молекуле эффекты излучения и радиояркости растут. Заранее предсказать суммарные изменения не представляется возможным из-за наличия взаимовлияний полярных и неполярных групп молекул.
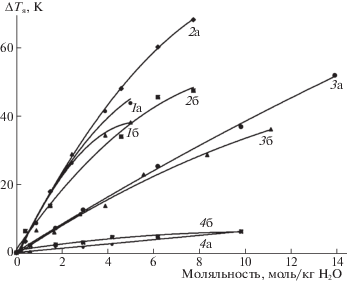
Были сопоставлены рассчитанные и измеренные радиояркостные параметры для всех изученных систем (рис. 2). Видно, что согласие реализуется для растворов формамида, ацетамида и диметилформамида в начальной области концентраций, где преобладают гидратационные изменения воды в растворах. Этот концентрационный интервал соответствует начальному участку зависимостей сравниваемых ∆Тя систем (видно на рис. 2, где рассматриваемые зависимости линейны). Из рис. 2 следует, что для растворов диметилацетамида с ростом концентрации неэлектролита наблюдается расхождение рассчитанных и измеренных параметров радиояркости. Это может быть связано с разными вариантами расчетов и выбором диэлектрической модели спектра. Сопоставление диэлектрических характеристик растворов с радиояркостными позволяет анализировать и корректировать набор литературных данных СВЧ-диэлектрической спектроскопии, а также уточнять выбор релаксационной модели.
Рис. 2.
Разность радиояркостных температур раствор–вода по расчетным (а) и экспериментальным (б) данным на частоте 61.2 ГГц. Растворы: 1 – диметилформамид, 2 – диметилацетамид, 3 – ацетамид, 4 – формамид.
Радиометрия может успешно зарекомендовать себя как метод дистанционного экспресс-анализа изменений концентраций и свойств растворов с различными структурными эффектами гидрофильной и гидрофобной гидратации.
Работа выполнена в рамках государственного задания ИОНХ РАН в области фундаментальных научных исследований и при частичной поддержке РФФИ (грант № 19-03-00033а).
Список литературы
Шутко А.М. СВЧ-радиометрия водной поверхности. М.: Наука, 1986. 188 с.
Meissner T., Wentz F.J. // IEEE Transactions on Geoscience and Remote Sensing, 2004. V. 42. № 9. P. 1836. https://doi.org/10.1109/TGRS.2004.831888
Терехин Ю.В., Пустовойтенко В.В. // Исследование Земли из космоса. 1986. № 2. С. 16.
Засецкий А.Ю., Лященко А.К. Квазиоптический метод измерения комплексной диэлектрической проницаемости водных растворов электролитов в миллиметровом диапазоне длин волн и релаксационные характеристики растворов: Деп. ВИНИТИ 06.07.99. М., 1999. № 2181-В99. 62 с.
Лященко А.К., Ефимов А.Ю., Дуняшев В.С., Каратаева И.М. // Журн. неорган. химии. 2020. Т. 65. № 2. С. 237. https://doi.org/10.31857/S0044457X20020099
Лященко А.К., Каратаева И.М. // Журн. неорган. химии. 2017. Т. 62. № 1. С. 127. https://doi.org/10.7868/S0044457X1701010X
Лященко А.К., Каратаева И.М., Козьмин А.С., Бецкий О.В. // Докл. АН. 2015. Т. 462. № 5. С. 561. https://doi.org/10.7868/S0869565215170168
Лященко А.К., Каратаева И.М., Дуняшев В.С. // Журн. физ. химии. 2019. Т. 93. № 4. С. 552. https://doi.org/10.1134/S0044453719040204
Козьмин А.С. Низкоинтенсивное электромагнитное излучение миллиметрового диапазона воды и водных растворов. Дисс. … канд. физ.-мат. наук. Волгоград, 2011. 180 с.
Lyashchenko A.K., Zasetsky A.Yu. // J. Mol. Liquids. 1998. V. 77. P. 61. https://doi.org/10.1016/S0167-7322(98)00068-3
Ястремский В.С., Лященко А.К., Ястремский П.С. // Журн. структур. химии. 1976. Т. 17. № 4. С. 662.
Lyaschenko A.K., Lillev A.S., Khar’kin V.S. etc. // Mendeleev Commun. 1977. № 5. P. 207.
Лилеев А.С. Диэлектрическая релаксация и молекулярно-кинетическое состояние воды в растворах: Дисс. … докт. хим. наук. М.: ИОНХ РАН, 2004. 276 с.
Stockhausen M., Utzel H., Seitz E. // Z. Phys. Chem. Neue Folge. 1982. Bd. 133. S. 69.
Лященко А.К., Харькин В.С., Лилеев А.С., Гончаров В.С. // Журн. физ. химии. 1992. Т. 66. № 8. С. 2256.
Лященко A.K., Лилеев A.C., Борина А.Ф. // Там же. 1998. Т. 72. № 10, с. 1863.
Лященко A.K., Лилеев A.C., Борина А.Ф. // Там же. 1999. Т. 73. № 8. С. 1382.
Шахпаронов М.И., Галиярова Н.М. // В сб. Физика и физикохимия жидкостей.М.: Изд-во МГУ, 1980. Вып. 4. С. 75.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии