Журнал физической химии, 2022, T. 96, № 4, стр. 479-487
Энтальпии сублимации и сольватации дипептидов аланинового ряда
Е. Ю. Тюнина a, *, В. П. Баранников a, В. В. Дунаева b, А. В. Краснов b
a Институт химии растворов им. Г.А. Крестова РАН
153045 Иваново, Россия
b Ивановский государственный химико-технологический университет
153000 Иваново, Россия
* E-mail: tey@isc-ras.ru
Поступила в редакцию 20.10.2021
После доработки 20.10.2021
Принята к публикации 25.10.2021
- EDN: HNFJXB
- DOI: 10.31857/S0044453722040331
Аннотация
Исследованы процессы сублимации дипептидов, DL-аланил-DL-норвалин и L-аланил-L-триптофан, эффузионным методом Кнудсена с масс-спектрометрическим контролем состава пара. Обсуждена фрагментация молекул под действием электронной ионизации. Значения молярной энтальпии сублимации изученных соединений получены с помощью уравнения Клаузиуса–Клапейрона. Методом дифференциальной сканирующей калориметрии измерены удельные изобарные теплоемкости кристаллических дипептидов DL-аланил-DL-норвалин и L-аланил-L-триптофан. Определены стандартные молярные энтальпии сублимации при Т = 298.15 К. Используя значения молярной энтальпии сублимации и энтальпии растворения веществ в воде, определены стандартные молярные энтальпии сольватации дипептидов аланинового ряда при Т = 298.15 К. Обсуждаются корреляции полученных энтальпийных параметров с обычно используемыми физико-химическими характеристиками дипептидов.
Важность термодинамического исследования пептидов связана с поведением этих соединений в водных растворах и их использованием в качестве модельных систем для понимания различных типов взаимодействий между более сложными биологическими молекулами (белками) в водных смесях. С практической точки зрения, некоторые кристаллические пептиды могут использоваться в качестве основы для биоматериалов, лекарств и биомиметиков [1–3]. За последние десятилетия наблюдается динамичный рост развития нанотехнологий с целью создания новых материалов с уникальными свойствами [3–5]. Не только неорганические атомы, но и биологические молекулы (аминокислоты, пептиды, белки и пр.) могут служить компонентами нанокомпозитов. Полученные системы находят применение в качестве биосенсоров, оптических фильтров, носителей лекарственных средств и биологически активных веществ [3, 6–8].
Энтальпия сублимации является важной экспериментальной характеристикой, которая часто используется для определения энтальпии образования в газовой фазе, изучения полиморфизма, прогнозирования молекулярной упаковки аминокислот и пептидов, а также для улучшения алгоритмов расчета энергии решетки белков [9–14]. Энтальпии сублимации важны для понимания сольватационного поведения белков, которое оказывает влияние на их конформационную стабильность в растворах [15, 16]. Однако экспериментальное измерение энтальпий сублимации пептидов представляет собой нетривиальную задачу вследствие низкой термостабильности этих веществ [16–18]. Поэтому термохимия пептидов мало изучена по сравнению с другими классами азотосодержащих органических соединений.
В представленной работе применен эффузионный метод Кнудсена с масс-спектрометрическим контролем состава пара, эффективность которого показана ранее при изучении процесса сублимации некоторых аминокислот и пептидов [19, 20]. Отметим, что впервые метод электронной ионизации (ЭИ) был применен авторами работ [21, 22]. В настоящее время наиболее популярными методами ионизации стали ESI (ионизация электрораспылением), химическая ионизация, CID (диссоциация, индуцированная столкновениями) и MALDI (матричная лазерная десорбция/ионизация) [23–25]. Однако только метод ЭИ может быть использован для исследования термодинамики сублимации аминокислот и пептидов на основе температурной зависимости ионных токов. Наряду с энтальпией сублимации, теплоемкость кристаллических веществ является важным параметром, знание которого необходимо для расчета термодинамических параметров. Можно сказать, что оба эти свойства напрямую связаны с энергией межмолекулярной когезии в кристаллической структуре, дают представление об энергии и структуре твердой фазы различных веществ [26, 27]. Таким образом, получение новых данных об энтальпии сублимации и теплоемкости модельных соединений белков до сих пор является актуальной задачей. Несмотря на важность пептидов, надежные экспериментальные термохимические исследования все еще редки, хотя и существуют исследовательские группы, занимающиеся этой проблемой [9, 19, 20, 28–32].
Авторы продолжают развивать то направление исследований аминокислот и пептидов в твердой фазе и растворах, основы которого были заложены в работах Г.А. Крестова [15, 19, 31, 33–37]. Здесь представлены новые результаты определения теплоемкости кристаллических дипептидов DL-аланил-DL-норвалина (DL-Ala-DL-Nvl) и L-аланил-L-триптофана (L-Ala-L-Trp) и изучения процессов их сублимации, а также проведено сравнение с данными, полученными ранее для глицил-L-аланина (Gly-L-Ala), DL-аланил-глицина (DL-Ala-Gly), L-аланил-L-аланина (L-Ala-L-Ala), DL-аланил-DL-аланина (DL-Ala-DL-Ala) и DL-аланил-DL-валина (DL-Ala-DL-Val). На основе использования значений энтальпий сублимации и энтальпий растворения дипептидов аланинового ряда определены энтальпии их сольватации (гидратации) в водных растворах.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Дипептиды, DL-аланил-DL-норвалин (DL-Ala-DL-Nvl) and L-аланил-L-триптофан (L-Ala-L-Trp) (производства Fluka/Acros organics) сушили в вакуумном шкафу при 320–350 К в течение 8 ч непосредственно перед использованием. Их молекулярная структура, молярная масса, чистота и происхождение представлены в табл. 1.
Таблица 1.
Молекулярная структура исследуемых дипептидов, их происхождение и степень чистоты
| Химическое соединение | M | CAS No. | Происхождение | Чистота |
|---|---|---|---|---|
DL-alanyl-DL-norvaline |
188.23 | 2325-18-0 | Acros Organics, USA | массовая доля >0.99 |
L-alanyl-L-tryptophan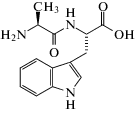 |
275.30 | 16305-75-2 | Fluka, Swetzerland | массовая доля ≥0.99 (TLC) |
Экспериментальные исследования сублимации выполнены эффузионным методом Кнудсена с масс-спектрометрическим контролем состава пара. Для этих целей использовали магнитный масс-спектрометр МИ 1201 (900; r = 200 мм) (“СЭЛМИ”, Сумы, Украина), адаптированный для эффузионных экспериментов. Детальное описание процедуры и метода исследования приведено в работах [19, 37, 38]. Образец примерно 50–100 мг помещали в эффузионную ячейку из молибдена (отношение “площади испарительной поверхности к площади эффузионного отверстия” составляло около 1000). Температура эффузионной ячейки измерялась вольфрам-рениевой термопарой WRe-5/20. Точность поддержания температуры составляла ±0.5 K. Ионизация нейтральных частиц, эффундирующих из ячейки Кнудсена в ионизирующую область, происходила за счет электронного удара с энергией ионизирующих электронов 50 эВ. Все эксперименты проводились в условиях вакуума (при давлении до 10–5–10–6 Па). Ионный ток измерялся ионным умножителем, совмещенным с электрометром. Усиленный сигнал через аналого-цифровой преобразователь записывали на ПК. Типы ионов, наблюдаемые при фрагментации пептидов, были идентифицированы и обозначены как отношение их массы к заряду (m/z).
В масс-спектрометрах с ячейкой Кнудсена давление пара (p) пропорционально величине ионных токов (IT), т.е. произведению интенсивности иона (I) на температуру (T) [39]. Наклон зависимости значений ln(IT) от обратной температуры (1/Т) определяет энтальпию сублимации согласно второму закону термодинамики. Следует отметить, что второй закон не требует преобразования интенсивности ионов в абсолютное давление [40]. Как показано ранее [20, 35, 41], тестирование оборудования было проведено с использованием простейшей аминокислоты глицина (Gly) и бензойной кислоты, рекомендуемого в качестве основного стандарта для измерения энтальпии сублимации органических соединений [42, 43]. Доказано, что температурные зависимости ln(IT) от 1/Т бензойной кислоты и Gly носят линейный характер (коэффициент корреляции rcorr > 0.9998) [20, 35, 41]. Полученные для них значения энтальпий сублимации хорошо согласуются с литературными данными [29, 35, 44].
Удельную теплоемкость пептидов при постоянном давлении (cp) в зависимости от температуры измеряли с помощью дифференциального сканирующего калориметра теплового потока DSC 204 F1 Phoenix (NETZSCH, Германия) с высокочувствительным μ-сенсором в сочетании с программным обеспечением Proteus для Windows, используя стандартный эталон α-Al2O3 для проверки калибровки прибора [45]. Предварительно высушенный образец (3.12) × 10–6 кг помещали в алюминиевый тигель и измеряли тепловой поток по сравнению с пустым эталонным алюминиевым тиглем как функцию температуры. Образец нагревали со скоростью 10 К/мин в атмосфере аргона и охлаждали газообразным азотом в интервале температур от (288.64 до 333.64) К. Процедура и техника эксперимента подробно описаны ранее [37, 38, 43, 45]. Калибровка прибора была выполнена на основе использования значений температур плавления шести эталонных веществ высокой степени чистоты: циклогексана (99.96%), ртути (99.99%), бифенила (99.5%), индия (99.999%), олова (99.999%) и висмута (99.9995%) [43, 45]. Точность измерения температуры составляла 0.1 К. Ранее [37] была показана надежность работы калориметра путем измерения теплоемкости рекомендуемого стандартного вещества – кристаллической бензойной кислоты C6H5COOH при различных температурах [43, 45]. Относительная стандартная погрешность ur(сp) составила ±0.6% для бензойной кислоты в твердом состоянии [37, 38]. В случае кристаллических дипептидов относительная комбинированная стандартная погрешность измерения удельной теплоемкости, учитывающая различные возможные источники ошибок, составила ±1% в пределах изученного диапазона температур.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Теплоемкость кристаллических дипептидов
Измерения удельной теплоемкости кристаллических дипептидов проводили в диапазоне (288.64–333.64) К. Молекулярные массы, используемые для преобразования удельных теплоемкостей в их молярные аналоги, были рассчитаны с учетом атомных масс, рекомендованных IUPAC [46]. Полученные значения стандартной изобарной молярной теплоемкости ($C_{{p{\text{,m}}}}^{^\circ }$(cr)) в исследованном диапазоне температур представлены в графической форме на рис. 1. Значения $C_{{p{\text{,m}}}}^{^\circ }$(cr) для L-Ala-L-Trp и DL-Ala-DL-Nvl в твердой фазе увеличиваются с повышением температуры и не проявляют каких-либо особенностей, что свидетельствует об отсутствии фазовых переходов в исследованном диапазоне температур. Экспериментальные значения молярной теплоемкости ($C_{{p{\text{,m}}}}^{^\circ }$(cr)) исследованных дипептидов представлены в табл. 2 и были использованы для оценки стандартной молярной энтальпии сублимации кристаллических дипептидов при T = = 298.15 К.
Рис. 1.
Температурные зависимости экспериментальных изобарных молярных теплоемкостей кристаллических дипептидов: L-аланил-L-триптофана (1) и DL-аланил-DL-норвалина (2).

Таблица 2.
Экспериментальные значения молярной теплоемкости L-Ala-L-Trp и DL-Ala-DL-Nvl в твердой фазе, $C_{{p{\text{,m}}}}^{^\circ }$(cr), при различных температурах и стандартном давлении (p0 = 0.1MПa)a
| Ta, K | $C_{{p{\text{,m}}}}^{^\circ }$(cr)$_{{{\text{exp}}}}^{{\text{b}}}$, Дж моль–1 K–1 | $C_{{p{\text{,m}}}}^{^\circ }$(cr)$_{{{\text{exp}}}}^{{\text{b}}}$, Дж моль–1 K–1 |
|---|---|---|
| L-Ala-L-Trp | DL-Ala-DL-Nvl | |
| 288.64 | 275.11 | 267.51 |
| 293.64 | 280.07 | 272.53 |
| 298.15 | 284.43 | 276.74 |
| 298.64 | 284.91 | 277.01 |
| 303.64 | 289.74 | 280.17 |
| 308.64 | 294.65 | 285.25 |
| 313.64 | 299.82 | 291.13 |
| 318.64 | 304.81 | 295.06 |
| 323.64 | 309.88 | 300.09 |
| 328.64 | 314.93 | 303.09 |
| 333.64 | 320.14 | 306.92 |
Фрагментация дипептидов
Ранее были рассмотрены масс-спектры некоторых пептидов и их производных [24, 47, 48]. Сравнение имеющихся масс-спектральных данных [18, 21, 49, 50] показывает, что фрагментации аминокислот и дипептидов имеют схожий характер. В условиях электронной ионизации молекул пики молекулярных ионов имеют низкую интенсивность, так как карбоксильная группа легко отделяется от молекулы [51]. Боковые цепи аминокислотных остатков (CH-R) отщепляются одновременно с образованием ионов, возникающих в результате расщепления связей CH–CO, CO–NH, NH–CH вдоль пептидного остова, что представляет собой обычную фрагментацию молекул пептидов [50]. Масс-спектры электронной ионизации, полученные для DL-Ala-DL-Nvl и L-Ala-L-Trp и представленные в табл. 3, отсутствуют в базе данных NIST [21, 31, 49, 50]. Наблюдается образование четырех доминирующих ионов (m/z: 45, 72, 99, 128) в масс-спектре DL-Ala-DL-Nvl, два из которых аналогичны доминирующим пикам в ЭИ масс-спектрах аминокислот: Ala (m/z 45) и Nvl (m/z 72) [49]. Для L-Ala-L-Trp наиболее интенсивным ионным фрагментом является ион с массой m/z 130, что характерно для боковой цепи аминокислотного остатка дипептида и присутствует в масс-спектрах Trp [49]. Следует отметить, что некоторые пептиды при нагревании (во время испарения) проявляют склонность к циклизации с образованием дикетопиперазина [18, 21, 31]. В случае DL-Ala-DL-Nvl был зарегистрирован ион с массой m/z 170, который может быть классифицирован как ион циклической формы, имеющий очень низкую интенсивность (<1%). Сублимация L-Ala-L-Trp не сопровождается циклизацией-дегидратацией в исследованном диапазоне температур.
Таблица 3.
Масс-спектры электронной ионизации дипептидов (Uioniz = 50 В)
| m/z | Ions | Irel, % | m/z | Ions | Irel, % |
|---|---|---|---|---|---|
| DL-alanyl-DL-norvaline (T = 477 K) | L-alanyl-L-tryptophan (T = 465 K) | ||||
| 29 | [NH2CH]+ | 4 | 29 | [NH2CH]+ | 3 |
| 45 | [COOH]+ | 59 | 45 | [COOH]+ | 4 |
| 57 | [NH2CHCO]+ | 29 | 57 | [NH2CHCO]+ | 2 |
| 72 | [NH2CH(CH3)CO]+ | 100 | 72 | [NH2CH(CH3)CO]+ | 1 |
| 87 | [NH2CH(CH3)CONH]+ | 6 | 77 | [C6H5]+ | 1 |
| 99 | [NHCH(CH2CH2CH3)CO]+ | 35 | 87 | [NH2CH(CH3)CONH]+ | 1 |
| 116 | [M-[NH2CH(CH3)CO]]+ | 5 | 105 | [C7H7N]+ | 2 |
| 128 | [NH2CH(CH3)CONHCHCO]+ | 52 | 130 | [C9H8N]+ | 100 |
| 144 | [M-[NH2CH(CH3)]]+ | 9 | 188 | [C9H8NCHCOOH]+ | 4 |
| 170 | ${\text{M}}_{{\text{c}}}^{ + }$ | <1 | 259 | [M-[NH2]]+ | 10 |
| 188 | M+ | 7 | 275 | M+ | 4 |
Энтальпия сублимации и энтальпия сольватации
Сублимация дипептидов изучена в интервалах температур 446.15–491.15 К и 458.15–485.15 К для DL-Ala-DL-Nvl и L-Ala-L-Trp, соответственно. Относительные интенсивности ионов в масс-спектрах дипептидов (табл. 3) соответствуют усредненным значениям из двух независимых экспериментов для каждого соединения. Установлено, что ионные фрагменты имеют температурные коэффициенты сублимации, идентичные родительскому иону (M+). Интенсивность ионов измерялась как при повышении, так и при понижении температуры, при этом гистерезиса не наблюдалось, что может свидетельствовать об установлении термодинамического равновесия в эффузионной ячейке. Поскольку измерения проводили в узком интервале температур, относительные интенсивности ионных токов имеют практически постоянные значения. Таким образом, сублимация дипептидов рассматривается как равновесный процесс, и влиянием температуры на дальнейшую фрагментацию молекул можно пренебречь. Если молекулярный ион имеет несколько ионных фрагментов, обычно выбирают наиболее интенсивные из них, для которых определяют ионные токи (IT), а затем вычисляют энтальпии сублимации с использованием второго закона термодинамики.
Сублимация L-Ala-L-Trp и DL-Ala-DLNvl происходила без разложения в исследованных диапазонах температур. Значения энтальпии сублимации (${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$(T)) при средней температуре в экспериментальном диапазоне температур были получены с использованием линеаризованной формы уравнения Клаузиуса–Клапейрона [39]:
(1)
$\ln p = - {{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }\left( T \right){\text{/}}RT + C,$Рис. 2.
Зависимости логарифма ионных токов ln(IT) от обратной температуры (1/T) для DL-alanyl-DL-norvaline (ионы m/z: 72 ($\square $), 99 ($\bigcirc $), 128 ($\vartriangle $)).

Рис. 3.
Зависимости логарифма ионных токов ln(IT) от обратной температуры (1/T) для L-alanyl-L-tryptophan (ионы m/z: 130 ($\square $), 275 ($\bigcirc $)).

Для определения энтальпии сублимации выбраны наблюдаемые температурные зависимости ионных токов с массой (72, 99 и 128) m/z для DL-Ala-DL-Nvl и (130 и 275) m/z для L-Ala-L-Trp. Обработка данных методом наименьших квадратов позволила получить значения энтальпии сублимации при средней температуре экспериментов (Tm), представленные в табл. 4. Указанные погрешности для значений ${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$(T) включают двойное стандартное отклонение наклона B, а также погрешности, отражающие ошибки калибровки и измерения температуры.
Таблица 4.
Значения молярной теплоемкости твердой фазы при T = 298.15 K, $C_{{p{\text{,m}}}}^{^\circ }$(cr) (298.15 K), стандартной молярной энтальпии сублимации, ${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$(Tm), при средней температуре эксперимента, Tm, и при T = 298.15 K, ${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$(298.15 K), молярной энтальпии растворения, ${{\Delta }_{{{\text{sol}}}}}H_{{\text{m}}}^{\infty }$, и молярной энтальпии сольватации, ${{\Delta }_{{{\text{solv}}}}}H_{{\text{m}}}^{\infty }$, в воде и объемы Ванн дер Вальса, Vw, для некоторых дипептидов
| Пептиды | $C_{{p{\text{,m}}}}^{^\circ }$(cr) (298.15 K), Дж моль–1 K–1 |
${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$(Tm), кДж моль–1 |
Tm, K | ${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$ (298.15 K), кДж моль–1 |
${{\Delta }_{{{\text{sol}}}}}H_{{\text{m}}}^{\infty }$, кДж моль–1 |
–${{\Delta }_{{{\text{solv}}}}}H_{{\text{m}}}^{\infty }$, кДж моль–1 |
$V_{{\text{w}}}^{{\text{c}}}$, Ǻ3 |
|---|---|---|---|---|---|---|---|
| Gly-L-Ala | 168 [31] | 107 ± 8 [19] | 432.15 | 109 ± 9 | 0.61 [54] | 108.4 | 120.5 |
| DL-Ala-Gly | 172 [31] | – | – | 103.7 ± 5 [53] | 1.30 [55] | 102.4 | 121.9 |
| L-Ala-L-Ala | 195 [31] | 113 ± 7 [19] | 451.15 | 118 ± 8 | –11.01 [56] | 129.0 | 137.3 |
| DL-Ala-DL-Ala | 189 [31] | – | – | 116 ± 8 [12] | –7.59 [57] | 123.5 | 137.4 |
| DL-Ala-DL-Val | 240 [31] | 156 ± 4 [19] | 436.15 | 160 ± 5 | –5.68 [55] | 165.6 | 165.4 |
| DL-Ala-DL-Nvl | 276 ± 0.6 | 177 ± 3 | 477.15 | 184.5 ± 3.6 | 3.03 [55] | 180.9 | 168.7 |
| L-Ala-L-Trp | 284 ± 0.8 | 173 ± 4 | 466.15 | 180.7 ± 4.1 | 11.06 [58] | 168.9 | 233.5 |
Примечание. Для ${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$(Tm) ошибка экспериментального определения средней величины равна двум стандартным отклонениям; величина Vw рассчитана по данным [52].
Tm – средняя температура экспериментов (Tm = 〈T〉).
Стандартная молярная энтальпия сублимации ${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$(298.15 K) при (p° = 0.1 MПa; T = 298.15 K) может быть определена из экспериментально измеренных значений ${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$(T) с помощью уравнения, предложенного в работах Чикоса и Акри [59, 60]:
(3)
$\begin{gathered} {{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }(298.15\;{\text{K}}) = {{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }(T) + [0.75 + \\ + \;0.15C_{{p{\text{,m}}}}^{^\circ }({\text{cr}})][T--298.15]{\text{/}}1000, \\ \end{gathered} $С ростом алифатической боковой цепи молекул дипептидов и введением гетероциклического кольца (в случае L-Ala-L-Trp) наблюдается увеличение молярной энтальпии сублимации в ряду DL-Ala-Gly, Gly-L-Ala, Dl-Ala-DL-Ala, L-Ala-L-Ala, DL-Ala-DL-Val, L-Ala-L-Trp, и DL-Ala-DL-Nvl. Величина энтальпии сублимации отражает силы межмолекулярных взаимодействий, существующие в твердом состоянии, а также может характеризовать стабильность кристаллической структуры соединений. Важные вклады в кристаллическую упаковку исследованных дипептидов вносят Ван-дер-Ваальсовы, дисперсионные и электростатические взаимодействия, а также образование водородных связей [13, 61–63].
Анализ данных, приведенных в табл. 4, показал, что значения ${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$ возрастают симбатно со значениями $C_{{p{\text{,m}}}}^{^\circ }$(cr) (рис. 4). В результате получено простое линейное соотношение для стандартных молярных энтальпий сублимации:
(4)
$\begin{gathered} {{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ } = (--15.56 \pm 6.7) + \\ + \;(0.7084 \pm 0.045)C_{{p{\text{,m}}}}^{^\circ }({\text{cr}}) \\ \end{gathered} $Рис. 4.
Зависимости молярной энтальпии сублимации (${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$) от молярной теплоемкости кристаллических дипептидов ($C_{{p{\text{,m}}}}^{^\circ }$(cr)): Gly-L-Ala (1), DL-Ala-Gly (2), DL-Ala-DL-Ala (3), L-Ala-L-Ala (4), DL-Ala-Dl-Val (5), DL-Ala-DL-Nvl (6) и L-Ala-L-Trp (7).

Важно отметить, что пептиды существуют в цвиттер-ионной форме в кристаллах и в водном растворе; в газовой фазе пептиды находятся в нейтральной молекулярной форме [17, 64]. В водных растворах имеет место соольватация (гидратация) как заряженных концевых групп (${\text{NH}}_{3}^{ + }$, COO–) в основной цепи, так и различных боковых цепей молекул, что находит отражение в различии величин энтальпий сольватации, наблюдаемых в ряду дипептидов. Молярные энтальпии сольватации при бесконечном разбавлении (i.d.) (${{\Delta }_{{{\text{solv}}}}}H_{{\text{m}}}^{\infty }$) пептидов в воде определены по разности между их стандартными молярными энтальпиями растворения при i.d. (${{\Delta }_{{{\text{sol}}}}}H_{{\text{m}}}^{\infty }$) и стандартными молярными энтальпиями сублимации (${{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }$):
(5)
${{\Delta }_{{{\text{solv}}}}}H_{{\text{m}}}^{\infty } = {{\Delta }_{{{\text{sol}}}}}H_{{\text{m}}}^{\infty } - {{\Delta }_{{{\text{sub}}}}}H_{{\text{m}}}^{^\circ }.$Рис. 5.
Корреляция молярной энтальпии сольватации (${{\Delta }_{{{\text{solv}}}}}H_{{\text{m}}}^{\infty }$) дипептидов в водном растворе с показателем гидрофобности ($\lg P$) для DL-Ala-Gly (1), Gly-L-Ala (2), DL-Ala-DL-Ala (3), L-Ala-L-Ala (4), DL-Ala-Dl-Val (5), L-Ala-L-Trp (6) и DL-Ala-DL-Nvl (7).

Таким образом, в данном исследовании мы применили эффузионный метод Кнудсена с масс-спектрометрическим контролем состава паров для нахождения энтальпии сублимации дипептидов, DL-аланил-DL-норвалина и L-аланил-L-триптофана. Получены масс-спектры электронной ионизации DL-Ala-DL-Nvl и L-Ala-L-Trp. Методом ДСК измерены изобарные теплоемкости кристаллических DL-Ala-DL-Nvl и L-Ala-L-Trp в интервале температур (288–333) K. Впервые получены молярные энтальпии сублимации DL-Ala-DL-Nvl и L-Ala-L-Trp в температурных интервалах (446–491) K и (458–485) K, соответственно. Стандартные молярные энтальпии сублимации соединений при T = 298.15 K определены. Предложена линейная корреляция для оценки энтальпии сублимации дипептидов аланинового ряда.
Определены молярные энтальпии сольватации (${{\Delta }_{{{\text{solv}}}}}H_{{\text{m}}}^{\infty }$) растворенных веществ при T = = 298.15 K на основе использования полученных стандартных молярных энтальпий сублимации и имеющихся в литературе стандартных молярных энтальпий растворения (${{\Delta }_{{{\text{sol}}}}}H_{{\text{m}}}^{\infty }$) дипептидов в воде. Показано, что более отрицательные значения ${{\Delta }_{{{\text{solv}}}}}H_{{\text{m}}}^{\infty }$ для водных растворов, содержащих DL-Ala-DL-Nvl и L-Ala-L-Trp, по сравнению с растворами других дипептидов, по-видимому, означают, что взаимодействия между цвиттер-ионными формами растворенных веществ и молекулами воды усиливаются с увеличением размера молекул дипептида и гидрофобности их боковых цепей.
Авторы выражают огромную благодарность профессору Г.В. Гиричеву за обсуждение масс-спектрометрических данных и особенностей сублимации пептидов.
Измерения теплоемкости выполнены на оборудовании центра коллективного пользования “Верхневолжский региональный центр физико-химических исследований” (http://www.isc-ras.ru/ ru/struktura/ckp) в рамках проекта № 01201260481 ИХР РАН.
Список литературы
Boldyreva E.V. Models, Mysteries, and Magic of Molecules. Berlin: Springer Verlag, 2007. P. 169–194.
Ketabi S., Rahmani L. // Mater. Sci. Eng. 2017. V. 73C. P. 173.
Кобаяси Н. Введение в нанотехнологию. М.: Бином, Лаборатория знаний, 2005. 134 с.
Агафонов А.В., Иванов К.В., Давыдова О.И. и др. // Журн. неорган. химии. 2011. Т. 56. № 7. С. 1087. [Russ. J. Inorg. Chem. 2011. V. 56. P. 1025.]
Li L., Ma R., Ebina Y.N. et al. // Chem. Mater. 2005. V. 17. P. 4386.
Ding L., Stilwell J., Zhang T. et al. // Nano Lett. 2005. V. 5. P. 2448.
Yevdokimov Yu.M., Sytchev V.V. // Russ. Chem. Rev. 2008. V. 77. P. 193.
Adler-Abramovich L., Reches M., Sedman V.L. et al. // Langmuir. 2006. V. 22. P. 1313.
Naef R., Acree Jr., W.E. // Molecules. 2017. V. 22. P. 1059.
Riffet V., Bouchoux G. // Phys. Chem. Chem. Phys. 2013. V. 15. P. 6097.
Blokhina S., Sharapova A., Ol’khovich M. et al. // J. Chem. Thermodynamics. 2017. V. 105. P. 37.
Dorofeeva O.V., Ryzhova O.N. // J. Phys. Chem. A. 2014. V. 118. P. 3490.
Kitaigorodskii A.I. Molecular crystals and molecules. New York: Academic Press, 1973.
No K.T., Kwon O.Y., Kim S.Y. et al. // J. Phys. Chem. 1995. V. 99. P. 13019.
Tyunina E.Yu., Badelin V.G. // Biophisics. 2005. V. 50. P. 835.
Chilikian T.V. // J. Phys. Chem. B. 2001. V. 105. P. 12566.
Якубке Х.-Д., Ешкайт Х. Аминокислоты, пептиды, белки. М.: Мир, 1985. 456 с.
De Kruif C.G., Voogd J., Offringa J.C.A. // J. Chem. Thermodynamics. 1979. V. 11. P. 651.
Баделин В.Г., Тюнина Е.Ю., Краснов А.В. и др. // Журн. физ. химии. 2012. Т. 86. № 3. С. 528. [Russ. J. Phys. Chem. A. 2012. V. 86. P. 457.]
Баделин В.Г., Тюнина Е.Ю., Гиричев Г.В. и др. // Журн. структ. химии. 2007. Т. 48. № 4. С. 698. [Russ. J. Struct. Chem. 2007. V. 48. P. 647.]
Svec H.J., Junk G.A. // J. Am. Chem. Soc. 1964. V. 86. P. 2278.
Junk G., Svec H. // J. Am. Chem. Soc. 1963. V. 85. P. 839.
Banoub J.H., Newton R.P., Esmans E. et al. // Chem. Rev. 2005. V. 105. P. 1869.
Song T., Hao Q., Law Ch.-H. et al. // J. Am. Soc. Mass Spectrom. 2012. V. 23. P. 264.
Demeure K., Gabilica V., De Pauw E.A. // J. Am. Soc. Mass Spectrum. 2010. V. 21. P. 1906.
Viegra-Eusebio M.T., Rojas A. // J. Chem. Eng. Data. 2011. V. 56. P. 5008.
Knyazev A.V., Letyanina I.A., Plesovskikh A.S. et al. // Thermochimica Acta. 2014. V. 575. P. 12.
Арнаутова Е.А., Захарова М.В., Пивина Т.С. и др. // Изв. АН. Сер. хим. 1996. Т. 45. № 12. С. 2723.
Acree Jr. W.E., Chickos J.S. // J. Phys. Chem. Ref. Data. 2010. V. 39. P. 1.
Сагадеев Е.В., Гимадеев А.А., Барабанов В.П. // Журн. физ. химии. 2010. Т. 84. № 2. С. 260. [Russ. J. Phys. Chem. A. 2010. V. 84. P. 209.]
Badelin V.G., Kulikov O.V., Vatagin V.S. et al. // Thermochimica Acta. 1990. V. 169. P. 81.
Chickos J.S. // Thermochimica Acta. 1998. V. 313. P. 19.
Тюнина Е.Ю., Крутова О.Н., Лыткин А.И. // Изв. Вузов. Хим. хим. технол. 2021. Т. 64. С. 12.
Tyunina E.Yu., Badelin V.G., Mezhevoi I.N. // J. Mol. Liq. 2019. V. 278. P. 505.
Tyunina V.V., Krasnov A.V., Badelin V.G. et al. // J. Chem. Thermodynamics. 2016. V. 98. P. 62.
Kulikov O.V., Badelin V.G., Krestov G.A. et al. // J. Solution Chem. 1993. V. 22. P. 59.
Tyunina V.V., Krasnov A.V., Tyunina E.Yu. et al. // J. Chem. Thermodynamics. 2019. V. 135. P. 287.
Tyunina E.Yu., Mezhevoi I.N., Dunaeva V.V. // J. Chem. Thermodynamics. 2020. V. 150. P. 106206.
Пентин Ю.А., Вилков Л.В. Физические методы исследования для химии. M.: Мир, 2006. 683 с.
Copland E.H., Jacobson N.S. // Electrochem. Soc. Interface. 2001. V. 10. P. 28.
Tyunina V.V., Krasnov A.V., Tyunina E.Yu. et al. // J. Chem. Thermodynamics. 2014. V. 74. P. 221.
Ribeiro da Silva M.A.V., Monte M.J.S., Santos L.M.N.B.F. // J. Chem. Thermodynamics. 2006. V. 38. P. 778.
Sabban R., Xu-wu A., Chickos J.S. et al. // Thermochim. Acta. 1999. V. 331. P. 93.
Svec H.J., Clyde D.D. // J. Chem. Eng. Data. 1965. V. 10. P. 151.
Della Gatta G., Richardson M.J., Sarge S.M. et al. // Pure Appl. Chem. 2006. V. 78. P. 1455.
Wieser M.E. // Pure Appl. Chem. 2011. V. 382. P. 17.
Biemann K., Cone C., Webster B.R. et al. // J. Am. Chem. Soc. 1966. V. 88. P. 5598.
Biemann K., Gapp F., Seibl J. // J. Am. Chem. Soc. 1959. V. 81. P. 2274.
NIST Standard Reference Database. Number 69; http: //webbook.nist.gov/chemistry
Вульфсон Н.С., Заикин В.Г., Микая А.И. Масс-спектрометрия органических соединений. М.: Химия, 1986. 157 с.
Fales H.M., Milne G.W.A., Winkier H.U. et al. // Anal. Chem. 1975. V. 47. P. 207.
Кузьмин В.С., Кацер С.Б. // Изв. Академии наук. Сер. химич. 1992. Т. 41. С. 922.
Баделин В.Г., Смирнов В.И., Межевой И.Н. // Журн. физ. химии. 2002. Т. 76. № 7. С. 1299.
Smirnov V.I. // J. Chem. Thermodynamics. 2021. V. 159. P. 106481.
Смирнов В.И., Баделин В.Г. // Журн. физ. химии. 2018. Т. 92. № 5. С. 732. [Russ. J. Phys. Chem. A. 2018. V. 92. P. 900.]
Смирнов В.И., Баделин В.Г. // Там же. 2008. Т. 82. № 7. С. 1359. [Russ. J. Phys. Chem. A. 2008. V. 82. P. 1206.]
Piekarski H., Nowicka B. // J. Therm. Anal. Calorim. 2010. V. 102. P. 31.
Rodante F., Fantauzzi F., Catalani G. // Thermochimica Acta. 1997. V. 296. P. 15.
Chickos J.S., Acree Jr. W.E. // J. Phys. Chem. Ref. Data. 2002. V. 31. P. 537.
Gutterman A., Rath N., Chickos J. // J. Chem. Eng. Data. 2013. V. 58. P. 749.
Калоус В., Павличек З. Биофизическая химия. М.: Мир, 1985. 446 с.
Gavezzotti A. // Acta Crystallogr. 1987. V. B43. P. 559.
Vinogradov S.N. // Int. J. Peptide Prot. Res. 1979. V. 14. P. 281.
Молекулярные взаимодействия / Под ред. Г. Ратайчак, У. Орвилл-Томаса. М.: Мир, 1984. 600 с.
Palecz B. // J. Am. Chem. Sos. 2002. V. 124. P. 6003.
Palekar D., Hiue M., Lien E.J. // Pharm. Res. 1996. V. 13. P. 1191.
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


