Физика и химия стекла, 2020, T. 46, № 2, стр. 174-183
Гемолитическая активность и сорбционная способность наночастиц цеолита Beta
Н. Ю. Ульянова 1, Л. Н. Куриленко 1, О. В. Шамова 2, Д. С. Орлов 2, О. Ю. Голубева 1, *
1 Институт химии силикатов им. И.В. Гребенщикова РАН
199034 Санкт, Петербург, наб. Макарова, 2, Россия
2 Институт экспериментальной медицины
197376 Санкт-Петербург, ул. акад. Павлова, 12, Россия
* E-mail: olga_isc@mail.ru
Поступила в редакцию 06.07.19
После доработки 18.10.19
Принята к публикации 05.12.19
Аннотация
Работа посвящена изучению влияния условий синтеза на гидротермальную кристаллизацию наночастиц цеолита со структурой Beta и исследованию их свойств. Экспериментально определены оптимальные условия получения наночастиц цеолита Beta различного размера путем варьирования температурно-временных параметров процесса. Синтезированные образцы охарактеризованы методами рентгеновского дифракционного анализа, сканирующей электронной микроскопии, низкотемпературной адсорбции азота. Исследована сорбционная способность образцов цеолитов разных размеров по отношению к неорганическим катионам (на примере ионов свинца) и органическим молекулам (на примере тиамина гидрохлорида), а также их гемолитическая активность в отношении эритроцитов человека. Установлено, что сорбционная способность образцов снижается при увеличении размеров частиц. Впервые получены результаты зависимости гемолитической активности наночастиц от их размера. На основании полученных результатов сделаны выводы о возможности применения наноцеолитов в медицине.
ВВЕДЕНИЕ
Синтетические пористые алюмосиликаты с заданными характеристиками являются перспективными материалами для решения целого круга актуальных междисциплинарных задач, связанных с разработкой новых лекарственных препаратов, систем их доставки, новых катализаторов и сорбентов [1–7]. Одной из быстро развивающихся отраслей фармацевтической промышленности является создание новых лекарственных форм пролонгированного действия на основе матриц-носителей, обеспечивающих направленный транспорт в орган-мишень. Актуально применение наноцеолитов в медицинских целях, в частности, для адресной доставки лекарственных препаратов. Часто к наночастицам относят частицы с размером менее 100 нм, однако при исследовании цеолитов природного происхождения размеры частиц лежат в микрометровом диапазоне. В случае синтетических цеолитов, наночастицами можно считать частицы, которые представляют собой кристаллиты или агломераты кристаллитов, менее 500 нм [8–11]. Более того, цеолиты интересны в качестве сорбентов медицинского назначения, их структура характеризуется высокой пористостью, наличием полостей и каналов. Большая внутренняя поверхность определяет адсорбционную емкость, которая влияет на эффективность сорбции.
В связи с этим, особый интерес представляет направленный синтез цеолитов, позволяющий регулировать дисперсность частиц, их пористо-текстурные характеристики, в том числе, удельную поверхность и удельный объем пор. Размер кристаллов, в свою очередь, зависит от соотношения скоростей образования центров кристаллизации и роста кристаллов, что также можно контролировать варьированием условий синтеза. В настоящее время активно развивается направление по получению наноразмерных цеолитов, при этом используются различные подходы к синтезу [12, 13]. Большинство из них основаны на использовании в качестве кристаллизационной среды различных органических растворителей, таких как диметилформамид, толуол, либо сложных органических прекурсоров [14, 15]. Недостатками таких подходов являются как сложность самого процесса синтеза, так и применение токсичных органических соединений. Таким образом, в настоящее время существует потребность в альтернативных простых и недорогих способах получения. Одним из таких относительно простых способов получения наноразмерных цеолитов является варьирование температурно-временных параметров процесса гидротермальной кристаллизации.
Поскольку одной из перспективных областей применения наноразмерных цеолитов является медицина, то существует необходимость исследования биологической активности таких частиц. Размер частиц обуславливает реакционную высокую активность, что может иметь как положительное, так и негативное влияние [16]. Крайне важно изучить влияние размерности наночастиц вообще и синтетических наноцеолитов в частности на их токсичность и гемолитическую активность, а также на изменения в сорбционной способности.
Целью работы является исследование влияния условий синтеза на дисперсность частиц цеолита со структурой Beta, сравнение физико-химических свойств полученных наночастиц различного размера и биологической активности с целью оценки возможности их дальнейшего применения для решения задач медицины.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез цеолитов. Синтез цеолита Beta проводили с использованием методики [17, 18], путем гидротермальной кристаллизации геля следующего состава (в мол. дол.): 2.2Na2O · Аl2O3 · 50SiO2 ⋅ 4.6(TEA)2О ⋅ 444H2O, где (TEA)2O – оксид тетраэтиламмония. В качестве исходных реактивов для синтеза использовали реактивы фирмы Sigma Aldrich высокой степени чистоты – гидроксид натрия (водный раствор, 50 мас. %), тетраэтиламмония гидроксид (водный раствор, 35 мас. %), натрия хлорид (“ч.”, ГОСТ 4233-77), натрия алюминат, калия хлорид (“х. ч.”, ГОСТ 4234-77), кремния (IV) оксид (LUDOX HS-40 водный раствор, 40 мас. %), деионизированная вода. Кристаллизацию геля проводили в стальных автоклавах с тефлоновыми вкладышами в интервале температур 90–140°С в течение различного периода времени (от 48 ч до 10 суток). Полученные образцы осаждали путем центрифугирования (центрифуга HeroLab HiCen F) и высушивали в термостате при 100°С. Для дальнейших исследований образцы прокаливали при температуре 550°С в течение 4 ч со скоростью нагревания 4°С/мин для удаления сорбированной воды и остатков органических молекул. Мольные отношения Н2О/SiO2, Al2О3/SiO2 во всех режимах были одинаковыми.
Методы исследования. Фазовый состав образцов определяли на порошковом дифрактометре D8-Advance (Bruker) (CuKα-излучение). Фазовый анализ проведен с использованием международной базы данных ICDD-2006.
Удельную поверхность и объем пор образцов оценивали по данным низкотемпературной адсорбции азота (Quantachrome NOVA 1200е) с использованием метода Лэнгмюра. Обработку полученных экспериментальных данных (анализ размеров пор и их распределение по размерам) проводили с помощью программного обеспечения NOVAWin. Погрешность при определении удельной поверхности составляла 1%. Навески исследуемых образцов в виде порошка составляли 0.1 ± 0.02 г.
Размер частиц цеолита определяли по изображениям сканирующей электронной микроскопии (СЭМ), полученным на приборе VEGA3 TESCAN, погрешность составляет 5%. Образцы готовили с использованием метода напыления углеродных пленок.
Дополнительно размер частиц оценивали методом динамического рассеяния света на лазерном анализаторе размера частиц Nanotrac, погрешность измерения ±3 нм [19]. Для проведения измерений 25 мг цеолита добавляли к 10 мл деионизированной воды. Полученную таким образом полидисперсную систему подвергали ультразвуковой обработке в течении 15 мин. Отбирали 2 мл суспензии и проводили измерения.
Гемолитическая активность наночастиц серебра в отношении эритроцитов человека была исследована с использованием методики [20]. Кровь, полученную от здоровых доноров и стабилизированную гепарином, центрифугировали при 300 g при температуре 4°С в течение 10 мин. К осадку добавляли фосфатно-солевой буферный раствор (ФСБР – 0.02 М натрий фосфатный буфер, содержащий 0.15 М хлорид натрия, рН 7.2–7.4) и центрифугировали в тех же условиях. Процедуру отмывания эритроцитов повторяли три раза. Из полученного осадка эритроцитов отбирали 280 мкл, доводили объем суспензии до 10 мл охлажденным ФСБР. К исследуемым препаратам в ФСБР добавляли суспензию эритроцитов (90 мкл суспензии на 10 мкл препарата), конечная концентрация препаратов в пробе составляла 1 и 10 мг/мл. Для получения положительного (100% лизис эритроцитов) и отрицательного (0% лизис эритроцитов) контролей в пробы вместо исследуемых препаратов вносили 10% Triton X-100 или ФСБР, соответственно. Пробы инкубировали в течение 30 мин при 37°С при периодическом перемешивании. По окончании инкубации реакцию останавливали добавлением охлажденного ФСБР и центрифугировали пробы при 3000 g в течение 4 мин. Супернатант отбирали и вносили в ячейки 96-луночного планшета (Costar, Corning Inc., США). Измерение оптической плотности проб при длине волны 540 нм (OD540), производили на спектрофотометре SpectraMax 250 фирмы Molecular Devices, США. Процент гемолиза эритроцитов подсчитывали по формуле [21]:
(1)
${\text{Гемолиз}}\left( {\text{\% }} \right) = {\text{\;}}\frac{{{\text{O}}{{{\text{D}}}_{{540}}}\left( {{\text{образца}}} \right) - {\text{O}}{{{\text{D}}}_{{540}}}\left( {0{\text{\% \;лизис}}} \right)}}{{{\text{O}}{{{\text{D}}}_{{540}}}\left( {100{\text{\% \;лизис}}} \right) - {\text{\;O}}{{{\text{D}}}_{{540}}}\left( {0{\text{\% \;лизис}}} \right)}} \times 100{\text{\% ,}}$Исследование сорбционной способности образцов по отношению к ионам свинца проводили с использованием сорбционно-фильтрационного метода в модельных растворах нитрата свинца (Pb(NO3)2, 99%, Sigma Aldrich) заданной концентрации с использованием модифицированной методики, описанной в [22–24].
Образцы для исследований предварительно сушили при 110°С в течение 2 ч. Образцы обрабатывали раствором нитрата свинца (II) с концентрацией 300 мг/л, время контакта раствора с сорбентом составляло 5 мин. Навеска цеолита была постоянной и составляла 0.2 г, объем раствора нитрата свинца (II) 100 мл. Образцы обрабатывали в изотермических условиях при температуре (25 ± 1)°С. Далее раствор фильтровали на бумажном фильтре, после чего проводили химический анализ фильтрата на содержание соответствующих ионов. Общее содержание ионов свинца в растворе определяли методом пламенной фотометрии на атомно-абсорбционном спектрометре iCE3000 с точностью ±2% отн.
Оценку сорбционных свойств по отношению к органическим молекулам проводили на примере витамина В1 (тиамина гидрохлорида). К 20 мл 0.002 М раствора тиамина гидрохлорида добавляли 0.15 г сорбента. Концентрацию исходного раствора тиамина гидрохлорида рассчитывали по формуле:
где С0 – концентрация исходного раствора тиамина гидрохлорида, q – навески тиамина, V – объем раствора, М.м – молекулярная масса тиамина.Через заданные промежутки времени отбирали пробы фильтрата для измерения оптической плотности раствора на УФ-спектрофотометре при длине волны λ = 242 нм. Количество адсорбированного тиамина в момент времени t рассчитывали по уравнению:
где ${{С}_{0}}$ и ${{С}_{t}}$ концентрации тиамина в растворе при t = 0 и в момент времени t, V – объем раствора, m – масса адсорбента.РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В табл. 1 представлено описание использованных методик с разными температурно-временными режимами получения цеолитов.
Таблица 1.
Влияние температуры и продолжительности синтеза на фазовый состав и размер частиц
| Номер режима температурно-временных параметров | Время синтеза, ч | Температура, °С | Размер частиц, нм |
Обозначение образцов |
|---|---|---|---|---|
| I | 48 | 140 | 350 | B350 |
| II | 264 | 120 | 220 | B220 |
| III | 264 | 90 | 190 | B190 |
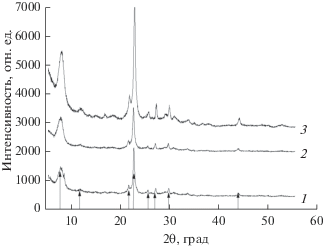
На рис. 1 приведены дифрактограммы синтезированных образцов, которые совпадают со штрих-диаграммами стандарта цеолита Beta (карточка № 560 467 в базе данных ICCD-2006).
Рис. 1.
Рентгеновские дифрактограммы цеолитов, полученных по методикам: B350 (1), B220 (2), B190 (3). Треугольники – штрих-диаграмма стандарта цеолита Beta.
На рис. 2а–в представлены результаты сканирующей электронной микроскопии, которые позволяют оценить размеры образцов, полученных в разных условиях. Размеры частиц были определены для методик, обозначенных как режимы синтеза I, II, III и составили 350, 220, 190 нм. Использование разных температурно-временных режимов приводит к образованию однородных микросфер с узким распределением по размерам. Также на микрофотографиях встречаются агломераты, причем с уменьшением размера кристаллов увеличивается степень их агрегации.
Рис. 2.
Электронные микрофотографии образца цеолита Beta, полученного при разных условиях: режим I (а), режим II (б), режим III (в).

Дополнительно размер частиц оценивали с помощью метода динамического рассеяния света на приборе Nanotrac, результаты процентного распределения по размерам приведены на рис. 3, 4. Расчет среднего размера частиц проведен с помощью программного обеспечения Nanotrac FLEX, которое учитывает такие параметры, как средний диаметр объемного распределения, распределение интенсивности сигнала, распределение области, а также расчетную область определенной поверхности и стандартное отклонение.
Рис. 3.
Распределение частиц по размерам по данным динамического рассеяния света: B350 (а), B220 (б), B190 (в).

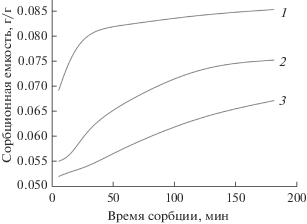
Рис. 4.
Кинетические кривые сорбции тиамина гидрохлорида для образцов: B350 (1), B220 (2), B190 (3).
Средний размер частиц, определенный в водной суспензии с использованием метода динамического рассеяния света, согласуется с результатами, полученными из изображений сканирующей электронной микроскопии.
По представленным в табл. 1 данным видно, что происходит уменьшение размеров частиц цеолита Beta с увеличение времени синтеза. При уменьшении температуры до 120°С цеолит кристаллизуется за 264 ч. Также однофазный цеолит Beta может быть получен при 90°С за 264 ч (11 суток).
В табл. 2 приведены результаты анализа изотерм адсорбции азота образцов цеолита Beta с разным размером частиц, рассчитаны основные характеристики пористости: диаметр и объем пор, удельная поверхность (Sуд).
Таблица 2.
Удельная поверхность, объем и диаметр пор образцов
| Образец | Sуд, м2/г | Vпор, см3/г | d, нм |
|---|---|---|---|
| B350 | 728 | 0.393 | 1.2 |
| B220 | 705 | 0.367 | 1.2 |
| B190 | 580 | 0.432 | 1.3 |
По данным низкотемпературной адсорбции азота видно, что удельная поверхность образцов меняется с изменением размера частиц. С уменьшением размеров частиц удельная поверхность образцов снижается, при этом объем пор возрастает. Объяснить это можно заметно более высокой степенью агломерации образцов с диаметром частиц 190 и 220 нм. Размеры агломератов в ряде случаев достигают 1 мкм. Далее образцы будут обозначены как B350, B220, B190.
Результаты исследования сорбционной способности образцов B350, B220, B190 по отношению к ионам свинца приведены в табл. 3. Для проведения сорбции использовали раствор Pb(NO3)2 с концентрацией 300 мг/мл.
Таблица 3.
Результаты химического анализа растворов Pb(NO3)2 после сорбции образцами цеолитов
| Образец | С5 min (Pb(NO3)2) в растворе после сорбции цеолитом, мкг/мл |
|---|---|
| Исходный раствор Pb(NO3)2 | 300 |
| B350 | 74.3 |
| B 220 | 149.3 |
| B190 | 160.6 |
По данным, представленным в табл. 3, определена зависимость между сорбционной способностью цеолита Beta и размером частиц. Она уменьшается с уменьшением размера частиц в ряду B350 > B220 > B190. Это может быть объяснено степенью доступности внутрикристаллической поверхности в условиях адсорбционного процесса.
Результаты исследования сорбционной способности образцов по отношению к молекулам тиамина гидрохлорида представлена на рис. 4.
Сорбционная способность цеолитов по отношению к тиамину гидрохлориду также уменьшается с уменьшением размера частиц. При этом формы кинетических кривых сорбции у исследованных образцов разные. Так, сорбционное равновесие для образца с размерами частиц 350 нм наступает через 180 мин, а в первые 25 мин процесс сорбции идет с максимальной скоростью, после чего скорость адсорбции снижается, и кривая более пологая. Для образца с размерами части 220 нм начало процесса также идет с нарастанием скорости, но гораздо медленнее, чем для образца с размерами частиц 350 нм. Для образца B190 характерно протекание процесса сорбции с одинаковой скоростью, при этом сорбционное равновесие за 180 мин так и не было достигнуто. Особенности процесса сорбции могут быть связаны как с размерами частиц, так и с их агломерацией. Степень агломерации частиц, как уже отмечалось выше, возрастает в ряду B350 < B220 < B190.
Образец B350 характеризуется самой высокой сорбционной емкостью, составляющей 0.85 г/г. Наименьшую сорбционную емкость 0.075 г/г показал образец с наименьшим размером частиц 190 нм. Соотношение вкладов внутрикристаллической и внешней поверхности, вероятно, определяет различия в сорбционной способности исследуемых цеолитов.
Результаты исследования гемолитической активности представлены в табл. 4. Измерения проводили при двух концентрациях цеолитов в исследуемых препаратах – 10 и 1 мг/мл. Полученные результаты свидетельствуют о том, что с уменьшением размера частиц цеолитов гемолитическая активность образцов уменьшается. Наиболее ярко эта тенденция проявляется при более высокой концентрации цеолитов – 10 мг/мл. Гемолитическая активность – это способность того или иного вещества повреждать мембраны красных кровяных клеток и вызывать их лизис (гемолиз), сопровождающийся утечкой внутриклеточных молекул эритроцитов, в том числе гемоглобина, и в конечном итоге гибелью этих клеток. По значению гемолитической активности можно сделать вывод о токсичности исследуемого препарата по отношению к клеткам крови. Чем больше значение показателей гемолиза эритроцитов, обработанных образцом, тем более токсичным он является. При контакте образца B350 в концентрации 10 мг/мл наблюдается разрушение около 75% эритроцитов, в то время как для образца B190 эта величина составляет лишь 20%. Некоторое выпадение результатов для образца B220 при той же концентрации может быть связано с достаточно широким распределением частиц по размерам и частичным перекрытием размерного диапазона образца B190 (рис. 3). При снижении концентрации наноцеолитов в исследуемых препаратах до 1 мг/мл также наблюдается тенденция к снижению гемолитической активности образцов с уменьшением их размеров.
Таблица 4.
Гемолиз эритроцитов человека (%), обработанных препаратами наноцеолитов, взятых в разных концентрациях*
| Образец | Концентрация образца, мг/мл | Гемолиз эритроцитов человека, % |
|---|---|---|
| B350 | 10 | 75.0 ± 8.4 |
| 1 | 2.4 ± 0.6 | |
| B220 | 10 | 10.1 ± 2.6 |
| 1 | 1.2 ± 0.6 | |
| Betа190 | 10 | 22.7 ± 3.5 |
| 1 | 0.7 ± 0.3 |
Из полученных результатов следует, что снижение размеров частиц Beta сопровождается снижением их гемолитической активности, т.е. токсичности.
ЗАКЛЮЧЕНИЕ
Проведено исследование влияния условий синтеза на размер частиц цеолита Beta, которое показало снижение размеров частиц цеолита при увеличении времени и уменьшении температуры синтеза. В результате варьирования условий синтеза были получены наноцеолиты со структурой Beta со средним размером частиц 350, 220, 190 нм.
Образцы цеолитов со структурой Beta отличаются значительной сорбционной способностью как по отношению к ионам свинца, так и к органическим молекулам, гидрохлориду тиамина.
Установлено, что уменьшение размеров частиц сопровождается снижением сорбционной емкости образцов и одновременным снижением их токсичности по отношению к клеткам крови человека.
С точки зрения возможного использования цеолитов в медицине в качестве медицинских сорбентов и носителей лекарственных препаратов, оптимальное сочетание сорбционной способности и низкой гемолитической активности позволяет сделать вывод о перспективности образцов цеолитов Beta с размерами частиц 220 и 190 нм.
Список литературы
Тяпкина Е.В. Фармакология препаратов на основе природных алюмосиликатов и их применение в ветеринарии. Автореф. дис. ... канд. Краснодар, 2018. 48 с.
Паничев А.М., Кулаков Ю.В., Гульков А.Н. Применение цеолитов в медицине // Тихоокеанский медицинский журнал. 2003. Т. 14. № 4. С. 21–24.
Кубасов А.А. Цеолиты в катализе: сегодня и завтра // Соросовский образовательный журн. 2000. Т. 6. С. 44–51.
Wong L.W., Sun W.Q., Chan N.W. Zeolite microneedles for Transdermal Drug Delivery // Studies in Surface Science and Catalysis. 2007. P. 525–530.
Rimoli M.G., Rabaioli M.R., Melisi D., Curcio A., Mondello S., Mirabelli R., Abignente E. Synthetic zeolites as a new tool for drug delivery // J. Biomedical Materials Research. Part A. 2007. V. 87A. № 1. P. 156–164.
Попов Ю.В., Мохов В.М., Небыков Д.М., Будко И.И. Наноразмерные частицы вкатализе: получение и использование в реакциях гидрирования и восстановления // Изв. ВолгГТУ. 2014. Т. 12. № 7. С. 5–44.
Niyaz Mohammad Mahmoodi, Mohammad Hosein Saffar-Dastgerdi. Zeolite nanoparticle as a superior adsorbent with high capacity: Synthesis, surface modification and pollutant adsorption ability from wastewater // Microchemical J. 2019. V. 145. P. 74–83.
Mintova S., Jean-Pierre Valtchev, V. Advances in nanosized zeolites // Nanoscale. 2013. V. 5. P. 6693–6703.
Bok T., Onuchin E., Zabil’skaya A., Konnov Stanislav, Knyazeva E., Panov A., Kleimenov A., Ivanova I. Nanocrystalline zeolites beta: Features of synthesis and properties // Petroleum Chemistry. 2016. V. 56. P. 1160–1167.
Knyazeva E.E., Ivanova I.I. Synthesis of Nanoscale Zeolites // Pet. Chem. 2019. V. 59. P. 262.
Mintova S., Jaber M., Valtchev V. Nanosized microporous crystals: emerging applications // Chemical Society Reviews. 2015. V. 44. I. 20. P. 7207–7233.
Gia-Thanh Vuong, Vinh-Thang Hoang, Dinh-Tuyen Nguyen, Trong-On Do. Synthesis of nanozeolites and nanozeolite-based FCC catalysts, and their catalytic activity in gas oil cracking reaction // Applied Catalysis A: General. 2010. № 2. P. 231–239.
Deborath Reinoso, Mar Adrover, Marisa Pedernera. Green synthesis of nanocrystalline faujasite zeolite // Ultrasonics Sonochemistry. 2018. V. 42. P. 303–309.
Cheng X., Mao J., Xinchun Lv., Tao Hua. Fast synthesis of nanosized zeolite beta from a low-seeded, low-templated dry gel with a seeding-steam-assisted conversion method // J. Materials Chemistry A. 2014. № 2. P. 1247–1251.
Shimojima A., Kuroda K. Designed synthesis of nanostructured siloxane–organic hybrids from amphiphilic silicon-based precursors // The Chemical Record. 2006. V. 6. № 2. P. 53–63.
Sean E. Lehman, Sarah C. Larsen. Zeolite and mesoporous silica nanomaterials: greener syntheses, environmental applications and biological toxicity // Environ. Sci.: Nano. 2014. V. 3. № 1. 200 p.
Голубева О.Ю., Ульянова Н.Ю. Стабилизация наночастиц и кластеров серебра в пористых цеолитных матрицах различных структур // Физ. и хим. стекла. 2015. Т. 41. № 5. С. 726–736.
Golubeva O.Yu., Ulyanova N.Yu. Stabilization of Silver Nanoparticles and Clusters in Porous Zeolite Matrices with Rho, Beta, and Paulingite Structures // Glass Phys. Chem. 2015. V. 41. № 5. P. 726–736.
Куликов К.Г., Кошлан Т.В. Определение размеров коллоидных частиц при помощи метода динамического рассеяния света // Журн. технической физики. 2015. Т. 85. № 12. С. 26–32.
Шамова О.В., Орлов Д.С., Кокряков В.Н. Антимикробные пептиды из лейкоцитов русского осетра (Acipenser guldenstadti) // Фундаментальные исследования. 2006. № 1. С. 10–13.
Bock T.K. A Novel Assay to Determine the Hemolytic Activity of Drugs Incorporated in Colloidal Carrier Systems // Pharmaceutical Research. 1994. V. 11. № 4. P. 589–591.
Голубева О.Ю., Ульянова Н.Ю., Масленникова Т.П., Дякина М.П. Сорбционные свойства синтетических гидро- и алюмосиликатов со слоистой, каркасной и нанотрубчатой морфологией по отношению к ионам свинца(II) и парам воды // Физ. и хим. стекла. 2014. Т. 40. № 2. С. 343–350.
Golubeva O.Yu., Maslennikova T.P., Ulyanova N.Yu., Dyakina M. P. Sorption of Lead(II) Ions and Water Vapors by Synthetic Hydro- and Aluminosilicates with Layered, Framework, and Nanotube Morphology // Glass Phys. Chem. 2014. V. 40. № 2. P. 343–350.
Шилина А.С. Сорбционная очистка природных и промышленных вод от катионов тяжелых металлов и радионуклидов новым типом высокотемпературного алюмосиликатного адсорбента // Сорбционные и хроматографические процессы. 2010. Т. 10. № 2. С. 237–245.
Дополнительные материалы отсутствуют.
Инструменты
Физика и химия стекла


