Физика и химия стекла, 2020, T. 46, № 3, стр. 331-336
Получение пористых частиц слоистого перовскитоподобного титаната HLaTiO4
С. А. Курносенко 1, О. И. Силюков 1, *, И. А. Зверева 1
1 Санкт-Петербургский государственный университет
199034 Санкт-Петербург, Университетская наб., 7/9, Россия
* E-mail: oleg.silyukov@spbu.ru
Поступила в редакцию 01.11.2019
После доработки 16.12.2019
Принята к публикации 05.02.2020
Аннотация
Слоистые перовскитоподобные оксиды NaLaTiO4 и K2La2Ti3O10, относящиеся к фазам Раддлесдена–Поппера, были синтезированы с использованием различного избытка карбоната щелочного металла в шихте (30%, 100%, 1000%) и превращены в соответствующие протонированные формы HLaTiO4 и H2La2Ti3O10 путем ионного обмена в водном растворе 0.1 M азотной кислоты. Установлено, что повышение содержания карбоната в реакционной смеси не сказывается на кристаллической структуре соединений, однако в случае NaLaTiO4 существенно влияет на морфологию получаемых в ходе протонирования поликристаллов HLaTiO4, что может быть использовано для целенаправленного получения частиц с порами размера 25–500 нм.
Слоистые перовскитоподобные титанаты ALnTiO4 и A2Ln2Ti3O10 (A = щелочной металл, Ln = La или лантаноид) представляют твердые кристаллические соединения, построенные по блочному принципу, в которых блоки со структурой перовскита толщиной в n = 1 и n = 3 октаэдра TiO6, соответственно, чередуются с межслоевыми пространствами, содержащими щелочные катионы A+. Помимо своих каталитических [1–3], фотокаталитических [4–7] и других практически значимых физико-химических свойств [8–10], данные соединения также интересны возможностью ионообменного замещения межслоевых катионов металла на протоны [11, 12]. Протонированные слоистые перовскитоподобные оксиды HLnTiO4 и H2Ln2Ti3O10 могут служить исходными соединениями для синтеза новых перовскитоподобных объектов с использованием реакций ионного обмена [13, 14], пиролиза [15], интеркаляции [16] и графтинга [17] органических соединений, а также могут применяться для получения перовскитных нанослоев и создания наноструктурированных композитов [18].
Одним из факторов, существенно влияющих на физико-химические свойства слоистых оксидов, является морфология частиц. Контроль размеров кристаллов, удельной площади их поверхности и количества дефектов имеет большое значение для гетерогенного катализа и фотокатализа, поскольку данные параметры определяют эффективность адсорбции реагентов и выраженность электрон-дырочной рекомбинации, непосредственно влияющие на скорость фотокаталитической реакции.
Морфология оксидных частиц преимущественно определяется применяемым методом синтеза. В настоящее время большинство слоистых перовскитоподобных оксидов синтезируется по стандартной керамической технологии, основными преимуществами которой являются простота, хорошая воспроизводимость и высокая кристалличность продуктов. Получаемые по высокотемпературной методике образцы представляют собой агрегаты сросшихся кристаллов (поликристаллы), форма и размеры которых зависят от химической природы, степени помола шихты, температурной программы синтеза и других факторов.
Одним из компонентов шихты для синтеза многих слоистых оксидов, включая титанаты ALnTiO4 и A2Ln2Ti3O10, является карбонат щелочного металла A2CO3, который берется в избытке для компенсации потерь при прокаливании, связанных с его испарением и выплавлением:
(1)
${\text{2Ti}}{{{\text{O}}}_{2}} + {\text{L}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{3}} + {{{\text{A}}}_{{\text{2}}}}{\text{C}}{{{\text{O}}}_{3}} \to 2{\text{ALnTi}}{{{\text{O}}}_{4}} + {\text{C}}{{{\text{O}}}_{2}},$(2)
${\text{3Ti}}{{{\text{O}}}_{2}} + {\text{L}}{{{\text{n}}}_{{\text{2}}}}{{{\text{O}}}_{3}} + {{{\text{A}}}_{{\text{2}}}}{\text{C}}{{{\text{O}}}_{3}} \to {{{\text{A}}}_{{\text{2}}}}{\text{L}}{{{\text{n}}}_{{\text{2}}}}{\text{T}}{{{\text{i}}}_{{\text{3}}}}{{{\text{O}}}_{{10}}} + {\text{C}}{{{\text{O}}}_{2}}.$Во многих работах синтез щелочных форм оксидов проводится с 10–50% избытком карбоната по отношению к стехиометрическому количеству [19–24], однако сведения о влиянии величины избытка карбоната на морфологию и иные характеристики продуктов синтеза в литературе отсутствуют.
В представленной работе показано, что за счет варьирования избытка карбоната щелочного металла, используемого при керамическом методе синтеза слоистых перовскитоподобных титанатов NaLaTiO4 и K2La2Ti3O10, удается влиять на морфологию поликристаллов их протонированных форм, получаемых путем обработки исходных соединений раствором азотной кислоты.
Синтез щелочных форм титанатов NaLaTiO4 и K2La2Ti3O10 проводили по стандартной керамической технологии при атмосферном давлении на воздухе. Реагенты TiO2 (≥99.9%, Вектон), La2O3 (≥99.9%, Вектон), Na2CO3 (≥99.8%, Вектон) и K2CO3 (≥99.8%, Вектон) предварительно прокаливали для удаления следов влаги. Для приготовления шихты оксиды брали в стехиометрических количествах, избыток карбоната варьировали (30%, 100%, 1000%). Шихту тщательно измельчали в агатовой ступке под слоем н-гептана из расчета 30 мин на 1 г. После просушивания шихту прессовали в цилиндрические таблетки массой 1.5 г и диаметром 1.5 см под давлением 50 атм, которые затем помещали в корундовый тигель с крышкой и прокаливали в муфельной печи LOIP LF-7/11-G1 в течение 16 ч при 900°C для NaLaTiO4 и при 1100°C для K2La2Ti3O10. После измельчения таблеток полученные щелочные формы подвергали замещению катионов межслоевых металлов на протоны. Для этого суспензии последних, приготовленные из расчета 5 г титаната на 1 л 0.1 М водного раствора азотной кислоты, перемешивали при комнатной температуре в течение 24 ч, затем осадки отделяли центрифугированием и просушивали в течение 48 ч в эксикаторе над CaO. В результате были получены протонированные формы HLaTiO4 и H2La2Ti3O10.
Фазовый состав полученных образцов контролировали с использованием рентгенодифракционного анализа (дифрактометр Rigaku Miniflex II, излучение CuKα, диапазон углов 2θ = 3°–60°, скорость сканирования 10°/мин, шаг 0.01°). Расчет структурных параметров и размеров кристаллитов выполняли с помощью программного обеспечения DiffracPlus Topas на основании всех наблюдаемых дифракционных максимумов. Морфологию частиц изучали с применением сканирующего электронного микроскопа (СЭМ) Zeiss Merlin с полевым эмиссионным катодом, колонной электронной оптики GEMINI-II и безмаслянной вакуумной системой.
Согласно результатам рентгенодифракционного анализа (рис. 1), как для однослойного, так и для трехслойного титаната были успешно получены исходные щелочные и протонированные формы. Найденные параметры элементарной ячейки в тетрагональной сингонии (табл. 1) согласуются с литературными данными [11, 12], однако можно отметить, что в целом параметры решетки соединений, полученных при 1000% избытке карбоната щелочного металла, отличаются от других в меньшую сторону. Анализ профилей полученных дифрактограмм позволяет определить область когерентного рассеяния для полученных образцов (табл. 1). В случае исходных щелочных форм она составила в среднем порядка 60 нм для NaLaTiO4 и 65 нм для K2La2Ti3O10, для соответствующих протонированных форм область когерентного рассеяния оказалась в среднем на 10 нм меньше, что, помимо наблюдаемых на СЭМ изменений в морфологии образцов, объясняется также и процессами разупорядочения решетки, связанными с ионным обменом и гидратацией.
Рис. 1.
Дифрактограммы титанатов NaLaTiO4 и K2La2Ti3O10, синтезированных с различным избытком карбоната, и их протонированных форм HLaTiO4 и H2La2Ti3O10.
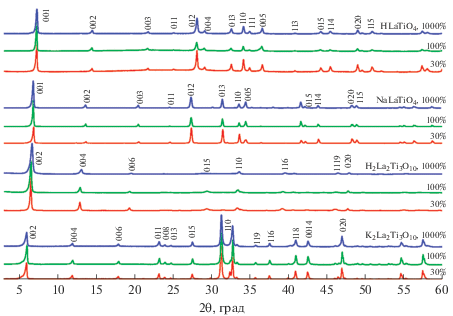
Таблица 1.
Параметры элементарной ячейки в тетрагональной сингонии и размеры кристаллитов щелочных форм титанатов, синтезированных с различным избытком карбоната, и их протонированных форм
| Соединение | Избыток карбоната, % | a, Å | c, Å | Размер кристаллита, нм |
|---|---|---|---|---|
| NaLaTiO4 | 30 | 3.77 | 13.02 | 71 |
| 100 | 3.77 | 13.02 | 87 | |
| 1000 | 3.75 | 12.98 | 67 | |
| HLaTiO4 | 30 | 3.72 | 12.28 | 50 |
| 100 | 3.72 | 12.31 | 51 | |
| 1000 | 3.70 | 12.22 | 51 | |
| K2La2Ti3O10 | 30 | 3.87 | 29.75 | 66 |
| 100 | 3.87 | 29.74 | 66 | |
| 1000 | 3.87 | 29.71 | 52 | |
| H2La2Ti3O10 | 30 | 3.81 | 27.48 | 48 |
| 100 | 3.81 | 27.58 | 38 | |
| 1000 | 3.81 | 27.14 | 28 |
Электронные микрофотографии щелочных и протонированных титанатов, полученных на основе синтезированных с различным избытком карбоната щелочных форм, представлены на рис. 2. Частицы полученных поликристаллов имеют пластинчатую форму, характерную для слоистых оксидов; линейные размеры кристаллов лежат в диапазоне 0.5–2 мкм, толщина 100–250 нм. В случае частиц HLaTiO4 края зерен имеют выраженную неправильную форму, частицы имеют отверстия и борозды, которые не наблюдались для исходных щелочных соединений. По всей видимости, данный факт связан с частичным растворением частиц соединения, как это уже отмечалось ранее [25]. С ростом избытка карбоната заметно возрастает пористость частиц HLaTiO4 (количество и размер отверстий в кристаллах). Так, анализ СЭМ-изображений образца c 30% избытком карбоната позволяет определить, что примерно 5% наблюдаемой поверхности подверглось частичному растворению, средний диаметр полученных пор составляет порядка 50 нм; для образцов с избытком карбоната 100% и 1000% эти показатели возрастают до 10%/150 нм и 35%/250 нм соответственно. В случае H2La2Ti3O10 повышение избытка карбоната до 100% не приводит к существенным изменениям формы частиц, образование цилиндрических пор не наблюдается. При избытке 1000% на изображениях СЭМ наблюдается значительное количество мелких частиц малой толщины и неправильной формы, возможно, полученных в результате частичного расслоения более крупных поликристаллов.
Рис. 2.
Изображения СЭМ титанатов NaLaTiO4 и K2La2Ti3O10, синтезированных с различным избытком карбоната, и их протонированных форм HLaTiO4 и H2La2Ti3O10.

Можно заключить, что титанаты HLaTiO4 и H2La2Ti3O10, относящиеся к фазам Раддлесдена–Поппера, претерпевают разные морфологические изменения при увеличении доли карбоната щелочного металла в шихте. Одной из возможных причин различного поведения данных оксидов являются их структурные особенности: однослойный титанат HLaTiO4 характеризуется малой толщиной перовскитного блока (один титан-кислородный октаэдр), в связи с чем его структура является менее устойчивой по сравнению со структурой титаната H2La2Ti3O10, обладающего перовскитными блоками толщиной в три октаэдра.
Таким образом, показана возможность управления морфологией протонированных форм слоистых перовскитоподобных титанатов путем варьирования избытка карбоната в реакционной смеси. В случае слоистого перовскитоподобного титаната HLaTiO4 удается целенаправленно добиться получения поликристаллических образцов с порами размера порядка 25–500 нм в зависимости от экспериментальных условий. По всей видимости, на интенсивность образования пор влияет скорость кислотного выщелачивания, зависящая от локального состава частиц полученных оксидных соединений, однако требуются дополнительные исследования для детального обоснования этого предположения. Полученные в рамках настоящей работы результаты представляют интерес в связи с возможностью использования рассмотренных слоистых оксидов и их производных в гетерогенном катализе и фотокатализе.
Работа поддержана РНФ (грант № 19-13-00184). Исследования проведены с использованием оборудования ресурсных центров Научного парка СПбГУ “Рентгенодифракционные методы исследования” и “Междисциплинарный ресурсный центр по направлению “Нанотехнологии”.
Список литературы
Силюков О.И., Минич Я.А., Зверева И.А. Получение протонированных производных слоистых перовскитоподобных титанатов висмута // Физ. и хим. стекла. 2018. Т. 44. № 2. С. 147–152.
Campbell K.D. Layered and double perovskites as methane coupling catalysts // Catal. Today. 1992. V. 13. № 2–3. P. 245–253.
Singh S.J., Jayaram R.V. Chemoselective O-tert-butoxycarbonylation of Hydroxy Compounds Using NaLaTiO4 as a Heterogeneous and Reusable Catalyst // Tetrahedron Lett. 2008. V. 49. № 27. P. 4249–4251.
Rodionov I.A., Mechtaeva E.V., Burovikhina A.A., Silyukov O.I., Toikka M.A., Zvereva I.A. Effect of Protonation on the Photocatalytic Activity of the K2La2Ti3O10 Layered Oxide in the Reaction of Hydrogen Production // Monatshefte für Chemie – Chem. Mon. 2018. V. 149. № 2. P. 475–482.
Родионов И.А., Силюков О.И., Уткина Т.Д., Числов М.В., Соколова Ю.П., Зверева И.А. Фотокаталитические свойства и гидратация слоистых перовскитоподобных титанатов A2Ln2Ti3O10 (А = = Li, Na, К; Ln = La, Nd) // Журн. общей химии. 2012. Т. 82. № 7. С. 1064–1070.
Родионов И.А., Силюков О.И., Зверева И.А. Исследование фотокаталитической активности слоистых оксидов – титанатов NaNdTiO4, LiNdTiO4 и HNdTiO4 // Журн. общей химии. 2012. Т. 82. № 4. С. 548–551.
Takata T., Furumi Y., Shinohara K., Tanaka A., Hara M., Kondo N.J. Photocatalytic Decomposition of Water on Spontaneously Hydrated Layered Perovskites // Chem. Mater. 1997. V. 9. № 5. P. 1063–1064.
Petrov A.A., Melnikova N.A., Petrov A.V., Silyukov O.I., Murin I.V., Zvereva I.A. Experimental Investigation and Modelling of the Na+ Mobility in NaLnTiO4 (Ln = La, Nd) Ceramics // Ceram. Int. 2017. V. 43. № 14. P. 10861–10865.
Song S., Ahn K., Kanatzidis M.G., Alonso J.A., Cheng J.-G, Goodenough J.B. Effect of an Internal Electric Field on the Redox Energies of ALnTiO4 (A = Na or Li, Ln = Y or Rare-Earth) // Chem. Mater. 2013. V. 25. № 19. P. 3852–3857.
Thangadurai V., Shukla A., Gopalakrishnan J. Proton Conduction in Layered Perovskite Oxides // Solid State Ionics 1994. V. 73. № 1–2. P. 9–14.
Byeon S., Yoon J.-J., Lee S.-O. A New Family of Protonated Oxides HLnTiO4 (Ln = La, Nd, Sm, and Gd) // J. Solid State Chem. 1996. V. 127. № 1. P. 119–122.
Gopalakrishnan J., Bhat V. A2Ln2Ti3O10 (A = Potassium or Rubidium; Ln = Lanthanum or Rare Earth): a New Series of Layered Perovskites Exhibiting Ion Exchange // Inorg. Chem. V. 26. № 26. P. 4299–4301.
Uppuluri R., Sen Gupta A., Rosas A.S., Mallouk T.E. Soft Chemistry of Ion-Exchangeable Layered Metal Oxides // Chem. Soc. Rev. 2018. V. 47. № 7. P. 2401–2430.
Зверева И.А., Силюков О.И., Числов М.В. Ионообменные реакции в структуре перовскитоподобных слоистых оксидов. I. Протонирование сложного оксида NaNdTiO4 // Журн. общей химии. 2011. Т. 81. № 7. С. 1083–1091.
Silyukov O.I., Abdulaeva L.D., Burovikhina A.A., Rodionov I.A., Zvereva I.A. Phase Transformations During HLnTiO4 (Ln = La, Nd) Thermolysis and Photocatalytic Activity of Obtained Compounds // J. Solid State Chem., 2015. V. 226. P. 101–106.
Силюков О.И., Курносенко С.А., Зверева И.А. Интеркаляция метиламина в протонированные формы слоистых перовскитоподобных оксидов HLnTiO4 (Ln = La, Nd). Физ. и хим. стекла. 2018. Т. 44. № 5. С. 494–499.
Tahara S., Ichikawa T., Kajiwara G., Sugahara Y. Reactivity of the Ruddlesden−Popper Phase H2La2Ti3O10 with Organic Compounds: Intercalation and Grafting Reactions // Chem. Mater. 2007. V. 19. № 9. P. 2352–2358.
Kawashima K., Hojamberdiev M., Wagata H., Yubuta K., Domen K., Teshima K. Protonated Oxide, Nitrided, and Reoxidized K2La2Ti3O10 Crystals: Visible-Light-Induced Photocatalytic Water Oxidation and Fabrication of Their Nanosheets // ACS Sustain. Chem. Eng. 2017. V. 5. № 1. P. 232–240.
Maeda K., Oshima T., Ishitani O. Emission Spectroscopy of a Ruthenium(II) Polypyridyl Complex Adsorbed on Calcium Niobate Lamellar Solids and Nanosheets // Phys. Chem. Chem. Phys. 2015. V. 17. № 27. P. 17962–17966.
Xiao P., Zheng S., You J., Zheng G., Chen H., Zeng H. Structure and Raman Spectra of Titanium Oxides // J. Solid State Chem. 2007. V. 27. № 5. P. 936–938.
Toda K., Kameo Y., Kurita S., Sato M. Crystal Structure Determination and Ionic Conductivity of Layered Perovskite Compounds NaLnTiO4 (Ln = Rare Earth) // J. Alloys Compd. 1996. V. 234. № 1. P. 19–25.
Ida S., Ogata C., Eguchi M., Youngblood W.J., Mallouk T.E., Matsumoto Y. Photoluminescence of Perovskite Nanosheets Prepared by Exfoliation of Layered Oxides, K2Ln2Ti3O10, KLnNb2O7, and RbLnTa2O7 (Ln: Lanthanide ion) // J. Am. Chem. Soc. 2008. V. 130. № 22. P. 7052–7059.
Nishimoto S., Matsudaa M, Harjob S., Hoshikawab A., Ishigakib T., Kamiyamac T., Miyake M. Neutron Diffraction Study on Protonated and Hydrated Layered Perovskite // J. Solid State Chem. 2006. V. 179. № 11. P. 3308–3313.
Зверева И.А., Силюков О.И., Маркелов А.В., Миссюль А.Б., Числов М.В., Родионов И.А., Лиу Д.-Ш. Процесс образования сложного оксида NaNdTiO4 // Физика и химия стекла. 2008. Т. 34. № 6. С. 984–991. [Zvereva I.A., Silyukov O.I., Markelov A.V., Missyul A.B., Chislov M.V., Rodionov I.A., Liu D.Sh. Formation of the Complex Oxide NaNdTiO4 // Glas. Phys. Chem., 2008. V. 34. № 6. P. 749–755.]
Abdulaeva L., Silyukov O., Zvereva I., Petrov Y. Soft Chemistry Synthesis of Complex Oxides Using Protonic Form of Titanates HLnTiO4 (Ln = La, Nd) // Solid State Phenom. 2012. V. 194. P. 213–216.
Дополнительные материалы отсутствуют.
Инструменты
Физика и химия стекла


