Геохимия, 2021, T. 66, № 9, стр. 799-810
Состав летучих компонентов, захваченных алмазами при росте в металл-углерод-силикатной системе при высоком давлении и температуре
А. А. Томиленко а, А. А. Чепуров a, *, В. М. Сонин a, Т. А. Бульбак a, А. М. Логвинова a, Е. И. Жимулев a, Т. Ю. Тимина a, А. И. Чепуров a
a Институт геологии и минералогии им. В.С. Соболева Сибирского отделения РАН
630090 Новосибирск, просп. Коптюга, 3, Россия
* E-mail: achepurov@igm.nsc.ru
Поступила в редакцию 17.11.2020
После доработки 20.01.2021
Принята к публикации 03.02.2021
Аннотация
В работе представлены результаты изучения состава флюидной фазы, законсервированной во включениях в алмазе, синтезированном в металл-углеродной системе в присутствии силикатного вещества. Эксперименты были проведены при давлении 5.5 ГПа и температуре 1500°C. В качестве силикатного вещества использовали природный оливин и щелочное базальтовое стекло. В ходе исследования, в алмазах было идентифицировано около 130 различных летучих соединений, при этом наблюдается преобладание средних (С5–С12) и тяжелых (С13–С18) алифатических углеводородов, что соответствует флюиду высоковосстановительного характера в среде кристаллизации. Сравнение полученных в работе результатов с обнаруженными в природных алмазах флюидными включениями, содержащими значительное количество средних и тяжелых алифатических углеводородов ряда С5–С18, указывает на то, что часть природных алмазов могла образоваться в высоковосстановительных условиях при участии металлических жидкостей в мантии Земли.
ВВЕДЕНИЕ
Большинство исследований флюидной составляющей земной коры и мантии Земли проводилось либо в рамках системы Н2О–СО2, либо в усложненных системах с добавлением СН4 и солевых соединений. Обсуждается возможность присутствия в глубинных недрах Земли Н2О, СО2 и СН4 вследствие процессов, связанных с субдукцией океанической коры. Алмаз, благодаря химической инертности и присущих ему физических свойств, является лучшим природным материалом для консервации и транспортировки не только минеральных, но и флюидных включений к поверхности Земли (Roedder, 1984; Shirey et al., 2013). В работах последних лет все чаще сообщается о находках флюидных включений в природных монокристаллах алмаза (Weiss et al., 2014; Nimis et al., 2016), хотя, например, флюидные включения углеводородов тяжелее, чем метан, были обнаружены в алмазах уже сравнительно давно (Осоргин и др., 1987; Чепуров и др., 1994; Томиленко и др., 1997, 2001). Недавние исследования указывают на широкое распространение в мантии Земли высокомолекулярных соединений, включая тяжелые углеводороды и их кислород-, азот-, серо- и галогенсодержащие производные. Так, применение метода газовой хромато-масс-спектрометрии (GC-MS) к изучению оливинов и пикроильменитов из кимберлитовых трубок Якутии показало присутствие в них сложных по составу флюидных включений, в том числе тяжелые углеводороды и их производные (Томиленко и др., 2016а, б). При этом, устойчивость углеводородов, включая тяжелые соединения, при высоких давлениях и температурах была установлена теоретически и экспериментально (Sephton, Hazen, 2013; Сонин и др., 2014; Tomilenko et al., 2015; Kolesnikov et al., 2017). Сложный состав летучих законсервирован и в природных алмазах (Соболев и др., 2018; Томиленко и др., 2018б; Sobolev et al., 2019a, b). Экспериментальные работы по синтезу алмаза в различных по составу системах, моделирующих природные процессы, демонстрируют широкие возможности алмазообразования, что было хорошо показано в одном из наиболее полных обзоров (Bobrov, Litvin, 2011). Необходимо отметить, что в последние годы значительно возрос интерес к изучению условий кристаллизации алмаза при участии металлических жидкостей, которые как предполагается (Smith et al., 2016), могут присутствовать в виде самостоятельных обособлений расплавов преимущественно Fe–Ni состава в силикатных породах мантии Земли. При этом рассматриваются очень разные источники углерода, в том числе карбонаты, разлагающиеся в присутствии металлического расплава (Чепуров и др., 2011). Представленная работа направлена на изучение флюидной фазы из алмазов, синтезированных в металл-углерод-силикатной системе с целью продемонстрировать существенную роль углеводородов при PT-параметрах литосферной мантии Земли в образовании октаэдрических кристаллов алмаза в металлических расплавах совместно с силикатными минералами.
МЕТОДИКА ИССЛЕДОВАНИЙ
Эксперименты были проведены на аппарате высокого давления типа разрезная сфера (БАРС) в соответствии с государственным заданием ИГМ СО РАН. Ячейки были изготовлены на основе тугоплавкого оксида ZrO2. Нагревательная цепь ячейки включала в себя трубчатый графитовый нагреватель и молибденовые контакты. Калибровка давления производилась до нагрева образца по фазовым переходам в реперных веществах Bi и PbSe (Turkin, 2003). Температуру измеряли PtRh30–PtRh6 термопарой, установленной в непосредственной близости с реакционной зоной ячейки. Погрешность измерения давления и температуры в опытах составляла ±0.2 ГПа и ±25°C, соответственно. Эксперименты проведены при давлении 5.5 ГПа и температуре 1500°C, что соответствует области стабильности алмаза (Day, 2012). Продолжительность опытов составляла 70 часов. Такая длительность экспериментов была выбрана для выращивания монокристаллов алмаза размером около 4 мм. Металлической составляющей образца для синтеза алмаза служила смесь Fe и Ni в соотношении 64/36 мас. %. Источником углерода служил графит марки “Ч”. Рост алмаза осуществляли на несколько затравок для получения большего количества кристаллов. Затравками служили синтетические микроалмазы, полученные промышленным синтезом. Силикатной добавкой в металлическую шихту был порошок природного оливина (мас. %): SiO2 – 40.47; TiO2 – 0.01; Cr2O3 – 0.04; FeO – 9.00; MgO – 49.62; MnO – 0.14; CaO – 0.04; NiO – 0.41; сумма – 99.96, и щелочного базальтового стекла (мас. %): SiO2 – 46.60; TiO2 – 2.24; Аl2O3 – 15.27; Fe2O3 – 4.82; FeO – 6.38; MnO – 0.15; CaO – 6.68; MgO – 4.25; NaO – 6.14; K2O – 4.70; P2O5 – 2.34; п.п.п. – 0.1; сумма–99.67. Для изучения были выбраны образцы из трех экспериментов (3-5, 1-22 и 5-52). В реакционный объем добавляли небольшое количество силикатного вещества, которое по задумке авторов, будет моделировать металлический расплав с отдельными кристаллами силикатных минералов: в опыты 3‑5 и 1-22 добавляли оливин в количестве 1 и 5 мас. % от веса металла, соответственно. В эксперимент 5-52 добавляли 5 мас. % базальта. Схема сборки реакционного объема ячейки высокого давления приведена на рис. 1. При закалке образца путем отключения электропитания нагревателя скорость охлаждения реакционной ячейки по показаниям термопары составляет 2–3 с от температуры опыта до температуры затвердевания металла; далее, в течение нескольких секунд температура достигает 100–200°С вследствие эффективного водяного охлаждения внутреннего блока твердосплавных пуансонов аппарата. Особенности сборки ячейки высокого давления и процедуры проведения экспериментов приведены в работе (Chepurov et al., 2020).
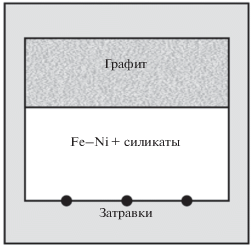
Рис. 1.
Принципиальная схема сборки реакционного объема ячейки высокого давления для проведения экспериментов по росту алмаза в металл-силикат-углеродной системе.
Морфологию поверхности образцов синтетических алмазов исследовали методами оптической (Olympus BX35) и сканирующей электронной микроскопии (1540 XB Crossbeam, Carl Zeiss).
Химический состав минеральных фаз расплавных включений в синтетических алмазах исследовали на сканирующем электронном микроскопе MIRA 3 LMU (“TESCAN” Orsay Holding), оборудованном системой микроанализа “INCA Energy” 450+Xmax80 (Oxford Instruments Nanoanalisys Ltd.) и на электронно-зондовом микроанализаторе JEOL JXA-8100, оснащенном пятью волновыми спектрометрами в ЦКП ИГМ СО РАН. Измерения проводили при ускоряющем напряжении 15–20 кВ, токе зонда 20–50 нА, времени счета 10–60 c. Для определения состава гомогенных фаз использовали зонд с минимальным диаметром пучка около 3 мкм. Для определения среднего состава смесей фаз применяли расфокусированный зонд диаметром от 20 до 100 мкм (в зависимости от размеров зерен в смеси). Контроль материального баланса данных химического анализа выполнялся с точностью 2%. Максимальные стандартные отклонения составляли 0.3 мас. %.
Составы газовой и кристаллических фаз в расплавных и флюидных включениях в синтетических алмазах были исследованы методом КР-спектроскопии (Dubessy et al., 1989; Kaindl et al., 2006, 2011; Frezzotti et al., 2012) на спектрометре Horiba Lab Ram HR 800 в ИГМ СО РАН, Новосибирск. Возбуждение проводилось твердотельным Nd YAG лазером с длиной волны 532 нм и мощностью 75 мВт. Регистрация спектра производилась полупроводниковым детектором Endor, охлаждаемом по методу Пельтье. Для локализации точки в анализируемом образце использована конфокальная система спектрометра на базе микроскопа OLYMPUS BX-41 с объективом 100× с большой числовой апертурой. Анализ проводился в геометрии обратного рассеяния. Время накопления сигнала и размер конфокальной диафрагмы варьировали в зависимости от размеров анализируемой фазы. Минимальный размер конфокального отверстия 30 нм (для объектов размером 5–10 мкм), максимальный размер – 300 нм (для объектов больше 100 мкм). Спектры получены в диапазоне 100–4200 см–1. Время накопления сигнала изменялось от 25 с/спектральное окно для крупных объектов до 400 с/спектральное окно для мелких объектов. Погрешность определения находится в пределах 1 см–1. При работе с КР-спектрами использовался программный пакет Origin 8.
Валовый состав летучих компонентов из расплавных и флюидных включений в синтетических алмазах был определен методом беспиролизной газовой хромато-масс-спектрометрии (GC-MS) на хромато-масс-спектрометре Thermo Scientific (USA) DSQ IIMS/Focus GC в ИГМ СО РАН, Новосибирск (Tomilenko et al., 2015; Sokol et al., 2017; Sobolev et al., 2019a,b; Бульбак и др., 2020). Образец синтетического алмаза помещался пинцетом в специальное устройство, включенное онлайн в газовую схему хроматографа перед аналитической колонкой, затем он прогревался при Т = = 140–160°С в течение 133 минут в токе газа-носителя – гелия (чистота 99.9999%, начальное давление 45 кПа). Разделение газовой смеси на компоненты осуществлялось на капиллярной аналитической колонке Restek Rt-Q-BOND (неподвижная фаза – 100% дивинилбензол, длина – 30 м, внутренний диаметр –0.32 мм, толщина неподвижной фазы – 10 мкм). Масс-спектры ионизации электронным ударом по полному ионному току получены на квадрупольном масс-селективном детекторе в режиме Full Scan. Старт анализа синхронизировался с моментом разрушения образца. Все газовые тракты хроматографа, по которым перемещалась газовая смесь, в том числе инжектор, кран и капилляры, имели сульфинертное покрытие. Ввод газовой смеси, извлеченной из образца при его одноактном ударном разрушении, осуществлялся в онлайн режиме в токе гелия без концентрирования, включая криофокусировку. Перед “рабочим” анализом и после него проводились холостые онлайн анализы. Предшествующий анализ позволял контролировать выделение сорбированных поверхностью образца газов, в том числе и атмосферных компонентов, а по окончании этого процесса записывать бланк системы (вся аналитическая процедура без разрушения образца). При необходимости аналитическая колонка термокондиционировалась до достижения необходимого бланка. Интерпретация хромато-масс-спектрометрических данных с идентификацией пиков и выделением из перекрывающихся пиков отдельных компонентов проводилась как с использованием программного обеспечения AMDIS (Automated Mass Spectral Deconvolution and Identification System) версии 2.66, так и в ручном режиме с коррекцией фона по библиотекам масс-спектров NIST 2017 и Wiley 11 с помощью программы NIST MS Search версии 2.3, параметры поиска стандартные. Относительные концентрации летучих компонентов в разделяемой смеси устанавливались методом нормирования: сумма площадей всех хроматографических пиков анализируемой смеси приравнивалась 100%, а по величине площади отдельного компонента определялось его относительное процентное содержание в анализируемой смеси. Площади пиков определены по алгоритму ICIS в хроматограмме с использованием Qual Browser 1.4 SR1 из пакета программ Xcalibur. Данная методика пригодна для обнаружения следовых содержаний индивидуальных летучих компонентов уже от десятков фемтограмм (10–15 г).
РЕЗУЛЬТАТЫ
В результате проведенных экспериментов были получены образцы, содержащие закаленный металлический сплав, синтезированный алмаз и новообразованные силикатные фазы. Силикатные фазы находились преимущественно в верхней части кристаллизационной камеры. Они представляли собой обособленные мелкозернистые агрегаты светло-серого цвета. Кристаллы алмаза представлены типичными для системы Fe–Ni–C октаэдрами с второстепенными гранями куба, однако, в ряде случаев кристаллы имели специфические особенности макроморфологии: в алмазах, полученных в опытах с содержанием силикатной добавки в количестве 5 мас. %, наблюдали эффект расщепления граней (рис. 2).
Рис. 2.
Кристалл алмаза с эффектом расщепления октаэдрической грани, вызванным добавкой силикатного вещества (опыт 1-22, 5 мас. % оливина).

В алмазах были обнаружены многочисленные расплавные включения. В алмазах из экспериментов 3-5 и 1-22 состав расплавных включений (рис. 3), согласно данным сканирующего электронного микроскопа и микрозондового анализа, а также КР-спектроскопии (рис. 4) представлен в основном металлическим сплавом Fe–Ni (тэнит) и оливином, а также редкими зернами клинопироксена.
Причем, соотношение силикатных фаз и металлического сплава в различных включениях может быть совершенно разным, даже в пределах одной ростовой зоны алмаза. Это, скорее всего, свидетельствует о гетерогенном состоянии металл-силикатного расплава при росте алмаза при данных РТ-параметрах эксперимента, т.е. в ростовой системе в этот момент присутствовало два несмесимых друг с другом расплава: металлический (Fe–Ni) и силикатный. При этом состав новообразованных оливинов в расплавных включениях, в отличие от исходного оливина, существенно обогащен FeO и NiO, и обеднен SiO2 и MgO (мас. %): SiO2 – 35.57–36.97; FeO – 26.05–33.23; MgO – 28.46–33.82; CaO – 0.24–0.31; NiO – 1.72–2.21. Химический состав клинопироксена в расплавных включениях представлен (мас. %): SiO2 – 52.95; TiO2 – 0.91; Al2O3 – 1.17; FeO – 7.62; MgO – 15.57; MnO – 0.31; CaO – 19.28; Na2O –0.98; NiO –0.54.
В алмазах из опыта с добавлением в металл-углеродную систему щелочного базальтового стекла (эксперимент 5-52) состав расплавных включений (рис. 5) согласно данным сканирующей электронной микроскопии и КР-спектроскопии (рис. 6) представлен металлическим сплавом Fe–Ni, гранатом, клинопироксеном и коэситом. При этом важно отметить, что для коэсита вне вскрытых расплавных включений характерен существенный сдвиг КР-линии в высокочастотную область КР-спектра до 532 см–1, что свидетельствует о достаточно высоком законсервированном давлении (не менее 3.0 ГПа) в расплавных включениях при комнатной температуре (Sobolev et al., 2000).
Рис. 3.
Микрофотография первичного включения силикатно-металлического расплава в синтетическом алмазе (Dia), выращенном в металл-углеродной системе с добавлением силикатов (Fe–Ni–C + оливин) при Р = 5.5 ГПа и Т = 1500°С. Опыт 1-22. Ol – оливин, Cpx – клинопироксен, FeNi – металлический расплав (тэнит). Фотография в отраженных электронах.
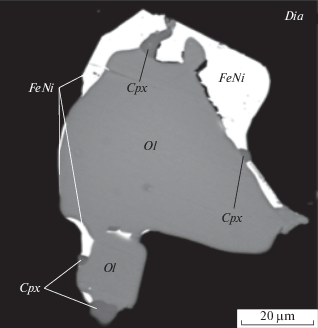
Рис. 4.
КР-спектры включения силикатно-металлического расплава в синтетическом алмазе (см. рис. 3), выращенном в металл-углеродной системе с добавлением силикатов (Fe–Ni–C + оливин) при Р = 5.5 ГПа и Т = 1500°С. а – КР-спектр оливина (КР-линии 820, 850 и 916 см–1, соответствуют оливину); б – КР-спектр оливина и клинопироксена (КР-линии 820 и 850 см–1, соответствуют оливину; КР-линии 668 и 1013 см–1 соответствуют клинопироксену); в – КР-спектр клинопироксена (КР-линии 128, 325, 390, 668 и 1013 см–1 соответствуют клинопироксену) (Frezzotti et al., 2012).
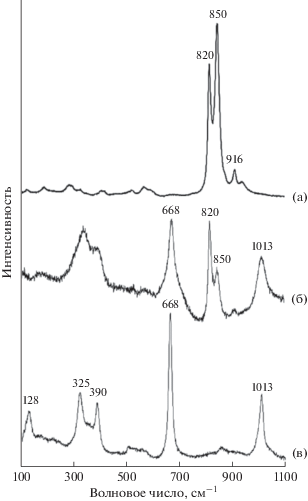
Рис. 5.
Микрофотография первичного включения силикатно-металлического расплава в синтетическом алмазе (Dia), выращенном в металл-углеродной системе с добавлением силикатов при Р = 5.5 ГПа и Т = 1500°С. Опыт 5-52. Grt – гранат, Cpx – клинопироксен, Coe ‒ коэсит, FeNi – металлический расплав (тэнит), Mag – магнетит. Фотография в отраженных электронах.
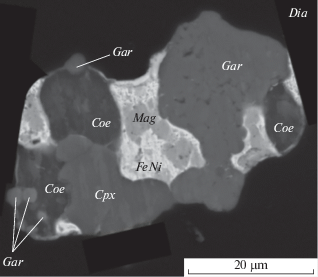
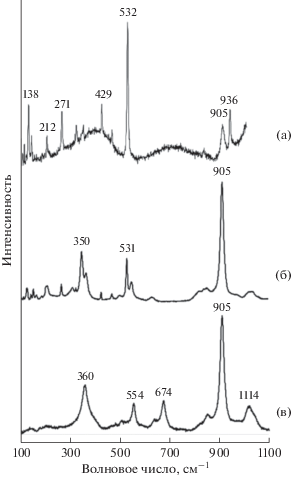
Рис. 6.
КР-спектры включения силикатно-металлического расплава в синтетическом алмазе (см. рис. 5), выращенном в металл-углеродной системе с добавлением силикатов (Fe–Ni–C + базальт) при Р = 5.5 ГПа и Т = 1500°С. а – КР-спектр коэсита и граната (КР‑линии 271, 429 и 532 см–1, соответствуют коэситу; КР-линия 905 см–1 соответствует гранату); б – КР-спектр граната и коэсита (КР-линии 350 и 905 см–1, соответствуют гранату; КР-линия 531 см–1 соответствует коэситу); в – КР-спектр граната и клинопироксенаа (КР-линии 360 и 905 см–1 соответствуют гранату; КР-линии 674 и 1114 см–1 соответствует клинопироксену) (Frezzotti et al., 2012).
Необходимо отметить, что в металл-углеродной системе (Fe–Ni–C + базальт), наряду с FeNi-расплавом, гранатом, клинопироксеном и коэситом, в составе расплавных включений в алмазах появляется магнетит (рис. 5, 7). При этом сохраняется присутствие Fe–Ni в самородном состоянии.
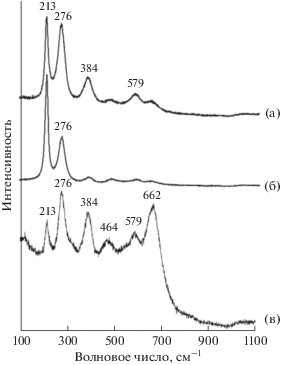
Рис. 7.
КР-спектры включения силикатно-металлического расплава в синтетическом алмазе, выращенном в металл-углеродной системе с добавлением силикатов (Fe–Ni–C + базальт – см. рис. 5) при Р = 5.5 ГПа и Т = 1500оС. а, б – КР-спектры FeNi – металлического сплава (КР-линии 213, 276, 384, 579 см–1 соответствуют FeNi– сплаву; в – КР-спектр FeNi – металлического сплава и магнетита (КР-линии 213, 276, 384, 579 см–1 соответствуют FeNi– сплаву; КР-линии 662 см–1 соответствует магнетиту) (Frezzotti et al., 2012).
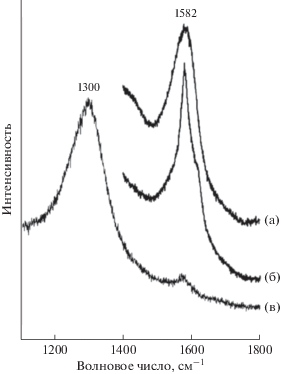
По данным КР-спектроскопии в расплавных включениях в синтетических алмазах из всех трех опытов были обнаружены графит (рис. 8а, 8б) и аморфный углерод (рис. 8в).
Рис. 8.
КР-спектры включения силикатно-металлического расплава в синтетическом алмазе, выращенном в металл-углеродной системе с добавлением силикатов (Fe–Ni–C + оливин, опыт 1-22 – см. рис. 3; Fe–Ni–C + базальт, опыт 5-52 – см. рис. 5) при Р = 5.5 ГПа и Т = 1500оС. а, б – КР-спектры графита (КР-линия 1582 см–1 соответствуют графиту); в – КР-спектр аморфного улглерода (КР-линии 1300 и 1582 см–1 соответствуют аморфному углероду) (Frezzotti et al., 2012).
По данным газовой хромато-масс-спектрометрии в синтетических алмазах из опытов 3-5 и 1-22 было установлено 126 и 130 летучих соединений, соответственно (таблица; рис. 9–12). Исследования показали, что основными компонентами летучих во включениях в алмазах являются углеводороды и их производные: алифатические (парафины, олефины), циклические (нафтены, арены), кислородсодержащие (спирты, эфиры, альдегиды, кетоны, карбоновые кислоты), гетероциклические соединения (диоксаны, фураны), азот- и серосодержащие соединения, а также углекислота и вода. Суммарное содержание углеводородов и их производных в алмазах составляет 70.4 и 61.7 отн. %, соответственно. При этом суммарная доля алифатических (СН4–С16Н34) и циклических углеводородов (С6Н12–С12Н18) в алмазах из опытов с добавлением в систему различных количеств силикатных составляющих существенно различается. Наибольшее относительное содержание этих углеводородов установлено для алмаза из опыта 3-5 (доля силиката 1 мас. %) – 42.9 отн. %. Для алмазов из опыта 1-22 (доля силиката 5 мас. %) их количество составляет 23.0 отн. %. Количество легких предельных углеводородов (метан СН4–н‑бутан С4Н10) в алмазах 3-5 и 1-22 достаточно близки – 1.7 и 2.0 отн. %, соответственно. Содержание средних предельных углеводородов (н-пентан С5Н12–н-додекан С12Н26) в алмазах 3-5 и 1-22 существенно отличается и составляет 19.1 и 3.0 отн. %, соответственно. Доля тяжелых предельных углеводородов (н-тридекан С13Н28–н-гексан С16Н34) для алмаза 3-5 также существенно выше по сравнению с алмазом 1-22 – 16.8 и 9.8 отн. %, соответственно (рис. 11б).
Рис. 9.
Хроматограммы летучих компонентов, выделившихся из флюидных включений при ударном разрушении алмаза из эксперимента 3-5 в системе FeNiC + оливин (1.0 мас. %) при Р = 5.5 ГПа и Т = 1500°С. а – хроматограмма по полному ионному току (TIC); реконструированные ионные хроматограммы по току ионов с m/z (43 + 57 + 71 + 85) (б), с m/z 60 (в) и с m/z 149 (г); д – бланк. 1. Диоксид углерода CO2; 2. Вода H2O; 3. Метиловый спирт CH4O; 4. н-Бутан C4H10; 5. Ацетон C3H6O; 6. 2-Бутанон C4H8O; 7. Уксусная кислота C2H4O2; 8. Бутановая кислота C4H8O2; 9. Пентановая кислота C5H10O2; 10. Октаналь C8H16O; 11. Гексановая кислота C6H12O2; 12. Нонаналь C9H18O; 13. Гептановая кислота C7H14O2; 14. Деканаль C10H20O; 15. 1-Додецен C12H24; 16. Додекан C12H26; 17. Октановая кислота C8H16O2; 18. 4‑Ацетилбензойная кислота C9H8O3; 19. 2-(1,1-диметилэтил)-6-метилфенол- C11H16O; 20. Гексадекан C16H34; 21. Диизопропилфталат C14H18O4.
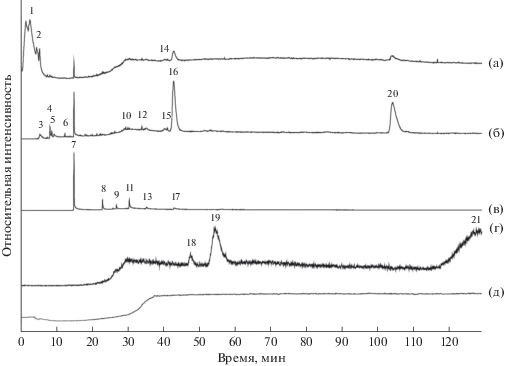
Рис. 10.
Хроматограммы летучих компонентов, выделившихся из флюидных включений при ударном разрушении алмаза из эксперимента 1-22 в системе FeNiC + оливин (5.0 мас. %) при Р = 5.5 ГПа и Т = 1500°С. а – хроматограмма по полному ионному току (TIC); реконструированные ионные хроматограммы по току ионов с m/z (43 + 57 + 71 + 85) (б), с m/z 60 (в) и с m/z 149 (г); д – бланк. 1. Диоксид углерода CO2; 2. Вода H2O; 3. Метиловый спирт CH4O; 4. Ацетальдегид C2H4O; 5. н-Бутан C4H10; 6. Ацетон C3H6O; 7. Пентан C5H12; 8. Ацетат аммония C2H7NO2; 9. 2-Бутанон C4H8O; 10. Уксусная кислота C2H4O2; 11. Гептан C7H16; 12. Гексаналь C6H12O; 13. Бутановая кислота C4H8O2; 14. 1-Нонен C9H18; 15. Пентановая кислота C5H10O2; 16. Гексановая кислота C6H12O2; 17. Нонаналь C9H18O; 18. Гептановая кислота C7H14O2; 19. Деканаль C10H20O; 20. Октановая кислота C8H16O2; 21. γ-Окталактон C8H14O2; 22. γ-Ноналактон C9H16O2.
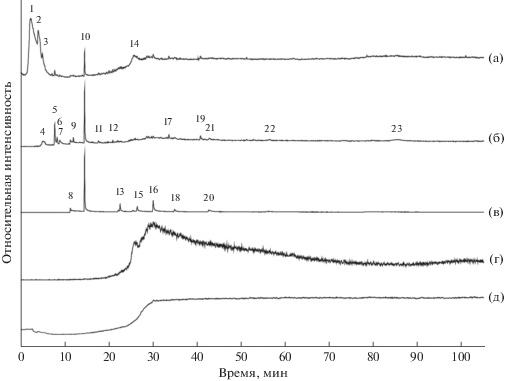
Рис. 11.
Относительное содержание летучих компонентов в синтетических алмазах из экспериментов 3-5 и 1-22 в системе Fe–Ni–C с добавлением силикатов при Р = 5.5 ГПа и Т = 1500°С: (a) – алифатические, циклические и кислородсодержащие углеводороды; (б) – “легкие” (С1–С4), “средние” (С5–С12) и “тяжелые” (С13–С16) предельные углеводороды (парафины); (в) – спирты и эфиры (простые и сложные), альдегиды, кетоны и карбоновые кислоты; (г) – суммарное количество алифатических, циклических, кислородсодержащих углеводородов и гетероциклических соединений, СО2, Н2О, азот- и серосодержащие соединения.
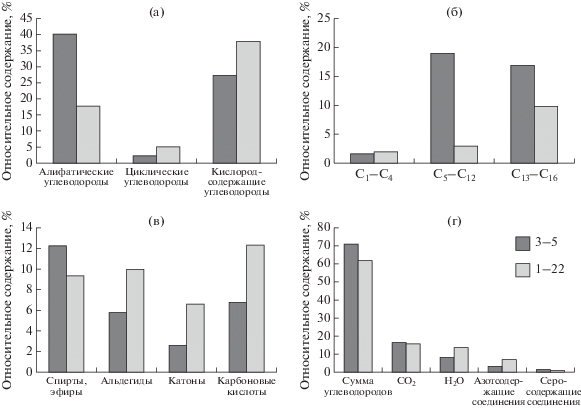
Рис. 12.
Относительное содержание летучих компонентов в синтетических алмазах из экспериментов 3-5 и 1-22 в системе Fe–Ni–C с добавлением силикатов при Р = 5.5 ГПа и Т = 1500°С.
Сопоставление содержания кислородсодержащих углеводородов показало, что их наибольшее количество (38.1 отн. %), характерно для алмазов из эксперимента 1-22 (табл. 1). Причем основными компонентами в составе кислородсодержащих углеводородов являются карбоновые кислоты (С2Н4O2–С14Н28O2) – 12.3 отн. %, а в алмазах из эксперимента 3-5 – спирты и эфиры (СН4O–С14Н18O4 – 12.1 отн. %) (табл. 1; рис. 11в).
Таблица 1.
Состав (в отн. %) летучих компонентов, выделившихся при механическом вскрытии флюидных включений в синтетических алмазах из экспериментов 3-5 и 1-22 в системе Fe–Ni–C с добавлением силикатов (по данным GC-MS анализа)
| Название | MW | 3-5 | 1-22 |
|---|---|---|---|
| Алифатические углеводороды: | 40.4 | 17.9 | |
| Парафины (СН4–С16Н34) Олефины (С2Н2–С13Н26) |
16–226 26–182 |
37.7 2.7 |
14.93.0 |
| Циклические углеводороды: Нафтены (С6Н12–С7Н14) Арены (С6Н6–С12Н18) |
84–98 78–162 |
2.50 0.38 2.12 |
5.1 0.2 4.9 |
| Кислородсодержащие углеводороды: Спирты и эфиры (С4НO–С14Н18O4) Альдегиды (С2Н4O–С11Н22O) Кетоны (С3Н6O–С11Н22O) Карбоновые кислоты (С2Н4O2–С10Н20O2) |
32–250 44–170 58–170 60–172 |
27.3 12.1 5.8 2.6 6.8 |
38.1 9.3 9.9 6.6 12.3 |
| Гетероциклические соединения: Диоксаны (С4Н8O2) Фураны (С5Н6O–С11Н18O) |
88 82–166 |
0.19 0.01 0.18 |
0.61 0.01 0.60 |
| Азотсодержащие соединения (N2–С10Н21NОS) | 28–203 | 3.3 | 6.8 |
| Серосодержащие соединения (H2S–С5Н6S) | 34–98 | 1.5 | 1.2 |
| СО2 | 44 | 16.0 | 15.8 |
| Н2О | 18 | 8.3 | 13.7 |
| Кремнийорганические соединения (C8H24O4Si4–C12H36O6Si6) | 296–444 | 0.51 | 0.79 |
| Общее количество компонентов | 126 | 130 | |
| Алканы/Алкены | 14.0 | 5.0 | |
| Н/(О+Н) | 0.84 | 0.80 |
Согласно рассчитанным отношениям Н/(О + Н) (0.84 и 0.80), алмазы из эксперимента 3-5 кристаллизовались в более восстановительных условиях, по сравнению с алмазами из эксперимента 1-22. Азот присутствовал в алмазах как в молекулярной форме (N2), так и в виде азотсодержащих соединений и азотсодержащих производных углеводородов. Было установлено от 16 (эксперимент 3-5) до 21 (эксперимент 1-22) азотсодержащих соединений (от ацетонитрила С2Н3N до н-амилбутиламина С9Н21N). Наибольшее содержание азотсодержащих соединений обнаружено в алмазах из эксперимента 1-22: 6.7 отн. %. Количество молекулярного азота в их составе весьма незначительно: 0.1–0.17 отн. %. Во всех изученных алмазах были обнаружены серосодержащие соединения: сероводород (H2S), диоксид серы (SO2), карбонил серы (СОS), дисульфид углерода (CS2), 2-метилтиофен и 3-метилтиофен (C5H6S). Наибольшее содержание углекислоты характерно для алмазов из эксперимента 3-5: 16.0 отн. %. Для алмазов из эксперимента 1-22 количество СО2 составило 13.7 отн. %. Содержание воды в алмазах из эксперимента 1-22 (15.8 отн. %) существенно выше по сравнению с алмазами из эксперимента 3-5: 8.3 отн. %.
ОБСУЖДЕНИЕ
Проведенные эксперименты продемонстрировали кристаллизацию алмаза в металл-углеродном расплаве, в котором содержатся силикатные компоненты. Это представляется чрезвычайно важным с той точки зрения, что присутствие в металлических расплавах силикатного вещества до 5 мас. % не сказывается на каталитических возможностях таких расплавов превращать графит в алмаз. Такая возможность предполагалась нами и ранее (Федоров и др., 2005, 2008). При этом морфологически образуются кристаллы алмаза октаэдрического габитуса, весьма типичные для природных алмазов из кимберлитов. Эффект расщепления граней, отмеченный в некоторых кристаллах алмаза из опытов данной серии (рис. 2) связан с присутствием силикатных минералов в металлическом расплаве. Этот механизм недавно был детально описан (Chepurov et al., 2020). В данном случае, эффект расщепления алмаза проявился в незначительной степени из-за сравнительно небольшого количества силикатного материала, добавленного в опыт.
Детальное изучение состава расплавных включений, законсервированных в алмазе в процессе его роста, с помощью КР-спектроскопии и сканирующей электронной микроскопии показало, что кристаллизация алмаза при РТ-параметрах рассматриваемых экспериментов происходила из гетерогенного металл-силикатного расплава, причем в металлическом расплаве присутствовала также обособленная флюидная фаза, которая могла захватываться кристаллами алмаза при росте. Такой эффект уже неоднократно изучался нами ранее (Осоргин и др., 1987; Чепуров и др., 1994; Tomilenko et al., 1998). По нашей оценке данных из эксперимента 5-52, значение “замороженного” давления в металл-силикатных расплавных включениях составляет не менее 3.0 ГПа при комнатной температуре. Эти впервые полученные прямые данные являются подтверждением сохранения высокого “замороженного” давления во включениях в синтетических алмазах, захваченных в процессе роста. Стоит подчеркнуть, что эффект сохранения давления внутри минералов высоких давлений играет весьма важную роль для осуществления реконструкций геологических процессов в Земле, что также было показано нами на основе экспериментов при высоких давлениях (Sonin et al., 2019).
Исследования с помощью газовой хромато-масс-спектрометрии позволили получить первые данные о составе флюидов при кристаллизации алмазов в металл-углеродной системе, содержащей силикатные компоненты. Исследования показали, что кристаллизация таких алмазов происходила при активном участии алифатических, циклических, гетероциклических и кислородсодержащих углеводородов, доля которых в составе флюидов превышала 70 отн. %, а также азот- и серосодержащих соединений. Важно отметить, что источник углерода для роста алмаза (графит) входит в металлический расплав и, несомненно, участвует в образовании углеводородов, т. к. другого углерода в системе нет. Азот – элемент воздуха и также входит в состав углеводородов, как и сера, незначительная примесь которой присутствует в материалах ячейки, исходном графите и флюидных включениях в природном оливине. При этом необходимо подчеркнуть, что обнаруженные в алмазах серосодержащие (SO2, COS, CS2, H2S, C2H6S2) и азотсодержащие соединения (N2, C2H3N, C5H7N, C6H10N2, C8H15N), а также Н2О и СО2 находятся в явно подчиненных количествах по сравнению с углеводородами (таблица; рис. 11г, 12). Как показали хромато-масс-спектрометрические исследования, с увеличением доли силикатов в металл-углеродной системе кристаллизация алмаза происходит в более окислительных условиях (значение отношения Н/(О + Н) изменяется от 0.84 до 0.80; табл. 1).
Сравнение полученных экспериментальных данных с ранее опубликованными результатами позволяет выделить несколько характерных особенностей. Так, для флюидных и расплавных включений, захваченных синтетическими алмазами при росте в многочасовых экспериментах (до 100 ч) в системе Fe–Ni–C без силикатных добавок, ярко выражено преобладание алифатических углеводородов, включая тяжелые соединения, при этом доля алифатических углеводородов составляет 65.4 отн. %, а с кислородсодержащими углеводородами достигает 86.5 отн. % (Томиленко и др., 2018a). Примечательно, что значение отношения Н/(О + Н) достигает 0.95, что отражает рост алмаза в чистой системе Fe–Ni–C в существенно более восстановительных условиях в сравнении с опытами данной серии, где был добавлен оливин. Анализы, полученные с помощью газовой хромато-масс-спектрометрии для природных алмазов пока немногочисленны, тем не менее, они уже сейчас позволяют утверждать, что природные алмазы кристаллизовались в обстановках с разным флюидным режимом. Имеющиеся данные свидетельствуют о широком присутствии в среде кристаллизации алмаза углеводородов, включая тяжелые, а также о подчиненном значении Н2О, СО2, азот- и серосодержащих соединений. Состав флюидных включений в большинстве проанализированных природных алмазов имеет довольно узкий диапазон содержания углеводородов (72.2–82.1 отн. %), с преобладанием кислородсодержащих углеводородов (спирты, эфиры, альдегиды, кетоны и карбоновые кислоты: 55.6–66.2 отн. %), а количество алифатических углеводородов находится в интервале 12.8–15.5 отн. % (Томиленко и др., 2018б). Такое соотношение алифатических углеводородов и кислородсодержащих углеводородов приближается к составу флюида, выделившегося из алмазов опыта 1-22 (табл. 1), в котором было повышенное содержание силикатного вещества. С другой стороны, важно отметить, что в россыпях северо-востока Сибирской платформы присутствуют алмазы с резким преобладанием алифатических углеводородов во включениях – 65.5 отн. %, и при этом, весьма низким содержанием кислородсодержащих углеводородов – 17.1 отн. % (Томиленко и др., 2018б). Подобное соотношение характерно для синтетических алмазов, выращенных в металл-углеродной системе без добавок силикатов. Таким образом, можно утверждать, что при кристаллизации алмаза в Fe–Ni расплаве, добавление силикатных компонентов приводит к снижению содержания алифатических углеводородов и, соответственно, к увеличению кислородсодержащих углеводородов, что связано с ростом фугитивности кислорода в ростовой среде. В то же время, при относительно небольшом присутствии силикатных минералов непосредственно в металлическом расплаве, Fe–Ni сохраняется в самородном состоянии, а алмаз продолжает расти в виде октаэдрических кристаллов.
ЗАКЛЮЧЕНИЕ
В работе представлены результаты изучения состава флюидной фазы, законсервированной во включениях в синтетических алмазах, выращенных на затравку в присутствии силикатного вещества. Небольшие количества силиката в проведенных экспериментах моделировали присутствие отдельных силикатных минералов мантийных парагенезисов, которые могут находиться непосредственно рядом с алмазом в его ростовой среде, представляющей собой металл-углеродный расплав. Сравнение полученных в настоящей работе результатов анализов с обнаруженными ранее в природных алмазах флюидными включениями, содержащими значительное количество средних и тяжелых алифатических углеводородов ряда С5–С18, указывает на то, что такие природные алмазы могли образоваться в мантии Земли в высоковосстановительных условиях при участии металлических жидкостей. Эта модель обсуждается уже давно (Wentorf, 1966; Чепуров, 1988), и недавние сенсационные находки металлических и высоковосстановительных флюидных включений в природных алмазах (Smith et al., 2016) позволяют говорить о существенной роли металлических жидкостей в образовании части природных алмазов в мантийных условиях.
Авторы благодарны А.В. Боброву за приглашение к участию в специальном выпуске журнала “Геохимия”, а также двум анонимным рецензентам, которые высказали полезные критические замечания.
Микрофотографирование кристаллов алмаза было проведено с использованием оборудования ЦКП “Наноструктуры”.
Исследования по газовой хромато-масс-спектрометрии выполнены за счет средств Российского научного фонда (грант № 19-17-00128). КР-спектроскопия фаз выполнена в рамках гранта РФФИ (№ 18-05-00761).
Список литературы
Бульбак Т.А., Томиленко А.А., Гибшер Н.А., Сазонов А.М., Шапаренко Е.О., Рябуха М.А., Хоменко М.О., Сильянов С.А., Некрасова Н.А. (2020) Углеводороды во флюидных включениях из самородного золота, пирита и кварца месторождения Советское (Енисейский кряж, Россия) по данным беспиролизной газовой хромато-масс-спектрометрии. Геология и геофизика. 61(11), 1535-1560.
Осоргин Н.Ю., Пальянов Ю.Н., Соболев Н.В., Хохрякова И.П., Чепуров А.И., Шугурова Н.А. (1987) Включения сжиженных газов в кристаллах алмаза. ДАН СССР. 293(5), 1214-1217.
Соболев Н.В., Соболев А.В., Томиленко А.А., Кузьмин Д.В., Граханов С.А., Батанова В.Г., Логвинова А.М., Бульбак Т.А., Костровицкий С.И., Яковлев Д.А., Федорова Е.Н., Анастасенко Г.Ф., Николенко Е.И., Толстов А.В., Реутский В.Н. (2018) Перспективы поисков алмазоносных кимберлитов в северо-восточной части Сибирской платформы. Геология и геофизика. 59(10), 1701-1719.
Сонин В.М., Бульбак Т.А., Жимулев Е.И., Томиленко А.А., Чепуров А.И., Похиленко Н.П. (2014) Синтез тяжелых углеводородов при температуре и давлении верхней мантии земли. ДАН. 454(1), 84.
Томиленко А.А., Бульбак Т.А., Логвинова А.М., Сонин В.М., Соболев Н.В. (2018б) Особенности состава летучих компонентов в алмазах из россыпей северо-востока Сибирской платформы (по данным газовой хромато–масс–спектрометрии). ДАН. 481(3), 310-314.
Томиленко А.А., Бульбак Т.А., Похиленко Л.Н., Кузьмин Д.В., Соболев Н.В. (2016а) Особенности состава летучих компонентов в пикроильменитах из разновозрастных кимберлитов якутской провинции (по данным газовой хромато-масс-спектрометрии). ДАН. 469(1), 82-85.
Томиленко А.А., Бульбак Т.А., Хоменко М.О., Кузьмин Д.В., Соболев Н.В. (2016б) Состав летучих компонентов в оливинах из разновозрастных кимберлитов Якутии (по данным газовой хромато-масс-спектрометрии). ДАН. 468(6), 684.
Томиленко А.А., Бульбак Т.А., Чепуров А.И., Сонин В.М., Жимулев Е.И., Похиленко Н.П. (2018а) Состав углеводородов в синтетических алмазах, выращенных в системе Fe–Ni–C (по данным газовой хромато-масс-спектрометрии). ДАН. 481(4), 422-425.
Томиленко А.А., Рагозин А.Л., Шацкий В.С., Шебанин А.П. (2001) Вариации состава флюидной фазы в процессе кристаллизации природных алмазов. ДАН. 378(6), 802.
Томиленко A.A., Чепуров A.И., Пальянов Ю.Н., Похиленко Л.Н., Шебанин А.П. (1997) Летучие компоненты в верхней мантии (по данным изучения флюидных включеий). Геология и геофизика. 38(1), 276-285.
Федоров И.И., Чепуров А.И., Чепуров А.А., Куроедов А.В. (2005) Оценка скорости “самоочищения” алмазов от металлических включений в мантии Земли в посткристаллизационный период. Геохимия. (12), 1340-1344.
Fedorov I.I., Chepurov A.I., Chepurov A.A., Kuroedov A.V. (2005) Estimation of the rate of postcrystallization self-purification of diamond from metal inclusions in the earth’s mantle. Geochem. Int. 43(12), 1235-1239.
Федоров И.И., Чепуров А.И., Сонин В.М., Чепуров А.А., Логвинова А.М. (2008) Экспериментальное и термодинамическое изучение кристаллизации алмаза и силикатов в металл-силикатно-углеродной системе. Геохимия. (4), 376-386.
Fedorov I.I., Chepurov A.I., Sonin V.M., Chepurov A.A., Logvinova A.M. (2008) Experimental and thermodynamic study of the crystallization of diamond and silicates in a metal-silicate-carbon system. Geochem. Int. 46(4), 340-350.
Чепуров А.И. (1988) О роли сульфидного расплава в процессе природного алмазообразования. Геология и геофизика. (8), 119-124.
Чепуров А.И., Томиленко А.А., Шебанин А.П., Соболев Н.В. (1994) Флюидные включения в природных алмазах из россыпей Якутии. ДАН СССР. 336(5), 662.
Чепуров А.И., Сонин В.М., Жимулев Е.И., Чепуров А.А., Томиленко А.А. (2011) Об образовании элементного углерода при разложении СаСО3 в восстановительных условиях при высоких Р-Т параметрах. ДАН. 441(6), 806-809.
Bobrov A.V., Litvin Yu.A. (2011) Mineral equilibria of diamond-forming carbonate-silicate systems. Geochem. Int. 49(13), 1267-1363.
Chepurov A.A., Sonin V.M., Dereppe J.M., Zhimulev E.I., Chepurov A.I. (2020) How do diamonds grow in metal melt together with silicate minerals? An experimental study of diamond morphology. Eur. J. Mineral. 32, 41-55.
Day H.W. (2012) A revised diamond-graphite transition curve. Am. Mineral. 97, 52-62.
Dubessy J., Poty B., Ramboz C. (1989) Advances in C–O–H–N–S fluid geochemistry based on micro-Raman spectrometric analysis of fluid inclusions. Eur. J. Miner. 1, 517-534.
Frezzotti M.L., Tecce F., Casagli A. (2012) Raman spectroscopy for fluid inclusion analysis. J. Geochem. Explor. 112, 1-20
Kaindl R., Többens D., Haefeker U. (2011) Quantum-mechanical calculations of the Raman spectra of Mg- and Fe‑cordierite. Am. Mineral. 96, 1568-1574.
Kaindl R., Tropper P., Deibla I. (2006) A semi-quantitative technique for determination of CO2 in cordierite by Raman spectroscopy in thin sections. Eur. J. Mineral. 18, 331-335.
Kolesnikov A.Y., Saul J.M., Kutcherov V.G. (2017) Chemistry of hydrocarbons under extreme thermobaric conditions. ChemistrySelect. 2, 1336-1352.
Nimis P., Alvaro M., Nestola F., Angel R.J., Marquardt K., Rustioni G., Harris J.W., Marone F. (2016) First evidence of hydrous silicic fluid films around solid inclusions in gem quality diamonds. Lithos. 260, 384-389.
Roedder E. (1984) Fluid inclusions. Reviews in mineralogy, Washington: Mineralogical Society of America, 646.
Sephton M.A., Hazen R.M. (2013) On the origins of deep hydrocarbons. Rev. Mineral. Geochem. 75, 449-465.
Shirey S.B., Cartigny P., Frost D.J., Keshav S., Nestola F., Nimis P., Pearson D.G., Sobolev N.V., Walter M.J. (2013) Diamonds and the geology of mantle carbon. Rev. Mineral. Geochem. 75(1), 355-421.
Smith E.M., Shirey S.B., Nestola F., Bullock E.S., Wang J., Richardson S.H., Wang W. (2016) Large gem diamonds from metallic liquid in Earth’s deep mantle. Science. 35, 403-1405.
Sobolev N.V., Fursenko B.A., Goryainov S.V., Shu J., Hemley R.J., Mao H.K., Boyd F.R. (2000) Fossilized high pressure from the Earth’s deep interior: coesite-in-diamond barometer. Proc. Natl. Acad. Sci. USA. 97(22), 11875-11879.
Sobolev N.V., Logvinova A.M., Tomilenko A.A., Wirth R., Bul’bak T.A., Luk’yanova L.I., Fedorova E.N., Reutsky V.N., Efimova E.S. (2019a) Mineral and fluid inclusions in diamonds from the Uralsplacers, Russia: Evidence for solid molecular N2and hydrocarbons in fluid inclusions. Geochim. Cosmochim. Acta. 266, 197-219.
Sobolev N.V., Tomilenko A.A., Bul’bak T.A., Logvinova A.M. (2019b) Composition of hydrocarbons in diamonds, garnet and olivine from diamondiferous peridotites from Udachnaya pipe in Yakutia, Russia. Engineering. 5, 451-478.
Sokol A.G., Tomilenko A.A., BulBak T.A., Palyanova G.A., Sokol I.A., Palyanov Y.N. (2017) Carbon and nitrogen speciation in N-poor C–O–H–N fluids at 6.3 GPa and 1100–1400°C. Sci. Rep. 7(1), 00679.
Sonin V.M., Leech M., Chepurov A.A., Zhimulev E.I., Chepurov A.I. (2019) Why are diamonds preserved in UHP metamorphic complexes? Experimental evidence for the effect of pressure on diamond graphitization. Int. Geol. Rev. 61(4), 504-519.
Tomilenko A.A., Chepurov A.I., Pal’Yanov Y.N., Shebanin A.P., Sobolev N.V., (1998) Hydrocarbon inclusions in synthetic diamonds. Eur. J. Mineral. 10, 1135-1141.
Tomilenko A.A., Chepurov A.I., Sonin V.M., Bul’bak T.A., Zhimulev E.I., Chepurov A.A., Timina T.Yu., Pokhilenko N.P. (2015) The synthesis of methane and heavier hydrocarbons in the system graphite-iron-serpentine at 2 and 4 GPa and 1200°C. High Temp. High Press. 44, 451-465.
Turkin A.I. (2003) Lead selenide as a continuous internal indicator of pressure in solid-media cells of high-pressure apparatus in the range of 4–6.8 GPa. High Temp. High Press. 35/36, 371-376.
Weiss Y., Kiflawi I., Davis N., Navon O. (2014) High-density fluids and growth of monocrystalline diamonds. Geochim. Cosmochim. Acta. 141, 145-159.
Wentorf R.H. (1966) Solutions of carbon at high pressure. Ber. Der Bunsengesells. 70, 975-982.
Дополнительные материалы отсутствуют.


