Геохимия, 2022, T. 67, № 1, стр. 57-68
Роль органических веществ гумусовой природы в формировании равновесных форм элементов в водах озер Кольского полуострова: экспериментальные исследования и расчетные результаты
М. И. Дину a, *, Д. Ю. Баранов a
a Институт геохимии и аналитической химии им. В.И. Вернадского РАН
119991 Москва, ул. Косыгина, 19, Россия
* E-mail: marinadinu999@gmail.com
Поступила в редакцию 15.04.2020
После доработки 25.05.2020
Принята к публикации 25.05.2020
- EDN: KKGENU
- DOI: 10.31857/S0016752522010058
Аннотация
В статье рассматриваются вопросы изменения миграционной активности элементов из почвообразующих пород под воздействием техногенных и геохимических факторов. Уникальные геологические характеристики и разнообразие минерально-сырьевой базы региона обусловливают достаточную восприимчивость водных объектов Кольского пол-ва к воздействию почвообразующих пород, слагающих водосбор, и к техногенным нагрузкам. Выбранные типичные щелочные и кислые породы региона послужили объектом динамических и статических экспериментов по выщелачиванию элементов. В качестве экстрагентов выбраны бидистиллированная вода, серная кислота и растворы фульвокислот, а также растворы фульвокислот после деградации серной кислотой. Результаты исследования показали различия в выщелачивании микроэлементов из пород под воздействием экстрагентов: для водной вытяжки характерно максимальное извлечение некоторых элементов в экспериментах со щелочными породами (Ni в 4 раза, Cu в 3 раза больше по сравнению с другими опытами), при воздействии серной кислоты на кислые породы выявлено большее содержание U (в 2 раза) и Cu (менее одного порядка). Фульвокислоты характеризуются наибольшим эффектом от воздействия на все исследованные породы. Согласно данным дискриминантного анализа выявлен наибольший вклад (коэффициент около 10) в дискриминацию следующих параметров – рассеянные элементы группы La, ионы тяжелых металлов (Ni, Cu, Pb), а также рН.
ВВЕДЕНИЕ
Формирование равновесных концентраций элементов в природных водах напрямую зависит от их поступления за счет выщелачивания, атмосферных выпадений, а также физико-химических реакций в водной среде (Моисеенко и др., 2010; Дину, 2018). Одним из важнейших факторов является химическая активность ионов, наличие конкурентных катионов и анионов в системе, в особенности, органических анионов гумусовой природы. Органические вещества гумусовой природы, как эффективные комплексообразующие лиганды играют ведущую роль в дезактивации ионов металлов и снижении неорганических форм нахождения элементов. В зависимости от региональных аспектов соотношение фульвокислот и гуминовых кислот значительно варьируются; фульвокислоты являются преобладающими компонентами северных регионов РФ в целом, и Кольского полуострова в частности. Кроме того, особое геологическое влияние и разнообразие минерально-сырьевой базы региона обусловливают особенности геохимического воздействия пород на потоки элементов с водосбора и формирования химического состава вод, а также их восприимчивость к техногенным нагрузкам.
Авторами (Алексеев, 2002; Ермолина и др., 2016; Колесов и др., 2012) в пределах Кольского региона выделяются шесть последовательно образовавшихся комплексов горных пород, представленных в основном гранитами и гранитоидами, сильно метаморфизованными складчатыми парагнейсами, различными амфиболитами и прорывающими их комплексами интрузивных пород. Геологические образования, относимые к протерозойской группе (гуронские или карельские), на территории Кольского полуострова имеют подчиненное, по сравнению с архейскими породами, распространение. Все породы, относящиеся к этой группе, залегают на фундаменте (нижнем структурной ярусе – архейских породах), часто с базальными конгломератами в основании. К комплексам раннего и среднего протерозоя относятся гнейсы и кристаллические сланцы, которые ранее представляли собой осадочные породы и вулканические лавы. Комплекс верхнего протерозоя представляют метаморфизованные осадочные, вулканогенные и интрузивные образования. Общий разрез характеризуется крупной ритмичностью, присутствием специфических осадочно-вулканогенных ассоциаций. Осадочные породы представлены алевролитами, аркозами и доломитами. Большую часть Кольского севера слагают граниты и гранитоиды, а в центральной части расположен уникальный магматический щелочной массив (Алексеев, 2002; Ермолина и др., 2016).
Рассматривая техногенные влияния, необходимо отметить вклад доминирующих предприятий региона. Медно-никелевое производство способствует (Израэль и др., 1989; Моисеенко, Гашкина, 2010) поступлению выбросов и стоков, что влияет на равновесное распределение элементов. Помимо непосредственного воздействия, которое увеличивает содержания металлов в водах возможно и опосредованное влияние от предприятий – снижение рН природных вод, значительная деградация структурны органических гумусовых веществ и, как следствие, снижение их молекулярной массы и прочности связей с некоторыми ионами металлов (Дину, 2018).
Для моделирования процессов поступления элементов и последующего формообразования с достаточной степенью достоверности применяют как теоретические, так и экспериментальные методы оценки.
Наиболее распространены методы теоретических термодинамических оценок поступления элементов в водную среду и их последующая миграция. Особенно важна систем “порода–вода” как объект изучения. Из актуальных моделей распределения элементов по формам в системах стоит отметить следующие (Дину, 2018).
1. Модель термодинамических равновесий, которые являются результатом взаимодействия “вода–порода” (Шваров, МГУ). В основе программного расчетного моделирования лежит минимизация энергии Гиббса, что позволяет определить химический состав раствора, количественный состав равновесных ассоциаций твердых фаз при заданных условиях
2. NICA-Donnan модель, описывающая взаимодействия гетерофаз в природных водах на основе неравновесной конкурентной адсорбции и хемосорбции. Активно применяется для расчета распределения элементов в системе “вода–донные отложения”, а также описания адсорбционных процессов на твердых природных носителях в открытой природной системе
Кроме того, достаточно широко известны в литературе работы по экспериментальному изучению миграции элементов из почвообразующих пород в воду (Glaskova et al., 2003; Алексеев и др., 2011; Новикова, Гаськова, 2013; Chincai et al., 2014; Savenko et al., 2017; Shan et al., 2019; Duan et al., 2019). В большинстве своем их цель – получение информации об увеличения выхода полезных/редких компонентов (благородные металлы, редкоземельные и трансурановые элементы и др.), а также для оценки степени опасности при выщелачивании элементов из шламов и шлаков, при неверном хранении шлама или шлака для окружающей среды (экологические изыскания). Подобная методология исследования крайне полезна с точки зрения анализа влияния антропогенных нагрузок и геохимических особенностей на механизмы поступления элементов и их распространения по формам в поверхностных водах. Тем не менее, вопрос о механизмах вымывания/выщелачивания элементов и последующее установление равновесия в условиях фоновых территорий, и воздействии органических веществ (в том числе деградированного органического вещества) в достаточной степени не изучен.
Целью проводимой работы было исследование процессов поступления и распределения широкого спектра элементов в воды озер при различном генезисе пород (геохимический состав) и в условиях различного антропогенного воздействия. Для оптимизации временного фактора и рассмотрения наибольших возможных эффектов вымывания применялись распространенные почвообразующие породы региона, а не соответствующая региону типичная почва. Для изучения вклада именно органической составляющей почвы при сильных техногенных нагрузках применялся метод параллельной экстракции в несколько ступеней от неорганических к органическим растворителям.
Нами рассмотрено 4 возможных сценария вымывания элементов в природные воды из породы:
1. Порода + вода (рН 5.5) как пример фоновых процессов вымывания элементов атмосферными осадками в природные воды;
2. Порода + серная кислота с целью оценки достаточно сильного антропогенного воздействия техногенных кислот из атмосферы (рН 4.0)
3. Порода + фульвокислоты для оценки геохимической роли фульвокислот (рН 3.0)
4. Воздействие на породу фульвокислотами, предварительно обработанными серной кислотой для оценки изменения протекторных свойств фульвокислот при достаточно сильном техногенном влиянии (рН 2.2).
МАТЕРИАЛЫ И МЕТОДЫ
Выбор и подготовка пород
Для эксперимента были выбраны два типа горных пород характерных для Кольского пол-ва: архейские граниты (Серебрянский и Териберский) и щелочные породы – фойяит и уртит Хибинского массива. Образцы горных пород подвергались раздроблению, методом квартования усреднялись и в них проводили определение химического элементарного состава рентгено-флюоресцентным методом и после разложения ICP-AES (макроэлементы) и ICP-MS (микроэлементы) техникой. Остатки измельченных образцов просеивали последовательно через сита 2–1, 1–0.5, 0.5–0.25, 0.25–0.1 и <0.1 мм. Из фракции 0.5–0.1 мм отбирали навески исследуемых горных пород для экстракции. Подготовку проб к анализу проводили методом многократного отмывания дробленой фракции пород в воде с использованием ультразвукового диспергатора УЗДН-1 для очистки дробленого материала от пылевидных частиц.
Основным преимуществом измельченных образцов до указанного размера является увеличение химически активной поверхности минералов и существенное ускорение процесса выщелачивания по сравнению с цельным образцом горной породы. Стоит отметить, что эксперименты с измельченной горной породой не могут полностью соответствовать природным процессам, но достаточно корректно проявляются основные тенденции миграции элементов из пород Кольского региона.
Методология эксперимента
Для моделирования природных процессов применяли три экстрагента или их смеси: 1) бидистиллированная вода с рН 5.5; 2) раствор серной кислоты (СК) с рН 4.0; 3) раствор фульвокислот (ФК), выделенных и подготовленных по стандартной методике Орлова и Тюрина (Бирюкова, Орлов, 2004) из почв Кольского полуострова, приуроченных к местам отбора образцов горных пород с рН 3.5, 4) раствор фульвокислот (ФК) предварительно обработанных (разрушенных) серной кислотой (рН 2.2). Соотношения объем экстрагента-масса навески были 1 : 1 и 2 : 1 для всех опытов, соответственно.
Изменения функциональных и физико-химических особенностей фульвокислот фиксировали методами ИК-спектрометрии (Nicolet), с помощью хроматографического измерения молекулярных масс (Agilent) и с помощью оценки изменения электрохимического потенциала (анализатор размера частица Malvern).
Эксперимент проведен в 2 возможных вариантах: динамическом и статическом. В ходе статического эксперимента образец с аликвотой раствора оставляли в темном месте на 1, 3, 5, 7 нед. при комнатной температуре (в ходе эксперимента температура в комнате колебалась от 17.4 до 21.2°С). Отделение раствора от породы после опытов производилось путем фильтрования под вакуумом (размер пор 0.05 мкм) с помощью насоса, что позволяло извлекать ~95% жидкости. Далее прибавлялась новая порция экстрагента и процесс продолжался (постановка эксперимента согласно Алексеев, 2002).
Динамический эксперимент включал параллельное добавление экстрагентов в ряд емкостей, с последующим помещением емкостей в термостат и перемешиванием на шейкере до времени отбора. В каждой точке отбора изымалась одна из параллельных емкостей. Сроки отбора проб и их фильтрация соответствовали первому эксперименту.
Выборочно, для ряда проб были проведены дубли экспериментов, сопоставления результатов измерений показали высокую сходимость (не менее 95%).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЯ
Минеральный и химический состав объектов исследования
Породообразующими минералами щелочных пород (фойяит, уртит) являются калиево-натриевые алюмосиликаты, с типичными примесями – оксидов железа, кальция, бария и стронция (табл. 1). Кислые магматические породы (граниты) характеризуются высокими содержаниями алюмосиликатов, из которых 1/3 часть – это кварц.
Таблица 1.
Минеральный (%) и химический (соединения в мас. %, элементы в мкг/г) составы почвообразующих пород
| Компоненты | Фойяит | Уртит | Гранит Териберский | Гранит Серебрянский |
|---|---|---|---|---|
| Нефелин | 26.8 | 82.4 | – | – |
| КПШ (Микроклин) | 36.0 | 0.8 | 28.2 | 18.7 |
| Плагиоклазы | 23.7 | 4.4 | 39.1 | 38.6 |
| Кварц | – | – | 31.3 | 28.2 |
| Иллит | 5.2 | 6.4 | 1.4 | 12.3 |
| Соединения | ||||
| Na2O | 9.7 | 15.3 | 4.2 | 4.1 |
| Al2O3 | 11.0 | 20.8 | 10.9 | 14.5 |
| P2O5 | 0.17 | 0.66 | 0.20 | 0.22 |
| Sобщ | 0.018 | 0.027 | 0.040 | 0.030 |
| K2O | 5.4 | 5.7 | 3.3 | 3.9 |
| CaO | 1.7 | 4.3 | 1.7 | 2.8 |
| TiO2 | 1.12 | 2.45 | 0.61 | 0.55 |
| MnO | 0.21 | 0.091 | 0.056 | 0.071 |
| Fe2O3 | 3.2 | 4.1 | 3.9 | 4.0 |
| Элементы | ||||
| V | 45.5 | 112 | 31.2 | 32.0 |
| Cr | 34.7 | 39.1 | 63.1 | 58.5 |
| Co | 1.4 | 6.5 | 7.4 | 8.2 |
| Ni | 42.8 | 34.5 | 57.2 | 64.6 |
| Cu | 10.8 | 25.5 | 27.8 | 15.3 |
| Zn | 89.6 | 73.1 | 32.2 | 53.8 |
| Pb | 6.2 | 1.9 | 8.5 | 18.9 |
| Ga | 27.4 | 31.4 | 18.3 | 20.2 |
| Rb | 93.1 | 93.8 | 56.7 | 157 |
| Sr | 1950 | 994 | 186 | 258 |
| Y | 49.1 | 27.5 | 24.6 | 30.5 |
| Zr | 961 | 324 | 375 | 386 |
| Nb | 527 | 231 | 17.1 | 22.7 |
| Ag | 0.64 | 0.29 | 0.079 | 0.11 |
| Sn | 3.6 | 1.8 | 2.6 | 2.1 |
| Ba | 1972 | 103 | 1030 | 659 |
| La | 158 | 82.8 | 82.4 | 47.6 |
| Ce | 306 | 159 | 147 | 105 |
| Pr | 37.9 | 17.4 | 18.3 | 14.1 |
| Nd | 146 | 60.6 | 57.4 | 53.4 |
| Sm | 24.3 | 10.4 | 8.9 | 10.5 |
| Eu | 6.5 | 3.0 | 1.3 | 1.7 |
| Gd | 18.2 | 8.8 | 7.0 | 8.3 |
| Tb | 2.4 | 1.2 | 1.0 | 1.2 |
| Dy | 11.8 | 6.1 | 4.7 | 5.6 |
Согласно полученным данным, гранит Серебрянский оказался более выветрелым по сравнению с гранитом Териберским, на это указывает меньшее содержание калиевого полевого шпата (КПШ, микроклин) и большего содержания иллита – промежуточного минерала при переходе КПШ в каолинит в процессе выветривания. Образец выветрелого гранита в нашем эксперименте представляет собой уникальный пример влияния временного фактора на выщелачивание элементов из горных пород.
Фойяит и уртит слагают минералы, имеющие преимущественно калиево-натриевый алюмосиликатный состав (табл. 1). В образце уртита нефелин составляет более 80% породы и соотношение Na к K в последнем, соответственно, 4 : 1, что обусловливает большее содержание оксидов Na и Al. Как показывает анализ, содержание примесей – оксидов Fe и Ca в уртите выше, чем в фойяите, а концентрации оксидов K примерно равны для обеих щелочных пород (Самсонова, 1973).
Характерными второстепенными минералами для уртита являются апатит и титаномагнетит, в которых преобладает содержание фосфора и титана соответственно. Для фойяита второстепенными минералами являются цирконосиликаты, редкоземельные силикаты, силикатофосфаты, циркон, что наблюдается в табл. 1. Широко распространено изморфное замещение Ca ионами Mn в альбите (типичный представитель группы плагиоклазов). Повышенное содержание оксида Mn в фойяите по сравнению с уртитом, соответствует содержанию плагиоклазов в горных породах. Различие в содержании S щелочных горных пород, главным образом, определяется образованием вторичного минерала по нефелину – натролита, главной примесью которого является S. Поэтому более высокое содержание S в уртите можно объяснить преобладанием нефелина при сравнении горных пород. Для фойяита акцессорным минералом является эвдиалит, в составе которого присутствуют примеси редкоземельных элементов. Вероятно, с этим связано большее содержание лантаноидов в фойяите по сравнению с уртитом (MacKenzie, 1957).
Примерно одинаковое количество оксидов основных петрогенных элементов в гранитах может быть объяснено равной составляющей K-Na минералов в составах пород. В иллитах гранитных пород часть ионов кремния в тетраэдрических пакетах замещена ионами Al, в граните Серебрянском иллита значительно больше, чем в другой пробе и, соответственно, Al тоже. В обоих образцах содержатся примерно равные количества оксида P и Mn, что можно объяснить соответствующим соотношением примесей полиморфной модификацией кварца (кристобалита). Повышенные содержания окислов Ca в граните Серебрянском могут быть связаны с гетеровалентным замещением ионов K в процессе преобразования микроклина в иллит при выветривании (Richet et al., 1982).
Проведенные анализы проб указывают на некоторые отличия в их составе, которые могут влиять на миграцию элементов. Наибольшее внимание при анализе полученных результатов будет направлено на физико-химические параметры и группировку элементов (щелочноземельные, редкоземельные, подгруппа Fe и т.д.).
Фульвокислоты, выделенные из типичных почв характеризовались следующими особенностями: повышенным содержанием кислородных фрагментов, в большей степени за счет присутствия карбоксильных и карбонильных фрагментов; азотсодержащими фрагментами за счет присутствия амидных групп, а также в меньшей степени углеводородными группами ароматического и алифатического ряда. Общее соотношение элементного состава О/N: 60% (кислородные группы) – 10% (азотные) Молекулярная масса фульвокислот (при выбранном рН 3.0–3.5) составляла около 15 000–20 000. При воздействии раствора серной кислоты на фульвокилоты происходили изменения в структуре природного полимера. Выявлено снижение молекулярной массы до максимальных 2000–5000, увеличение содержание кислородных групп (краевых активных функциональных групп). Уменьшение рН также влияет на изменение дзета-потенциала полимера: при рН более 3, заряд фульвокислот отрицательный, что влияет на большее сродство металлов к лиганду. При снижении величины рН до 2, выявлена более сильная конкуренция протона водорода и металлов за краевые группы, величина дзета потенциала группы с протонированным атомом кислорода смещается в положительную сторону.
Особенности химического состава водных растворов
К наиболее общим показателям, характеризующим состояние полученной системы можно отнести рН и электропроводность. На рис. 1, показаны значения рН для образцов кислых и щелочных горных пород. Согласно полученным данным выявлено наибольшее изменение величины рН при воздействии серной кислоты на породы Териберского гранита в первые дни эксперимента, в среднем скачек составляет от 3–4 единиц.
Рис. 1.
Изменение рН раствора (сред. знач.) в условиях проведения экспериментов 1 и 2: по оси у – недели эксперимента.
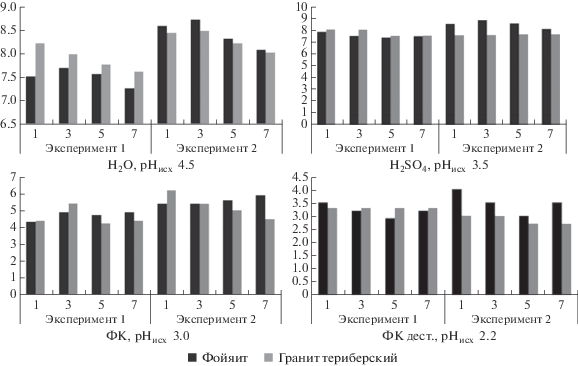
Многие авторы (Алексеев и др., 2011; Новикова и др., 2013; Duana, 2019) указывают именно на начальные этапы взаимодействия порода-вода с точки зрения активности элементов, наши результаты оценки изменения физико-химических параметров подтверждают эти выводы. Стоит отметить, что при взаимодействии воды со щелочными породами (пример фойяит) и кислыми породами (пример Териберский гранит) в условиях еженедельной смены экстрагента (эксперимент 1) градиент изменения рН значительно больше проявляется для кислых пород. В условиях выдерживания образцов в растворе определенное количество недель (эксперимент 2), подобного значимого различия в изменении величины рН не найдено. Можно предположить, что достаточная активность именно гранитного типа пород по отношению к нейтральным экстрагентам связана с расположением элементов в структуре твердого вещества.
Воздействие серной кислоты на фойяит и гранит Териберский проявляется в различии более чем на 1-цу величины рН в двух экспериментах. Тем не менее, в случае 1-го варианта эксперимента различия в указанном параметре минимальны как для кислых, так и для щелочных пород. В ходе 2-го эксперимента различия превышали 1 единицу.
Растворы фульвокислот – исходные и после разрушения серной кислотой – представляют собой наиболее стабильные с точки зрения изменения рН экстрагенты. Для обеих выбранных типов ФК выявлены не такие резкие скачки рН (не более 2 единиц) и достаточно стабильное (фиксированное) значения во все недели эксперимента. Последний факт указывает на некоторую возможную сходимость процессов при взаимодействии ФК и раствора серной кислоты.
Сравнение полученных значений электропроводности между вытяжками из кислых и щелочных пород указывает на более значимое изменение величины и, соответственно, содержания ряда компонентов для щелочных пород (пример фойяит): 43–96 мкСим в водной вытяжке и 34–62 мкСим в вытяжке серной кислоты. Для образцов гранита изменения величины электропроводности не такие резкие: при воздействии воды 45–59 и серной кислоты 48–67 мкСим, соответственно, что значительно ниже, чем в предыдущем примере. Подобная тенденция характерна и для других представителей щелочных и кислых пород.
Опираясь на данные об электропроводности можно сказать, что воздействие водного экстрагента эффективнее в пробах щелочных пород, а при воздействии неорганического кислотного реагента – в образцах кислых пород.
Сравнивая образцы фойяита и уртита, а также гранитов Териберского и Серебрянского стоит отметить, что изменения величин рН и электропроводности при экспериментах с ними сопоставимы. Наиболее значимые различия в величинах рН выявлены при обработке ФК образцов гранита (около 0.5–0.7), для ФКдестр. и других образцов различия не превышали 0.2–0.3 единиц рН.
Содержания некоторых химических элементов в сернокислотных и водных вытяжках отражены в табл. 2 (здесь и далее данные представлены с учетом суммирования в эксперименте 2). В качестве примера представлены образцы гранита Териберского и фойяита, которые являются репрезентативными представителями кислых и щелочных горных пород. С целью оптимальной подачи результатов выбраны наиболее важные 3 периода эксперимента.
Таблица 2.
Содержание химических элементов в вытяжках из щелочных и кислых пород (мкг/л)
| Элемент | Фойяит | Гранит Териберский | ||||
| 1 неделя | 3 недели | 7 недель | 1 неделя | 3 недели | 7 недель | |
| вода | ||||||
| Ca | 3353 | 4433 | 8053 | 10 652 | 16 279 | 23 025 |
| Mg | 0 | 185 | 739 | 483 | 1036 | 1884 |
| Na | 14 829 | 25 196 | 48 148 | 3455 | 3996 | 6838 |
| K | 3981 | 6240 | 29 958 | 2276 | 4105 | 39 819 |
| Si | 4036 | 5440 | 37796 | 5913 | 6298 | 8586 |
| Cr | 0 | 0.0 | 18.8 | 0.0 | 0.0 | 0.0 |
| Mn | 8.1 | 13.1 | 249 | 4.2 | 1003 | 23.6 |
| Fe | 0.0 | 0.0 | 2624 | 0.0 | 0.0 | 133 |
| Al | 538 | 453 | 12 238 | 153 | 96.0 | 246 |
| Ni | 10.8 | 0.0 | 8.7 | 0.0 | 0.0 | 2.5 |
| Cu | 0.0 | 0.0 | 17.2 | 0.0 | 0.0 | 6.3 |
| Pb | 1.1 | 12.8 | 16.5 | 0.43 | 0.39 | 1.5 |
| Zn | 78.3 | 158 | 67.4 | 12.4 | 0.0 | 36.4 |
| Rb | 7.09 | 10.47 | 34.99 | 4.45 | 5.64 | 9.19 |
| Y | 0.80 | 0.46 | 30.01 | 0.11 | 0.49 | 1.18 |
| Zr | 2.77 | 2.63 | 124.56 | 0.36 | 0.47 | 0.36 |
| Nb | 2.44 | 2.59 | 154.22 | 0.24 | 0.24 | 0.24 |
| Mo | 24.37 | 39.72 | 83.52 | 3.79 | 3.18 | 7.10 |
| Ag | 0.09 | 0.00 | 1.28 | 0.00 | 0.08 | 0.33 |
| Cd | 0.00 | 0.00 | 0.26 | 0.00 | 0.00 | 0.21 |
| Sn | 0.57 | 0.51 | 1.19 | 0.47 | 0.48 | 0.39 |
| Sb | 0.72 | 1.10 | 1.56 | 0.49 | 0.55 | 0.54 |
| Cs | 0.04 | 0.05 | 0.35 | 0.00 | 0.00 | 0.01 |
| La | 2.74 | 2.20 | 112.53 | 1.60 | 0.82 | 3.05 |
| Ce | 5.58 | 3.88 | 207.69 | 2.69 | 0.63 | 3.20 |
| Pr | 0.62 | 0.43 | 25.90 | 0.13 | 0.14 | 0.60 |
| Nd | 2.36 | 1.45 | 93.65 | 0.44 | 0.43 | 2.13 |
| Sm | 0.41 | 0.33 | 14.08 | 0.13 | 0.12 | 0.35 |
| Eu | 0.09 | 0.07 | 3.76 | 0.00 | 0.01 | 0.03 |
| Gd | 0.28 | 0.24 | 10.88 | 0.05 | 0.10 | 0.23 |
| Tb | 0.04 | 0.03 | 1.45 | 0.00 | 0.01 | 0.03 |
| Dy | 0.17 | 0.11 | 7.07 | 0.02 | 0.06 | 0.16 |
| Ho | 0.03 | 0.02 | 1.20 | 0.00 | 0.01 | 0.03 |
| Er | 0.14 | 0.04 | 2.94 | 0.00 | 0.02 | 0.10 |
| Tm | 0.01 | 0.01 | 0.35 | 0.00 | 0.37 | 0.01 |
| Yb | 0.05 | 0.03 | 1.99 | 0.00 | 0.01 | 0.04 |
| Lu | 0.01 | 0.00 | 0.25 | 0.00 | 0.00 | 0.01 |
| Hf | 0.09 | 0.13 | 3.88 | 0.02 | 0.03 | 0.02 |
| Ta | 0.06 | 0.12 | 4.41 | 0.00 | 0.00 | 0.00 |
| W | 1.40 | 2.00 | 3.91 | 0.96 | 0.49 | 1.08 |
| Pt | 0.00 | 0.00 | 0.08 | 0.00 | 0.00 | 0.00 |
| Au | 0.00 | 0.00 | 0.34 | 0.03 | 0.00 | 0.00 |
| Tl | 0.00 | 0.00 | 0.02 | 0.00 | 0.00 | 0.02 |
| Bi | 0.26 | 0.08 | 0.17 | 0.05 | 0.05 | 0.06 |
| Th | 0.50 | 0.42 | 14.43 | 0.06 | 0.02 | 0.35 |
| U | 0.37 | 2.35 | 12.26 | 2.83 | 7.14 | 16.00 |
| Элемент | Фойяит | Гранит Териберский | ||||
| 1 неделя | 3 недели | 7 недель | 1 неделя | 3 недели | 7 недель | |
| серная кислота | ||||||
| Ca | 4475 | 5370 | 8301 | 11 123 | 47 738 | 45 340 |
| Mg | 148 | 211 | 682 | 450 | 2392 | 2999 |
| Na | 20 147 | 28 419 | 52 331 | 3102 | 9286 | 12 553 |
| K | 5712 | 7645 | 39 806 | 1946 | 41 163 | 57 213 |
| Si | 5603 | 6665 | 29 459 | 6885 | 9068 | 6134 |
| Cr | 0.0 | 0.0 | 9.0 | 0.0 | 0.0 | 0.0 |
| Mn | 10.9 | 17.7 | 174.1 | 4.2 | 75.7 | 33.5 |
| Fe | 0.0 | 0.0 | 1883 | 0.0 | 0.0 | 0.0 |
| Al | 370 | 679 | 8086 | 206 | 104 | 68.1 |
| Ni | 0.0 | 3.0 | 9.7 | 0.0 | 11.9 | 6.0 |
| Cu | 0.0 | 0.0 | 17.0 | 0.0 | 20.1 | 19.3 |
| Pb | 1.7 | 1.7 | 11.8 | 0.0 | 2.5 | 7.4 |
| Zn | 0.0 | 11.0 | 146.2 | 0.0 | 51.5 | 21.2 |
| Rb | 8.85 | 12.70 | 31.96 | 4.00 | 12.85 | 21.79 |
| Y | 0.66 | 1.13 | 19.45 | 0.16 | 0.90 | 1.68 |
| Zr | 2.62 | 6.32 | 88.34 | 0.77 | 0.42 | 0.32 |
| Nb | 2.41 | 5.99 | 90.51 | 0.55 | 0.27 | 0.24 |
| Mo | 25.69 | 40.21 | 73.42 | 3.35 | 3.47 | 8.89 |
| Ag | 0.00 | 0.22 | 0.85 | 0.00 | 0.09 | 0.27 |
| Cd | 0.00 | 0.00 | 0.36 | 0.00 | 0.68 | 0.30 |
| Sn | 0.50 | 0.68 | 0.63 | 0.47 | 0.90 | 0.29 |
| Sb | 0.83 | 1.20 | 1.28 | 0.57 | 0.37 | 0.50 |
| Cs | 0.04 | 0.07 | 0.30 | 0.00 | 0.02 | 0.02 |
| La | 2.47 | 3.85 | 72.56 | 1.16 | 0.87 | 1.02 |
| Ce | 4.62 | 7.46 | 131.90 | 1.70 | 0.60 | 0.83 |
| Pr | 0.57 | 0.88 | 16.69 | 0.21 | 0.16 | 0.20 |
| Nd | 2.03 | 3.08 | 61.20 | 0.68 | 0.58 | 0.76 |
| Sm | 0.33 | 0.62 | 9.25 | 0.21 | 0.11 | 0.15 |
| Eu | 0.08 | 0.14 | 2.51 | 0.03 | 0.01 | 0.01 |
| Gd | 0.26 | 0.43 | 7.09 | 0.12 | 0.09 | 0.14 |
| Tb | 0.04 | 0.06 | 0.92 | 0.01 | 0.01 | 0.02 |
| Dy | 0.14 | 0.25 | 4.58 | 0.05 | 0.07 | 0.12 |
| Ho | 0.03 | 0.05 | 0.78 | 0.01 | 0.02 | 0.05 |
| Er | 0.08 | 0.10 | 1.93 | 0.02 | 0.05 | 0.17 |
| Tm | 0.01 | 0.01 | 0.23 | 0.00 | 0.00 | 0.02 |
| Yb | 0.04 | 0.05 | 1.27 | 0.01 | 0.01 | 0.09 |
| Lu | 0.00 | 0.01 | 0.16 | 0.00 | 0.00 | 0.02 |
| Hf | 0.11 | 0.22 | 2.75 | 0.05 | 0.04 | 0.02 |
| Ta | 0.10 | 0.14 | 2.72 | 0.00 | 0.00 | 0.00 |
| W | 1.40 | 1.99 | 2.86 | 0.90 | 0.24 | 0.99 |
| Pt | 0.00 | 0.00 | 0.03 | 0.00 | 0.00 | 0.00 |
| Au | 0.00 | 0.00 | 0.16 | 0.03 | 0.00 | 0.00 |
| Tl | 0.00 | 0.00 | 0.01 | 0.00 | 0.04 | 0.05 |
| Bi | 0.08 | 0.11 | 0.14 | 0.00 | 0.17 | 0.10 |
| Th | 0.38 | 0.70 | 9.19 | 0.06 | 0.00 | 0.07 |
| U | 0.54 | 2.84 | 11.71 | 2.06 | 7.08 | 29.47 |
Согласно полученным данным, щелочные породы характеризуются большей миграционной активностью элементов в заданных условиях, чем кислые породы. Сравнивая воздействие растворителей – серной кислоты и воды на 2 принципиально разных типа пород была выявлена преобладающая миграция элементов в кислой среде. При сравнении воздействия сернокислотной и водной вытяжек на породы, можно говорить о большей роли водной миграции для щелочных пород и сернокислотной миграции для гранитных пород. В особенности это проявляется для переходных металлов и рассеянных элементов.
Анализируя общие данные, характерные для всех экспериментов возможно выделить группы элементов с определенной динамикой поступления – в первые недели активно перемещаются щелочные и щелочноземельные металлы. Можно заключить, что после первой обработки образцов растворами, на поверхности образовывается выщелоченный слой и далее происходит реакция с новообразованным слоем иного состава, обедненного щелочными и щелочноземельными элементами. В этот же период (1–3 дата отбора) происходит обогащение элементами группы лантаноидов и актиноидов и некоторыми ионами металлов (Pb, Zn), как сопутствующих основным компонентам.
В завершении процессов (4 точка отбора) широкий ряд ионов переходных металлов вымывается (Fe, Ni, Cd и т.д.) и поступают в элюент. Некоторые редкоземельные элементы характеризуются максимальным выщелачиванием в середине эксперимента (2 или 3 нед.) с последующим спадом концентрации в вытяжках, что может свидетельствовать о протекании физико-химических процессов и изменении равновесия в растворах.
Влияние ФК (табл. 3) проявляется в увеличении степени выщелачивания всех элементов – для ионов Fe, Al (более 10 раз) и других элементов. В ходе выщелачивания, вне зависимости от недели обработки происходит буферирование системы.
Таблица 3.
Влияние органических веществ на выщелачивание элементов (мкг/л)
| Элемент | Фойяит | Гранит Териберский | ||||
|---|---|---|---|---|---|---|
| 1 неделя | 3 недели | 7 недель | 1 неделя | 3 недели | 7 недель | |
| ФК | ||||||
| Cr | 35 | 36.0 | 40.0 | 20.4 | 20.4 | 20.8 |
| Mn | 85.0 | 13.1 | 249 | 1050.0 | 1049 | 1028.0 |
| Fe | 30000.0 | 35000.0 | 45000 | 1350.0 | 1345.5 | 1452 |
| Al | 78000 | 80654 | 80248 | 2450 | 2650.0 | 2680 |
| Ni | 88.6 | 90.4 | 91.6 | 16.8 | 18.9 | 19.2 |
| Cu | 65.2 | 68.0 | 65.2 | 118.9 | 120.6 | 125.0 |
| Pb | 31.6 | 32.4 | 33.0 | 3.25 | 3.84 | 3.8 |
| Zn | 325.0 | 326 | 328.5 | 95.6 | 98.9 | 100.0 |
| Rb | 0.56 | 0.60 | 0.70 | 0.89 | 0.90 | 1.00 |
| Cs | 1.30 | 1.10 | 1.20 | 0.20 | 0.20 | 0.20 |
| La | 115.60 | 115.80 | 116.00 | 32.60 | 40.60 | 41.00 |
| Th | 20.00 | 26.30 | 25.60 | 2.60 | 2.50 | 2.50 |
| U | 18.20 | 16.20 | 19.00 | 22.50 | 23.00 | 23.00 |
| Элемент | Фойяит | Гранит Териберский | ||||
| 1 неделя | 3 недели | 7 недель | 1 неделя | 3 недели | 7 недель | |
| ФК дестр. | ||||||
| Cr | 5.5 | 5.5 | 5.3 | 10.0 | 11.0 | 10.0 |
| Mn | 180.0 | 185.0 | 200.0 | 40.0 | 40.0 | 40.0 |
| Fe | 2200.0 | 2000.0 | 2220 | 250.0 | 250.0 | 260.0 |
| Al | 12000 | 12680 | 12950 | 350 | 325 | 365.0 |
| Ni | 65.0 | 65.0 | 62.0 | 70.0 | 70.0 | 72.0 |
| Cu | 22.0 | 22.0 | 25.0 | 25.0 | 25.0 | 25.0 |
| Pb | 50.1 | 50.0 | 50.2 | 60.0 | 60.0 | 62.0 |
| Zn | 175.0 | 170.0 | 170.0 | 30.0 | 30.0 | 30.0 |
| Rb | 0.16 | 0.20 | 0.20 | 0.50 | 0.50 | 0.50 |
| Cs | 0.10 | 0.10 | 0.10 | 0.50 | 0.50 | 0.50 |
| La | 80.00 | 80.00 | 89.00 | 2.00 | 2.00 | 2.00 |
| Th | 12.00 | 12.00 | 12.00 | 1.00 | 1.00 | 1.00 |
| U | 177.00 | 17.00 | 17.00 | 32.00 | 32.00 | 32.00 |
Воздействие ФК после деструкции серной кислотой, которая формирует более положительный дзета-потенциал системы, проявляется в снижение степени выщелачивания для ряда элементов – в особенности Fe, Al.
Несмотря на более интенсивное вымывание элементов исходными фульвокилотами, для ряда ионов металлов выявлено увеличение миграционной активности после воздействия ФКдестр – Pb, Cu. Для Cr и Mn миграционная способность становится сопоставима с экспериментальным воздействием только серной кислоты. Это может быть связано с раскрытием активных центров органических веществ, а также более предпочтительной для выбранных металлов молекулярной массой.
Статистический анализ
Статистическая обработка полученных данных позволила наиболее информативно проследить влияние геохимического фактора (корреляционный анализ) и влияние техногенных параметров (дискриминантный анализ).
Результаты корреляционного анализа указывают на большую достоверную связь (не менее 0.85) между рассеянными элементами (ряд La-Lu) и элементам подгруппы Cr, Fe, а также переходными металлам – Ni, Cu, Pb, Co для щелочных пород. Особенно высока корреляция для уртита. Различия 2 видов щелочных пород проявляются также в большем коэффициенте корреляции между переходными элементами (ряд тяжелых металлов Cu–Pb) для пород фойяита.
Для кислых пород выявлены высокие корреляционные показатели трансурановых элементов со щелочными, щелочноземельными элементами, элементами подгруппы Fe, Cr а также переходными металлами – Ni, Cu, Co и т.д. Более выветрелый Серебрянский гранит характеризуется большим сродством некоторых рассеянных элементов (Tm-Ta) к ионам переходных металлов (не менее 0.9). Тем не менее, значимых различий между поведением элементов при выщелачивании из Серебрянского и Териберского гранитов не найдено. Можно заключить, что более выветрелый образец характеризуется примерно теми же способностями к выщелачиванию, что и другой гранит. Найденные закономерности можно связать с геохимическими особенностями распределения основных и ассоциативных элементов в породах.
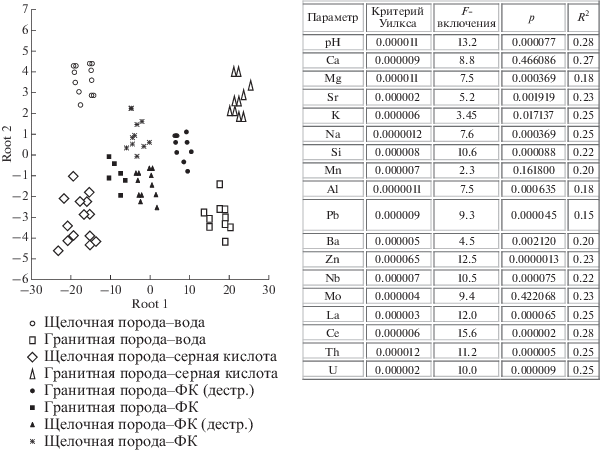
Дискриминантный анализ показал влияние каждого типа растворителей на щелочные и кислые породы. Для примера (на рис. 2) представлены данные о процессах вымывания из фойяита и Териберского гранита. Результаты канонической визуализации показали явное различие в обработке серной кислотой и водой для двух типов пород (симметрия относительно обеих осей) и достаточно сходные механизмы воздействия ФК любого типа (в центре 4 группы). Несмотря на близость механизмов воздействия ФК, каждый из вариантов обработки характеризуется своей микро-группой на графике. Согласно данным о дискриминирующих параметрах, наибольший вклад (коэффициент от 10 и выше) у рассеянных элементов, рН, а также ионов тяжелых металлов. Можно заключить, что воздействие любых из ФК основано на механизмах комплексообразования примерно равной силы относительно активных центров, а различия связаны с уникальными функциональными особенностями природного полимера, его координационными возможностями – дзета-потенциал, молекулярный вес и т.д.
Кинетика процессов перемещения
Реакции породы с растворителями характеризуются различной скоростью вымывания и порядком реакции относительно конкретных элементов. Естественно, воздействие экстрагентов различной кислотно-основной и окислительно-восстановительной силы изменяет механизм реакции сложной системы. Небольшая выборка точек не позволяет делать подробные выводы и сложные расчеты скоростей перемещения элементов. Но, возможность описать тенденции в кинетике перемещения существует. Говоря о порядках реакций, стоит отметит, что реакции 1-го порядка относятся к необратимым механизмам, 2 и 3, соответствуют более сложным окислительно-восстановительным реакциям и реакциям комплексообразования, с определенной долей обратимости.
При воздействии воды с щелочными и кислыми породами для групп элементов прослеживается следующая тенденция: щелочные, щелочноземельные, анионогенные – преимущественно реакция 1-го порядка, для элементов подгруппы Fe, лантоноидов и актиноидов – 2-го порядка, элементы подгруппы Cr – реакции 3 порядка.
Кислотно-основные свойства серной кислоты проявляются в большем влиянии на ряд элементов (тяжелые металлы, As, S), миграция большинства соответствует реакции 1-2 порядка, либо смещается в сторону 2-го порядка (анионогенные элементы).
Рассматривая весь массив данных, выявлено, что влияние ФК и ФКдестр способствуют смещению порядка реакции в сторону 2 и 3, т.е. более сложных механизмов взаимодействия между породой и экстрагентом. Mn, Cr, Fe и др. переходные металлы характеризуются наиболее смешенным типом взаимодействия со всеми экстрагентами, что можно связать с изменениями их степеней окисления.
Распределение элементов по формам в сложных системах
Несмотря на сложность полученной водной системы, для наиболее значимых модельных экспериментов можно выстроить ряды сродства металлов к органическому веществу. Водные вытяжки и воздействие серной кислотой способствуют образованию соответствующих равновесий между неорганическими соединениями, что не так усложняет расчеты.
Наиболее интересны воздействия ФК и ФКдестр как примеры: в первом случае, воздействия органических веществ гумусовой природы, во втором, влияния антропогенных факторов на процессы формирования равновесных форм. В этих случаях наиболее явно прослеживается конкуренция ионов металлов за неорганические и органические лиганды.
Полученные с помощью моделирование (программа Acidformmet) ряды активности металлов (РАМ) относительно фульвокислот следующие:
ФК
Fe > Al > Cu = Ni > Pb > Zn > Cr = Mn,
ФКдестр
Fe = Cu, Pb > Al > Ni > Mn > Cr.
Влияние серной кислоты (воздействие на ФК при деструкции) на молекулярную массу и электрохимический заряд ФК проявляется в изменении РАМ, в том числе и в зависимости от физико-химических особенностей ионов металлов. Несмотря на доминирующие позиции ионов Fe, роль более низкомолекулярных фракций ФК проявляется в снижении степени связывания большой группы элементов. В тоже время ФК, разрушенные серной кислотой, создают возможность большей инактивации ионов Pb и Cu.
ЗАКЛЮЧЕНИЕ
Проведенные экспериментальные исследования по воздействию различных экстрагентов на породы позволили выявить ряд геохимических и техногенных особенностей миграции элементов. В ходе работы найден наибольший “отклик” щелочных пород на воздействие водного экстрагента (как пример фоновых атмосферных осадков) и на кислые породы неорганического кислотного реагента (как пример сильных техногенных воздействий) для рассеянных элементов. Влияния ФК и ФКдестр проявляются в значительном изменении миграционной активности большой группы элементов.
Применение дискриминантного анализа с канонической визуализацией показали явное различие при обработке серной кислотой и водой для двух типов пород (симметрия относительно обеих осей) и достаточно сходные механизмы воздействия ФК любого типа (в центре близкие 4 группы). Наиболее значимыми факторами, определяющими различия в экспериментах, являются рассеянные элементы, рН, а также ионы некоторых тяжелых металлов.
В период длительного взаимодействия раствора с породой буферные свойства активнее проявляются у кислой горной породы с преобладающим количеством глинистых минералов. В короткий период взаимодействия образца горной породы с раствором буферные свойства проявляются у щелочной породы активнее за счет преимущественного вступления в реакцию на границе раствор\порода обменных катионов.
Воздействие разрушенной ФК несколько изменяет РАМ, увеличивая способность к образованию комплексов для ионов Pb и Cu, и снижая для ионов Fe и Al.
Работа выполнена при финансовой поддержке гранта РНФ 18-77-00018.
Список литературы
Алексеев В.А. (2002) Кинетика и механизмы реакций полевых шпатов с водными растворами. М.: ГЕОС, 256 с.
Алексеев В.А., Кочнова Л.Н., Бычкова Я.В., Кригман Л.В. (2011) Экспериментальное исследование извлечения нормируемых элементов водой из загрязненных пород. Геохимия. (12), 1317-1342.
Alekseyev V.A., Kochnova L.N., Bychkova Y.V., Krigman L.V. (2011) Extraction of hazardous elements by water from contaminated rocks: an experimental study. Geochem. Int. 49(12), 1239-1262.
Бирюкова О.Н., Орлов Д.С. (2004) Содержание и состав гумуса в основных типах почв России. Почвоведение. (2), 171-188.
Ермолаева В.Н., Михайлова А.В., Когарко Л.Н., Колесов Г.М. (2016) Выщелачивание редкоземельных и радиоактивных элементов из щелочных пород Ловозерского массива (Кольский полуостров). Геохимия. (7), 651-658.
Ermolaeva V.N., Mikhailova A.V., Kogarko L.N., Kolesov G.M. (2016) Leaching rare-earth and radioactive elements from alkaline rocks of the Lovozero massif, Kola Peninsula. Geochem. Int. 54(7), 633-639.
Дину М.И. (2018) Геохимические особенности распределения элементов по формам существования в озерах Европейской территории России и Западной Сибири. Геохимия. (10), 988-997.
Dinu M.I. (2018) Geochemical specifics of the distribution of elements between their forms in lakes in the European part of Russia and Western Siberia. Geochem. Int. 56(10), 1036-1045.
Израэль Ю.А., Назаров И.М., Прессман А.Я. и др. (1983) Кислотные дожди. Л.: Гидрометеоиздат, 206 с.
Колесов Г.М., Ермолаева В.Н., Михайлова А.В., Когарко Л.Н. (2012) Гидрогели как новые концентраторы редкоземельных и радиоактивных элементов после их выщелачивания из пород Ловозёрского массива при ИНАА определении. Геохимия. (10), 333-336.
Kolesov G.M., Ermolaeva V.N., Mikhailova A.V., Kogarko L.N. (2012) Hydrogels as new rare-earth and radioactive elements after their leaching from the rocks of the Lovozero massif during INAA determination. Geochem. Int. 50(3), 304-307.
Моисеенко Т.И., Гашкина Н.А. (2010) Формирование химического состава озер в условиях изменения окружающей среды. М.: Наука, 268 с.
Новикова С.П., Гаськова О.Л. (2013) Влияние природных фульвокислот на растворимость сульфидных руд (экспериментальное изучение). Геология и геофизика. 54(5), 665-675.
Самсонова Н.С. (1973) Минералы группы нефелина. М.: Наука, 155 с.
Chuncai Z., Guijian L., Ting F., Ruoyu S., Dun W. (2014) Leaching characteristic and environmental implication of rejection rocks from Huainan Coalfield, Anhui Province, China. JGE. 143, 54-63.
Duan P., Wang W., Sang S., Tang Y., Liang B., Zhao X. (2019) Leaching behavior and organic affinity of potentially toxic elements V, Cr, Mo, and U in flotation-cleaned coal from the Ganhe Mine, China. JGE. 200, 152-158.
Gaskova O.L., Bessonova E.P., Bortnikova S.B. (2003) Leaching experiments on trace element release from the arsenic-bearing tailings of Khovu–Aksy (Tuva Republic, Russia). Appl. Geochem. 18(9), 1361-1371.
MacKenzie W.S. (1957) The crystalline modifications of NaAlSi3O8. Am. J. Sci. 255, 481-516.
Richet P., Bottinga Y., Deniélou L., Petitet J.P., and Téqui C. (1982) Thermodynamic properties of quartz, cristobalite, and amorphous SiO2: drop calorimetry measurements between 1000 and 1800 K and a review from 0 to 2000 K. Geochim. Cosmochim. Acta. 46, 2639-2658.
Savenko A.V., Savenko V.S., Dubinin A.V. (2017) Leaching of trace elements from the rocks under action of organic acids. Mosc. Univers. Bull. Geol. 4(6), 66-73.
Shan Y., Wang W., Qin Y., Gao L. (2019) Multivariate analysis of trace elements leaching from coal and host rock. Groundwater for Sustainable Development. (8), 402-412.
Дополнительные материалы отсутствуют.