Геохимия, 2022, T. 67, № 7, стр. 668-685
Изменение геохимии вод суши в условиях потепления климата и снижения выпадений кислот: восстановление или эволюция озер?
Т. И. Моисеенко a, *, М. М. Базова a, М. И. Дину a, Н. А. Гашкина a, Л. П. Кудрявцева b
a Институт геохимии и аналитической химии им. В.И. Вернадского РАН
119991 Москва, ул. Косыгина, 19, Россия
b Институт проблем промышленной экологии Севера КНЦ РАН
184209 Мурманская область, Апатиты, мкр. Академгородок, 14А, Россия
* E-mail: moiseenko.ti@gmail.com
Поступила в редакцию 18.05.2021
После доработки 07.10.2021
Принята к публикации 10.10.2021
- EDN: UIZYDU
- DOI: 10.31857/S0016752522060036
Аннотация
Представлены результаты долговременных исследований изменения геохимии вод суши на территории Кольского региона (1990–2018 гг.), которые произошли вследствие потепления климата и снижения эмиссии кислотообразующих газов в региональной и глобальной шкалах. В основу работы легли исследования 75 малых озер региона, которые проводились с 1990 по 2018 гг. с интервалом в 4–5 лет. На основании анализа архивов погоды выявлены достоверные тренды повышения температуры за 28-летний период исследований. Установлено повсеместное снижение содержаний техногенных сульфатов в воде и повышения кислотонейтрализующей способности вод вследствие сокращения выбросов в атмосферу антропогенной серы. Доказано увеличение содержания органического вещества и биогенных элементов в воде озер, которое достоверно связано с нарастанием температур в регионе. Ряд озер в кислотоуязвимых регионах сохраняют критические значения кислотонейтрализующей способности вод, что может быть связано как с локальным, так и с трансрегиональным переносом загрязненных воздушных масс. Приведенный анализ изменчивости химического состава вод в многолетнем ряду наблюдений демонстрирует эволюционное развитие озер и изменение биогеохимических циклов, как следствие преобразований водосборов под влиянием снижения выпадений кислот из атмосферы на водосборы и потепления климата в регионе.
ВВЕДЕНИЕ
Экологические последствия выбросов газов в атмосферу (CO2, SO2, NOx, NH4) от индустриальной деятельности наиболее ярко проявились в 70-х годах прошлого столетия. В.И. Вернадский (1991) в начале прошлого столетия отмечал, что человеческая деятельность резким и радикальным образом изменяет течение естественных процессов и преображает то, что мы называем законами природы. Рост парниковых газов привел к изменениям климатической системы на планете (IPCC, 2014). Наиболее яркими последствиями повышения парниковых газов в атмосфере были неустойчивость погоды, изменение осадков и нарушение гидрологических циклов – увеличение засушливых периодов и опустынивание в теплом климате; увеличение осадков – в гумидных зонах. Возрастание содержания органического вещества в сочетании с температурой приводит к повышению биопродуктивности лесов, океанов, рек и озер (Campbell et al., 2009; Melillo et al., 2014). Несмотря на снижение эмиссии парниковых газов, в глобальной шкале, с 1980 г. средняя температура воздуха на планете увеличилась на 0.5 градуса по Цельсию, и Земля продолжает нагреваться примерно на 0.16 градуса за десятилетие с вариабельностью на разных участках Планеты (IPCC, 2014). По данным Г.В. Груза, Э.Я. Раньковой (2012) в северо-западном регионе России температура возрастает на 0.53°С каждые 10 лет.
С увеличением выбросов парниковых газов и повышением температуры в течение прошлого столетия происходили выбросы кислотообразующих газов (SO2 и NOx), главным образом от сгорания мазута, каменного угля и в процессе выплавки металлических руд, что привело к формированию кислотных осадков. Уровень эмиссии антропогенной серы в Европе и Северной Америке быстро нарастал в начале прошлого века и к его середине достиг максимальных значений (Galloway, 1995). В последние 30 лет, несмотря на существенное снижение выбросов SO2 в Северной Америке и Европе, а также и в Китае с 2005 г. (Garmo et al., 2014), выпадения кислот на водосборы пока превышают уровень доиндустриального периода. Кислотные осадки изменяют транспортные потоки элементов в оболочках Земли, ускоряют химическое выветривание основных катионов и металлов, изменяют биогеохимические циклы элементов в литосфере и пресноводной гидросфере (Моисеенко и др., 2017). Воды суши находятся в числе природных компонентов, сознательные преобразования которых или попутные изменения наиболее существенны. Малые озера преимущественно атмосферного питания отражают те изменения, которые происходят под влиянием как потепления климата, так и атмосферных выпадений.
Климат и химический состав атмосферных выпадений оказывает существенное влияние на биогеохимические циклы элементов в водоеме и на водосборе. В литературе появляется все больше свидетельств, указывающих на влияние климатического фактора, приводящее к изменчивости химического состава вод (Clark et al., 2010; Feuchtmayr et al., 2009; Watmough et al., 2016; Gavin et al., 2018). D. Houle et al. (2010) отметили, что более высокие годовые температуры воздуха коррелируют с щелочностью и pH озер в многолетнем ряду наблюдений. J.R. Corman et al. (2018) установили, что нарастание органического вещества связано с поступлением биогенных элементов – нитратов и фосфатов. Повышение уровня общего фосфора установлено повсеместно в озерах и ручьях США, которые не связаны ни с точечными, ни с диффузными потоками фосфора с водосборов (Stoddard et al., 2016).
Закисление вод проявилось в кислоточувствительных регионах многих стран к 60-м годам прошлого столетия и продолжало интенсифицироваться до 70–90-х годов. Исследования влияния кислотных осадков на воды и почвы в этот период были проведены в Северной Америке и Европе. Принятие ряда международных решений в 1980-е годы по сокращению выпадений кислотообразующих газов привели к снижению выпадений кислот на водосборы в центральной Европе и северной Америке. Поверхностные воды во многих кислоточувствительных регионах стали частично восстанавливаться от закисления в ответ на уменьшение эмиссии SO2 и NOx (Monteith et al., 2007; Stoddard et al., 1999; Skjelkvale et al., 2001, 2005; Clair et al., 2011; Strock et al., 2014; Rogora et al., 2016). Отмечаются общие тенденции изменения ряда показателей химического состава вод, которые наблюдаются в озёрах и реках Европы и Северной Америки: увеличение содержания растворенного органического вещества, азота и фосфора, снижения содержания основных катионов (Skjelkvale et al., 2001, 2005; Monteith et al., 2007; Stoddard et al., 2016; Strock et al., 2014, 2017). В России в начале 1990-х годов было выявлено закисление вод в ряде регионов – в Мурманской обрасти, Карелии, Архангельской и Вологодской областях, где геологическая структура водосборов уязвима к кислотным выпадениям (Moiseenko, 1994; Комов и др., 1997; Моисеенко и др., 2017). Позднее было установлено наличие до 5% антропогенно- закисленных озер на обширных пространствах гумидных регионов Европейской территории России и Западной Сибири (Moiseenkо et al., 2018). Наиболее высокие выбросы диоксида серы в прошлом веке были характерны для предприятий цветной металлургии, в частности концерна “НорНикель”, которые функционируют в Кольском и Норильском регионах. Как и в странах Европы и Северной Америки, выбросы SO2 здесь значительно снизились за последние 30 лет. Недавние исследования показали, что вследствие высокой буферной способности пород на водосборах Норильского региона закисление вод не развивается, тогда как на Кольском Севере и в арктической зоне Западной Сибири, несмотря на снижение выбросов, критические нагрузки по выпадению кислот превышены над способностью водосборов к их нейтрализации (Moiseenkо et al., 2020).
Тенденции изменения химического состава вод в Европейских странах и США произошли в большинстве озер, как отмечалось выше. Однако в ряде озер в кислотоуязвимых регионах, несмотря на значительное сокращение выбросов SO2, восстановление кислотонейтрализующей способности вод не всегда происходит. Долговременный мониторинг химического состава вод озер дает возможность изучения эволюции озер и оценку эффективности снижения аэротехногенного загрязнения при сопутствующем потеплении климата.
Целью исследований было дать понимание ключевым факторам, контролирующим скорость восстановления кислотонейтрализующей способности вод для прежде закисленных озер; оценить влияние повышения температуры на эволюцию озер в течении длительного периода снижения выпадений сульфатов и потепления климата. В основу работы были положены данные регулярных исследований на Кольском Севере, которые проводились с 1990 по 2018 гг. с интервалом в 4–5 лет.
МАТЕРИАЛЫ И МЕТОДЫ
Объекты исследования
Большая часть территории Кольского Севера расположена за Полярным кругом в двух географических зонах – тундре и тайге. С трех сторон – севера, востока и юга она омывается Баренцевым и Белыми морями, примерно две трети территории занимает Кольский полуостров. Ландшафты северо-восточной части региона представлены тундрой. По мере продвижения на юг территория тундры сменяется лесотундрой, в центральной и южной части региона – северной тайгой. Полярная зима длится 6–7 мес. (Атлас…, 1971).
Для оценки вариаций климата мы использовали доступные данные по температуре и количеству осадков за 28 летний период наблюдений (Архив погоды, 2019). Имея возможность получения данных по среднемесячным показателям температуры и осадков за исследованный период, мы использовали среднемесячные температуры приземного слоя воздуха в период открытой воды (июнь, июль, август и сентябрь) по четырем станциям, расположенным в северо-западной части региона, на севере (побережье Баренцева моря), в центральной части региона (водораздел между полуостровом) и на юге Кольского п-ова (побережье Белого моря).
Геологическая структура Кольского региона очень разнообразна. Обнажения кислых гранитовых пород характеры для северо-восточной и юго-восточной части Кольского п-ва. Центральная часть региона, в районе Хибинских и Ловозерских гор сложена щелочными породами (апатит-нефелиновыми сиенитами). Расположение Кольских медно-никелевых плавилен приурочено к основным породам, которые определяют хорошие буферные свойства вблизи расположенных от них озер (Пожиленко и др., 2002).
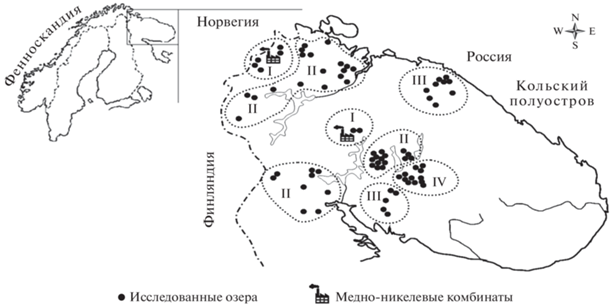
Картосхема региона со схемой точек исследования, которые повторялись раз в 4–5 лет, представлены на рис. 1. Учитывая высокое разнообразие геохимических условий формирования вод, нами были выделены 4 субрегиона, в зависимости от удаленности от плавилен, геологических и ландшафтных условий формирования вод, а также чувствительности к кислотным выпадениям: I – промышленная зона, II – устойчивые породы, III – кислотоуязвимые породы; IV – заболоченные и лесные массивы (табл. 1). На картосхеме локация субрегионов обозначена римскими цифрами. Наиболее уязвимым по геологическому строению является субрегион III (северо-восточная и юго-восточная часть региона). В восточной части региона большие территории заняты болотными массивами. Остальные регионы (Западные территории) на большей части по геохимическим условиям формирования вод обладают хорошей буферной способностью, здесь развиты лесные массивы. Общая характеристика геологической структуры и ландшафтов в пределах выделенных субрегионов представлена в таблице 1.
Таблица 1.
Ландшафтные (залесенность, заболоченность) и геохимические характеристики (основной тип пород) в выделенных субрегионах Кольского Севера
| Субрегион | Основной тип пород | Залесенность, % | Заболоченность, % | Расстояние от плавилен, км |
|---|---|---|---|---|
| I | Базальты, гнейсы | 47 | 12 | <40 км |
| амфиболиты, сланцы | 2–58 | 3–17 | ||
| II | Базальты, габбро, гнейсы | 63 | 15 | 40–120 км |
| нефелиновые сиениты, уртиты | 6–92 | 0–47 | ||
| III | Граниты, | 54 | 22 | >120 км |
| кварцевые пески | 0–76 | 0–29 | ||
| IV | Гнейсы, диориты, мигматиты | 74 | 23 | >120 км |
| тоналиты, пироксены | 56–81 | 16–46 |
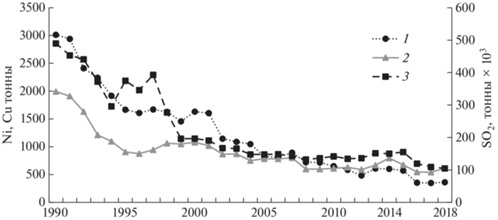
Более 70-лет на Кольском севере функционируют производства по переработке медно-никелевых руд “Североникель” и “Печенганикель. На рис. 2 представлена динамика выбросов Кольскими плавильнями SO2, Ni и Cu (Доклады…, 2019). Максимальные выбросы серы от медно-никелевых комбинатов были в середине 70-х годов и сохранялись до 80-х годов, когда Кольские плавильни работали на медно-никелевой руде с высоким содержанием серы, доставляемой из Норильска. В 1980-е годы выпадения антропогенной серы оценивались вблизи производств в 1.5–3.0 гS/м2 год, на удалении более 200 м – выпадения оценивались в 0.5 гS/м2 год. В течении 30-летнего периода исследований эмиссия серы устойчиво снижалась до 2010 года и в последние десятилетия была относительно низкой. Среднегодовое влажное выпадение серы составило 0.37 гS/м2 год (2018 г.) (Ежегодник о состоянии…, 2019).
База данных и аналитическая программа
Первые исследования химического состава вод озер были организованы в 1990 г., когда активно начала развиваться кооперация Кольского научного центра Российской академии наук с Институтами соседних стран (Финляндии, Норвегии и Швеции). В 1995 г. в рамках совместного проекта “Northern European lake survey” были исследованы 460 озер на Кольском Севере, включая отдаленные озера восточной части Кольского полуострова. Результаты представлены в работе (Henriksen et al., 1998). В дальнейшем, раз в 5 лет (2000, 2005, 2010, 2014 и 2018 гг.) в западной части региона повторялось обследование 75 малых озер на Кольском Севере, используя те же методы, как в работах в 1995, изложенных в программе по изучению проблемы закисления вод (ICP-waters, 2010).
В исследования включались озера, площадь водного зеркала которых варьировала от 0.4 до 20 км2 и не имеющие прямых источников антропогенного загрязнения. Чтобы минимизировать влияние внутригодовых и сезонных изменений, отбор проб воды осуществлялся в период осеннего охлаждения (в сентябре для тундровых озер, в октябре для таежных озер). Пробы воды были отобраны в полиэтиленовые несорбирующие бутыли фирмы “Nalgen”. Отбор проб воды осуществлялся путем повторного ополаскивания бутылей водой из озера, которые далее помещали в темные контейнеры и в охлажденном виде (~+4°С) транспортировали в кратчайшие сроки (в течении 5–10 дней) в лабораторию Института проблем промышленной экологии Севера КНЦ РАН (ИППЭС КНЦ РАН), где пробы анализировались. Определение химического состава вод выполняли по единым методикам в соответствии с рекомендациями (Standart Methods, 1992; ICP-Water report, 2007).
Аналитическая программа включала в себя определение: pH, щелочности (Alk), основных катионов и анионов, нитратов (${\text{NO}}_{3}^{ - }$), общего азота (Ntot), фосфатов (${\text{PO}}_{4}^{{3 - }}$), общего фосфора (Рtot), содержание растворенного органического вещества (DOC), цветности. рН определяли потенциометрическим методом; электропроводность при 20°C – кондуктометрическим; щелочность – потенциометрическое титрование по методу Грана; содержание органического вещества по перманганатной окисляемости. Катионы (Са2+, Mg2+) были определены методом атомно-абсорбционной спектрометрии в пламени; К+, Na+-атомно-2-эмиссионной спектрометрией в пламени; анионы (${\text{SO}}_{4}^{{2 - }}$, Сl–) – ион-хроматографическое определение. Нитраты, общий азот, фосфаты и общий фосфор – спектрофотометрическое определение.
Показатель кислотонейтрализующей способности вод (АNС) рассчитывался без коррекции ионов на морские соли по следующей формуле (Henriksen et al., 1992):
(1)
$\begin{gathered} {\text{ANC\;}} = [{\text{C}}{{{\text{a}}}^{{2 + }}}] + [{\text{M}}{{{\text{g}}}^{{2 + }}}] + [{\text{N}}{{{\text{a}}}^{ + }}] + [{{{\text{K}}}^{ + }}] + \\ + \,\,[{\text{N}}{{{\text{H}}}^{{4 + }}}]~ - [{\text{SO}}_{4}^{{2 - }}]~ - [{\text{NO}}_{3}^{ - }]~ - [{\text{С}}{{{\text{l}}}^{ - }}]. \\ \end{gathered} $Для оценки содержания антропогенной серы (${\text{SO}}_{4}^{*}$) общая концентрация сульфатов в озерах была откорректирована на устранение доли сульфатов морского происхождения. Содержания основных катионов и анионов, щелочность и кислотонейтрализующая способность представлены в микромолльэквивалентах (Мкм-экв/л).
Концентрация Al, Fe, Сu, Ni определялась атомно-абсорбционным методом (GFAAS, model Perkin-Elmer – 5000, Corp., Norwalk, USA) с непламенной атомизацией (HGA-400). Статистическая обработка данных осуществлялась с использованием компьютерной программы “Статистика 10”. Для выявления тренда в выделенных субрегионах был использован непараметрический тест Манна–Кендалля (SKT), в качестве параметров были выбраны6показателей:${\text{SO}}_{4}^{*}$, BC,ANC, DOC, Ntot, Ptot.
Было применено многомерное шкалирование, основанное на сродстве данных (точки) к векторам основных параметров (независимые переменные). Анализ избыточности (RDA) как метод множественной регрессии в многомерном масштабировании широко используется для изучения сложных природных объектов. Исследована достоверность связей между температурой (T), ${\text{SO}}_{4}^{*}$ (антропогенная нагрузка), жесткостью (геохимические особенности) и DOC как биоорганический фактор, а также ANC, Cu и Ni, Ptot и Ntot как биологические особенности окружающей среды.
РЕЗУЛЬТАТЫ
Климатические условия и тенденции их изменений
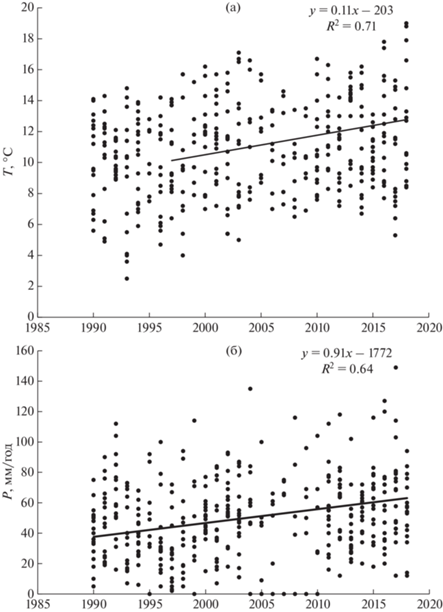
Расположение региона за полярным кругом определяет его климатические особенности. Северо-западная часть региона характеризуется низкими среднегодовыми значениями температуры воздуха (–1°С) и высокими значениями осадков (до 800 мм/год). Для тундровой зоны побережья Баренцева моря среднегодовая температура воздуха колеблется в пределах – 1°С, среднегодовое количество осадков составляет 700 мм/год. Центральная часть региона характеризуется более низким количеством осадков (550–600 мм/год), значения среднегодовой температуры воздуха составляют –1°С. Для южной части региона характерно самое низкое количество осадков (500 мм/год) и самые высокие значения температуры воздуха (Атлас…, 1971). Данные этих станций метеонаблюдений отражают общую тенденцию изменения осадков и температуры в исследуемом регионе в летне-осенний период. На рис. 3а представлены данные по среднемесячным температурам приземного слоя воздуха в период открытой воды с 1990 по 2018 гг. При высокой вариабельности температур воздуха мы видим достоверный тренд повышения температуры в период открытой воды. Наряду с повышением температуры статистически значимо увеличилось количество атмосферных осадков (рис. 3б). Оба этих параметра отражают достоверный положительный наклон тренда температуры и осадков: SKT = +4.71, p < 0.001 и = +2.71, p < 0.01 соответственно.
Долговременные изменения основных параметров химического состава вод
Низкую минерализацию и олиготрофность озер Кольского региона можно объяснить геологическими и климатическими особенностями региона. Na+ и Cl– являются преобладающими ионами в озерах тундры и лесотундры, а также в северной тайге, что вызвано влиянием Белого и Баренцева морей; морское влияние также объясняет высокое естественное содержание ${\text{SO}}_{4}^{{2 - }}$ в этих озерах. Однако ${\text{SO}}_{4}^{*}$ антропогенного происхождения также были обнаружены в воде озер импактных зон из-за влияния выбросов “Печенганикеля” и “Североникеля”, которые работают на Кольском полуострове и выбрасывают диоксид серы в атмосферу, поэтому возникновение антропогенных сульфатов (${\text{SO}}_{4}^{*}$) можно объяснить длительным сроком эксплуатации предприятий (Moiseenko et al., 2015). Широкая вариабельность химического состава вод в этих озерах также, вероятно, является результатом разнообразия геологических условий и типов почв.
В таблице 2 представлена динамика основных показателей химического состава вод в выделенных субрегионах за 28-летний период. В воде озер, расположенных в промышленной зоне (I субрегион) высокое содержание сульфатов обусловлено влиянием комбинатов “Печенганикель” и “Североникель”. Однако в период с 1990 по 2018 гг. по медианным и минимальным значениям отмечено их снижение. Цветность в этих озерах низкая и по медианным значениям имеет тенденцию к снижению (на 12° Pt-Co). Значения ANC сильно варьируют в течение исследуемого периода (15–292 Мкм-экв/л) и не имеют четких тенденций. Содержания Ntot в среднем ниже по сравнению с озерами других субрегионов, содержания Ptot мало изменялись и находятся в пределах варьирования. Воды озер вследствие высокого уровня аэротехногенной нагрузки характеризуются повышенными концентрациями Cu и Ni в 1990 г., к 2018 в среднем имеют тенденцию к снижению.
Таблица 2.
Медианные, минимальные и максимальные значения показателей химического состава вод за 28-летний период (1990–2018) в выделенных субрегионах Кольского Севера
| Год | Цветность | DOC | ВС | S${\text{O}}_{4}^{*}$ | ANC | Ntot | Ptot | Cu | Ni |
|---|---|---|---|---|---|---|---|---|---|
| 0 Pt-Co | мгС/л | Мкм-экв/л | Мкм-экв/л | Мкм-экв/л | мкгN/л | мкгP/л | мкг/л | мкг/л | |
| I – промышленная зона, n = 7 | |||||||||
| 1990 | $\frac{{26}}{{12 - 33}}$ | $\frac{{3.7}}{{2.9 - 4.0}}$ | $\frac{{404}}{{298 - 527}}$ | $\frac{{124}}{{87 - 150}}$ | $\frac{{89}}{{61 - 147}}$ | $\frac{{49}}{{25 - 184}}$ | $\frac{3}{{0 - 12}}$ | $\frac{{9.5}}{{2.2 - 15.0}}$ | $\frac{{24.5}}{{5 - 65}}$ |
| 1995 | $\frac{{24}}{{23 - 50}}$ | $\frac{{3.8}}{{2.9 - 5.6}}$ | $\frac{{381}}{{243 - 568}}$ | $\frac{{100}}{{80 - 266}}$ | $\frac{{118}}{{48 - 152}}$ | $\frac{{70}}{{33 - 103}}$ | $\frac{{2.5}}{{1 - 3}}$ | $\frac{{3.3}}{{1.1 - 14.1}}$ | $\frac{{12}}{{5 - 65}}$ |
| 2000 | $\frac{{14}}{{4 - 25}}$ | $\frac{{4.0}}{{2.8 - 4.8}}$ | $\frac{{282}}{{241 - 517}}$ | $\frac{{105}}{{71 - 209}}$ | $\frac{{140}}{{15 - 150}}$ | $\frac{{84}}{{103 - 150}}$ | $\frac{{4.5}}{{1 - 6.0}}$ | $\frac{{2.5}}{{1.1 - 12}}$ | $\frac{{7.5}}{{3.1 - 60}}$ |
| 2005 | $\frac{{15}}{{8 - 33}}$ | $\frac{{3.6}}{{2.4 - 6.1}}$ | $\frac{{274}}{{195 - 479}}$ | $\frac{{100}}{{50 - 187}}$ | $\frac{{128}}{{68 - 147}}$ | $\frac{{106}}{{87 - 157}}$ | $\frac{6}{{4 - 10}}$ | $\frac{{7.3}}{{2.7 - 54}}$ | $\frac{{5.6}}{{1.6 - 8.9}}$ |
| 2010 | $\frac{{14}}{{6 - 20}}$ | $\frac{{4.9}}{{3.1 - 5.9}}$ | $\frac{{361}}{{213 - 504}}$ | $\frac{{102}}{{49 - 178}}$ | $\frac{{143}}{{78 - 162}}$ | $\frac{{146}}{{82 - 176}}$ | $\frac{5}{{2 - 6}}$ | $\frac{{6.2}}{{2.3 - 12}}$ | $\frac{{8.4}}{{3.4 - 74}}$ |
| 2014 | $\frac{{15}}{{9 - 49}}$ | $\frac{{3.9}}{{2.9 - 8.4}}$ | $\frac{{377}}{{226 - 514}}$ | $\frac{{112}}{{47 - 189}}$ | $\frac{{153}}{{32 - 292}}$ | $\frac{{118}}{{94 - 202}}$ | $\frac{{10}}{{5 - 17}}$ | $\frac{8}{{2.2 - 14.2}}$ | $\frac{{12}}{{3.1 - 79}}$ |
| 2018 | $\frac{{14}}{{4 - 22}}$ | $\frac{{4.2}}{{2.6 - 5.4}}$ | $\frac{{363}}{{237 - 506}}$ | $\frac{{106}}{{49 - 187}}$ | $\frac{{131}}{{92 - 172}}$ | $\frac{{126}}{{108 - 226}}$ | $\frac{7}{{4 - 22}}$ | $\frac{{6.3}}{{2 - 11.8}}$ | $\frac{{11.4}}{{2.2 - 65}}$ |
| II – устойчивые породы (основные и щелочные породы), n = 42 | |||||||||
| 1990 | $\frac{{33}}{{14 - 84}}$ | $\frac{{4.9}}{{2.6 - 8.0}}$ | $\frac{{310}}{{218 - 1265}}$ | $\frac{{62}}{{48 - 81}}$ | $\frac{{242}}{{88 - 388}}$ | $\frac{{166}}{{106 - 476}}$ | $\frac{7}{{0 - 20}}$ | $\frac{2}{{1 - 11}}$ | $\frac{{4.4}}{{1 - 9}}$ |
| 1995 | $\frac{{27}}{{1 - 58}}$ | $\frac{{6.5}}{{2.6 - 14.5}}$ | $\frac{{324}}{{57 - 1062}}$ | $\frac{{52}}{{22 - 195}}$ | $\frac{{199}}{{8 - 648}}$ | $\frac{{206}}{{75 - 747}}$ | $\frac{6}{{1 - 81}}$ | $\frac{{0.7}}{{0.1 - 5.6}}$ | $\frac{{0.6}}{{0.1 - 31}}$ |
| 2000 | $\frac{{31}}{{0 - 105}}$ | $\frac{{6.7}}{{1.6 - 14.5}}$ | $\frac{{310}}{{54 - 1005}}$ | $\frac{{49}}{{23 - 174}}$ | $\frac{{310}}{{48 - 682}}$ | $\frac{{202}}{{57 - 477}}$ | $\frac{5}{{2 - 54}}$ | $\frac{{0.7}}{{0.2 - 5.4}}$ | $\frac{{0.9}}{{0.2 - 15}}$ |
| 2005 | $\frac{{29}}{{5 - 123}}$ | $\frac{{6.9}}{{3.0 - 18.7}}$ | $\frac{{309}}{{109 - 918}}$ | $\frac{{43}}{{18 - 132}}$ | $\frac{{204}}{{66 - 642}}$ | $\frac{{208}}{{99 - 766}}$ | $\frac{6}{{3 - 90}}$ | $\frac{{0.7}}{{0.2 - 6.7}}$ | $\frac{{0.9}}{{0.3 - 10.4}}$ |
| 2010 | $\frac{{22}}{{5 - 90}}$ | $\frac{{7.3}}{{2.6 - 22.5}}$ | $\frac{{318}}{{\begin{array}{*{20}{l}} {51 - 997} \end{array}}}$ | $\frac{{43}}{{12 - 131}}$ | $\frac{{232}}{{66 - 789}}$ | $\frac{{233}}{{70 - 779}}$ | $\frac{6}{{3 - 80}}$ | $\frac{{1.1}}{{0.3 - 12}}$ | $\frac{{0.9}}{{0.4 - 6}}$ |
| 2014 | $\frac{{28}}{{6 - 128}}$ | $\frac{{6.7}}{{4.0 - 21.0}}$ | $\frac{{329}}{{105 - 957}}$ | $\frac{{47}}{{16 - 139}}$ | $\frac{{240}}{{62 - 794}}$ | $\frac{{240}}{{130 - 639}}$ | $\frac{{10}}{{5 - 76}}$ | $\frac{{0.8}}{{0.1 - 7.7}}$ | $\frac{{0.5}}{{0.1 - 19.5}}$ |
| 2018 | $\frac{{20}}{{4 - 136}}$ | $\frac{{5.4}}{{2.7 - 16.5}}$ | $\frac{{366}}{{119 - 684}}$ | $\frac{{41}}{{13 - 116}}$ | $\frac{{265}}{{56 - 608}}$ | $\frac{{304}}{{110 - 836}}$ | $\frac{8}{{4 - 93}}$ | $\frac{{0.8}}{{0.3 - 12.5}}$ | $\frac{{0.7}}{{0.2 - 65}}$ |
| III – кислотоуязвимые (граниты и кварцевые пески), n = 14 | |||||||||
| 1990 | $\frac{{27}}{{2 - 50}}$ | $\frac{{4.7}}{{2.8 - 8.2}}$ | $\frac{{189}}{{61 - 283}}$ | $\frac{{57}}{{18 - 106}}$ | $\frac{{ - 12}}{{\left( { - 18} \right) - 14}}$ | $\frac{{171}}{{97 - 312}}$ | $\frac{4}{{2 - 9}}$ | $\frac{{1.6}}{{0.5 - 4}}$ | $\frac{{1.70}}{{0.2 - 2.0}}$ |
| 1995 | $\frac{{11}}{{1 - 43}}$ | $\frac{{3.8}}{{2.3 - 10.4}}$ | $\frac{{244}}{{70 - 335}}$ | $\frac{{34}}{{24 - 70}}$ | $\frac{{59}}{{ - 10 - 187}}$ | $\frac{{184}}{{86 - 470}}$ | $\frac{6}{{2 - 17}}$ | $\frac{{0.5}}{{0.2 - 0.7}}$ | $\frac{{0.4}}{{0.10 - 1.5}}$ |
| 2000 | $\frac{{16}}{{0 - 62}}$ | $\frac{{4.4}}{{2.3 - 10}}$ | $\frac{{225}}{{54 - 352}}$ | $\frac{{31}}{{17 - 64}}$ | $\frac{{80}}{{4 - 276}}$ | $\frac{{171}}{{86 - 420}}$ | $\frac{5}{{2 - 20}}$ | $\frac{{0.4}}{{0.2 - 1.1}}$ | $\frac{{0.3}}{{0.1 - 1.5}}$ |
| 2005 | $\frac{{21}}{{0 - 69}}$ | $\frac{{5.5}}{{2.4 - 10.9}}$ | $\frac{{230}}{{53 - 389}}$ | $\frac{{27}}{{8 - 61}}$ | $\frac{{59}}{{1 - 129}}$ | $\frac{{250}}{{113 - 488}}$ | $\frac{{11}}{{4 - 21}}$ | $\frac{{0.6}}{{0.4 - 2.2}}$ | $\frac{{0.7}}{{0.2 - 1.4}}$ |
| 2010 | $\frac{{14}}{{0 - 32}}$ | $\frac{{5.1}}{{2.2 - 7.0}}$ | $\frac{{245}}{{57 - 324}}$ | $\frac{{24}}{{9 - 51}}$ | $\frac{{68}}{{7 - 141}}$ | $\frac{{244}}{{94 - 478}}$ | $\frac{6}{{2 - 21}}$ | $\frac{{0.6}}{{0.1 - 2.0}}$ | $\frac{{0.8}}{{0.4 - 1.4}}$ |
| 2014 | $\frac{{21}}{{2 - 54}}$ | $\frac{{5.9}}{{2.2 - 9.4}}$ | $\frac{{262}}{{46 - 320}}$ | $\frac{{23}}{{15 - 49}}$ | $\frac{{54}}{{12 - 286}}$ | $\frac{{255}}{{95 - 432}}$ | $\frac{9}{{5 - 27}}$ | $\frac{{0.7}}{{0.3 - 1.8}}$ | $\frac{{0.5}}{{0.4 - 0.9}}$ |
| 2018 | $\frac{{22}}{{3 - 69}}$ | $\frac{6}{{2.7 - 9.6}}$ | $\frac{{264}}{{54 - 304}}$ | $\frac{{24}}{{9 - 44}}$ | $\frac{{91}}{{11 - 210}}$ | $\frac{{275}}{{159 - 563}}$ | $\frac{8}{{4 - 35}}$ | $\frac{{0.6}}{{0.3 - 1.4}}$ | $\frac{{0.6}}{{0.3 - 1.4}}$ |
| IV – заболоченные и лесные массивы, n = 12 | |||||||||
| 1990 | – | – | – | – | – | – | – | – | – |
| 1995 | $\frac{{123}}{{8 - 135}}$ | $\frac{{11.3}}{{3.5 - 22.2}}$ | $\frac{{161}}{{116 - 313}}$ | $\frac{{40}}{{18 - 59}}$ | $\frac{{82}}{{8 - 402}}$ | $\frac{{159}}{{77 - 290}}$ | $\frac{{6.5}}{{3 - 24}}$ | $\frac{{0.7}}{{0.1 - 4.2}}$ | $\frac{{0.8}}{{0.3 - 3.2}}$ |
| 2000 | $\frac{{81}}{{5 - 102}}$ | $\frac{{12.2}}{{4.3 - 15.1}}$ | $\frac{{153}}{{110 - 325}}$ | $\frac{{24}}{{18 - 47}}$ | $\frac{{82}}{{15 - 350}}$ | $\frac{{270}}{{62 - 420}}$ | $\frac{{10}}{{5 - 13}}$ | $\frac{{1.5}}{{0.6 - 2.3}}$ | $\frac{{1.5}}{{0.2 - 2.9}}$ |
| 2005 | $\frac{{92}}{{5 - 122}}$ | $\frac{{14.7}}{{2.4 - 19.0}}$ | $\frac{{168}}{{79 - 214}}$ | $\frac{{27}}{{20 - 53}}$ | $\frac{{54}}{{5 - 125}}$ | $\frac{{342}}{{136 - 760}}$ | $\frac{{20}}{{2 - 38}}$ | $\frac{{1.2}}{{0.2 - 2.4}}$ | $\frac{{0.9}}{{0.6 - 2.7}}$ |
| 2010 | $\frac{{70}}{{5 - 91}}$ | $\frac{{14.6}}{{2.2 - 16.4}}$ | $\frac{{136}}{{113 - 191}}$ | $\frac{{20}}{{14 - 52}}$ | $\frac{{80}}{{3 - 137}}$ | $\frac{{239}}{{94 - 714}}$ | $\frac{{17}}{{4 - 41}}$ | $\frac{{1.3}}{{0.6 - 2.2}}$ | $\frac{{1.9}}{{0.6 - 2.2}}$ |
| 2014 | $\frac{{58}}{{24 - 128}}$ | $\frac{{9.4}}{{2.4 - 20}}$ | $\frac{{158}}{{67 - 229}}$ | $\frac{{21}}{{13 - 51}}$ | $\frac{{51}}{{9 - 389}}$ | $\frac{{330}}{{95 - 552}}$ | $\frac{{12}}{{5 - 22}}$ | $\frac{{1.3}}{{0.3 - 4.8}}$ | $\frac{{0.6}}{{0.2 - 1.4}}$ |
| 2018 | $\frac{{19}}{{4 - 121}}$ | $\frac{{8.6}}{{2.7 - 19.3}}$ | $\frac{{139}}{{78 - 447}}$ | $\frac{{18}}{{4 - 40}}$ | $\frac{{39}}{{5 - 385}}$ | $\frac{{380}}{{312 - 529}}$ | $\frac{{10}}{{5 - 16}}$ | $\frac{{0.8}}{{0.5 - 2.0}}$ | $\frac{{0.7}}{{0.4 - 2.5}}$ |
Озера, приуроченные к основным и щелочным породам (II субрегион), отличаются от других озер Кольского региона геохимическими особенностями пород и соответственно химическим составом вод. Воды озер на фоне снижения ${\text{SO}}_{4}^{*}$ характеризуются высокими буферными свойствами: сумма катионов (BC) по медианным значениям варьирует в пределах 309–366 Мкм-экв/л, ANC – от 190 до 310 Мкм-экв/л). Цветность варьирует в широких пределах (4°–128° Pt-Co), DOC (1.6–22.5) мгС/л, что свидетельствует об устойчивости вод к процессам закисления. Содержания биогенных элементов в воде озер достоверно увеличились за исследуемый период по медианным и максимальным значениям.
Влияние ${\text{SO}}_{4}^{*}$ на озера, приуроченные к кислотоуязвимым породам (III субрегион) минимальное в силу отдаленности от металлургических плавилен, и имеет тенденцию к снижению к 2018 г. по медианным значениям (с 57 к 24 Мкм-экв/л). В воде озер с 1990 к 2018 г. отмечено увеличение ANC по медианным значениям с критического значения (–12 Мкм-экв/л) до 91 Мкм-экв/л, а также по максимальным значениям, что свидетельствует об улучшении буферных свойств вод. Что касается биогенных элементов, к 2018 г. как по медианным, так и по максимальным значениям отмечено нарастание Ntot и Ptot, значения цветности и DOC в течение длительного периода были в пределах вариабельности.
В озерах, расположенных в заболоченных и лесных массивах (IV субрегион), с 1990 к 2018 гг. на фоне снижения содержаний ${\text{SO}}_{4}^{*}$ продолжают развиваться процессы закисления, о чем свидетельствуют снижения содержаний BC (по минимальным и медианным значениям), а также ANC (по медианным значениям). С 1990 к 2018 гг. отмечена четкая тенденция снижения цветности по медианным значениям (со 123° до 19° Pt-Co). В период с 1990 по 2005 г. произошло нарастание Ptot (в среднем в 3 раза), Ntot (в среднем в 2 раза) и DOC (на 3.4 мгС/л), что свидетельствует об обогащении вод гумусовыми веществами. Далее, с 2005 к 2018 г. произошло четкое снижение Ptot и DOC.
Эмиссия Ni и Cu от Кольских комбинатов в целом снижалась с 1990-х годов (рис. 2), что непосредственно сказалось на распределении металлов в водных системах. Однако к 2005 г. в водах преимущественно отмечено нарастание концентраций металлов вследствие пиковых выбросов диоксида серы SO2 и металлов.
Наиболее высокие концентрации Ni и Cu существуют в озерах, расположенных в зоне непосредственного влияния комбинатов (I субрегион), что закономерно. В этом субрегионе наблюдается значимое увеличение их концентраций до 2005 г., а затем тенденция к снижению. Во II субрегионе к 2018 г. по сравнению с 1990 отмечен тренд нарастания содержания Ni по максимальным значениям. В III и IV субрегионах содержания этих элементов близки к региональным значениям (Moiseenko, 1999).
В целом для озер, которые были исследованы c 1990 г. раз в 4–5 лет, к 2018 г. снизились содержания ${\text{SO}}_{4}^{*}$ и возрос ANC. В ответ на снижение эмиссии антропогенной серы Кольскими медно-никелевыми комбинатами (рис. 2), содержания ${\text{SO}}_{4}^{*}$ в воде исследуемых озер достоверно снизились с 121 до 41 Мкм-экв/л (по медианным значениям) (рис. 4а). В 1990-х годах было отмечено 34% озер, в воде которых среди анионов доминировали сульфаты, к 2010 году их количество снизилось до 25%, к 2018 г – до 8%. Содержания ${\text{NO}}_{3}^{ - }$ очень низки, и они не оказывают влияния на закисление вод на Кольском Севере. Содержания Cl– как по медианным, так и по минимальным и максимальным значениям мало изменились за исследуемый период.
Рис. 4.
Распределение ${\text{SO}}_{4}^{*}$, BC, ANC, DOC, Ntot, Ptot в воде озер Кольского региона за период 1990–2018 гг.
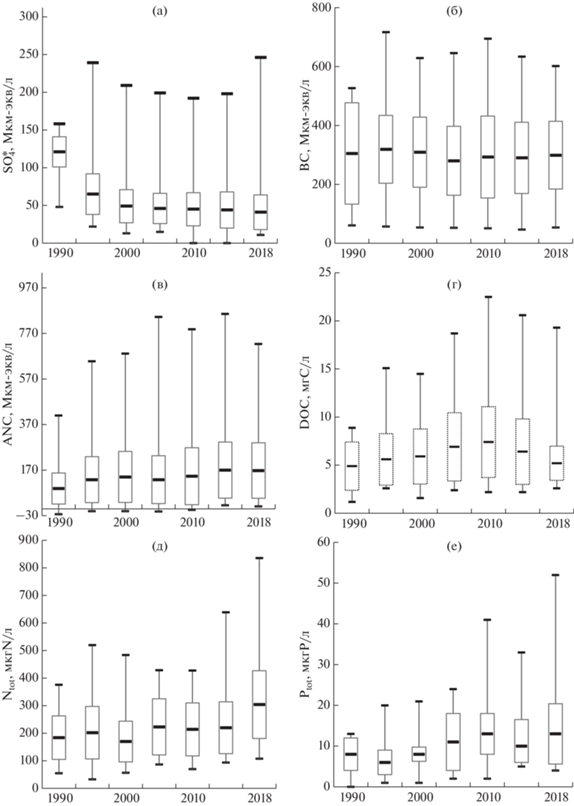
Для BC (рис. 4б) в воде озер по максимальным значениям за исследуемый период наблюдается тенденция роста (от 527 до 601 Мкм-экв/л). Однако если судить по медианным и минимальным значениям для всей популяции озер, то эти значения мало изменились, колебались в пределах 299–305 и 54–61 Мкм-экв/л соответственно за исследуемый 28-летний период. Содержания BC (рис. 4б) в воде озер за исследуемый период также имеют незначительную, но достоверную тенденцию к снижению содержаний (r = 0.62, p < 0.01).
Показатель ANC показал достоверные тенденции нарастания (рис. 4в): медианные значения увеличились с 89 до 168 Мкм-экв/л, минимальные значения также возросли, но остались в ряде озер в категории критических низких значений (от –23 до 11 Мкм-экв/л).
Особо следует отметить неоднозначную динамику DOC в водах озер, медианные значения закономерно увеличивались до 2010 г., в последующие 8 лет значения DOC понижались (рис. 4г). В то же время минимальные и максимальные значения существенно увеличились. Отмечен факт, что к 2018 г. по медианным значениям цветность снизилась на 29° Pt-Co, а по максимальным увеличилась на 48° Pt-Co. На динамике поведения этого показателя мы детально остановимся в обсуждении.
Содержания Ntot носит неоднородный характер в течение периода исследования (рис. 4д), несмотря на это по медианным значениям отмечено его увеличение (от 184 до 304 мкгN/ л), а также по минимальным в 2 раза, максимальным в 2.5 раза. Содержания Ptot в области минимальных значений, характерные для половины исследуемых озер, скорее всего, связаны с активной утилизацией продукционных процессов (рис. 4е). Максимальные содержания, отмеченные для небольшой группы озер обусловлены особенностями рудопроявлений, а также поступлением с водосборных территорий. В связи с потеплением климата, поступление и накопление биогенных элементов и органических веществ происходит быстрее. Увеличение миграции фосфора и азота с водосборных бассейнов может способствовать эвтрофикации озер (Feuchtmayr et al., 2009).
Для выявления тренда в выделенных субрегионах был использован непараметрический тест Манна–Кендалля (SKT), в качестве параметров были выбраны 6 показателей: ${\text{SO}}_{4}^{*}$, BC, ANC, DOC, Ntot, Ptot (табл. 3).
Таблица 3.
Результаты непараметрического теста Кендалля (SKT, уклон) для основных показателей химического состава вод
| Тренд SO4* | Жесткость | ANC | DOC | Ntot | Ptot | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| M ± m, Мкм-экв/л |
SKT | M ± m, Мкм-экв/л |
SKT | M ± m, Мкм-экв/л |
SKT | M ± m, Мкм-экв/л |
SKT | M ± m, мкгN/л |
SKT | M ± m, мкгР/л |
SKT |
| I – промышленная зона, n = 7 | |||||||||||
| 87 ± 49 | –0.62◇ | 208 ± 43 | –0.49◇ | 128 ± 39 | +0.93◇ | 3.9 ± 0.8 | +0.11◇ | 111 ± 31 | +1.93* | 5.0 ± 3.1 | +1.21◇ |
| II – устойчивые, n= 42 | |||||||||||
| 49 ± 26 | –4.03*** | 212 ± 78 | +3.14** | 198 ± 118 | +6.63*** | 6.0 ± 2.1 | +3.07** | 203 ± 98 | +5.62*** | 7.0 ± 3.7 | +2.16* |
| III – кислотоуязвимые, n = 14 | |||||||||||
| 27 ± 11 | –2.61** | 80 ± 36 | –2.25* | 63 ± 42 | +2.25* | 6.0 ± 2.9 | +2.32*** | 247 ± 110 | +2.43* | 7.5 ± 3.8 | +0.31◇ |
| IV– заболоченные, n = 12 | |||||||||||
| 27 ± 10 | –0.06◇ | 88 ± 78 | –0.53◇ | 88 ± 78 | –0.69◇ | 7.0 ± 4.0 | –0.81◇ | 322 ± 117 | +2.16* | 9.0 ± 5.4 | +2.65** |
| Весь регион, n = 75 | |||||||||||
| 42 ± 23 | –5.85*** | 283 ± 130 | +1.99* | 137 ± 117 | +7.15*** | 6.0 ± 2.3 | +2.29* | 215 ± 107 | +2.42* | 11.2 ± 7.3 | +2.74* |
Примечание. Результаты мета-анализа трендов показателей ${\text{SO}}_{4}^{*}$, жесткости, ANC, DOC, Ntot, Ptot в различных субрегионах Кольского Севера за период 1990–2018 гг. Статистические данные (значения p, основанные на тестах x2) получены из анализа дисперсии Z-уклонов и представляют собой тест на однородность тенденций в субрегионах и во всем регионе. *p < 0.05; **p < 0.01; ***p < 0.0001; ◇ тренд гетерогенный.
В I субрегионе (промышленная зона) для всех показателей, кроме Ntot, тренды гетерогенные вследствие того, что в течении длительного периода отмечается неравномерное нарастание или снижение рассматриваемого показателя. Однако, несмотря на гетерогенность, содержания ${\text{SO}}_{4}^{*}$ и жесткость снизились, а показатель ANC увеличился, что обусловлено снижением эмиссии техногенной серы. Тренд увеличения Ptot обусловлен длительностью аэротехногенного воздействия на водные объекты, в отличие от озер, расположенных на удалении от комбинатов.
Во II субрегионе (устойчивые породы) на фоне достоверного тренда снижения ${\text{SO}}_{4}^{*}$ происходит восстановление озер, которое выражается в увеличении жесткости, ANC и DOC. Повышение концентраций Ntot и Ptot связаны с высокой степенью залесенности и заболоченности субрегиона.
В III субрегионе (кислотоуязвимые породы) процесс восстановления озер происходит с запаздыванием, а именно на фоне снижения ${\text{SO}}_{4}^{*}$, с одной стороны продолжается снижение жесткости, с другой – увеличение ANC и DOC. Озера этого субрегиона характеризуются высоким промывным режимом. К 2018 г. отмечено повышение содержаний Ntot и Ptot (рис. 3д–е), которое скорее всего обусловлено распространением торфяно-глеевых и торфяно- болотных почв со сфагновым и травяным торфом.
В заболоченных и лесных массивах (IV субрегион) продолжают развиваться процессы закисления, о чем свидетельствуют тренды снижения показателей ${\text{SO}}_{4}^{*}$, BC, ANC, DOC, несмотря на гетерогенность. Однако достоверные тренды нарастания отмечены для Ntot и Ptot вследствие высокой доли заболоченности и залесенности, характерной для данного субрегиона (табл. 1).
В целом для исследованных озер Кольского региона прослеживается достоверный тренд снижения ${\text{SO}}_{4}^{*}$ , увеличение жесткости и ANC.
ОБСУЖДЕНИЕ
Изменения химического состава вод после снижения закисления
Множество сложных геохимических, биологических и климатических взаимодействий усложняют выявление ответных реакций химического состава вод озёр на снижение выпадений кислот. Несколько крупномасштабных обобщений показывают изменения химического состава вод озер в ответ на значительное сокращение кислотного выпадения на водосборы озер за последние 2–3 десятилетия (Stoddard et al., 1999; Skjelkvale et al., 2001; Garmo et al., 2014; Strock et al., 2014, 2017). Исследования, показывают значимое снижение ${\text{SO}}_{4}^{*}$ (r = 0.77, p < 0.001), однако значения ANC и рН в большинстве случаев вариабельны, которые авторы объясняют антагонистическими или аддитивными взаимодействиями между сокращением поступления техногенной S и изменениями частоты и интенсивности экстремальных влажных и сухих лет (Meingast et al., 2020). В целом, большинство исследований доказывают улучшение химического состава вод озер вследствие сокращения выпадений сильных кислот. Однако значения рН и ANC являются вариабельными в различных озерах в зависимости от ряда сопутствующих факторов.
Сходные различия в восстановлениях были выявлены в кислоточувствительных озерах Кольского Севера. В этом регионе наиболее очевидным является сокращение ${\text{SO}}_{4}^{*}$ и восстановление ANC, характеризующиеся достоверными трендами за последние 28 лет, как в целом по региону, так и в отдельных субрегионах (табл. 3). Тренд нарастания ANC характеризуется высокой степенью достоверности (r = 0.91, p < 0.001). Этот феномен наиболее характерен для вод субрегионов I и II, где водосборы имеют хорошую буферную способность. Однако для ряда озер ANC остается неизменным или продолжает снижаться, особенно в кислотоуязвимых и заболоченных водосборах (III и IV). Отметим, что концентрации N${\text{O}}_{3}^{ - }$ в водах субарктической зоны России очень низки и не вносят заметного вклада в расчеты ANC (табл. 2) во все периоды наших исследований.
Показано, что к 2010 г. отклик химического состава вод на сокращение выпадения сульфатов был неоднозначен: в 24% исследованных озер продолжали развиваться процессы закисления, в 46% – происходит восстановление и в 30% – не обнаружен отклик на сокращение эмиссии диоксида серы (Moiseenko et al., 2015). К 2018 это распределение сохраняется. Исследования долговременных тенденций на северо-востоке и юго-востоке США показали, что восстановление в ряде озер также не наблюдались вследствие влияния ряда сопутствующих факторов: снижения выпадений основных катионов, увеличения растворенного органического вещества (DOC), снижения поступления основных катионов с обедненных почв на водосборах, высвобождением из почв накопленных сульфатов за длительный период в годы интенсивной нагрузки (Stoddard et al., 1999; Driscoll et al., 2003, 2016; Kline et al., 2016).
Насыщение почв катионами на водосборах играет ключевую роль в процессах восстановления. Пул обменных основных катионов (особенно кальция) почв на водосборе в уязвимых регионах понижен вследствие длительных кислотных нагрузок и исторического их выщелачивания сильными кислотами. Истощение водосборов обменными катионами ограничивает способность почвы нейтрализовать кислотные выпадения. Рассмотрим более внимательно ответ жёсткости вод на динамику эмиссии за период наблюдений на Кольском Севере по субрегионам. К 2000–2010 гг. наблюдается снижение содержаний катионов (r = 0.62, p < 0.01), особенно в кислото-чувствительных регионах, сходных с процессами в Скандинавии и северо-востоке США. Отчасти этим может объясняться, что ожидаемое восстановление, в частности повышение ANC в ряде озер происходит медленнее или продолжает снижаться.
Однако в последующие годы жесткость вод повышается в большинстве субрегионов за исключением наиболее удаленного – III (табл. 3). Нарастание жесткости вод в озерах II субрегиона объясняются не столько восстановлением водосборов после кислотной нагрузки, но также усилением влияния распространения пыли от отвалов горных пород и складированных отходов обогащения руд. Кольский регион характеризуется развитием горной индустрии и наличием складированных отходов обогащения руд, которые в летний период являются источником распространения пыли. В работе отмечается повышенные выпадения кальция в составе атмосферных выпадений на Кольском Севере (Ежегодник о состоянии…, 2019). Повышенное содержание кальция наряду с высоким содержанием гидрокарбонатов в осадках может указывать на высокую запыленность воздуха. M. Rogora et al. (2016) отмечал влияние переноса пыли из Сахары на появление щелочных осадков в озерах Альпийских гор. На Кольском регионе “пылят” отходы обогащения руд. Особенно данный феномен характерен для II субрегиона (табл. 3).
В то же время нельзя исключить влияние климатических факторов, таких как повышение температуры, но в особенности усиление промывного режима в озерах, как следствие увеличения осадков в регионе. Таким образом, несмотря на общую тенденцию снижения сульфатов и повышение ANC, мы можем отметить продолжающееся закисление вод в ряде озер в кислотоуязвимых регионах, связанное с комплексом сопутствующих факторов. Эти районы удалены от влияния локальной эмиссии от Кольских производств. Однако мы допускаем влияние трансграничного переноса загрязненных сульфатами воздушных масс из более южных регионов.
Увеличение органического вещества и биогенных элементов
Тенденции восстановления ANC после подкисления и изменения климата сопряжены с нарастанием DOC в озерах, которое наблюдалось на всей территории США и Северной Европы. Многие поверхностные воды показали компенсационное увеличение DOC природного происхождения в водах озер и рек в ответ на уменьшение осаждения кислоты и/или изменение климата (Monteith et al., 2007; Strock et al., 2014; Driscoll et al., 2016). Временное увеличение DOC было названо “brownification”, которое описывает окрашивание воды в желто-коричневый цвет, вызванное поступлением растворенного гуминового вещества из наземных и водно-болотных угодий, что характерно для озер с высоким содержанием DOC (Monteith et al., 2007; de Wit et al., 2016; Strock et al., 2017; SanClements et al., 2018). В то же время, в этих работах не отрицается возможное влияние также и климатического фактора на повышение DOC в озерах и реках.
Растворенные органические вещества действуют как органические кислоты с характерными функциональными группами как сильных, так и слабых кислот (Evans et al., 2008; Driscoll et al., 2016). Увеличение поступления DOC с сильнокислыми функциональными группами подкисляет воды, компенсируя потенциальное увеличение АNC (Fakhraei, Driscoll, 2015). В исследованиях вод Западной Сибири показано, что гумусовые кислоты в этом регионе преимущественно проявляют свойства сильных кислот. Они могут усиливать закисление вследствие продуцирования протонов при их диссоциации, в которых катализом служат сильные техногенные кислоты (Moiseenko et al., 2018). Увеличение содержания органического вещества в водах озер наблюдалось и на Кольском Севере до 2010 года, особенно отчетливо в лесных и заболоченных субрегионах (II и IV). Динамика увеличения DOC описывается полиномиальной достоверной зависимостью:
(2)
$\begin{gathered} {\text{DOC}} = - 0.009{{х}^{2}} + 35х--35{\kern 1pt} 546 \\ (r = 0.76,\,\,p < 0.05). \\ \end{gathered} $В работе C. D. Evans et al. (2008) доказано, что в Великобритании при уменьшении поступления в озера сильных неорганических кислот техногенного происхождения (на 15–50%) увеличивается содержание природных органических кислот. В удаленных регионах Великобритании (Шотландии и северной Ирландии) эта пропорция может быть выше и объяснена другими факторами, например, влиянием потепления климата.
После 2010 г. содержания DOC в водах озер Кольского региона или сохраняли стабильность, или снизились. Если проанализировать динамику органического вещества по субрегионам, то тенденция к увеличению содержаний сохранялась только в регионах тундры побережья Баренцева моря и юго-восточной части Кольского региона (субрегион III). Понимание факторов повышения концентраций DOC трудно из-за сопряженных сигналов изменения климата и восстановления после подкисления. Наряду с влиянием химического состава выпадений, влияющих на поступление DOC, есть все больше доказательств в литературе, показывающих влияние климатических факторов на повышение DOC (Clark et al., 2010; de Wit et al., 2016; Gavin et al., 2018).
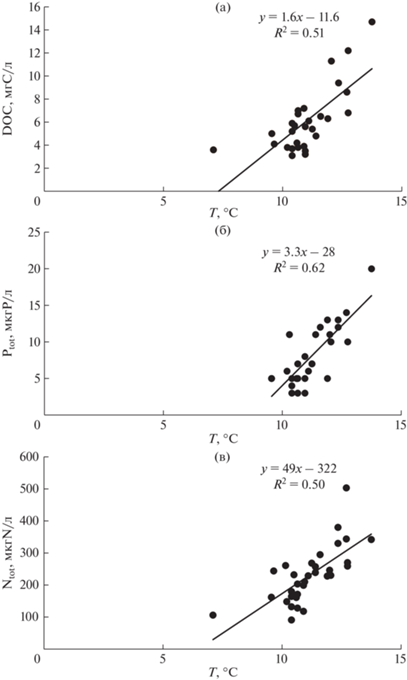
Потепление климата влияет на биогеохимические процессы на водосборах и внутри водоемов. Происходит более активное потребление в продукционных процессах биодоступных элементов (${\text{PO}}_{4}^{{2 - }}$ и ${\text{NO}}_{3}^{ - }$) как наземными растениями на водосборе, так и в озерах. Одновременно увеличивается содержание общих Ntot и Ptot, которые могут образовываться как внутри водоема, так и выноситься с водосборов вместе с DOC. Синхронное нарастание по годам и субрегионам содержаний DOC и общих форм биогенных элементов подтверждается корреляцией между DOC и Ptot (r = 0.68, n = 29), между DOC и Ntot (r = 0.60, n = 29). Наши данные показывают достоверную зависимость содержания в воде DOC, как и общих форм азота и фосфора от температурных условий (рис. 5а–в). Возрастающее из года в год соотношения Ptot/${\text{PO}}_{4}^{{2 - }}$ и Ntot/${\text{NO}}_{3}^{ - }$ свидетельствуют об успешной утилизации биодоступных форм в экосистемах и нарастании органического вещества в экосистемах.
Рис. 5.
Зависимости между DOC (а), Ptot (б), Ntot (в) и среднемесячной температурой приземного слоя воздуха (T) в период 1990–2018 гг.
В работе K.M. Meingast et al. (2020) сделано заключение об усилении экспорта DOC с водосбора при усилении промывного режима на водосборе, с которым также могут поступать Ptot и Ntot. J.L. Stoddard (2016) отмечает повсеместное увеличение фосфора и повышение трофического статуса озер в Северной Америке, что наблюдается и на Кольском Севере. Для озер, расположенных в кислотоуязвимых субрегионах характерна тесная положительная связь между DOC и Цветностью, как и в других регионах Европы и Северной Америке (Monteith et al., 2007; de Wit et al., 2016; Strock et al., 2017):
(3)
$\begin{gathered} {\text{Цветность}} = 7.5{\text{ }} \times {\text{DOC}} - 19.7 \\ (r = 0.74,n = 25). \\ \end{gathered} $В табл. 2 продемонстрировано труднообъяснимое снижении цветности вод за 28 летний период на фоне увеличения DOC, которое не равномерно происходит по субрегионам. Для озер, расположенных в устойчивых к закислению субрегионах наблюдается отрицательная связь между DOC и цветностью, которая подтверждается уравнением:
(4)
$\begin{gathered} {\text{Цветность}} = - 3.9 \times {\text{DOC}} + 2.3 \\ (r = 0.65,n = 50). \\ \end{gathered} $Остается дискуссионным вопросом, как меняется структура гумусовых веществ? Можно предположить, что в озерах при усилении продукционных процессов увеличивается доля образованного автохтонного органического вещества, которое имеет более низкую цветность, как низкомолекулярные вещества. Как правило, ‘‘brownification" связано с поступлением DOC c водосбора органического вещества аллохтонной природы, которое представлено крупными молекулами гумусовых кислот, поступающими с водосборами. Цветность вод определяется преимущественно крупными молекулами гуминовых кислот, молекулярная масса которых исчисляется десятками тысяч Da. Между тем, образованное внутри озера автохтонное вещество не приводит к столь значимому увеличению цветности вод. Однако, это не отрицает также причин повышения содержаний органического вещества за счет снижения выпадений сильных кислот.
В ряде работ отмечается, что при потеплении климата происходит снижение цветности природных вод из-за повышенного УФ-воздействия (Kohler et al., 2002; Ward, Cory, 2016; Drozdova et al., 2020). Авторами на основании экспериментальных и натурных исследований установлены процессы деградации органического вещества под воздействием УФ излучения, приводящее к снижению как молекулярного веса, так и параметра цветности. Можно предположить, что за счет уменьшения содержания более высокомолекулярной составляющей гумусовых веществ – гуминовых кислот, роль менее окрашенных фульвокислот в химическом составе вод возрастает.
Восстановление или эволюция озер?
Климат является основным регулятором биогеохимических процессов на водосборах, изменение климата, несомненно, влияет на эволюцию озер при уменьшении кислотных выпадений. На большей части северо-востока США, зарегистрировано повышение температуры, особенно с 1980-х годов и увеличение количества осадков в летний период (Campbell et al., 2009; Melillo et al., 2014). Сходные тенденции мы выявили на Кольском Севере в последние 28 лет – повышение температуры и количества осадков (рис. 4а и 4б).
Возможно, снижение выпадений кислот на водосборы и повышение температуры оказывают комплексное влияние на ряд водных систем (Feuchtmayr et al., 2009; Gavin et al., 2018; San Clements et al., 2018). В работе Watmough S.A. et al. (2016) отмечаются препятствия для восстановления химического состава вод после кислотных выпадений при значительном снижении (более 70%) поступления на водосборы сульфатов и нитратов. Продолжающееся закисление вод объясняется биогеохимическими процессами, происходящими на водно-болотных угодьях под влиянием вариаций климата. Активизация вегетации в более теплом климате будет способствовать поглощению биогенных элементов и трансформации DOC (Driscoll et al., 2016).
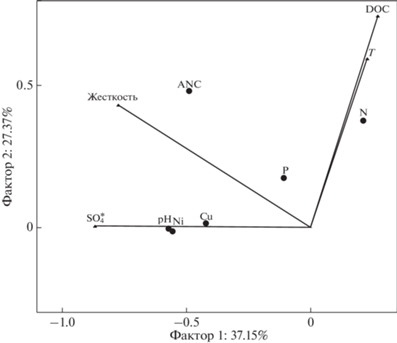
Мы провели многомерный факторный анализ (RDA), основанный на представлении данных в векторной шкале независимых параметров (осей) и точек как зависимых от состояния компонентов (рис. 6). Результаты анализа (RDA) для всех озер указывают на тесную взаимосвязь между повышением температуры и органическим веществом в период исследования. Жесткость воды, которую мы выбрали в качестве независимого параметра, отражает буферную емкость водосбора. Согласно полученным статистическим результатам, поступление Ni, Cu и протонов связано с обогащением системы ${\text{SO}}_{4}^{*}$, а также выявлен доминирующий вклад выщелачивания катионов в формирование жесткости воды. Влияние DOC и температурного фактора (T) на содержание биогенных компонентов (Ptot и Ntot) связано с увеличением биопродукции синхронно с независимым параметром температуры.
Рис. 6.
Осевая диаграмма RDA распределения независимых и зависимых переменных. Оси – независимые параметры: техногенные сульфаты (${\text{SO}}_{4}^{*}$), жесткость, температура (Т), органическое вещество (DOC); точки – зависимые параметры: ANC, Ptot, Ntot, Cu, Ni, рН.
Наши исследования показали, что происходящая трансформация озер происходит синхронно с изменением климата. Из-за отсутствия исходных данных по DOC (природных концентраций) до начала антропогенного закисления, вызванного ${\text{SO}}_{4}^{*}$, неясно, представляют ли повышенные концентрации DOC в последние десятилетия возвращением к естественному состоянию, которое существовало до антропогенного атмосферного осаждения кислот, или биогеохимический статус озер эволюционировал в новое состояние, отвечающее на ряд антропогенных воздействий, таких как кислотные выпадения и изменение климата. В Квебеке D. Houle et al. (2010) предположили, что улучшение состояния 47 озер не может быть связано исключительно со снижением выпадений ${\text{SO}}_{4}^{*}$, изменения климата имеют также важное значение. В работе отмечено, что более высокие годовые температуры воздуха чаще положительно коррелируют с щелочностью и рН озер, что повышает кислотонейтрализующую способность вод. Аналогичные данные влияния температуры на химический состав вод были зарегистрированы для альпийских озер в Европе (Sommaruga-Wӧgrath et al., 1997).
В наших исследованиях гипотезу о преобладающем влиянии климатического фактора подтверждает нарастание биогенных элементов, проявляющемся в повышении содержаний их общих форм при стабильных содержаниях биодоступных форм – нитратов и фосфатов, которые быстро утилизируются в продукционных экосистемных процессах. Зависимости представлены для всего субрегиона за 28-летний период следующим уравнением:
Активизация вегетации в более теплом климате будет способствовать поглощению биогенных элементов и трансформации DOC (Driscoll et al., 2016; Stoddard, 2016). Для региона в целом характерно снижение выбросов и поступлений токсичных металлов в озера (рис. 2, табл. 2). В работе Moiseenko, Sharov (2019) раскрыта эволюция озер Северо-Запада России, включая озеро Имандра на Кольском п-ове в период после прекращения интенсивного загрязнения. Показано, что озеро не способно вернуться к природным условиям, эволюционировало через критическое состояние в новую стадию с устойчивыми биогеохимическими циклами, обеспечивающие его более высокую продуктивность и соответственно – изменения структуры фауны и флоры.
Следствием повышения продуктивности озер может являться интенсивное образование автохтонного органического вещества и стимулирование продукционных процессов в более теплом климате.
Поэтому термин “восстановление” не отражает те процессы, которые развиваются в озерах Кольской Cубарктики. Мы наблюдаем необратимую эволюцию малых озер c разной степенью изменчивости геохимии природных вод, в которую вносят вклад два фактора: снижение потока выпадений сильных кислот и потепление климата.
ЗАКЛЮЧЕНИЕ
Несмотря на широкое использование термина “восстановление”, он не характеризует те процессы, которые развиваются в водах суши Кольского Севера за последние 28 лет. В целом, в ответ на снижение эмиссии металлов и диоксида серы от Кольских медно-никелевых комбинатов произошло снижение содержаний в воде ${\text{SO}}_{4}^{*}$, Cu, Ni и повышение АNС. Однако в ряде озер сохраняются критические значения АNС, особенно в кислотоуязвимых субрегионах, которые свидетельствуют о продолжающемся закислении вод.
Для Кольского Севера, как и для других кислотоуязвимых регионов Европы и Северной Америки доказано увеличение содержания в водах озер DOC, которое нарастало в регионе до 2010 года, тогда как за последние 8 лет этот процесс либо стабилизировался, либо DOC несколько снизился, однако остался выше природных значений. Два фактора могут контролировать указанный процесс: 1) снижение поступления сильных кислот, 2) влияние потепления климата. Наряду с повышением DOC возрастают содержания биогенных веществ (Ntot и Ptot) из года в год синхронно с повышением температуры. Возможно, этот феномен может быть связан не только с поступлением гумусовых кислот с водосбора, но также с образованием автохтонного органического вещества вследствие эвтрофирования вод. Это явление может быть объяснено повышением трофического статуса озер вследствие повышения температуры в регионе. Дополнительное влияние на биогеохимический круговорот оказывает влияние антропогенных факторов со стороны горнорудной индустрии, который приводит к дополнительному поступлению катионов и фосфора вследствие пыления складированных отходов обогащения руд.
Приведенный анализ изменчивости химического состава вод в многолетнем ряду наблюдений под влиянием снижения потока кислот на водосборы и в условиях потепления климата запускают цепь биогеохимических процессов на водосборе и в водоеме. Анализ наших данных, как и научной литературы, показывает эволюцию озер, которая проявляется с разной степенью интенсивности в изменениях: катионно-анионного состава вод, потоков и структуры гумусовых кислот, круговорота содержаний биогенных элементов. Дискуссионным вопросом является – возможно ли восстановление озер к природным показателям? Нам представляется, что биогеохимические циклы и в дальнейшем могут трансформироваться в ту или иную сторону, но возврата к природным показателям не будет в условиях продолжающегося потепления климата и изменяющихся антропогенных нагрузках, как в сторону их увеличения, так и снижения.
Работа выполнена в рамках Госзадания ГЕОХИ РАН № 0137-2019-0008 и при финансовой поддержке гранта РФФИ № 18-05-60012.
Список литературы
Архив погоды: Мурманская область (2019) Справочно-информационный портал “Погода и климат”. (http:// www.pogodaiklimat.ru/archive.php?id=ru®ion=51).
Атлас Мурманской области (Карты) (1971). Ред. коллегия: гл. ред. канд. геогр. наук А.Г. Дуров и др. Москва, 1 атл, 33 с.
Вернадский В.И. (1991) Научная мысль как планетное явление. М.: Наука, 270 с.
Груза Г.В., Ранькова Э.Я. (2012) Наблюдаемые и ожидаемые изменения климата Российской Федерации: температура воздуха. Обнинск: ФГБУ “ВНИИГМИ-МЦД”, 194 с. Доклады о состоянии и об охране окружающей среды Мурманской области в 1990–2018 гг. (2019).
Ежегодник о состоянии загрязнения в городах на территории России за 2018 год (2019), Санкт-Петербург: ФГБУ “ГГО” Росгидромета
Комов В.Т., Лазарева В.И., Степанова И.К. Антропогенное загрязнение малых озер Севера европейской России Биология внутренних вод 3, 5-17.
Моисеенко Т.И., Гашкина Н.А., Дину М.И. (2017) Закисление вод: уязвимость и критические нагрузки. URSS.ЛЕНАНД, 400с.
Пожиленко В.И., Гавриленко Б.В., Жиров Д.В., Жабин С.В. (2002) Геология рудных районов Мурманской области. Апатиты: Изд. Кольского научного центра РАН, 359 с.
Campbell J.L., Rustad L.E., Boyer E.W., Christopher S.F., Driscoll C.T., Fernandez I.J., Groffman P.M., Houle D., Kiekbusch J., Magill A.H., Mitchell M.J., Ollinger S.V. (2009). Consequences of climate change for biogeochemical cycling in forests of northeastern North America Can. J. For. Res. 39, 264-284.
Clair T.A., Dennis I.F., Vet R. (2011) Water chemistry and dissolved organic carbon trends in lakes from Canada’s Atlantic Provinces: no recovery from acidification measured after 25 years of lake monitoring J. Fish. Aquat. Sci. 68, 663-674.
Clark J.M., Bottrell S.H., Evans C.D., Monteith D.T., Bartlett R., Rose R., Newton R.J. and Chapman P.J. (2010) The importance of the relationship between scale and process in understanding long-term DOC dynamics Sci. Total Environ. 408, 2768
Corman J.R., Bertolet B.L., Casson N.J., Sebestyen S.D., Kolka R.K., Stanley E.H. (2018). Nitrogen and phosphorus loads to temperate seepage lakes associated with allochthonous dissolved organic carbon loads Geoph. Res. Lett. 45, 5481-5490.
De Wit H.A., Valinia S., Weyhenmeyer G.A., Futter M.N., Kortelainen P., Austnes K., Hessen D.O., Räike A., Laudon H., Vuorenmaa J. (2016) Current browning of surface waters will be further promoted by wetter climate Environ. Sci. Technol. Lett. 3, 430-5.
Driscoll C.T., Driscoll K.M., Roy K.M., Mitchell M.J. (2003) Chemical response of lakes in the Adirondack Region of New York to declines in acidic deposition Environ. Sci. Technol. 37, 2036-2042 (https://doi.org/).https://doi.org/10.1021/es020924h
Driscoll C.T., Driscoll K.M., Fakhraei H., Civerolo K. (2016) Long-term temporal trends and spatial patterns in the acid-base chemistry of lakes in the Adirondack region of New York in response to decreases in acidic deposition Atmos. Environ. 146, 5-14.
Drozdova O.Yu., Aleshina A.R., Tikhonov V.V., Lapitskiy S.A., Pokrovsky O.S. (2020) Coagulation of Organo-Mineral Colloids and Formation of Low Molecular Weight Organic and Metal Complexes in Boreal Humic River Water Under UV-Irradiation Chemosphere 250, 1-10.
Evans C.D., Monteith D.T., Reynolds B., Clark J.M. (2008) Buffering of recovery from acidification by organic acids Sci. Total Environ. 404, 316-325.
Fakhraei H., Driscoll C.T. (2015) Proton and Aluminum Binding Properties of Organic Acids in Surface Waters of the Northeastern U.S. Environ. Sci. Technol. 49, 2939-2947.
Feuchtmayr H., Moran R., Hatton K., Cannor L., Yeyes T., Harley J., Arkinson, D. (2009) Global warming and eutrophication: effects on water chemistry and autotrophic communities in experimental hypertrophic shallow lake mesocosms. J. Appl. Ecol. 46, 713-723.
Galloway J.N. (1995) Acid deposition: perspectives in time and space Water, Air, Soil Pollut. 85, 15-24.
Garmo O.G, Skjelkvåle B.L., de Wit H.A., Colombo L., Curtis C., Folster J., Hoffmann A. (2014) Trends in surface water chemistry in acidified areas in Europe and North America from 1990 to 2008 Water, Air, Soil Pollut. 225, 1880.
Gavin A.L., Nelson S.J., Klemmer A.J., Fernandez I.J., Strock K.E., McDowell W.H. (2018) Acidification and climate linkages to increased dissolved organic carbon in high elevation lakes Water Resour. Res. 54, 5187-5877.
Henriksen A., Kämäri I., Posh M., Wilander A. (1992) Critical loads of acidity: Nordic surface waters Ambio 21, 356-363.
Henriksen A., Skjelvåle B.L., Mannio J. et al (1998) Northern European Lake Survey, Finland, Norway, Sweden, Denmark, Russian Kola, Russian Karelia, Scotland and Wales Ambio 27, 80-91.
Houle D., Couture S., Gagnon C. (2010) Relative role of decreasing precipitation sulfate and climate on recent lake recovery Global Biogeochem. Cycles 24, 4029.
IPCC (2014). Climate change: fifth assessment report (ar5)https://www.ipcc-wg1.unibe.ch/ Ar5/ar5.html.
ICP-water report: Acidification of surface water in Europe and North America (2007): Trends, biological recovery and heavy metals.
ICP-waters 2010 Waters Programme Manual. Report105/2010, International cooperative programme on assessment and monitoring effects of air pollution on rivers and lakes. https://niva.brage.unit.no/niva-xmlui/handle/11250/ 215220?locale-ttribute=en
Kline K.M., Eshleman K.N., Garlitz J.E., U’Ren S.H. (2016) Long-term response of surface water acid neutralizing capacity in a central Appalachian (USA) river basin to declining acid deposition Atmos. Environ. 146, 195-205.
Kohler S., Buffam I., Jonsson A., Bishop K. (2002) Photochemical and microbial processing of stream and soil water dissolved organic matter in a boreal-forested catchment in northern Sweden Aquat. Sci. 64, 269-281.
Meingast K.M., Kane E., Coble A.A., Marcarelli A.M., Toczydlowski D. (2020) Climate, snowmelt dynamics and atmospheric deposition interact to control dissolved organic carbon export from a northern forest stream over 26 years Environ. Res. Lett. 15, 104 034.
Melillo J.M., Richmond T.C., Yohe G.W. (2014) Climate Change Impacts in the United States: the Third National Climate Assessment U.S. Global Change Research Program, 841 p Moiseenko T.I. (1994) Acidification and Critical Loads in Surface Waters: Kola, Northern Russia. Ambio 23, 418-424.
Moiseenko T.I. (1999) The fate of metals in Arctic surface waters: Method for defining critical levels Sci. Total. Environ. 236, 19-39.
Moiseenko T.I., Dinu M.I., Bazova M.M., de Wit H.A. (2015) Long-Term Changes in the Water Chemistry of Arctic Lakes as a Response to Reduction of Air Pollution: Case Study in the Kola, Russia Water, Air, Soil Pollut. 226, 98.
Moiseenko T.I., Dinu M.I., Gashkina N.A., Jones V., Khoroshavin V.Y., Kremleva T.A. (2018) Present status of water chemistry and acidification under nonpoint sources of pollution across European Russia and West Siberia. Environ. Res. Lett. 13, 105007.
Moiseenko T.I., Gashkina N.A., Dinu M.I., Kremleva T.A., Khoroshavin V.Yu. (2020) Water Chemistry of Arctic Lakes under Airborne Contamination of Watersheds. Water 12, 1659.
Moiseenko T.I., Sharov A. (2019) Large Russian lakes Ladoga, Onega, and Imandra under strong pollution and in the period of revitalization: a review Geosciences 9, 492.
Monteith D.T., Stoddard J.L., Evans C.D., de Wit H.A., Forsius M., Hogasen T., Wilander A., Skjelkvale B.L., Jeffries D.S., Vuorenmaa J., Keller B., Kopacek J. and Vesely J. (2007) Dissolved organic carbon trends resulting from changes in atmospheric deposition chemistry Nature 450, 537-539.
Rogora M., Colombo L., Marchetto A., Mosello R., Steingruber S. (2016) Temporal and spatial patterns in the chemistry of wet deposition in Southern Alps Atmos. Environ. 146, 44-54.
San Clements M.D., Fernandez I.J., Lee R.H., Roberti J.A., Adams M.B., Rue G.A., McKnight D.M. (2018) Long-Term Experimental Acidification Drives Watershed Scale Shift in Dissolved Organic Matter Composition and Flux Environ. Sci. Technol. 52, 2649-2657.
Skjelkvale B.L., Stoddard J.L., Andersen T. (2001) Trends in surface water acidification in Europe and North America (1989-1998) Water, Air, Soil Pollut. 130, 787-792.
Skjelkvale B.L., Stoddard J.L., Jeffries D.S., Torseth K., Hogasen T.J. et al (2005) Regional scale evidence for improvements in surface water chemistry 1990-2001 Environ. Pollut. 137, 165-176.
Sommaruga-Wӧgrath S., Koinig K.A., Schmidt R., Sommaruga R., Tessadri R., Psenner R. (1997) Temperature effects on the acidity of remote alpine lakes Nature 387, 64-67.
Standart methods for the examination of water and wasterwater. (1992) Wash. (D.C.): Amer, Publ, Health Assoc.
Stoddard J.L., Jeffries D.S., Lukewille A., Clair T.A., Dillon P.J., Driscoll C.T., Forsius M. (1999) Regional trends in aquatic recovery from acidification in North America and Europe Nature 401, 575-578.
Stoddard J.L., Van Sickle J., Herlihy A.T., Brahney J., Paulsen S., Peck D.V. et al. (2016) Continental-scale increase in lake and stream phosphorus: Are oligotrophic systems disappearing in the United States? Environ. Sci. Technol. 50, 3409-3415.
Strock K.E, Nelson S.J., Kahl J.S., Saros J.E., McDowell W.H. (2014) Decadal trends reveal recent acceleration in the rate of recovery from acidification in the northeastern U.S. Environ. Sci. Technol. 48, 4681-4689.
Strock K.E., Theodore N., Gawley W.G., Ellsworth A.C., Saros J.E. (2017) Increasing dissolved organic carbon concentrations in northern boreal lakes: implications for lake water transparency and thermal structure J. Geophys. Res. Biogeosci. 122, 1022-35
Ward C.P, Cory R.M. (2016) Complete and partial photo-oxidation of dissolved organic matter draining permafrost soils Environ. Sci. Technol. 50, 3545-3553.
Watmough S.A., Eimers C., Baker S. (2016) Impediments to recovery from acid deposition Atmos. Environ. 146, 15-27.
Дополнительные материалы отсутствуют.