Химическая физика, 2022, T. 41, № 10, стр. 28-37
Распределение концентраций положительных и отрицательных ионов в тропосфере
Ю. Чэнсюнь 1, Л. Чжицзянь 1, В. Л. Бычков 2, Д. В. Бычков 2, М. Г. Голубков 3, *, Т. А. Маслов 2, И. Д. Родионов 3, И. П. Родионова 3, И. Г. Степанов 3, С. Я. Уманский 3, Г. В. Голубков 3, 4
1 Харбинский политехнический университет
Харбин, Китай
2 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
3 Федеральный исследовательский центр химической физики им. Н.Н. Семёнова Российской академии наук
Москва, Россия
4 Национальный исследовательский центр “Курчатовский институт”
Москва, Россия
* E-mail: golubkov@chph.ras.ru
Поступила в редакцию 19.05.2022
После доработки 09.06.2022
Принята к публикации 20.06.2022
- EDN: BNBMLA
- DOI: 10.31857/S0207401X22100041
Аннотация
Рассмотрен процесс формирования сложно заряженных грозовых облаков, обладающих слоями положительных и отрицательных ионов и крупных ионных кластеров, появляющихся в тропосфере под действием космических лучей. Для расчета концентраций ионов разработана кинетическая модель, включающая 34 компонента и 102 реакции. Расчет проведен с использованием программного пакета KINET. Показано, что на высотах от 5 до 35 км ионизация воздуха под действием космических лучей приводит к образованию слабоионизованной плазмы, состоящей в основном из ионов ${\text{O}}_{2}^{ - },$ ${\text{O}}_{2}^{ + }$ и ${\text{O}}_{4}^{ + }.$ В условиях минимальной магнитной жесткости максимумы концентраций ионов ${\text{O}}_{2}^{ - }$ и ${\text{O}}_{4}^{ + }$ наблюдаются на высотах от 15 до 20 км. Установлено, что в приземном слое от 0 до 5 км ионизация воздуха, вызываемая γ-излучением, значительно слабее ионизации космическими лучами.
1. ВВЕДЕНИЕ
Информация о распределении концентраций ионов в нижней атмосфере Земли на высотах до 40 км имеет большое теоретическое и прикладное значение, поскольку положительные и отрицательные ионы определяют электропроводность нижней атмосферы и существенно влияют на формирование заряда тропосферы и облаков [1]. Тропосфера является нижним слоем атмосферы, высота которого составляет 8–10 км в полярных областях, 10–12 км в умеренных широтах и 16–18 км на экваторе [2]. Традиционно сведения о процессах, приводящих к накоплению и изменению сорта ионов, представляют значительный интерес для исследователей, использующих различные типы разрядов в плазмохимических технологиях [3]. При оценках воздействия атмосферы на приборы и распространение радиоволн возникают значительные трудности, так как свойства атмосферного воздуха постоянно изменяются [4].
Нижняя атмосфера Земли характеризуется наличием вертикальных и горизонтальных неоднородностей [5, 6], которые могут быть причиной сбоев в работе глобальных навигационных спутниковых систем. Вертикальные неоднородности в тропосфере формируются, как правило, вследствие резкого изменения давления и температуры воздуха по высоте [7, 8]. Горизонтальные неоднородности возникают вследствие процессов, протекающих вблизи поверхности Земли [9, 10], где существуют водяной пар, туманы и облака, атмосферные осадки и т.д. Такие неоднородности образуются во время метеорологических штормов и других атмосферных явлений вследствие неравномерного нагрева атмосферного воздуха или распределения атмосферного давления [11, 12]. Характерным примером здесь являются слоистые облака, которые, так же как и туман, создают однородный слой. Они образуются при контакте холодного и теплого воздуха, когда последний медленно поднимается вверх вдоль холодного [13]. Совокупность результирующих горизонтальных и вертикальных движений носит название общей циркуляции атмосферы [14].
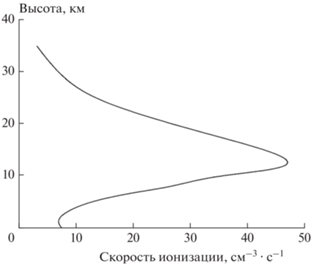
Отметим, что механизм влияния электрических полей и быстрых частиц на процессы формирования ионов в нижней атмосфере различен на разных высотах. В нижних слоях атмосферы основную роль при образовании однозарядных ионов играет естественное радиоактивное излучение от поверхности почвы, т.е. γ-излучение [15]. Однако этот процесс активно протекает на высоте до 500 м над Землей, где образованные заряженные частицы воздействуют на распределение слабого электрического поля. В диапазоне высот от 0 м до 6 км электрическое поле Земли убывает на порядок от величины 130 В/м до 10–20 В/м, т.е. слабо влияет на столкновительные процессы электрон-ионной рекомбинации и прилипания электронов к молекулам кислорода. На высотах от 5 до 25 км важнейшим процессом является ионизация воздуха под действием космических лучей [16–18]. Сказанное наглядно демонстрируется на рис. 1, где представлена альтитудная зависимость полной скорости ионизации атмосферы, Q [15]. Видно, что скорость Q максимальна на высоте 12 км. Кроме того, небольшое увеличение Q наблюдается вблизи поверхности Земли, что обусловлено γ‑излучением от поверхности почвы.
Магнитное поле Земли оказывает существенное влияние на проникновение в атмосферу заряженных частиц или частиц, обладающих магнитным моментом [19–21]. Оно имеет вид магнитного диполя, что препятствует свободному прохождению заряженных низкоэнергетических частиц в атмосферу Земли (за исключением областей, расположенных вблизи магнитных полюсов). Земля действует своим магнитным полем на нуклоны подобно масс-спектрометру. Мерой воздействия магнитного поля является магнитная жесткость $\xi ,$ которая пропорциональна магнитному моменту частицы [1]:
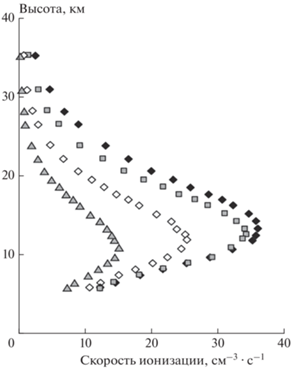
где q и p – заряд и проекция импульса частицы на плоскость, перпендикулярную направлению вектора магнитной индукции B; R – ларморовский радиус; c – скорость света в вакууме.На рис. 2 приведены альтитудные зависимости скорости ионизации Q космическими лучами, измеренные в различных точках земного шара, т.е. при различных значениях магнитной жесткости [1]. Видно, что зависимость Q от высоты имеет колоколообразную форму с максимумом на расстоянии 10–13 км от поверхности Земли. Кроме того, из данных рис. 2 следует, что с ростом магнитной жесткости ξ максимальное значение Q падает, а положение максимума смещается в сторону меньших высот.
Рис. 2.
Альтитудные зависимости скорости ионизации воздуха космическими лучами при различных значениях магнитной жесткости ξ: черные ромбы – ξ = 0–0.6 · 109 Тл · м, серые квадраты – ξ = 2.4 · 109–2.5 · 109 Тл · м, белые ромбы – ξ = 6 · 109 Тл · м, серые треугольники – ξ = 13.5 · 109 Тл · м.
Цель данного исследования заключалась в определении альтитудной зависимости концентрации ионов, образующихся в тропосфере в спокойной геомагнитной обстановке под действием космических лучей и радиоактивного γ-излучения от поверхности почвы. Эти данные необходимы для управления процессом формирования слоистых грозовых облаков и искусственного стимулирования выпадения осадков.
Статья организована следующим образом. В разд. 2 обсуждаются процесс формирования и структура слоистых облаков в тропосфере. Приведена общая схема действия ионов, появляющихся в результате торможения космических лучей в тропосфере. Раздел 3 посвящен анализу элементарных процессов, протекающих в тропосфере. Выделены доминирующие процессы с участием молекул ${{{\text{O}}}_{{\text{2}}}}$ и ${{{\text{N}}}_{{\text{2}}}}$ и их молекулярных ионов. В разд. 4 подробно обсуждаются особенности системы уравнений баланса для электронов, положительно и отрицательно заряженных молекулярных ионов. Раздел 5 посвящен краткому описанию кинетической схемы, которая использовалась для расчета концентраций ионов. Результаты и их обсуждение приведены в разд. 6. Здесь представлены временн ы́е зависимости концентраций ионов в тропосфере и зависимости распределения концентраций основных тропосферных ионов по высоте, рассчитанные при различных значениях магнитной жесткости, что отвечает разным точкам географической локации. Завершает статью разд. 7, где обсуждается возможность практического применения полученных результатов.
2. ОБРАЗОВАНИЕ И СТРУКТУРА СЛОИСТЫХ ОБЛАКОВ В ТРОПОСФЕРЕ
Ионы, появляющиеся в тропосфере под действием космических лучей, приводят к формированию сложно заряженных грозовых облаков, обладающих слоями положительных и отрицательных ионов и крупных ионных кластеров. Возникающие при этом электрические разряды (молнии) могут отвечать за многие неблагоприятные последствия. Причем, помимо экологического воздействия, при грозах создаются униполярно заряженные ионами облака, что может приводить к образованию сильных электрических полей в нижней атмосфере. При возникновении таких полей происходит кардинальное изменение электропроводности ионосферы. Последнее значительно влияет на распространение радиосигналов [22]. Кроме того, появляются различные ионосферные плазменные объекты (спрайты), которые отвечают за изменение химико-физических свойств атмосферы.
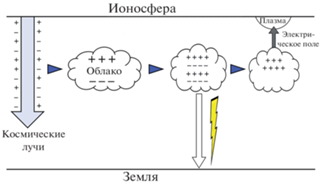
На рис. 3 приведена общая схема воздействия ионов, появляющихся в результате торможения космических лучей в тропосфере, на электрические поля в ионосфере. Вначале происходит образование ионов в тропосфере под воздействием космических лучей, что приводит к заряду обычных облаков и образованию заряженных кластеров [1]. При этом тяжелые отрицательно заряженные кластеры опускаются в нижнюю часть облака. Далее происходит разделение зарядов и облако становится подобным конденсатору (грозовым) [13]. Во время грозы отрицательный заряд переносится молнией вниз, на землю. В результате облако остается заряженным только положительными зарядами [23]. Их концентрация становится ∼${{10}^{3}}$ см–3, поэтому происходит формирование электрического поля около облака. В связи с тем, что плотность нейтральных частиц экспоненциально падает с увеличением высоты, в ионосфере создаются условия, когда в этом поле электроны фона, испытывая мало соударений, ускоряются до энергий, при которых происходит ионизация молекул. В результате ионизации во внешнем электрическом поле образуются ионизованные области в ионосфере, которые перемещаются вместе с облаками и влияют на условия распространения радиоволн в нижней ионосфере [22]. В работе [23] было показано, что потоки ионов к поверхности облаков могут также изменять свойства последних и создавать центры конденсации, что позволяет искусственно стимулировать выпадение осадков. Другими словами, появляется дополнительный метод борьбы с грозовыми облаками, который отличается от способа ликвидации облаков с использованием дорогостоящих химических препаратов.
3. ЭЛЕМЕНТАРНЫЕ ПРОЦЕССЫ В ТРОПОСФЕРЕ
Анализ элементарных процессов, протекающих в тропосфере, показывает, что после рождения электронов и ионов эффективно активизируются процессы с участием молекул ${{{\text{O}}}_{{\text{2}}}}$ и ${{{\text{N}}}_{{\text{2}}}}$ и их молекулярных ионов. Доминирующими здесь являются следующие процессы [24]:
1) атмосферная фоновая ионизация молекул ${{{\text{O}}}_{{\text{2}}}}$ и ${{{\text{N}}}_{{\text{2}}}}$ быстрыми электронами:
(2)
${\text{e}}{\kern 1pt} {\text{'}} + {{{\text{O}}}_{2}} \to {\text{O}}_{2}^{ + } + {\text{e}}{\kern 1pt} '\, + {\text{e}},$(3)
${\text{e}}{\kern 1pt} '\, + {{{\text{N}}}_{2}} \to {\text{N}}_{2}^{ + } + {\text{e}}{\kern 1pt} {\text{'}} + {\text{e}};$2) прямая ионизация молекул ${{{\text{O}}}_{{\text{2}}}}$ и ${{{\text{N}}}_{{\text{2}}}}$ медленными электронами:
которая сопровождается перезарядкой ионов ${\text{N}}_{{\text{2}}}^{{\text{ + }}}$ при последующем столкновении с нейтральными молекулами кислорода, т.е.3) диссоциативное прилипание электронов к молекулам ${{{\text{O}}}_{{\text{2}}}}$ с образованием отрицательных ионов ${{{\text{O}}}^{ - }}$ и атомов O кислорода:
4) трехчастичное прилипание медленных электронов к молекулам O2:
(8)
${\text{e}} + {{{\text{O}}}_{2}} + {{{\text{O}}}_{2}} \to {\text{O}}_{2}^{ - } + {{{\text{O}}}_{2}};$5) образование ионов ${\text{O}}_{2}^{ - }$ и ${\text{O}}_{3}^{ - }$ в реакциях
(10)
${{{\text{O}}}^{ - }} + {{{\text{O}}}_{2}} + {{{\text{O}}}_{2}} \to {\text{O}}_{3}^{ - } + {{{\text{O}}}_{2}};$6) последующий отрыв электронов от ионов ${{{\text{O}}}^{ - }},$ ${\text{O}}_{2}^{ - }$ и ${\text{O}}_{3}^{ - }$ при взаимодействии с молекулами азота, кислорода и частицами M нейтральной среды:
(14)
${\text{O}}_{3}^{ - }{\kern 1pt} + {{{\text{O}}}_{2}} \to {\text{e}} + {{{\text{O}}}_{3}} + {{{\text{O}}}_{2}}.$При этом баланс положительно заряженных частиц на начальной стадии существования фоновой плазмы определяется реакциями электрон-ионной и ион-ионной рекомбинации, т.е.
(19)
${\text{O}}_{2}^{ - } + {\text{O}}_{2}^{ + } + {\text{M}} \to {{{\text{О}}}_{2}} + {{{\text{O}}}_{2}} + {\text{M}},$(20)
${\text{O}}_{2}^{ - } + {\text{N}}_{2}^{ + } + {\text{M}} \to {{{\text{О}}}_{2}} + {{{\text{N}}}_{2}} + {\text{M}}.$Нас не интересует здесь сорт положительных ионов, поскольку процессы ионизации и перезарядки далее приводят к образованию ионов ${\text{O}}_{2}^{ + }.$ Как следует из детального расчета, проведенного в [24], этот сорт ионов остается неизменным на небольших временах, меньших по сравнению с характерным временем образования ионов ${\text{N}}{{{\text{O}}}^{{\text{ + }}}}{\text{.}}$
Реакции (9)–(12) и (14) протекают эффективно, когда активным является диссоциативное прилипание электронов к молекулам кислорода с образованием ${{{\text{O}}}^{ - }}$ (см. (7)), т.е. на стадии, близкой к лавинной ионизации. В этом случае именно реакция (13) является одним из источников электронов на фоновой стадии, так как температура электронов близка к комнатной.
4. ОСНОВНЫЕ УРАВНЕНИЯ ТЕОРИИ
Система уравнений баланса для электронов, положительно и отрицательно заряженных молекулярных ионов кислорода в процессах (2)–(5), (8), (13), (15)–(20) имеет вид
(21)
$\begin{gathered} \frac{{d{{n}_{e}}}}{{dt}} = ({{k}_{2}} + {{k}_{4}}){{n}_{e}}{{n}_{{{{{\text{O}}}_{{\text{2}}}}}}} + ({{k}_{3}} + {{k}_{5}}){{n}_{e}}{{n}_{{{{{\text{N}}}_{{\text{2}}}}}}} - {{k}_{8}}{{n}_{e}}n_{{{{{\text{O}}}_{{\text{2}}}}}}^{2} + \\ + \,\,{{k}_{{13}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{\kern 1pt} {{n}_{{\text{M}}}} - {{k}_{{15}}}{{n}_{e}}{{n}_{{{\text{O}}{\kern 1pt} _{{\text{2}}}^{{\text{ + }}}}}} - {{k}_{{16}}}{{n}_{e}}{{n}_{{{\text{N}}_{{\text{2}}}^{{\text{ + }}}}}}, \\ \end{gathered} $(22)
$\begin{gathered} \frac{{d{{n}_{{{\text{O}}_{{\text{2}}}^{ - }}}}}}{{dt}} = {{k}_{8}}{{n}_{e}}n_{{{{{\text{O}}}_{2}}}}^{2} - {{k}_{{13}}}{{n}_{{{\text{O}}{\kern 1pt} _{2}^{ - }}}}{\kern 1pt} {{n}_{{\text{M}}}} - {{k}_{{17}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{O}}_{2}^{ + }}}} - {{k}_{{18}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{N}}_{2}^{ + }}}} - \\ - \,\,{{k}_{{19}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{O}}_{2}^{ + }}}}{{n}_{{\text{M}}}} - {{k}_{{20}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{N}}_{2}^{ + }}}}{{n}_{{\text{M}}}}, \\ \end{gathered} $(23)
$\begin{gathered} \frac{{d{{n}_{{{\text{O}}_{2}^{ + }}}}}}{{dt}} = ({{k}_{2}} + {{k}_{4}}){{n}_{e}}{{n}_{{{{{\text{O}}}_{2}}}}} - {{k}_{{15}}}{{n}_{e}}{{n}_{{{\text{O}}_{2}^{ + }}}} - \\ - \,\,{{k}_{{17}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{O}}_{2}^{ + }}}} - {{k}_{{19}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{O}}_{2}^{ + }}}}{{n}_{{\text{M}}}}, \\ \end{gathered} $(24)
$\begin{gathered} \frac{{d{{n}_{{{\text{N}}_{2}^{ + }}}}}}{{dt}} = ({{k}_{3}} + {{k}_{5}}){{n}_{e}}{{n}_{{{{{\text{N}}}_{2}}}}} - {{k}_{{16}}}{{n}_{e}}{{n}_{{{\text{N}}_{2}^{ + }}}} - \\ - \,\,{{k}_{{18}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{N}}_{2}^{ + }}}} - {{k}_{{20}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{N}}_{2}^{ + }}}}{{n}_{{\text{M}}}}. \\ \end{gathered} $Заметим, что, согласно данным из работы [23], в тропосфере выполняется неравенство
где коэффициенты ион-ионной, ${{\alpha }_{{ii}}},$ и электрон-ионной, ${{\alpha }_{{ei}}},$ рекомбинации определяются как(26)
$\begin{gathered} {{\alpha }_{{ii}}} = \left( {{{k}_{{17}}}{{n}_{{{\text{O}}_{2}^{ + }}}} + {{k}_{{18}}}{{n}_{{{\text{N}}_{{\text{2}}}^{{\text{ + }}}}}} + {{k}_{{19}}}{{n}_{{{\text{O}}_{{\text{2}}}^{{\text{ + }}}}}}{{n}_{{\text{M}}}}} \right. + \\ {{\left. { + \,\,{{k}_{{20}}}{{n}_{{{\text{N}}_{{\text{2}}}^{{\text{ + }}}}}}{{n}_{{\text{M}}}}} \right)} \mathord{\left/ {\vphantom {{\left. { + \,\,{{k}_{{20}}}{{n}_{{{\text{N}}_{{\text{2}}}^{{\text{ + }}}}}}{{n}_{{\text{M}}}}} \right)} {\left( {{{n}_{{{\text{O}}_{{\text{2}}}^{{\text{ + }}}}}} + {{n}_{{{\text{N}}_{{\text{2}}}^{{\text{ + }}}}}}} \right)}}} \right. \kern-0em} {\left( {{{n}_{{{\text{O}}_{{\text{2}}}^{{\text{ + }}}}}} + {{n}_{{{\text{N}}_{{\text{2}}}^{{\text{ + }}}}}}} \right)}}, \\ \end{gathered} $(27)
${{\alpha }_{{ei}}} = {{\left( {{{k}_{{15}}}{{n}_{{{\text{O}}_{{\text{2}}}^{{\text{ + }}}}}} + {{k}_{{16}}}{{n}_{{{\text{N}}_{{\text{2}}}^{{\text{ + }}}}}}} \right)} \mathord{\left/ {\vphantom {{\left( {{{k}_{{15}}}{{n}_{{{\text{O}}_{{\text{2}}}^{{\text{ + }}}}}} + {{k}_{{16}}}{{n}_{{{\text{N}}_{{\text{2}}}^{{\text{ + }}}}}}} \right)} {\left( {{{n}_{{{\text{O}}_{{\text{2}}}^{{\text{ + }}}}}} + {{n}_{{{\text{N}}_{{\text{2}}}^{{\text{ + }}}}}}} \right)}}} \right. \kern-0em} {\left( {{{n}_{{{\text{O}}_{{\text{2}}}^{{\text{ + }}}}}} + {{n}_{{{\text{N}}_{{\text{2}}}^{{\text{ + }}}}}}} \right)}}.$Будем считать, что на начальной стадии процесса концентрации положительных молекулярных ионов ${\text{X}}_{2}^{ + }$ и отрицательных ионов кислорода ${\text{O}}_{2}^{ - }$ близки, т.е. ${{n}_{{{\text{X}}_{2}^{ + }}}} \approx {{n}_{{{\text{O}}_{2}^{ - }}}}.$ При нормальном атмосферном давлении, когда прилипание электронов происходит достаточно быстро по сравнению с электрон-ионной рекомбинацией, скорость реакции (8) много больше скорости реакций (15) и (16), т.е. частота процесса (8)
(28)
${{\nu }_{{t{\kern 1pt} r}}} = {{k}_{8}}n_{{{{{\text{O}}}_{2}}}}^{2} \gg {{\alpha }_{{ei}}}{{n}_{{{\text{O}}_{2}^{ + }}}}.$В этом случае реакции перезарядки (17), (18) протекают по парному, а (19), (20) – по тройному механизмам и коэффициент ион-ионной рекомбинации можно представить в виде [25]:
где(30)
$\begin{gathered} \alpha _{{ii}}^{{(2)}} = 2 \cdot {{10}^{{ - 7}}}{{\left( {\frac{{300}}{{T(h)}}} \right)}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}\,\,\frac{{{\text{с}}{{{\text{м}}}^{3}}}}{{\text{с}}}; \\ \alpha _{{ii}}^{{(3)}} = 2 \cdot {{10}^{{ - 25}}}{{\left( {\frac{{300}}{{T(h)}}} \right)}^{{5{\text{/}}2}}}\,\,\frac{{{\text{с}}{{{\text{м}}}^{6}}}}{{\text{с}}}, \\ \end{gathered} $В стационарных фоновых условиях (концентрации положительных и отрицательных ионов не меняются) для скорости ионизации Q нейтральных молекул космическими лучами выполняется соотношение
(31)
$\begin{gathered} Q = ({{k}_{2}} + {{k}_{4}}){{n}_{e}}{{n}_{{{{{\text{O}}}_{{\text{2}}}}}}} + ({{k}_{3}} + {{k}_{5}}){{n}_{e}}{{n}_{{{{{\text{N}}}_{{\text{2}}}}}}} \approx {{k}_{{17}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{O}}_{2}^{ + }}}} + \\ + \,\,{{k}_{{18}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{N}}_{2}^{ + }}}} + {{k}_{{19}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{O}}_{2}^{ + }}}}{{n}_{{\text{M}}}} + {{k}_{{20}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{N}}_{2}^{ + }}}}{{n}_{{\text{M}}}} \approx {{\alpha }_{{ii}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{{\text{X}}_{2}^{ + }}}}. \\ \end{gathered} $С учетом квазинейтральности плазмы тропосферы, когда ${{n}_{{{\text{X}}_{2}^{ + }}}} \approx {{n}_{{{\text{O}}_{2}^{ - }}}},$ для концентрации ионов ${\text{O}}_{2}^{ - }$ имеем
(32)
${{n}_{{{\text{O}}_{2}^{ - }}}} = {{\left( {\frac{Q}{{{{\alpha }_{{ii}}}}}} \right)}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}.$Если считать, что давление вблизи поверхности Земли является атмосферным, то величина $Q = 4.0\,\,{\text{с}}{{{\text{м}}}^{{ - 3}}} \cdot {{{\text{с}}}^{{ - 1}}}$ [23], а коэффициент ион-ионной рекомбинации ${{\alpha }_{{i{\kern 1pt} i}}} \approx 2.0 \cdot {{10}^{{ - 6}}}$ см3/с [25]. Используя далее выражение (32), для концентрации отрицательных молекулярных ионов кислорода получим величину ${{n}_{{{\text{O}}_{2}^{ - }}}} \approx 1.4 \cdot {{10}^{3}}$ см–3, которая хорошо согласуется с экспериментальными данными [26] и результатами расчетов [27, 28].
В стационарном случае концентрация электронов определяется при подстановке в уравнение (21) величины концентрации отрицательных молекулярных ионов кислорода, полученной по формуле (32), т.е.
(33)
${{n}_{e}} = \frac{{Q + {{k}_{{13}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{\text{M}}}}}}{{{{k}_{8}}n_{{{{{\text{O}}}_{2}}}}^{2}}} = \frac{{Q + {{k}_{{13}}}{{n}_{{{\text{O}}_{2}^{ - }}}}{{n}_{{\text{M}}}}}}{{{{\nu }_{{tr}}}}}.$(34)
${{k}_{{13}}} = 2.7 \cdot {{10}^{{ - 10}}}{{\left( {\frac{T}{{300}}} \right)}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}\exp \left( { - \frac{{5590}}{T}} \right),$5. МОДЕЛИРОВАНИЕ ПРОЦЕССОВ ИОНИЗАЦИИ
Для расчета концентраций ионов была использована кинетическая схема, включающая 34 компонента и 102 реакции. В табл. 1 представлены основные реакции, протекающие в тропосфере, и даны температурные зависимости соответствующих констант скорости процессов, взятые из работы [29]. Расчет проводился с использованием программного пакета KINET [24], в котором реализован алгоритм решения кинетических уравнений для компонентов ионизованной плазмы с учетом альтитудной зависимости их концентраций и температуры.
Таблица 1.
Температурные зависимости констант скорости k учитываемых реакций
| Реакция | Константа скорости |
|---|---|
| ${\text{O}}_{2}^{ - }$ + ${\text{O}}_{4}^{ + }$ + M → O2 + O2 + O2 + M | 2 ∙ 10–25(300/Т)2.5, см6/с |
| ${\text{O}}_{2}^{ + }$ + O2 + O2 → ${\text{O}}_{4}^{ + }$ + O2 | 2.4 ∙ 10–30(300/T)3.2, см6/с |
| O+ + N2 → NO+ + N | 3.0 ∙ 10–12exp(–0.00311T), см3/с |
| e– + O2 + O2 → ${\text{O}}_{2}^{ - }$ + O2 | 1.4 ∙ 10–29(300/T)exp(–600/T), см6/с |
| e + ${\text{O}}_{2}^{ + }$ → O + O | 2 ∙ 10–7(300/T), см3/с |
| e + NO+ → N + O | 4 ∙ 10–7(300/T)1.5, см3/с |
| e + N${\text{O}}_{2}^{ + }$ → NO + O | 2 ∙ 10–7(300/T)0.5, см3/с |
| O– + NO+ → NO + O | 5 ∙ 10–7(300/T), см3/с |
| O– + NO+ + M → NO + O + M | 1 ∙ 10–25(300/T)2.5, см6/с |
| ${\text{O}}_{2}^{ - }$ + ${\text{O}}_{2}^{ + }$ → O2 + O2 | 3.2 ∙ 10–7(300/T), см3/с |
| ${\text{O}}_{2}^{ - }$ + NO+ → NO + O2 | 3 ∙ 10–7(300/T), см3/с |
| ${\text{O}}_{2}^{ - }$ + ${\text{O}}_{2}^{ + }$ + M → O2 + O2 + M | 3 ∙ 10–25(300/T)2.5, см6/с |
| ${\text{O}}_{2}^{ - }$ + ${\text{O}}_{2}^{ + }$ → O2 + O + O | 1 ∙ 10–7(300/T), см3/с |
| ${\text{O}}_{3}^{ - }$ + NO+ → O3 + NO | 3 ∙ 10–7(300/T), см3/с |
| ${\text{O}}_{3}^{ - }$ + NO+ + M → O3 + NO + M | 1 ∙ 10–25(300/T)2.5, см6/с |
| ${\text{O}}_{3}^{ - }$ + ${\text{O}}_{2}^{ + }$ + M → O3 + O2 + M | 1 ∙ 10–25(300/T)2.5, см6/с |
| ${\text{O}}_{3}^{ - }$ + ${\text{O}}_{2}^{ + }$ + M → O3 + O + O + M | 1 ∙ 10–25(300/T)2.5, см6/с |
| O– + O+ → O + O | 9.3 ∙ 10–8(300/T), см3/с |
Альтитудные зависимости концентраций молекулярных ионов на высотах от 5 до 35 км определялись в результате решения системы уравнений баланса, в которой использовались приведенные в табл. 2 значения скорости ионизации воздуха космическими лучами [1] при различных значениях магнитной жесткости. Для аналогичного расчета концентраций ионов в приземном слое (от 0 до 5 км), где основную роль играет ионизация, вызванная γ-излучением, использовались физические параметры тропосферы в различных точках географической локации (см. табл. 3). Отметим, что в использованной модели практически не учитываются процессы с участием положительных молекулярных ионов азота, поскольку достаточно быстро протекает реакция перезарядки (6). При этом на уровне Земли характерное время перезарядки составляет 3 ∙ 10–10 с.
Таблица 2.
Альтитудная зависимость скорости ионизации Q (см–3 ∙ с–1) воздуха космическими лучами при различных значениях магнитной жесткости ξ (Тл · м)
| h, км | ξ1 = 0.6 · 109 | ξ2 = 2.5 · 109 | ξ3 = 6 · 109 | ξ4 = 13.5 · 109 |
|---|---|---|---|---|
| 5 | 12.5 | 12.5 | 10.0 | 6.0 |
| 10 | 32.5 | 30.0 | 22.5 | 15.0 |
| 15 | 35.0 | 33.0 | 22.5 | 10.0 |
| 20 | 22.0 | 20.0 | 10.0 | 5.0 |
| 25 | 12.5 | 7.5 | 5.0 | 2.5 |
| 30 | 8.0 | 5.0 | 2.0 | 1.5 |
| 35 | 4.0 | 3.0 | 1.0 | 1.0 |
Таблица 3.
Физические параметры тропосферы в различных точках географической локации
| Локация | Высота над уровнем моря, км | Q, см–3 · c–1 | Концентрация нейтральных частиц, 1019 cм–3 | Средняя температура, °С | |
|---|---|---|---|---|---|
| Восточно-Китайское море, бухты вблизи Японии | 0 | 1.9 | [30] | 2.70 | 19.5 |
| Мауна-Лоа, Гавайские острова | 4.200 | 5.0 | [31] | 1.63 | 20.0 |
| Слуцк, Белоруссия | 0.150 | 8.5 | [32] | 2.60 | 6.8 |
| Воейково, Россия | 0.072 | 15.0 | [33] | 2.70 | 7.2 |
| Нагойя, Япония | 0.017 | 14.0 | [34] | 2.70 | 19.5 |
| Норикура, Япония | 2.300 | 15.0 | [34] | 2.00 | 19.5 |
| Вашингтон, США | 0.011 | 16.0 | [34] | 2.70 | 13.7 |
| Хуанкайо, Перу | 3.300 | 40.0 | [32, 35] | 1.80 | 12.0 |
6. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Все расчетные данные, представленные в данном разделе, получены с помощью программного пакета KINET и использованием кинетической схемы, описанной в разд. 5. На рис. 4 представлены временн ы́е зависимости концентраций основных ионов, ${\text{O}}_{2}^{ - },$ ${\text{O}}_{2}^{ + }$ и ${\text{O}}_{4}^{ + }$ в тропосфере, соответствующие величине магнитной жесткости ξ = = 0.6 · 109 Тл · м. Выбор указанных ионов и соответствующих кривых обусловлен тем, что концентрации других ионов в тропосфере пренебрежимо малы. Их суммарный вклад в общую концентрацию заряженных частиц не превышает 1%. Из рис. 4 видно, что безусловным лидером является ион ${\text{O}}_{2}^{ - },$ что также соответствует расчетам, проведенным в работах [27, 28]. Отличие наших данных от данных, полученных в работе [27], заключается в том, что последние отвечают уровню аварийного выброса из вентиляционной трубы атомной электростанции, т.е. соответствуют величине Q ∼ 108 см–3 · с–1. Расчеты же в [28] проводились для нормальных условий, но для высот нижней ионосферы (90–110 км). Поэтому сравнивать здесь абсолютные величины концентрации ${{n}_{{{\text{O}}_{2}^{ - }}}}$ смысла не имеет. Отметим также, что на временах порядка 10–7–10–6 с происходит интенсивная конверсия иона ${\text{O}}_{2}^{ + }$ в ион ${\text{O}}_{4}^{ + }.$ Вследствие этого концентрация иона ${\text{O}}_{2}^{ + },$ которая на временах до 3 · 10–7 с растет наиболее быстро, в итоге оказывается меньше концентраций ионов ${\text{O}}_{4}^{ + }$ и ${\text{O}}_{2}^{ - }.$ Это соотношение будет справедливо на высотах до 30 км.
Рис. 4.
Временнáя зависимость концентраций ионов в тропосфере: ${{n}_{{{\text{O}}_{4}^{ + }}}}$ – сплошная линия, ${{n}_{{{\text{O}}_{2}^{ + }}}}$ – штриховая, ${{n}_{{{\text{O}}_{2}^{ - }}}}$ – штрих-пунктирная. Величина магнитной жесткости ξ = 0.6 · 109 Тл · м.

Альтитудные зависимости концентраций ионов ${\text{O}}_{2}^{ - },$ ${\text{O}}_{2}^{ + }$ и ${\text{O}}_{4}^{ + }$ приведены в табл. 4. Расчеты проведены для величины магнитной жесткости ξ = = 0.6 · 109 Тл · м, что соответствует полярным областям магнитного поля Земли. Данные отвечают моменту времени $t = 300$ с, когда концентрации основных ионов достигли стационарных значений. Заметим, что в этих условиях максимальные значения концентраций ионов ${\text{O}}_{2}^{ - }$ и ${\text{O}}_{4}^{ + }$ в тропосфере практически совпадают (${{n}_{{{\text{O}}_{2}^{ - }}}} \approx {{n}_{{{\text{O}}_{4}^{ + }}}} \approx 4 \cdot {{10}^{3}}$ см–3), тогда как величина ${{n}_{{{\text{O}}_{2}^{ + }}}}$ почти на порядок меньше. Сами максимумы концентраций располагаются на высотах 30, 20 и 15 км для ионов ${\text{O}}_{2}^{ + },$ ${\text{O}}_{2}^{ - }$ и ${\text{O}}_{4}^{ + }$ соответственно.
Таблица 4.
Альтитудные зависимости концентраций ионов ${\text{O}}_{2}^{ - },{\text{O}}_{4}^{ + },{\text{O}}_{2}^{ + },$ рассчитанные при ξ = 0.6 · 109 Тл · м
| Высота, км | T, K | Q*, см–3 ∙ с–1 | ${{n}_{{{\text{O}}_{2}^{ - }}}},$ см–3 | ${{n}_{{{\text{O}}_{4}^{ + }}}},$ см–3 | ${{n}_{{{\text{O}}_{2}^{ + }}}},$ см–3 |
|---|---|---|---|---|---|
| 0 | 298 | 4.0 | 7.59 ∙ 102 | 7.50 ∙ 102 | 9.40 ∙ 100 |
| 5 | 260 | 12.5 | 1.64 ∙ 103 | 1.62 ∙ 103 | 2.27 ∙ 101 |
| 10 | 223 | 32.5 | 2.97 ∙ 103 | 2.93 ∙ 103 | 4.47 ∙ 101 |
| 15 | 215 | 35.0 | 4.22 ∙ 103 | 4.12 ∙ 103 | 1.19 ∙ 102 |
| 20 | 215 | 22.0 | 4.27 ∙ 103 | 4.06 ∙ 103 | 2.55 ∙ 102 |
| 25 | 223 | 12.5 | 3.18 ∙ 103 | 2.80 ∙ 103 | 4.42 ∙ 102 |
| 30 | 230 | 8.0 | 2.16 ∙ 103 | 1.63 ∙ 103 | 6.18 ∙ 102 |
| 35 | 240 | 4.0 | 1.06 ∙ 103 | 5.95 ∙ 102 | 5.67 ∙ 102 |
* Для расчета использовались величины скорости ионизации Q, взятые из табл. 2.
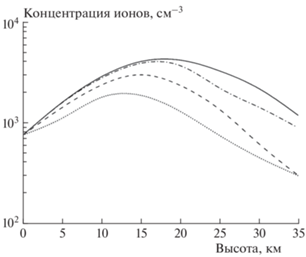
На рис. 5 изображены альтитудные зависимости концентраций основных тропосферных ионов ${\text{O}}_{2}^{ - },$ ${\text{O}}_{2}^{ + }$ и ${\text{O}}_{4}^{ + },$ рассчитанные при различных значениях магнитной жесткости $\xi .$ Это отвечает разным точкам географической локации: малые значения $\xi $ соответствуют полярным областям, а большие – экваториальным. Видно, что характер поведения кривых слабо изменяется в зависимости от величины $\xi $. Так, зависимости стационарных значений концентраций ионов ${\text{O}}_{2}^{ - }$ и ${\text{O}}_{4}^{ + }$ практически совпадают на высотах от 0 до 20 км. На бόльших высотах наблюдаются быстрый спад концентраций ионов ${\text{O}}_{4}^{ + }$ и рост концентрации ${\text{O}}_{2}^{ + }.$ На высоте 35 км концентрации ионов ${\text{O}}_{2}^{ + }$ и ${\text{O}}_{4}^{ + }$ сравниваются, однако их абсолютные величины заметно уменьшаются по мере приближения к экватору. Это связано с тем, что с ростом $\xi $ падает скорость ионизации Q (см. рис. 2) и, соответственно, концентрация ионов. Сказанное наглядно продемонстрировано на рис. 6, где представлены альтитудные зависимости суммы концентраций положительных ионов ${\text{O}}_{2}^{ + }$ и ${\text{O}}_{4}^{ + }$ при различных значениях магнитной жесткости.
Рис. 5.
Альтитудные зависимости концентраций ионов при различных значениях магнитной жесткости ξ, Тл · м: 0–0.6 · 109 (а), 2.4 · 109–2.5 · 109 (б), 6 · 109 (в), 13.5 · 109 (г). Кривые, соответствующие концентрациям различных ионов, обозначены: ${{n}_{{{\text{O}}_{4}^{ + }}}}$ – сплошная, ${{n}_{{{\text{O}}_{2}^{ + }}}}$ – штриховая, ${{n}_{{{\text{O}}_{2}^{ - }}}}$ – штрих-пунктирная.
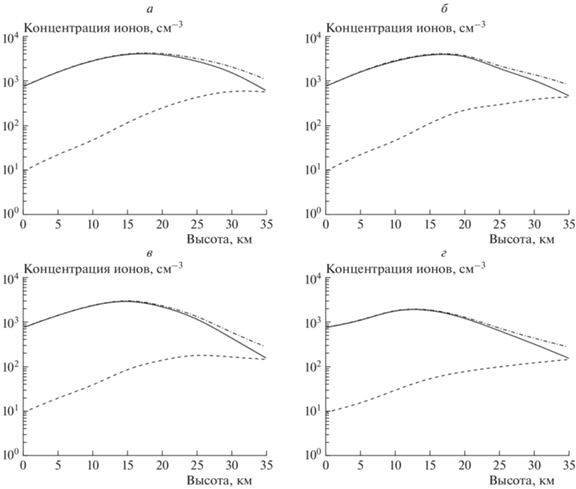
Рис. 6.
Альтитудные зависимости суммы концентраций положительных ионов ${\text{O}}_{4}^{ + }$ и ${\text{O}}_{2}^{ + }$ при различных значениях магнитной жесткости ξ, Тл · м: сплошная линия – 0–0.6 · 109, штрих-пунктирная – 2.4 · 109–2.5 · 109, штриховая – 6 · 109, точечная – 13.5 · 109.
Данные расчета концентрации ионов ${\text{O}}_{2}^{ - },$ ${\text{O}}_{2}^{ + }$ и ${\text{O}}_{4}^{ + }$ в приземном слое (от 0 до 5 км) в различных точках географической локации представлены в табл. 5. Наибольший интерес представляют высокие значения концентраций ионов, полученные на высоте 3300 м в г. Хуанкайо (Перу). Этот эффект объясняется тем, что в данном случае происходит ионизация как под действием космических лучей, так и γ-излучения. Высокое значение Q связано с геотектоническими процессами, при которых происходит выброс большого количества радиоактивных частиц [15, 36] в отличие, например, от г. Мауна-Лоа на Гавайских островах (см. табл. 3).
Таблица 5.
Рассчитанные значения концентраций ионов ${\mathbf{O}}_{{\mathbf{2}}}^{ - }{\mathbf{,O}}_{{\mathbf{4}}}^{{\mathbf{ + }}}{\mathbf{,O}}_{{\mathbf{2}}}^{{\mathbf{ + }}}$ в приземном слое (от 0 до 5 км) на различных высотах
| Высота, км | T, °С | Q*, см–3 ∙ с–1 | ${{n}_{{{\text{O}}_{2}^{ - }}}},$ см–3 | ${{n}_{{{\text{O}}_{4}^{ + }}}},$ см–3 | ${{n}_{{{\text{O}}_{2}^{ + }}}},$ см–3 |
|---|---|---|---|---|---|
| 0 | 19.5 | 2.0 | 7.57 ∙ 102 | 7.48 ∙ 102 | 9.40 ∙ 100 |
| 4.200 | 20.0 | 5.0 | 9.24 ∙ 102 | 9.13 ∙ 103 | 1.20 ∙ 101 |
| 0.150 | 6.8 | 8.5 | 1.20 ∙ 103 | 1.19 ∙ 103 | 1.50 ∙ 101 |
| 0.072 | 7.2 | 10.0 | 1.32 ∙ 103 | 1.30 ∙ 103 | 1.63 ∙ 101 |
| 0.017 | 19.5 | 14.0 | 1.58 ∙ 103 | 1.56 ∙ 103 | 2.00 ∙ 101 |
| 2.300 | 19.5 | 15.0 | 1.85 ∙ 103 | 1.88 ∙ 103 | 3.10 ∙ 101 |
| 0.011 | 13.7 | 16.0 | 1.70 ∙ 103 | 1.68 ∙ 103 | 2.10 ∙ 101 |
| 3.300 | 12.0 | 40.0 | 2.78 ∙ 103 | 2.75 ∙ 103 | 3.27 ∙ 101 |
* Для расчета использовались величины скорости ионизации Q, взятые из табл. 3.
7. ЗАКЛЮЧЕНИЕ
В настоящей работе рассмотрен процесс формирования сложно заряженных грозовых облаков, обладающих слоями положительных и отрицательных ионов и крупных ионных кластеров, появляющихся в тропосфере под действием космических лучей. Для расчета концентраций ионов разработана кинетическая модель, включающая 34 компонента и 102 реакции. Расчет проведен с использованием программного пакета KINET. Показано, что ионизация воздуха космическими лучами на высотах от 5 до 35 км приводит к образованию слабоионизованной плазмы, состоящей в основном из ионов ${\text{O}}_{2}^{ - },$ ${\text{O}}_{2}^{ + }$ и ${\text{O}}_{4}^{ + }.$ Максимумы концентраций ионов ${\text{O}}_{2}^{ - }$ и ${\text{O}}_{4}^{ + }$ наблюдаются на высотах от 15 до 20 км в условиях минимальной магнитной жесткости. Установлено также, что ионизация воздуха, обусловленная естественной радиоактивностью, в приземном слое значительно слабее ионизации космическими лучами.
Полученные данные о распределении концентрации ионов в тропосфере позволяют реализовать газовые разряды и искусственно стимулировать выпадение осадков без применения дорогостоящих химических реагентов, таких как, например, AgI. С этой целью необходимо поместить направленный источник ионов вблизи облаков или на поверхности Земли под облаками. В результате образованные ионы будут формировать дополнительные центры конденсации, приводящие к выпадению осадков. Данные по ионному составу тропосферы и альтитудному распределению концентраций ионов позволяют правильно оценить высоту, на которой следует установить источник, и определить его мощность для эффективного управления процессом. Кроме того, интерес к рассмотренным в настоящей работе явлениям обусловлен фундаментальными проблемами, связанными с глобальной спутниковой навигацией и дистанционным зондированием поверхности Земли [37].
Работа выполнена в рамках госзадания Министерства науки и высшего образования Российской Федерации (регистрационный номер темы 122040500060-4).
Список литературы
Смирнов Б.М. Физика глобальной атмосферы. Парниковый эффект, атмосферное электричество, эволюция климата. Долгопрудный: ИД “Интеллект”, 2017.
Хромов С.П., Мамонтова Л.И. Метеорологический словарь. Л.: Гидрометеоиздат, 1974.
Blankson I.M., Foster J.E. // 11-th International Conference on Plasma Assisted Technologies (ICPAT-11). Abu Dhabi: New York University Abu Dhabi, 2018. P. 15.
Голубков Г.В., Голубков М.Г., Карпов И.В. и др. // Хим. физика. 2011. Т. 30. № 5. С. 3; https://doi.org/10.7868/S0207401X1510012X
Saha K. The Earth’s atmosphere: Its physics and dynamics. Berlin: Springer, 2008; https://doi.org/10.1007/978-3-540-78427-2
Голубков Г.В., Адамсон С.О., Борчевкина О.П. и др. // Хим. физика. 2022. Т. 41. № 5. С. 53; https://doi.org/10.31857/S0207401X22050053
Borchevkina O.P., Adamson S.O., Dyakov Y.A. et al. // Atmosphere. 2021. V. 12. № 9. 1116; https://doi.org/10.3390/atmos12091116
Мохов И.И. Диагностика структуры климатической системы. СПб: Гидрометеоиздат, 1993.
Мазуров Г.И., Акселевич В.И., Иошпа А.Р. Учение об атмосфере. Ростов-на-Дону, Таганрог: Из-во ЮФУ, 2019.
Borchevkina O.P., Kurdyaeva Y.A., Dyakov Y.A. et al. // Atmosphere. 2021. V. 12. № 11. 1384; https://doi.org/10.3390/atmos12111384
Zurbenko I., Luo M. // Am. J. Clim. Chang. 2012. V. 1. № 3. P. 154; https://doi.org/10.4236/ajcc.2012.13013
Dunn R.J.H., Aldred F., Gobron N. et al. // Bull. Am. Meteorol. Soc. 2021. V. 102. № 8. P. S11; https://doi.org/10.1175/BAMS-D-21-0098.1
Андреев А.О., Дукальская М.В., Головина Е.Г. Облака: происхождение, классификация, распознавание / Под ред. А.И. Угрюмова. СПб: Из-во РГГМУ, 2007.
Переведенцев Ю.П., Мохов И.И., Елисеев А.В. Теория общей циркуляции атмосферы / Под ред. Э.П. Наумова. Казань: Казанский (Приволжский) федеральный университет, 2013.
Брикар Д. // Проблемы электричества атмосферы. Тр. III Междунар. конф. по электричеству атмосферы и космического пространства / Под ред. Я.М. Шварца. Л.: Гидрометеоиздат, 1969. С. 68.
Cooke D.J., Humble J.E., Shea M.A. et al. // Il Nuov. Cim. C. 1991. V. 14. № 3. P. 213; https://doi.org/10.1007/BF02509357
Simpson J.A. // Ann. Rev. Nucl. Part. Sci. 1983. V. 33. № 1. P. 323; https://doi.org/10.1146/annurev.ns.33.120183.001543
Neher H.V. // J. Geophys. Res. 1971. V. 76. № 7. P. 1637; https://doi.org/10.1029/JA076i007p01637
Голубков М.Г., Суворова А.В., Дмитриев А.В. и др. // Хим. физика. 2020. Т. 39. № 10. С. 69; https://doi.org/10.31857/S0207401X20100064
Голубков М.Г., Дмитриев А.В., Суворова А.В. и др. // Хим физика. 2022. Т. 41. № 5. С. 84; https://doi.org/10.31857/S0207401X22050065
Dmitriev A.V., Suvorova A.V., Ghosh S. et al. // Atmosphere. 2022. V. 13. № 2. 322; https://doi.org/10.3390/atmos13020322
Голубков Г.В., Бычков В.Л., Арделян Н.В. и др. // Хим. физика. 2019. Т. 38. № 7. С. 23; https://doi.org/10.1134/S0207401X19070045
Ardelyan N., Bychkov V., Belousov A. et al. // J. Phys.: Conf. Ser. 2017. V. 927. № 1. 012012; https://doi.org/10.1088/1742-6596/927/1/012012
Практикум по физической химии. Кинетика и катализ. Электрохимия / Под ред. Лунина В.В., Агеева Е.П. М.: Издат. центр “Академия”, 2012.
Kossyi I.A., Kostinsky A.Y., Matveyev A.A. et al. // Plasma Sourc. Sci. Techn. 1992. V. 1. № 3. P. 207; https://doi.org/10.1088/0963-0252/1/3/011
Ивлев Л.С., Довгалюк Ю.А. Физика атмосферных аэрозольных систем. СПб: НИИХ СПбГУ, 1999.
Боярчук К.А. // ЖТФ. 1999. Т. 69. № 3. С. 2.
Арделян Н.В., Бычков В.Л., Голубков Г.В. и др. // Хим. физика. 2018. Т. 37. № 1. С. 91; https://doi.org/10.7868/S0207401X18010028
Физика и химия газовых разрядов в пучках СВЧ-волн. Труды Института общей физики. Т. 47 / Под. ред. Коврижных Л.М. М.: Наука, 1994.
Shimo M., Ikebe Y., Nakayama T. et al. // Pure Appl. Geophys. 1972. V. 100. № 1. P. 109; https://doi.org/10.1007/BF00880232
Cobb W.E. // J. Atmos. Sci. 1968. V. 25. № 3. P. 470; https://doi.org/10.1175/1520-0469(1968)025<0470: TAECAM>2.0.CO;2
Тверской П.Н. Атмосферное электричество. Л.: Гидрометеоиздат, 1949.
Куповых Г.В. // Изв. вузов. Сев.-Кавк. рег. Естеств. науки. 2004. № 1. С. 40.
Ikebe Y., Kawano M. // Pure Appl. Geophys. 1971. V. 83. № 1. C. 120; https://doi.org/10.1007/BF00875105
Юнге Х.Е. Химический состав и радиоактивность атмосферы / Пер. с англ. / Под. ред. Израэля Ю.А. М.: Мир, 1965.
Голубков Г.В., Бычков В.Л., Готовцев В.О. и др. // Хим. физика. 2020. Т. 39. № 4. С. 51; https://doi.org/10.31857/S0207401X2004007X
Голубков Г.В., Манжелий М.И., Берлин А.А. и др. // Хим. физика. 2021. Т. 40. № 3. С. 86; https://doi.org/10.31857/S0207401X21030055
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика