Химическая физика, 2022, T. 41, № 6, стр. 3-6
Окисление монооксида углерода на покрытии из наночастиц золота в присутствии электрического поля
М. В. Гришин 1, *, А. К. Гатин 1, В. Г. Слуцкий 1, А. С. Федотов 2, В. А. Харитонов 1, Б. Р. Шуб 1
1 Федеральный исследовательский центр химической физики им. Н.Н. Семёнова
Российской академии наук
Москва, Россия
2 Институт нефтехимического синтеза им. А.В. Топчиева Российской академии наук
Москва, Россия
* E-mail: grishin@.chph.ras.ru
Поступила в редакцию 17.05.2021
После доработки 25.05.2021
Принята к публикации 21.06.2021
- EDN: NALINP
- DOI: 10.31857/S0207401X22060048
Аннотация
Впервые экспериментально установлена возможность увеличения каталитической активности покрытия из наночастиц золота при окислении монооксида углерода (СО) путем подачи на покрытие положительного электрического напряжения. Подача на покрытие напряжения U = +10 В приводит к увеличению скорости окисления СО на 28% при температуре 430 °С, атмосферном давлении и начальном составе смеси 1.8% СО + 10.2% О2 + Ar.
ВВЕДЕНИЕ
Платина и палладий (в виде покрытий из их наночастиц) используются как катализаторы окисления монооксида углерода (СО) в конверторах, которыми оснащаются современные автомобили для снижения концентрации вредных выбросов в выхлопных газах [1–4]. В последние годы проводятся исследования по возможной замене платиновых и палладиевых катализаторов в конверторах на обладающие большей сырьевой базой катализаторы на основе золота [5–8]. Увеличение активности указанных катализаторов является актуальной задачей, решение которой будет способствовать как повышению экологической чистоты двигателей внутреннего сгорания, так и снижению стоимости конверторов за счет уменьшения требуемой для окисления СО массы дорогостоящих катализаторов из благородных металлов.
В настоящее время основным приемом, позволяющим влиять на активность каталитических покрытий из наночастиц, является варьирование материала подложки, на которую наносится покрытие (см. обзоры [9, 10]). В общем случае подложка может оказывать следующие воздействия на состояние нанесенных на нее наночастиц: 1) предотвращать слипание наночастиц либо способствовать противоположному процессу; 2) изменять форму, состав и заряд наночастиц; 3) стабилизировать промежуточные продукты реакции. В результате описанных выше эффектов взаимодействия в системе наночастица–подложка химические свойства первых могут изменяться в широких пределах. Взаимосвязь каталитических свойств и структуры, электронных свойств, природы подложки и других параметров структурированных на наноуровне покрытий рассмотрено в ряде работ (см., например, [11–17]).
Впервые возможность увеличения активности электропроводящих каталитических покрытий из наночастиц методом подачи на них электрического напряжения от внешнего источника установлена в нашей работе [18]. Примером катализируемой реакции было разложение аммиака, а примером покрытий – покрытия из электропроводящих борорганических наночастиц (БОН) со средним размером 14.6 нм состава (C2B10H4)n. В экспериментах [18] подача на БОН положительного напряжения U = +6 В приводила к увеличению скорости разложения NH3 на 26%.
Работоспособность указанного метода применительно к платиновым и палладиевым покрытиям из их наночастиц продемонстрирована в наших опытах по каталитическому окислению СО на таких покрытиях. Показано, что подача на платиновое или палладиевое покрытие напряжения U = +10 В приводила к увеличению скорости окисления СО на 18% или 14% соответственно [19, 20]. Увеличение подаваемого напряжения приводило к пропорциональному увеличению скорости реакции. Так, при подаче на платиновое или палладиевое покрытие напряжения U = +30 В скорость окисления СО возрастала на 54% или 42% соответственно [21, 22]. В то же время эффект увеличения скорости реакции при подаче на эти покрытия отрицательного напряжения был существенно ниже.
Целью данной работы было экспериментальное доказательство возможности увеличения каталитической активности золотых нанопокрытий при окислении СО методом подачи на них электрического напряжения.
ОПИСАНИЕ ЭКСПЕРИМЕНТА
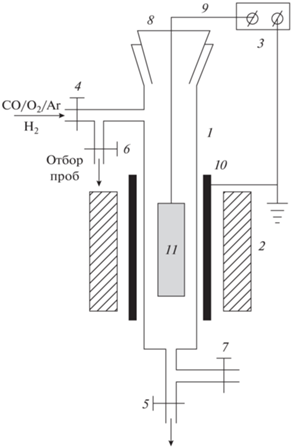
Эксперименты по окислению СО в смеси начального состава 1.8% СО + 10.2% О2 + Ar проводили при температуре 430 °С и атмосферном давлении в статической установке, состоящей из вертикального реактора 1, электронагреваемой печи 2 и источника напряжения 3 (рис. 1). Реактор состоял из стеклянной трубки высотой 250 мм с внутренним диаметром 5 мм, снабженной вентилями 4–7 и шлифом 8 с впаянным в него электродом 9 из молибденовой проволоки диаметром 0.25 мм. Электрод подсоединяли к незаземленной клемме источника напряжения 3. Заземленную клемму соединяли с металлической фольгой 10, охватывающей стеклянную трубку реактора. К электроду крепили алюминиевую пластину 11 размером 100 × 3 мм с нанесенными на нее с двух сторон наночастицами золота.
Рис. 1.
Схема установки для каталитического окисления CO: 1 – реактор, 2 – электронагреваемая печь, 3 – источник напряжения, 4–7 – вентили, 8 – разъемный шлиф, 9 – электрод, 10 – металлическая фольга, 11 – алюминиевая пластина с двусторонним покрытием из наночастиц золота.
Нанесение покрытия осуществлялось методом пропитки следующим образом. Вначале на каждую из сторон пластины наносили и высушивали на воздухе 150 мкл водного раствора тетрахлораурата водорода HAuCl4 · 4H2O c содержанием золота 0.7 · 10–2 мг/мл. Затем пластину подсоединяли к электроду 9 (рис. 1) и с помощью шлифа 8 помещали в реактор, где в потоке аргона с расходом 30 мл/мин пластину прогревали с использованием печи 2 до 400 °С в течение 4 ч. При этом происходило разложение HAuCl4 и на пластине образовывались наночастицы золота. После этого печь выключали и приготовленный образец пластины охлаждали до комнатной температуры в потоке аргона. Затем реактор продували указанной смесью CO/O2/Ar, (расход смеси – 30 мл/мин), вентили 4 и 5 закрывали и в таком виде реактор оставляли в течение нескольких часов до начала экспериментов.
Эксперименты начинали с прогрева реактора до 430 °С в потоке исходной смеси с расходом 30 мл/мин при открытых вентилях 4 и 5 (рис. 1). После этого проводили три серии экспериментов. В первой серии напряжение U от источника 3 на образец 11 с золотым покрытием не подавали (U = 0). Первый опыт этой серии начинали сразу по достижении реактором температуры в 430 °С. После этого реактор дополнительно продували исходной смесью с указанным расходом в течение 5 мин. Затем вентили 4 и 5 закрывали и заполнившую реактор смесь выдерживали в нем в течение 10 мин. По истечении этого времени вентили 6 и 7 открывали и с помощью подсоединенного к вентилю 6 шприца проводили отбор пробы из реактора для хроматографического анализа состава продуктов реакции. Затем реактор опять продували исходной смесью (время продувки – 5 мин, расход смеси – 30 мл/мин) и аналогично первому проводили второй, а затем и третий опыты с целью оценки воспроизводимости результатов.
После этого на образец подавали положительное напряжение U = +10 В и начинали вторую серию экспериментов. Реактор снова продували исходной смесью с расходом 30 мл/мин в течение 5 мин, закрывали реактор и выдерживали в нем смесь в течение 10 мин, осуществляли отбор пробы из реактора и хроматографически определяли в ней содержание СО и СО2. Подобная процедура проводилась трижды. Затем напряжение отключали (U = 0) и по той же методике, что и в экспериментах с подачей напряжения на образец, определяли состав продуктов реакции при отсутствии напряжения на золотом покрытии. Повторное проведение экспериментов с U = 0 связано с тем, что подача на образец напряжения могла приводить к частичному уносу с образца заряженных золотых наночастиц под действием электрического поля и последующему уносу этих частиц из реактора во время его продувки свежей смесью. Третья серия экспериментов полностью повторяла вторую серию с целью доказательства воспроизводимости результатов.
Для оценки влияния материала подложки на окисление СО проводили контрольные опыты, в которых использовали алюминиевую пластину без покрытия. Опыты проводили по той же методике, что и опыты с золотым покрытием. Структуру покрытия из наночастиц золота, созданного на алюминиевой подложке описанным выше методом, определяли по данным сканирующей туннельной микроскопии.
ЭКСПЕРИМЕНТАЛЬНЫЕ РЕЗУЛЬТАТЫ
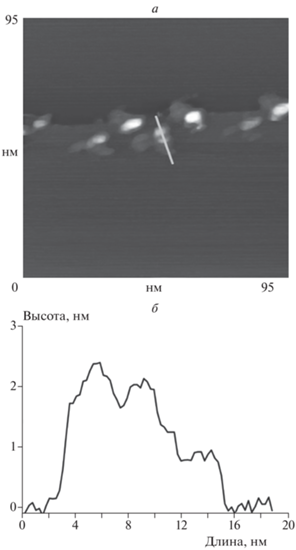
На рис. 2 приведены топографическое изображение золотого покрытия на поверхности алюминиевой пластины (а) и профиль покрытия (б). Как следует из этого рисунка, покрытие состоит из наночастиц размером 0.2–3 нм.
Рис. 2.
Топографическое изображение покрытия из наночастиц золота на поверхности алюминиевой пластины (а) и профиль покрытия (б) вдоль линии, указанной на фотографии.
На рис. 3 приведены экспериментальные данные по степени превращения (конверсии) СО в СО2:
(1)
${{\left[ {{\text{C}}{{{\text{O}}}_{2}}} \right]} \mathord{\left/ {\vphantom {{\left[ {{\text{C}}{{{\text{O}}}_{2}}} \right]} {{{{\left[ {{\text{CO}}} \right]}}_{0}}}}} \right. \kern-0em} {{{{\left[ {{\text{CO}}} \right]}}_{0}}}} = {{\left[ {{\text{C}}{{{\text{O}}}_{{\text{2}}}}} \right]} \mathord{\left/ {\vphantom {{\left[ {{\text{C}}{{{\text{O}}}_{{\text{2}}}}} \right]} {\left( {\left[ {{\text{CO}}} \right] + \left[ {{\text{C}}{{{\text{O}}}_{{\text{2}}}}} \right]} \right)}}} \right. \kern-0em} {\left( {\left[ {{\text{CO}}} \right] + \left[ {{\text{C}}{{{\text{O}}}_{{\text{2}}}}} \right]} \right)}},$Рис. 3.
Конверсия CO на покрытии из наночастиц золота с последовательной подачей напряжения на покрытие. Светлые метки – U = 0, черные – U = +10 В. Опыты проведены при 430 °С, атмосферном давлении, начальном составе смеси 1.8% СО + 10.2% О2 + Ar и времени экспозиции 10 мин.

Аналогичный эффект уменьшения каталитической активности нанесенных методом пропитки нанопокрытий из Pt или Pd после подачи на них напряжения наблюдался ранее в наших опытах по окислению СО на указанных покрытиях [19, 20]. Однако падение активности было более существенным – после подачи U = +10 В падение активности платиновых или палладиевых покрытий при U = 0 составляло 20% или 15%, что существенно ниже по сравнению с активностью покрытий в первой серии экспериментов.
Обнаруженный для золотых покрытий эффект уноса наночастиц означает, что для корректного определения влияния напряжения на каталитическую активность образца с таким покрытием необходимо сравнивать степени конверсии СО при подаче напряжения и при U = 0. Сравнивая подобным образом данные при U = +10 В с данными при U = 0, представленные на рис. 3, заключаем, что в условиях эксперимента подача на золотое покрытие напряжения U = +10 В приводит к увеличению каталитической активности покрытия на 28% при 430 °С. Такое увеличение существенно выше определенного по аналогичной методике увеличения активности платинового (18% при 250 °С) [19] или палладиевого покрытий (14% при 330 °С) [20] при подаче на них напряжения U = +10 В. Отметим, что в контрольных опытах с образцом без золотого покрытия конверсия CO не наблюдалась как при U = 0, так и при U = +10 В.
Таким образом, полученные результаты свидетельствуют о возможности увеличения каталитической активности золотых нанопокрытий при окислении СО путем подачи на покрытия положительного напряжения.
ЗАКЛЮЧЕНИЕ
Экспериментально доказана возможность увеличения каталитической активности покрытий из наночастиц золота при окислении СО путем подачи на них положительного электрического напряжения. В условиях эксперимента при 430 °С, атмосферном давлении и начальном составе смеси 1.8% СО + 10.2% О2 + Ar скорость окисления СО возрастает на 28% при подаче на покрытие напряжения +10 В.
Работа выполнена в рамках госзадания ФИЦ ХФ РАН по теме 45.9, 0082-2014-0011 (регистрационный номер АААА-А20-120013190076-0) и при финансовой поддержке Российским фондом фундаментальных исследований (грант № 20-03-00419).
Список литературы
Csere C. // Car and Driver. 1988. V. 33. № 7. P. 63.
Kaspar J., Fornasiero P., Graziani M. // Catal. Today. 1999. V. 50. № 2. P. 285.
Brandt E., Wang Y., Grizzle J. // IEEE Trans. Control Syst. Technol. 2000. V. 8. № 5. P. 767.
Алексахин А.В., Кириченко А.С. // Экономика в промышленности. 2013. № 4. С. 3.
Guzman J., Gates B.C. // J. Amer. Chem. Soc. 2004. V. 126. P. 2672.
Ануфриенко В.Ф., Мороз Б.Л., Ларина Т.В. и др. // ДАН. 2007. Т. 413. № 4. С. 493.
Nikolaev S.A., Golubina E.V., Krotova L.N. et al. // Appl. Catal., B: Environmental. 2015. V. 168. P. 303.
Takei T., Akira T., Nakamura J. et al. // Adv. Catal. 2012. V. 55. P. 1.
Бухтияров В.И., Слинько М.Г. // Успехи химии. 2001. Т. 70. № 2. С. 167.
Roldan Cuenya B. // Thin Solid Films. 2010. V. 518. P. 3127.
Гришин М.В., Гатин А.К., Дохликова Н.В. и др. // Кинетика и катализ. 2015. Т. 56. № 4. С. 539.
Эллерт О.Г., Цодиков М.В., Николаев С.А., Новоторцев В.М. // Успехи химии. 2014. Т. 83. № 8. С. 718.
Николаев С.А., Смирнов В.В., Васильков А.Ю., Подшибихин В.Л. // Кинетика и катализ. 2010. Т. 51. № 3. С. 396.
Simakova I.L., Solkina Yu.S., Moroz B.L. et al. // Appl. Catal., A: General. 2010. V. 385. № 1–2. P. 136.
Roldan Cuenya B., Behafarid F. // Surf. Sci. Rep. 2015. V. 70. P. 135.
Ланин С.Н., Пичугина Д.А., Шестаков А.Ф. и др. // ЖФХ. 2010. Т. 84. № 12. С. 2330.
Гришин М.В., Гатин А.К., Слуцкий В.Г., Харитонов В.А., Шуб Б.Р. // Хим. физика. 2015. Т. 34. № 7. С. 3.
Гришин М.В., Гатин А.К., Слуцкий В.Г. и др. // Хим. физика. 2016. Т. 35. № 6. С. 85.
Гришин М.В., Гатин А.К., Слуцкий В.Г. и др. // Хим. физика. 2020. Т. 39. № 3. С. 29.
Гришин М.В., Гатин А.К., Слуцкий В.Г. и др. // Хим. физика. 2021. Т. 40. № 6. С. 10.
Гришин М.В., Гатин А.К., Слуцкий В.Г. и др. // Хим. физика. 2020. Т. 39. № 5. С. 84.
Гришин М.В., Гатин А.К., Слуцкий В.Г. и др. // Хим. физика. 2021. Т. 40. № 9. С. 3.
Дополнительные материалы отсутствуют.
Инструменты
Химическая физика


