Химия твердого топлива, 2019, № 3, стр. 19-25
СТРУКТУРНО-ГРУППОВОЙ СОСТАВ И БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ ГУМИНОВЫХ КИСЛОТ, ПОЛУЧЕННЫХ ИЗ БУРЫХ УГЛЕЙ РОССИИ И МОНГОЛИИ
С. И. Жеребцов 1, *, Н. В. Малышенко 1, **, К. С. Вотолин 1, ***, В. А. Андроханов 2, ****, Д. А. Соколов 2, *****, Ж. Дугаржав 3, ******, З. Р. Исмагилов 1, *******
1 ФГБУН Федеральный исследовательский центр угля и углехимии СО РАН
650000 Кемерово, Россия
2 ФГБУН Институт почвоведения и агрохимии СО РАН
630090 Новосибирск, Россия
3 Институт химии и химической технологии Монгольской Академии Наук
13330 Улан-Батор, Монголия
* E-mail: sizh@yandex.ru
** E-mail: profkemsc@yandex.ru
*** E-mail: kostvot@mail.ru
**** E-mail: androhan@rambler.ru
***** E-mail: sokolovdenis@mail.ru
****** E-mail: dugar21mn@yahoo.com
******* E-mail: zinfer1@mail.ru
Поступила в редакцию 04.12.2018
После доработки 14.01.2019
Принята к публикации 06.02.2019
Аннотация
Исследована биологическая активность гуминовых препаратов в виде гуматов натрия и калия в зависимости от структурно-групповых параметров гуминовых кислот (ГК): степени ароматичности (fa), гидрофильно-гидрофобного параметра (fhh) и параметра, отражающего соотношение ароматических и алифатических фрагментов органической массы ГК (far/al). В качестве препаратов использовали нативные и модифицированные ГК, выделенные из торфа, бурых углей России и Монголии, состав которых охарактеризован с помощью технического и элементного анализов, 13С ЯМР (CPMAS)-спектроскопии. Установлено, что модифицирование путем деструктивного алкилирования и последующее дебитуминирование изменяет структурно-групповой состав ГК, увеличивает степень ароматичности и приводит к повышению их биологической активности.
ВВЕДЕНИЕ
Гуминовые вещества (ГВ) представляют собой особый класс природных соединений, образующихся из остатков отмерших организмов с отбором и накоплением устойчивых к биоразложению структур. Их ежегодный прирост на планете [1] составляет от 0.6 до 2.5 ⋅ 109 т/г. Они присутствуют в почвах, водах, твердых горючих ископаемых. Твердые горючие ископаемые низкой степени углефикации содержат в своей структуре значительные количества гуминовых веществ, которые характеризуются нестехиометричностью состава, нерегулярностью и гетерогенностью строения, а также полидисперсностью [2]. Несмотря на давнюю историю исследований, структура ГВ пока рассматривается только гипотетически.
Причина интереса к ГВ – наличие у них разнообразных специфических свойств, открывающих возможности их широкого практического использования во многих областях. Наряду с множеством функций, таких, как аккумулятивная, транспортная и протекторная, ГВ выполняют также регуляторную и физиологическую функции [1]. К регуляторной функции, прежде всего, относится формирование почвенной структуры и водно-физических свойств и, как следствие, теплового режима почвы.
Обработка почвы гуматами, выделенными из угля обработкой растворами щелочей, повышает ее влагонасыщение, что имеет важное значение для песчаных грунтов, влагоудерживающая способность которых под действием гуматов увеличивается более чем в 10 раз. На этих же принципах основано применение гуминовых препаратов в качестве мелиорантов. Гуматы калия, натрия и аммония оказывают существенное положительное влияние на водно-физические и физико-химические свойства почвы: повышают влагоемкость легких почв (в среднем на 30%), способствуя образованию агрономически ценной комковато-зернистой структуры; улучшают порозность и водопроницаемость тяжелых почв, препятствуя образованию трещин и корок; регулируют реакции ионного обмена между почвой и водными растворами; влияют на буферную емкость почв, тем самым способствуя поддержанию естественного уровня рН даже при избыточном поступлении кислых или щелочных агентов. Важной задачей является восстановление плодородия почв, предотвращение опустынивания.
ГВ повышают устойчивость растений к неблагоприятным факторам внешней среды: избыточным дозам минеральных удобрений, высоким или низким температурам, химическим средствам защиты растений, радиации и др. [1]. Отмечено [3–7] стимулирующее действие малых доз ГВ на развитие растений, на использование ими азота минеральных удобрений. Большие дозы гуматов (выше 0.1%) угнетают развитие растений. К физиологической функции относят воздействие ГВ на различные организмы. При использовании гуматов в сельском хозяйстве отмечают увеличение урожайности зерновых, кормовых и овощных культур в среднем на 10–30%, повышение всхожести семян и их прорастания, улучшение обмена веществ у растений: повышается поглощение минеральных веществ, усиливается корнеобразование.
Наиболее подвижной и реакционноспособной частью ГВ являются гуминовые кислоты – фракция, растворимая в щелочах и нерастворимая в кислотах (при рН < 2). ГК в виде водорастворимых форм принимают активное участие в окислительно-восстановительных процессах клетки, являясь, с одной стороны, источником активированного кислорода, а другой – акцептором водорода [8].
На основании проведенных экспериментов [9] не удалось обнаружить прямую зависимость биологической активности ГК от содержания в них карбоксильных и фенольных гидроксилов. С другой стороны, предполагается [10], что их биологическая активность определяется способностью участвовать в окислительно-восстановительных реакциях в растительной клетке и усилением этих процессов согласно теории Баха–Паладина–Сент-Дьёрди. Отмечено [10], что биологическая активность зависит от концентрации свободных радикалов, содержания хиноидных групп и фенольных гидроксилов. Менее биологически активные ГК характеризуются меньшим содержанием хиноидных групп. ГК бурых и окисленных углей содержат (мг-экв/г): карбоксильные группы 1.8–5.5; фенольные – гидроксилы 0–6.0; хиноидные группы 0.6–4.0 [10]. Опыты применения гуминовых препаратов к зерновым культурам – овсу и пшенице – показали о прямо пропорциональной зависимости биологической активности ГК не только от fa, но и от других структурно-групповых параметров, таких, как гидрофильно-гидрофобный параметр fhh и параметр, отражающий соотношение ароматических и алифатических фрагментов органической массы ГК (ароматичность/алифатичность) far/al [11].
Биологическая активность также была протестирована на ряде природных и модифицированных ГВ, полученных из различных источников [12], и оценена по изменениям в строении корня на примере томата и кукурузы. Для модифицирования были применены реакции гидролиза, восстановления, алкилирования метилом, отщепления алкильных фрагментов. Обнаружено, что окисленные перманганатом калия, а также алкилированные метилом ГВ самые эффективные. Предположено, что гидрофобный домен ГВ заключает внутри себя биологически активные молекулы, подобные ауксинам. При контакте с органическими кислотами, поступающими из корня, нарушается гидрофобная оболочка и высвобождаются биологически активные компоненты.
Таким образом, применение гуминовых препаратов позволят улучшить структуру почвы, повысить урожайность растений и их устойчивость к негативным факторам окружающей среды. Несмотря на большой опыт использования гуминовых препаратов в качестве стимуляторов роста растений, в настоящее время нет единого мнения о действующем факторе (или совокупности факторов) и механизме биологического стимулирования растений и почвенных микроорганизмов ГК и его связи с их свойствами. ГК объединены общим принципом строения, но имеют различия по составу в широком интервале в зависимости от характера исходного вещества. В связи с этим необходимо выполнять систематические фундаментальные исследования, направленные на получение зависимостей “структура – свойство” между элементным и структурно-групповым составом, строением ГВ, их физико-химическими характеристиками и наличием у гуминовых веществ биологической активности.
Цель работы – определение физико-химических характеристик ряда углей и ГК, выбор факторов структурно-группового состава ГК, связанных с биологической активностью; обоснование характеристик ГК для последующего отбора сырьевых источников и получения физиологически активных препаратов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для исследования был выбран ряд гумусовых бурых углей месторождений Багануур (БАГ) и Шивээ-Овоои (ШО) (Монголия), Тисульского месторождения Канско-Ачинского бассейна (БУТС), его естественно-окисленная форма (БУТСО), Тюльганского (БУТ) и Маячного (БУМ) месторождений Южного Урала (Россия), а также торф Крапивинского месторождения Кемеровской области (ТК). Гуминовые кислоты получали из гуматов натрия (ГумNa) или калия (ГумK) осаждением из раствора при добавлении соляной кислоты [13]. Ряд гуминовых кислот был получен из последовательно алкилированных спиртами и дебитуминированных образцов углей (ГКА) в соответствии с методиками [14–16].
Проведена наработка опытных образцов гуматов натрия и калия из бурого угля и его естественно-окисленной формы. Исходные лигниты и образцы гуматов охарактеризованы элементно-техническим и функциональным анализами (табл. 1 и 2).
Таблица 1.
Данные технического и элементного анализа исследуемых образцов, мас. %
| Образец | W a | Ad | V daf | Cdaf | Hdaf | (O + N + S)daf (по разности) | H/C (атомн.) | $({\text{HA}})_{t}^{{daf}}$ |
|---|---|---|---|---|---|---|---|---|
| БАГ | – | 26.3 | 52.6 | 67.5 | 4.4 | 28.1 | 0.78 | 31.2 |
| ГумNa БАГ | 6.9 | 17.9 | – | 60.5 | 3.8 | 35.7 | 0.75 | 52.8 |
| ШО | – | 31.6 | 52.2 | 70.5 | 4.4 | 25.1 | 0.75 | 34.0 |
| ГумNa ШО | 16.2 | 24.8 | – | 66.8 | 4.5 | 28.7 | 0.81 | 58.9 |
| БУТС | 8.3 | 10.3 | 48.3 | 61.4 | 5.0 | 33.5 | 0.98 | 22.1 |
| ГК ГумK БУТС | 5.0 | 4.0 | – | 60.8 | 4.2 | 35.0 | 0.83 | – |
| ГК ГумNa БУТС | 3.8 | 1.9 | – | 59.8 | 3.5 | 36.7 | 0.70 | – |
| БУТСО | 10.0 | 43.5 | 80.3 | 69.3 | 6.0 | 24.7 | 1.04 | 60.9 |
| ГК ГумK БУТСО | 4.6 | 17.0 | – | 46.2 | 3.2 | 50.6 | 0.83 | – |
| ГК ГумNa БУТСО | 10.6 | 10.9 | – | 59.7 | 6.2 | 34.0 | 1.25 | – |
| БУТ | 6.5 | 23.5 | 67.3 | 66.2 | 7.0 | 26.8 | 1.27 | 39.1 |
| ГК ГумNa БУТ | 3.63 | 7.57 | – | 62.9 | 5.82 | 31.3 | 1.11 | – |
| БУМ | 5.3 | 20.0 | 63.6 | 58.6 | 6.8 | 34.6 | 1.39 | 73.5 |
| ГК ГумNa БУМ | – | – | – | 57.3 | 7.4 | 35.3 | 1.55 | – |
| ТК | 11.2 | 12.3 | 72.6 | 46.8 | 5.9 | 47.3 | 1.51 | 32.4 |
| ГК ГумNa ТК | – | – | – | 45.1 | 5.5 | 49.4 | 1.46 | – |
Таблица 2.
Содержание активных кислородсодержащих групп в гуминовых кислотах углей месторождений Багануур и Шивээ-Овоо
| Образец | Содержание кислых групп, мг-экв/г | Хиноидные группы, мг-экв/г | ||
|---|---|---|---|---|
| карбоксильные группы | фенольные гидроксилы | сумма | ||
| ГумNa БАГ | 4.33 | 3.42 | 7.75 | 2.75 |
| ГумNa ШО | 5.13 | 3.52 | 8.65 | 3.17 |
Для определения общего содержания кислых (карбоксильных и гидроксильных) групп использовали баритовый метод, а для содержания карбоксильных групп – ацетатный [17]. Содержание гидроксильных групп определяли как разницу между общим содержанием кислых групп и карбоксильных.
Содержание хиноидных групп определяли восстановлением их хлоридом олова (II) в щелочной среде с последующим оттитровыванием его избытка раствором бихромата калия [18]. Расчет содержания функциональных групп проводили с учетом результатов холостых опытов.
Для установления зависимости “структура–свойство” были проведены тесты по определению биологической активности ГК в виде гуматов калия и натрия (концентрация 0.02%), полученных как из исходных, так и модифицированных последовательным алкилированием и дебитуминированием образцов углей и торфа.
В экспериментах использовали сортовые пшеницы “Новосибирская 89”, “Ирень” и редис сорта “Смак” в соответствии с методиками [19, 20] и ГОСТ 12038-84, ГОСТ 54221-2010 [21, 22]. Семена проращивали при постоянной температуре 20°С в темноте в специальных растильнях-лотках между слоями увлажненной фильтровальной бумаги. Биологическую активность ГК и ГКА определяли по увеличению длины корней пшеницы Δ1 (превышение над контролем, %) и по величиине индекса фитоактивности (ИФ) (% к контролю, Δ2) с учетом энергии прорастания семян (ЭП), длине корня (ДК) и высоте проростка (ВП). Величина ИФ является обобщающим индексом и вычисляется как средняя величина суммы показателей ЭП, ДК и ВП, выраженная в долях единицы:
Относительная ошибка во всех экспериментах составляла 3–5% для уровня значимости α = 0.05.
Спектры 13С-ЯМР высокого разрешения в твердом теле регистрировались на приборе “Bruker AVANCEIII 300 WB” на частоте 75 МГц с использованием стандартной методики кросс-поляризации и вращением под магическим углом (CPMAS).
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
На основании анализа литературных данных [10, 12, 23] для обнаружения связи структурно-группового состава ГК с их биологической активностью были выбраны три параметра, вычисленные по данным 13С ЯМР (CPMAS):
1) степень ароматичности
2) гидрофильно-гидрофобный параметр
3) ароматичность/алифатичность
В табл. 3 приведены интегральные интенсивности спектральных областей углей, гуминовых кислот и структурные параметры исследуемых образцов, вычисленные по данным 13С ЯМР-спектров. Структурный параметр fa отражает содержание всех ароматических структурных групп, в том числе фенольных.
Таблица 3.
Интегральные интенсивности спектральных областей в 13С ЯМР-спектрах (%) и структурные параметры образцов углей и гуминовых кислот
| Образец | Химический сдвиг, м.д. | Структурный параметр | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 220-187 | 187-165 | 165-145 | 145-108 | 108-90 | 90-48 | 48-5 | fa | fh/h | far/al | |
| C=О | COOH(R) | CAr–OH | CAr | СO–Alk–O | CAlk–O | СAlk | ||||
| БУТС | 4.4 | 4.7 | 4.2 | 19.1 | 3.5 | 7.5 | 55.6 | 23.3 | 0.3 | 0.3 |
| ГК ГумK | 4.4 | 6.1 | 5.0 | 15.1 | 4.2 | 8.0 | 55.2 | 20.1 | 0.4 | 0.3 |
| ГК ГумNa | 4.4 | 7.3 | 5.4 | 17.9 | 3.6 | 10.8 | 50.7 | 23.3 | 0.5 | 0.4 |
| БУТСО | 2.6 | 6.0 | 8.9 | 31.9 | 5.4 | 12.7 | 30.3 | 40.8 | 0.6 | 0.8 |
| ГК ГумK | 3.8 | 6.7 | 9.5 | 33.1 | 6.3 | 14.0 | 25.4 | 42.6 | 0.7 | 0.9 |
| ГК ГумNa | 3.5 | 7.4 | 8.2 | 31.7 | 6.3 | 14.8 | 26.8 | 39.9 | 0.7 | 0.8 |
| БУТ | 4.2 | 5. 8 | 3.6 | 25.1 | 19.6 | 41.6 | 28.7 | 0.5 | 0.5 | |
| ГК ГумNa | 4.3 | 7.9 | 6.8 | 22.5 | 4.9 | 16.3 | 36.5 | 29.3 | 0.7 | 0.5 |
| БУМ | 4.3 | 4.1 | 4.5 | 28.3 | 6.1 | 12.5 | 40.2 | 32.8 | 0.5 | 0.6 |
| ГК ГумNa | 4.7 | 4.9 | 3.7 | 26.1 | 5.9 | 13.7 | 41.1 | 29.8 | 0.5 | 0.5 |
| ТК | 2.7 | 8.2 | 4.8 | 11.4 | 55.7 | 17.2 | 16.2 | 2.5 | 0.2 | |
| ГК ГумNa | 3.4 | 8.0 | 7.0 | 15.8 | 9.2 | 38.5 | 18.1 | 22.8 | 1.9 | 0.3 |
Деструктивное О-алкилирование твердых горючих ископаемых (ТГИ) спиртами деполимеризует органическую массу угля и, с одной стороны, увеличивает выход битумоидов преимущественно алифатического характера, с другой – приводит к повышению ароматичности дебитуминированного исследуемого образца [14–16, 24]. Гуминовые кислоты, извлекаемые из такого объекта, соответственно, более ароматичные, чем извлеченные из исходных ТГИ. Таким образом, существуют предпосылки, что эти ГК должны иметь повышенную биологическую активность. В табл. 4 представлены данные структурно-группового состава образцов гуминовых кислот, полученных из исходных углей торфа, после деструктивного алкилирования и дебитуминирования (ГКА), имеющие значимый разброс показателя fa. Действительно, данные табл. 4 иллюстрируют увеличение степени ароматичности ГКА по сравнению с соответствующими ГК для всех изученных ТГИ гумусовой природы. Так, для ГК, извлеченных из бурого угля Тисульского месторождения, fa составляет 23.3. ГКА, извлеченные из того же угля, но предварительно алкилированного бутанолом и затем дебитуминированного, имеют показатель fa, равный 31.9. В то же время минимальное увеличение степени ароматичности наблюдается для гуминовых кислот, выделенных из крапивинского торфа – для ГК fa = 22.6; для ГКА fa = 22.8.
Таблица 4.
Интегральные интенсивности спектральных областей образцов ГК и ГКА по данным 13С ЯМР, %
| Образец ГК | Химический сдвиг, м.д. | |||||||
|---|---|---|---|---|---|---|---|---|
| 220-187 С=О | 187-165 СООН(R) | 165-145 СAr–O | 145-108 CAr | 108-90 CO-Alk–O | 90-48 CAlk–O | 48-5 CAlk | fa | |
| Бурый уголь Тисульского месторождения | ||||||||
| ГК | 4.4 | 7.3 | 5.4 | 17.9 | 3.6 | 10.8 | 50.7 | 23.3 |
| ГКА | 1.3 | 6.3 | 6.9 | 25.0 | 4.3 | 10.6 | 45.6 | 31.9 |
| Бурый уголь Тисульского месторождения, естественно-окисленный в пласте | ||||||||
| ГК | 3.5 | 7.4 | 8.2 | 32.7 | 6.3 | 14.8 | 26.8 | 40.9 |
| ГКА | 1.6 | 5.3 | 10.2 | 32.9 | 5.1 | 11.0 | 33.8 | 43.1 |
| Бурыйуголь Тюльганского месторождения | ||||||||
| ГК | 4.3 | 7.9 | 6.8 | 22.5 | 4.9 | 16.3 | 36.5 | 29.3 |
| ГКА | 3.8 | 8.6 | 8.5 | 28.2 | 5.8 | 16.9 | 27.9 | 36.7 |
| Бурый уголь Маячного месторождения | ||||||||
| ГК | 4.7 | 4.9 | 3.7 | 26.1 | 5.9 | 13.7 | 41.1 | 29.8 |
| ГКА | 4.1 | 8.2 | 7.4 | 34.8 | 7.5 | 16.5 | 20.9 | 42.2 |
| Торф Крапивинский | ||||||||
| ГК | 3.4 | 7.9 | 6.7 | 15.9 | 8.6 | 35.4 | 22.2 | 22.6 |
| ГКА | 3.4 | 8.0 | 7.0 | 15.8 | 9.2 | 38.5 | 18.1 | 22.8 |
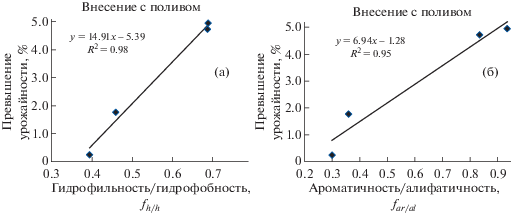
Было обнаружено, что биологическая активность ГК, оцененная по увеличению урожайности, прямо пропорциональна выбранным структурным параметрам. На рис. 1 представлены зависимости, из которых видно, что увеличение степени ароматичности и гидрофильности ГК приводит к повышению урожайности на примере пшеницы сорта “Новосибирская 89”.
Рис. 1.
Зависимость урожайности пшеницы “Новосибирская-89” от значения параметров гидрофильность/гидрофобность (а) и ароматичность/алифатичность (б) образцов ГК.
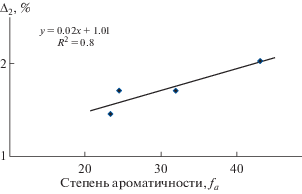
На рис. 2 и 3 приведены результаты экспериментов с семенами пшеницы и редиса, а именно зависимости превышения длины корней семян пшеницы над контрольным опытом Δ1 и индекса фитоактивности Δ2 семян редиса от степени ароматичности fa используемых гуминовых кислот.
Рис. 2.
Зависимость длины корней пшеницы (превышение над контролем Δ1, %) от степени ароматичности fa образцов ГК.
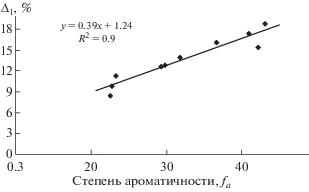
Из рис. 2, 3 видно, что биологическая активность ГК и ГКА бурых углей и торфа, оцененная по параметрам Δ1 и Δ2 по отношению к испытанным культурам – пшенице и редису – также прямо пропорциональна структурному параметру – степени ароматичности fa. Гуминовые кислоты, выделенные из углей, предварительно алкилированных и дебитуминированных, по степени ароматичности близки к высокоактивным природным ГВ естественно-окисленных углей (табл. 4) буроугольной стадии зрелости и проявляют повышенную биологическую активность по сравнению с ГК, выделенными из исходных углей. В то же время последовательное алкилирование и дебитуминирование крапивинского торфа приводит к минимальному увеличению степени ароматичности ГК (табл. 4), которые проявляют самую низкую биологическую активность.
ВЫВОДЫ
Исходные угли и полученные из них ГК обладают различным структурно-групповым составом. Естественно-окисленная форма угля и полученные из нее ГК имеют более ароматический характер и большее содержание фенольных гидроксилов. Установлено, что биологическая активность ГК прямо пропорциональна следующим структурным параметрам: степени ароматичности fa, гидрофильно-гидрофобному параметру fhh и параметру, отражающему соотношение ароматических и алифатических фрагментов органической массы ГК (ароматичность/алифатичность) far/al.
Показано, что последовательное алкилирование и дебитуминирование гумусовых бурых углей приводит к увеличению содержания ароматических структур в получаемых из модифицированных источников ГК. Данные гуминовые кислоты близки по составу к высокоактивным природным ГВ естественно-окисленных углей буроугольной стадии зрелости и проявляют повышенную биологическую активность. Последовательное алкилирование и дебитуминирование крапивинского торфа приводит к минимальному увеличению степени ароматичности fa и биологической активности.
Полученные результаты помогут планировать выбор сырьевой базы бурых углей для получения активных ГК. Для условий Монголии перспективными углями являются гумусовые бурые угли месторождений Багануур и Шивээ-Овоо Монголии, которые характеризуются достаточно высокими значениями содержания фенольных и хиноидных функциональных групп.
Кроме того, перспективно целенаправленное изменение функционального состава гуминовых препаратов с помощью предварительного алкилирования и дебитуминирования первоисточника для получения субстанций с определенным структурно-групповым составоми высоким содержанием ароматических фрагментов. Полученные результаты могут быть использованы для прогноза биологической активности ГК и получения высокоэффективных препаратов на их основе.
Список литературы
Орлов Д.С. // Соросовский образовательный журнал. 1997. № 2. С. 56.
Перминова И.В. Анализ, классификация и прогноз свойств гумусовых кислот // Дисс. … докт. хим. наук. М.: МГУ, 2000. 359 с.
Христева Л.А. // Гуминовые удобрения. Теория и практика их применения. 1973. № 4. С. 5.
Горовая А.И., Кулик А.Ф. // Гуминовые удобрения. Теория и практика их применения. 1980. № 7. С. 74.
Александрова И.В. // Органическое вещество целинных и освоенных почв. М.: Наука, 1972. С. 30.
Александрова И.В. // Почвоведение. 1977. № 5. С. 31.
Александрова И.В. // Почвоведение. 1983. № 11. С. 22.
Драгунов С.С. // Гуминовые удобрения. Теория и практика их применения. 1980. № 7. С. 5.
Апраксина С.М., Думбай И.Н., Дуленко В.И. // Пути переработки углей Украины. Киев: Наук. думка, 1988. С. 98.
Кухаренко Т.А. // ХТТ. 1976. № 2. С. 24.
Жеребцов С.И., Малышенко Н.В., Смотрина О.В., Лырщиков С.Ю., Брюховецкая Л.В., Исмагилов З.Р. // ХИУР. 2015. Т. 23. № 4. С. 439. https://doi.org/10.15372/KhUR20150413
Dobbs L.B., Canellas L.P., Olivares F.L., Aguiar N.O., Facanha A.R., Peres L.E.P., Azevedo M., Spaccini R., Piccolo A. // J. Agricultural and Food Chem. 2010. V. 58. № 6. P. 3681.
Тайц Е.М., Андреева И.А. Методы анализа и испытания углей. М.: Недра,1983. 301 с.
Жеребцов С.И., Исмагилов З.Р. // ХТТ. 2012. № 6. С. 7.
Жеребцов С.И., Моисеев А.И. // ХТТ. 2009. № 2. С. 12.
Жеребцов С.И., Мусин Ю.В., Моисеев А.И. // Химия растительного сырья. 2009. № 2. С. 125.
Хилько С.Л., Ковтун А.И., Рыбаченко В.И. // ХТТ. 2011. № 5.
Глебко Л.И., Максимов О.Б. О функциональном анализе гуминовых кислот // Новые методы исследования гуминовых кислот. / Под ред. Елякова Г.Б. Владивосток: Изд-во АН СССР, 1972. 135 с.
Воронина Л.П., Якименко О.С., Терехова В.А. // Агрохимия. 2012. № 6. С. 50.
Практикум по растениеводству. Под ред. П.П. Вавилова, В.В. Гриценко, В.С. Кузнецова. М.: Колос, 1983. 352 с.
ГОСТ 12038-84. Семена сельскохозяйственных культур. Методы определения всхожести. М.: Изд-во стандартов, 1984. 30 с.
ГОСТ Р 54221-2010. Гуминовые препараты из бурых и окисленных каменных углей. Методы испытания.М.: Стандартинформ, 2012. 10 с.
Калабин Г.А., Каницкая Л.В., Кушнарев Д.Ф. Количественная спектроскопия ЯМР природного органического сырья и продуктов его переработки. М.: Химия, 2000. 408 с.
Жеребцов С.И., Малышенко Н.В., Соколов Д.А., Исмагилов З.Р. // Вестн. КузГТУ. 2016. № 4. С. 108.
Дополнительные материалы отсутствуют.
Инструменты
Химия твердого топлива