Химия твердого топлива, 2021, № 3, стр. 58-64
МОДЕЛИРОВАНИЕ ФИЗИЧЕСКИХ ХАРАКТЕРИСТИК ЧАСТИЦ ДИСПЕРСНОЙ ФАЗЫ ПО РЕЗУЛЬТАТАМ МЕТОДА ДИНАМИЧЕСКОГО РАССЕЯНИЯ СВЕТА
Х. М. Кадиев 1, *, А. М. Гюльмалиев 1, **, М. Х. Кадиева 1, ***
1 ФГБУН Ордена Трудового Красного Знамени Институт нефтехимического синтеза имени А.В. Топчиева РАН
119991 Москва, Россия
* E-mail: kadiev@ips.ac.ru
** E-mail: gyulmaliev@ips.ac.ru
*** E-mail: mkadieva@ips.ac.ru
Поступила в редакцию 18.12.2020
После доработки 01.02.2021
Принята к публикации 03.02.2021
Аннотация
Предложена методика построения аппроксимирующей функции распределения частиц дисперсной фазы по размерам по методу динамического рассеяния света, позволяющая переходить от экспериментального спектра в координатах “размер частиц–интенсивность” к теоретическим спектрам “размер частиц–число частиц” и “размер частиц–масса частиц” и получить дополнительные данные о характере распределения частиц по размерам. Приведен иллюстрированный на конкретных примерах алгоритм метода расчета.
Разработка прикладных математических методов расчета на основе экспериментальных данных и определения физических параметров частиц суспензии в конкретной среде: размер, концентрация и распределение по размерам, по массе имеют большое значение для моделирования структуры и свойств дисперсной системы. В настоящее время широко применяются лазерные и оптические методы экспериментального измерения характерных параметров суспензии и параллельно разрабатываются прикладные математические методы моделирования технологий синтеза и свойств частиц суспензий [1–4].
Недостаточная изученность многих технологических проблем, таких как получение стабильных суспензий с высокой массовой долей твердой фазы, обусловливает актуальность поиска новых комплексных методов для оценки свойств дисперсных систем, в частности при разработке технологии переработки угольных шламов с получением стабильного суспензионного угольного топлива [5].
Одним из перспективных направлений разработки новых эффективных технологических процессов глубокой переработки тяжелого углеводородного сырья является использование наногетерогенных каталитических систем, которые проявляют уникальные свойства и имеют большое преимущество по сравнению с традиционными катализаторами [5–7]. При синтезе наноразмерных каталитических систем из прекурсоров катализатора в процессах гидроконверсии остатков вакуумной дистилляции нефтей, гидрирования индивидуальных ароматических углеводородов и технических смесей, синтеза Фишера–Тропша получают полидисперсную суспензию наногетерогенного катализатора [5]. Размеры частиц в суспензии определяют на приборе N5 Submicron Particle Size Analyzer, который базируется на методе фотонно-корреляционной спектроскопии (PCS) или динамического светорассеяния (DLS) [6, 7]. Спектр распределения частиц по размерам строится в координатах “размер частиц–интенсивность” (рис. 1). В работе для аппроксимации экспериментального спектра распределения частиц по размерам введена функция $n(d) = ad{{e}^{{ - b{{d}^{2}} + c}}}$, где a, b, c – константы, значения которых определяются из спектра. Однако для более детального анализа физико-химических свойств дисперсной фазы необходимо иметь информацию о числе частиц с заданным диаметром, представленных в координатах “размер частиц–число частиц”, что дает возможность оценить каталитическую активность частиц дисперсной фазы и стабильность дисперсной системы в зависимости от количества частиц с определенным диаметром.
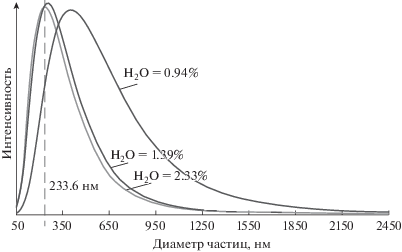
Рис. 1.
Распределение по размерам частиц MoO2 при разном содержании воды в исходной эмульсии “водный раствор (NH4)6Mo7O24/легкий газойль”.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Предложен метод моделирования экспериментального спектра в координатах “размер частиц–интенсивность” для построения теоретического спектра в координатах “размер частиц–число частиц”. Метод строится в предположении, что частицы сферически симметричны, кроме того, размер сольватной оболочки не входит в размер частицы, а “интенсивность распределения частиц” косвенно характеризует количество частиц.
Спектр распределения по размерам частиц MoO2 при разном содержании воды в исходной эмульсии водный раствор (NH4)6Mo7O24/легкий газойль представлен на рис. 1. Содержание прекурсора в эмульсии составляет 503 ppm Mo. Суспензии получены при температуре 207 ± 2 °С.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Для описания экспериментальных спектров распределения частиц по размерам примем функцию:
где D – диаметр частицы, нм; А и В – константы, значения которых определяются по экспериментальным данным.Положение экстремума функции $F(D)$ определяется из уравнения
Отсюда находим, что функция $F(D)$ достигает максимума в точке $D = 2{\text{/}}B$.
Общее число частиц ${{N}_{\Sigma }}$ равно площади под кривой
(3)
${{N}_{\Sigma }} = \mathop \smallint \limits_0^{{{D}_{k}}} F(D)dD = \frac{{2A[1 - (B{{D}_{k}} + 0.5{{B}^{2}}D_{k}^{2} + 1){{e}^{{ - B{{D}_{k}}}}}]}}{{{{B}^{3}}}},$Очевидно, что в общем случае для 1 моль дисперсной фазы число частиц $N \leqslant {{N}_{{\text{A}}}}$ (NA – число Авогадро).
Для определения массового распределения частиц по диаметрам частиц в приближении сферической модели вычислим массу частицы с диаметром D [7]:
где ρ – плотность вещества (дисперсной фазы), г/см3.Гистограмма массового распределения частиц по размерам строится по функции
Отсюда суммарная масса частиц c диаметром D будет равна (г):
Для построения модели из экспериментального спектра определяются два параметра: А и В. Значение параметра В находится из условия равенства положения максимума в экспериментальном и теоретическом спектрах:
Константа A находится из условия равенства расчетной массы дисперсной фазы $~{{m}_{{{\Sigma }}}}~$и экспериментального значения содержания дисперсной фазы в составе суспензии С0: при $~{{m}_{\Sigma }} = {{C}_{0}}$
Вставляя значение А в формулу (1), находим число частиц ND с диаметром D:
Число молекул в одной частице дисперсной фазы равно
Отсюда, для суспензии МоО2 в легком газойле, полученной из эмульсии с содержанием воды 2.33% (${{D}_{{{\text{ma}}x}}}$ = 233.6 нм), получаем В = 0.00856, а с содержанием воды 0.94% (${{D}_{{{\text{max}}}}}$ = 410 нм) – В = = 0.004878 нм.
При концентрации Mo 503 ppm в суспензиях МоО2 в легком газойле количество МоО2 в предположении, что дисперсная фаза состоит только из частиц МоО2, составляет 0.06706 г на 100 г дисперсионной среды в суспензии (1 ppm = 0.0001%). Тогда суммарная масса всех частиц будет равна C0 = 0.06706 г. Из этого условия для суспензии МоО2 в легком газойле, полученной из эмульсии с содержанием воды 2.33%, находим А = 6.49 ⋅ 105 и А = 2.224 ⋅ 104 при содержании воды 0.94%.
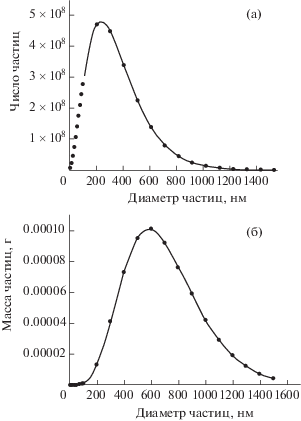
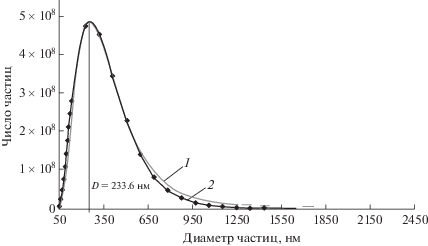
На рис. 2 результаты расчета распределения частиц по размерам по аналитической функции (1) сопоставлены с автоматически построенной по данным эксперимента гладкой кривой. Видно, что аппроксимация экспериментальных данных хорошая.
Рис. 2.
Сопоставление автоматически построенной функции распределения частиц по диаметрам (1) с аналитической (2).
Результаты аналогичных расчетов характеристик частиц дисперсной фазы в координатах “размер частиц–число частиц” для случая, когда содержание воды в эмульсии составляет 2.33%, представлены в табл. 1. Сумма числа всех частиц составляет ${{N}_{\Sigma }}$ = 2.06944 ⋅ 1011. Максимум распределения частиц по массам смещается в сторону больших размеров (рис. 3). Представляет интерес число молекул МоО2, совмещенных в одной частице дисперсной фазы, значение которого с увеличением размера частиц возрастает по кубической зависимости (табл. 1).
Таблица 1.
Общие характеристики частиц дисперсной фазы при Н2О = 2.33% (А = 6.49 ⋅ 104, В = 0.00856, C0 = 0.06706 г МоО2/100 г эмульсии, NΣ = 2.06944 ⋅ 1011)
| Диаметр частиц D, нм | Число частиц, ND (формула 8) |
Масса одной частицы ND, г (формула 5) | Число молекул MoO2 в одной частице, n (формула 9) | Масса всех частиц mΣ, г |
|---|---|---|---|---|
| 0.397* | 10194.100000 | 2.119700 ⋅ 10–22 | 1.000000 | 2.160840 ⋅ 10–18 |
| 1 | 64346.900000 | 3.387680 ⋅ 10–21 | 15.981900 | 2.179870 ⋅ 10–16 |
| 10 | 5.957570 ⋅ 106 | 3.387680 ⋅ 10–18 | 15981.9000 | 2.018230 ⋅ 10–11 |
| 20 | 2.187530 ⋅ 107 | 2.710150 ⋅ 10–17 | 1.278550 ⋅ 105 | 5.928530 ⋅ 10–10 |
| 30 | 4.518150 ⋅ 107 | 9.146750 ⋅ 10–17 | 4.315110 ⋅ 105 | 4.132640 ⋅ 109 |
| 40 | 7.373300 ⋅ 107 | 2.168120 ⋅ 10–16 | 1.022840 ⋅ 106 | 1.598620 ⋅ 10–8 |
| 50 | 1.057560 ⋅ 108 | 4.234600 ⋅ 10–16 | 1.997740 ⋅ 106 | 4.478340 ⋅ 10–8 |
| 60 | 1.397960 ⋅ 108 | 7.317400 ⋅ 10–16 | 3.452090 ⋅ 106 | 1.022940 ⋅ 10–7 |
| 70 | 1.746670 ⋅ 108 | 1.161980 ⋅ 10–15 | 5.481790 ⋅ 106 | 2.029600 ⋅ 10–7 |
| 80 | 2.094210 ⋅ 108 | 1.734500 ⋅ 10–15 | 8.182730 ⋅ 106 | 3.632410 ⋅ 10–7 |
| 90 | 2.433040 ⋅ 108 | 2.469620 ⋅ 10–15 | 1.165080 ⋅ 107 | 6.008680 ⋅ 10–7 |
| 100 | 2.757330 ⋅ 108 | 3.387680 ⋅ 10–15 | 1.598190 ⋅ 107 | 9.340950 ⋅ 10–7 |
| 200 | 4.685880 ⋅ 108 | 2.710150 ⋅ 10–14 | 1.278550 ⋅ 108 | 0.000013 |
| 300 | 4.479390 ⋅ 108 | 9.146750 ⋅ 10–14 | 4.315110 ⋅ 108 | 0.000041 |
| 400 | 3.383290 ⋅ 108 | 2.168120 ⋅ 10–14 | 1.022840 ⋅ 109 | 0.000073 |
| 500 | 2.245980 ⋅ 108 | 4.234600 ⋅ 10–13 | 1.997740 ⋅ 109 | 0.000095 |
| 600 | 1.374080 ⋅ 108 | 7.317400 ⋅ 10–13 | 3.452090 ⋅ 109 | 0.000101 |
| 700 | 7.945990 ⋅ 107 | 1.161980 ⋅ 10–12 | 5.481790 ⋅ 109 | 0.000092 |
| 800 | 4.409380 ⋅ 107 | 1.734500 ⋅ 10–12 | 8.182730 ⋅ 109 | 0.000076 |
| 900 | 2.370960 ⋅ 107 | 2.469620 ⋅ 10–12 | 1.165080 ⋅ 1010 | 0.000059 |
| 1000 | 1.243610 ⋅ 107 | 3.387680 ⋅ 10–12 | 1.598190 ⋅ 1010 | 0.000042 |
| 1100 | 6.393120 ⋅ 106 | 4.509000 ⋅ 10–12 | 2.127190 ⋅ 1010 | 0.000029 |
| 1200 | 3.232470 ⋅ 106 | 5.853920 ⋅ 10–12 | 2.761670 ⋅ 1010 | 0.000019 |
| 1300 | 1.611760 ⋅ 106 | 7.442730 ⋅ 10–12 | 3.511220 ⋅ 1010 | 0.000012 |
| 1400 | 7.941740 ⋅ 105 | 9.295800 ⋅ 10–12 | 4.385430 ⋅ 1010 | 0.000007 |
| 1500 | 3.873340 ⋅ 105 | 1.143340 ⋅ 10–11 | 5.393890 ⋅ 1010 | 0.000004 |
* Диаметр молекулы МоО2 [8].
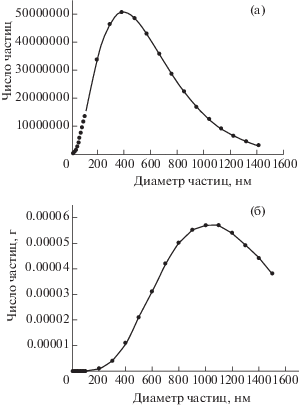
Для суспензии МоО2 в легком газойле, полученной из эмульсии с содержанием воды 0.94%, результаты расчетов представлены в табл. 2 и на рис. 4. В этом случае ${{N}_{\Sigma }}$ = 3.8321 ⋅ 1010, т.е. общее число частиц уменьшается в 5.4 раза по сравнению с первым. В остальном закономерности распределения частиц аналогичны полученным в первом случае.
Таблица 2.
Общие характеристики частиц дисперсной фазы при Н2О = 0.94% (А = 2.224 ⋅ 103, В = 0.004878, C0 = 0.06706 г МоО2/100 г эмульсии, ${{N}_{\Sigma }}$ = 3.8321 ⋅ 1010)
| Диаметр частиц D, нм | Число частиц, ND (формула 8) | Масса одной частицы ND, г (формула 5) | Число молекул MoO2 в одной частице, n (формула 9) | Масса всех частиц mΣ, г |
|---|---|---|---|---|
| 0.397 | 349.844000 | 2.119700 ⋅ 10–22 | 1.000000 | 7.415640 ⋅ 10–20 |
| 1 | 2213.18000 | 3.387680 ⋅ 10–21 | 15.981900 | 7.497550 ⋅ 10–18 |
| 10 | 2.118120 ⋅ 105 | 3.387680 ⋅ 10–18 | 15981.900 | 7.175510 ⋅ 10–13 |
| 20 | 8.069100 ⋅ 105 | 2.710150 ⋅ 10–17 | 1.278550 ⋅ 105 | 2.186850 ⋅ 10–11 |
| 30 | 1.729110 ⋅ 106 | 9.146750 ⋅ 10–17 | 4.315110 ⋅ 105 | 1.581570 ⋅ 10–10 |
| 40 | 2.927620 ⋅ 106 | 2.168120 ⋅ 10–16 | 1.022840 ⋅ 106 | 6.347430 ⋅ 10–10 |
| 50 | 4.356630 ⋅ 106 | 4.234600 ⋅ 10–16 | 1.997740 ⋅ 106 | 1.844860 ⋅ 10–9 |
| 60 | 5.974860 ⋅ 106 | 7.317400 ⋅ 10–16 | 3.452090 ⋅ 106 | 4.372040 ⋅ 10–9 |
| 70 | 7.745270 ⋅ 106 | 1.161980 ⋅ 10–15 | 5.481790 ⋅ 106 | 8.999850 ⋅ 10–9 |
| 80 | 9.634640 ⋅ 106 | 1.734500 ⋅ 10–15 | 8.182730 ⋅ 106 | 1.671130 ⋅ 10–8 |
| 90 | 1.161330 ⋅ 107 | 2.469620 ⋅ 10–15 | 1.165080 ⋅ 107 | 2.868040 ⋅ 10–8 |
| 100 | 1.365480 ⋅ 107 | 3.387680 ⋅ 10–15 | 1.598190 ⋅ 107 | 4.625810 ⋅ 10–8 |
| 200 | 3.353490 ⋅ 107 | 2.710150 ⋅ 10–14 | 1.278550 ⋅ 108 | 9.088460 ⋅ 10–7 |
| 300 | 4.632660 ⋅ 107 | 9.146750 ⋅ 10–14 | 4.315110 ⋅ 108 | 0.000004 |
| 400 | 5.056590 ⋅ 107 | 2.168120 ⋅ 10–13 | 1.022840 ⋅ 109 | 0.000011 |
| 500 | 4.850990 ⋅ 107 | 4.234600 ⋅ 10–13 | 1.997740 ⋅ 109 | 0.000021 |
| 600 | 4.288880 ⋅ 107 | 7.317400 ⋅ 10–13 | 3.452090 ⋅ 109 | 0.000031 |
| 700 | 3.584180 ⋅ 107 | 1.161980 ⋅ 10–12 | 5.481790 ⋅ 109 | 0.000042 |
| 800 | 2.874250 ⋅ 107 | 1.734500 ⋅ 10–12 | 8.182730 ⋅ 109 | 0.000050 |
| 900 | 2.233460 ⋅ 107 | 2.469620 ⋅ 10–12 | 1.165080 ⋅ 1010 | 0.000055 |
| 1000 | 1.692960 ⋅ 107 | 3.387680 ⋅ 10–12 | 1.598190 ⋅ 1010 | 0.000057 |
| 1100 | 1.257720 ⋅ 107 | 4.509000 ⋅ 10–12 | 2.127190 ⋅ 1010 | 0.000057 |
| 1200 | 9.189910 ⋅ 106 | 5.853920 ⋅ 10–12 | 2.761670 ⋅ 1010 | 0.000054 |
| 1300 | 6.621940 ⋅ 106 | 7.442730 ⋅ 10–12 | 3.511220 ⋅ 1010 | 0.000049 |
| 1400 | 4.715260 ⋅ 106 | 9.295800 ⋅ 10–12 | 4.385430 ⋅ 1010 | 0.000044 |
| 1500 | 3.323420 ⋅ 106 | 1.143340 ⋅ 10–11 | 5.393890 ⋅ 1010 | 0.000038 |
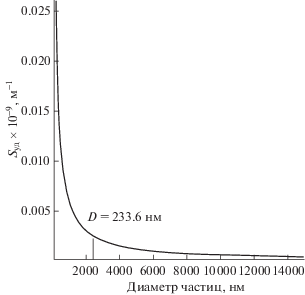
Аналитическая функция распределения частиц по размерам позволяет оценить важные физические характеристики частиц дисперсной фазы. На рис. 5 приведены значения удельной (межфазной) поверхности Sуд частиц дисперсной фазы, полученные при разных условиях
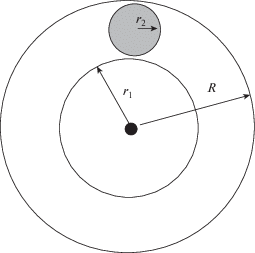
Одна из важнейших характеристик дисперсной фазы – доля молекул в поверхностном слое – необходима для оценки энергии сольватации частиц дисперсной фазы в различных средах и их устойчивости к агрегации. Модель поверхностного слоя представлена на рис. 6. Доля молекул слоя (указана черным кружком) N вокруг частицы дисперсной фазы с радиусом r будет равна отношениям объемов поверхностного слоя VС и дисперсной частицы VЧ. Согласно модели, N выражается через радиусы сфер
Согласно рис. 6, $R = {{r}_{1}} + 2{{r}_{2}}$, а следовательно, число частиц слоя N равно
Если ввести толщину поверхностного слоя $2{{r}_{2}}$ и размер частиц дисперсной фазы $D = 2{{r}_{1}}$, то можно вычислить доли молекул в поверхностном слое N.
Полученные результаты показывают, что предложенный способ построения аналитической функции распределения частиц дисперсной фазы по размерам может быть успешно применен для моделирования их физико-химических характеристик.
В заключение отметим, что предложенный метод определения зависимости числа частиц от диаметра частиц дисперсной фазы, достоверность которой контролируется расчетом распределения по массам, может быть использован как дополнительный параметр, характеризующий физико-химические свойства дисперсной системы. Он применим для анализа и других аналогичных спектров, полученных по методу динамического светорассеяния (DLS). Результаты математического моделирования могут быть использованы для исследования других свойств частиц дисперсной фазы, например для оценки динамической устойчивости дисперсной системы.
Список литературы
Bunin V. Experimental measurement of the average size and the axial ratio of suspended particles by electrooptical technique. Abstracts ELOPTO 2010, Mainz, Germany, 2010. 79 p.
Zakharov P., Scheffold F. Light Scattering Reviews 4. Springer Praxis Books, 2009. 433 p.
Redouane Borsali, Robert Pecora. Soft Matter Characterization Springer, 2008. 1445 p.
Chu B., LiuT. // J. Nanoparticle Res. 2000. V. 2. P. 29.
Зайденварг В.Е., Трубецкой К.Н., Мурко В.И., Нехороший И.Х. Производство и использование водоугольного топлива. М.: Академия горных наук, 2001. 172 с.
Хаджиев С.Н. // Наногетерогенный катализ. 2016. Т. 1. № 1. С. 3.
Кадиева М.Х., Хаджиев С.Н., Кадиев Х.М., Яковенко Т.В. Закономерности формирования наноразмерных частиц катализатора в жидких средах // Тез. III Рос. конф. “Актуальные проблемы нефтехимии”. 2009. С. 161.
Кадиева М.Х., Хаджиев С.Н., Кадиев Х.М., Гюльмалиев А.М., Яковенко Т.В. // Нефтехимия. 2011. Т. 51. № 1. С. 1.
Дополнительные материалы отсутствуют.
Инструменты
Химия твердого топлива