Кинетика и катализ, 2021, T. 62, № 6, стр. 791-802
Перспективные способы формирования “корочковых” катализаторов для окислительной десульфуризации
А. А. Брыжин a, Т. Н. Ростовщикова a, К. И. Маслаков a, И. В. Лукиянчук b, М. С. Васильева b, c, А. Ю. Устинов b, С. А. Гуревич d, Д. А. Явсин d, И. Г. Тарханова a, *
a Московский государственный университет им. М.В. Ломоносова, химический факультет
119991 Москва, Ленинские горы, 1/3, Россия
b Институт химии Дальневосточного отделения РАН
690022 Владивосток, просп. 100-летия Владивостока, 159, Россия
c Дальневосточный федеральный университет
690922 Приморский край, Владивосток, о. Русский, п. Аякс, 10, Россия
d Физико-технический институт им. А. Ф. Иоффе РАН
194021 Санкт-Петербург, Политехническая ул., 26, Россия
* E-mail: itar_msu@mail.ru
Поступила в редакцию 15.06.2021
После доработки 31.07.2021
Принята к публикации 31.07.2021
Аннотация
Исследованы каталитические свойства W- и NiW-слоистых структур, полученных методами
лазерного диспергирования (ЛЭД) и плазменно-электролитического оксидирования (ПЭО),
в реакциях окислительной десульфуризации. Проведен сравнительный анализ влияния состава,
концентрации активной фазы и структуры композитов в модельных реакциях окисления тиофена
(Т), дибензотиофена (ДБТ), метилфенилсульфида (МФС) пероксидом водорода, а также удаления
серы из дизельной фракции нефтяного сырья. В обоих случаях введение никеля в состав
W-содержащих композитов повышает их активность и устойчивость к вымыванию и травлению
продуктами реакции. Установлено, что ряды активности в отношении сероорганических
субстратов отличаются для катализаторов NiW-ЛЭД (ДБТ > Т > МФС) и NiW-ПЭО (МФС > ДБТ
> Т). Катализатор NiW-ПЭО позволяет очистить дизельную фракцию от серы на 98%.
Графический
реферат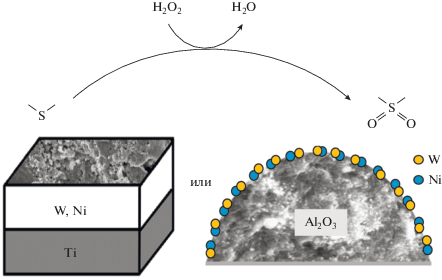
ВВЕДЕНИЕ
Использование новых подходов к синтезу гетерогенных катализаторов открывает возможности создания уникальных материалов с необычными свойствами. Особый интерес представляет направленный дизайн сложных многокомпонентных композиций, в которых важную роль играют коллективные взаимодействия в системе оксидов и металлических частиц, объединенных в единый каталитический центр, доступный для субстратов. Существующие методы получения моно- и биметаллических композиций нуждаются в разработке способов формирования оксидных или металлических слоев, равномерно распределенных на поверхности носителей различной природы, причем для ряда каталитических процессов с участием объемных субстратов важно, чтобы такие слои находились именно на внешней поверхности. В связи с этим развиваются современные методы синтеза молекулярно-организованных поверхностных структур на основе металлов и их оксидов, обладающих высокой эффективностью в катализе, а также химической и термической устойчивостью. Указанным требованиям, в частности, отвечает метод плазменно-электролитического оксидирования (ПЭО), позволяющий формировать оксидные покрытия на поверхностях металлов или сплавов в условиях действия электрических искровых и/или дуговых разрядов на границе раздела между электролитом и растущей оксидной фазой [1–3]. Этот метод, широко применяемый для создания антикоррозионных покрытий, лишь в последние годы стал использоваться для формирования катализаторов, при этом условия синтеза позволяет регулировать структуру и эффективность каталитических систем [4, 5]. Такие композиции уже зарекомендовали себя как перспективные катализаторы ряда процессов [6–8].
Еще одним способом формирования “корочковых” катализаторов с высокой доступностью активных компонентов является метод лазерного электродиспергирования (ЛЭД) [9]. Его основное отличие от традиционных методов лазерной абляции [10] состоит в том, что используются условия формирования монодисперсных наночастиц из капель расплавленного материала мишени, а не из атомов металлов. Уникальность этого метода заключается в возможности создавать покрытия с высокой степенью заполнения внешней поверхности носителя отдельными наночастицами металлов или их ансамблями. На модельных катализаторах, приготовленных этим методом, для реакций разных типов авторами показано, что оптимальная организация наночастиц и рациональный выбор носителя на порядки повышают эффективность катализаторов при низком содержании металла [11]. Анализируя достоинства двух указанных методов можно сказать, что они позволяют создавать “корочковые” катализаторы, при этом ПЭО дает возможность формировать на металлах и сплавах гетерогенные микро- и наноструктурированные оксидные слои с заданным набором оксидов, а ЛЭД – диспергировать на поверхность носителя наноразмерные пленки и ансамбли наночастиц нужных металлов и сплавов. Степень взаимодействия металла с носителем и, соответственно, его электронное состояние зависят от степени заполнения поверхности [12–15].
В настоящей работе сопоставлены возможности применения указанных методов для создания ряда многокомпонентных каталитических систем окислительной десульфуризации. Актуальность этого направления обусловлена тем, что в последние годы наблюдается тенденция к увеличению содержания гетероатомов, в частности, серы, в добываемом углеводородном сырье. Наряду с совершенствованием традиционных водородных методов удаления серосодержащих соединений, интенсивно идут разработки альтернативных процессов. Среди них наибольшее распространение получил метод окислительной десульфуризации, который, в отличие от гидроочистки, позволяет вести процесс в относительно мягких условиях. К его достоинствам можно отнести также отсутствие давления водорода, что особенно важно для малотоннажных нефтеперерабатывающих предприятий, где нет возможности применения сложного оборудования гидроочистки [16, 17].
В качестве модельных каталитических систем для проведения сравнительных испытаний выбраны WNi-композиции (рис. 1).
Комбинация этих металлов или их оксидов обеспечивает формирование на поверхности носителей как центров адсорбции серосодержащих субстратов, так и необходимых окислительных центров. Из литературы известны адсорбционные свойства Ni-содержащих композиций в десульфуризации [18, 19]. Центрами окисления могут выступать пероксокомплексы, образование которых хорошо известно для металлов V–VI групп, в том числе и вольфрама, при использовании пероксида водорода в качестве окислителя [20].
Таким образом, целью работы является сравнительный анализ каталитического действия WNi-систем, полученных двумя способами (ПЭО и ЛЭД) в окислении ряда серосодержащих соединений пероксидом водорода. В качестве субстратов применяли дибензотиофен и метилфенилсульфид, поскольку эти соединения моделируют серосодержащие соединения дизельного топлива, а кроме того, тиофен – наиболее трудноокислямый представитель ряда гетероароматических производных серы [20]. Также сопоставлены возможности каталитических систем двух типов на примере удаления серы из дизельной фракции нефтяного сырья.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Формирование и исследование ПЭО-композитов
W- и NiW-содержащие оксидные слои формировали методом ПЭО в гальваностатическом режиме при плотности тока i = 0.2 А/см2 в течение t = 10 мин на титане. Для получения W-композитов применяли электролит состава 0.1 моль/л Na2WO4 + 0.1 моль/л CH3COOH, NiW-композиты формировали в электролите, состава 0.1 моль/л Na2WO4 + 0.1 моль/л CH3COOH + 0.05 моль/л Ni(CH3COO)2, аналогично [21]. В качестве подложки использовали плоские образцы титана ВТ1-0 размером 2 × 2 × 0.03 см. Для стандартизации поверхности и удаления естественной оксидной пленки с поверхности титана образцы предварительно полировали в смеси плавиковой и азотной кислот HF : HNO3 = 1 : 3 (по объему) при 70°С, затем промывали дистиллированной водой и сушили на воздухе.
Толщину ПЭО-покрытий находили с помощью вихретокового толщиномера ВТ‑201 (НТЦ “Эксперт”, Россия) и рассчитывали как среднее значение не менее 10 отдельных измерений с обеих сторон плоского образца.
Фазовый состав образцов с ПЭО-покрытиями изучали на дифрактометре D8 ADVANCE (“Bruker”, Германия) в CuKα-излучении. При анализе рентгенограмм использовали программу поиска EVA с банком данных PDF-2 (Powder Diffraction File; Kabekkodu, 2007). Морфологию поверхности и элементный состав анализировали с помощью сканирующего электронного микроскопа высокого разрешения Hitachi S5500 (“Hitachi”, Япония), оснащенного приставкой Thermo Scientific EDX (“Thermo Fisher Scientific”, США) для проведения энергодисперсионного анализа. Глубина проникновения сканирующего луча составляла ~1 мкм.
Данные о составе поверхностного слоя катализаторов толщиной ~3 нм получали с помощью рентгеновской фотоэлектронной спектроскопии (РФЭС). Рентгеновские фотоэлектронные спектры (РФЭ-спектры) ПЭО-катализаторов регистрировали на спектрометре Specs (Германия) с использованием немонохроматического MgKα-излучения. Спектры записывали с шагом 0.1 эВ при энергии пропускания анализатора 50 эВ. Для изучения распределения элементов по глубине образца верхний слой травили сканирующим пучком ионов Ar+ с энергией 5 кэВ в течении 5 мин, что соответствовало удалению слоя толщиной ~3 нм.
Получение и исследование ЛЭД-катализаторов
Синтез WNi-катализаторов методом ЛЭД подробно описан нами в работах [11, 22]. Для формирования биметаллических катализаторов применяли мишени из смеси Ni и W с мольным соотношением компонентов 1 : 1, приготовленные холодным прессованием порошков металлов с размером зерен 3–8 мкм. Монометаллические W-образцы сравнения получали лазерным электродиспергированием металлической мишени. В качестве носителя использовали γ-Al2O3 АОК-63-11, марка “В” (Sуд = 180 м2/г, Vпор = 0.55 см3/г, размер гранул 0.4–1.0 мм).
Содержание металлов в катализаторе находили на основании калибровочных зависимостей скорости роста осажденных пленок, определенных предварительно с помощью кварцевого измерителя толщины пленок SCT-2000A (“Sycon Instruments”, США): для вольфрама в моно- и биметаллическом образцах эта величина составляла 5 × 10–3 мас. %, Ni – 2 × 10–3 мас. %.
Текстурные характеристики образцов определяли методом адсорбции и десорбции азота на приборе Autosorb 1 (“Quantachrome”, США) после предварительного вакуумирования в течение 3 ч при 300°С.
Микрофотографии поверхности образцов получали методом сканирующей электронной микроскопии (СЭМ) на приборе JSM 6000 NeoScope (“JEOL”, Япония). Качественный анализ поверхности проводили с помощью энергодисперсионного анализа (ЭДА) на приборе JED-2300 (“JEOL”, Япония) in situ.
РФЭ-спектры ЛЭД-катализаторов регистрировали на спектрометре Axis Ultra DLD (“Kratos Analytical”, Великобритания) с применением монохроматического AlKα-излучения при энергии пропускания 40 эВ и шаге 0.1 эВ. Калибровку РФЭ-спектров ПЭО- и ЛЭД-катализаторов для устранения зарядки осуществляли по спектрам C1s адсорбированных углеводородов, положение максимума которых было принято равным 285.0 эВ. При обработке и интерпретации спектров использовали данные из работ [23, 24].
Каталитические испытания
Для проведения каталитических тестов в термостатированный реактор помещали 10 мл модельной смеси, содержащей 1 мас. % тиофена (Т), дибензотиофена (ДБТ) или метилфенилсульфида (МФС) в изооктане, 0.1 г катализатора и 0.4 мл 50% водного раствора H2O2. Таким образом, мольное соотношение пероксид водорода : субстрат составляло от 6 до 10. Окисление сероорганических субстратов выполняли при оптимальной температуре (60°С), установленной в ряде работ [25, 26]. Содержимое реактора перемешивали при 60°С в течение 4 ч, периодически отбирая пробы органической фазы для анализа методом газожидкостной хроматографии на приборе Кристалл 4000 (“Мета-хром”, Россия) с капиллярной колонкой Zebron ZB-1 длиной l = 30 м и жидкой фазой 100% диметилполисилоксан, пламенно-ионизационный детектор. Содержание субстратов определяли в режиме линейного программирования при температурах 90–250°С с применением внутреннего стандарта (нонана или додекана). После окончания реакции жидкую фазу декантировали, катализатор промывали изооктаном. Далее в реактор помещали новую порцию реагентов и испытания проводили аналогичным образом в течение 5 циклов. При дробной загрузке пероксида водорода окислитель добавляли по 0.2 мл через 2 ч.
Для окислительного обессеривания дизельного топлива производства ОАО “Варьеганнефть” (20 мл, общее содержание серы – 1080 ppm) использовали катализатор (0.04 г) и H2O2 50% (0.4 мл), которые помещали в стеклянный реактор и термостатировали при 60°С и интенсивном перемешивании в течение 4 ч. Смесь охлаждали до комнатной температуры и промывали 5 мл диметилформамида в делительной воронке. ДМФА применяли как наиболее эффективный экстрагент для удаления продуктов окисления сероорганических компонентов дизельного топлива [27]. Затем топливо помещали в реактор, добавляли свежую порцию окислителя (0.4 мл) и отработанный катализатор, промытый изооктаном. Смесь перемешивали еще 4 ч при 60°С и повторяли процедуру экстракции продуктов окисления. Остаточное содержание серы определяли на рентгеновском флуоресцентном спектрометре AСЭ-2 (НПП “Буревестник”, Россия) (предел погрешности измерения ±0.5%).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Характеристики катализаторов
СЭМ-изображения поверхности NiW-катализаторов, полученных двумя методами, показаны на рис. 2. В условиях ПЭО под действием электрических разрядов на титане образуются плотные оксидные слои, пронизанные порами размерами от 1 до 10 мкм. При этом плотность пор для W-образца выше, чем для NiW. Отметим, что удельная поверхность ПЭО-покрытий невелика и равна 4 м2/г, а пористость обычно составляет около 20%. Полагают, что поры – следы каналов электрических разрядов или выхода газовых пузырей [28]. Толщины W- и NiW-покрытий составляют 14 ± 2 и 12±2 мкм соответственно.
Рис. 2.
СЭМ-изображения и спектры ЭДА поверхности биметаллических катализаторов NiW-ЛЭД (а) и NiW-ПЭО (б).

По данным энергодисперсионного анализа для для образца NiW-ПЭО внешний слой толщиной ~1 мкм содержит металлы в мольном соотношении около 1 : 5, т.е. обогащен вольфрамом (отношение металлов в исходных растворах электролитов было 1 : 2). Это обусловлено особенностями электролитического процесса: большее количество вольфрама по сравнению с никелем связано с тем, что вольфрам в электролите находится в составе аниона, в то время как никель – в составе катиона, поэтому в прианодном слое концентрация вольфрамат-ионов больше. Для образца W-ПЭО содержание металла в покрытии около 25 ат. %, в пересчете на весь образец это составляет 7 мас. %. Для NiW-ПЭО концентрация Ni в покрытии – 4.3 ат. %, W – 23 ат. %, что соответствует общему количеству металлов в образце 0.3 и 5.6 мас. % соответственно. Кроме того, в состав покрытий входит Ti (7–8 ат. %).
По данным РФА [21] в составе W-образцов присутствует кристаллический WO3, в то время как NiW-образцы рентгеноаморфны.
Текстурные характеристики катализаторов W- и NiW-ЛЭД мало отличаются от исходного носителя. По данным адсорбционных измерений удельная поверхность катализаторов равна 178–180 м2/г. Это связано с низкой концентрацией и высокой дисперсностью металлов в образцах. Энергодисперсионный анализ образца NiW-ЛЭД показал, что мольное соотношение металлов близко к 1, что полностью соответствует условиям синтеза.
Наиболее информативным методом для исследования образцов ЛЭД с низким содержанием металлов (10–3 мас. %) является РФЭС, поскольку активные компоненты расположены на поверхности носителя во внешнем слое толщиной несколько нм и доступны для анализа (табл. 1 и рис. 3). Важно отметить, что не удается зафиксировать сигналы металлических компонент при измельчении гранул катализатора. В табл. 1 сопоставлены параметры РФЭ-спектров образцов ЛЭД и ПЭО.
Таблица 1.
Содержание компонент никеля и вольфрама в моно- и биметаллических образцах и соответствующие им значения энергии связи по данным РФЭС
| Катализатор | Содержание компонент металлов, ат. % | |||||
|---|---|---|---|---|---|---|
| Ni0 (852.6 эВ) |
Ni2+ (855.9 эВ) |
W0 (31.1 эВ) |
W4+ (33.6 эВ) |
W6+ (35.5 эВ) |
||
| W-ПЭО | поверхностный слой | –* | –* | –** | –** | 100 |
| приповерхностный слой | –* | –* | 1 | 33 | 66 | |
| W-ЛЭД | –* | –* | 1 | 20 | 79 | |
| NiW-ПЭО | поверхностный слой | 19 | 81 | 2 | 15 | 83 |
| приповерхностный слой | 79 | 21 | 3 | 28 | 69 | |
| NiW-ЛЭД | 31 | 69 | 32 | 7 | 61 | |
Рис. 3.
РФЭ-спектры W4f (а, в) и Ni2p (б) для моно- (в) и биметаллических (а, б) катализаторов, полученных методами ЛЭД и ПЭО.

Как видно из параметров РФЭ-спектров, в монометаллических образцах, полученных двумя методами, вольфрам присутствует преимущественно в высокоокисленном состоянии, соотношения W6+/W4+ на поверхности образца ЛЭД и в приповерхностном слое ПЭО-покрытия достаточно близки. В отличие от этого в двойной ЛЭД-системе на поверхности металлы находятся как в окисленном, так и металлическом состояниях. Сохранение металлов в восстановленной форме именно в биметаллическом покрытии свидетельствует о возможности взаимодействия двух металлов в ходе синтеза с образованием устойчивых к окислению интерметаллидов [29]. Их появление становится весьма вероятным при высоких температурах процесса лазерной абляции. Одновременное присутствие металлов в нескольких степенях окисления может положительно влиять на каталитические свойства образцов [30].
В случае ПЭО-образцов мы не наблюдали образования металлического вольфрама, хотя после травления ионами аргона в составе приповерхностных слоев ПЭО-покрытий обнаруживаются частично восстановленные формы никеля и вольфрама. Наличие металлов в более низких степенях окисления по сравнению с прекурсорами, вводимыми в раствор, фиксировали в составе ПЭО-слоев и другие авторы. В частности, в составе вольфраматных ПЭО-покрытий на алюминии и магнии авторы работы [31, 32] обнаружили металлический вольфрам. Восстановление металлов в процессе ПЭО может происходить под действием водорода, выделяющегося на аноде в результате термического разложения воды [33–35]. В то же время нельзя исключить частичного восстановления металлов при воздействии высокоэнергетических ионов аргона.
Сравнение каталитических свойств ЛЭД- и ПЭО-образцов
Каталитические свойства образцов сопоставлены на примере трех серосодержащих модельных соединений, прежде всего – тиофена. Интерес к этому субстрату, кроме устойчивости к окислению, вызван тем, что продуктом его превращения является серная кислота – это известно из литературы, в том числе, показано нами в [8, 36]. На рис. 4 представлены зависимости конверсии тиофена от времени в окислении пероксидом водорода на моно- и биметаллических катализаторах двух типов. В присутствии W-ЛЭД конверсия исследуемого субстрата составила 30%, а в присутствии W-ПЭО, несмотря на большее содержание в нем металла – не более 20%. Биметаллические катализаторы двух типов оказались более эффективными по сравнению с монометаллическими, максимальная конверсия субстрата (43% за 4 ч) достигнута на образце NiW-ЛЭД. Ранее нами было установлено, что монометаллический Ni-катализатор, приготовленный методом ЛЭД в аналогичных условиях и включающий только оксид никеля, в выбранных условиях катализа неактивен [11]. Также из литературы следует, что по активности в окислительной десульфуризации катализаторы на основе Ni значительно уступают металлам V–VI групп [20]. Скорее всего, роль Ni заключается в промотировании каталитического действия W. Такой эффект, вероятно, связан тем, что частицы никеля служат центрами хемосорбции тиофена, причем есть данные о значительно более сильной адсорбции на Ni0 по сравнению с NiO [37, 38]. Кроме того, как показано выше, присутствие Ni влияет на электронное состояние вольфрама. Появление частично или полностью восстановленных форм W4+ и W0 может способствовать более эффективному протеканию стадий переноса электрона в каталитическом окислении тиофена.
Рис. 4.
Зависимость конверсии тиофена (1 мас. % в изооктане) от времени на моно- и биметаллических катализаторах, полученных методами ПЭО и ЛЭД. Условия реакции: 60°С, 0.1 г катализатора, однократная загрузка 0.4 мл H2O2, 4 ч.

При окислении тиофена важной характеристикой катализаторов является их стабильность, поскольку образующаяся серная кислота способна разрушать металлическое покрытие катализаторов. В табл. 2 приведены сравнительные результаты испытаний образцов в течение 5 последовательных каталитических циклов. Как видно из табл. 2, монометаллические катализаторы, полученные разными методами, менее стабильны, чем биметаллические, причем образец W-ЛЭД-полностью дезактивируется за время испытаний. Таким образом, введение Ni в состав катализаторов не только увеличивает активность образцов, но и повышает их стабильность. Длительное сохранение каталитических свойств образцов ЛЭД может быть обусловлено наличием устойчивого к вымыванию биметаллического “корочкого” покрытия, включающего металлические частицы. Катализаторы ПЭО также оказались стабильными, наибольшую устойчивость показал образец, содержащий смешанные оксидные Ni–W-слои.
Таблица 2.
Конверсия тиофена в пяти последовательных циклах окисления на разных катализаторах*
| Образец | Конверсия тиофена в цикле, % | ||||
|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | |
| W-ЛЭД | 30 | 27 | 21 | 15 | 0 |
| W-ПЭО | 20 | 21 | 19 | 17 | 15 |
| NiW-ЛЭД | 43 | 42 | 43 | 41 | 42 |
| NiW-ПЭО | 31 | 30 | 30 | 29 | 27 |
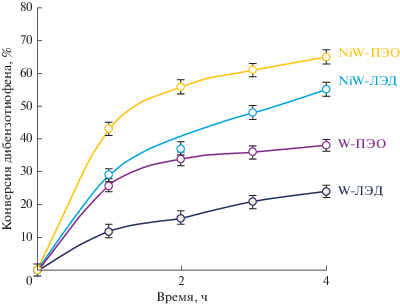
Активность катализаторов в окислении дибензотиофена иллюстрирует рис. 5. Как видно из представленных зависимостей, конверсия оказалась выше для биметаллического образца, приготовленного методом ПЭО. Основным продуктом окисления ДБТ в присутствии катализаторов обоих типов является соответствующий сульфон.
Рис. 5.
Зависимость конверсии ДБТ (1 мас. % в изооктане) от времени на моно- и биметаллических катализаторах, полученных методами ПЭО и ЛЭД. Условия реакции: 60°С, 10 мл модельного раствора, 0.4 мл 50% H2O2, 0.1 г катализатора, 4 ч.
Результаты испытаний катализаторов в окислении МФС приведены на рис. 6. Оказалось, что катализатор NiW-ЛЭД практически неактивен в этом процессе. При этом конверсия МФС с образованием сульфона на образце NiW-ПЭО достигала 100% за 1.5 ч. Такой ряд активности (МФС $ \gg $ ДБТ $ \gg $ Т), полученный из сравнения данных рис. 4–6 для катализаторов NiW-ПЭО, полностью соответствует известному из литературы ряду активности W-содержащих систем в отношении сероорганических субстратов. Он определяется различиями в величине электронной плотности на атоме серы, обуславливающими их реакционную способность в нуклеофильном механизме окисления: в указанном ряду она составляет 5.92, 5.76 и 5.69 соответственно [39, 40]. Аналогичный ряд реакционной способности субстратов мы наблюдали ранее при анализе WZn-катализаторов, полученных методом ПЭО [41].
Рис. 6.
Конверсия тиоанизола (1 мас. % в изооктане) от времени на моно- и биметаллических катализаторах, полученных методами ПЭО и ЛЭД. Условия процесса: 60°, 10 мл модельного раствора, 0.4 мл 50% H2O2, 0.1 г катализатора, 1.5 ч.

Изменение реакционной способности субстратов на биметаллическом образце ЛЭД может быть связано с особенностями протекания процесса на катализаторах с ультранизким содержанием активной фазы, включающей в свой состав металлы, имеющие разные функции – адсорбционную и окислительную. По-видимому, в этих условиях адсорбция начинает играть ключевую роль, при этом селективность Ni-содержащих адсорбентов зависит от природы субстрата. Вероятно, МФС, обладающий наибольшей электронной плотностью на атоме серы, более прочно, чем тиофеновые производные, адсорбируется на никеле и не участвует в последующей окислительной реакции. Согласно литературным данным прочная хемосорбция производных серы на никелевых адсорбентах при определенных условиях приводит даже к образованию сульфидов металла [42]. В результате такой фактор, как электрофильность субстрата, в данном случае играет отрицательную роль, что приводит к изменению ряда реакционной способности серосодержащих соединений на биметаллическом катализаторе ЛЭД.
Заметное уменьшение скорости окисления от времени, наиболее ярко проявляющееся для катализаторов W-ПЭО (рис. 5), принято связывать с разложением пероксида водорода. Повысить эффективность процесса позволяет хорошо известный из литературы и опробованный нами ранее способ дробной загрузки окислителя в подобных процессах [43, 44]. Результаты испытаний катализаторов в условиях разной загрузки приведены в табл. 3.
Таблица 3.
Влияние способа загрузки H2O2 на конверсию серосодержащих соединений*
| Катализатор | Степень удаления серы, % | |||||
|---|---|---|---|---|---|---|
| однократная загрузка 0.4 мл H2O2 | дробная загрузка 0.2 + 0.2 мл H2O2 | |||||
| субстрат | субстрат | |||||
| тиофен | ДБТ | МФС | тиофен | ДБТ | МФС | |
| WNi-ПЭО | 31 | 65 | 100 | 45 | 78 | 100 |
| WNi-ЛЭД | 43 | 55 | 10 | 49 | 59 | – |
Как видно из табл. 3, дробная загрузка окислителя оказывает большее влияние на катализатор ПЭО, позволяя увеличить конверсию субстратов на 20–50%, в то время как в случае катализатора ЛЭД этот прием не позволил увеличить степень удаления серы более чем на 10%. Такой эффект в последнем случае мы связываем с низким содержанием металлсодержащих активных центров, ответственных за разложение пероксида водорода. Это предположение подтверждает анализ кривых конверсии субстратов, в особенности ДБТ. Как хорошо видно из рис. 5, характер зависимостей для катализаторов ЛЭД и ПЭО различен. Кривые конверсии на катализаторах ЛЭД в большей степени соответствуют экспоненциальной зависимости, характерной для реакции первого порядка по серосодержащему субстрату [45]. Дробная загрузка окислителя дает возможность повысить эффективность процесса на катализаторах ПЭО с высоким содержанием металлов и тем самым уменьшить негативные эффекты, связанные с разложением пероксида водорода.
Анализ закономерностей процессов с участием биметаллических образцов ПЭО и ЛЭД позволил заключить, что катализаторы ПЭО, в отличие от образцов ЛЭД, более активны в окислении серосодержащих компонентов дизельного топлива – ДБТ и МФС. Как видно из табл. 4, где представлены результаты испытаний катализаторов по сероочистке контрольного образца дизельной фракции нефтяного сырья, наибольшая степень удаления серы достигается именно при использовании WNi-ПЭО. В его присутствии остаточное содержание серы удалось снизить до 24 ppm, что весьма близко к тому, чего требуют современные экологические стандарты. Это согласуется с обнаруженными в работе особенностями протекания процессов для субстратов разной природы на катализаторах ПЭО и ЛЭД и обусловлено разными вкладами адсорбционных и каталитических стадий процесса.
ЗАКЛЮЧЕНИЕ
Таким образом, в работе исследованы катализаторы на основе комбинации двух металлов – никеля и вольфрама – в окислительной десульфуризации нефтяного сырья. Образцы получены с использованием двух разных методов, однако обладают важной общей характеристикой: активная фаза в обоих случаях располагается преимущественно на внешней поверхности, что дает возможность говорить о “корочковой” структуре этих систем. Хотя исходно катализаторы синтезированы из разных прекурсоров (чистых металлов и их солей), они содержат широкий набор валентных состояний металлов, причем присутствие никеля влияет на соотношение форм вольфрама в разных степенях окисления. Существенным различием двух типов катализаторов является содержание в них металлов, а также текстурные характеристики образцов – удельная поверхность и пористость. В образцах ЛЭД активные компоненты распределены по внешней поверхности носителя даже при сверхнизком содержании металлов (10–3 мас. %). В покрытиях ПЭО такие центры формируются во внешнем оксидном слое, обладающем высокой пористостью. Ультранизкое содержание металлов в катализаторах ЛЭД не меняет характеристики носителя, в данном случае, оксида алюминия, в то время как удельная поверхность образцов ПЭО составляет лишь несколько м2/г. При этом оксидное покрытие является широкопористым, что делает его весьма привлекательным для проведения каталитических процессов в мультифазных системах с участием объемных субстратов. Совокупность указанных сходств и различий влияет на каталитические свойства двух типов катализаторов. Прежде всего это касается порядка реакционной способности субстратов и влияния на протекание побочной реакции разложения пероксида водорода. Кроме того, важной характеристикой обоих типов катализаторов является их устойчивость к вымыванию и травлению продуктами реакции, причем присутствие двух металлов или их оксидов в композиции способствует повышению устойчивости.
Список литературы
Kaseem M., Fatimah S., Nashrah N., Ko Y.G. // Prog. Mater. Sci. 2021. V. 117. P. 100735. https://doi.org/. pmatsci.2020.100735.https://doi.org/10.1016/j
Simchen F., Sieber M., Kopp A., Lampke T. // Coatings. 2020. V. 10. № 7. P. 628. https://doi.org/10.3390/coatings10070628
Clyne T.W., Troughton S.C. // Int. Mater. Rev. 2019. V.64. № 3. P. 127. https://doi.org/10.1080/09506608.2018.1466492
Patcas F., Krysmann W. // Appl. Catal. A: Gen. 2007. V. 316. № 2. P. 240. https://doi.org/10.1016/j.apcata.2006.09.028
Lukiyanchuk I.V., Rudnev V.S., Tyrina L.M. // Surf. Coat. Technol. 2016. V. 307. P. 1183. https://doi.org/10.1016/j.surfcoat.2016.06.076
Petrovic S., Stojadinovic S., Rozic L., Radic N., Grbic B., Vasilic R. // Surf. Coat. Technol. 2015. V. 269. P. 250. https://doi.org/10.1016/j.surfcoat.2014.12.026
Васильева М.С., Руднев В.С., Тулуш А.И., Недозоров П.М., Устинов А.Ю. // Журн. физ. химии. 2015. Т. 89. № 6. С. 938. https://doi.org/10.7868/S0044453715060321
Rudnev V.S., Lukiyanchuk I.V., Vasilyeva M.S., Morozova V.P., Zelikman V.M., Tarkhanova I.G. // Appl. Surf. Sci. 2017. V. 422. P. 1007. https://doi.org/10.1016/j.apsusc.2017.06.071
Rostovshchikova T.N., Lokteva E.S., Golubina E.V., Maslakov K.I., Gurevich S.A., Yavsin D.A., Kozhevin V.M. / Advanced Size-Selected Catalysts Prepared by Laser Electrodispersion, Advanced Nanomaterials for Catalysis and Energy: synthesis, characterization and application. Ed. V. Sadykov. Elsevier Inc. 2019. P. 61.
Zhang J., Chaker M., Ma D. // J. Colloid Interface Sci. 2017. V. 489. P. 138. https://doi.org/10.1016/j.jcis.2016.07.050
Bryzhin A., Golubina E., Maslakov K., Lokteva E., Tarkhanova I., Gurevich S., Yavsin D., Rostovshchikova T.N. // ChemCatChem. 2020. V. 12. P. 4396. https://doi.org/10.1002/cctc.202000501
Golubina E.V., Rostovshchikova T.N., Lokteva E.S., Maslakov K.I., Nikolaev S.A., Shilina M.I., Gurevich S.A., Kozhevin V.M., Yavsin D.A., Slavinskaya E.M. // Appl. Surf. Sci 2021. V. 536. P. 147656. https://doi.org/10.1016/j.apsusc.2020.147656
Голубина Е.В., Локтева Е.С., Маслаков К.И., Ростовщикова Т.Н., Шилина М.И., Гуревич С.А., Кожевин В.М., Явсин Д.Ф. // Российские нанотехнологии. 2017. Т. 12. № 1–2. С. 16. https://doi.org/10.1134/S1995078017010049
Ильющенков Д.С., Кожевин В.М., Гуревич С.А. // Физика твердого тела. 2015. V. 57. № 9. P. 1670.
Ильющенков Д.С., Кожевин В.М., Гуревич С.А. // Физика твердого тела. 2019. Т. 61. № 10. С. 1731.
Houda S., Lancelot C., Blanchard P., Poinel L., Lamonier C. // Catalysts. 2018. V. 8. № 9. P. 344.
Rajendran A., Cui T., Fan H., Yang Z., Feng J., Li W. // J. Mater. Chem. A. 2020. V. 8. № 5. P. 2246.
Park J.G., Ko C.H., Yi K.B., Park J.H., Han S.S., Cho S.H., Kim J.N. // Appl. Catal. B: Environ. 2008. V. 81. № 3–4. P. 244.
Ma X., Sprague M., Song C. // Ind. Eng. Chem. Res. 2005. V. 44. № 15. P. 5768.
Ismagilov Z., Yashnik S., Kerzhentsev M., Parmon V., Bourane A., Al-Shahrani F.M., Hajji A.A., Koseoglu O.R. // Catal. Rev. 2011. V. 53 P. 199. https://doi.org/10.1080/01614940.2011.596426
Руднев В.С., Лукиянчук И.В., Черных И.В., Васильева М.С. // Физикохимия поверхности и защита материалов. 2020. Т. 56. № 6. С. 651.
Ростовщикова Т.Н., Локтева Е.С., Шилина М.И., Голубина Е.В., Маслаков К.И., Кротова И.Н., Брыжин А.А., Тарханова И.Г., Удалова О.В., Кожевин В.М., Явсин Д.А., Гуревич С.А. // Журн. физ. химии. 2021. Т. 95. № 3. С. 348.
Moulder J.F., Stickle W.F., Sobol P.E., Bomben K.D. Handbook of X-ray Photoelectron Spectroscopy. Chigasaki: ULVAC-PHI, Inc., 1995. 261 p.
Mansour A.N. // Surf. Sci. Spectra. 1994. V. 3. № 3. P. 231.
Craven M., Xiao D., Kunstmann-Olsen C., Kozhevni-kova E.F., Blanc F., Steiner A., Kozhevnikov I. V. // Appl. Catal. B: Environ. 2018. V. 231. P. 82.
Gao H., Wu X., Sun D., Niu G., Guan J., Meng X., Liu C., Xia W., Song X. // Dalton Transactions. 2019. V. 48. № 17. P. 5749.
García-Gutiérrez J.L., Fuentes G.A., Hernández-Terán M.E., García P., Murrieta-Guevara F., Jiménez-Cruz F. // Appl. Catal. A: General. 2008. V. 334. № 1–2. P. 366.
Curran J.A., Clyne T.W. // Acta Mater. 2006. V. 54. № 7. P. 1985. https://doi.org/10.1016/j.actamat.2005.12.029
Krstajic N.V., Jovic V.D., Gajic-Krstajic Lj., Jovic B.M., Antozzi A.L., Martelli G.N. // Inter. J. Hydrogen Energy. 2008. V. 33. № 4. P. 3676.
Тарханова И.Г., Анисимов А.В., Вержичинская С.В., Буряк А.К., Зеликман В.М., Гантман М.Г. // Нефтехимия. 2016. Т. 56. № 2. С. 178.
Zhu Z.D., Tu W.B., Cheng Y.L., Cheng Y.L. // Surf. Coat. Technol. 2019. V. 361. P. 176. https://doi.org/10.1016/j.surfcoat.2019.01.024
Tu W.B., Cheng Y.L., Wang X.Y., Zhan T.Y., Han J.X., Cheng Y.L. // J. Alloy. Compd. 2017. V. 725. P. 199. https://doi.org/10.1016/j.jallcom.2017.07.117
Snezhko L.A., Erokhin A.L., Kalinichenko O.A., Misnyankin D.A. // Mater. Sci. 2016. V. 52. № 3. P. 421. https://doi.org/10.1007/s11003-016-9974-5
Снежко Л.А. // Физикохимия поверхности и защита материалов. 2014. Т. 50. № 6. С. 705. https://doi.org/10.7868/S0044185614060217
Wei K.J., Zhang Y.F., Yu J.H., Liu R.H., Du J.C., Jiang F.B., Xue W.B. // Mater. Chem. Phys. 2020. V. 251. P. 123054. https://doi.org/10.1016/j.matchemphys.2020.123054
Брыжин А.А., Тархановa И.Г., Маслаков К.И., Николаев С.А., Гуревич С.А., Кожевин В.М., Явсин Д.А., Гантман М.Г., Ростовщикова Т.Н. // Журн. физ. химии. 2019. Т. 93. № 10. С. 1575. https://doi.org/10.1134/S0036024419100029
Babich I. // Fuel. 2003. V. 82. № 6. P. 607.
Ma X., Sprague M., Song C. // Indust. Eng. Chem. Res. 2005. V. 44. № 15. P. 5768.
Li J., Yang Z., Li S., Jin Q., Zhao J. // J. Indust. Eng. Chem. 2020. V. 82. P. 1.
Craven M., Xiao D., Kunstmann-Olsen C., Kozhevnikova E.F., Blanc F., Steiner A., Kozhevnikov I.V. // Appl. Catal. B: Environ. 2018. V. 231. P. 82.
Брыжин А.А., Руднев В.С., Лукиянчук И.В., Васильева М.С., Тарханова И.Г. // Кинетика и катализ. 2020. Т. 61. № 2. С. 262.
Park J.G., Ko C.H., Yi K.B., Park J.H., Han S.S., Cho S.H., Kim J.N. // Appl. Catal. B: Environ. 2008. V. 81. № 3–4. P. 244.
Tarkhanova I.G., Bryzhin A.A., Gantman M.G., Yarovaya T.P., Lukiyanchuk I.V., Nedozorov P.M., Rudnev V.S. // Surf. Coat. Technol. 2019. V. 362. P. 132.
Bryzhin A.A., Gantman M.G., Buryak A.K., Tarkhanova I.G. // Appl. Catal. B: Environ. 2019. V. 257. P. 117938.
Konga L., Lia G., Wang X. // Catal. Lett. 2004. V. 92. № 3. P. 163.
Дополнительные материалы отсутствуют.
Инструменты
Кинетика и катализ



