Кинетика и катализ, 2022, T. 63, № 1, стр. 138-144
Функционирование твердооксидных топливных элементов с неразделенными электродными пространствами и анодами на основе Ni и сплава Ni–Cu в метан-воздушной смеси
М. В. Юсенко a, В. Д. Беляев a, c, А. К. Демин b, Д. И. Бронин b, А. Н. Саланов a, В. А. Собянин a, c, П. В. Снытников a, *, Д. И. Потемкин a
a ФГБУН ФИЦ Институт катализа им. Г.К. Борескова СО РАН
630090 Новосибирск, просп. Акад. Лаврентьева, 5, Россия
b ФГБУН Институт высокотемпературной электрохимии УрО РАН
620066 Екатеринбург, ул. С. Ковалевской, 22/ул. Академическая, 20, Россия
c ФГБУН Институт химии твердого тела и механохимии СО РАН
630128 Новосибирск, ул. Кутателадзе, 18, Россия
* E-mail: pvsnyt@catalysis.ru
Поступила в редакцию 28.09.2021
После доработки 04.10.2021
Принята к публикации 04.10.2021
- EDN: UFEXKC
- DOI: 10.31857/S0453881122010117
Аннотация
Исследованы электрохимические характеристики твердооксидных топливных элементов с неразделенными электродными пространствами Ni|YSZ|LSM и Ni–Cu|YSZ|LSM, питаемых смесью метана и воздуха (мольное отношение [CH4]/[O2] = 2), в интервале температур 550–700°С. Показано, что эти устройства генерируют электрическую энергию. Добавление меди к никелю улучшает электрохимические характеристики анода. Максимальное значение удельной мощности составляет величину 17 мВт/см2 при температуре 700°С и скорости потока метан-воздушной смеси 240 см3/мин.
ВВЕДЕНИЕ
Четвертый энергопереход, который отождествляется с потреблением возобновляемых источников энергии, электрификацией, повышением энергоэффективности, комплексным применением “зеленых” технологий и декарбонизацией промышленности, подразумевает кроме всего прочего разработку новых подходов на стыке катализа и электрохимии, связанных с использованием водорода или синтез-газа (водородсодержащего газа). На первый план выходят технологии топливных элементов и, в частности, твердооксидных топливных элементов (ТОТЭ) с рабочей температурой 800–1000°С. Их привлекательность обусловлена тем, что они могут потреблять в качестве топлива непосредственно метан, при электрохимическом окислении которого когенерируется электроэнергия и тепло и образуются такие ценные продукты, как синтез-газ и углеводороды С2 [1].
Для кардинального упрощения конструкции ТОТЭ были предложены твердооксидные топливные элементы с неразделенными электродными пространствами (ТОТЭ с НЭП) [2–7]. Конструктивно ТОТЭ с НЭП также состоит из двух электродов (катода и анода) и электролита. Отличие от традиционных ТОТЭ заключается в том, что в анодное и катодное пространства ТОТЭ с НЭП подается одинаковая по составу смесь топлива и окислителя (обычно кислород воздуха). Такое упрощение предъявляет специфические требования к катоду и аноду. С одной стороны, анод и катод не должны проявлять высокую каталитическую активность в отношении реакции глубокого окисления топлива, а с другой – быть высокоактивны в отношении электрохимического окисления топлива в присутствии окислителя и электрохимического восстановления окислителя в присутствии топлива [7].
Основные усилия исследователей в области ТОТЭ с НЭП были направлены на поиск новых материалов для электролита, обладающих лучшей ионной проводимостью, а также более активных электродов. Обобщенная информация представлена в обзорных работах [8, 9]. В топливном элементе на электродах образуются или потребляются газообразные реагенты и протекают процессы окисления или восстановления. Благодаря их развитой каталитически активной поверхности, контактирующей с ионопроводящим электролитом, максимально увеличивается зона электрохимической реакции, и интенсифицируются процессы массопереноса реагентов и продуктов реакции.
Электроды на основе благородных металлов (Pt, Pd) достаточно активны в отношении реакции окисления метана, но для практического применения целесообразны поиски электродов, не содержащих дорогостоящих металлов.
К настоящему времени в качестве анодных материалов для ТОТЭ с НЭП предложены композиции на основе Ni, а именно, керметы Ni–YSZ, Ni–GDC, Ni–SDC (табл. 1). Добавка материала электролита (YSZ, GDC, SDC) к электроду дает, по крайней мере, следующие положительные эффекты: увеличивается адгезия электрода с электролитом; происходит выравнивание коэффициентов линейного термического расширения электродного материала и электролита; формируется стабильная во времени пористая структура электрода; расширяется трехфазная граница “электролит–электрод–газовая фаза”. В качестве катода (табл. 1) используют различные оксидные композиции, в том числе на основе перовскитов типа манганита лантана–стронция La1 –xSrxMnO3 – δ (LSM).
Таблица 1.
Характеристики топливных элементов с неразделенными электродными пространствами в смеси топливо-окислитель (кислород воздуха)
| Анод | Электролит | Толщина электролита, мм |
Катод | T, °C | Топливо | U0, мВ | Jmax, мА/см2 | Pmax, мВт/см2 | Ссылка |
|---|---|---|---|---|---|---|---|---|---|
| Ni–YSZ | YSZ | н.д.*** | Au | 600 950 |
CH4 | 600 350 |
н.д. | 2.36 | [10] |
| Ni–SDC | SDC | 0.15 | SSC | CH4 | ~150 | н.д. | ~0 | [11] | |
| 450 | C2H6 | ~900 | 280 | ||||||
| C3H8 | ~900 | 230 | |||||||
| 500 | C2H6 | ~900 | 403 | ||||||
| Ni–SDC | LSGM YSZ SDC |
3 0.5 3 |
SSC | 700 | CH4 | 920 920 <733 |
н.д. | 355 150 120 |
[12] |
| LSGM | 3 | 550 | C2H6 | 1000 | 163 | ||||
| YSZ | 0.5 | C3H8 | 972 | 125 | |||||
| SDC | 3 | C2H5OH | 710 | 42 | |||||
| Ni–SDC** | SDC | 0.01–0.02 | SSC–SDC | 525 | C3H8 | 750 | 450 | 185 | [13] |
| Ni–SDC | LSGM* YSZ* SDC* |
1 | SSC | 600 | C2H6 | 820 920 970 |
350 230 80 |
70 50 20 |
[14] |
| Ni–SDC–Pd | SDC | 0.15 | SSC | 550 | CH4 | >800 | н.д. | 644 | [15] |
| Ni–YSZ Ni–SDC Ni–GDC |
YSZ | 0.1 | LSCF | 600 650 600 |
C3H8 | 800 | >70 120 >70 |
н.д. | [16] |
| Ni Ni–GDC |
YSZ | 0.3 | LSM LSM–MnO2 |
950 | CH4 | 500 900 |
н.д. | н.д. | [17] |
| Ni–GDC | YSZ | LSM–MnO2 | CH4 | 830 | 1000 | 204 | |||
| Ni Ni–GDC |
YSZ | 0.5 | LSM LSM–MnO2 |
CH4 | 795 830 |
н.д. | 121 161 |
||
| Ni–GDC | YSZ | 1 | LSM | CH4 | 830 | 500 | 102 | ||
| Ni–GDC | GDC | 0.3 | SSC | 600 | CH4 | <800 | 2250 | 468 | [18] |
| NiO + GDC + + LDM | LAMOX | н.д. | BSCF | 675 | CH4 | 800 | 1500 | 300 | [19] |
| Ni/CGO | CGO | н.д. | CFA + FeOx | 670 | CH4 | 760 | 40 | 5.5 | [20] |
| Ni–YSZ** | YSZ | 0.010 | LSM | 700 | CH4 | 900 | 590 | 75 | [21] |
| Ni–YSZ** | YSZ | 0.008 | LSM | 700 | CH4 | 1050 | 1700 | 490 | [22] |
| Ni–YSZ** | YSZ | 0.010 | LSM | 700 | CH4 | 1030 | 1340 | 390 | [23] |
| Ni–YSZ** | SDC | 0.005 | SSTF75 | 650 | CH4 | 900 | 5400 | 1430 | [24] |
| CeO2–Ni, допированный Dy и Tb | YSZ | н.д. | LSM | 650 | CH4 | 316 | 0.94 | н.д. | [25] |
В настоящей работе приведены результаты исследований электрохимических характеристик ТОТЭ с НЭП с Ni- и Ni–Cu-анодами, YSZ-электролитом и LSM-катодом в метан-воздушной смеси.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе были изучены две электрохимические ячейки с неразделенными электродными пространствами (ТОТЭ с НЭП). Каждый ТОТЭ с НЭП представлял собой трубку из твердого газоплотного кислородпроводящего электролита YSZ (состава 0.9ZrO2 + 0.1Y2O3). На внутреннюю поверхность трубки наносили катод из LSM. Катод готовили из пасты, содержащей смесь мелкодисперсных порошков La0.7Sr0.3MnO3 (50 вес. %) и YSZ (50 вес. %). К электролиту пасту припекали на воздухе при температуре 1200оС. На внешнюю поверхность трубки наносили Ni-керамический или Ni–Cu-керамический анод. Аноды готовили из пасты, в состав которой входила смесь мелкодисперсных порошков NiO и YSZ (20–50 вес. %) или 0.5NiO–0.5CuO и YSZ (20–50 вес. %), припеканием при температурах 1350 и 1150°С соответственно. Восстановление анодов до Ni и сплава Ni–Cu проводили в смеси 10 об. % H2 + 90 об. % He. Далее эти электроды обозначены как Ni и Ni–Cu. Схематически устройство ТОТЭ с НЭП представлено на рис. 1.
Геометрические параметры изготовленных ТОТЭ с НЭП приведены в табл. 2.
Таблица 2.
Геометрические параметры топливных элементов с неразделенными электродными пространствами
| ТОТЭ с НЭП | Длина, мм | Диаметр, мм | Толщина электролита, мм | Площадь электрода, см2 |
|---|---|---|---|---|
| Ni│YSZ│LSM | 70 | 9 | 0.3 | 4.5 |
| Ni–Cu│YSZ│LSM | 55 | 11 | 0.3 | 5.2 |
В качестве токовыводов с электродов использовали платиновую проволоку. ТОТЭ с НЭП помещали в нагреваемый электрической печкой кварцевый реактор, через который пропускали метан-воздушную смесь ([CH4]/[O2] = 2) со скоростью 120–240 см3/мин. Эксперименты проводили в проточной кинетической установке при атмосферном давлении в интервале температур 550–700°С. Состав газа на входе в реактор и на выходе из него анализировали при помощи газового хроматографа “Цвет-500” (Россия). Измерение электрических характеристик ТОТЭ с НЭП осуществляли с помощью потенциостата-гальваностата “ПИ-50-1” (Россия). За выходом системы на стационарное состояние следили по установлению постоянных концентраций газов на выходе из реактора и по достижению постоянных значений тока и напряжения. Обратим внимание, что во всех экспериментах конверсия метана не превышала 20%. Продуктами превращений были Н2О, СО2, Н2 и СО.
Исследование микрорельефа границ раздела электрод–электролит и электродов проводили после завершения экспериментов при помощи автоэмиссионного высоковакуумного растрового электронного микроскопа BS-350 (“Tesla”, Чехословакия).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
ТОТЭ с НЭП Ni|YSZ|LSM
На рис. 2 представлены микрофотографии границ раздела электролит YSZ – LSM-катод и электролит YSZ – Ni-анод.
Рис. 2.
Микрофотографии границ раздела электролит YSZ – LSM-катод (слева) и электролит YSZ – Ni-анод (справа).

Видно, что границы раздела электроды–электролит четко различимы. Пористые электроды имеют хороший контакт с электролитом. Толщина анода и катода была 40 и 110 мкм соответственно. Размер частиц, из которых состояли LSM-катод и Ni-анод, не превышал 5 мкм. Размер пор электродов был сопоставим с размером частиц.
На рис. 3 приведены зависимости напряжения и удельной электрической мощности ТОТЭ‑НЭП Ni|YSZ|LSM от плотности тока в метан-воздушной смеси.
Рис. 3.
Зависимости напряжения и удельной мощности ТОТЭ с НЭП Ni│YSZ│LSM от плотности тока. Скорость потока метан-воздушной смеси – 120 см3/мин; T = 600°C.
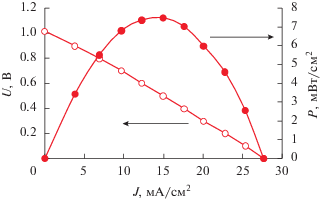
Видно, что напряжение (U) линейно уменьшается с возрастанием плотности тока (J). Такой характер зависимости U от J указывает на то, что основной вклад в падение напряжения вносит омическое сопротивление электролита, которое по оценкам составляет 4.4 Ом. Удельная мощность (P) с увеличением плотности тока носит типичный характер и проходит через максимум (J = = 15 мА/см2, P = 7.4 мВт/см2).
На рис. 4 показано влияние температуры на максимальную удельную мощность и концентрации О2, Н2 и СО на выходе из реактора при работе ТОТЭ с НЭП Ni|YSZ|LSM в метан-воздушной смеси.
Рис. 4.
Температурные зависимости максимальной удельной мощности и концентраций О2, Н2 и СО на выходе из реактора для ТОТЭ с НЭП Ni|YSZ|LSM. Скорость потока метан-воздушной смеси – 120 см3/мин.
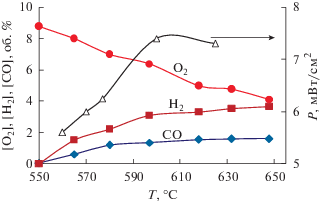
Видно, что с повышением температуры удельная мощность растет и достигает значения 7.4 мВт/см2 при 600°С. Это связано с уменьшением поляризации электродов и образованием водорода и СО за счет протекания каталитической реакции селективного окисления метана. Действительно, из рис. 4 следует, что концентрации водорода и СО увеличиваются, а концентрация кислорода, как и ожидалось, снижается.
ТОТЭ с НЭП Ni–Cu|YSZ|LSM
Медь является хорошим электронным проводником и не зауглероживается в атмосфере метана, поскольку неактивна в отношении реакции СН4 → С + 2Н2. Следовательно, были все основания считать, что наличие меди в составе анода на основе Ni позволило бы повысить электронную проводимость топливного электрода и свести к минимуму возможную вероятность протекания процессов зауглероживания при работе топливного элемента. Для проверки этого предположения была изучена ячейка Ni–Cu|YSZ|LSM.
На рис. 5 представлены микрофотографии Ni–Cu-анода и границ раздела электролит YSZ – LSM-катод и электролит YSZ – Ni–Cu-анод. Видно, что, как и для ТОТЭ с НЭП Ni|YSZ|LSM (рис. 2), границы раздела электроды–электролит четко различимы, а пористые электроды имеют хороший контакт с электролитом. Толщина анода составляет 50 мкм. Размер пор анода был сопоставим с размером частиц (<5 мкм). Следует отметить, Ni–Cu- и Ni-аноды имеют близкую микроструктуру.
Рис. 5.
Микрофотографии Ni–Cu-анода (а) и границ раздела электролит YSZ – Ni–Cu-анод (б) и электролит YSZ – LSM-катод (в).

На рис. 6 приведены зависимости напряжения и удельной электрической мощности ТОТЭ–НЭП Ni–Cu|YSZ|LSM от плотности тока в метан-воздушной смеси при двух температурах. Видно, что вольтамперные характеристики, как и в случае Ni-анода, носят линейный характер. Значения удельной мощности с увеличением плотности тока также проходят через максимум. При 620°С наибольшее значение удельной мощности равняется 13 мВт/см2 при плотности тока 30 мА/см2. При повышении температуры до 700°С максимальная удельная мощность возрастает до 17 мВт/см2 при плотности тока 35 мА/см2. Отметим, что эти значения удельной мощности превышали таковые для ТОТЭ с НЭП с никелевым анодом.
Рис. 6.
Зависимости напряжения и удельной мощности ТОТЭ с НЭП Ni–Cu|YSZ|LSM от плотности тока при T = 620 (треугольники) и 700°C (круги). Скорость потока реакционной смеси – 240 см3/мин.

Наблюдаемое в присутствии меди увеличение электрохимической активности анода, очевидно, связано с расширением зоны протекания электрохимических процессов на границе электрод–электролит. Сравнивая работу ячеек Ni–Cu|YSZ|LSM и Ni|YSZ|LSM, можно сделать вывод о том, что добавка меди к никелевому аноду улучшает электрохимические характеристики ячейки.
Обратим внимание на то, что электрохимические характеристики ТОТЭ с НЭП, полученные в настоящей работе, были ниже известных из литературы (табл. 1). Такое положение дел вполне понятно и связано с большими омическими потерями и использованием неактивированных электродов.
ЗАКЛЮЧЕНИЕ
Исследовано функционирование твердооксидных топливных элементов с неразделенными электродными пространствами с Ni- и Ni–Сu-анодами, LSM-катодом и YSZ-электролитом в метан-воздушной смеси. Показано, что эти ТОТЭ с НЭП генерируют электрическую энергию в области температур 600–700°С и мольном отношении [CH4]/[O2] = 2. Обнаружено, что Ni–Cu-анод обладает более высокой электрохимической активностью, чем Ni-анод. Оказалось, что при работе ТОТЭ c НЭП степень использование метана была низкой (<20%), поэтому оставшийся метан целесообразно вовлекать в дальнейшую переработку, например, путем сжигания с целью получения тепла или конверсии в синтез-газ.
Список литературы
Собянин В.А. // Рос. Хим. Журн. 2003. Т. 47. № 6. С. 62
Dyer C.K. // Nature. 1990. V. 343. P. 547.
Moseley P., Willians D. // Nature. 1990. V. 346. P. 23.
Gottesfeld S. // Nature. 1990. V. 345. P. 673.
Asano K., Hibino T., Iwahara H. // Denki Kagaky. 1996. V. 64. P. 649.
Demin A.K., Gulbis F.Ya. // Solid State Ionics. 2000. V. 135. P. 451.
Riess I. Van der Put P.S., Schonman J. // Solid State Ionics. 1995. V. 82. P. 1.
Yano M., Tomita A., Sano M., Hibino T. // Solid State Ionics. 2007. V. 177. P. 3351.
Kuhn M., Napporn T.W. // Energies. 2010. V. 3. P. 57.
Hibino T., Iwahara H. // Chem. Lett. 1993. P. 1131.
Hibino T., Hashimoto A., Inoue T., Tokuno J.-I., Yoshida S.-I., Sano M. // Science. 2000. V. 288. P. 2031.
Hibino T., Hashimoto A., Inoue T., Tokuno J.-I., Yoshida S.-I., Sano M. // J. Electrochem. Soc. 2000. V. 147. № 8. P. 2888.
Shao Z., Kwak Ch., Haile S.M. // Solid State Ionics. 2004. V. 175. P. 39.
Hibino T., Hashimoto A., Suzuki M., Yano M., Yoshida S.-I., Sano M. // J. Electrochem. Soc. 2002. V. 149. № 2. P. A195.
Hibino T., Hashimoto A., Yano M., Suzuki M., Yoshida S.-I., Sano M. // J. Electrochem. Soc. 2002. V. 149. № 2. P. A133.
Jasinski P., Suzuki T., Dogan F., Anderson H.U. // Solid state Ionics. 2004. V. 175. P. 35.
Hibino T., Wang S., Kakimoto S., Sano M. // Solid State Ionics. 2000. V. 127. P. 89.
Buergler B.E., Siegrist M.E., Gauckler L.J. // Solid State Ionics. 2005. V. 176. P. 1717.
Le M.-V., Tsai D.-Sh., Nguyen T.-A. // Ceramics International. 2018. V. 44. P. 1726.
Bedon A., Viricelle J. P., Rieu M., Mascotto S., Glisenti A. // Int. J. Hydrogen Energy. 2021. V. 46. P. 14735.
Tian Y., Lu Zh., Wang Zh., Wei B., Guo X., Wu P. // J. Solid State Electrochem. 2019. V. 23. P. 1651.
Tian Y., Lu Zh., Wang Zh., Wei B., Nie Zh., Zhai A. // Ionics. 2019. V. 25. P. 1281.
Tian Y., Wu P., Zhang X., Guo X., Ding L. // Ionics. 2020. V. 26. P. 6217.
Zhang Y. // ACS Appl. Energy Mater. 2018. V. 1. P. 1337.
Catalano M., Taurino A., Zhu J., Crozier P.A., Dalzilio S., Amati M., Gregoratti L., Bozzini B., Mele C. // J. Solid State Electrochem. 2018. V. 22. P. 3761.
Дополнительные материалы отсутствуют.
Инструменты
Кинетика и катализ



