Кинетика и катализ, 2022, T. 63, № 3, стр. 372-381
Каталитические свойства и структура поверхностного слоя палладия, формирующегося в процессе автоколебательной реакции окисления метана
В. Ю. Бычков a, *, Ю. П. Тюленин a, А. А. Гулин a, В. Н. Корчак a
a ФГБУН ФИЦ химической физики им. Н.Н. Семенова РАН
119991 Москва, ул. Косыгина, 4, Россия
* E-mail: bychkov@chph.ras.ru
Поступила в редакцию 21.10.2021
После доработки 02.11.2021
Принята к публикации 02.11.2021
- EDN: SEYPAQ
- DOI: 10.31857/S0453881122030054
Аннотация
В результате протекания реакции окисления метана на Pd-фольге в автоколебательном режиме при температуре 400°С в течение 1 ч на поверхности фольги образуется слой, содержащий объемистые пористые агломераты нанокристаллов. По данным СЭМ агломераты диаметром 1–20 мкм состоят из кристаллов размером ~100 нм с порами такого же размера между ними. Над поверхностью фольги агломераты выступают на 5–10 мкм. Измерена каталитическая активность таких образцов в реакции окисления СО. Показано, что температура начала каталитической реакции (3% конверсия СО) снижается от 400°С для исходной Pd-фольги до 200°С для Pd-фольги после автоколебательного окисления метана. Данные рентгенофазового анализа и энергодисперсионной рентгеновской спектроскопии (ЭДС) позволяют заключить, что обнаруженные агломераты состоят из кристаллов оксида палладия PdO. Продемонстрировано, что окисление поверхности Pd-фольги в стационарном режиме, наоборот, способствует формированию ровного слоя оксида палладия без заметных пористых структур, каталитическая активность которого ниже, чем таковая образца Pd после автоколебаний. Изучена устойчивость полученных пористых слоев в инертной (Не), восстановительной (Н2) или окислительной (воздух) атмосфере при нагреве до 700°С. В инертной или восстановительной среде происходит и исчезновение оксида палладия, и разрушение агломератов наночастиц, что приводит к снижению каталитической активности Pd-фольги в реакции окисления СО. Напротив, прогрев в потоке воздуха вызывает и увеличение содержания PdO в образце, и рост числа пористых агломератов нанокристаллов на поверхности, в результате чего происходит дополнительное повышение каталитической активности Pd-фольги.
ВВЕДЕНИЕ
Палладий является катализатором различных реакций, включая гидрирование и дегидрирование [1–4], окисление органических соединений и СО [5], декарбонилирование и декарбоксилирование [1, 6], конверсию этанола [7] и др. Приготовление образцов металлического палладия с развитой поверхностью может представлять интерес с точки зрения получения катализаторов, сочетающих в себе высокую каталитическую активность благодаря большой площади доступной поверхности, относительно быстрый теплообмен через металлическую основу массивных систем и низкое сопротивление газовому потоку образцов, изготовленных на основе фольги или проволоки.
Известно, что каталитическое окисление низших углеводородов [8–19] на металлическом палладии, массивном или нанесенном, может протекать в автоколебательном режиме. В ходе автоколебаний происходит периодическое окисление–восстановление поверхности палладия, а также образование и окисление карбида палладия. В результате этих процессов поверхность металла разрыхляется, что было установлено, например, в работах [8, 9]. Очевидно, что такие образцы могут иметь более высокую каталитическую активность в гетерогенных реакциях. Ранее [20] мы изучили влияние автоколебательного режима процесса окисления метана на фольге и порошке Pd на формирование развитого поверхностного слоя и его каталитическую активность в реакциях окисления алканов С1–С4. Методом сканирующей электронной микроскопии (СЭМ) было обнаружено, что такая обработка образцов Pd в условиях автоколебательного окисления метана (далее, для краткости, автоколебательная обработка) действительно приводит к образованию рыхлого поверхностного слоя, каталитическая активность которого в несколько раз превышает активность исходной Pd-фольги или порошка.
В настоящей работе была поставлена задача продолжить изучение каталитических и структурных (морфология, фазовый состав) свойств поверхностного слоя Pd-фольги, формирующегося в ходе автоколебательного окисления метана на палладии. В частности, была протестирована каталитическая активность Pd-образцов в другой реакции, а именно в окислении СО. Кроме того, исследовано влияние высокотемпературной обработки полученных пористых слоев в инертной, восстановительной и окислительной газовых средах на их морфологию и каталитическую активность.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Опыты проводили с образцами Pd-фольги размером 5.5 × 8 × 0.1 мм. Анализ газообразных реагентов и продуктов выполняли с помощью масс-спектрометра OmniStar (“Pfeiffer”, Германия) или хроматографа Кристалл-2000 (“Хроматэк”, Россия). Каталитические эксперименты осуществляли в проточном кварцевом реакторе (внутренний диаметр – 6 мм) при атмосферном давлении. Образец фольги помещали в вертикально расположенный реактор параллельно направлению течения газа, не деформируя образец. Температуру реактора измеряли снаружи, температуру фольги отдельно не меряли.
Автоколебательные режимы каталитической реакции получали при пуске на образцы смеси 80% СН4–20% О2 (20 мл/мин) при 400°С. Стандартная продолжительность такого эксперимента составляла 1 ч. Автоколебания скорости реакции фиксировали по изменениям состава газовой смеси на выходе из реактора с помощью масс-спектрометра OmniStar GSD 301 или по колебаниям температуры катализатора с помощью термопары.
Каталитическую активность тестировали в реакции окисления СО в потоке смеси 2% СО + + 5% О2 + Не при ступенчатом повышении температуры. Концентрации газовых реагентов и продуктов находили с помощью газового хроматографа “Кристалл 2000м”. Интервал времени перед первым измерением в каждом опыте составлял 5 мин.
Морфологию поверхности исходной Pd-фольги и образцов фольги после различных обработок изучали с помощью сканирующего электронного микроскопа Prisma E (“Thermo Fisher Scientific”, Чехия), также оснащенного детектором для энергодисперсионной рентгеновской спектроскопии (ЭДС).
Фазовый состав определяли с помощью рентгеновского дифрактометра Smartlab SE (“Rigaku”, Япония) с излучением CuKα. При измерениях шаг сканирования был 0.005°, скорость сканирования – 1°/мин. Достоверность фаз подтверждали табличными данными из базы данных SmartLab Studio II (“Rigaku”) для Pd и PdO.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Параметры автоколебаний при окислении метана на Pd
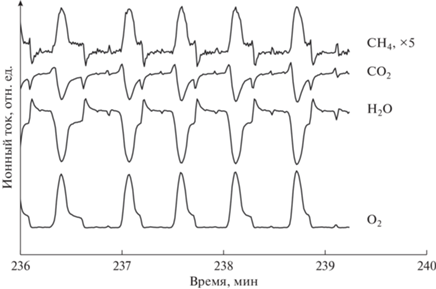
На рис. 1 показаны автоколебания концентраций реагентов и продуктов в реакции окисления метана в смеси 80% СН4–20% О2 при температуре 400°С. Примеры автоколебаний для газовых смесей с другим соотношением СН4 и О2, а также при других температурах можно найти в работах [8–19]. Для возникновения автоколебаний в вышеуказанной реакции существенным является относительный избыток метана в исходной смеси. Период колебаний составляет от долей минуты до нескольких минут в зависимости от температуры реакции. Цикл колебаний состоит из фазы с относительно высокой скоростью окисления метана и последующей фазы с относительно низкой скоростью реакции. В обеих фазах происходит глубокое окисление метана до СО2 и Н2О. Установлено [14, 19], что в фазе с высокой скоростью катализатор находится в восстановленном металлическом состоянии и содержит значительное количество растворенного углерода. В фазе с низкой скоростью растворенный углерод отсутствует, а поверхность палладия окисляется, образуя оксид палладия PdO. Более детальную информацию о механизме автоколебаний на Pd в реакции окисления метана можно найти в работах [8–19].
Влияние автоколебательной обработки на каталитическую активность
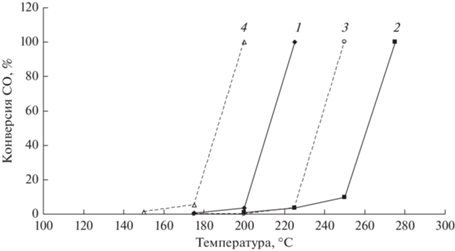
Автоколебательную обработку проводили в потоке смеси 80% СН4–20% О2 (20 мл/мин) при температуре реактора 400°С в течение 1 ч. Полученный образец охлаждали и тестировали его каталитическую активность в реакции окисления СО в смеси с относительным избытком кислорода 2% СО + 5% О2 + Не при ступенчатом повышении температуры. На рис. 2 показано изменение конверсии СО для образца исходной фольги Pd и аналогичного образца Pd после автоколебательной обработки. Видно, что на исходной фольге величина конверсии СО 3% наблюдается при 400°С и постепенно увеличивается до 90% с повышением температуры до 550°С. На образце после проведения автоколебательной реакции конверсия СО достигает 3.5% уже при 200°С и резко возрастает до 100% при нагреве до 225°С.
Рис. 2.
Зависимость конверсии СО от температуры в процессе окисления СО на Pd-фольге в потоке смеси 2% СО + + 5% О2 + Не (20 мл/мин): 1 – исходная Pd-фольга; 2 – Pd-фольга после автоколебательной реакции окисления метана при 400°С в течение 1 ч; 3 – Pd-фольга после обработки в потоке воздуха при 700°С в течение 1 ч.

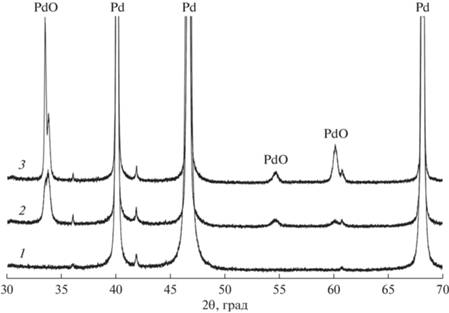
На рис. 3 представлены результаты рентгенофазового анализа исходной фольги Pd и образца Pd после автоколебательной реакции. Для исходного образца были обнаружены только линии металлического Pd, соответствующие табличным данным (карточка Pd 9008478:COD в базе данных SmartLab Studio II). Образец после автоколебательной обработки содержал также некоторое количество оксида палладия PdO (карточка PdO 4124668:COD в базе данных SmartLab Studio II).
Рис. 3.
Спектры РФА образцов Pd-фольги: 1 – исходная Pd-фольга; 2 – Pd-фольга после автоколебательной реакции окисления метана при 400°С в течение 1 ч; 3 – Pd-фольга после обработки в потоке воздуха при 700°С в течение 1 ч.
Так как результаты РФА показали присутствие PdO в образце после автоколебательной реакции, представляло интерес сравнить его каталитическую активность с таковой исходного образца Pd, окисленного в стационарных условиях. Для этого свежий образец Pd-фольги окисляли в потоке воздуха при температуре 700°С в течение 1 ч. Данный образец содержал гораздо больше оксида палладия PdO, чем образец после автоколебательной обработки (рис. 3). На рис. 2 представлена температурная зависимость конверсии СО для такого окисленного образца в реакции окисления СО. Видно, что каталитическая активность окисленного Pd также гораздо выше таковой исходного металлического Pd, но ниже, чем у Pd-фольги после автоколебательной обработки, то есть скорость окисления СО не коррелирует с количеством оксида палладия в образце.
Исследование морфологии поверхности
Морфологию поверхности Pd-фольги изучали с помощью СЭМ. На рис. 4а–4в представлены СЭМ-изображения Pd-фольги до и после автоколебательного окисления метана при 400°С в течение 1 ч. Видно, что относительно гладкая поверхность исходной фольги (рис. 4а) после автоколебательной обработки становится более развитой (рис. 4б), с агломератами наноразмерных кристаллов. Размер кристаллов составляет ~100 нм, агломератов – 1–20 мкм. Агломераты содержат многочисленные поры диаметром ~100 нм. Из рис. 4в, на котором показан вид поверхности образца сбоку, следует, что агломераты выступают над поверхностью фольги на 5–10 мкм. На рис. 5 приведено изображение образца с агломератами, полученное для измерения элементного состава поверхности методом ЭДС. Метки №№ 1–4 указывают центры областей измерения сигналов ЭДС. Точки 1 и 3 были выбраны на агломератах нанокристаллов, а точки 2 и 4 находятся на участках поверхности без агломератов. В табл. 1 представлены данные об атомных концентрациях Pd, О и С, определенных в этих точках поверхности. Видно, что концентрация кислорода в точках 1 и 3 сопоставима с концентрацией палладия, а в точках 2 и 4 существенно ее ниже. По-видимому, обнаруженные агломераты состоят из кристаллов оксида палладия.
Рис. 4.
СЭМ-изображения фольги Pd: исходной (а) и после автоколебательной реакции окисления метана при 400°С в течение 1 ч (б, в).

Рис. 5.
СЭМ-изображение фольги Pd после автоколебательной реакции окисления метана при 400°С с отмеченными точками, в которых определяли химический состав методом ЭДС.

Таблица 1.
Атомные концентрации элементов по данным ЭДС в точках, обозначенных на рис. 5
| Номер точки | С | О | Pd |
|---|---|---|---|
| ат. % | |||
| 1 | 19.7 | 40.1 | 39.4 |
| 2 | 10.6 | 17.1 | 71.3 |
| 3 | 11.1 | 60.2 | 28.2 |
| 4 | 10.6 | 14.2 | 74.5 |
На рис. 6а и 6б показаны изображения образца Pd-фольги, который не участвовал в реакции окисления метана, а был окислен в потоке воздуха при 700°С. На поверхности такого образца пористые агломераты отсутствуют, а оксид палладия, наблюдаемый по данным РФА, образует ровный плотный слой. Снимок на рис. 6б, который демонстрирует вид сбоку на поперечный разрез окисленного образца, позволяет заметить растрескивание и разрушение поверхностного оксидного слоя по месту разреза.
Рис. 6.
СЭМ-изображения Pd-фольги, окисленной в потоке воздуха при 700°С в течение 1 ч. Вид сверху (а) и вид разреза образца сбоку (б).

На основании полученных данных можно заключить, что к повышению каталитической активности палладия в реакции окисления СО приводят два фактора – образование оксида палладия на поверхности образца и увеличение пористости вследствие формирования пористых агломератов наночастиц оксида палладия. Образец Pd-фольги после автоколебательной обработки демонстрирует и то, и другое, и имеет самую высокую каталитическую активность из изученных трех образцов. Вероятно, причиной образования обнаруженной микропористой структуры являются частые периодические процессы восстановления/окисления поверхности в ходе автоколебательной реакции окисления метана при 400°С, а также быстрые процессы растворения углерода в палладии и его удаления/окисления.
Исследование влияния различных газовых сред
Было проведено исследование влияния высокотемпературной обработки в инертной, восстановительной или окислительной газовой среде на каталитические свойства и морфологию поверхностного слоя Pd, образовавшегося при автоколебательном окислении метана. Для этого образцы Pd-фольги после автоколебательной обработки выдерживали при температуре 700°С в потоке гелия, Н2 или воздуха в течение 1 ч, затем охлаждали и определяли каталитическую активность в реакции окисления СО. Результаты тестирования показаны на рис. 7. Видно, что нахождение образца в потоке гелия или водорода снижает его активность, тогда как нагрев в потоке воздуха увеличивает ее.
Рис. 7.
Зависимость конверсии СО от температуры в процессе окисления СО на Pd-фольге в потоке смеси 2% СО + + 5% О2 + Не (20 мл/мин): образец Pd-фольги после автоколебательного окисления метана при 400°С в течение 1 ч (1), а также образцы Pd после автоколебательной реакции при 400°С и последующей обработкой при 700°С в течение 1 ч в потоке гелия (2), водорода (3) или воздуха (4).
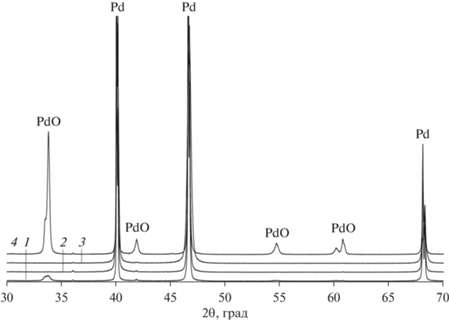
На рис. 8 приведены рентгенограммы образцов Pd-фольги после автоколебательного окисления метана при 400°С и после их последующего нагрева при 700°С в потоке гелия, водорода или воздуха. Как было указано выше, непосредственно после автоколебательной обработки образец содержит небольшое количество оксида палладия PdO. Этот оксид исчезает после выдерживания образца в токе гелия или водорода. Напротив, после нахождения в потоке воздуха количество PdO в образце сильно возрастает.
Рис. 8.
Спектры РФА образцов Pd-фольги после автоколебательного окисления метана при 400°С (1), а также после автоколебательной реакции и последующей обработки при 700°С в течение 1 ч в потоке гелия (2), Н2 (3) или воздуха (4).
На рис. 9а–9г представлены СЭМ-изображения поверхности вышеуказанных образцов после прогрева при 700°С. Видно, что пористые структуры, сформировавшиеся на поверхности Pd-фольги в результате автоколебательного окисления метана (рис. 4в), после высокотемпературной обработки в потоке гелия или водорода сильно преобразуются и существенно теряют в объеме агломератов и их пористости (рис. 9а, 9б). Нанокристаллы размером 100 нм, составляющие пористые агломераты после автоколебательной обработки, превращаются в частицы размером ~1 мкм, которые не создают объемистых пористых структур. Напротив, после нагрева в потоке воздуха количество и объем пористых агломератов увеличивается (рис. 9в, 9г).
ЗАКЛЮЧЕНИЕ
В результате проведения реакции окисления метана на палладиевой фольге в автоколебательном режиме на ее поверхности формируется микропористый слой, содержащий пористые агломераты наноразмерных частиц оксида палладия. Размер частиц PdO составляет ~100 нм, а размер агломератов – 1–20 мкм. Объемистые структуры агломератов выступают над поверхностью фольги на 5–10 мкм. Показано, что окисление Pd-фольги в стационарном режиме не приводит к образованию подобных пористых структур.
Установлено, что возникновение такого поверхностного слоя приводит к значительному росту каталитической активности палладия в реакции окисления СО: температура начала каталитической реакции (3% конверсия СО) снижается от 400°С для исходной Pd-фольги до 200°С для Pd-фольги после автоколебательного окисления метана. Показано, что повышение активности вызывается двумя факторами: увеличением площади поверхности и образованием оксида палладия на поверхности палладия.
Изучена устойчивость полученных пористых слоев при их нагреве до 700°С в инертной (Не), восстановительной (Н2) или окислительной (О2) атмосферах. В инертной или восстановительной средах происходит и исчезновение оксида палладия, и разрушение объемистых агломератов наночастиц, что приводит к снижению каталитической активности Pd-фольги в реакции окисления СО. Напротив, прогрев в потоке воздуха увеличивает и содержание PdO в образце, и количество пористых агломератов нанокристаллов на поверхности. В результате происходит дополнительное повышение каталитической активности Pd-фольги.
Список литературы
Беренблюм А.С., Данюшевский В.Я., Кацман Е.А. // Кинетика и катализ. 2019. Т. 60. № 4. С. 411.
Шляпин Д.А., Глыздова Д.В., Афонасенко Т.Н., Темерев В.Л., Цырульников П.Г. // Кинетика и катализ. 2019. Т. 60. № 4. С. 479.
Рассолов А.В., Брагина Г.О., Баева Г.Н., Машковский И.С., Стахеев А.Ю. // Кинетика и катализ. 2020. Т. 61. № 6. С. 837.
Скрипов Н.И., Белых Л.Б., Стеренчук Т.П., Левченко А.С., Шмидт Ф.К. // Кинетика и катализ. 2021. Т. 62. № 2. С. 245.
Панафидин М.А., Бухтияров А.В., Клюшин А.Ю., Просвирин И.П., Четырин И.А., Бухтияров В.И. // Кинетика и катализ. 2019. Т. 60. № 6. С. 806.
Шамсиев Р.С., Соколов И.Е., Данилов Ф.О., Флид В.Р. // Кинетика и катализ. 2019. Т. 60. № 5. С. 634.
Николаев С.А., Цодиков М.В., Чистяков А.В, Чистякова П.А., Эзжеленко Д.И., Кротова И.Н. // Кинетика и катализ. 2020. Т. 61. № 6. С. 864.
König D., Weber W.H., Poindexter B.D., Mcbride J.R., Graham G.W., Otto K. // Catal. Lett. 1994. V. 29. P. 329.
Graham G.W., König D., Poindexter B.D., Remillard J.T., Weber W.H. // Top. Catal. 1999. V. 8. P. 35.
Deng Y., Nevell T.G. // Faraday Discuss. 1996. V. 105. P. 33.
Deng Y., Nevell T.G. // J. Mol. Catal. A. 1999. V. 142. P. 51.
Ozkan U.S., Kumthekar M.W., Karakas G. // J. Catal. 1997. V. 171. P. 67.
Zhang X.L., Lee C.S.-M., Mingos D.M.P., Hayward D.O. // Appl. Catal. A: General. 2003. V. 240. P. 183.
Bychkov V.Yu., Tyulenin Yu.P., Slinko M.M., Shashkin D.P., Korchak V.N. // J. Catal. 2009. V. 267. P. 181.
Bychkov V.Yu., Tyulenin Yu.P., Slinko M.M., Korchak V.N. // Catal. Lett. 2011. V. 141. P. 602.
Kimmerle B., Baiker A., Grunwaldtz J.-D. // Phys. Chem. Chem. Phys. 2010. V. 12. P. 2288.
Stötzel J., Kimmerle B., Nachtegaal M., Grunwaldtz J.-D. // J. Phys. Chem. C. 2012. V. 116. P. 599.
Bychkov V.Yu., Tyulenin Yu.P., Gorenberg A.Ya., Sokolov S., Korchak V.N. // Appl. Catal. A: General. 2014. V. 485. P. 1.
Kaichev V.V., Vinokurov Z.S., Saraev A.A. // Catal. Sci. Technol. 2021. V. 11. P. 4392.
Bychkov V.Yu., Tulenin Yu.P., Slinko M.M., Sokolov S., Korchak V.N. // Catal. Lett. 2017. V. 147. P. 1019.
Дополнительные материалы отсутствуют.
Инструменты
Кинетика и катализ