Кинетика и катализ, 2023, T. 64, № 2, стр. 243-248
Исследование регенерации катализатора Rh/Ce0.75Zr0.25O2 – δ/θ-Al2O3/FeCrAl после автотермического риформинга дизельного топлива
В. А. Шилов a, b, *, В. Н. Рогожников a, Д. И. Потемкин a, b, П. В. Снытников a
a ФГБУН Институт катализа им. Г.К. Борескова СО РАН
630090 Новосибирск, просп. Акад. Лаврентьева, 5, Россия
b ФГАОУ ВО Новосибирский национальный исследовательский государственный университет
630090 Новосибирск, ул. Пирогова, 2, Россия
* E-mail: sva@catalysis.ru
Поступила в редакцию 26.08.2022
После доработки 24.10.2022
Принята к публикации 03.11.2022
- EDN: GNRHLT
- DOI: 10.31857/S0453881123020077
Аннотация
Проведено исследование сажеобразования на поверхности структурированного катализатора Rh/Ce0.75Zr0.25O2/Al2O3/FeCrAl в ходе автотермического риформинга дизельного топлива в синтез-газ. Методом СЭМ на поверхности катализатора обнаружено формирование частиц волокнистого углерода размером 5–50 мкм. Установлено, что процесс зауглероживания происходит на поверхности каталитического покрытия и не вызывает его отслоения и повреждения, а расположение углеродных отложений не препятствует их окислению во время регенерации с использованием кислорода воздуха или водяного пара. Показано, что реакция окисления сажи кислородом начинает активно протекать при температуре 450°С, большая часть углерода окисляется еще до выхода печи реактора на рабочую температуру автотермического риформинга дизельного топлива (750°С). Водяной пар также способен окислять образующиеся углеродные отложения, но с меньшей эффективностью, чем кислород. Процесс регенерации паром активно протекает при температуре 750°С, что указывает на возможность саморегенерации катализатора в автотермическом риформинге дизельного топлива, где вода подается в избытке.
ВВЕДЕНИЕ
Последние годы все бóльшую популярность набирают энергоустановки на основе топливных элементов, работающие на водородсодержащем газе [1–3]. Но, несмотря на достигнутые успехи, одним из основных сдерживающих факторов их применения является отсутствие достаточно развитой инфраструктуры – хранилищ водорода и заправочных станций. Очевидно, что для стимулирования массового использования топливных элементов она должна уже существовать, также как и должна быть отлажена логистика. На сегодняшний же день даже в наиболее технологически развитых странах водородных заправок на порядки меньше, чем углеводородных автозаправочных станций. В этой связи логичным и обоснованным представляется подход, когда на начальном “переходном” этапе получение водорода осуществляется из привычных обычному потребителю моторных топлив, например, дизельного, непосредственно в месте его потребления в электрохимическом генераторе (ЭХГ) [4]. Дизельное топливо (ДТ) является удобным носителем водорода – по сравнению с другими альтернативными носителями на единицу объема ДТ приходится наибольшее количество водорода, а его длительное хранение осуществляется при температуре и давлении окружающей среды. Работающие на дизельном топливе ЭХГ могут быть использованы в качестве стационарного, резервного или вспомогательного источника электроэнергии.
В большинстве исследований было показано, что наиболее оптимальный способ получения синтез-газа из дизельного топлива – автотермический риформинг (АТР) [4–25]:
(I)
$\begin{gathered} {{{\text{C}}}_{n}}{{{\text{H}}}_{m}} + ~\frac{n}{4}{{{\text{O}}}_{2}} + ~\frac{n}{2}{{{\text{H}}}_{{\text{2}}}}{\text{O}} \to \\ \to n{\text{CO}} + \left[ {~\frac{m}{2} + ~\frac{n}{2}} \right]{{{\text{H}}}_{2}},~\,\,\,\,\Delta H \leqslant 0. \\ \end{gathered} $Трудности с созданием эффективного катализатора конверсии дизельного топлива в синтез-газ, пригодный по составу для питания твердооксидных топливных элементов, связаны с присутствием в моторных топливах ароматических соединений, зачастую содержащих серу и обладающих низкой активностью в АТР. Наличие в дизельном топливе ди- и полиароматических соединений, конверсия которых вызывает наибольшие затруднения [8, 16, 19], приводит к зауглероживанию катализатора и ухудшению его каталитических свойств: происходит снижение активности и селективности в ходе реакции. Такая дезактивация может быть обратимой (фазовый переход активного компонента или закоксовывание) или иметь необратимый характер (спекание, отравление, термическое или химическое разложение). В случае обратимой дезактивации возможно частично или полностью регенерировать катализатор, что увеличивает срок его использования. Так как наиболее частая причина снижения активности – зауглероживание, то регенерацию катализаторов обычно проводят кислородом воздуха при температуре не выше рабочей, чтобы избежать спекания активного компонента [26].
Ранее нами был разработан структурированный Rh-содержащий катализатор конверсии дизельного топлива в синтез-газ [13, 14, 27], который был исследован в процессах превращения модельного и коммерческого жидкого углеводородного топлива [17–19]. В ходе ресурсных испытаний в автотермическом риформинге дизельного топлива было установлено, что катализатор постепенно подвергается зауглероживанию, обусловленному присутствием ди- и полиароматических углеводородов в ДТ [28]. Целью настоящей работы является более детальное исследование процесса образования сажи на поверхности катализатора, ее удаления, а также возможности саморегенерации катализатора в ходе автотермического риформинга.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для изучения протекания процессов зауглероживания и преимущественной локализации углерода в структуре катализатора был проведен цикл экспериментов с образцом состава (вес. %) 0.24 Rh/6 Ce0.75Zr0.25O2 – δ/4 θ-Al2O3/FeCrAl (Rh/CZ/FCA). Катализатор был приготовлен в соответствии с разработанной методикой [24, 25, 27, 28] в форме цилиндрического блока диаметром 17 мм, длиной 50 мм и массой 10.8 г, изготовленного из фехралевой сетки (X23Ю5T, размер ячейки – 0.5 мм, диаметр проволоки – 0.25 мм, производитель – ООО “НПО Союзнихром”, Россия).
Автотермический риформинг дизельного топлива зимней марки (“Газпромнефть”, Россия), соответствующего ГОСТ 32511-2013 (стандарт EN 590:2009), осуществляли в проточном реакторе с неподвижным слоем катализатора при температуре печи 750°С и атмосферном давлении (табл. 1) [28].
Таблица 1.
Условия проведения процессов АТР ДТ и регенерации катализатора Rh/CZ/FCA
| Процесс | Подача реагентов | GHSV, ч–1 | Т, °C | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Топливо, г/ч | Н2О, | Воздух, л/ч | Кислород | Аргон, л/ч | |||||
| г/ч | моль/ч | л/ч | моль/ч | ||||||
| АТР ДТ | 37.7 | 127 | 7.06 | 127 | – | – | – | 20 000 | 750 |
| Регенерация кислородом | – | – | – | – | 0.3 | 0.013 | 1.2 | – | 350–750 |
| Регенерация водой | – | 3 | 0.17 | – | – | – | 1.2 | ||
Для исследования процессов удаления углерода, образовавшегося в ходе проведения каталитических экспериментов, проводили окислительную регенерацию катализатора кислородом воздуха или водяным паром (табл. 1) со скоростью нагрева печи реактора 10°С/мин от 350 до 750°С в потоке смеси 20 об. % О2 + 80 об. % Ar или 75 об. % H2O + + 25 об. % Ar. Состав продуктов реакции отслеживали с помощью масс-спектрометра QMS 200 (“Stanford Research Systems” США) в режиме реального времени.
Морфологию и микроструктуру поверхности изучали с помощью сканирующей электронной микроскопии (СЭМ) на приборе JSM-6460 LV (“Jeol”, Япония). Химический состав поверхности исследовали на энергодисперсионном рентгеновском микроанализаторе INCA Energy-350 (“Oxford Instruments”, Великобритания).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Так как автотермический риформинг дизельного топлива осуществляли при температуре 750°С [28] с использованием водяного пара и кислорода воздуха, то для окислительной регенерации катализатора было целесообразно применять один из этих реагентов. Для изучения процессов удаления углеродных отложений предварительно проводили АТР ДТ при соотношении H2O/C = 2.7 и O2/C = 0.4 (табл. 1), что способствовало ускоренному зауглероживанию катализатора. Методом ТПО было показано, что после 10 ч в потоке средняя скорость образования углерода на поверхности катализатора Rh/CZ/FCA составила 23.5 мгсажи${\text{г}}_{{{\text{кат}}}}^{{ - 1}}$ ч–1.
После АТР дизельного топлива каталитический блок был извлечен из реактора без регенерации и изучен методом СЭМ с энергодисперсионным рентгеновским анализом. Автотермический риформинг объединяет экзотермические реакции полного окисления и эндотермический паровой риформинг. Процесс полного окисления углеводородов с участием кислорода воздуха идет быстро и локализован в передней части каталитического блока, тогда как паровая конверсия протекает более медленно и охватывает почти весь слой катализатора [17]. Для СЭМ-исследований были выбраны образцы передней и концевой части каталитического блока, использовавшегося в процессах каталитического риформинга.
Изображения СЭМ, полученные для свежеприготовленного и использованного каталитического блока, показали, что каталитическое покрытие не повреждается в ходе автотермического риформинга дизельного топлива (рис. 1а, 1б), покрытие Rh/Ce0.75Zr0.25O2/Al2O3 остается плотным и однородным как в передней, так и в концевой части блока. Это имеет особенное значение для передней части каталитического блока, где происходят высоко экзотермические реакции полного окисления углеводородов, поскольку эта часть подвергается быстрым изменениям температуры во время процедур запуска и останова реактора.
Рис. 1.
СЭМ-изображения катализатора до (а) и после (б, в, г) автотермического риформинга дизельного топлива.

На поверхностях как передней, так и концевой частей каталитического блока наблюдается появление “наростов” размером 5–50 мкм. Согласно данным энергодисперсионного микроанализа эти образования сформировались из углеродных нановолокон (рис. 1в, 1г). Стоит отметить, что процесс коксообразования идет на внешней поверхности каталитического покрытия и не вызывает его отслоения или значительного повреждения. Расположение углеродных отложений на поверхности катализатора упрощает процесс их окисления и удаления в процессе регенерации.
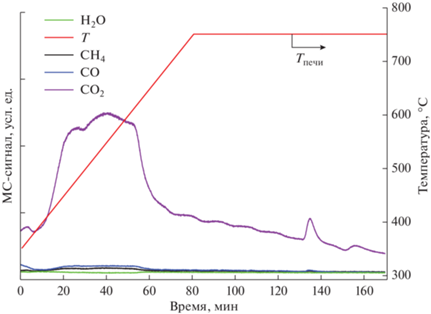
Из рис. 2 видно, что реакция окисления углерода кислородом начинает активно протекать уже при температуре 450°С, окисление сопровождается выделением СО2 по реакции (II). Значительная часть углерода окисляется еще до выхода печи реактора на рабочую температуру АТР ДТ (750°С). После регенерации активность катализатора возвращается на начальный уровень, при этом с помощью сканирующего электронного микроскопа было показано, что видимые следы разрушения каталитического покрытия отсутствуют [28].
Автотермичский риформинг дизельного топлива проводится в избытке водяного пара при соотношении H2O/C = 2–3, причем, в отличие от кислорода, который расходуется в лобовой части каталитического блока, взаимодействие с водяным паром протекает по всей длине каталитического слоя [17]. Поэтому целесообразно было выяснить возможность саморегенерации катализатора водяным паром в ходе протекания АТР ДТ. Из рис. 3 видно, что реакция окисления образовавшегося углерода активно начинает протекать при температуре выше 550°С. При контакте перегретого водяного пара с углеродом на поверхности катализатора идут реакции (III), (IV) с образованием водорода, углекислого газа и монооксида углерода:
(III)
${\text{С + }}{{{\text{H}}}_{{\text{2}}}}{\text{O}} \to {\text{CO + }}{{{\text{H}}}_{2}},~\,\,\,\,\Delta H > 0,$(IV)
${\text{С + 2}}{{{\text{H}}}_{{\text{2}}}}{\text{O}} \to {\text{C}}{{{\text{O}}}_{{\text{2}}}}{\text{ + 2}}{{{\text{H}}}_{2}},~\,\,\,\,\Delta H > 0.$Высокая интенсивность сигнала H2 по сравнению с сигналами остальных продуктов реакции окисления углерода водяным паром связана с высокой чувствительностью прибора к водороду. Следы углерода наблюдаются и после 2 ч окислительной регенерации катализатора водой при температуре печи реактора 750°С.
Вероятно, водород образуется не только в ходе реакции окисления волокнистого углерода (whisker carbon), но и при паровой конверсии сажи полимерной природы (gum carbon), содержащей в своем составе водород.
Водород, выделяющийся в реакциях (III), (IV), участвует в образовании метана (реакции (V)–(VII)), наличие которого также наблюдали на выходе из реактора:
(VI)
${\text{СO + 3}}{{{\text{H}}}_{{\text{2}}}} \rightleftarrows {\text{C}}{{{\text{H}}}_{{\text{4}}}}{\text{ + }}{{{\text{H}}}_{{\text{2}}}}{\text{O}},\,\,\,\,\Delta H < 0,$(VII)
${\text{С}}{{{\text{O}}}_{{\text{2}}}}{\text{ + 4}}{{{\text{H}}}_{2}} \rightleftarrows {\text{C}}{{{\text{H}}}_{{\text{4}}}}{\text{ + 2}}{{{\text{H}}}_{{\text{2}}}}{\text{O}},~\,\,\,\,\Delta H < 0.$Стоит отметить, что водяного пара в мольном соотношении подавали в ~13 раз больше, чем кислорода (табл. 1). Судя по динамике падения интенсивности сигнала СО2, удаление углеродных отложений кислородом практически завершается после 170 мин проведения процесса. В случае же регенерации водяным паром даже после 200 мин наблюдается ее активное протекание, поскольку не отмечается существенного снижения интенсивности сигналов СО, СО2 и Н2. В нашей предыдущей работе было продемонстрировано, что регенерация кислородом воздуха способствует полному удалению углерода с поверхности, не вызывая разрушения его микроструктуры [28].
Исследования показали, что окисление углерода, образовавшегося в ходе АТР дизельного топлива, кислородом воздуха – наиболее эффективный способ регенерации катализатора. Скорость окисления углеродных отложений водяным паром при температурах АТР ДТ задает межрегенерационный период работы катализатора, являясь одной из важнейших характеристик катализатора. Проведения процедуры регенерации катализатора можно избежать, если удастся создать реакционные условия, в которых скорость углеродообразования не будет превышать скорость окисления углеродных отложений водяным паром. Согласно термодинамическим расчетам и полученным результатам экспериментальных исследований пары воды эффективно окисляют углерод только при температурах >650°С, поэтому для обеспечения стабильной работы катализатора на реальном ДТ, содержащем ди- и полиароматические углеводороды, необходимо повысить температуру концевой части блока. Это может быть достигнуто за счет увеличения входного отношения О2/С.
ЗАКЛЮЧЕНИЕ
В представленной работе проведено исследование дезактивации структурированного Rh-содержащего катализатора в ходе автотермического риформинга дизельного топлива. Установлено, что нановолокнистые углеродные отложения размером 5–50 мкм образуются на поверхности как передней, так и концевой частей каталитического блока и не вызывают отслоения и повреждения активного компонента. Расположение углеродных отложений на внешней поверхности каталитического покрытия упрощает процесс регенерации катализатора.
Из двух изученных процессов удаления сажи с поверхности катализатора (кислородом и водяным паром) наиболее эффективным способом регенерации является окисление углерода кислородом. Водяной пар также вступает в реакцию с углеродом с выделением H2, CO, CO2 и CH4. Так как в условиях автотермического риформинга дизельного топлива вода подается в избытке, существует принципиальная возможность создания реакционных условий, позволяющих катализатору саморегенерироваться непосредственно в ходе протекания процесса АТР ДТ.
В результате выполненной работы показано, что приготовленный каталитический блок стабилен и регенерируется в условиях автотермического риформинга дизельного топлива, нарушения морфологии и деградация микроструктуры не наблюдаются ни в лобовой части, ни на выходе из блока [28].
Список литературы
Бадмаев С.Д., Беляев В.Д., Собянин В.А. // Кинетика и катализ. 2022. Т. 63. С. 394.
Горлова А.М., Симонов П.А., Стонкус О.А., Пахарукова В.П., Снытников П.В., Потемкин Д.И. // Кинетика и катализ. 2021. Т. 62. № 6. С. 773.
Юсенко М.В., Беляев В.Д., Демин А.К., Бронин Д.И., Саланов А.Н., Собянин В.А., Снытников П.В., Потемкин Д.И. // Кинетика и катализ. 2022. Т. 63. № 1. С. 138.
Shigarov A.B., Kireenkov V.V., Kuzmin V.A, Kuzin N.A, Kirillov V.A. // Catal. Today. 2009. V. 144. № 3–4. P. 341.
Alvarez-Galvan M.C., Navarro R.M, Rosa F., Briceño Y., Gordillo Alvarez F., Fierro JL.G. // Int. J. Hydrogen Energy. 2008. V. 33. № 2. P. 652.
Bae J., Lee S., Kim S., Oh J., Choi S., Bae M., Kang I., Katikaneni S.P. // Int. J. Hydrogen Energy. 2016. V. 41. № 44. P. 19990.
Bae M., Cheon H., Oh J., Kim D., Bae J., Katikaneni S.P. // Int. J. Hydrogen Energy. 2021. V. 46. № 52. P. 26575.
Ju D.G., Jo S.B., Ha D.S., Kim T.Y., Jung S.Y., Chae H.J., Lee S.C., Kim J.C. // Catalysts. 2019. V. 9. № 7. P. 573.
Karatzas X., Jansson K., Dawody J., Lanza R., Pettersson L.J. // Appl. Catal. B: Env. 2011. V. 101. № 3–4. P. 226.
Karatzas X., Dawody J., Grant A., Svensson E.E., Pettersson L.J. // Catal. Today. 2011. P. 515.
Kim D., Choi S., Jeong S., Bae M., Katikaneni S.P., Bae J., Heo S., Lee J.H. // Chem. Eng. J. 2021. V. 424. P. 13 0564.
Pasel J., Samsun R.C., Meißner J., Tschauder A., Peters R. // Int. J. Hydrogen Energy. 2019. V. 11. P. 137.
Rogozhnikov V.N., Kuzin N.A., Snytnikov P.V., Potemkin D.I., Shoynkhorova T.B., Simonov P.A., Shilov V.A., Ruban N.V., Kulikov A.V., Sobyanin V.A. // Chem. Eng. J. 2019. V. 374. P. 511.
Rogozhnikov V.N., Potemkin D.I., Ruban, N.V., Shilov V.A., Salanov A.N., Kulikov A.V., Simonov P.A., Gerasimov E.Y., Sobyanin V.A., Snytnikov P.V. // Mater. Lett. 2019. V. 257. P. 126715.
Samsun R.C., Prawitz M., Tschauder A., Meißner J., Pasel J., Peters R. // Appl. Energy. 2020. V. 279. P. 115 882.
Shekhawat D., Gardner T.H., Berry D.A., Salazar M., Haynes D.J., Spivey J.J. // Appl. Catal. A: Gen. 2006. V. 311. № 1–2. P. 8.
Shilov V.A., Rogozhnikov V.N., Zazhigalov S.V., Potemkin D.I., Belyaev V.D., Shashkov M.V., Zagoruiko A.N., Sobyanin V.A., Snytnikov P.V. // Int. J. Hydrogen Energy. 2021. V. 46. № 72. P. 35866.
Shilov V.A., Rogozhnikov V.N., Ruban N.V., Potemkin D.I., Simonov P.A., Shashkov M.V., Sobyanin V.A., Snytnikov P.V. // Catal. Today. 2021. V. 379. P. 42.
Shilov V.A., Rogozhnikov V.N., Potemkin D.I., Belyaev V.D., Shashkov M.V., Sobyanin V.A., Snytnikov P.V. // Int. J. Hydrogen Energy. 2022. V. 47. № 21. P. 11316.
Younis M.N., Malaibari Z.O., Ahmad W., Ahmed S. // Energy and Fuels. 2018. V. 32. № 6. P. 7054.
Zazhigalov S.V., Rogozhnikov V.N., Snytnikov P.V., Potemkin D.I., Simonov P.A., Shilov V.A., Ruban N.V., Kulikov A.V., Zagoruiko A.N., Sobyanin V.A. // Chem. Eng. Process. Process Intensif. 2020. V. 150. P. 107876.
Zazhigalov S.V., Shilov V.A., Rogozhnikov V.N., Potemkin D.I., Sobyanin V.A., Zagoruiko A.N., Snytnikov P.V. // Catal. Today. 2021. V. 378. P. 240.
Zazhigalov S.V., Shilov V.A., Rogozhnikov V.N., Potemkin D.I., Sobyanin V.A., Zagoruiko A.N., Snytnikov P.V. // Chem. Eng. J. 2022. V. 442. P. 136 160.
Симонов П.А., Шойнхорова Т.Б., Снытников П.В., Потемкин Д.И., Беляев В.Д. Патент RU 2653360 C1, 2017.
Porsin A.V., Kulikov A.V., Rogozhnikov V.N., Serkova A.N., Salanov A.N., Shefer K.I. // Catal. Today. 2016. V. 273. P. 213.
Reshetnikov S.I., Petrov R.V., Zazhigalov S.V., Zagoruiko A.N. // Chem. Eng. J. 2020. V. 380. P. 122374.
Shoynkhorova T.B., Simonov P.A., Potemkin D.I., Snytnikov P.V., Belyaev V.D., Ishchenko A.V., Svintsitskiy D.A., Sobyanin V.A. // Appl. Catal. B: Env. 2018. V. 237. P. 237.
Шилов В.А., Рогожников В.Н., Потемкин Д.И., Снытников П.В. // Кинетика и катализ. 2023. Т. 64. № 1. (в печати).
Дополнительные материалы отсутствуют.
Инструменты
Кинетика и катализ