Коллоидный журнал, 2019, T. 81, № 6, стр. 795-802
Адсорбционная и термическая деформация микропористого углеродного адсорбента при адсорбции н-октана
А. В. Школин 1, *, А. А. Фомкин 1, И. Е. Меньщиков 1, А. Л. Пулин 1, В. Ю. Яковлев 1
1 Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119071 Москва, Ленинский проспект, 31, Россия
* E-mail: shkolin@bk.ru
Поступила в редакцию 26.04.2019
После доработки 13.05.2019
Принята к публикации 16.05.2019
Аннотация
Измерена относительная линейная адсорбционная деформация гранул микропористого углеродного адсорбента АР-В при адсорбции н-октана в интервале давления p от 1 Па до 1.6 кПа и значениях температуры T = 273, 293, 313, 353 и 393 К. При p > 200 Па адсорбционная деформация положительна и растет с увеличением p во всем исследуемом температурном интервале. В изобарных условиях адсорбционная деформация увеличивается с понижением T, при этом крутизна изотерм деформации возрастает. В области p < 200 Па и при T < 350 К, адсорбционная деформация отрицательна. Область сжатия адсорбента уменьшается с ростом T, и при T > 350 K адсорбент расширяется во всем интервале давлений. Методом молекулярной динамики исследована структура адсорбционных ассоциатов н-октана в модельных щелевидных микропорах, имеющих ширину, соответствующую эффективному размеру микропор адсорбента АР-В, рассчитанному по теории объемного заполнения микропор. Структура адсорбционных ассоциатов соотнесена с характерными особенностями адсорбционной деформации адсорбента АР-В.
ВВЕДЕНИЕ
Взаимодействие адсорбированных молекул с поверхностью твердого тела вызывает его деформацию [1–4]. Этот эффект особенно ярко выражен при адсорбции на микропористых адсорбентах, поры которых соизмеримы по размерам с адсорбируемыми молекулами. Поскольку сжимаемость твердых тел обычно невелика, то деформация относительно “жестких” адсорбентов, таких как активные угли, при адсорбции газов и паров также невелика и, как правило, не превосходит нескольких процентов [5–12]. При этом обычно не происходит существенного изменения прочности и адсорбционной активности адсорбента, если относительное давление далеко от давления насыщения. Однако увеличение относительного давления паров и его приближение к давлению насыщения приводит к экстремальному нарастанию деформации расширения и разрушению гранул адсорбента [13].
Исследования адсорбционной деформации крайне важны для развития термодинамики адсорбции, особенно в области высоких давлений, а также для разработки новых процессов высокоскоростного разделения газов, сопровождающихся волновой сорбострикцией при адсорбции смесей веществ [14–16]. С практической точки зрения исследование адсорбционной деформации позволяет найти подходы к оценке увеличения срока службы адсорбентов в периодических процессах и оптимизации их параметров.
Ввиду отсутствия четких представлений о деформационном поведении адсорбентов для широкого круга адсорбционных систем, для оценки величин деформации и ее влияния на промышленные адсорбционные процессы предпочтительным представляется исследование адсорбционной деформации промышленного углеродного адсорбента с широким распределением пор по размерам и развитым объемом микро- и мезопор.
Данная работа посвящена исследованию адсорбционной деформации углеродного адсорбента АР-В, применяемого для очистки газов и имеющего широкое распределение пор по размерам и высокую степень гетерогенности поверхности, при адсорбции н-октана в широком температурном интервале.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Адсорбент АР-В
Адсорбент АР-В – промышленный микропористый углеродный адсорбент, полученный из каменноугольной пыли и лесотехнической смолы методом парогазовой активации. Щелевидные микропоры образуются в адсорбенте в процессе парогазовой активации при 800–900°C при селективном выгорании отдельных гексагональных слоев углерода в графитоподобных нанокристаллитах [17].
Содержание углерода в таком адсорбенте по данным элементного анализа составляет около 85%, кислорода – около 8%, кремния – 2.9%, алюминия – 2.2%; остальные примеси представлены в основном железом, кальцием и серой.
Структурно-энергетические характеристики АР-В определяли по изотерме адсорбции азота при 77 К на установке Autosorb iQ (Quantachrome). Характеристики пористой структуры рассчитывали с использованием теории объемного заполнения микропор Дубинина (ТОЗМ) [18] для микропор и уравнения Кельвина [19] для мезопор.
Адсорбент АР-В имеет следующие характеристики: суммарный объем пор WS = 0.49 см3/г, удельный объем мезопор WME = 0.21 см3/г, удельный объем микропор W0 = 0.28 см3/г, характеристическая энергия адсорбции в пересчете на бензол E0= 19.5 кДж/моль, эффективная полуширина (радиус) микропор х0= 0.64 нм, удельная поверхность по БЭТ SБЭТ = 780 м2/г, удельная поверхность мезопор SМЕ = 80 м2/г.
Адсорбтив н-октан
В качестве адсорбтива использовали н-октан (н-С8Н18) марки “хроматографически чистый” с массовой долей основного вещества 99.9%. Перед измерениями н-октан дегазировали путем криовакуумной перегонки. Чистоту н-октана после дегазации проверяли путем сверки давления насыщенного пара н-октана при 273 K со справочными данными [20]. Различия составили менее 0.1%. По данным [20] н-октан обладает следующими физико-химическими характеристиками: критическая температура Tcr = 569.2 К, критическое давление Рcr = 2.496 МПа, критическая плотность ρcr= 235.0 кг/м3, температура кипения Тb= 398.66 К, температура плавления Tm = 216.22 К.
Методика эксперимента
Величины адсорбционной деформации измеряли с помощью дилатометра индукционного типа на универсальной адсорбционно-дилатометрической установке, разработанной в ИФХЭ РАН [21]. Эксперименты проводили с гранулами адсорбента АР-В цилиндрической формы со специально обработанными торцами (высота – 6.75 мм, диаметр около 3.2 мм).
В опытах измеряли линейную деформацию гранул, т.е. изменение длины l образца с ростом равновесного давления адсорбтива (н-октана) при заданной температуре T. Погрешность определения l – примерно ±5 × 10–7 м с доверительной вероятностью 95%, что для исследуемого образца адсорбента составляет ±0.005%.
Непосредственно перед каждым экспериментом дилатометр с адсорбентом заполняли газообразным азотом чистотой не менее 99.999% до атмосферного давления и выдерживали при 333 К в течение 1 ч для десорбции примесей из порового пространства. Затем проводили регенерацию адсорбента при 533 К в течение 6 ч до достижения статического вакуума менее 0.1 Па.
Давление p н-октана в диапазоне 0.13 Па…130 кПа измеряли манометрами абсолютного давления М10 и М1000, разработанными и изготовленными в ИФХЭ РАН. Погрешность измерения p манометром М10 в интервале 0.13…1330 Па составляла ±0.066 Па, а манометром М1000 в интервале 13 Па…130 кПа равнялась ±4.0 Па.
Температуру образца адсорбента в интервале от 293 до 353 К поддерживали с помощью жидкостного термостата с погрешностью ±0.05 К, при T ≥ 373 К использовали электрический термостат, позволявший поддерживать температуру с погрешностью ±0.2 К.
Исследование адсорбции как полного содержания (абсолютная адсорбция) н-октана на АР-В проводили гравиметрическим методом на адсорбционном стенде, разработанном в ИФХЭ РАН, по методике, описанной в [22]. Перед измерением проводили регенерацию адсорбента при T = 573 ± 10 K до остаточного давления не более 0.1 Па. Суммарная и расширенная неопределенности измерения адсорбции составили не более 1.5 и 4% соответственно при доверительном уровне 99%.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Зависимость относительной линейной деформации адсорбента АР-В от давления н-октана
Зависимости относительной линейной адсорбционной деформации Δl/l микропористого углеродного адсорбента АР-В от p н-октана в интервале от 1 Па до 1.6 кПа при T от 273 до 393 К представлены на рис. 1. Как следует из рис. 1, за исключением небольшой начальной области, при р < 200 Па, адсорбционная деформация АР-В положительна, обратима и растет с увеличением р во всем исследуемом температурном интервале. В этой области при одном и том же р, адсорбционная деформация увеличивается с понижением T, при этом крутизна изотерм деформации возрастает. Максимальное расширение адсорбента наблюдается при T = 273 К при давлениях, близких к р насыщенного пара, и составляет 0.38%.
Рис. 1.
Зависимости относительной линейной адсорбционной деформации АР-В от давления н-октана при 273.1 (1), 293 (2), 313 (3), 353 (4) и 393 К (5). Символы – экспериментальные данные, линии – сплайн-аппроксимация. Пунктир – линия давления насыщенного пара н-октана при 273 К.

Характерно, что качественно так же ведут себя кривые адсорбционной деформации полностью микропористого адсорбента АУК при адсорбции углеводородов. Это показано при изучении адсорбции метана [8], н-гептана [11], н-пентана [12], н-октана [23].
Однако, в отличие от адсорбента АУК, адсорбент АР-В сжимается в начальной области давлений (р < 200 Па) при T < 313 К (рис. 2). При этом максимальное сжатие наблюдается при минимальной исследованной температуре 273 К и составляет около 0.12%, что примерно в 3 раза меньше максимального расширения АР-В при этой температуре. С ростом T начальное сжатие адсорбента уменьшается и при T = 353 К переходит в расширение, которое также увеличивается с ростом температуры. При T = 393 К начальное расширение адсорбента составляет около 0.04%, что в среднем в 4 раза меньше максимального расширения при данной T.
Подобное поведение деформационных зависимостей, которое можно видеть на рис. 2, в начальной области давлений характерно для большинства исследованных адсорбционных систем и уже отмечалось ранее [8, 13, 24].
Тем не менее, имеются и отличия. В частности, при адсорбции н-октана на микропористом углеродном адсорбенте АУК адсорбционная деформация при тех же значениях T в начальной области заполнения микропор отсутствует [23]. Вероятной причиной такого поведения являются стерический фактор, т.е. соотношение эффективного диаметра d микропор адсорбента (для АР-В d = 1.28 нм, для АУК d = 0.82 нм) и эффективного диаметра молекулы н-октана (d = 0.49 нм), определенного из данных по молекулярно-ситовым свойствам цеолитов [25].
Для дальнейшего анализа зависимости адсорбционной деформации углеродного адсорбента АР-В от величины заполнения порового пространства исследовали адсорбцию н-октана в тех же интервалах температуры и давления.
Адсорбция н-октана на углеродном адсорбенте АР-В
На рис. 3 представлены изотермы адсорбции н-октана на адсорбенте АР-В в том же интервале изменения параметров адсорбционного равновесия, что и деформационные зависимости.
Рис. 3.
Изотермы адсорбции н-октана на адсорбенте АР-В при 273.1 (1), 293 (2), 313 (3), 353 (4) и 393 К (5). Символы – экспериментальные данные, линии – сглаживающие кривые.

Как следует из рис. 3, адсорбция н-октана в изобарных условиях падает с ростом температуры, что характерно для физической адсорбции. Начальный интенсивный рост адсорбции связан с высокой гетерогенностью адсорбента. В области малых заполнений молекулы н-октана заполняют высокоэнергетические адсорбционные центры в микропорах, а при переходе в область средних и высоких заполнений, когда все такие центры заняты, адсорбция протекает по механизму объемного заполнения.
Зависимость относительной линейной деформации адсорбента АР-В от адсорбции н-октана
На основе экспериментальных изотерм адсорбции a = f(p), приведенных на рис. 3, и изотерм адсорбционной деформации (Δl/l) = f(p) (рис. 1) были построены зависимости деформации адсорбента от адсорбции (Δl/l) = f(а) для системы н-октан–АР-В. Результаты представлены на рис. 4.
Рис. 4.
Зависимости относительной линейной адсорбционной деформации адсорбента АР-В от адсорбции н-октана при 273.1 (1), 293 (2), 313 (3), 353 (4) и 393 К (5). Символы – экспериментальные данные, линии – сглаживающие кривые.

Как следует из рис. 4, адсорбент АР-В при T ≤ ≤ 313 K с ростом адсорбции н-октана сначала относительно медленно сжимается, а затем резко расширяется. При этом интенсивность нарастания деформации расширения уменьшается с увеличением T. При T > 313 К адсорбент АР-В расширяется при всех значениях адсорбции н-октана. В этой температурной области начальное расширение тем больше, чем выше T. Такое поведение адсорбционной деформации адсорбента АР-В в области повышенных температур может быть следствием наложения нескольких факторов – увеличения сжимаемости (расширяемости) твердого тела с ростом T и перехода адсорбции молекул н-октана в микропорах от частично локализованной к нелокализованной с ростом T. При этом с ростом T должен расти вклад кинетической энергии движения молекул и внутреннего давления в микропорах даже при малых заполнениях. Рост адсорбции, а, следовательно, и увеличение внутреннего давления приводит к перераспределению молекул в микропорах и нарастанию сил отталкивания.
В области максимальных величин адсорбции для T = 273.1–313 К величины деформации адсорбента АР-В становятся близкими. Такая необычная зависимость адсорбционной деформации от T может быть связана с нелинейным изменением температурного коэффициента расширения твердого тела (адсорбента). В связи с этим измерили зависимость термической деформации адсорбента АР-В в вакууме [24].
Результаты измерений представлены на рис. 5. Как следует из рис. 5, при изменении температуры от 310 до 260 К деформация адсорбента АР-В слабо зависит от температуры, а термический коэффициент линейного расширения (ТКЛР) адсорбента АР-В (dη/dТ) меняет знак с положительного на отрицательный, с 8.8 × 10–5 до примерно –3 × 10–5 1/K [24]. Такое поведение ТКЛР твердых тел отмечалось и ранее [26], в том числе при исследовании металлорганических каркасных структур [27, 28].
Рис. 5.
Зависимость термической деформации адсорбента АР-В в вакууме от температуры. За нулевое значение деформации принято значение при температуре 260 К.

Характер термической деформации микропористого углеродного адсорбента АР-В качественно совпадает с таковым для термической деформации графита [29]. Данный факт является следствием сходства морфологий активного угля АР-В и кристаллов графита. По данным рентгенографического анализа 1 г адсорбента АР-В содержит в своей структуре порядка 1020 графитоподобных нанокристаллитов (турбостратные структуры), хаотически ориентированных в его гранулах [30].
Численное моделирование адсорбции н-октана на адсорбенте АР-В
Для понимания процессов, происходящих в микропорах исследуемого адсорбента при адсорбции н-октана и стимулирующих его деформацию, мы провели моделирование методом молекулярной динамики адсорбции н-октана в модельных щелевидных микропорах.
В качестве модели микропоры адсорбента АР‑В была принята щелевидная пора, стенки которой образованы двумя графеновыми слоями квадратной формы со стороной около 1.5 нм. Углерод в этих слоях находится в гексагональной координации. Висячие связи атомов углерода на краях слоев компенсированы атомами водорода. Боковая поверхность поры – щель, открытая для адсорбции. Расстояние между графеновыми слоями (ширина поры) Х0 = 1.28 нм выбрана равной средней эффективной ширине поры с учетом радиуса C-атомов, определенной по ТОЗМ для адсорбента АР-В. Средний размер графеновых слоев, образующих модельную микропору, выбрали на основе данных о размере углеродных нанокристаллитов в активных углях [30]. В ячейку моделирования помещали различное количество молекул н-октана, от 20 до 240. Температура системы составляла 293 К.
На рис. 6 представлены мгновенные снимки молекулярно-динамической траектории для модельной поры при содержании в ячейке моделирования 20 и 200 молекул н-октана.
Рис. 6.
Мгновенный снимок молекулярно-динамической траектории молекул н-октана в щелевидной микропоре при наличии в ячейке моделирования 20 и 200 молекул. Атомы C молекул н-октана показаны черными кружками, атомы H – светлыми. Две структурированные плоскости соответствуют графеновым слоям, образующим щелевидную пору.

Расчеты показали, что в области малых заполнений молекулы н-октана статистически достоверно располагаются планарно вблизи стенок поры. При этом в области средних заполнений часть молекул ориентируется преимущественно по нормали к стенкам пор, соединяя слои молекулярного ассоциата, расположенные у противоположных стенок. С ростом заполнения доля молекул, расположенных под углом к поверхности графеновых слоев, достоверно растет.
Отметим, что наличие молекул, соединяющих слои молекулярного ассоциата в микропоре в области средних заполнений (20 молекул в системе моделирования), свидетельствует в пользу теории Лакханпала и Флада, которые предполагали, что эффект сжатия в области малых и средних заполнений обусловлен возникновением “мостика”, который “стягивает” противоположные стенки пор [31].
В области высоких заполнений адсорбент расширяется за счет увеличения внутреннего давления в поре. На рис. 7 представлены распределения плотности вероятности нахождения молекул в модельной микропоре при разном количестве молекул н-октана в системе моделирования.
Рис. 7.
Зависимость плотности вероятности нахождения молекул dz от ширины поры х0 при наличии в системе 20 (1), 40 (2), 80 (3), 120 (4), 160 (5), 200 (6) и 240 (7) молекул н-октана. Температура 293 К. (х0 = 0 – центр поры).

Как следует из рис. 7, когда в системе находится всего 20 молекул н-октана, профиль плотности вероятности нахождения молекул в поре имеет два ярко выраженных максимума вблизи стенок поры и слабо выраженные флуктуации вероятности в центре поры, связанные с появлением незначительного количества молекул, соединяющих ее стенки. С ростом числа молекул в поре максимумы плотности вероятности нахождения адсорбированных молекул вблизи стенок размываются в направлении центра поры. Отметим, что при наличии 20 молекул н-октана в системе моделирования в поре находится в среднем около 17 молекул, тогда как при наличии 240 молекул в поре находится в среднем 43 молекулы.
Исследование плотности вероятности пространственной ориентации связей С–С молекул н-октана в модельной поре (рис. 8), позволило установить, что эти связи находятся в поре преимущественно в трех состояниях. Одна часть связей образует с графеновыми слоями небольшой угол, до 10°, т.е. молекулы н-октана ориентируются параллельно стенкам. Вторая часть связей С–С ориентируется преимущественно под углом 45°…55°, т.е. поворачивается относительно поверхности стенки микропоры, что наблюдается как размытие и смещение максимума на плотности вероятности распределения молекул н-октана по ширине поры (см. рис. 7). Третья часть связей С–С ориентируется преимущественно под углом 75°…85°, т.е. почти перпендикулярно графеновым стенкам.
Рис. 8.
Плотность вероятности ориентации молекулы н-октана в модельной поре dφ при наличии в системе 20 (1), 40 (2), 80 (3), 120 (4), 160 (5), 200 (6) и 240 (7) молекул н-октана. Зависимость построена в полярных координатах. В скобках указаны главные плоскости в системе моделирования, относительно которых анализируется ориентация молекул: (xy) – плоскость поры, параллельная графеновым слоям, z – плоскость поры, перпендикулярная этим слоям.
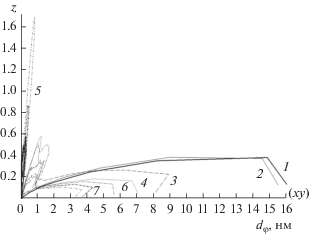
Анализ результатов, представленных на рис. 8, в первом приближении свидетельствует об уменьшении вероятности расположения молекул н-октана параллельно стенкам модельной поры с увеличением их количества в системе, т.е. с ростом адсорбции. Часть молекул с ростом адсорбции ориентируется либо под углом 45°…55° относительно поверхности углеродных стенок, либо практически перпендикулярно им. Таким образом, механизм адсорбции в анализируемом случае изменяется. Имеет место переход от частично локализованной адсорбции вблизи стенок поры при малых заполнениях к объемному заполнению пор в области средних и высоких заполнений.
Переход к объемному заполнению микропор и переориентация молекул в них связаны, прежде всего, с уменьшением среднего расстояния между адсорбированными молекулами, что увеличивает энергию отталкивания, и сжатие адсорбента сменяется его расширением.
ЗАКЛЮЧЕНИЕ
Исследована деформация микропористого углеродного адсорбента АР-В, стимулированная адсорбцией н-октана при температуре 273, 293, 313, 353 и 393 К в интервале давления от 1 Па до 1.6 кПа. В области температур ниже 313 K адсорбент сначала сжимается, а затем, с ростом адсорбции, расширяется. Эффекты сжатия и расширения адсорбента растут с понижением температуры. Зависимости деформации от адсорбции для разных значений температуры сближаются, вероятно, вследствие изменения знака температурного коэффициента линейного расширения самого адсорбента. При температуре выше 313 K адсорбент расширяется с ростом адсорбции во всем исследованном интервале давлений.
Анализ адсорбции н-октана в модельной щелевидной микропоре, проведенный методом молекулярной динамики, показал, что характер деформационной зависимости определяется, с одной стороны, соотношением размера молекул н-октана и средних размеров микропор, а с другой стороны, – механизмом адсорбции. В области малых заполнений, когда молекулы н-алкана адсорбируются по механизму частичной локализации вблизи стенок пор, адсорбент АР-В сжимается. Это, вероятно, связано с увеличением притяжения между стенками микропор за счет дополнительного вклада в баланс сил твердого тела молекул, находящихся вблизи стенок. Следует отметить, что для более узких пор, когда адсорбированные молекулы находятся в центре микропоры, такого эффекта не наблюдается [23].
С ростом количества молекул в поре уменьшается среднее расстояние между адсорбированными молекулами, при этом изменяется и механизм адсорбции: имеет место переход от частично локализованной адсорбции к объемному заполнению микропор, увеличиваются силы отталкивания, и сжатие адсорбента сменяется его расширением.
Список литературы
Ребиндер П.А. // Успехи физ. наук. 1972. Т. 108. С. 3.
Русанов А.И. // Докл. АН. 2006. Т. 406. С. 776.
Русанов А.И. Термодинамические основы механохимии. СПб.: Наука, 2006.
Русанов А.И. // Коллоид. журн. 2007. Т. 69. С. 861.
Фомкин А.А., Школин А.В., Пулин А.Л., Меньщиков И.Е., Хозина Е.В. // Коллоид. журн. 2018. Т. 80. С. 610.
Школин А.В., Потапов С.В., Фомкин А.А. // Колл-оид. журн. 2015. Т. 77. С. 802.
Потапов С.В., Школин А.В., Фомкин А.А. // Ко-ллоид. журн. 2014. Т. 76. С. 382.
Школин А.В., Фомкин А.А. // Коллоид. журн. 2009. Т. 71. С. 116.
Balzer C., Wildhage T., Braxmeier S., Reichenauer G., Olivier J.P. // Langmuir. 2011. V. 27. P. 2553.
Yakovlev V.Yu., Fomkin A.A., Tvardovski A.V. // J. Colloid Interface. Sci. 2004. V. 280. P. 305.
Школин А.В., Фомкин А.А. // Физикохимия поверхности и защита материалов. 2013. Т. 49. С. 345.
Школин А.В., Фомкин А.А., Синицын В.А. // Физикохимия поверхности и защита материалов. 2011. Т. 47. С. 451.
Yakovlev V.Y., Fomkin A.A., Tvardovski A.V. // J. Colloid Interface Sci. 2003. V. 268. P. 33.
Fomkin A.A. // Adsorption. 2005. V. 11. P. 425.
Фомкин А.А., Школин А.В. // Докл. АН. 2008. Т. 423. С. 80.
Фомкин А.А., Школин А.В., Петухова Г.А. // Физикохимия поверхности и защита материалов. 2012. Т. 48. С. 138.
Фенелонов В.Б. Пористый углерод. Новосибирск: ИК СО РАН, 1995.
Дубинин М.М. Адсорбция и пористость. М.: ВАХЗ, 1972.
Экспериментальные методы в адсорбции и хроматографии / Под ред. Киселева А.В., Древинга В.П. М.: Изд-во МГУ, 1973.
Варгафтик Н.Б. Справочник по теплофизическим свойствам газов и жидкостей. М.: Наука, 1972.
Школин А.В., Фомкин А.А., Пулин А.Л., Яковлев В.Ю. // Приборы и техника эксперимента. 2008. № 1. С. 163.
Школин А.В., Фомкин А.А. // Измерительная техника. 2018. № 4. С. 56.
Школин А.В., Фомкин А.А., Меньщиков И.Е., Пулин А.Л., Яковлев В.Ю. // Коллоид. журн. 2019. Т. 81. C. 667.
Меньщиков И.Е., Школин А.В., Фомкин А.А. // Измерительная техника. 2017. № 10. С. 58.
Кельцев Н.В. Основы адсорбционной техники. М.: Химия, 1976.
Barrera G.D., Bruno J.A.O., Barron T.H.K., Allan N.L. // J. Phys.: Condens. Matter. 2005. V. 17. R217.
Dubbeldam D., Walton K.S., Ellis D.E., Snurr R.Q. // Angew. Chem. Int. Ed. 2007. V. 46. P. 4496.
Peterson V.K., Kearley G.J., Wu Y., Ramirez-Cuesta A.J., Kemner E., Kepert C.J. // Angew. Chem. Int. Ed. 2010. V. 49. P. 585.
Новикова С.И. Тепловое расширение твердых тел. М.: Наука, 1974.
Дубинин М.М. // Углеродные адсорбенты и их применение в промышленности / Под ред. Плачено-ва Т.Г. М.: Наука, 1983. С. 100.
Lakhanpal M.L., Flood E.A. // Can. J. Chem. 1957. V. 35. P. 887.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал



