Коллоидный журнал, 2021, T. 83, № 3, стр. 311-319
Химический состав, структура и электрокинетический потенциал никель- и железосодержащих стеклообразных материалов
А. С. Кузнецова 1, 2, *, Л. Э. Ермакова 1, Т. В. Антропова 2, И. Н. Анфимова 2, А. В. Волкова 1
1 Санкт-Петербургский государственный университет
199034 Санкт-Петербург, Университетская наб., 7/9, Россия
2 Институт химии силикатов им. И.В. Гребенщикова РАН
199034 Санкт-Петербург, наб. Адмирала Макарова, 2, Россия
* E-mail: a_kuznetsova95@mail.ru
Поступила в редакцию 28.12.2020
После доработки 08.01.2021
Принята к публикации 13.01.2021
Аннотация
Исследованы химический состав, структура и электрокинетические характеристики различных стеклообразных материалов – базовых силикатных и модифицированных в процессе варки стекла оксидами железа и никеля. Проанализировано влияние химического состава материала и структуры поверхности на положение изоэлектрической точки и величины электрокинетического потенциала для монолитных частиц (двухфазных стекол и кварцоидов) и микропористых образцов, полученных путем кислотного выщелачивания, в растворе индифферентного электролита NaCl. Изучено влияние специфически сорбирующихся ионов никеля на электрокинетические характеристики силикатных и никельсодержащих стеклообразных материалов.
ВВЕДЕНИЕ
Развитие современных технологий ставит задачу получения новых композитных наноструктурированных материалов с практически важными функциональными (магнитными, оптическими, электрическими и др.) характеристиками [1]. Одним из классов таких наноструктур являются обладающие магнитными свойствами монолитные и пористые стеклообразные материалы, которые особенно интересны благодаря низкой стоимости, химической, термической и механической стабильности, а также невысокой кислотности поверхности, обусловленной силанольными и боранольными группами [2–11]. Наноструктурированные стеклообразные композиты могут быть получены путем добавки легирующих компонентов, например оксида железа(III), в шихту при варке щелочноборосиликатных стекол [12–15]. Синтезированное таким способом монолитное стекло содержит включения магнетита, и при его дальнейшей термической и химической обработке получают высококремнеземные пористые магнитные материалы, использующиеся в качестве сорбентов, компонентов микроэлектронных устройств и сенсоров, базовых матриц для мультиферроиков и т.п. [16–21]. Такого типа пористые материалы с магнитными свойствами могут быть получены и при использовании в качестве легирующего компонента оксида никеля. Пористые стекла являются также прекурсорами для получения монолитных кварцоидных наноструктурированных материалов.
Свойства наноструктурированных систем, в том числе и их функциональные характеристики, в первую очередь определяются параметрами их поверхности и процессами, происходящими на границе фаз. Одним из наиболее важных параметров заряженной поверхности, доступных экспериментальному определению, является электрокинетический потенциал. Поэтому представляет интерес исследовать и сопоставить характеристики исходных монолитных и пористых образцов, изготовленных из базового натриевоборосиликатного стекла, и материалов, полученных из натриевоборосиликатных стекол, модифицированных оксидами железа и никеля.
ОБЪЕКТЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В качестве объектов исследования были выбраны базовые натриевоборосиликатные стекла 8В-НТ заводской варки с двухкаркасной структурой. В лабораторных условиях заводское стекло заново гомогенизировали и подвергали стандартной термообработке при 550°C в течение 144 ч для достижения фазового равновесия [22]. Железосодержащие (Fe-4-6, Fe-4-7) и никельсодержащие (Ni-1, Ni-2) стекла были сварены в лабораторных условиях при температуре 1550°C и также термообработаны при 550°C в течение 144 ч. При варке таких двухфазных стекол в шихту добавляли оксиды железа(III) или никеля(III). Для получения микропористых (МИП) образцов со средними размерами поровых каналов 2.6–4.4 нм двухфазные стекла (диски или пластинки толщиной около 1 мм) выщелачивали растворами азотной (8В-НТ) или соляной (Fe-4-6, Fe-4-7, Ni-1) кислот [22, 23]. Из образцов базового пористого стекла 8В-НТ МИП и стекол Fe-4-6 МИП, Fe-4-7 МИП были также получены монолитные кварцоиды путем спекания материалов при 870°C (КС-8В-НТ) и 815°C (КС-Fe-4-6, КС-Fe-4-7), что обеспечивало схлопывание поровых каналов.
Изучение пористой структуры полученных микро- и макропористых стекол различного состава было проведено с помощью сканирующей электронной микроскопии (СЭМ, микроскоп Carl Zeiss Merlin).
Содержание компонентов в двухфазном стекле и пористых стеклах (в пересчете на оксиды) определяли как стандартными химико-аналитическими методами [24–27], так и с помощью энергодисперсионной рентгеновской спектроскопии (ЭДС, спектрометр INCAx-act, Oxford Instruments) и рентгенофазового анализа (настольный порошковый дифрактометр с медным и кобальтовым анодами D2 Phaser, Bruker). Идентификация фазы Fe3O4 проводилась с использованием базы данных порошковой дифракции Powder Diffraction File (PDF-2, 2011, номера карточек 01-089-0688 и 01-087-2334).
Для изучения электрокинетических характеристик стекол методом доплеровского электрофореза были использованы порошки монолитных и пористых стекол, полученные с помощью растирания в агатовой ступке. Измерения электрофоретической подвижности (Ue) частиц были проведены на фоне растворов NaCl, NaNO3 и NiCl2 с ионной силой 10–2 М в диапазоне pH от 1 до 9.5 на анализаторе Zetasizer Nano ZS (Malvern). Эксперименты проводили при температуре 20°C в универсальной капиллярной U-образной поликарбонатной кювете (DTS1060) с интегрированными позолоченными электродами.
Величины электрокинетического потенциала были рассчитаны по уравнению Смолуховского
где η – вязкость, ε, ε0 – диэлектрические проницаемости среды и вакуума соответственно.Измерение pH суспензий проводили с помощью pH-метра Seven Multi S47-К (Mettler Toledo). Погрешность измерений не превышала 0.1 единицы pH. Растворы электролитов готовили с использованием химических реактивов марки “ос. ч.” или “х. ч.” с использованием воды, деионизованной на установке УВОИ-“М-Ф”, с удельной электропроводностью ${{\kappa }_{{\text{V}}}}$ ≤ 1.5 × 10−6 Ом–1 см–1).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
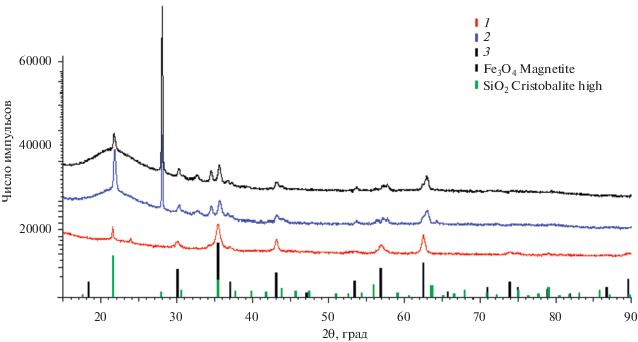
Данные о химическом составе двухфазных и пористых стекол, полученные аналитическими методами, суммированы в табл. 1. Наличие кристаллической фазы магнетита в двухфазных железосодержащих стеклах было также подтверждено с помощью метода рентгенофазового анализа. Пример дифрактограммы для стекла Fe-4-6 приведен на рис. 1.
Таблица 1.
Химический состав двухфазных и пористых стекол
| Стекло | Состав стекла, мол. % | ||||||
|---|---|---|---|---|---|---|---|
| Na2O | B2O3 | SiO2 | Al2O3 | Fe2O3 | FeO | NiO | |
| 8В-НТ [29] | 6.73 | 18.28 | 74.93 | 0.06 | – | – | – |
| Fe-4-6 [28] | 5.19 | 14.32 | 70.23 | – | 5.20 | 5.06 | – |
| Fe-4-7 [23] | 5.27 | 14.18 | 70.63 | – | 5.56 | 4.36 | – |
| Ni-1 | 7.40 | 12.62 | 65.60 | – | – | – | 14.38 |
| Ni-2 | 7.28 | 19.97 | 58.14 | – | – | – | 14.61 |
| 8В-НТ МИП [23] | 0.48 | 1.98 | 97.47 | 0.07 | – | – | – |
| Fe-4-4 МИП [29] | 0.97 | 4.79 | 89.18 | – | 2.35 | 2.71 | – |
Рис. 1.
Дифрактограммы железосодержащих стеклообразных материалов: 1 – Fe-4-6, 2 – КС-Fe-4-6, 3 – КС-Fe-4-7.
Стекло Fe-4-4 МИП получено из двухфазного железосодержащего стекла, близкого по составу к стеклам Fe-4-6 и Fe-4-7. Результаты анализа показывают (табл. 1), что как базовые, так и железосодержащие МИП-стекла, являются типичными высококремнеземными материалами, поскольку в процессе кислотного выщелачивания содержание кремнезема возрастает более чем до 89 мол. %. Видно также, что пористый образец сохраняет достаточно большое количество железа – суммарное содержание оксидов железа в матрице стекла составляет около 5 мол. %.
Исследования железосодержащих пористых стекол методом ЭДС показали, что распределение железа как по толщине образцов, так и по их поверхности достаточно равномерно, что согласуется с данными, полученными ранее для стекла Fe-4 [30]. Примеры полученных результатов приведены на рис. 2а и 2б (на рис. 2б железу соответствуют светлые точки). В табл. 2 указано найденное методом ЭДС содержание железа в поверхностных слоях образцов (эти величины являются результатом усреднения по нескольким спектрам). Анализ проводили для образца Fe-4-6 МИП, который в течение длительного времени контактировал с раствором электролита, и для образца Fe-4-7 МИП сразу после его получения. Видно, что длительный контакт с раствором приводит к значительному уменьшению содержания железа в поверхностном слое образца.
Рис. 2.
Распределение железа: (а) по толщине образца Fe-4-6 МИП [28], (б) по поверхности образца Fe-4-7 МИП.
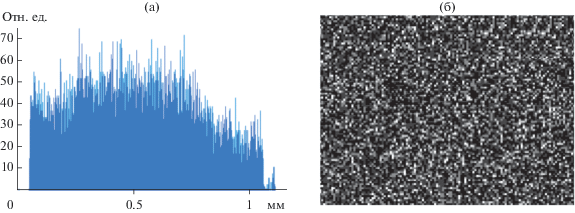
Таблица 2.
Относительное содержание металлов в исследованных образцах
| Содержание металла | Железо | Никель | ||
|---|---|---|---|---|
| Fe-4-6 МИП | Fe-4-7 МИП | Ni-1 | Ni-2 | |
| Весовые % | 2.59 | 5.00 | 14.99 | 14.72 |
| Атомные % | 1.14 | 1.70 | 5.07 | 5.16 |
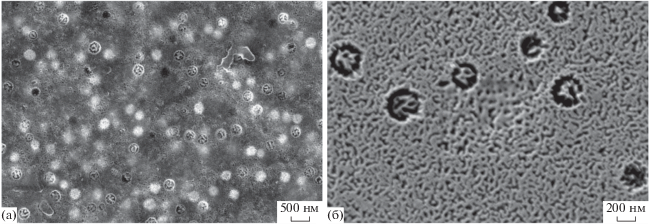
Примеры изображений содержащих магнетит микропористых стекол, полученные методом СЭМ, представлены на рис. 3. Видно, что для этих образцов характерно наличие в структуре гетерогенных областей округлой формы со средним размером порядка 200–300 нм. Данные неоднородности соответствуют расположению агломератов частиц магнетита (светлые участки). Темные “кратеры”, которые видны на поверхности стекла Fe-4-7 МИП, по-видимому, образовались за счет вымывания железосодержащей фазы при выщелачивании.
Рис. 3.
СЭМ-изображения поверхности железосодержащих пористых стеклообразных материалов: (а) Fe-4-6 МИП, (б) Fe-4-7 МИП.
Для образцов кварцоидов КС-Fe-4-6, КС-Fe-4-7, полученных из соответствующих МИП-стекол, был выполнен рентгенофазовый анализ, результаты которого представлены на рис. 1 (дифрактограммы 2, 3). Видно, что характер дифрактограмм исходного двухфазного стекла Fe-4-6 и кварцоидных материалов полностью совпадает.
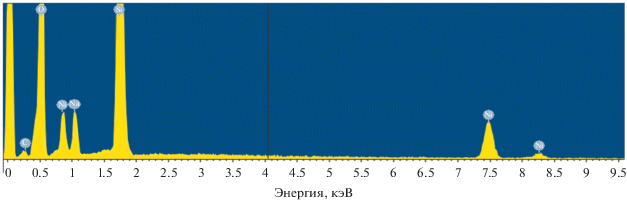
Пример ЭДС-спектра двухфазного никельсодержащего стекла Ni-1 приведен на рис. 4. В табл. 2 суммированы усредненные по 11–14 спектрам результаты определения содержания никеля в двухфазных стеклах. Видно, что полученные данные подтверждают результаты прямых аналитических измерений и свидетельствуют о близких характеристиках двух образцов никельсодержащего стекла. Рентгенофазовый анализ стекол Ni-1 и Ni-2 не выявил наличия кристаллической фазы оксида никеля в этих материалах. По-видимому, оксид никеля в синтезированных стеклах мог находиться либо в аморфном состоянии, либо в виде кристаллических нестехиометрических соединений оксидов никеля.
Примеры СЭМ-изображений поверхности двухфазного (Ni-1) и микропористого (Ni-2 МИП) никельсодержащих стекол представлены на рис. 5. На поверхности двухфазного стекла видны светлые области, соответствующие агломератам оксида никеля. Поверхность образца Ni-2 МИП имеет обычный для микропористых стекол вид. Темные области справа, так же как и на железосодержащем стекле Fe-4-7 МИП, по-видимому, соответствуют растворившемуся при выщелачивании оксиду никеля.
Рис. 5.
СЭМ-изображения поверхности никельсодержащих стеклообразных материалов: (а) Ni-1, (б) Ni-2 МИП.

Определить содержание никеля в образце пористого никельсодержащего стекла с удовлетворительной точностью пока не удалось, однако данные, полученные методом ЭДС, свидетельствуют о достаточно равномерном распределении никеля в этом стекле (рис. 6).
Для пористого образца никельсодержащего стекла методом БЭТ по тепловой десорбции азота была также определена удельная поверхность S0, оказавшаяся равной 200 м2/г. Расчет среднего радиуса пор (${{r}_{{{{{\text{S}}}_{{\text{0}}}}}}} = {{{\text{2}}W} \mathord{\left/ {\vphantom {{{\text{2}}W} {{\text{(1}} - W{\text{)}}}}} \right. \kern-0em} {{\text{(1}} - W{\text{)}}}}{{\rho }_{{\text{S}}}}{{S}_{{\text{0}}}}$), W – объемная пористость, ρS – плотность силикатного каркаса), если предположить, что величина объемной пористости такая же, как у обычных МИП-стекол 8В-НТ (W = 0.23–0.24), дает величину около 1.4 нм, близкую к размерам поровых каналов железосодержащих микропористых образцов.
На рис. 7 приведены результаты измерений электрофоретической подвижности и значения электрокинетического потенциала двухфазных никельсодержащих силикатных материалов на фоне 10–2 М раствора NaCl. Видно, что их электрокинетические характеристики близки и положение изоэлектрической точки (ИЭТ, ζS = 0) на фоне индифферентного электролита соответствует pHИЭТ = 2.30.
Рис. 7.
Зависимость электрофоретической подвижности и электрокинетического потенциала час-тиц двухфазных никельсодержащих стеклообразных материалов от pH на фоне 10–2 М раствора NaCl: 1 – Ni-1, 2 – Ni-2.
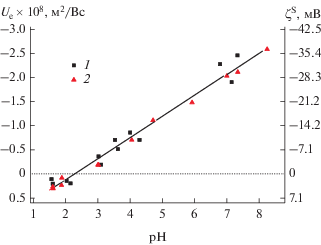
Сопоставление электрокинетических характеристик всех исследованных двухфазных стекол, представленное на рис. 8 (для никельсодержащих стекол приведены значения, усредненные по двум образцам), показывает, что введение магнитных модификаторов в структуру стекла приводит к смещению положения ИЭТ в нейтральную область от величины pHИЭТ = 1.75 для базового стекла 8В-НТ до pHИЭТ = 3.19 для содержащего магнетит стекла Fe-4-6. Отметим, что в исследованной области составов растворов небольшие положительные величины электрокинетического потенциала наблюдаются только для модифицированных силикатных стекол. Полученные результаты также показывают, что в кислой области pH электрокинетические характеристики никельсодержащих стекол близки к таковым для базового стекла, а в нейтральной области pH приближаются к характеристикам стекла Fe-4-6.
Рис. 8.
Зависимости электрофоретической подвижности и электрокинетического потенциала час-тиц двухфазных стеклообразных материалов от pH на фоне 10–2 М раствора NaCl: 1 – 8В-НТ МИП, 2 – Ni-1(2), 3 – Fe-4-6.
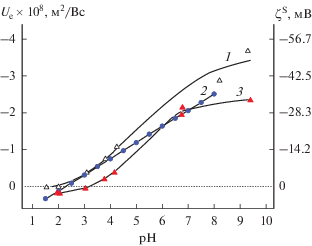
Величины электрофоретической подвижности частиц пористых стекол и полученных из них кварцоидов были измерены на фоне 10–2 М растворов NaCl и NaNO3. Поскольку во всей исследованной области pH силикатные поверхности, в том числе и мозаичные, содержащие вкрапления магнетита, заряжены отрицательно [31], то анионы являются коионами, влияние которых на характеристики поверхности незначительно, что дает нам право рассматривать нитрат натрия в качестве такого же индифферентного электролита, как и хлорид натрия. Анализ полученных результатов показывает (рис. 9), что для исследованных систем наблюдаются только отрицательные величины электрокинетического потенциала, а ИЭТ находятся в кислой области при pH < 1.5, что, по-видимому, связано с изменением химического состава стекол в процессе выщелачивания.
Рис. 9.
Зависимости электрофоретической подвижности и электрокинетического потенциала частиц стеклообразных материалов от pH на фоне 10–2 М растворов электролитов. 1 – 8В-НТ МИП, NaNO3; 2 – КС-8В-НТ, NaNO3; 3 – Fe-4-6 МИП, NaCl; 4 – КС-Fe-4-6, NaCl.
Отметим, что различия в электрофоретической подвижности пористых частиц и монолитных кварцоидных частиц одного химического состава должны быть связаны, в первую очередь, со структурой поверхностного слоя, поскольку влияние собственной проводимости частиц и электроосмоса в порах на электрофоретическую подвижность для аналогичных МИП-стекол (как базовых, так и содержащих магнетит) незначительно [31, 32]. Увеличение значений |ζS | при переходе от стекла 8В-НТ МИП к кварцоиду при pH > 3 может быть связано с изменением структуры межфазной поверхности при высокотемпературной обработке, вызвавшей изменение положения границы скольжения – ее приближение к поверхности частиц за счет спекания вторичного кремнезема, находившегося в поровом пространстве. Для материалов, содержащих магнетит, наблюдалась противоположная тенденция – термообработка приводила к уменьшению величин |ζS | и сближению их со значениями электрокинетического потенциала силикатного кварцоида КС-8В-НТ. Возможно, что при термообработке, вследствие “сплавления” лакун, в которых до выщелачивания находился гематит, на поверхности кварцоида оставался преимущественно силикатный компонент материала.
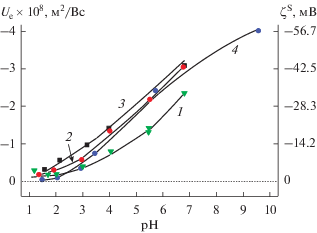
На рис. 10, 11 сопоставлены электрокинетические характеристики силикатных и железосодержащих стеклообразных материалов соответственно. Видно, что для силикатных материалов выщелачивание, т.е. изменение состава как материала в целом, так и его поверхностного слоя, приводит к смещению ИЭТ в кислую область, но величины электрокинетического потенциала двухфазного и пористого образцов остаются достаточно близкими во всей исследованной области pH. Термообработка пористого образца при неизменном составе материала приводит к росту абсолютных величин электрокинетического потенциала. Аналогичные изменения происходят и в случае образцов, содержащих магнетит, – после выщелачивания стекла в исследованной области составов электролита исчезает область положительных значений электрокинетического потенциала вследствие смещения ИЭТ в кислую область, а величины |ζS | возрастают при pH = const. Для кварцоидных железосодержащих материалов при постоянном pH соотношение значений |ζS| зависит от количества магнетита (табл. 2) – чем его больше, тем выше абсолютные значения ζS.
Рис. 10.
Зависимости электрофоретической подвижности и электрокинетического потенциала частиц стеклообразных силикатных материалов от pH на фоне 10–2 М растворов электролитов. 1 – 8В-НТ, NaCl; 2 – 8В-НТ МИП, NaNO3; 3 – КС-8В-НТ, NaNO3.
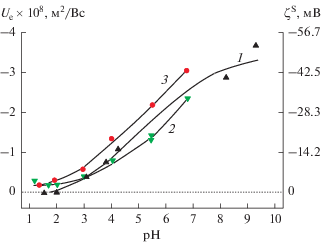
Рис. 11.
Зависимости электрофоретической подвижности и электрокинетического потенциала частиц железосодержащих стеклообразных материалов от pH на фоне 10–2 М раствора NaCl: 1 – Fe-4-6, 2 – Fe-4-6 МИП, 3 – КС-Fe-4-6, 4 – КС-Fe-4-7.
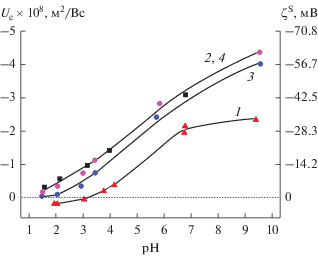
Исследования электрокинетических характеристик силикатных и никельсодержащих стеклообразных материалов были проведены и в растворе хлорида никеля с ионной силой 10–2 М, содержащем специфически сорбирующийся катион Ni2+. Постоянство ионной силы в растворах NaCl и NiCl2 обеспечивает равенство приведенных толщин двойного электрического слоя δ = = ${{\left[ {{{\left( {{{F}^{{\text{2}}}}\sum\nolimits_i {z_{i}^{{\text{2}}}} {{С}_{i}}} \right)} \mathord{\left/ {\vphantom {{\left( {{{F}^{{\text{2}}}}\sum\nolimits_i {z_{i}^{{\text{2}}}} {{С}_{i}}} \right)} {\varepsilon {{\varepsilon }_{{\text{0}}}}RT}}} \right. \kern-0em} {\varepsilon {{\varepsilon }_{{\text{0}}}}RT}}} \right]}^{{{{ - 1} \mathord{\left/ {\vphantom {{ - 1} 2}} \right. \kern-0em} 2}}}}$ (zi – заряды ионов, входящих в состав электролита, Сi – их концентрации, моль/м3) и позволяет сравнивать характеристики поверхности в присутствии противоионов с разной величиной заряда. Видно (рис. 12), что в присутствии специфически сорбирующихся катионов никеля ИЭТ двухфазного базового стекла смещается в нейтральную область (по сравнению с индифферентным электролитом) на единицу pH – до 2.75. Для никельсодержащих двухфазных стекол, как и в растворе хлорида натрия, наблюдаются близкие величины электрофоретической подвижности частиц, а ИЭТ в растворе NiCl2 смещается в нейтральную область практически на единицу pH – до 3.26. Такие смещения положения ИЭТ характерны для поверхностей оксидов в присутствии специфически сорбирующихся катионов.
Рис. 12.
Зависимости электрофоретической подвижности и электрокинетического потенциала частиц стеклообразных материалов от pH на фоне 10–2 М раствора NiCl2: 1 – 8В-НТ, 2 – Ni-1, 3 – Ni-2, 4 – 8В‑НТ МИП [33].
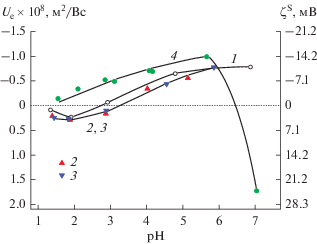
Что касается базового стекла 8В-НТ МИП, то в кислой области pH при малых отрицательных зарядах поверхности двухзарядный противоион ведет себя практически как индифферентный: ИЭТ, как и в растворе NaCl, лежит в области значений pH, близких к 1. С ростом абсолютной величины поверхностного заряда при смещении pH в нейтральную область у поверхности быстро накапливаются двухзарядные положительные ионы, возрастает степень заполнения штерновского слоя, что приводит к появлению второй ИЭТ – при pH 6.46. Появление такой второй ИЭТ следует, по-видимому, ожидать и для никельсодержащих стекол в более щелочной области рН.
ЗАКЛЮЧЕНИЕ
Исследованы химический состав, структура и электрокинетические характеристики стеклообразных материалов – базовых силикатных стекол, а также стекол, модифицированных в процессе варки оксидами железа и никеля. Проанализированы зависимости положения ИЭТ и величин электрокинетического потенциала ζS для частиц монолитных стеклообразных материалов (двухфазных стекол и кварцоидов) и микропористых образцов, полученных путем кислотного выщелачивания, от состава и структуры поверхности в растворе индифферентного электролита NaCl. Показано, что положительные области ζS наблюдаются только для магнитных стеклообразных материалов, причем pHИЭТ возрастает в ряду базовое стекло 8В-НТ, никельсодержащие стекла Ni-1 и Ni-2, железосодержащее стекло Fe-4-6. Установлено, что термообработка микропористых образцов в процессе получения кварцоидов приводит к увеличению абсолютных величин электрокинетического потенциала для силикатных стекол и к их уменьшению для стекол, содержащих магнетит. Исследования электрокинетических характеристик двухфазных базового и никельсодержащего стекла в растворах хлорида никеля показали, что в присутствии специфически сорбирующихся двухзарядных катионов наблюдается смещение ИЭТ в нейтральную область pH.
Список литературы
Антропова Т.В. Неорганические функциональные стеклообразующие материалы на основе ликвирующих щелочноборосиликатных систем // ИХС РАН – 80 лет. Современные проблемы неорганической химии. Под ред. В.Я. Шевченко. СПб.: Арт-Экспресс, 2016. С. 117.
Мазурин О.В., Роскова Г.П., Аверьянов В.И., Антропова Т.В. Двухфазные стекла: структура, свойства, применение. Л.: Наука, 1991.
Liao M.-H., Chen D.-H. // J. Mater. Chem. 2002. V. 12. P. 3654.
Kikukawa T., Kuraoka K., Kawabe K., Yamashita M., Fukumi K., Hirao K., Yazawa T. // J. Membr. Sci. 2005. V. 259. P. 161.
Eerenstein W., Mathur N.D., Scott J.F. // Nature. 2006. V. 442. P. 759.
Martın J., Vazquez M., Hernandez-Velez M., Mijangos C. // Nanotechnology. 2008. V. 19. P. 175304.
Golosovsky I.V., Mirebeau I., Fauthc F., Kurdyukov D.A., Kumzerov Yu.A. // Solid State Commun. 2007. V. 141. P. 178.
Акбашев А.Р., Кауль А.Р. // Успехи химии. 2011. Т. 80. С. 1211.
Cizman A., Antropova T., Anfimova I., Drozdova I., Rysiakiewicz-Pasek E., Radojewska E.B., Poprawski R. // J. Nanoparticle Res. 2013. V. 15. Article 1807.
Cizman A., Marciniszyn T., Rysiakiewicz-Pasek E., Sieradzki A., Antropova T.V., Poprawski R. // Phase Transitions. 2013. V. 86. P. 910.
Cizman A., Bednarski W., Antropova T.V., Pshenko O., Rysiakiewicz-Pasek E., Waplak S., Poprawski R. // Composites. B. 2014. V. 64. P. 16.
Пшенко О.А., Дроздова И.А., Полякова И.Г., Rogacki K., Cizman A., Poprawski R., Rysiakiewicz-Pasek E., Antropova T.V. // Физика и химия стекла. 2014. Т. 40. С. 215.
Пшенко О.А., Антропова Т.В., Арсентьев М.Ю., Дроздова И.А. // Физика и химия стекла. 2015. Т. 41. С. 687.
Конон М.В. Фазовое разделение и физико-химические свойства стекол системы Na2O–B2O3–SiO2–Fe2O3. Дис. … канд. хим. наук. СПб.: ИХС РАН, 2016.
Пшенко О.А. Синтез, структура и свойства диэлектрических и ферромагнитных пористых стекол и композитов со свойствами сегнетоэлектриков и мультиферроиков на их основе. Дис. … канд. хим. наук. СПб.: ИХС РАН, 2017.
Chang Y.-C., Chen D.-H. // J. Colloid Interface Sci. 2005. V. 28. P. 446.
Cheong S.-W., Mostovoy M. // Nat. Mater. 2007. V. 6. P. 13.
Hua M., Zhang S., Pan B., Zhang W., Lv L., Zhang Q. // J. Hazard. Mater. 2012. V. 211–212. P. 317.
Rybak A., Kaszuwara W. // J. Alloys Compd. 2015. V. 648. P. 205.
Cizman A., Rogacki K., Rysiakiewicz-Pasek E., Antropova T., Pshenko O., Poprawski R. // J. Alloys Compd. 2015. V. 649. P. 447.
Podoynitsyn S.N., Sorokina O.N., Kovarski A.L. // J. Magn. Magn. Mater. 2016. V. 397. P. 51.
Ермакова Л.Э., Антропова Т.В., Волкова А.В., Кузнецова А.С., Гринкевич Е.А., Анфимова И.Н. // Физика и химия стекла. 2018. Т. 44. С. 346.
Ермакова Л.Э., Кузнецова А.С., Антропова Т.В., Волкова А.В., Анфимова И.Н. // Коллоид. журн. 2020. Т. 82. С. 310.
Полуэктов Н.С. Методы анализа по фотометрии пламени. М.: Химия, 1967.
Пирютко М.М., Бенедиктова-Лодочникова Н.В. // Журн. аналит. химии. 1970. Т. 25. С. 136.
Пирютко М.М., Бенедиктова Н.В., Корсак Л.Ф. // Стекло и керамика. 1981. № 8. С. 30.
Васильев В.П. Аналитическая химия. Кн. 1. Титриметрические и гравиметрические методы анализа. М.: Дрофа, 2004.
Ermakova L.E., Kuznetsova A.S., Volkova A.V., Antropova T.V. // Colloids Surf. A. 2019. V. 576. P. 91.
Ермакова Л.Э., Гринкевич Е.А., Волкова А.В., Антропова Т.В.// Коллоид. журн. 2018. Т. 80. С. 518.
Rysiakiewicz-Pasek E., Cizman A., Antropova T., Gorokhovatsky Y., Pshenko O., Fomicheva E., Drozdova I. // Mater. Chem. Phys. 2020. V. 243. Article 122 585.
Ермакова Л.Э., Гринкевич Е.А., Волкова А.В., Кузнецова А.С., Куриленко Л.Н., Антропова Т.В. // Коллоид. журн. 2019. Т. 81. С. 306.
Ермакова Л.Э., Волкова А.В., Антропова Т.В., Жуков А.Н. // Коллоид. журн. 2015. Т. 77. С. 302.
Ермакова Л.Э., Кузнецова А.С., Антропова Т.В., Волкова А.В. // Коллоид. журн. 2021. Т. 83.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал