Коллоидный журнал, 2021, T. 83, № 3, стр. 258-268
Аэрогели на основе графена с супергидрофобными и супергидрофильными свойствами и их применение для электровосстановления молекулярного кислорода
Ю. М. Вольфкович 1, *, В. Е. Сосенкин 1, Н. А. Майорова 1, А. Ю. Рычагов 1, С. А. Баскаков 2, Е. Н. Кабачков 2, В. И. Корепанов 3, Н. Н. Дремова 2, Ю. В. Баскакова 2, Ю. М. Шульга 2, 4, **
1 Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119071 Москва, Ленинский просп., 31, Россия
2 Институт проблем химической физики РАН
142432 Черноголовка, Московская область, Россия
3 Институт технологии микроэлектроники и высокочистых материалов РАН
142432 Черноголовка, Московская область, Россия
4 Национальный исследовательский технологический университет “МИСиС”
119049 Москва, Ленинский просп., 4, Россия
* E-mail: yuvolf40@mail.ru
** E-mail: yshulga@gmail.com
Поступила в редакцию 10.12.2020
После доработки 22.12.2020
Принята к публикации 25.12.2020
Аннотация
Синтезирован композитный аэрогель на основе восстановленного оксида графена и политетрафторэтилена в массовом соотношении 1 : 1 с супергидрофобной наружной поверхностью; его пористая структура исследована методом эталонной контактной порометрии (МЭКП). Порометрические кривые для октана и воды пересекаются в области мелких пор, что приводит к тому, что удельная поверхность аэрогеля в воде намного больше, чем в октане, несмотря на то что, как известно, октан практически идеально смачивает все материалы. Это явление, названное “супергидрофильностью”, объясняется набуханием образца в воде в области мезопор вследствие гидратации поверхностных групп –CO и –COH, идентифицированных с помощью инфракрасной спектроскопии и спектроскопии комбинационного рассеяния. Таким образом, гранулы аэрогеля супергидрофобны снаружи и супергидрофильны внутри, в области мелких пор. Как следует из данных МЭКП, общая пористость аэрогеля, а также его удельная поверхность значительно больше, чем у сажи Vulcan XC-72 – стандартного носителя для Pt-катализатора в топливных элементах с протонообменной мембраной. Электровосстановление кислорода при навеске Pt на аэрогеле 28 мкг/см2 изучали методом вращающегося дискового электрода (ВДЭ) в 0.5 М водном растворе H2SO4 и сравнивали с таковым на стандартном коммерческом катализаторе Pt (20%)/Vulcan XC-72. Показано, что предельные диффузионные токи на ВДЭ для Pt, электроосажденной на гидрофобно-гидрофильный аэрогель, значительно выше, чем для стандартного катализатора, что объясняется лучшим доступом кислорода к зоне реакции по сравнению c гидрофильной сажей Vulcan XC-72.
1. ВВЕДЕНИЕ
Важно учитывать, что углерод является переходным элементом не только между металлами и металлоидами, но также между гидрофильными и гидрофобными материалами [1, 2]. Согласно [2] практически все пористые углеродные материалы имеют как гидрофильные, так и гидрофобные поры.
Реакция электровосстановления молекулярного кислорода на платиновом катализаторе в топливном элементе является одной из наиболее важных и наиболее изученных электрохимических реакций в области электрохимической энергетики. Эта реакция проводится на пористом газодиффузионном электроде, содержащем поры, заполненные как газом, так и жидкостью [3, 4]. Чтобы свести к минимуму потребление драгоценного металла и максимизировать поверхность платины, ее частицы должны иметь минимальный размер в несколько нанометров. Однако из-за действия поверхностных сил такие мелкие частицы со временем обычно агломерируют, что приводит к уменьшению их общей поверхности и, следовательно, каталитической активности. Для предотвращения агломерации эти наночастицы осаждают на пористом электропроводящем носителе, в качестве которого чаще всего используются высокодисперсные углеродные материалы. Углеродные носители имеют достаточно высокую пористость и большую удельную поверхность. Кроме того, желательно, чтобы они имели как гидрофильные, так и гидрофобные поры: первые содержат электролит, а через вторые происходит снабжение кислородом поверхности Pt-катализатора [3, 4]. Углеродные носители могут быть представлены наночастицами [5–7], нанотрубками [8–10] или нановолокнами [8, 11], графенами [8, 12, 13], графеновыми нанолентами [14] и т.д. В работе [15] в качестве носителя для реакции электровосстановления кислорода на платиновом катализаторе была использована шихта, содержащая частицы наноалмаза и углерода, причем последние вводились для придания шихте достаточной электропроводности. Было показано, что данная система устойчива во времени, что связано с существенно меньшей скоростью коррозии носителя из наноалмазного композита по сравнению со стандартными сажами при потенциалах кислородного электрода, что, в свою очередь, приводило к снижению степени агрегирования частиц катализатора. В качестве носителя были также использованы углерод-углеродные композиты, а точнее, – композиты типа макропористый углерод–графен [16]. В [17] углеродные носители подвергали окислительной обработке для обогащения их кислородсодержащими функциональными группами. Это приводило к усилению взаимодействия между металлическими частицами и носителем, что повышало электрохимическую стабильность Pt/C-катализатора. В [18] в качестве носителя (подложки) использовался композит из одностенных углеродных нанотрубок и полианилина. Такой композит обеспечивал большую устойчивость частиц Pt к агломерации. При этом нужно иметь в виду, что полианилин обладает электронной проводимостью.
Несмотря на описанное выше большое разнообразие видов углеродных носителей, в настоящее время в качестве стандартного коммерческого носителя для катализатора реакции электровосстановления кислорода в топливных элементах с протонообменной мембраной (ТЭПОМ) используется практически только сажа Vulcan XC-72 [3, 19, 20]. Кроме хороших электрохимических результатов важную роль играет дешевизна этой сажи.
В данном исследовании мы сравнивали электрохимические и структурные свойства разработанного нами композитного аэрогеля из восстановленного оксида графена (ВОГ) и политетрафторэтилена (ПТФЭ), предлагаемого в качестве носителя платинового катализатора для электровосстановления молекулярного кислорода, с упомянутой выше сажей Vulcan XC-72.
Ранее сообщалось об успешном синтезе аэрогеля на основе ПТФЭ (70%) и оксида графена (30%) [21] (здесь и далее состав композитных аэрогелей указан в мас. %). После восстановления гидразином и отжига при 370°C аэрогель с очень малым удельным весом, около 30 мг/см3, имел угол смачивания наружной поверхности водой от 166° до 170°. Следовательно, он стал супергидрофобным, поскольку супергидрофобными можно считать материалы, для которых угол смачивания водой равен или больше 150° [22, 23]. В продолжение этих исследований были синтезированы аэрогели ПТФЭ–ВОГ состава 60 : 40 и 50 : 50 [24].
Для исследования пористой структуры и гидрофильно-гидрофобных свойств образцов аэрогелей использовался разработанный нами ранее метод эталонной контактной порометрии (МЭКП) [2, 25, 26]. Этот метод основан на термодинамике распределения жидкости в пористых системах. Он дает возможность измерять следующие характеристики пористых материалов: интегральные и дифференциальные кривые распределения объема и поверхности пор по радиусам пор в максимально широком диапазоне радиусов – от примерно 1 нм до 3 × 105 нм, величины полной и гидрофильной удельной поверхности, величину среднего угла смачивания водой, зависимость угла смачивания водой от радиуса пор, изотермы адсорбции и десорбции воды, интегральные и дифференциальные кривые распределения воды по величинам капиллярного давления и по величинам свободной энергии связи воды с материалом. МЭКП был признан IUPAC в качестве современного порометрического метода [27].
Очевидно, что МЭКП более информативен по сравнению с другими методами в отношении описания свойств материалов на основе графена при их электрохимических применениях с водным электролитом (аккумуляторы, электрохимические суперконденсаторы, топливные элементы, установки для емкостной деионизации воды и т.д.), так как в МЭКП можно использовать воду в качестве рабочей жидкости. На протяжении десятилетий этот метод применялся для исследования структуры и гидрофильно-гидрофобных свойств различных углеродных материалов, имеющих как гидрофильные, так и гидрофобные поры [2, 25, 26].
В настоящей работе сравниваются структурные характеристики синтезированного аэрогеля (ВОГ 50%/ПТФЭ 50%) и сажи Vulcan XC-72, а также электрохимические характеристики электровосстановления молекулярного кислорода на платиновом катализаторе, нанесенном на такой аэрогель и на сажу Vulcan XC-72.
2. ЭКСПЕРИМЕНТ
2.1. Материалы
Источником ПТФЭ служила суспензия, содержащая ПТФЭ (молекулярная масса 140–500 кДа), ПАВ (смесь этоксилированных алкилфенолов) и воду в соотношении 6 : 1 : 3 (Ф-4Д, ТУ 6-05-1246-81, ООО “ГалоПолимер Кирово-Чепецк”). Для синтеза оксида графена (ОГ) использовали модифицированный метод Хаммерса [28], детали которого описаны в [29, 30].
2.2. Синтез аэрогелей ВОГ–ПТФЭ
При приготовлении аэрогеля 30 мл водной суспензии ОГ с концентрацией 11 мг/мл помещали в стеклянный стакан и обрабатывали ультразвуком в течение 5 мин. Затем в суспензию ОГ по каплям вводили требуемый объем суспензии ПТФЭ, не прекращая ультразвуковой обработки. После полного введения суспензии, содержащей ПТФЭ, обработку ультразвуком продолжали еще 5 мин. Для получения гранулированного аэрогеля гелеобразную суспензию смеси ОГ–ПТФЭ медленно, капля за каплей, вводили дозирующим шприцем в стеклянный сосуд Дьюара с жидким азотом. После замораживания на дно сосуда выпали каплевидные гранулы. Дальнейшая обработка этих гранул подробно описана в [21, 24]. В настоящей работе использован полученный аэрогель состава ВОГ (50%)/ПТФЭ (50%) с плотностью 26 мг/см3.
2.3. Методы
Электронные микрофотографии получали на растровом электронном микроскопе JEOL JSM-5910LV (энергия электронов 20 кВ, давление в камере 2 × 10–5 Па).
ИК-спектры образца аэрогеля были получены в диапазоне от 700 до 4000 см–1 на фурье-спектрометре Shimadzu с приставкой нарушенного полного внутреннего отражения.
Спектры комбинационного рассеяния (КР) были измерены с помощью конфокального КР-микроскопа SENTERRA (Bruker). Длина волны возбуждения составляла 532 нм, мощность лазера ~1 мВт в точке образца с перетяжкой пучка ~1 мкм.
Углы смачивания аэрогеля водой (θw) измеряли на приборе OCA 20 (Data Physics Instruments GmbH, Германия) при комнатной температуре.
2.4. Измерение углов смачивания
Невозможно было измерить угол смачивания гранул аэрогеля водой стандартным методом (методом лежащей капли), поскольку плоская поверхность гранул не могла быть получена неразрушающим способом. В случае, когда плоская поверхность была получена прессованием гранул аэрогеля, значение θw не превышало 120°. Для корректного измерения угла смачивания из образцов аэрогеля были сформированы цилиндры диаметром примерно 2 см, одна из базовых поверхностей которых была плоской в результате действия силы тяжести. Такая поверхность не смачивалась водой до такой степени, что было трудно остановить движение по ней капли воды. Характерные значения θw для такой поверхности были равны 166°–170°.
2.5. Измерения распределения пор по размерам
Для сравнительного исследования пористой структуры и гидрофильно-гидрофобных свойств образцов аэрогеля и сажи Vulcan XC-72 был использован МЭКП [2, 25]. И исследуемые образцы, и эталоны сушили в вакууме при 170°C и взвешивали по отдельности. Затем каждый образец помещали между двумя эталонами, вакуумировали, пропитывали водой или октаном и частично высушивали в вакууме. Периодически комплект разбирали, а его компоненты взвешивали. Состояние капиллярного равновесия контролировали в каждой точке кривой распределения пор по размерам. Измерения продолжали до тех пор, пока вес исследуемого образца не становился постоянным.
На рис. 1 приведена фотография автоматического эталонного поромера роботизированного типа, в котором все процедуры осуществляются автоматически [26]. Строится равновесная кривая относительного влагосодержания, которая представляет собой зависимость количества рабочей жидкости (октана или воды) в исследуемом образце от ее количества в эталонах. Используя уравнение [2]
(1)
$S = 2\int\limits_0^r {\left( {\frac{1}{r}} \right)\left( {\frac{{{\text{d}}V}}{{{\text{d}}r}}} \right){\text{d}}r} ,$2.6. Электровосстановление молекулярного кислорода
Образец аэрогеля ВОГ (50%)/ПТФЭ (50%) (далее именуемый просто аэрогелем) был испытан в качестве носителя для платинового катализатора с использованием метода вращающегося дискового электрода (ВДЭ). Все измерения проводили при комнатной температуре в стандартной трехэлектродной стеклянной ячейке со стержнем из стеклоуглерода (СУ) (диаметр 3 мм) в качестве рабочего электрода, платиновой сеткой в качестве противоэлектрода и Hg/HgSO4 в качестве электрода сравнения. Фоновый водный электролит (0.5 М H2SO4) продували аргоном или насыщали кислородом при атмосферном давлении. Вольтамперометрические измерения проводили с помощью автоматического потенциостата ЭЛ-02.06, подключенного к компьютеру. Потенциал рабочего электрода изменяли в диапазоне 0.0–1.2 В со скоростью 5 или 50 мВ/с. Значения потенциала были пересчитаны относительно обратимого водородного электрода.
Для приготовления рабочего электрода навеску измельченного аэрогеля смешивали с раствором этанола в воде и обрабатывали ультразвуком. Аликвоту полученной суспензии пипеткой переносили на диск из СУ и сушили на воздухе. Для фиксации пленки аэрогеля на поверхность СУ наносили аликвоту разбавленного раствора нафиона и затем сушили. Электрод с пленкой стандартного катализатора на носителе, Pt (20%)/ Vulcan XC-72, готовили по той же методике из соответствующей суспензии. В случае пленки аэрогеля платину осаждали на электрод электрохимически при постоянном потенциале из разбавленного раствора H2PtCl6.
3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
3.1. Изображения аэрогелей
На рис. 2 показаны: (а) фотография гранул аэрогеля, (б) микрофотография раскола гранулы аэрогеля, (в) ИК-спектр аэрогеля и (г) спектры КР пленки ПТФЭ (1) и аэрогеля (2). Видно, что полученные гранулы имеют форму, близкую к форме половины эллипсоида вращения. При замораживании наблюдается быстрое разделение капли аэрогеля на две примерно равные половины. Микрофотография на рис. 2б показывает, что макропоры образуют очень сложную структуру.
Рис. 2.
(а) – Фотография гранул аэрогеля; (б) – микрофотография скола гранулы аэрогеля; (в) – ИК-спектр аэрогеля (врезка – фотография капли воды на поверхности аэрогеля); (г) – спектры КР пленки ПТФЭ (1) и аэрогеля (2).
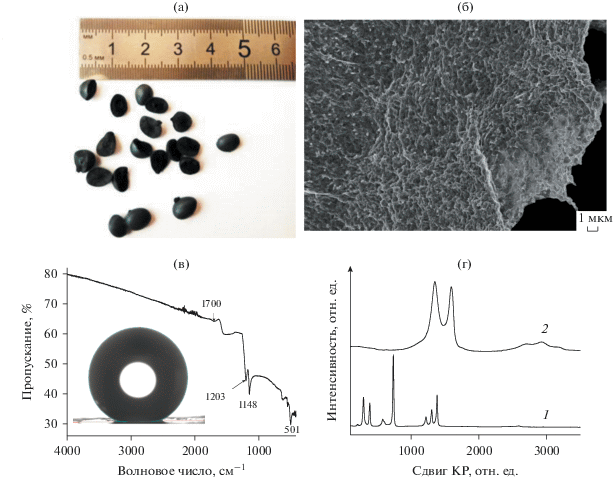
На врезке рис. 2в приведена фотография капли воды на наружной поверхности гранулы аэрогеля. Для нескольких капель были получены величины θw = 166°–170°. Это означает, что наружная поверхность гранул аэрогеля является супергидрофобной [22, 23].
Рассмотрим возможные причины супергидрофобности наружной поверхности частиц аэрогеля. Согласно [1] максимальный наблюдаемый угол смачивания водой гладких поверхностей составляет 120°–125°, в основном на поверхностях с плотноупакованными –CF3 и –CF2-группами. Такие поверхностные группы были обнаружены в исследуемом аэрогеле (см. ниже). Для шероховатых поверхностей возможны и более высокие значения краевого угла, вплоть до 180° [1, 29, 30]. Смачивание шероховатой поверхности определяется не только ее химией, но и топографией. Согласно уравнению Вензеля [1, 31]
где γ – фактор шероховатости (отношение площади шероховатой поверхности к площади соответствующей гладкой поверхности), θr – угол смачивания шероховатой поверхности, θs – угол смачивания гладкой поверхности. Из этого уравнения следует, что в случае гидрофильной поверхности (θs < 90°) шероховатость улучшает смачиваемость, а в случае гидрофобной поверхности (θs > 90°) шероховатость, наоборот, ухудшает смачиваемость. Шероховатость характеризуется наличием на поверхности образца выступов и впадин относительно крупных размеров (десятки микронов). Как видно на рис. 2б, поры таких больших размеров имеются в аэрогеле. Они, вероятно, обеспечивают достаточно большую величину фактора шероховатости его наружной поверхности.3.2. Данные ИК- и КР-спектроскопии
В ИК-спектре аэрогеля (рис. 2в) хорошо видны полосы поглощения (ПП), обусловленные валентными колебаниями (ν) связей C–F (1203 и 1148 см–1). ПП в низкочастотной области спектра связаны с веерными, деформационными и маятниковыми (501 см–1) колебаниями CF2-групп ПТФЭ. Полосу при 1700 см–1 можно отнести к колебаниям C=O и C–OH [32, 33]. Наклон спектра мы связываем с присутствием в аэрогеле ВОГ, что делает образец проводящим [32]. С наличием ВОГ мы также связываем ПП при 1700 см–1 и широкую ПП в области 1545–1465 см–1.
Спектр КР для пленки ПТФЭ представлен несколькими узкими пиками, максимумы которых расположены при 296.0, 388.6, 588.1, 600.9, 736.8, 1219.7, 1303.5 и 1384.1 см–1. Полученный нами спектр пленки ПТФЭ по положению пиков близок к спектрам ПТФЭ, полученным ранее (см., например, [32, 34, 35]). Отнесение отдельных пиков в спектре ПТФЭ также хорошо известно [32, 34, 35].
Отсутствие этих пиков в спектре КР аэрогеля (рис. 2г) связано с тем, что поляризуемость ВОГ намного больше, чем ПТФЭ. Кстати, в ИК-спектре аэрогеля, где интенсивность определяется изменением дипольного момента атомных групп, существенно более интенсивными оказываются ПП, обусловленные ПТФЭ.
Максимальную интенсивность в спектре КР аэрогеля имеют пики D и G с максимумами приблизительно при 1350 и 1580 см–1 соответственно (рис. 2г). Отношение интенсивностей этих пиков (ID/IG) может служить мерой беспорядка в углеродной sp2-решетке. Величину ID/IG можно использовать также для оценки размера sp2-доменов (La) в ВОГ [36, 37]:
(3)
${{L}_{{\text{a}}}} = ({\text{2}}.{\text{4}} \times {\text{1}}{{0}^{{ - {\text{1}}0}}})\lambda _{{\text{L}}}^{{\text{4}}}{{({{{{I}_{{\text{D}}}}} \mathord{\left/ {\vphantom {{{{I}_{{\text{D}}}}} {{{I}_{{\text{G}}}}}}} \right. \kern-0em} {{{I}_{{\text{G}}}}}})}^{{ - {\text{1}}}}},$Таким образом, пики, характерные для ПТФЭ, отсутствуют в спектре КР аэрогеля ПТФЭ–ВОГ. В спектре КР синтезированного нами композитного аэрогеля присутствуют только пики, обусловленные ВОГ. Установлено также, что в композитном аэрогеле ВОГ сохраняет характерную sp2-структуру.
3.3. Распределение пор по размерам и удельная поверхность
Интегральные кривые распределения объема пор по эффективным радиусам, измеренные для образцов аэрогеля (1, 2) и сажи Vulcan XC-72 (3, 4) с использованием октана (1, 3) и воды (2, 4), показаны на рис. 3, а соответствующие интегральная и дифференциальная кривые распределения поверхности пор по эффективным радиусам – на рис. 4а и 4б. Поскольку угол смачивания октаном практически всех материалов близок к нулю [1], кривые 1, 3 описывают распределение по размерам всех пор, тогда как “водяные” кривые 2, 4 – только распределение по размерам гидрофильных пор. Ось X соответствует значениям эффективного радиуса поры, r * = r/cos θ, где r – действительный радиус пор, измеренный по октану, θ – угол смачивания. В случае октана θ ≈ 0° и r * ≈ r, тогда как в случае воды θ > 0 и r * > r.
Рис. 3.
Интегральные кривые распределения объема пор (V) по эффективным радиусам пор (r *) для образцов аэрогеля (1, 2) и сажи Vulcan XC-72 (3, 4), измеренные с использованием октана (1, 3) и воды (2, 4).
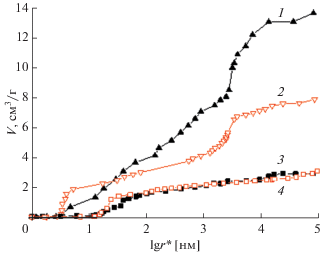
Рис. 4.
Интегральное (а) и дифференциальное (б) распределения поверхности пор по эффективным радиусам для композитного аэрогеля (1, 2) и сажи Vulcan XC-72 (3, 4), измеренные с использованием октана (1, 3) и воды (2, 4).
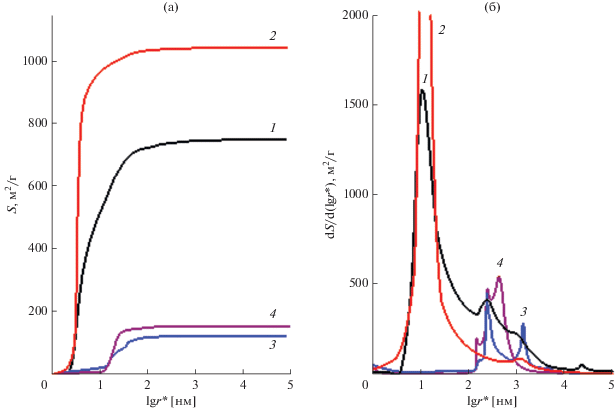
Следует также отметить, что пористость композитного аэрогеля, измеренная с помощью октана, коррелирует с содержанием ВОГ в образце (13.8 см3/г против 28.1 см3/г для чистого аэрогеля ВОГ [38]). Согласно рис. 3, удельный объем гидрофильных пор составляет 7.8 см3/г, а удельный объем гидрофобных пор равен 5.7 см3/г.
По данным ИК- и КР-спектроскопии (см. выше), исследуемый аэрогель содержит группы CO, COH, CF2 и CF3. Порометрические кривые 1 и 2, измеренные для октана и воды, пересекаются при r ≈ 20 нм (рис. 3). Поскольку, как уже было сказано, для октана краевой угол на поверхности практически всех материалов близок к 0°, то пересечение кривых в этом случае означает, что образец аэрогеля в области мелких пор с r < 20 нм намного лучше смачивается водой, чем даже октаном. Это явление можно назвать “супергидрофильностью” и объяснить набуханием материала образца в воде в области мезопор, вероятно, из-за гидратации поверхностных групп –CO и –COH. Из-за набухания образца в воде образуются дополнительные мезопоры с радиусами в диапазоне от 2.5 до 20 нм, и удельная поверхность, измеренная по воде Sw = = 1050 м2/г, намного больше, чем в отсутствие набухания, т.е. измеренная по октану So = 750 м2/ г. Отметим, что для аэрогеля из чистого ВОГ Sw = = 1570 м2/г и So = 750 м2/г [38]. Таким образом, наружная поверхность гранул композитного аэрогеля является супергидрофобной, а их внутренняя поверхность супергидрофильна.
Из рис. 4а и 4б следует, что для композитного аэрогеля поры с r от 1 до 5 нм вносят основной вклад в площадь поверхности, измеренную по октану, а поры с r от 5 до 100 нм вносят основной вклад в площадь поверхности, измеренную по воде. Доминирующий вклад мельчайших пор в значение удельной поверхности следует из уравнения (1).
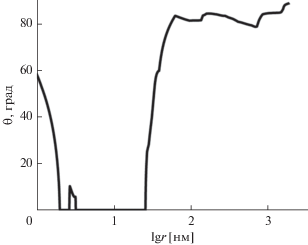
На рис. 5 показана зависимость угла смачивания водой от радиуса пор для образца композитного аэрогеля, рассчитанная согласно [2, 24, 25]. Видно, что радиусы гидрофильных пор находятся в диапазоне от 2 до 14 нм. Из них поры с радиусами от 2.5 до 4 нм являются супергидрофильными и, по-видимому, имеют формально отрицательный эффективный угол смачивания водой. Таким образом, исследуемый образец аэрогеля обладает как гидрофильными, так и гидрофобными свойствами.
Отметим, что явление супергидрофильности наблюдалось ранее для аэрогеля ВОГ [38]. Аналогичный эффект был также продемонстрирован для активного слоя газодиффузионного электрода топливных элементов с протонообменной мембраной, а именно: наличие гидрофобных пор на поверхности частиц нафиона и гидрофильных пор внутри этих частиц [2]. Гидратированные ионогенные группы SO3H в этом случае оказались внутри частиц, а гидрофобные цепи ПТФЭ (CF2)n остались снаружи.
При сравнении полученных порометрических данных для образцов аэрогеля и сажи Vulcan XC-72 можно сделать несколько основных выводов. 1. Общая пористость Vulcan XC-72 в 3.5 раза меньше, чем аэрогеля (см. рис. 3). 2. Интегральные кривые распределения объема пор по эффективным радиусам для Vulcan XC-72, измеренные по октану и воде (кривые 3 и 4 на рис. 3), близки друг к другу, что означает гидрофильность Vulcan XC-72 при практически полном отсутствии гидрофобных пор. 3. Явление супергидрофильности не наблюдается для сажи Vulcan XC-72 в отличие от аэрогеля. Как следует из рис. 4, основной вклад в удельную поверхность аэрогеля вносят поры радиусом от 2 до 10 нм, а в случае Vulcan XC-72 – поры значительно большего размера, радиусом от 20 до 40 нм. В результате удельная поверхность Vulcan XC-72 (Sо = 260 м2 г–1, Sw = 208 м2 г–1) намного меньше, чем композитного аэрогеля (So = 750 м2 г–1, Sw = 1050 м2 г–1).
Согласно [2], МЭКП в числе многих видов информации позволяет получать интегральные и дифференциальные кривые распределения воды по величинам свободной энергии ее связи (A) с материалом, распределения воды по величинам капиллярного давления рк, а также изотермы адсорбции и десорбции воды, т.е. зависимости влагосодержания v от относительной упругости водяного пара (p/ps) [39]. Эти характеристики важны для ТЭПОМ [4, 40]. Все они связаны термодинамическими соотношениями [2]:
(4)
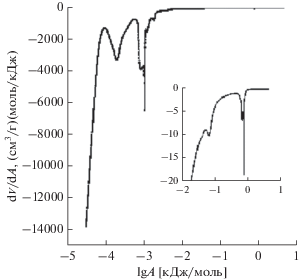
${{p}^{{\text{к}}}} = {{ - 2\sigma {\text{cos}}\theta } \mathord{\left/ {\vphantom {{ - 2\sigma {\text{cos}}\theta } r}} \right. \kern-0em} r} = ({{RT} \mathord{\left/ {\vphantom {{RT} {{{V}_{{\text{m}}}}}}} \right. \kern-0em} {{{V}_{{\text{m}}}}}}){\kern 1pt} {\text{ln(}}{p \mathord{\left/ {\vphantom {p {{{p}_{{\text{s}}}}}}} \right. \kern-0em} {{{p}_{{\text{s}}}}}}{\text{)}} = {{ - A} \mathord{\left/ {\vphantom {{ - A} {{{V}_{{\text{m}}}}}}} \right. \kern-0em} {{{V}_{{\text{m}}}}}},$На рис. 6 приведена дифференциальная кривая распределения воды по величинам свободной энергии ее связи (A) с материалом, полученная в максимальном диапазоне величин A, составляющем 6 порядков. Она характеризует следующие типы воды, связанной с материалом, по мере уменьшения A: гидратная вода, вода в микропорах, вода в мезопорах и в макропорах. Как видим, доля воды, соответствующая большим значениям A, очень мала, что объясняется большой долей гидрофобного ПТФЭ.
Рис. 6.
Дифференциальная кривая распределения воды по величинам свободной энергии ее связи (A) с материалом композитного аэрогеля.
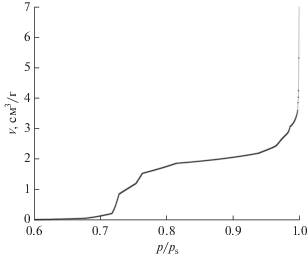
На рис. 7 представлена изотерма десорбции воды для композитного аэрогеля. Видно, что она имеет две явные ступени при значениях р/рs, равных примерно 0.73 и 0.99. Знание изотермы десорбции (и адсорбции) важно для ТЭПОМ потому, что при достаточно большой влажности имеет место максимальная электропроводность протонообменной мембраны типа Нафион, однако при слишком малом влагосодержании газодиффузионных электродов возрастает их поляризация вследствие затрудненности доступа активных газов (О2 и Н2) к реакционным поверхностям соответствующих электродов. Следовательно, зная изотерму десорбции (или адсорбции) можно оптимизировать влагосодержание газодиффузионных электродов.
3.4. Электровосстановление молекулярного кислорода
Электровосстановление молекулярного кислорода в топливных элементах, как известно, происходит на газодиффузионном электроде, содержащем два типа пор: заполненные жидкостью (гидрофильные) и заполненные газом (гидрофобные) [3, 4]. Как следует из данных, представленных выше, образец аэрогеля ВОГ (50%)/ПТФЭ (50%) удовлетворяет этому условию. Поэтому мы испытали этот образец в качестве носителя для платинового катализатора и сравнили электрохимическое поведение аэрогеля, содержащего Pt, и традиционного катализатора Pt (20%)/Vulcan XC-72 в реакции восстановления кислорода (в модельных условиях) с использованием циклической вольтамперометрии и метода ВДЭ [41]. Процедура изготовления электродов описана выше.
На рис. 8 показаны поляризационные кривые ВДЭ при восстановлении кислорода на платине, нанесенной в микроколичестве (28 мкг/см2) на пленку аэрогеля (а), и на обычном коммерческом катализаторе Pt (20%)/Vulcan XC-72 (б), записанные в диапазоне потенциала 1.1–0.3 В при различной скорости вращения электродов в растворе серной кислоты, насыщенном кислородом при атмосферном давлении (кривые 1–4).
Рис. 8.
Поляризационные кривые ВДЭ при восстановлении кислорода на платине, электроосажденной на аэрогеле (а), и на стандартном катализаторе Pt (20%)/Vulcan XC-72 (б) в 0.5 М водном растворе H2SO4, насыщенном кислородом при атмосферном давлении и комнатной температуре. Загрузка платины на оба электрода составляет около 28 мкг/см2. Скорость развертки потенциала 5 мВ/с. Скорость вращения электрода (об./мин): (а) 600 (1), 900 (2), 1300 (3), 2400 (4) и (б) 600 (1), 1200 (2), 1500 (3), 2200 (4).
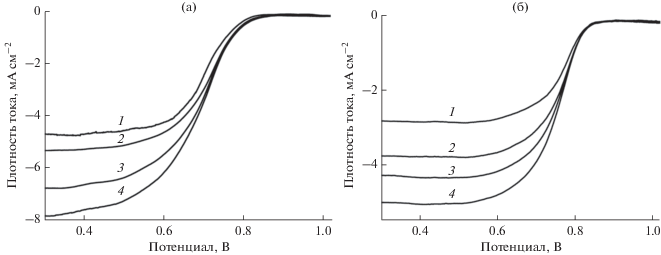
Как следует из рис. 8, при минимальной скорости вращения и значениях потенциала, больших 0.7 В, плотности тока для платины, нанесенной на аэрогель, меньше, чем для платины на стандартном носителе (в нашем случае – саже Vulcan XC-72), что, скорее всего, является результатом повышенного электрического сопротивления композита, содержащего ПТФЭ. Однако при значениях потенциала ниже 0.7 В плотности тока для платины, нанесенной на аэрогель, существенно больше, чем для стандартного электрода.
Следует отметить, что тестирование модельного активного слоя при низких скоростях вращения дискового электрода можно рассматривать как в большей мере соответствующее внешнему диффузионному режиму электровосстановления кислорода в ТЭПОМ. Это приводит к тому, что предельные диффузионные токи для катализатора, нанесенного на гидрофобно-гидрофильный аэрогель, почти вдвое выше, чем для катализатора на стандартном гидрофильном носителе вследствие лучшего транспорта кислорода в случае аэрогеля.
ЗАКЛЮЧЕНИЕ
Синтезирован композитный аэрогель на основе восстановленного оксида графена и ПТФЭ в массовом соотношении 1 : 1 с супергидрофобной наружной поверхностью, а его пористая структура исследована методом эталонной контактной порометрии. Порометрические кривые, полученные с использованием октана и воды, пересекаются в области мелких пор, что указывает на то, что удельная поверхность аэрогеля в воде намного выше, чем в октане, несмотря на то, что, как известно, октан полностью смачивает практически все материалы. Это явление, названное “супергидрофильностью”, объясняется набуханием образца в воде в области мезопор вследствие гидратации поверхностных групп –СO и –COH, идентифицированных с помощью ИК- и КР-спектроскопии.
Как следует из данных МЭКП, общая пористость аэрогеля, а также его удельная поверхность значительно больше, чем у сажи Vulcan XC-72. Электровосстановление кислорода при навеске Pt на аэрогеле 28 мкг/см2 изучали методом ВДЭ в 0.5 М водном растворе H2SO4 и сравнивали с таковым на стандартном коммерческом катализаторе Pt (20%)/Vulcan XC-72. Показано, что предельные диффузионные токи на ВДЭ для электроосажденной на гидрофобно-гидрофильный аэрогель платины значительно выше, чем для стандартного гидрофильного катализатора, что объясняется лучшим доступом кислорода к зоне реакции по сравнению с сажей Vulcan XC-72.
Список литературы
Zisman W.A. // Contact Angle, Wettability, and Adhesion. Adv. Chem. Ser. 43. Washington, D.C.: 1964. P. 1.
Volfkovich Yu.M., Filippov A.N., Bagotsky V.S. Structural Properties of Porous Materials and Powders Used in Different Fields of Science and Technology. London: Springer, 2014.
Gottesfeld S., Zawodzinski T.A. // Advances in Electrochemical Science and Engineering. V. 5. Ed. by Alkire L.C., Gerischer H., Kolb D.M., Tobias C.W. Toronto: Wiley, 1997. P. 195.
Bagotsky V.S., Skundin A.M., Volfkovich Yu.M. Electrochemical Power Sources. Batteries, Fuel Cells, and Supercapacitors. Hoboken, New Jersey: Wiley, 2015.
Huang Y., Liu W., Kan S., Liu P., Hao R., Hu H., Zhang J., Liu H., Liu M., Liu K. // Int. J. Hydrog. Energy. 2020. V. 45. P. 6380.
Sui S., Wang X., Zhou X., Su Y., Riffat S., Liu C. // J. Mater. Chem. A. 2017. V. 5. P. 1808.
Zhang J., Mo Y., Vukmirovic M.B., Klie R., Sasaki K., Adzic R.R. // J. Phys. Chem. B. 2004. V. 108. P. 10955.
Sharma S., Pollet B.G. // J. Power Sources. 2012. V. 208. P. 96.
Görlin M., Ferreira de Araújo J., Schmies H., Bernsmeier D., Dresp S., Gliech M., Jusus Z., Chernev P., Kraehnert R., Dau H., Strasser P. // J. Am. Chem. Soc. 2017. V. 139. P. 2070.
Zhang Y., Wang Y., Huang J., Han C., Zang J. // Int. J. Hydrog. Energy. 2020. V. 45. P. 6529.
Zaragoza-Martın F., Sopena-Escario D., Morallon E., Salinas-Martınez de Lecea C. // J. Power Sources. 2007. V. 171. P. 302.
Stevanovic S.I., Panic V.V., Dekanski A.B., Tripkovic A.V., Jovanovic V.M. // Phys. Chem. Chem. Phys. 2012. V. 14. P. 9475.
Dong L., Gari R.S., Li Z., Craig M.M., Hou S. // Carbon. 2010. V. 48. P. 781.
Wang C., Li H., Zhao J., Zhu Y., Yuan W.Z., Zhang Y. // Int. J. Hydrog. Energy. 2013. V. 38. P. 13230.
Sosenkin V.E., Aleksenko A.E., Rychagov A.Yu., Mayorova N.A., Ovchinnikov-Lazarev M.A., Spitsyn B.V., Vol’fkovich Yu.M. // Protection of Metals and Physical Chemistry of Surfaces. 2019. V. 55. P. 646.
Bo X., Guo L. // Electrochim. Acta. 2013. V. 90. P. 283.
Chen W., Xin Q., Sun G., Wang Q., Mao Q., Su H. // J. Power Sources. 2008. V. 180. P. 199.
Mikhaylova A.A., Tusseeva E.K., Mayorova N.A., Rychagov A.Yu., Volfkovich Yu.M., Krestinin A.V., Khazova O.A. // Electrochim. Acta. 2011. V. 56. P. 3656.
Calvillo L., Celorrio V., Moliner R., Lazaro M.J. // Mater. Chem. Phys. 2011. V. 127. P. 335.
Volfkovich Yu.M., Sosenkin V.E. // Russ. Chem. Rev. 2012. V. 81. P. 936.
Baskakov S.A., Baskakova Y.V., Kabachkov E.N., Dremova N.N., Michtchenko A., Shulga Yu.M. // ACS Appl. Mater. Interfaces. 2019. V. 35. P. 32517.
Boinovich L.B., Emelyanenko A.M. // Russ. Chem. Rev. 2008. V. 77. P. 583.
http://www.ras.ru/news/shownews.aspx?id=b53dad2c- d02c-44b3-8955-305136cb8a30
Volfkovich Yu.M., Sosenkin V.E., Mayorova N.A., Rychagov A.Y., Baskakov S.A., Kabachkov E.N., Korepanov V.I., Dremova N.N., Baskakova Y.V., Shulga Yu.M. // Energy Fuels. 2020. V. 34. P. 7573.
VolfkovichYu.M., Bagotzky V.S. // J. Power Sources. 1994. V. 48. P. 339.
Volfkovich Yu.M., Blinov I.A., Sakar A. Pat. 7 059 175 USA. 2006.
Rouquerol J., Baron G., Denoyel R., Giesche H., Groen J., Klobes P., Levitz P., Neimark A.V., Rigby S., Skudas R., Sing K., Thommes M., Unger K. // Pure Appl. Chem. 2012. V. 84. P. 107.
William S., Hummers J.R., Offeman R.E. // J. Am. Chem. Soc. 1958. V. 80. P. 1339.
Shulga Yu.M., Baskakov S.A., Smirnov V.A., Shulga N.Yu., Belay K.G., Gutsev G.L. // J. Power Sources. 2014. V. 245. P. 33.
Baskakov S.A., Baskakova Y.V., Lyskov N.V., Dremova N.N., Irzhak A.V., Kumar Y., Michtchenko A., Shulga Y.M. // Electrochim. Acta. 2018. V. 260. P. 557.
Wenzel R.N. // Ind. Eng. Chem. 1936. V. 28. P. 988.
Shulga Y.M., Melezhik A.V., Kabachkov E.N., Milovich F.O., Lyskov N.V., Irzhak A.V., Dremova N.N., Gutsev G.L., Michtchenko A., Tkachev A.G., Kumar Y. // Appl. Phys. A. 2019. V. 125. P. 460.
Gupta R.K., Malviya M., Ansari K.R., Lgaz H., Chauhan D.S., Quraishi M.A. // Mater. Chem. Phys. 2019. V. 236. Article 121727.
Wu C.-K., Nicol M. // Chem. Phys. Lett. 1973. V. 21. P. 153.
Gruger A., Régis A., Schmatko T., Colomban P. // Vib. Spectrosc. 2001. V. 26. P. 215.
Pimenta M.A., Dresselhaus G. // Annu. Rep. Prog. Chem. Sect. C: Phys. Chem. 2007. V. 9. P. 1276.
Brown R.G. // J. Chem. Phys. 1964. V. 40. P. 2900.
Volfkovich Yu.M., Lobach A.S., Spitsyna N.G., Baskakov S.A., Sosenkin V.E., Rychagov A.Yu., Kabachkov E.N., Sakars A., Michtchenko A., Shulga Yu.M. // J. Porous Mater. 2019. V. 26. P. 1111.
Gregg S.J., Sing K.S.W. Adsorption, Surface Area and Porosity. N.Y.: Academic Press, 1967.
Eikerling M., Kharkats Y.I., Kornyshev A.A., Volfkovich Y.M. // J. Electrochem. Soc. 1998. V. 145. P. 2684.
Bard A.J., Faulkner L.R. Electrochemical Methods: Fundamentals and Applications. London: Wiley, 2001.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал