Коллоидный журнал, 2021, T. 83, № 4, стр. 404-411
Кинетика роста воздушных пузырьков на кремниевой подложке в спиртовой и водно-спиртовой средах
Н. Е. Есипова 1, *, С. В. Ицков 1
1 Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119071 Москва, Ленинский проспект, 31, Россия
* E-mail: nesipova@mail.ru
Поступила в редакцию 22.02.2021
После доработки 01.03.2021
Принята к публикации 09.03.2021
Аннотация
Представлены результаты экспериментального исследования самопроизвольного роста воздушных пузырьков размером 1 мм и менее, посаженных на твердую поверхность в этаноле и его водных растворах, при постоянных внешних условиях (атмосферное давление и температура 20°С). Заметный рост объема пузырьков в течение двух часов и более обнаружен в растворах этанола, начиная с концентрации спирта 50%. Зависимости объема пузырька от времени имеют разный характер в растворах этанола и в неразбавленном спирте.
ВВЕДЕНИЕ
На практике пузырьки обычно присутствуют в многофазных системах в виде облака дисперсных частиц различного размера, способных взаимодействовать и сливаться друг с другом. Исторически наиболее интересная ранняя задача о пузырьках принадлежит Рэлею (1917 г.), который рассматривал пульсацию сферической полости в безграничной несжимаемой жидкости. Предполагалось, что в пузырьке присутствует постоянное количество газа. Поскольку выражение для роста пузырьков, основанное на подходе Рэлея, в целом не согласуется с экспериментальными скоростями роста газовых и паровых пузырьков, было очевидно, что проблема должна рассматриваться с другой точки зрения. Позднее, в монографии Левича [1] было дано решение задачи о диффузионном потоке газа в движущийся относительно жидкости пузырек. Было показано, что пузырек меняет свои размеры вследствие нарушения диффузионного равновесия при движении жидкости в замкнутых каналах либо за счет растворения содержащихся в нем газов, либо за счет выделения в него газов, растворенных в жидкости. Используя подход Левича, автор работы [2] теоретически и экспериментально показал, что скорость диффузии газа в пузырек, при его движении в воде, возрастает пропорционально скорости обтекания пузырька в степени 1/2. Однако автор отмечает, что и при падении скорости обтекания, когда пузырек прилипает к стенке, интенсивность диффузии уменьшается незначительно, примерно в ln 2 раз. Обобщить описание движения пузырьков для всех реальных газожидкостных систем и точно предсказать рост пузырьков газа для широкого диапазона свойств жидкой фазы и размеров пузырьков довольно сложно. Однако, поскольку на поведение пузырьков большое влияние оказывают физико-химические свойства и структура объемной жидкости (плотность, вязкость, поверхностное натяжение, концентрация растворенного вещества и т.д.), можно получать конкретные результаты, варьируя эти свойства.
С развитием современного оборудования и методов исследования появляются сообщения (см., например, [3]) о заметном изменении размеров пузырьков при конвективном движении в жидкостях с разными свойствами и структурой. В частности, речь идет о спиртовых растворах, которые постоянно используются во многих промышленных, биологических и фармацевтических процессах. Здесь возникает большая мотивация для их практического исследования.
Водные растворы короткоцепочечных спиртов, таких как метанол, этанол и пропанол, представляют большой интерес в связи с их нетипичными физико-химическими свойствами в широком диапазоне концентраций. Во многих работах, например, в [3–6], было установлено, что ряд свойств бинарных систем спирт–вода (такие как уменьшение объема смеси, коэффициент диффузии, поверхностное натяжение, теплоемкость, смачивающая способность, вязкость и т.д.) значительно изменяются по сравнению со свойствами чистых спирта или воды. Было показано, что необычное поведение смешанных систем – это результат формирования организованных, четко выраженных локальных микроскопических структур или даже мицеллоподобных кластеров. На молекулярном уровне образование этих структур регулируются водородными связями и гидрофобными взаимодействиями [4]. Отрицательный объем смешения является наиболее известной особенностью водно-спиртовых растворов, и это также свидетельствует о некоторых структурных изменениях в бинарной смеси в широком диапазоне ее состава. Еще в 1966 г. Зельцер [7], основываясь на термодинамических характеристиках растворов этанола, установил состав ассоциатов и гидратов в зависимости от концентрации спирта. Так, например, в растворах этанола с массовой концентрацией до 17% в окружении 1 молекулы спирта присутствуют более 12 молекул воды. С ростом концентрации происходит изменение структуры сетки, образуемой молекулами воды. При концентрации спирта в интервале 17.5–46% на одну его молекулу приходится три молекулы воды. В области концентраций спирта приблизительно от 46% до 88% устанавливается динамическое равновесие ассоциатов из одинаковых молекул, агрегатов из разнородных молекул и одиночных молекул спирта и воды, т.е. происходит стабилизация структуры системы и образуется смесь С2Н5ОН·3Н2О и 3С2Н5ОН·Н2О. В растворах концентрации выше 88% преобладает структура чистого спирта с включенным в нее моногидратом 3С2Н5ОН·Н2О. Позднее эти результаты были проверены с помощью современных инструментальных методов, таких как инфракрасная спектроскопия [8], ультразвуковое исследование [9], рентгеновская дифракция и масс-спектроскопия [10, 11]. Наблюдали растущую агрегацию компонентов смеси и переход к гидратации. С ростом концентрации спирта его молекулы, имеющие больший размер, при встраивании в тетраэдрическую структуру воды нарушают ее и образуют так называемые полимерные гидраты спирта. В работе [12] с использованием колебательной спектроскопии была доказана повышенная концентрация спирта в поверхностном слое спиртового раствора на границе с воздухом. В недавней работе [13] по результатам экспериментального исследования по гидродинамике всплывающих пузырьков было установлено, что при достаточно низких концентрациях растворы этанола обладают свойствами растворов ПАВ с высоким градиентом концентрации спирта вблизи границы фаз. С ростом концентрации спирта этот градиент уменьшается.
Значительно удобнее рассматривать поведение одного пузырька, который сам по себе сложен по природе. В работе [14] приводятся экспериментальные и теоретические результаты, демонстрирующие различия в росте сидящих на стенке пузырьков двух видов – паровых и газовых. Паровые пузырьки растут относительно быстро, основной вклад в их рост вносит испарение. Испарение происходит с поверхности как пузырька, так и тонкой жидкой прослойки, оставшейся на подложке, которая может вносить заметный вклад в скорость роста паровых пузырьков. Для газовых пузырьков испарение не играет такой важной роли, они растут посредством диффузии растворенного в жидкости газа в пузырек.
Таким образом, во всех исследованных задачах, в которых наблюдается рост пузырька, существенным объединяющим фактором является процесс диффузии газа в пузырек или испарения на его межфазной границе. Согласно представленным в литературе данным, смеси спирта с водой имеют довольно сложную структуру, и ее влияние на объемный рост пузырей посредством диффузии неоднозначно. В этой связи представляется важным рассмотреть процесс роста воздушного пузырька в концентрированном спирте и в его водных растворах. Изучая механизм роста одиночного пузырька на твердой подложке, также существенно иметь точные знания об изменении его параметров.
В данной работе, исходя из известных сведений о связи структуры раствора спирта и его концентрации, мы исследовали кинетику самопроизвольного роста воздушных пузырьков, посаженных на твердую поверхность в дистиллированной воде и в водных растворах этанола, включая концентрированные растворы.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве твердой подложки использовались зеркально-полированные кремниевые пластины. Для получения гидрофобных поверхностей пластины обрабатывались парами гексаметилдисилазана, [(CH3)3Si]2NH, в течение суток. Гидрофобизация пластин проводилась с целью достижения более устойчивого положения пузырьков в спирте и его растворах. Как правило, угол смачивания их водой составлял 90° ± 5°.
Для приготовления растворов использовались тридистиллят воды и 96%-ный этанол. Концентрация оценивалась в массовых процентах. Смеси тщательно встряхивали для полного перемешивания и давали остыть до комнатной температуры для достижения теплового равновесия.
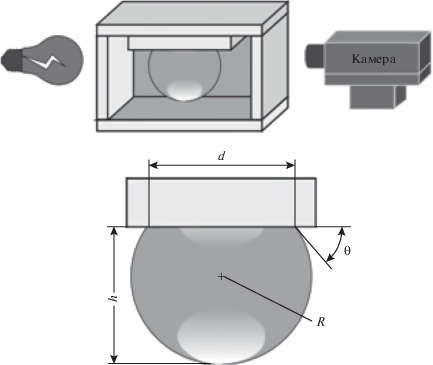
Экспериментальная установка и пузырек схематично показаны на рис. 1. Кремниевая пластина закреплялась в оптической кювете объемом 2 мл, заполненной жидкостью. С помощью микрошприца в герметично закрытую кювету через мягкую прокладку вдавливался пузырек, который садился на пластину. Связь кюветы с атмосферой поддерживалась через микроиглу. Кювета помещалась в камеру с прозрачными стеклами и устанавливалась на столик горизонтального микроскопа. С помощью видеокамеры изображение пузырька передавалось на компьютер.
Пузырек газа, сидящий на горизонтальной поверхности (рис. 1), имеет форму сферического сегмента. Его основание контактирует с оставшимся на пластине тонким жидким слоем, при этом образуется краевой угол θ, который и является наблюдаемым углом. Угол θ определяется из эксперимента и зависит от толщины смачивающей пленки между пузырьком и твердой подложкой, а также от радиуса круговой линии трехфазного контакта r = d/2. Рост радиуса контактной линии имеет характер скольжения вдоль поверхности, причем из-за локальных сдвиговых напряжений скорость роста радиуса r иногда отстает от скорости роста высоты пузырька h (известное явление “пиннинга” – “закрепления” линии трехфазного контакта [14]). Из измеренных параметров сидячего пузырька – диаметра площади посадки d и высоты h – рассчитывались такие характеристики как объем пузырька V и краевой угол θ.
Ввиду того, что размер исследуемых пузырьков был хоть и малым, но макроскопическим, пузырьки имели форму шарового сегмента, а потому их объем и краевой угол оценивались при помощи стандартных геометрических формул
(2)
$\operatorname{tg} \frac{\theta }{2} = \frac{r}{h},\,\,\,\,\theta = 2\operatorname{arctg} \frac{r}{h},$Инструментальная погрешность измерений составляла 1%. В процессе эксперимента наблюдалась кинетика роста воздушных пузырьков разного объема в этаноле и его водных растворах при атмосферном давлении и температуре 20°C в течение 120 мин. Характерные зависимости для разбавленного и концентрированного этанола и пузырьков разного размера были получены по результатам, по крайней мере, 10 измерений.
ЭКСПЕРИМЕНТАЛЬНЫЕ РЕЗУЛЬТАТЫ
Сначала исследование воздушных пузырьков, посаженных на твердую поверхность, проводилось в чистой воде. В течение двух часов не было замечено никаких изменений параметров сидячих пузырьков. В водном растворе спирта не слишком высокой концентрации (ниже 40%) за это же время заметного роста объема сидячего пузырька также не происходило.
В 50%-ном растворе этанола, в отличие от предыдущих опытов, объем прилипшего к подложке пузырька с первых минут начинал увеличиваться. Графики на рис. 2 и 3 показывают рост объема V двух пузырьков с начальными его значениями V0 = 0.1018 мкл (рис. 2) и V0 = 0.0011 мкл (рис. 3) в течение 120 мин. Объем обоих пузырьков в первые минуты растет достаточно быстро, а затем наблюдается замедление скорости их роста. Хотя значения начального объема пузырьков значительно различаются, характер хода кинетических кривых одинаков.
Рис. 2.
Рост абсолютного значения объема пузырька с V0 = 0.1018 мкл в 50%-ном этаноле в течение 120 мин.
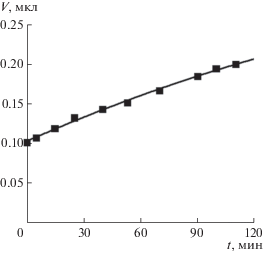
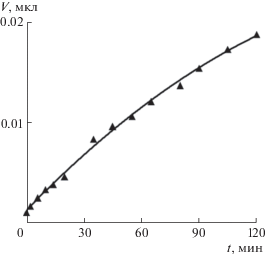
Рис. 3.
Рост абсолютного значения объема пузырька с V0 = 0.0011 мкл в 50%-ном этаноле в течение 120 мин.
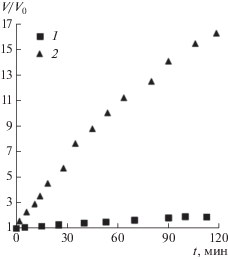
Данные об относительном изменении объема двух пузырьков, V/V0, представлены на рис. 4. Объем миллиметрового пузырька за два часа вырос примерно в 2 раза. В контрасте с ним меньший пузырек с начальным объемом 0.0011 мкл за это же время вырос примерно в 16 раз. Полученный результат иллюстрирует тот факт, что рост пузырька определяется площадью его поверхности, которая изменяется относительно начальной величины намного быстрее у маленьких пузырьков.
Рис. 4.
Изменение относительного объема V/V0 пузырьков с начальными объемами V0 = 0.1018 мкл (1) и V0 = 0.0011 мкл (2) в 50%-ном этаноле в течение 120 мин.
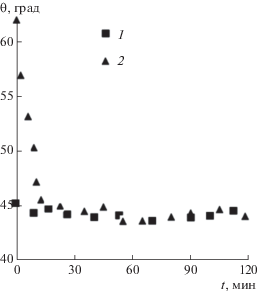
Оба этих эксперимента в 50%-ном растворе этанола проводились одновременно на одной и той же гидрофобной пластине, и в процессе роста пузырьков были измерены краевые углы. Результаты этих измерений показаны на рис. 5. При посадке миллиметрового пузырька объемом 0.1018 мкл с увеличением его объема и площади контакта начальный краевой угол θ0 ≈ 45° остается постоянным в пределах разброса данных эксперимента и является отступающим краевым углом (θr). Его значение зависит от состояния поверхности пластины, т.е. от толщины тонкой пленки, сформировавшейся между пузырьком и твердой подложкой. При посадке маленького пузырька, объемом 0.0011 мкл (диаметром ~0.1 мм), начальный краевой угол составляет θ0 = 62° и в процессе расширения пузырька уменьшается, достигая значения θr = 44° ± 2°, а при дальнейшем росте и пузырька и линии трехфазного контакта остается практически неизменным.
Рис. 5.
Изменение краевого угла при росте пузырьков с начальными объемами V0 = 0.1018 мкл (1) и V0 = = 0.0011 мкл (2) в 50%-ном этаноле в течение 120 мин.
Здесь нужно отметить следующее. При посадке пузырька на твердой поверхности остается тонкая смачивающая пленка, и толщина этой пленки по Дерягину определяется расклинивающим давлением [16, 17]. В нашем случае расклинивающее давление совпадает с капиллярным давлением Лапласа
где pα и pβ – давления в газовой и жидкой среде соответственно и γ – поверхностное натяжение. Фрумкин [17] показал, что при неполном смачивании поверхностное натяжение межфазной области, включающей тонкую пленку, можно связать с расклинивающим давлением и толщиной пленки. Автором работы [18], в результате уточнения теории Фрумкина, получено упрощенное выражение, связывающее поверхностное натяжение на границе газ–твердое тело σ αγ с толщиной пленки τ: С ростом радиуса R и соответственно падением давления в пузырьке p α растет толщина пленки на твердой поверхности. В этом случае, согласно выражению (4), поверхностное натяжение на границе газ–твердое тело σ αγ будет увеличиваться. Связь поверхностных натяжений с краевым углом на линии трехфазного контакта дается уравнением Юнга(5)
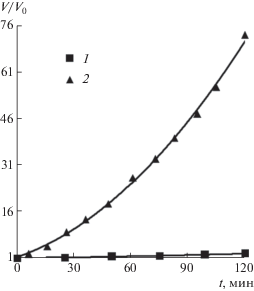
$\cos \theta = \frac{{{{\sigma }^{{\gamma \alpha }}} - {{\sigma }^{{\gamma \beta }}}}}{{{{\sigma }^{{\alpha \beta }}}}},$В 96%-ном спирте наблюдался иной характер роста объема воздушных пузырьков за то же время. На рис. 6 представлены экспериментальные данные о росте абсолютного объема пузырьков с начальными значениями V0 = 0.1167 мкл и V0 = = 0.0017 мкл в течение 120 мин. Полученные зависимости показывают, что в концентрированном этаноле рост объема пузырьков во времени идет с ускорением. Из графика на рис. 7 следует, что пузырек меньшего объема (V0 = 0.0017 мкл) в этом случае увеличился почти в 70 раз, т.е. почти в 5 раз больше в сравнении с близким по размеру пузырьком в 50%-ном растворе этанола. Пузырек большего, миллиметрового объема увеличился примерно в 3 раза.
Рис. 6.
Рост абсолютного значения объема пузырьков с V0 = 0.1167 мкл (1) и V0 = 0.0017 мкл (2) в 96%-ном этаноле в течение 120 мин.
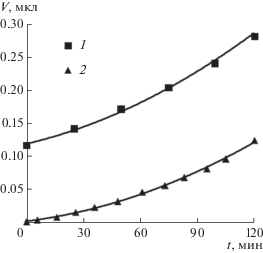
Рис. 7.
Изменение относительного объема V/V0 пузырьков с V0 = 0.1167 мкл (1) и V0 = 0.0017 мкл (2) в 96%-ном этаноле в течение 120 мин.
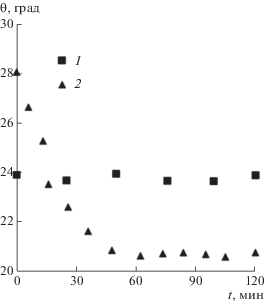
На рис. 8 показано изменение со временем углов смачивания в концентрированном этаноле. В этом случае, аналогично опыту с разбавленным раствором, для пузырька миллиметрового размера с V0 = 0.1167 мкл начальный отступающий краевой угол, равный примерно 24°, практически не изменяется. Для меньшего пузырька с V0 = 0.0017 мкл образовавшийся при посадке угол θr ≈ 28° уменьшается и с увеличением объема и площади контакта пузырька достигает значения θr ≈ 21°, после чего остается постоянным. Таким образом, изменение краевых углов для пузырьков малого объема в процессе их роста находится в согласии с концепцией Дерягина для смачивающих пленок и углов смачивания [15, 16].
Рис. 8.
Изменение краевого угла при росте пузырьков с начальными объемами V0 = 0.1167 мкл (1) и V0 = = 0.0017 мкл (2) в 96%-ном этаноле в течение 120 мин.
Как уже было показано, рост объема пузырьков в концентрированном этаноле идет с ускорением. Этот факт находит подтверждение и в опытах с промежуточными концентрациями спирта. Эксперименты проводились для пузырьков малых и близких по величине начальных объемов. На рис. 9 приведены пять графических зависимостей роста относительного объема пузырьков во времени для концентрации этанола в интервале от 50 до 96%. Видно, что постепенное повышение концентрации водно-спиртового раствора приводит к увеличению скорости роста пузырьков. При длительном выдерживании пузырьков воздуха (около 20 ч) в растворах спирта и в концентрированном этаноле, пузырьки продолжали расширяться, однако характер зависимости, отвечающей данной концентрации, не изменялся.
Рис. 9.
Изменение во времени относительного объема V/V0 пузырьков в растворах этанола разной концентрации: 50% (V0 = 0.0011 мкл), 60% (V0 = 0.0019 мкл), 70% (V0 = 0.0020 мкл), 80% (V0 = 0.0018 мкл), 96% (V0 = 0.0017 мкл).
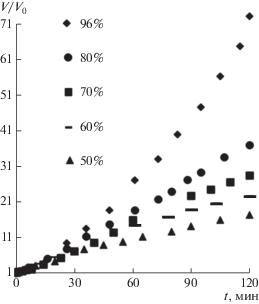
Итак, характер роста объема пузырьков со временем в растворах спирта средних и высоких концентраций различен. Если в растворах средних концентраций (например, 50–70%) изменение объема пузырька стремится к насыщению, то в концентрированном спирте скорость изменения объема возрастает со временем.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Как уже отмечалось ранее, в воде в течение двух часов не наблюдалось роста объема пузырьков. Конечно, в течение короткого начального промежутка времени (для пузырька миллиметрового размера это время составляет около секунды) водяной пар в пузырьке становится насыщенным, в результате чего пузырек может несколько увеличиться в объеме, но это составит порядка процента объема. В результате слегка нарушенного равновесия между воздухом в пузырьке и воздухом, растворенным в жидкости, возникнет диффузия воздуха из жидкости в пузырек, что приведет к его росту. Для воды этот процесс является очень медленным, и поэтому изменения размера пузырька за указанное время не наблюдалось.
Этанол, даже в смеси с водой, является весьма летучим уже при комнатной температуре. Поэтому как в концентрированном спирте, так и в его растворах рост пузырьков обеспечивается, в основном, за счет испарения спирта в пузырек. Известно, что скорость испарения растворов спирта определяется силой межмолекулярных связей (энергией водородных связей спирта, воды) и давлением насыщенного пара, а также она зависит от давления воздуха над поверхностью жидкости, температуры и площади, с которой происходит испарение. Энергия водородных связей в воде составляет 25, в спирте – 20 кДж/моль. Молекулы воды связаны между собой сильнее, чем молекулы этанола, и поэтому с меньшей скоростью переходят в газовую фазу. Давление насыщенного пара при 20°C составляет для воды 17.36, а для этанола 43.9 мм рт. ст. Таким образом, при прочих равных условиях скорость испарения водного раствора спирта выше, чем скорость испарения воды, за счет перехода молекул спирта из раствора в газовую среду пузырька.
Не являясь ПАВ, этанол все же обладает определенной поверхностной активностью в водных растворах и адсорбируется положительно на поверхности пузырька. Поэтому концентрация спирта у поверхности максимальна, а вдали от поверхности соответствует объемной концентрации раствора. Как уже отмечалось, в наших экспериментах с разбавленными растворами на начальной стадии имеет место активное испарение спирта в пузырек из прилегающих к межфазной границе слоев жидкости с высокой концентрацией спирта. Очевидно, это происходит в неравновесном состоянии. Снижение концентрации спирта на границе фаз пузырек–жидкость включает механизм диффузии молекул спирта из объема раствора для обеспечения их транспорта к стенкам пузырька. Процесс диффузии замедляет и регулирует испарение при росте пузырька в разбавленных растворах, где молекулы спирта связаны в гидратных структурах. Такой механизм обеспечивает нестационарный характер диффузии, скорость которой уменьшается со временем.
В водно-спиртовом растворе с концентрацией этанола ниже 50% объем газового пузырька, сидящего на поверхности, практически не изменяется за период наблюдения, поскольку молекулы спирта оказываются связанными молекулами воды в составе гидратов. В такой ассоциированной жидкости уменьшается способность молекул спирта к диффузии на поверхность пузырька. В области средних концентраций, начиная приблизительно с 50%-ного раствора этанола, наблюдается заметный рост объема пузырька во времени. Установившееся динамическое равновесие ассоциатов и агрегатов из одинаковых и разнородных молекул позволяет диффузионному потоку регулировать процесс испарения спирта при расширении пузырька. Поэтому со временем происходит снижение скорости потока массы спирта через единицу площади межфазной поверхности, что делает процесс испарения в этом случае нестационарным. То есть, в водно-спиртовых растворах испарение спирта является функцией диффузии его молекул в растворе к поверхности пузырька, что, в свою очередь, определяется концентрацией раствора. Увеличение скорости роста объема пузырька при увеличении концентрации спирта в нашем эксперименте это подтверждает.
При росте пузырька в концентрированном этаноле поток пара через поверхность пузырька становится стационарным. Радиус пузырька при диффузионном стационарном режиме, согласно уравнению диффузии, определяется выражением [19]:
где β – безразмерная константа роста, зависящая от природы жидкой среды, в которой расширяется пузырек, D – коэффициент диффузии, t – время. Отсюда следует, что при стационарном режиме диффузии радиус возрастает пропорционально корню квадратному из времени и соответственно изменение объема пузырька будет пропорциональным t 3/2. Именно такие зависимости и наблюдались в нашем эксперименте с концентрированным этанолом.ЗАКЛЮЧЕНИЕ
В нашей работе установлено, что за время наблюдения (120 мин) заметный рост объема воздушных пузырьков, сидящих на твердой подложке, имеет место только при концентрации спирта от 50% и выше.
В разбавленных водных растворах этанола молекулы спирта связаны в гидратных структурах, и наблюдаемое в начале увеличение скорости расширения пузырька в дальнейшем сменяется ее падением в результате уменьшения концентрации спирта вблизи поверхности пузырька. Это способствует диффузии молекул спирта в ассоциированной жидкости, что, в свою очередь, снижает скорость потока массы спирта через единицу площади межфазной поверхности и делает процесс испарения нестационарным. С ростом концентрации раствора роль диффузии возрастает, и диффузионный поток контролирует процесс испарения спирта при расширении пузырька в разбавленных растворах. Это – квазистатический процесс испарения жидкости в пузырек, при котором пузырек и окружающая среда остаются в равновесном состоянии. В концентрированном этаноле преобладает структура чистого спирта. Свободные молекулы спирта в процессе испарения обеспечивают стационарный диффузионный рост пузырька. Режим стационарного роста пузырька с постоянным потоком этанола через единицу площади межфазной поверхности реализуется только в случае концентрированного спирта и существенно заметен при очень малом начальном размере пузырька. Характер роста газовых пузырьков отражает изменения в структуре раствора спирта, которая, в свою очередь, является функцией его концентрации. Несмотря на то, что полученные нами экспериментальные результаты носят, скорее, качественный характер, они достаточно полно отражают особенности роста пузырьков в растворах спирта разной концентрации.
Список литературы
Левич В.Г. Физико-химическая гидродинамика. 2-е изд. М.: Физматгиз, 1959.
Калашников Ю.Н. // ПМТФ. 1964. № 3. С. 105.
Alves S.S., Orvalho S.P., Vasconcelos J.M.T. // Chem. Eng. Sci. 2005. V. 60. P. 1.
Dixit S., Crain J., Poon W.C.K., Finney J.L., Soper A.K. // Nature. 2002. V. 416. P. 829.
Chodzińska A., Zdziennicka A., Jańczuk B. // J. Solution Chem. 2012. V. 41. P. 2226.
Dolenko T.A., Burikov S.A., Dolenko S.A., Efitorov A.O., Plastinin I.V., Yuzhakov V.I., Patsaeva S.V. // J. Phys. Chem. A. 2015. V. 119. P. 10806.
Зельцер Я.В. // Ферментная и спиртовая промышленность. 1966. № 4. С. 11.
D’Angelo M., Onori G., Santucci A. // J. Chem. Phys. 1994. V. 100. P. 3107.
Mijaković M., Kežić B., Zoranić L., Sokolić F., Asenbaum A., Pruner C., Wilhelm E., Perera A. // J. Mol. Liq. 2011. V. 164. P. 66.
Takamuku T., Maruyama H., Watanabe K., Yamaguchi T. // J. Solution Chem. 2004. V. 33. P. 641.
Takamuku T., Saisho K., Nozawa S., Yamaguchi T. // J. Mol. Liq. 2005. V. 119. P. 133.
Sung J.H., Park K., Kim D. // J. Phys. Chem. B. 2005. V. 109. P. 18507.
Basarová P., Pišlová J., Mills J., Orvalho S. // Chem. Eng. Sci. 2018. V. 192. P. 74.
Zijl W. Departure of a Bubble Growing on a Horizontal Wall. Ph.D. Thesis. Eindhoven: Eindhoven University of Technology, 1978.
Есипова Н.Е., Русанов А.И., Соболев В.Д., Ицков С.В. // Коллоид. журн. 2019. Т. 81. С. 563.
Дерягин Б.В., Чураев Н.В. Смачивающие пленки. М.: Наука, 1984.
Зорин З.М., Коларов Т., Есипова Н.Е., Платиканов Д., Сергеева И.П. // Коллоид. журн. 1990. Т. 52. С. 666.
Фрумкин А.Н. // Журн. физ. химии. 1938. Т. 12. С. 337.
Русанов А.И. // Коллоид. журн. 2019. Т. 81. С. 767.
Scriven L.E. // Chem. Eng. Sci. 1959. V. 10. P. 1.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал