Коллоидный журнал, 2022, T. 84, № 1, стр. 114-124
Работа образования прямой и обратной мицеллы как функция числа агрегации
А. К. Щёкин 1, *, Л. Ц. Аджемян 1, Ю. А. Ерошкин 1, Н. А. Волков 1
1 Санкт-Петербургский государственный университет
199034 Санкт-Петербург,
Университетская набережная, 7–9, Россия
* E-mail: akshch@list.ru
Поступила в редакцию 11.01.2022
После доработки 15.01.2022
Принята к публикации 17.01.2022
- EDN: AODYXJ
- DOI: 10.31857/S0023291222010128
Аннотация
Рассмотрен вывод выражения для минимальной работы мицеллообразования (работы агрегации) в случае прямых и обратных сферических мицелл на основе расширенной капельной модели мицелл. Учтены вклады в работу агрегации, обусловленные гидрофобным эффектом при образовании ядра прямой мицеллы и вкладом электростатического взаимодействия при образовании ядра обратной мицеллы, эффектами конформации углеводородных хвостов и полярных головных групп в короне и ядре прямой и обратной мицеллы, влиянием поверхностного натяжения на границе между ядром мицеллы и раствором. Показано, что важную роль в стабилизации как прямых, так и обратных мицелл играет уравнение состояния молекулярных групп на поверхности ядра мицеллы. Учтенные вклады в работу агрегации позволяют объяснить механизм агрегации ПАВ в неполярном растворителе в отсутствие воды и убедиться в существовании ККМ, а также оценить среднее число агрегации сухих обратных мицелл при разной брутто-концентрации ПАВ.
ВВЕДЕНИЕ
Ключевой характеристикой термодинамической и кинетической теории мицеллообразования является минимальная работа образования агрегатов из молекул поверхностно-активного вещества (ПАВ). С работой образования связано равновесное распределение агрегатов по числам агрегации молекул ПАВ при заданных значениях объемной концентрации мономеров ПАВ в растворе и температуры. В термодинамике мицеллообразования равновесное распределение определяет степень мицеллизации, среднее число агрегации и дисперсию чисел агрегации мицелл [1–6]. В кинетической теории это распределение играет роль начального или граничного условия и определяет кинетические коэффициенты, связанные со скоростью испускания мономеров ПАВ при молекулярном механизме мицеллярной релаксации [6–11] или скоростью распада при механизме слияния–распада мицелл [6, 8, 12].
Именно по появлению при увеличении концентрации мономеров ПАВ разнесенных максимума и минимума работы образования агрегатов можно судить о достижении критической концентрации мицеллообразования (ККМ), то есть такой брутто-концентрации ПАВ, при которой заметная его доля оказывается в мицеллах и можно говорить о мицеллярном растворе.
Поэтому первым шагом на пути к построению термодинамической и кинетической теории мицеллообразования прямых мицелл является нахождение минимальной работы образования сферического молекулярного агрегата ПАВ как аналитической функции числа агрегации и концентрации мономеров ПАВ в растворе. Первый подход к решению этой задачи, предложенный в [1–5, 13–17], опирается на минимизацию термодинамического потенциала Гиббса раствора, закон действующих масс и молекулярно-термодинамическое моделирование различных вкладов в работу образования в расчете на одну молекулу ПАВ в мицелле. Второй подход состоит в рассмотрении капельной модели работы агрегации [6, 18–20] в духе представлений теории нуклеации.
Как известно [1–6], самосборка прямой мицеллы ПАВ в полярных растворителях обусловлена гидрофобным эффектом для неполярных “хвостов” молекул ПАВ, при этом размер мицелл стабилизируется за счет электростатических отталкиваний в двойном электрическом слое в короне мицеллы и эффекта исключенной поверхности на границе ядро–корона. Менее определенным является механизм самосборки обратных мицелл. Так как сольвофобный эффект при растворении ПАВ в неполярном растворителе мал, то сборка “мокрых” обратных мицелл из ПАВ, углеводородов и воды обычно считается вызванной электростатическим притяжением диполей или ионов головных групп молекул ПАВ, противоионов и диполей молекул воды в ядре мицеллы. За счет чего происходит стабилизация обратных мицелл – остается дискуссионным вопросом. Еще более противоречивая картина возникает при рассмотрении основных факторов, обуславливающих образование “сухих” обратных мицелл в неполярных растворителях в отсутствие молекул воды. Рукенштейн и Нагараджан впервые в [21], а затем в [2] обобщили и расширили модель для прямых мицелл на случай формирования обратных мицелл ПАВ в неводных и в неполярных растворах. При этом они предположили, что присутствие даже малого количества молекул воды в растворах ПАВ в неполярном растворителе, которые могли бы накапливаться в ядрах обратных мицелл, является необходимым условием существования ККМ, и в случае отсутствия воды ККМ для “сухих” обратных мицелл не существует. Это предположение было поддержано и авторами ряда других работ [22–25], в которых главный вклад в формирование обратных мицелл ПАВ в неполярных растворителях, по крайней мере, в случае ионных ПАВ возникает вследствие сильных электростатических взаимодействий в ядре в присутствии молекул воды. В последнее десятилетие появились экспериментальные работы и работы по молекулярно-динамическому моделированию обратных мицелл, как ионных, так и неионных, где показано, что ККМ и сухие обратные неионные и ионные мицеллы в неполярных растворах реально существуют [26–29]. К этому выводу приводят и наши собственные результаты молекулярного моделирования обратных мицелл С12Е4 в гептане [30]. Как показано в [31], наличие полярных добавок, которые могут быть солюбилизированы в ядрах обратных мицелл, снижает ККМ и увеличивает размер обратных мицелл.
Таким образом, объяснение механизма агрегации ПАВ в неполярном растворителе в отсутствие воды, предсказание ККМ и характерных чисел агрегации сухих обратных мицелл остается актуальной проблемой. В данном сообщении рассматривается вывод выражения для минимальной работы мицеллообразования в случае прямых и обратных сферических мицелл на основе расширенной капельной модели мицелл. Эта модель будет построена с учетом вкладов, обусловленных гидрофобным эффектом при образовании ядра прямой мицеллы и электростатическим взаимодействием при образовании ядра обратной мицеллы, эффектами изменения конформации углеводородных хвостов и полярных головных групп, влиянием поверхностного натяжения на границе между ядром мицеллы и раствором. Показано, что важную роль в стабилизации как прямых, так и обратных мицелл играет уравнение состояния молекулярных групп на поверхности ядра мицеллы.
1. ОБЩЕЕ ВЫРАЖЕНИЕ ДЛЯ РАБОТЫ АГРЕГАЦИИ ПРЯМОЙ И ОБРАТНОЙ НЕИОННОЙ МИЦЕЛЛЫ
Пусть единица объема раствора включает ${{c}_{{{\text{sol}}}}}$ молекул растворителя и ${{c}_{{1t}}}$ молекул ПАВ. В равновесии молекулы ПАВ распределены между мономерами с объемной концентрацией ${{c}_{1}}$ и молекулярными агрегатами с объемными концентрациями ${{c}_{n}}$, где $n > 1$ – число агрегации молекул ПАВ в агрегате. При наличии агрегатов величина брутто-концентрации ПАВ ${{c}_{{1t}}}$ может быть представлена в виде
Пусть величина $W\left( n \right)$ представляет собой деленную на ${{k}_{{\text{B}}}}T$ (${{k}_{{\text{B}}}}$ – постоянная Больцмана, $Т$ – абсолютная температура раствора) разность термодинамического потенциала Гиббса агрегата с числом агрегации $n$ и потенциала Гиббса $\left( {n - \operatorname{l} } \right){{\mu }_{1}}$ для $n - 1$ мономера ПАВ при равновесной концентрации мономеров ПАВ $c_{{\text{1}}}^{{\left( {\text{e}} \right)}}$ в растворе. Это разность описывает изменение термодинамического потенциала Гиббса совокупности из $n$ молекул ПАВ в результате обратимого образования агрегата в растворе при заданных значениях давления и температуры за счет присоединения $n - \operatorname{l} $ мономеров ПАВ к некоторому зафиксированному мономеру ПАВ, с которого это образование начиналось. Как известно [32], такое изменение равно минимальной работе образования агрегата (работе агрегации). При $n = \operatorname{l} $ имеем $W\left( {n = 1} \right) = 0$, что естественно, так как агрегат из одной молекулы ПАВ уже есть в растворе (более подробно об этом пределе в теории нуклеации и мицеллообразования сказано в [6, 8, 33, 34]). Можно показать [12], что выражение для равновесной объемной концентрации агрегатов $c_{n}^{{\left( {\text{e}} \right)}}$ в растворе имеет вид(2)
$c_{n}^{{\left( {\text{e}} \right)}} = c_{1}^{{\left( {\text{e}} \right)}}{{e}^{{ - W\left( {n,c_{1}^{{\left( {\text{e}} \right)}}} \right)}}} = c_{1}^{{\left( {\text{e}} \right)}}{{e}^{{ - W\left( {n,{{c}_{1}}} \right)\,\, + \,\,\left( {n\,\, - \,\,\operatorname{l} } \right)\ln \frac{{c_{1}^{{\left( {\text{e}} \right)}}}}{{{{c}_{1}}}}}}}(n > 1),$Полное число ${{N}_{{{\text{agg}}}}}$ устойчивых агрегатов в единице объема раствора равно
Удобно определить нормированное на полное число ${{N}_{{{\text{agg}}}}}$ распределение агрегатов $\tilde {c}_{n}^{{\left( {\text{e}} \right)}}$ как
(4)
$\tilde {c}_{n}^{{\left( {\text{e}} \right)}} \equiv \frac{{c_{n}^{{\left( {\text{e}} \right)}}}}{{{{N}_{{{\text{agg}}}}}}} = \frac{{{{e}^{{ - W\left( {n,\,c_{1}^{{\left( {\text{e}} \right)}}} \right)}}}}}{{\sum\limits_{n = 2}^\infty {{{e}^{{ - W\left( {n,c_{{\text{1}}}^{{\left( {\text{e}} \right)}}} \right)}}}} }}.$Важной дополнительной характеристикой будет степень мицеллизации $\alpha \equiv \frac{1}{{{{c}_{{1t}}}}}\sum\nolimits_{n = 2}^\infty {nc_{n}^{{\left( {\text{e}} \right)}}\left( {c_{{\text{1}}}^{{\left( {\text{e}} \right)}}} \right)} $ – доля молекул ПАВ в агрегатах по отношению к брутто-концентрации ${{c}_{{1t}}}$ ПАВ. С учетом (1) и (2) имеем
(5)
$\alpha \left( {c_{1}^{{\left( e \right)}}} \right) = \frac{{\sum\limits_{n = 2}^\infty {n{{e}^{{ - W\left( {n,c_{1}^{{\left( {\text{e}} \right)}}} \right)}}}} }}{{1 + \sum\limits_{n = 2}^\infty {n{{e}^{{ - W\left( {n,c_{1}^{{\left( {\text{e}} \right)}}} \right)}}}} }}.$Работа агрегации $W\left( {n,{{c}_{1}}} \right)$ молекулярного агрегата связана с химическим потенциалом мономеров ПАВ ${{\mu }_{{1n}}}$ в ядре агрегата и химическим потенциалом ${{\mu }_{1}}\left( {{{c}_{1}}} \right)$ мономеров в растворе термодинамическим соотношением
(6)
${{k}_{{\text{B}}}}T{{\partial W} \mathord{\left/ {\vphantom {{\partial W} {\partial n}}} \right. \kern-0em} {\partial n}} = {{\mu }_{{1n}}} - {{\mu }_{1}}.$Для агрегата, который находится в химическом равновесии с раствором при значении ${{\mu }_{1}} = {{\mu }_{{1n}}},$ в правой части в (6) будет стоять нуль. Соответствующие корни уравнения ${{\partial W} \mathord{\left/ {\vphantom {{\partial W} {\partial n}}} \right. \kern-0em} {\partial n}} = 0$ определяют максимумы и минимумы работы агрегации.
Соотношение (2) предполагает, что работа агрегации $W$ зависит от концентрации ${{с}_{1}}$ как $\ln {\kern 1pt} {{с}_{1}}$. Это соответствует идеальной смеси мономеров и агрегатов в растворе. Дальнейшие шаги на пути к количественной теории мицеллообразования требуют явного термодинамического определения работы $W$ как функции числа агрегации n.
В [1–5, 13–17] были предложены молекулярно-термодинамические модели различных вкладов в величину ${{W\left( {n,{{c}_{1}}} \right)} \mathord{\left/ {\vphantom {{W\left( {n,{{c}_{1}}} \right)} n}} \right. \kern-0em} n}$ как для прямых, так и для обратных мицелл. С учетом этих результатов и представлений капельной модели сферической мицеллы [6, 18, 19] мы в данном сообщении попробуем построить термодинамическое выражение в духе теории нуклеации для полной работы агрегации $W\left( {n,{{c}_{1}}} \right)$ как функции чисел агрегации n.
Согласно представлениям термодинамики нуклеации и капельной модели [6, 18, 19] выражение для работы $W = W\left( {n,{{c}_{1}}} \right)$ изотермического образования молекулярного агрегата из молекул ПАВ может быть представлено в виде
(7)
${{k}_{{\text{B}}}}TW = - n\left( {{{\mu }_{1}} - \mu _{1}^{\alpha }\left( n \right)} \right) + \gamma A\left( n \right) + {{W}_{{{\text{dl}}}}},$Представим разность химических потенциалов $\mu _{1}^{\alpha }\left( n \right) - {{\mu }_{1}}$ в виде [6, 18, 19]
(8)
$\mu _{1}^{\alpha }\left( n \right) - {{\mu }_{1}} = {{k}_{{\text{B}}}}T{{w}_{1}} + {{k}_{{\text{B}}}}T{\kern 1pt} \ln \left( {{{{{c}_{{1n}}}} \mathord{\left/ {\vphantom {{{{c}_{{1n}}}} {{{c}_{1}}}}} \right. \kern-0em} {{{c}_{1}}}}} \right),$Для прямой мицеллы работа ${{w}_{1}}$ включает при ${{n}_{{\text{C}}}} \gg 1$ так называемый гидрофобный вклад
где $B$ – положительная (что и означает гидрофобность углеводородных групп) безразмерная величина, зависящая только от температуры. Для обратной мицеллы аналогичный вклад должен возникать вследствие электростатических взаимодействий связанных зарядов, входящих в состав полярных групп. Обозначим этот вклад как ${{w}_{{{\text{el}}}}}{\text{:}}$где ${{B}_{{{\text{el}}}}}$ – положительная безразмерная величина, зависящая не только от температуры, но и от числа агрегации $n$. Как показали численные оценки для решеточной модели “сухой” обратной мицеллы [35] и молекулярно-динамическое моделирование обратных мицелл С12Е4 в гептане [30], ${{B}_{{{\text{el}}}}} \gg 1$ и имеет тенденцию выхода на постоянное значение при $n \gg 1.$Следует теперь учесть положительный вклад в разность $\mu _{1}^{\alpha }\left( n \right) - {{\mu }_{1}}$, который возникает из-за того, что образующая корону часть молекулы ПАВ с площадью сечения ${{a}_{0}}$ должна быть на поверхности ядра мицеллы, доступная площадь которой ограничена при заданном числе агрегации $n$ величиной $A\left( n \right) - n{{a}_{0}}.$ Появление такого вклада в свободную энергию мицеллы ранее подробно обсуждалось в [1, 2]. Здесь же поступим следующим образом. Без учета привязки к поверхности и эффекта исключенной площади в приближении однородности фазы ядра мицеллы можно записать ${{k}_{{\text{B}}}}T\ln \left( {{{{{c}_{{1n}}}} \mathord{\left/ {\vphantom {{{{c}_{{1n}}}} {{{c}_{1}}}}} \right. \kern-0em} {{{c}_{1}}}}} \right)$ как
(11)
${{k}_{{\text{B}}}}T{\kern 1pt} \ln {\kern 1pt} \frac{{{{c}_{{1n}}}}}{{{{c}_{1}}}} \approx {{k}_{{\text{B}}}}T{\kern 1pt} \ln {\kern 1pt} \frac{{{{c}^{\alpha }}}}{{{{c}_{1}}}},$(12)
${{c}^{\alpha }} = {n \mathord{\left/ {\vphantom {n {V\left( n \right)}}} \right. \kern-0em} {V\left( n \right)}},$(13)
$\begin{gathered} {{k}_{{\text{B}}}}T{\kern 1pt} \ln {\kern 1pt} \frac{{{{c}_{{1n}}}}}{{{{c}_{1}}}} = {{k}_{{\text{B}}}}T{\kern 1pt} \ln {\kern 1pt} \frac{{{{c}^{\alpha }}}}{{{{c}_{1}}}}\frac{{A\left( n \right)}}{{A\left( n \right) - n{{a}_{0}}}} = \\ = \,\,{{k}_{{\text{B}}}}T\left[ {\ln {\kern 1pt} \frac{{{{c}^{\alpha }}}}{{{{c}_{1}}}} - \ln \left( {1 - \frac{{n{{a}_{0}}}}{{A\left( n \right)}}} \right)} \right]. \\ \end{gathered} $Второе слагаемое в квадратных скобках в правой части (13) положительно и требует выполнения неравенства ${{n{{a}_{0}}} \mathord{\left/ {\vphantom {{n{{a}_{0}}} A}} \right. \kern-0em} A} < 1$.
Далее будем нижним индексом ${\text{d}}$ помечать величины, относящиеся к прямым мицеллам, и нижним индексом ${\text{in}}$ – величины, относящиеся к обратным мицеллам. Подставляя (9), (10) и (13) в (8), получаем
(14)
${{\left. {\mu _{1}^{\alpha }\left( n \right) - {{\mu }_{1}}} \right|}_{{\text{d}}}} = {{k}_{{\text{B}}}}T\left[ { - B{{n}_{{\text{C}}}} - \ln \left( {1 - \frac{{n{{a}_{{0{\text{d}}}}}}}{{A\left( n \right)}}} \right) + \ln {\kern 1pt} \frac{{c_{{\text{d}}}^{\alpha }}}{{{{c}_{1}}}}} \right],$(15)
${{\left. {\mu _{1}^{\alpha }\left( n \right) - {{\mu }_{1}}} \right|}_{{{\text{in}}}}} = {{k}_{{\text{B}}}}T\left[ { - {{B}_{{{\text{el}}}}} + \ln {\kern 1pt} \frac{{c_{{{\text{in}}}}^{{{\alpha }}}}}{{{{c}_{1}}}} - \ln \left( {1 - \frac{{n{{a}_{{{\text{0in}}}}}}}{{A\left( n \right)}}} \right)} \right],$2. РАБОТА ОБРАЗОВАНИЯ И КОНФОРМАЦИОННЫЕ ВКЛАДЫ
Помимо ${{w}_{{\text{h}}}}$ или ${{w}_{{{\text{el}}}}}$ в работу переноса следует включить вклады, связанные с изменением конформации молекул ПАВ при переносе их в мицеллу [1–5]. Обсудим ниже эти вклады подробнее. Конформационный вклад в свободную энергию мицеллы определяется уменьшением числа доступных состояний молекулы ПАВ, обладающей протяженными головной и хвостовой частями, при включении ее в мицеллу – уменьшением энтропии из-за влияния соседних молекул. Такое ограничение числа состояний имеет разную природу для короны мицеллы и ее ядра, поэтому можно говорить о сумме соответствующих конформационных вкладов в работу образования мицеллы. Для обратных мицелл углеводородные хвосты, образующие корону мицеллы, как мы наблюдали в молекулярно-динамическом моделировании для молекул C12E4 в гептане [30], двигаются относительно свободно.
Как изображено на рис. 1, по сравнению со случаем идеальной свободной цепи движение некоторого выбранного хвоста ограничивается эффективной силой $\vec {f}$, действующей со стороны ближайших соседних хвостов. Ось $x$ будем считать направленной по нормали к поверхности мицеллы так же, как и силу $\vec {f}$.
При заданном расстоянии между концами цепи $\vec {R}$ число возможных конформаций $W(\vec {R})$ определяет энтропию ${{S}_{{{\text{conf}}}}}(\vec {R})$ соотношением Больцмана
(16)
${{S}_{{{\text{conf}}}}}(\vec {R}) = {{k}_{{\text{B}}}}{\kern 1pt} \ln {\kern 1pt} W(\vec {R}).$Очевидно, $W(\vec {R}) = CP(\vec {R})$, где $P(\vec {R})$ – плотность вероятности того, что конец цепи имеет координату $\vec {R}$, $C$ – коэффициент пропорциональности. Таким образом,
(17)
${{S}_{{{\text{conf}}}}}(\vec {R}) = {{k}_{{\text{B}}}}{\kern 1pt} \ln {\kern 1pt} P(\vec {R}) + {{k}_{{\text{B}}}}{\kern 1pt} \ln {\kern 1pt} C.$В гауссовом приближении [26]
(18)
$P(\vec {R}) = {{(2\pi {{l}_{{{\text{sg}}}}}l{\text{/}}3)}^{{ - 3/2}}}{\text{exp}}\left( { - \frac{{3{{R}^{2}}}}{{2{{l}_{{{\text{sg}}}}}l}}} \right),$(19)
${{S}_{{{\text{conf}}}}}(\vec {R}) = - \frac{{3{{k}_{{\text{B}}}}{{R}^{2}}}}{{2{{l}_{{{\text{sg}}}}}l}} + {\text{const}}.$Усреднение этого выражения для свободной идеальной цепи производится с помощью вытекающих из (18) соотношений
(20)
$\left\langle {R_{{x0}}^{2}} \right\rangle = \left\langle {R_{{y0}}^{2}} \right\rangle = \left\langle {R_{{z0}}^{2}} \right\rangle = \frac{1}{3}{{l}_{{{\text{sg}}}}}l,\,\,\,\,\left\langle {R_{0}^{2}} \right\rangle = {{l}_{{{\text{sg}}}}}l.$Учет действия эффективной внешней силы проведем по Флори [36]. Пусть в результате действия внешней силы возникло “утолщение” мицеллярной короны в $b$ раз: $\left\langle {R_{x}^{2}} \right\rangle = {{b}^{2}}\left\langle {R_{{x0}}^{2}} \right\rangle \equiv \frac{{{{D}^{2}}}}{3}$, где введена эффективная толщина короны $D$, в терминах которой параметр растяжения $b$ выражается в виде
(21)
${{b}^{2}} = \frac{{{{D}^{2}}}}{{\left\langle {R_{0}^{2}} \right\rangle }} = \frac{{{{D}^{2}}}}{{{{l}_{{{\text{sg}}}}}l}}.$Строго говоря, параметр растяжения $b$ должен зависеть от числа агрегации $n$. Из условия несжимаемости мономера для составляющих $x$ и $y$ имеем [36]
(22)
$\left\langle {R_{y}^{2}} \right\rangle = \frac{1}{b}\left\langle {R_{{y0}}^{2}} \right\rangle ,\,\,\,\,\left\langle {R_{z}^{2}} \right\rangle = \frac{1}{b}\left\langle {R_{{z0}}^{2}} \right\rangle .$Для усредненного изменения энтропии $\left\langle {\Delta {{S}_{{{\text{conf}}}}}} \right\rangle $ под действием эффективной внешней силы получаем
(23)
$\begin{gathered} \left\langle {\Delta {{S}_{{{\text{conf}}}}}} \right\rangle = \frac{{ - 3{{k}_{{\text{B}}}}}}{{2{{l}_{{{\text{sg}}}}}l}} \times \\ \times \,\,\left[ {\left( {{{b}^{2}} - 1} \right)\left\langle {R_{{x0}}^{2}} \right\rangle + \left( {\frac{1}{b} - 1} \right)\left\langle {R_{{y0}}^{2}} \right\rangle + \left( {\frac{1}{b} - 1} \right)\left\langle {R_{{z0}}^{2}} \right\rangle } \right], \\ \end{gathered} $(24)
$\left\langle {\Delta {{S}_{{{\text{conf}}}}}} \right\rangle = - \frac{1}{2}{{k}_{{\text{B}}}}\left[ {{{b}^{2}} + \frac{2}{b} - 3} \right].$Таким образом, искомый конформационный вклад от короны мицеллы $w_{{{\text{conf}}}}^{{{\text{cr}}}} = - T\left\langle {\Delta {{S}_{{{\text{conf}}}}}} \right\rangle $ в свободную энергию мицеллы в расчете на одну молекулу ПАВ равен
(25)
$w_{{{\text{conf}}}}^{{{\text{cr}}}} = \frac{1}{2}{{k}_{{\text{B}}}}T\left[ {{{b}^{2}} + \frac{2}{b} - 3} \right].$При расчете конформационного вклада от ядра прямой мицеллы в работах [5, 37] была принята следующая модель. Головные группы молекул ПАВ считались закрепленными на поверхности ядра мицеллы с радиальной координатой $R = 0$ (в центре мицеллы $R = r$, где $r$– радиус ядра мицеллы), свободный конец цепи находился внутри мицеллы при $R = {{R}_{0}}$. Цепи рассматривались как непрерывные нити длиной $l = {{l}_{{{\text{sg}}}}}{{N}_{{{\text{sg}}}}},$ где ${{N}_{{{\text{sg}}}}}$ – эффективное число сегментов. Форма цепи описывалась функцией $R(k)$, где $k$ – номер сегмента, а $R(k)$ – его радиальное расстояние от поверхности мицеллы; $0 \leqslant k \leqslant {{N}_{{{\text{sg}}}}}.$ По определению, на поверхности мицеллы $R(0) = 0$, а для внутреннего конца цепи $R({{N}_{{{\text{sg}}}}}){\text{ }} = {{R}_{0}}.$ Локальное растяжение цепи в радиальном направлении характеризовалось функцией $E({{R}_{0}},R) = {{dR} \mathord{\left/ {\vphantom {{dR} {dk}}} \right. \kern-0em} {dk}}$ ($0 < {{R}_{0}} \leqslant r$), обратная величина, ${1 \mathord{\left/ {\vphantom {1 {E({{R}_{0}},R)}}} \right. \kern-0em} {E({{R}_{0}},R)}} = {{dk} \mathord{\left/ {\vphantom {{dk} {dR}}} \right. \kern-0em} {dR}}$, определяла количество сегментов (данной молекулы) на единицу длины в радиальном направлении.
Для получения конформационного вклада соотношение (19) применялось к каждому фрагменту углеводородного хвоста мономера внутри ядра мицеллы. Для фрагмента, концы которого разнесены на $\Delta R$ и содержат $\Delta k$ сегментов, формула (19) с заменами $R \to \Delta R,\,\,l \to {{l}_{{{\text{sg}}}}}\Delta k$ дает $\Delta {{S}_{{{\text{conf}}}}}{\text{ = }} - \frac{3}{2}\frac{{{{{(\Delta R)}}^{2}}}}{{\Delta kl_{{{\text{sg}}}}^{2}}}$, или, для бесконечно малого фрагмента,
(26)
$d{{S}_{{{\text{conf}}}}}{\text{ = }} - \frac{3}{{2l_{{{\text{sg}}}}^{2}}}\frac{{dR}}{{dk}}dR = - \frac{3}{{2l_{{{\text{sg}}}}^{2}}}E({{R}_{0}},R)dR.$Для усреднения этого выражения по всем цепям (всем молекулам ПАВ, входящим в мицеллу) вводилась величина $G({{R}_{0}})d{{R}_{0}}$ – среднее число молекул, у которых хвосты лежат в интервале $d{{R}_{0}}.$ Полный конформационный вклад в свободную энергию ${{F}_{{{\text{conf}}}}}$ получался интегрированием выражения (26) с функцией $G({{R}_{0}}){\text{:}}$
(27)
$\frac{{{{F}_{{{\text{conf}}}}}}}{{{{k}_{{\text{B}}}}T}} = \frac{3}{{2l_{{{\text{sg}}}}^{2}}}\int\limits_0^r {G({{R}_{0}})\left[ {\int\limits_0^{{{R}_{0}}} {E({{R}_{0}},R)} dR} \right]} d{{R}_{0}}.$Здесь интегрирование по $R$ эквивалентно суммированию вкладов от всех сегментов данной молекулы, а интегрирование по ${{R}_{0}}$ – суммированию по всем молекулам ПАВ. Функции $G({{R}_{0}})$ и $E({{R}_{0}},R)$ были найдены в [5] из условия максимума полной энтропии при условии постоянства плотности сегментов внутри ядра мицеллы. В результате было получено следующее выражение для конформационного вклада в свободную энергию ядра мицеллы на одну молекулу:
(28)
$w_{{{\text{conf}}}}^{{{\text{nu}}}} = \frac{{{{F}_{{{\text{conf}}}}}}}{{{{k}_{{\text{B}}}}Tn}} = \frac{{3{{\pi }^{2}}{{r}^{2}}\left( n \right)}}{{80{{l}_{{{\text{sg}}}}}l}}.$При постоянной плотности сегментов в ядре $r(n) \sim {{n}^{{1/3}}}$, поэтому $w_{{{\text{conf}}}}^{{{\text{nu}}}} \sim {{n}^{{2/3}}}$. Такая же зависимость конформационного вклада от числа агрегации имеет место при отличной от сферической геометрии ядра [5]. В этом случае изменяется лишь численный коэффициент в (28).
Число конформаций в ядре обратной мицеллы, по-видимому, значительно меньше, чем в ядре прямой мицеллы. Это связано с тем, что ядро прямых мицелл формируется в результате гидрофобного эффекта со стороны полярного растворителя, и число конформаций внутри ядра ограничивается объемом ядра при постоянной средней плотности сегментов. В случае же обратных мицелл ядро формируется за счет кулоновских взаимодействий внутри ядра, что резко уменьшает число допустимых конформаций. Это приводит к значительному уменьшению энтропии при переносе головной части мономера внутрь ядра. Однако эта величина не зависит от параметров мицеллы и лишь переопределяет постоянную составляющую в $w_{{{\text{conf}}}}^{{{\text{nu}}}},$ что приводит к линейному положительному вкладу в работу образования обратной мицеллы.
3. РАБОТА ОБРАЗОВАНИЯ МИЦЕЛЛЫ И УРАВНЕНИЕ СОСТОЯНИЯ ЧАСТЕЙ МОЛЕКУЛЫ ПАВ НА ПОВЕРХНОСТИ ЯДРА МИЦЕЛЛЫ
Еще более точное, чем (14) или (15), представление для разности химических потенциалов $\mu _{1}^{\alpha }\left( n \right) - {{\mu }_{1}}$ в (7) можно получить из уравнения состояния для системы жестких дисков с исключенной поверхностью. С этой целью возьмем двумерное уравнение состояния теории масштабируемых частиц [38, 39], которое в наших обозначениях имеет вид
где ${{\rho \equiv n} \mathord{\left/ {\vphantom {{\rho \equiv n} A}} \right. \kern-0em} A}$ – поверхностная плотность полярных групп в случае прямой мицеллы или углеводородных хвостов в случае обратной мицеллы, $\Pi $ – двумерное давление. Как известно, это уравнение является двумерным аналогом известного уравнения Карнахана–Старлинга для жестких шаров. Как отмечалось в [39], уравнение (29), несмотря на его аналитическую простоту, хорошо применимо при всех значениях плотности ${n \mathord{\left/ {\vphantom {n A}} \right. \kern-0em} A}$. Нас интересует вклад $\Delta \mu _{1}^{\alpha }\left( \rho \right)$ в $\mu _{1}^{\alpha }\left( n \right) - {{\mu }_{1}}$, который возникает от разности давления $\Pi $ и вклада ${{k}_{{\text{B}}}}T{n \mathord{\left/ {\vphantom {n A}} \right. \kern-0em} A}$ в приближении идеального газа. Интегрируя соотношение Гиббса–Дюгема с учетом (29), находим(30)
$\begin{gathered} \Delta \mu _{1}^{\alpha }\left( \rho \right) = \int\limits_0^\rho {\frac{{d\left[ {\Pi \left( {\rho {\kern 1pt} '} \right) - {{k}_{{\text{B}}}}T\rho {\kern 1pt} '} \right]}}{{\rho {\kern 1pt} '}}} = \\ = {{k}_{{\text{B}}}}T\left[ { - \ln \left( {1 - {{a}_{0}}\rho } \right) + \frac{{\left( {3 - 2{{a}_{0}}\rho } \right){{a}_{0}}\rho }}{{{{{\left( {1 - {{a}_{0}}\rho } \right)}}^{2}}}}} \right]. \\ \end{gathered} $Подставляя (30) в (8), учитывая (9), (10), (25) (28) и (30), получаем
(31)
$\begin{gathered} {{\left. {\mu _{1}^{\alpha }\left( n \right) - {{\mu }_{1}}} \right|}_{{\text{d}}}} = {{k}_{{\text{B}}}}T\left[ { - B{{n}_{{\text{C}}}} - \ln \left( {1 - \frac{{n{{a}_{{0{\text{d}}}}}}}{{A\left( n \right)}}} \right) + } \right. \\ + \,\,\frac{{\left( {3 - 2{{a}_{{0{\text{d}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}} \right){{a}_{{0{\text{d}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}}}{{{{{\left( {1 - {{a}_{{0{\text{d}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}} \right)}}^{2}}}} + \\ \left. { + \,\,\frac{1}{2}\left( {b_{{\text{d}}}^{2} + \frac{2}{{{{b}_{{\text{d}}}}}} - 3} \right) + w_{{{\text{conf}}}}^{{{\text{nu}}}}\left( n \right) + \ln \frac{{c_{{\text{d}}}^{\alpha }}}{{{{c}_{1}}}}} \right], \\ \end{gathered} $(32)
$\begin{gathered} {{\left. {\mu _{1}^{\alpha }\left( n \right) - {{\mu }_{1}}} \right|}_{{{\text{in}}}}} = {{k}_{{\text{B}}}}T\left[ { - {{B}_{{{\text{el}}}}} - \ln \left( {1 - \frac{{n{{a}_{{0{\text{in}}}}}}}{{A\left( n \right)}}} \right) + } \right. \\ + \,\,\frac{{\left( {3 - 2{{a}_{{0{\text{in}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}} \right){{a}_{{0{\text{in}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}}}{{{{{\left( {1 - {{a}_{{0{\text{in}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}} \right)}}^{2}}}} + \\ \left. { + \,\,\frac{1}{2}\left( {b_{{{\text{in}}}}^{2} + \frac{2}{{{{b}_{{{\text{in}}}}}}} - 3} \right) + \ln {\kern 1pt} \frac{{c_{{{\text{in}}}}^{{{\alpha }}}}}{{{{c}_{1}}}}} \right], \\ \end{gathered} $В итоге, с учетом (7) и (31), (32) приходим к следующим выражениям для работы ${{W}_{{\text{d}}}}$ образования прямой мицеллы и работы ${{W}_{{{\text{in}}}}}$ образования обратной мицеллы произвольной формы:
(33)
$\begin{gathered} {{W}_{{\text{d}}}} = n\left[ { - B{{n}_{{\text{C}}}} - \ln \left( {1 - \frac{{n{{a}_{{0{\text{d}}}}}}}{{A\left( n \right)}}} \right) + } \right. \\ + \,\,\frac{{\left( {3 - 2{{a}_{{0{\text{d}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}} \right){{a}_{{0{\text{d}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}}}{{{{{\left( {1 - {{a}_{{0{\text{d}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}} \right)}}^{2}}}} + \\ \left. { + \frac{1}{2}\left( {b_{{\text{d}}}^{2} + \frac{2}{{{{b}_{{\text{d}}}}}} - 3} \right) + w_{{{\text{conf}}}}^{{{\text{nu}}}}\left( n \right) + \ln \frac{{c_{{\text{d}}}^{\alpha }}}{{{{c}_{1}}}}} \right] + \\ + \,\,\frac{{{{\gamma }_{{\text{d}}}}}}{{{{k}_{{\text{B}}}}T}}A\left( n \right) + \frac{{{{W}_{{{\text{dl}}}}}\left( n \right)}}{{{{k}_{{\text{B}}}}T}}, \\ \end{gathered} $(34)
$\begin{gathered} {{W}_{{{\text{in}}}}} = n\left[ { - {{B}_{{el}}} - \ln \left( {1 - \frac{{n{{a}_{{0{\text{in}}}}}}}{{A\left( n \right)}}} \right) + } \right. \\ + \,\,\frac{{\left( {3 - 2{{a}_{{0{\text{in}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}} \right){{a}_{{0{\text{in}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}}}{{{{{\left( {1 - {{a}_{{0{\text{in}}}}}{n \mathord{\left/ {\vphantom {n {A\left( n \right)}}} \right. \kern-0em} {A\left( n \right)}}} \right)}}^{2}}}} + \\ \left. { + \,\,\frac{1}{2}\left( {b_{{{\text{in}}}}^{2} + \frac{2}{{{{b}_{{{\text{in}}}}}}} - 3} \right) + \ln {\kern 1pt} \frac{{c_{{{\text{in}}}}^{\alpha }}}{{{{c}_{1}}}}} \right] + \frac{{{{\gamma }_{{{\text{in}}}}}}}{{{{k}_{{\text{B}}}}T}}A\left( n \right). \\ \end{gathered} $В случае сферической мицеллы радиус ядра мицеллы в капельной модели связан с числом агрегации $n$ как [6, 18, 19]
Для прямой мицеллы
(36)
${{\lambda }_{{\text{d}}}} \equiv {{\left[ {\frac{{3\upsilon \left( {{{n}_{{\text{C}}}} + 1} \right)}}{{4\pi }}} \right]}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}},$(37)
${{\lambda }_{{{\text{in}}}}} \equiv {{\left[ {\frac{{3{{\upsilon }_{{\text{p}}}}}}{{4\pi }}} \right]}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}},$(38)
${{A}_{{\text{d}}}}\left( n \right) = 4\pi \lambda _{{\text{d}}}^{{\text{2}}}{{n}^{{{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}}}},$(39)
${{A}_{{{\text{in}}}}}\left( n \right) = 4\pi \lambda _{{{\text{in}}}}^{2}{{n}^{{{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}}}}.$Если в ${{W}_{{{\text{dl}}}}}$ для прямых мицелл учитывать вклад диполей полярных головных групп молекул ПАВ, то имеем [6, 18, 19]
(40)
${{W}_{{{\text{dl}}}}} = \frac{{\delta {{{\left( {ze} \right)}}^{2}}{{n}^{{{4 \mathord{\left/ {\vphantom {4 3}} \right. \kern-0em} 3}}}}}}{{8\pi {{\varepsilon }_{0}}\varepsilon {{\lambda }_{{\text{d}}}}^{2}}},$С учетом (35)–(40) перепишем выражения (33) и (34) для ${{W}_{{\text{d}}}}$ и ${{W}_{{{\text{in}}}}}$ в случае сферических мицелл в виде
(41)
$\begin{gathered} {{W}_{{\text{d}}}} = n\left[ { - B{{n}_{{\text{C}}}} - \ln \left( {1 - \frac{{{{a}_{{0{\text{d}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}}}{{\lambda _{{\text{d}}}^{2}}}} \right) + } \right. \\ + \,\,\frac{{\left( {3 - {{2{{a}_{{0{\text{d}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} \mathord{\left/ {\vphantom {{2{{a}_{{0{\text{d}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} {\lambda _{{\text{d}}}^{2}}}} \right. \kern-0em} {\lambda _{{\text{d}}}^{2}}}} \right){{{{a}_{{0{\text{d}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} \mathord{\left/ {\vphantom {{{{a}_{{0{\text{d}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} {\lambda _{{\text{d}}}^{2}}}} \right. \kern-0em} {\lambda _{{\text{d}}}^{2}}}}}{{{{{\left( {1 - {{{{a}_{{0{\text{d}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} \mathord{\left/ {\vphantom {{{{a}_{{0{\text{d}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} {\lambda _{{\text{d}}}^{2}}}} \right. \kern-0em} {\lambda _{{\text{d}}}^{2}}}} \right)}}^{2}}}} + \\ \left. { + \,\,\frac{{3{{\pi }^{2}}\lambda _{{\text{d}}}^{2}{{n}^{{{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}}}}}}{{80{{l}_{{{\text{sg}}}}}l}} + \frac{1}{2}\left( {b_{{\text{d}}}^{2} + \frac{2}{{{{b}_{{\text{d}}}}}} - 3} \right) + \ln {\kern 1pt} \frac{{c_{{\text{d}}}^{\alpha }}}{{{{c}_{1}}}}} \right] + \\ + \,\,\frac{{{{\gamma }_{{\text{d}}}}\lambda _{{\text{d}}}^{2}{{n}^{{{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}}}}}}{{{{k}_{{\text{B}}}}T}} + \frac{{\delta {{{\left( {ze} \right)}}^{2}}{{n}^{{{4 \mathord{\left/ {\vphantom {4 3}} \right. \kern-0em} 3}}}}}}{{8\pi {{k}_{{\text{B}}}}T{{\varepsilon }_{0}}\varepsilon {{\lambda }_{{\text{d}}}}^{2}}}, \\ \end{gathered} $(42)
$\begin{gathered} {{W}_{{{\text{in}}}}} = n\left[ { - {{B}_{{{\text{el}}}}} - \ln \left( {1 - \frac{{{{a}_{{0{\text{in}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}}}{{\lambda _{{{\text{in}}}}^{2}}}} \right) + } \right. \\ + \,\,\frac{{\left( {3 - 2{{{{a}_{{0{\text{in}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} \mathord{\left/ {\vphantom {{{{a}_{{0{\text{in}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} {\lambda _{{{\text{in}}}}^{2}}}} \right. \kern-0em} {\lambda _{{{\text{in}}}}^{2}}}} \right){{{{a}_{{0{\text{in}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} \mathord{\left/ {\vphantom {{{{a}_{{0{\text{in}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} {\lambda _{{{\text{in}}}}^{2}}}} \right. \kern-0em} {\lambda _{{{\text{in}}}}^{2}}}}}{{{{{\left( {1 - {{{{a}_{{0{\text{in}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} \mathord{\left/ {\vphantom {{{{a}_{{0{\text{in}}}}}{{n}^{{{1 \mathord{\left/ {\vphantom {1 3}} \right. \kern-0em} 3}}}}} {\lambda _{{{\text{in}}}}^{2}}}} \right. \kern-0em} {\lambda _{{{\text{in}}}}^{2}}}} \right)}}^{2}}}} + \\ \left. { + \,\,\frac{1}{2}\left( {b_{{{\text{in}}}}^{2} + \frac{2}{{{{b}_{{{\text{in}}}}}}} - 3} \right) + \ln {\kern 1pt} \frac{{c_{{{\text{in}}}}^{\alpha }}}{{{{c}_{1}}}}} \right] + \frac{{{{\gamma }_{{{\text{in}}}}}\lambda _{{{\text{in}}}}^{2}{{n}^{{{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}}}}}}{{{{k}_{{\text{B}}}}T}}. \\ \end{gathered} $4. ЧИСЛЕННЫЕ ОЦЕНКИ
Для численных оценок в качестве молекулы ПАВ возьмем молекулу C12E4, в качестве полярного растворителя – воду, в качестве неполярного растворителя – гептан. На рис. 2а и 2б изображена молекула C12E4 и указаны ее характерные размеры. Заметим, что длина ее углеводородного хвоста согласно [2] равна l = l(CH3) + 11l(CH2) = 1.67 нм, где $l\,({\text{C}}{{{\text{H}}}_{{\text{3}}}}) = 0.280\,$ нм, $l\,({\text{C}}{{{\text{H}}}_{{\text{2}}}}) = 0.1265$ нм. Видим, что данные [2] и данные, полученные нами путем анализа структуры молекулы C12E4 [43], несколько различаются. Поперечные размеры двух групп СН2 совпадают с поперечными размерами группы E на рис. 2б.
Рис. 2.
(а) Структура молекулы C12E4 [43]. Серо-зеленые сферы отображают атомы углерода, красные – атомы кислорода, светлые – атомы водорода. Линейные размеры указаны в ангстремах. Размеры атомов и атомных групп, входящих в молекулу C12E4, были получены путем анализа структуры молекулы в программе Avogadro v.1.2.0 [44]. (б) Поперечные размеры головной группы Е. Линейные размеры указаны в ангстремах.

Возьмем следующие значения параметров системы и учтем (36), (37):
$T = 293\,\,K,$ $\upsilon = {\text{26}}{\text{.9}} \times {\text{1}}{{{\text{0}}}^{{ - 30}}}$ м3 [2], ${{v}_{{\text{p}}}} = {\text{63}} \times {\text{4}} \times {\text{1}}{{{\text{0}}}^{{ - 30}}} = 252 \times {\text{1}}{{{\text{0}}}^{{ - 30}}}$ м3 [2], $B = 1.4$ [2], ${{B}_{{{\text{el}}}}} = 20$ [30], ${{n}_{{\text{C}}}} = 12$, ${{\lambda }_{{\text{d}}}} = 4.4 \times {{10}^{{ - 10}}}$ м,
${{\lambda }_{{{\text{in}}}}} = 3.9 \times {{10}^{{ - 10}}}$ м, γd = 40 мН/м [5], ${{\gamma }_{{{\text{in}}}}} = 30$ мН/м, ${{a}_{{0{\text{d}}}}} = 21 \times {{10}^{{ - 20}}}$ м2 [2], ${{a}_{{0{\text{in}}}}} = 21 \times {{10}^{{ - 20}}}$ м2 [2],
Для эффективной длины гидрофобного сегмента примем значение ${{l}_{{{\text{sg}}}}} = 0.46\,\,$ нм [45]. Тогда эффективное число сегментов ${{N}_{{{\text{sg}}}}} = {l \mathord{\left/ {\vphantom {l {{{l}_{{{\text{sg}}}}}}}} \right. \kern-0em} {{{l}_{{{\text{sg}}}}}}} \approx 4.$ Максимальное значение ${{D}_{{\max }}} = l,$ поэтому согласно (21) $b_{{\max }}^{2} = {{N}_{{{\text{sg}}}}} \approx 4,$ откуда ${{b}_{{\max }}} \approx 2,$ и из (25) находим
(44)
${{w_{{{\text{conf}}}}^{{{\text{cr}}}}} \mathord{\left/ {\vphantom {{w_{{{\text{conf}}}}^{{{\text{cr}}}}} {{{k}_{{\text{B}}}}T}}} \right. \kern-0em} {{{k}_{{\text{B}}}}T}} = \frac{1}{2}\left( {b_{{{\text{in}}}}^{2} + \frac{2}{{{{b}_{{{\text{in}}}}}}} - 3} \right) \leqslant 1.$На рис. 3а показана зависимость работы ${{W}_{{\text{d}}}}\left( {n,{{c}_{1}}} \right)$ образования прямой мицеллы в водном растворе от равновесной концентрации ${{c}_{1}}$ мономеров ПАВ в растворе и числа агрегации n. Расчет был сделан по формуле (41) с учетом (43), где мы положили $n = n - 1$, чтобы обеспечить ${{W}_{{\text{d}}}}\left( {n = 1} \right) = 0.$
Рис. 3.
(а) Работа ${{W}_{{\text{d}}}}\left( {n,{{c}_{1}}} \right)$ образования сферической прямой мицеллы как функция равновесной концентрации ${{c}_{1}}$ мономеров ПАВ в водном растворе и числа агрегации $n$; (б) степень мицеллизации ${{\alpha }_{{\text{d}}}}\left( {{{c}_{1}}} \right)$ в водном растворе ПАВ как функция равновесной концентрации ${{c}_{1}}$ мономеров ПАВ.
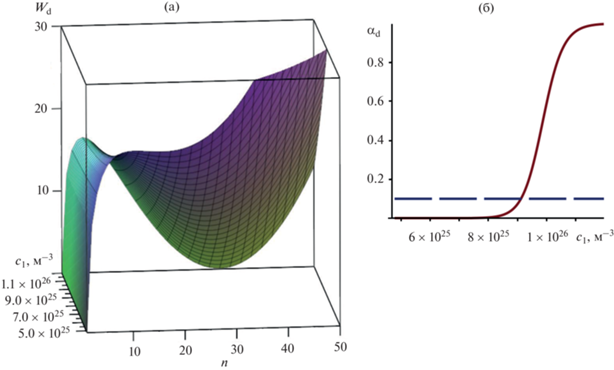
На рис. 3б изображена степень мицеллизации ${{\alpha }_{{\text{d}}}}\left( {{{c}_{1}}} \right)$ молекул ПАВ в прямых мицеллах в водном растворе ПАВ, рассчитанная по формулам (5) и (41). На рис. 3б горизонтальной линией показано значение степени мицеллизации ${{\alpha }_{{{\text{ККМ}}}}} = 0.1,$ при котором достигается ККМ в водном растворе.
Из рис. 3а следует, что при выбранных значениях параметров работа ${{W}_{{\text{d}}}}\left( {n,{{c}_{1}}} \right)$ агрегации прямой мицеллы как функция числа агрегации $n$ имеет точку перегиба, отвечающую корню уравнения ${{{{\partial }^{2}}{{W}_{{\text{d}}}}\left( {n,{{c}_{1}}} \right)} \mathord{\left/ {\vphantom {{{{\partial }^{2}}{{W}_{{\text{d}}}}\left( {n,{{c}_{1}}} \right)} {\partial {{n}^{2}}}}} \right. \kern-0em} {\partial {{n}^{2}}}} = 0.$ Именно наличие точки перегиба приводит с ростом концентрации мономеров ПАВ ${{c}_{1}}$ к появлению максимума работы ${{W}_{{\text{d}}}}\left( {n,{{c}_{1}}} \right)$ левее и минимума работы ${{W}_{{\text{d}}}}\left( {n,{{c}_{1}}} \right)$ правее точки перегиба на рис. 3а. Числа агрегации для максимума и минимума работы агрегации отвечают корням уравнения (6) с учетом выражения (41). С ростом концентрации ${{c}_{1}}$ высота максимума работы агрегации медленно убывает, а сам максимум сдвигается в сторону меньших чисел агрегации. При этом минимум работы агрегации сдвигается в сторону больших чисел агрегации, а его глубина быстро растет. Накопление числа агрегатов в области минимума работы агрегации ${{W}_{{\text{d}}}}\left( {n,{{c}_{1}}} \right)$ (потенциальной ямы для образования прямых мицелл) с увеличением ${{c}_{1}}$ приводит к достижению ККМ и быстрому росту степени мицеллизации при ${{c}_{1}} > {{\left. {{{c}_{1}}} \right|}_{{{\text{ККМ}}}}}$ на рис. 3б. Результаты расчета очень чувствительны к выбору параметров υ, ${{a}_{{0{\text{d}}}}}$ и учету или отбрасыванию вклада ${{W}_{{{\text{dl}}}}}.$ Учет конформационных вкладов слабо влияет на положение точки перегиба, но заметно изменяет значение ККМ.
На рис. 4а показана зависимость работы образования ${{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)$ обратной мицеллы в гептане от равновесной концентрации ${{c}_{1}}$ мономеров ПАВ в растворе и числа агрегации $n$. Расчет был сделан по формуле (42) с учетом (43) и (44). Мы положили $n = n - 1$ в (42), чтобы обеспечить ${{W}_{{{\text{in}}}}}\left( {n = 1} \right) = 0$. На рис. 4б изображена степень мицеллизации ${{\alpha }_{{{\text{in}}}}}\left( {{{c}_{1}}} \right)$ молекул ПАВ в прямых мицеллах в водном растворе ПАВ, рассчитанная по формулам (5) и (42). На рис. 4б горизонтальной линией показано значение степени мицеллизации ${{\alpha }_{{{\text{ККМ}}}}} = 0.1,$ при котором достигается ККМ в гептане.
Рис. 4.
(а) Работа ${{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)$ образования сферической обратной мицеллы как функция равновесной концентрации ${{c}_{1}}$ мономеров ПАВ в гептане и числа агрегации $n$; (б) степень мицеллизации ${{\alpha }_{{{\text{in}}}}}\left( {{{c}_{1}}} \right)$ в растворе ПАВ в гептане как функция равновесной концентрации ${{c}_{1}}$ мономеров ПАВ.
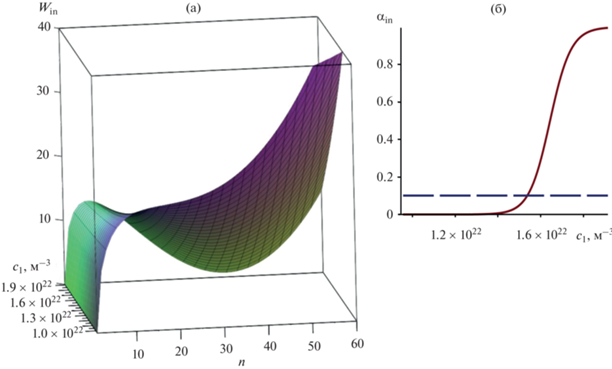
На рис. 4а видно, что при выбранных значениях параметров работа агрегации ${{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)$ сухой обратной мицеллы как функция числа агрегации $n$ так же, как и работа ${{W}_{{\text{d}}}}\left( {n,{{c}_{1}}} \right)$, имеет точку перегиба, отвечающую в данном случае корню уравнения ${{{{\partial }^{2}}{{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)} \mathord{\left/ {\vphantom {{{{\partial }^{2}}{{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)} {\partial {{n}^{2}}}}} \right. \kern-0em} {\partial {{n}^{2}}}} = 0$. Соответственно с ростом концентрации мономеров ПАВ ${{c}_{1}}$ в неполярном растворителе появляется максимум работы ${{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)$ левее и минимум работы ${{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)$ правее точки перегиба на рис. 4а. Числа агрегации для максимума и минимума работы агрегации ${{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)$ отвечают корням уравнения (6) с учетом выражения (42). С ростом концентрации ${{c}_{1}}$ высота максимума работы агрегации ${{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)$ медленно убывает, а сам максимум сдвигается в сторону меньших чисел агрегации. При этом минимум работы агрегации ${{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)$ сдвигается в сторону больших чисел агрегации, а его глубина быстро растет. Как следствие накопления числа обратных мицелл в области минимума работы ${{W}_{{{\text{in}}}}}\left( {n,{{c}_{1}}} \right)$ (потенциальной ямы для образования обратных мицелл) на рис. 4б закономерно возникает ККМ для сухих обратных мицелл. При ${{c}_{1}} > {{\left. {{{c}_{1}}} \right|}_{{{\text{ККМ}}}}}$ степень мицеллизации на рис. 4б демонстрирует характерный быстрый рост. Результаты расчета очень чувствительны к выбору параметров ${{a}_{{0{\text{in}}}}}$ и ${{v}_{{\text{p}}}}.$ Учет конформационного вклада слабо влияет на положение точки перегиба, но значительно влияет на значение ККМ в случае обратных мицелл.
ЗАКЛЮЧЕНИЕ
В данном сообщении обоснованы новые выражения для зависимости работы агрегации прямых и обратных мицелл, определяемые формулами (33), (34) и (41), (42). Показано, что важную роль в стабилизации как прямых, так и обратных мицелл играет уравнение состояния молекулярных групп на поверхности ядра мицеллы. Учтенные вклады в работу агрегации позволяют объяснить механизм агрегации ПАВ в неполярном растворителе в отсутствие воды, убедиться в существовании ККМ и оценить средние числа агрегации сухих обратных мицелл при разных брутто-концентрациях ПАВ.
Список литературы
Blankschtein D., Thurston G.M., Benedek G.B. // J. Chem. Phys. 1986. V. 85. P. 7268.
Nagarajan R., Ruckenstein E. // Langmuir. 1991. V. 7. P. 2934.
Nagarajan R. // Structure-Performance Relationships in Surfactants. Ed. by Esumi K., Ueno M. V. 112 of Surfactant Science. Boca Raton: CRC Press, 2003. P. 1.
Nagarajan R. // Surfactant Science and Technology. Retrospects and Prospects. Ed. by Romsted L.S. Boca Raton: CRC Press, 2014. P. 4.
Danov K.D., Kralchevsky P.A., Stoyanov S.D., Cook J.L., Stott I.P., Pelan E.G. // Adv. Colloid Interface Sci. 2018. V. 256. P. 1.
Русанов А.И., Щёкин А.К. Мицеллообразование в растворах поверхностно-активных веществ. 2-е изд. СПб.: Лань, 2016.
Shchekin A.K., Kuni F.M., Grinin A.P., Rusanov A.I. // Nucleation Theory and application. Ed. by Schmelzer J.W.P. New York: Wiley, 2005. Ch. 9. P. 31.
Куни Ф.М., Русанов А.И., Щёкин А.К., Гринин А.П. // Журн. физ. химии. 2005. Т. 79. С. 967.
Shchekin A.K., Babintsev I.A., Adzhemyan L.Ts. // J. Chem. Phys. 2016. V. 145. Article 174105.
Eroshkin Yu.A., Adzhemyan L.Ts., Shchekin A.K. // Colloid J. 2020. V. 82. P. 513.
Adzhemyan L.Ts., Eroshkin Yu.A., Shchekin A.K. // Physica A. 2021. V. 572. Article 125912.
Щёкин А.К., Аджемян Л.Ц., Бабинцев И.А., Волков Н.А. // Коллоид. журн. 2018. Т. 80. С.115.
Nagarajan R., Ruckenstein E. // J. Colloid Interface Sci. 1977. V. 60. P. 221.
Nagarajan R., Ruckenstein E. // J. Colloid Interface Sci. 1979. V. 71. P. 580.
Blankschtein D., Thurston G.M., Benedek G.B. // Phys. Rev. Lett. 1985. V. 54. P. 955.
Nagarajan R., Ruckenstein E. // Equations of State for Fluids and Fluid Mixtures. Ed. by Sengers J.V., Kayser R.F., Peters C.J., White H.J. V. 5 of Experimental Thermodynamics. Amsterdam: Elsevier, 2000. P. 589.
Nagarajan R. // New Horizons: Detergents for the New Millennium Conference Invited Papers. Fort Myers: American Oil Chemists Society and Consumer Specialty Products Association, 2001.
Русанов А.И., Куни Ф.М., Гринин А.П., Щёкин А.К. // Коллоид. журн. 2002. Т. 64. С. 670.
Русанов А.И., Гринин А.П., Куни Ф.М., Щекин А.К. // Журн. общей химии. 2002. Т. 72. С. 651.
Щёкин А.К., Волков Н.А., Кольцов И.Н., Третьяков Н.Ю., Волкова С.С., Турнаева Е.А.// Коллоид. журн. 2021.Т. 83. С. 484.
Ruckenstein E., Nagarajan R. // J. Phys. Chem. 1980. V. 84. P. 1349.
Eicke H.-F., Christen H. // Helv. Chim. Acta. 1978. V. 61. P. 2258.
Fathi H., Kelly J.P., Vasquez V.R., Graeve O.A. // Langmuir. 2012. V. 28. P. 9267.
Chowdhary J., Ladanyi B.M. // J. Phys. Chem. B. 2009. V. 113. P. 15029.
Eskici G., Axelsen P.H. // J. Phys. Chem. B. 2016. V. 120. P. 11337.
Smith G.N., Brown P., Rogers S.E., Eastoe J. // Langmuir. 2013. V. 29. P. 3252.
Bradley-Shaw J.L., Camp P.J., Dowding P.J., Lewtas K. // J. Phys. Chem. B. 2015. V. 119. P. 4321.
Smith G.N., Brown P., James C., Rogers S.E., Eastoe J. // Colloids Surf. A. 2016. V. 494. P. 194.
Urano R., Pantelopulos G.A., Straub J.E. // J. Phys. Chem. B. 2019. V. 123. P. 2546.
Волков Н.А., Щёкин А.К., Посысоев М.В., Ерош-кин Ю.А., Аджемян Л.Ц. // Современная химическая физика на стыке физики, химии и биологии. Отв. ред. Березин М.П. Черноголовка: ИПХФ РАН, 2021. С. 418. ISBN 978-5-6044508-5-7.
Khoshnood A., Firoozabadi A. // Langmuir. 2015. V. 31. P. 5982.
Ландау Л.Д., Лифшиц Е.М. Статистическая физика. Часть 1. 5-е изд. М.: Физматлит, 2005.
Русанов А.И., Куни Ф.М., Щекин А.К. // Коллоид. журн. 1987. Т. 49. С. 309.
Куни Ф.М., Гринин А.П., Щекин А.К., Русанов А.И. // Вопросы физики формообразования и фазовых превращений / Под ред. Щербакова П.М. Калинин: Изд-во КГУ, 1987. С. 25.
Babintsev I.A., Adzhemyan L.Ts., Shchekin A.K. // Science SPbU – 2020. Materials of International Conference on Natural and Humanitarian Sciences on 25 December of 2020. St Petersburg: Skifia-Print, 2021. P. 439. ISBN 978-5-98620-509-0.
Flory P.J. Principles of Polymer Chemistry. Ithaca: Cornell University Press, 1962.
Semenov A.N. // Sov. Phys. JETP. 1985. V. 61. P. 733.
Helfand E., Frisch H.L., Lebowitz J.L. // J. Chem. Phys. 1961. V. 34. P. 1037.
Santos A., Haro M.L., Yuste S.B. // J. Chem. Phys. 1995. V. 103. P. 4622.
Русанов А.И. // Коллоид. журн. 2007. Т. 69. С. 149.
Mulero A., Galán C.A., Parra M.I., Cuadros F. // Theory and Simulation of Hard-sphere Fluids and Related Systems. The Lecture Notes in Physics 753. Ed. by Mulero A. Berlin: Springer, 2008. Ch. 3. P. 37.
Николаев П.Н. // Ученые записки физического факультета Московского университета. 2018. № 5. Article 1850101.
http://www.chemspider.com/Chemical-Structure. 71267.html
Hanwell M.D., Curtis D.E., Lonie D.C., Vandermeersch T., Zurek E., Hutchison G.R. // J. Cheminformatics. 2012. V. 4. Article 17.
Dill K.A., Flory P.J. // Proc. Natl. Acad. Sci. U.S.A. 1980. V. 77. P. 3115.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал



