Коллоидный журнал, 2022, T. 84, № 1, стр. 105-113
Синтез наностержней золота в бинарной смеси катионных поверхностно-активных веществ
М. Г. Спирин 1, *, С. Б. Бричкин 1, А. А. Лизунова 2, В. Ф. Разумов 1, 2, 3
1 Институт проблем химической физики РАН
142432 Московская обл., Черноголовка, просп. акад. Семенова, 1, Россия
2 Московский физико-технический институт (Национальный исследовательский университет)
141701 Московская обл., Долгопрудный,
Институтский пер., 9, Россия
3 Московский государственный университет им. М.В. Ломоносова, факультет фундаментальной
физико-химической инженерии
119991 Москва, Ленинские горы, 1, стр. 51, Россия
* E-mail: max2004@icp.ac.ru
Поступила в редакцию 20.09.2021
После доработки 14.10.2021
Принята к публикации 15.10.2021
- EDN: ITVYCB
- DOI: 10.31857/S002329122201013X
Аннотация
Обнаружено, что в бинарной смеси бромида цетилтриметиламмония и бензилзамещенного ПАВ можно синтезировать наностержни золота с максимумом продольного плазмонного резонанса на длине волны от 750 до 1150 нм. Показано, что длина образующихся частиц зависят от мольного соотношения ПАВ и длины углеводородной цепи бензилзамещенного ПАВ, влияющей на свойства бислойной мицеллярной структуры, в которой формируются наностержни.
ВВЕДЕНИЕ
Характерной особенностью наностержней золота (Au-НС) является наличие в их спектрах поглощения двух полос плазмонного резонанса: поперечного с максимумом при 500–540 нм и продольного, положение которого может изменяться в диапазоне от видимой до ближней ИК-области при варьировании отношения длины к ширине Au-НС (аксиального отношения) [1, 2]. Такие частицы могут найти широкое применение в качестве оптических наноантенн для фотодетекторов нового поколения [3], при создании сенсорных элементов [4] и в различных биомедицинских приложениях [5, 6].
Для получения Au-НС в однородной среде необходимо создать специальные условия для их анизотропного роста. Это можно реализовать, например, за счет применения жестких (пористый оксид алюминия [7]) или мягких (несферические мицеллы [8]) темплатов. Однако наиболее перспективным оказался так называемый зародышевый метод, предложенный еще в 2001 г. [9]. Он состоит из двух стадий: на первой формируются сферические зародыши, а на второй на этих зародышах выращиваются анизотропные частицы. Данный метод позволяет легко управлять ростом наностержней и, соответственно, их оптическими свойствами.
Для синтеза Au-НС необходима среда, содержащая протяженные мицеллярные структуры из поверхностно-активных веществ (ПАВ). Молекулы ПАВ формируют бислои, которые преимущественно сорбируются на боковых сторонах наностержней, а рост наночастиц (НЧ) происходит за счет диффузии вещества к относительно свободным от ПАВ торцам [10]. При этом на длину и выход Au-НС влияют различные факторы: природа молекул ПАВ и их концентрация [11], присутствие ионов серебра [12, 13], величина pH [14] и т.д. Так, длина Au-НС увеличивается с ростом длины углеводородного “хвоста” молекул ПАВ (числа C-атомов Cn). В связи с этим наибольшее распространение получил цетилтриметиламмония бромид (CTAB) – катионное ПАВ с длинным углеводородным хвостом (n = 16) и относительно высокой растворимостью в воде. С его помощью можно синтезировать достаточно однородные Au-НС с максимумом продольного плазмонного резонанса, согласно данным [15], вплоть до 850 нм (в присутствии L-аскорбиновой кислоты).
Вместе с тем, у данного ПАВ есть, по крайней мере, два недостатка. Во-первых, Au-НС, полученные в присутствии CTAB, имеют невысокую стабильность при хранении, и с течением времени пик продольного резонанса довольно заметно сдвигается в коротковолновую сторону (на 100 нм и больше). Это обусловлено изменением формы Au-НС за счет их перекристаллизации [16]. Во-вторых, на формирование и рост Au-НС сильно влияют примеси, содержащиеся в ПАВ. Использование CTAB разной степени чистоты и от разных производителей часто приводит к тому, что приготовленные по одному и тому же протоколу частицы золота в одном случае представляют собой преимущественно наностержни, а в другом образуются практически только сферические НЧ [17].
Наиболее эффективным методом, существенно повышающим стабильность Au-НС, является их синтез в присутствии двух ПАВ. Данный метод был впервые продемонстрирован в работе [15], в которой было предложено использовать в ростовом растворе смесь CTAB и бензилдиметилгексадециламмония хлорида (BDAC). Оказалось, что такая смесь не только замедляет перекристаллизацию наностержней, но и способствует увеличению их длины [18]. При этом пик продольного плазмонного резонанса удалось смещать в длинноволновую область до 1300 нм.
В последующих работах BDAC пытались заменить другими веществами, например, неионогенным ПАВ Pluronic F-127 [19], ароматической добавкой типа 5-бромсалициловой кислоты [20], олеатом натрия [21–23] или бензилдиметилтетрадециламмония хлоридом (BDTAC) [24]. Управлять ростом Au-НС в данных смесях можно путем изменения как мольного соотношения CTAB/ПАВ, так и времени реакции. Кроме того, 5-бромсалициловая кислота и олеат натрия выполняют функцию не только стабилизирующего агента, но и восстановителя, что способствует повышению однородности стержней. При этом пик продольного резонанса Au-НС в присутствии олеата натрия сдвигается до 1150 нм, 5-бромсалициловой кислоты – до 1246 нм, Pluronic F-127 – до 1450 нм. При использовании BDTAC – в определенных условиях и при длительном выдерживании системы (до 3 месяцев) – полосу продольного резонанса удается сдвинуть до 1600 нм. Кроме того, оказалось, что на положение данной полосы влияет также природа восстанавливающего агента. Так, замена аскорбиновой кислоты на гидрохинон позволяет получать Au-НС, стабилизированные только одним CTAB, с максимумом продольного резонанса на длине волны до 1230 нм [25].
Au-НС с плазмонным резонансом в ближнем ИК-диапазоне привлекают особое внимание исследователей, так как этот диапазон очень перспективен для различных практических применений. Для этого необходимы однородные частицы с компактной оболочкой из молекул ПАВ. Бензилзамещенные ПАВ, такие как BDAC и BDTAC, по крайней мере, на стадии синтеза вполне удовлетворяют такому условию. BDAC широко используется для направленного роста НЧ Au, причем не только стержней, но и других структур – нанотреугольников [26], нанозвезд [27] или даже “нанонаушников” [28]. Данные вещества достаточно безопасны для человека, например, BDTAC используется в фармацевтике и медицине [29]. Его молекула имеет более короткий углеводородный хвост (n = 14) и он лучше растворяется в воде по сравнению с BDAC (n = 16). Как было показано в [24], использование BDTAC вместо BDAC приводит к расширению концентрационного диапазона соотношений CTAB/ПАВ, благоприятствующего формированию Au-НС. Однако такой процесс протекает в течение длительного времени (недели и даже месяцы).
В данной работе предложена методика синтеза Au-НС в присутствии, помимо CTAB, бензилзамещенных ПАВ, позволяющая существенно ускорить рост наностержней и практически завершить их формирование в пределах одних суток. Это было достигнуто за счет использования CTAB со степенью чистоты ≥98% вместо 99% и оптимизации мольного соотношения CTAB/ПАВ. Цель работы – исследовать процессы образования Au-НС с продольным плазмонным резонансом в ближнем ИК-диапазоне в присутствии смесей CTAB/BDAC и CTAB/BDTAC и определить условия, способствующие формированию Au-НС, продольный резонанс которых максимально сдвинут в длинноволновую область.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В работе использовались следующие реактивы: тетрахлороаурат(III) водорода (≥49.0% Au, Sigma-Aldrich), нитрат серебра (“х.ч.”, ГОСТ 1277-75), борогидрид натрия (98%, Sigma-Aldrich), аскорбиновая кислота (≥99.0%, Sigma), CTAB (≥98%, Sigma, каталожный номер H5882), BDTAC (98%, Aldrich), BDAC (≥97%, Sigma), дистиллированная вода. Все используемые реагенты дополнительной очистке не подвергались.
Синтез Au-НС осуществляли при температуре 28°C на основе методики [24]. Сначала готовили зародышевый раствор путем смешения водных растворов CTAB (5 мл, 0.2 М), HAuCl4 (5 мл, 5 × 10–4 М) и NaBH4 (0.6 мл, 0.01 М). Данную смесь затем интенсивно перемешивали в течение 2 мин до появления светло-коричневой окраски, свидетельствующей об образовании частиц золота, имеющим по данным [30] сферическую форму и средний размер около 2 нм. Ростовой раствор получали путем смешения 5 мл водных растворов CTAB/BDAC (или CTAB/BDTAC) в мольном соотношении от 0.8 до 3, AgNO3 (0.2 мл, 4 × 10–3 М), HAuCl4 (5 мл, 1 × 10–3 М) и аскорбиновой кислоты (0.07 мл, 0.0778 М). Далее к ростовому раствору добавляли 0.012 мл свежеприготовленного зародышевого раствора (через 60 мин выдерживания) и полученную смесь перемешивали в течение 16 ч. Концентрации ПАВ, используемые в работе, во много раз превышали критическую концентрацию мицеллообразования (ККМ), в результате чего в водном растворе происходило формирование сложных молекулярных структур из ПАВ, типа бислоев. Для CTAB величина ККМ составляла 0.83 мМ [31], для BDTAC – 1.9 мМ, а для BDAC – 0.52 мМ [32].
Спектры поглощения растворов, содержащих НЧ Au, измеряли на спектрофотометре Shimadzu UV 3101PC. Микрофотографии этих частиц были получены на просвечивающем электронном микроскопе JEOL JEM-2100. Для этого образцы НЧ Au были предварительно отмыты от избытка ПАВ, причем в случае смеси CTAB/BDTAC двукратным, а смеси CTAB/BDAC трехкратным осаждением на центрифуге ОПН-16 (11 000 мин–1, 10 мин), с последующим диспергированием осадка в воде. Затем каплю полученной дисперсии НЧ Au наносили на медную сеточку, покрытую тонким слоем углерода, и высушивали при нормальных условиях.
РЕЗУЛЬТАТЫ
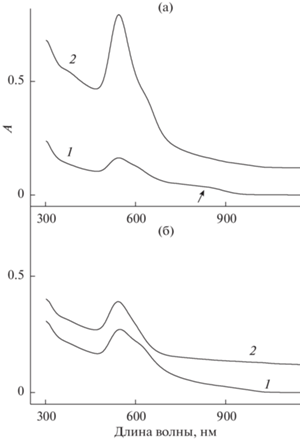
На рис. 1 представлены спектры поглощения Au-НС, измеренные спустя 16 ч после смешения зародышевого и ростового растворов, при [CTAB]/[ПАВ] = 1 : 1.2 (а) и 1 : 2.7 (б) для BDTAC (1) и BDAC (2). Из рисунка следует, что на всех спектрах поглощения наблюдается коротковолновая полоса в области 515–550 нм (в случае кривой 2 на рис. 1а эта полоса расщепляется на две) и длинноволновая в диапазоне 870–1150 нм. При соотношении [CTAB]/[ПАВ] = 1 : 1.2 длинноволновая полоса имеет максимум при 870 нм в присутствии BDTAC и при 980 нм в присутствии BDAC, а при [CTAB]/[ПАВ] = 1 : 2.7 – вблизи 1150 и 1080 нм соответственно. Рисунок также свидетельствует о том, что в случае использования BDAC значения интенсивности длинноволновой полосы больше, чем в случае BDTAC, как и отношения амплитуд длинноволновой и коротковолновой полос (3.74 и 2.34 по сравнению с 3 и 2.1 соответственно).
Рис. 1.
Спектры поглощения Au-НС, измеренные спустя 16 ч после их синтеза при соотношении [CTAB]/[ПАВ] = 1 : 1.2 (а) и 1 : 2.7 (б): 1 – ПАВ = = BDTAC, 2 – ПАВ = BDAC.
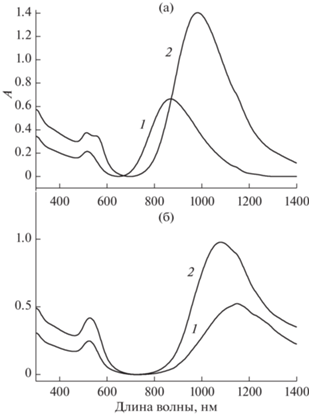
На рис. 2 и 3 приведены микрофотографии и гистограммы распределения по длине исследуемых образцов Au-НС. Как следует из этих микрофотографий, частицы, синтезированные при соотношении [CTAB]/[ПАВ] = 1 : 1.2, представляют собой достаточно однородные наностержни шириной 8–10 нм, при этом доля частиц с формой, близкой к сферической, и коротких (до 40 нм) стержней составляет не более 12–15% от общего их количества (рис. 2а, 2в). Это подтверждается соответствующими гистограммами распределения Au-НС по размеру, из которых следует, что их длина находится в диапазоне 45–60 нм при использовании BDTAC и 50–65 нм – BDAC (рис. 2б, 2г). Доля Au-НС с длиной более 65 нм при использовании BDTAC и более 75 нм в случае BDHAC составляет около 5%.
Рис. 2.
Микрофотографии Au-НС, полученных при соотношении [CTAB]/[ПАВ] = 1 : 1.2 (а, в), и гистограммы их распределения по длине (б, г); (а, б) ПАВ = BDTAC, (в, г) ПАВ = BDAC.
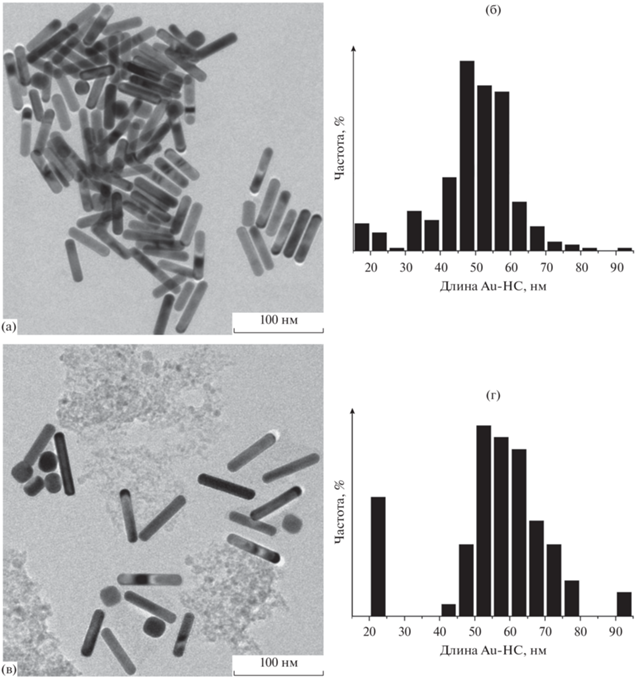
Рис. 3.
Микрофотографии Au-НС, полученных при соотношении [CTAB]/[ПАВ] = 1 : 2.7 (а, в), и гистограммы их распределения по длине (б, г); (а, б) ПАВ = BDTAC, (в, г) ПАВ = BDAC.
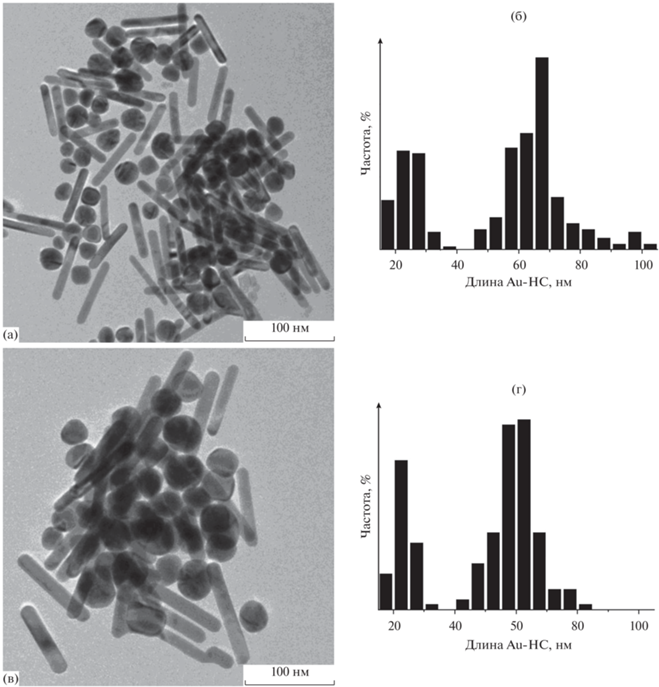
При соотношении [CTAB]/[ПАВ] = 1 : 2.7 доля частиц с формой, близкой к сферической, существенно возрастает – до 30% (рис. 3а, 3в), а гистограммы распределения Au-НС по длине явно приобретают бимодальный характер (рис. 3б, 3г). Длина основного количества Au-НС увеличивается до 60–70 нм в случае BDTAC и остается в диапазоне 55–65 нм для BDAC, а их ширина не изменяется (8–10 нм). Доля стержней с длиной более 75 нм при использовании BDTAC составляет 10%, а в случае BDHAC – около 3%.
Здесь необходимо отметить, что спектры поглощения, приведенные на рис. 1, записаны до отмывки Au-НС от избытка ПАВ, а ПЭМ-фотографии уже после его удаления. Эта процедура не влияет на форму и положение полос плазмонного резонанса, однако при этом изменяется соотношение их амплитуд. Так, при [CTAB]/[ПАВ] = 1 : 1.2 в результате отмывки Au-НС в присутствии BDTAC отношение амплитуд длинноволнового и коротковолнового пиков увеличивалось от 3 до 3.3, а в присутствии BDAC, наоборот, уменьшалось от 3.74 до 3.5. При [CTAB]/[ПАВ] = 1 : 2.7 наблюдалось уменьшение отношения амплитуд от 2.2 до 1.75 для BDTAC и от 2.3 до 1.8 для BDAC. Несмотря на то, что в случае использования BDAC отмывку проводили 3 раза, а в случае BDTAC – только 2 раза, при [CTAB]/[BDAC] = 1 : 1.2 на микрофотографии видны “облака” ПАВ (рис. 2в), отсутствующие на других снимках, что является следствием меньшей растворимости BDAC в воде.
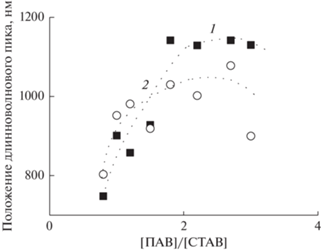
Для изучения влияние соотношения [CTAB]/[ПАВ] на процессы образования Au-НС был синтезирован ряд образцов при его варьировании от 0.8 : 1 до 1 : 3. На рис. 4 представлены зависимости положения максимума длинноволнового резонансного пика от [CTAB]/[ПАВ] для BDTAC (кривая 1) и BDAC (кривая 2). Видно, что положение максимума изменяется от 750 до 1150 нм, причем в диапазоне значений [CTAB]/[ПАВ] от 0.8 до 1.8 в присутствии BDAC он смещен в длинноволновую область спектра в среднем на 50–100 нм относительно положения максимума при использовании BDTAC. В диапазоне [CTAB]/[ПАВ] = 1.8–2.7 ситуация становится прямо противоположной, и при соотношении 1 : 3 максимум этого пика в присутствии BDTAC оказывается сдвинутым в длинноволновую область почти на 250 нм относительно его положения в присутствии BDAC.
Рис. 4.
Зависимости положения длинноволнового плазмонного пика от соотношения [CTAB]/[ПАВ]: 1 – ПАВ = BDTAC, 2 – ПАВ = BDAC.
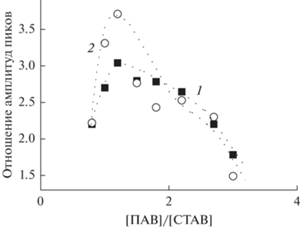
На рис. 5 приведена зависимость отношения амплитуд длинноволнового и коротковолнового пиков поглощения от [CTAB]/[ПАВ] для BDTAC (кривая 1) и BDAC (кривая 2). Данные кривые в исследуемом диапазоне ведут себя примерно одинаково: сначала это отношение увеличивается, достигая максимального значения при [CTAB]/[ПАВ] = 1 : 1.2, затем начинает уменьшаться. Наилучший результат (т.е. наибольшее значение, равное 3.74) наблюдается при использовании BDAC, тогда как в случае BDTAC это отношение равно 3. В то же время при [CTAB]/[ПАВ] = = 1 : 3 оно уменьшается до 1.5 для BDAC и до 1.8 для BDTAC.
Рис. 5.
Зависимости отношения амплитуд длинноволнового и коротковолнового пиков плазмонного резонанса от соотношения [CTAB]/[ПАВ]: 1 – ПАВ = = BDTAC, 2 – ПАВ = BDAC.
В табл. 1 представлены данные по изменению полуширины длинноволновой полосы плазмонного резонанса на полувысоте (ПШПВ) в зависимости от соотношений [CTAB]/[BDTAC] и [CTAB]/[BDAC]. В случае BDAC с увеличением его концентрации наблюдается монотонное уширение полосы – значение ПШПВ возрастает от 0.304 до 0.38 эВ. В присутствии BDTAC эта зависимость имеет более сложный характер: ПШПВ сначала увеличивается, достигая максимального значения (0.385) при [CTAB]/[BDTAC] = 1 : 1.5, а затем уменьшается до 0.31 при соотношении этих двух ПАВ, равном 1 : 3.
Таблица 1.
Влияние молярного соотношения [CTAB]/[ПАВ] на ПШПВ длинноволновой полосы плазмонного резонанса через 16 ч после смешения зародышевого и ростового растворов
| [CTAB]/[ПАВ] | ПШПВ, эВ | |
|---|---|---|
| ПАВ = BDTAC | ПАВ = BDAC | |
| 0.8 : 1 | 0.3 | 0.304 |
| 1 : 1 | 0.35 | 0.315 |
| 1 : 1.2 | 0.377 | 0.336 |
| 1 : 1.5 | 0.385 | 0.364 |
| 1 : 1.8 | 0.32 | 0.345 |
| 1 : 2.2 | 0.329 | 0.356 |
| 1 : 2.7 | 0.323 | 0.347 |
| 1 : 3 | 0.31 | 0.38 |
Нами также были синтезированы НЧ Au при значениях соотношения [CTAB]/[ПАВ] = 1 : 1 и 1 : 2.7 в отсутствие ионов серебра (рис. 6). Как следует из этого рисунка, у исследуемых образцов наблюдается ярко выраженная полоса поглощения при 545 нм с плечом в области 620–650 нм, причем при соотношении 1 : 2.7 в случае использования BDAC (рис. 6а, кривая 2) ее оптическая плотность в 4 раза выше, чем при 1 : 1 (рис. 6а, кривая 1). На последней кривой также присутствует слабовыраженная полоса 850 нм, которая практически не заметна на других кривых. При применении BDTAC значения амплитуды полосы 545 нм при соотношениях ПАВ 1 : 1 и 1 : 2.7 совпадают, а различие в спектрах заключается только в отсутствие плеча в области 620–650 нм.
ОБСУЖДЕНИЕ
Наблюдаемые на рис. 1 полосы поглощения в диапазонах 515–550 нм и 870–1150 нм принадлежат поперечному и продольному плазмонным резонансам Au-НС соответственно [33–35]. При этом полоса продольного резонанса всегда значительно интенсивнее полосы поперечного. Из рисунка следует, что с увеличением концентрации BDAC или BDTAC пик продольного резонанса смещается в длинноволновую сторону (и увеличивается средняя длина Au-НС). В присутствии BDAC оптическая плотность резонансных полос больше, чем в случае использования BDTAC, что указывает на более высокий конечный выход Au-НС. При [CTAB]/[ПАВ] = 1 : 1.2 в случае BDAC стержни вырастают длиннее, чем в присутствии BDTAC, однако при соотношении 1 : 2.7, наоборот, более длинные частицы формируются в присутствии BDTAC. Наиболее наглядно это продемонстрировано на рис. 4, из которого следуют, что в диапазоне соотношения двух ПАВ 0.8–1.8 аксиальное отношение Au-НС выше при использовании BDAC, а в диапазоне 1.8–3 – BDTAC.
Наблюдающаяся в ряде случаев большая амплитуда коротковолновой полосы связана с присутствием в растворе наряду с наностержнями большого количества частиц сферической или близкой к сферической формы, поглощение которых может накладываться на полосу поперечного плазмонного резонанса Au-НС, усиливая ее интенсивность. Для качественной оценки их количества может быть использовано отношение амплитуд длинноволнового и коротковолнового пиков поглощения. Очевидно, что чем выше это отношение, тем больше доля Au-НС в образце. Рисунок 5 показывает, что зависимость данной величины от [CTAB]/[ПАВ] носит экстремальный характер, то есть по мере увеличения концентрации BDAC или BDTAC доля Au-НС увеличивается, достигая максимального значения при соотношении двух ПАВ 1 : 1.2, после чего начинает уменьшаться. При этом в максимуме доля Au-НС при использовании BDAC выше, чем BDTAC.
Одновременно с этим изменяется ПШПВ длинноволновой резонансной полосы. В присутствии BDAC она растет во всем диапазоне значений соотношения [CTAB]/[ПАВ], от 0.8 : 1 до 1 : 3, что свидетельствует о постепенном уширении распределения НЧ по размеру. В случае использования BDTAC она проходит через максимум при соотношении 1 : 1.5, то есть стадия уширения этого распределения сменяется стадией его “фокусировки”.
Исходя из этих фактов, можно предположить, что в данном случае образование Au-НС происходит следующим образом. Молекулы ПАВ формируют сложные структуры типа бислоев, размеры которых определяются концентрацией ПАВ и ионной силой раствора. После смешения зародышевого и ростового растворов образуются зародыши будущих Au-НС, изначально растущие с одинаковой скоростью во всех направлениях. По мере достижения ими некоторого критического размера, когда грани {100} становятся достаточно большими для адсорбции молекул CTAB, эти грани блокируются, а дальнейший рост, осуществляемый за счет диффузии золотосодержащих ионов к торцевым граням {111}, становится возможным преимущественно вдоль направления {110} [36]. Конечная форма НЧ определяется относительной скоростью роста различных граней, а их размер зависит от количества золотосодержащих ионов в растворе, поэтому формирование Au-НС продолжается до истощения запаса этих ионов.
Очевидно, что в бислои, адсорбирующиеся на гранях Au-НС, встраиваются молекулы не только CTAB, но и BDTAC (BDAC). Бинарная смесь ПАВ способствует формированию более гибкого мицеллярного шаблона, что позволяет выращивать Au-НС большей длины по сравнению с Au-НС, растущими в присутствии структур, состоящих только из CTAB. Однако способность бензилзамещенных ПАВ адсорбироваться на боковых гранях {100} существенно ниже, чем у CTAB [15], поэтому BDAC и BDTAC слабо препятствуют росту частиц в данном направлении. При этом “лишние” молекулы BDAC или BDTAC вытесняются с боковых граней в раствор либо концентрируются на торцах наностержней, сродство к которым у молекул CTAB выражено слабее [24].
Молекулы BDTAC (с n = 14) обладают большей подвижностью по сравнению с BDAC (с n = 16), которые имеют углеводородный хвост такой же длины, что и CTAB. Вследствие этого в бинарной смеси BDAC–CTAB молекулы ПАВ упаковываются в более плотный бислойный мицеллярный темплат, чем в смеси BDTAC–CTAB. Такая смесь очень эффективна для синтеза однородных Au-НС при соотношении ПАВ, близком к эквимольному (0.8–1.2), однако по мере увеличения концентрации BDAC избыточные молекулы последнего локализуются не только на торцах наностержня, но и встраиваются в мицеллярную структуру на его боковых гранях, способствуя тем самым их росту. Это приводит к замедлению удлинения стержней, уширению их распределения по размеру и увеличению доли сферических и сфероидальных частиц. Наиболее наглядно это проявляется при соотношении [CTAB]/[BDAC] = 1 : 3, когда наблюдается резкий гипсохромный сдвиг пика продольного плазмонного резонанса (рис. 4, кривая 2), уменьшение отношения амплитуд резонансных пиков (рис. 5, кривая 2) и уширение длинноволновой полосы (табл. 1).
В бинарной смеси BDTAC–CTAB молекулы ПАВ формируют менее плотный мицеллярный темплат, поэтому молекулы BDTAC легче покидают эту бислойную структуру и встраиваются в нее. Такая структура не столь эффективна при соотношении ПАВ 0.8–1.2, как смесь BDAC–CTAB, однако она позволяет выращивать стержни с большим аксиальным отношением в диапазоне значений [CTAB]/[BDAC] = 1.8–3. По всей вероятности, последний факт связан с тем, что из-за своей относительно высокой подвижности BDTAC присутствует в бислойной структуре на боковых гранях Au-НС в меньшем количестве по сравнению с BDAC. Это способствует более надежному блокированию боковых граней молекулами CTAB, а диффузионный рост происходит, в основном, на торцах Au-НС до истощения запаса золотосодержащих ионов. С одной стороны, с увеличением относительного количества BDTAC в диапазоне 1.8–3 наблюдается устойчивое образование Au-НС с максимумом продольного резонанса вблизи 1150 нм (рис. 4, кривая 1) и сужение ПШПВ (табл. 1), а с другой стороны, уменьшается отношение амплитуд длинноволнового и коротковолнового пиков. Это значит, что независимо от бислойных структур, в которых формируются Au-НС, образуются и другие структуры, состоящие, главным образом, из молекул бензилзамещенного ПАВ. В этих структурах локализуются сферические или сфероидальные НЧ, доля которых растет с увеличением концентрации BDTAC. Аналогичные процессы протекают и при участии BDAC, только в этом случае все развивается быстрее, и уже при соотношении [CTAB]/[BDAC] = 1 : 3 молекулярные структуры, образуемые этим ПАВ, становятся доминирующими. Наличие двух таких разных молекулярных структур объясняет бимодальное распределение НЧ, представленное на гистограммах (рис. 3), и практически полное отсутствие частиц промежуточного размера (коротких стержней). В диапазоне [CTAB]/[ПАВ] = 0.8–1.2 молекулярные структуры из BDTAC или BDAC, в которых локализуются сферические НЧ золота, также могут формироваться, но доля их невелика.
Эти два типа молекулярных структур можно разделить с помощью простого центрифугирования. Наиболее легко это удается сделать в присутствии BDTAC при соотношении ПАВ 1 : 1.2 благодаря высокой подвижности этих молекул и небольшой доли сформированных из них структур. Для других случаев необходимо подбирать специальные режимы осаждения.
Как известно, важным условием, способствующим образованию Au-НС с высоким аксиальным отношением и существенно увеличивающим их выход, является присутствие ионов серебра в ростовом растворе [37, 38]. При этом механизм роста наностержней в таких условиях до сих пор остается неясным. Согласно [15], Ag+-ионы формируют монослой на торцах Au-НС и выступают в качестве комплексообразующего агента, “связывающего” две молекулы CTAB, образуя пары Ag–Br. При этом уменьшается плотность заряда на ионах бромида и отталкивание между соседними головными группами молекул ПАВ на поверхности НЧ, что приводит к удлинению Au-НС. Вследствие того, что хлорид-ионы имеют меньшие размер и поляризуемость по сравнению с бромид-ионами, связь в паре Ag–Cl будет более слабой и рост Au-НС в присутствии BDAC и BDTAC будет происходить быстрее. Другие авторы связывают инициализацию анизотропного роста Au-НС с тем, что Ag+-ионы, имеющие более низкий стандартный электродный потенциал по сравнению c Au+-ионами, адсорбируются на гранях {100} или {110}, ограничивая тем самым их рост [39].
В отсутствие ионов серебра Au-НС также могут образовываться, но, как правило, с небольшим выходом – до 20% [12]. Анализ спектров НЧ Au, приведенных на рис. 6, показывает, что в нашем случае образуются преимущественно частицы сферической и сфероидальной формы. Небольшое количество стержней, возможно, наблюдается только в присутствии BDAC при [CTAB]/[ПАВ] = 1 : 1 (рис. 6а, кривая 1). Данный факт можно считать косвенным подтверждением плотной упаковки молекул ПАВ в мицеллярном темплате при таких условиях, способным направить рост частиц. В остальных случаях молекулы ПАВ в темплате упакованы менее плотно, наиболее наглядно это проявляется при [CTAB]/[BDTAC] = 1 : 1 (рис. 6б, кривая 2), когда в спектре присутствует только полоса 545 нм и отсутствует плечо в области 620–650 нм. Это свидетельствует об образовании практически только сферических частиц.
ЗАКЛЮЧЕНИЕ
В данной работе оптимизированы условия синтеза Au-НС с использованием бинарных смесей катионных ПАВ: CTAB/BDAC и CTAB/BDTAC, позволяющие в пределах одних суток получить Au-НС с максимумом полосы продольного плазмонного резонанса в диапазоне от 750 до 1150 нм за счет изменения мольного соотношения CTAB/ПАВ от 0.8 : 1 до 1 : 3. Показано, что в смеси CTAB/BDAC выход Au-НС выше, чем в смеси CTAB/BDTAC, однако при участии BDTAC можно синтезировать Au-НС большей длины. Обнаружено, что при этом также образуются сферические (сфероидальные) НЧ Au, доля которых увеличивается с уменьшением мольного соотношения CTAB/ПАВ. При этом сферические НЧ и наностержни золота локализованы в разных молекулярных структурах, образуемых ПАВ.
Список литературы
Foss C.A., Hornyak, G.L. Stockert J.A., Martin C.R. // J. Phys. Chem. 1994. V. 98. P. 2963.
Yu Y.-Y., Chang S.-S., Lee C.-L., Wang C.R.C. // J. Phys. Chem. B. V. 101. 1997. P. 6661.
Berkovitch N., Ginzburg P., Orenstein M. // J. Phys.: Condens. Matter. 2012. V. 24. 073202.
Liyanage T., Qamar A.Z., Slaughter G. // IEEE Sens. J. 2021. V. 21. P. 12407.
Zhou J., Cao Z., Panwar N., Hu R., Wang X., Qu J., Tjin S.C., Xu G., Yong K.-T. // Coord. Chem. Rev. 2017. V. 352. P. 15.
Sagar V., Nair M. // Expert Opin. Drug Deliv. 2018. V. 15. P. 137.
Pan S.L., Chen M., Li H.L. // Colloids Surf. A. 2001. V. 180. P. 55.
Спирин М.Г., Бричкин С.Б., Разумов В.Ф. // Химия высоких энергий. 2010. Т. 44. С. 54.
Jana N.R., Gearheart L., Murphy C.J. // J. Phys. Chem. B. 2001. V. 105. P. 4065.
Gao J., Bender C.M., Murphy C.J. // Langmuir. 2003. V. 19. P. 9065.
Алексеева А.В., Богатырев В.А., Хлебцов Б.Н., Мельников А.Г., Дыкман Л.А., Хлебцов Н.Г. // Коллоид. журн. 2006. Т. 68. С. 725.
Jana N.R., Gearheart L., Murphy C.J. // Adv. Mater. 2001. V. 13. P. 1389.
Angelats-Silva L.M., Asmat-Campos D., León-León H., Wilkinson K.A., Sánchez-Vaca D.A., López-Milla A. // MRS Adv. 2016. V. 1. P. 2186.
Altansukh B., Yao J.-X., Wang D. // J. Nanosci. Nanotechnol. 2008. V. 8. P. 1.
Nikoobakht B., El-Sayed M.A. // Chem. Mater. 2003. V. 15. P. 1957.
Iqbal M., Tae G. // J. Nanosci. Nanotechnol. 2006. V. 6. P. 3355.
Smith D.K., Korgel B.A. // Langmuir. 2008. V. 24. P. 644.
Park K., Vaia R.A. // Adv. Mater. 2008. V.20. P. 3882.
Iqbal M., Chung Y.-I., Tae G. // J. Mater. Chem. 2007. V. 17. № 4. P. 335.
Ye X., Jin L., Caglayan H., Chen J., Xing G., Zheng C., Doan-Nguyen V., Kang Y., Engheta N., Kagan C.R., Murray C.B. // ACS Nano. 2012. V. 6. P. 2804.
Khlebtsov B.N., Khanadeev V.A., Ye J., Sukhorukov G.B., Khlebtsov N.G. // Langmuir. 2014. V. 30. P. 1696.
Ханадеев В.А., Хлебцов Н.Г., Буров А.М., Хлебцов Б.Н. // Коллоид. журн. 2015. Т. 77. С. 659.
Ye X., Zheng C., Chen J., Gao Y., Murray C.B. // Nano Lett. 2013. V. 13. P. 765.
Спирин М.Г., Бричкин С.Б., Юшков Е.С., Разумов В.Ф. // Химия высоких энергий. 2020. Т. 54. С. 339.
Vigderman L., Zubarev E.R. // Chem. Mater. 2013. V. 25. P. 1450.
Kuttner C., Mayer M., Dulle M., Moscoso A., López-Romero J.M., Förster S., Fery A., Pérez-Juste J., Contreras-Cáceres R. // ACS Appl. Mater. Interfaces. 2018. V. 10. P. 11152.
Ndokoye P., Li X., Zhao Q., Li T., Tade M.O., Liu S. // J. Colloid Interface Sci. 2016. V. 462. P. 341.
Roy D., Xu Y., Rajendra R., Wu L., Bai P., Ballav N. // J. Phys. Chem. Lett. 2020. V. 11. P. 3211.
Fan T., Wall G. // J. Pharm. Sci. 1993. V. 82. P. 1172.
Ozdil Z.C.C., Spalla O., Menguy N., Testard F. // J. Phys. Chem. C. 2019. V. 123. P. 25320.
Великов А.А. // Журн. физ. химии. 2017. Т. 91. С. 1094.
Farías T., de Ménorval L.C., Zajac J., Rivera A. // Colloids Surf. A. 2009. V. 345. P. 51.
Wang D.-S., Kerker M. // Phys. Rev. B. 1981. V. 24. P. 1777.
Chang S.-S., Shih C.-W., Chen C.-D., Lai W.-C., Wang C.R.C. // Langmuir. 1999. V. 15. P. 701.
Van der Zande B.M.I., Böhmer M.R., Fokkink L.G.J., Schönenberger C. // J. Phys. Chem. B 1997. V. 101. P. 852.
Johnson C.J., Dujardin E., Davis S.A., Murphy C.J., Mann S. // J. Mater. Chem. 2002. V. 12. P. 1765.
Liu M., Guyot-Sionnest P. // J. Phys. Chem. B. 2005. V. 109. P. 22192.
Lohse S.E., Murphy C.J. // Chem. Mater. 2013. V. 25. P. 1250.
Mehere A., Chaure N.B. // Appl. Phys. A. 2020. V. 126. P. 662.
Дополнительные материалы отсутствуют.
Инструменты
Коллоидный журнал