Координационная химия, 2019, T. 45, № 5, стр. 311-320
Координационные соединения иттрия с нитрило-трис-метиленфосфоновой кислотой
Н. В. Сомов 1, *, Ф. Ф. Чаусов 2, 3, Н. В. Ломова 2, Р. М. Закирова 3, В. Г. Петров 2, Д. К. Жиров 2, М. А. Шумилова 2
1 Национальный исследовательский университет им. Н.И. Лобачевского
Нижний Новгород, Россия
2 Удмуртский федеральный исследовательский центр УрО РАН
Ижевск, Россия
3 Удмуртский государственный университет
Ижевск, Россия
* E-mail: somov@phys.unn.ru
Поступила в редакцию 08.06.2018
После доработки 16.08.2018
Принята к публикации 24.08.2018
Аннотация
Синтезированы и исследованы нитрило-трис-метиленфосфонатоиттрий [YH3{N(CH2PO3)3}] · 2H2O (I) и пентадекагидрат моногидро-бис-нитрило-трис-метиленфосфонатоиттриата октакалия K8[YH{N(CH2PO3)3}2] · 5H2O (II). Методом РСА установлена структура II (CIF file CCDC № 1847628). Кристаллы II триклинные, пр. гр. P$\bar {1}$, Z = 2, a = 11.0264(8), b = 11.3857(8), c = 16.6938(6) Å, α = 86.455(4)°, β = 85.269(4)°, γ = 85.319(6)°. Молекулы лиганда кристаллографически и функционально неэквивалентны. Одна, полностью депротонированная, хелатирует атом Y одним N- и тремя O-донорными центрами; другая – хелатирует атом Y двумя атомами O.
Иттрий ([Kr]5s24d1) часто рассматривается как химический аналог лантанидов, особенно тяжелых представителей этой группы [1–3].
В онкологии координационные соединения 90Y, как β–-излучателя, свободного от сопутствующей γ-радиации, используются для лучевой терапии метастазов в костных тканях [4, 5]. При этом избирательное связывание комплексов Y в организме обеспечивает адресную доставку лекарственного средства и снижает лучевую нагрузку на здоровые ткани.
В металлургии Y в концентрациях 0.5–1.5% существенно повышает жаростойкость и снижает скорость газовой и плазменной коррозии хромистых сталей [6, 7] и других тугоплавких сплавов [8, 9]. Это объясняется поверхностной сегрегацией Y [10, 11] и образованием слоя, состоящего из очень устойчивого Y2O3 ($\Delta {\rm H}_{{f298}}^{0}$ = –1903 кДж/моль [12]), смешанных оксидов и прочно сцепленного с поверхностью металла. Высокая стоимость и дефицит Y обусловливает интерес к разработке технологий поверхностного легирования стальных изделий: электровзрывного напыления [13, 14], лазерной обработки [15], ионной имплантации [16]. Все эти способы не свободны от недостатков, к которым относятся неравномерность покрытия, образование трещин, нарушение структуры поверхностного слоя металла. Предложен способ модификации поверхности стали термической конверсией адсорбированного слоя Y-содержащего прекурсора [17]. Можно ожидать, что наиболее перспективными прекурсорами для получения равномерного адсорбционного Y-содержащего слоя являются координационные соединения Y с промискуитетными лигандами, способными образовывать донорно-акцепторные связи со многими элементами поверхностного слоя сплава. В связи с этим актуально исследование координационной химии Y.
Имея сходство как с типичными d-элементами 4 и 5 периодов, так и с лантанидами, Y обнаруживает богатую координационную химию и широкий диапазон координационных чисел (КЧ). Так, в комплексах с пиридин-2,6-дикарбоновой [18] и щавелевой кислотами [19] иттрий проявляет КЧ 9 в конфигурации искаженной трехшапочной тригональной призмы. В двухъядерном комплексе с хинолин-4-карбоновой кислотой [20] атом Y координирован девятью атомами O (включая две молекулы воды) в конфигурации искаженной одношапочной квадратной антипризмы; в этом обнаруживается групповая аналогия Y с лантаном и лантанидами. Наоборот, в комплексах с фосфонатными лигандами иттрий проявляет сходство с аналогами по 4 и 5 периодам. Так, в комплексе с N,N'-2-метилпиперазин-бис-метиленфосфоновой кислотой [21] КЧ(Y) 6, а координационный полиэдр (КП) близок к тригональной антипризме. При координации Y (1,1′-бифенил)-3,3',5,5'-тетракис-фосфоновой кислотой [22] КП иттрия – слегка искаженный октаэдр. По-видимому, это обусловлено бóльшим объемом и стерической жесткостью фосфонатных лигандов по сравнению с карбоксилатными.
В последнее время как в России, так и за рубежом уделяется большое внимание такому классу N,O-лигандов, как аминополифосфоновые кислоты, ярким представителем которых является нитрило-трис-метиленфосфоновая кислота (N(CH2PO3)H6, NTP). Исследованы координационные соединения NTP со многими металлами [23–32], в том числе с La [32]. Ступенчатое депротонирование O- и N-донорных центров NTP позволяет эффективно управлять структурой и свойствами получаемых комплексов [33, 34] и формируемых при их адсорбции поверхностных слоев [35–37]. Однако структура комплексов Y с NTP не исследована.
Исследование констант устойчивости комплексов NTP с лантанидами Sc и Y показало [38], что первая константа протонирования комплекса (pKMHL) зависит от ионного радиуса металла-комплексообразователя и определяется конкуренцией между протоном и ионом металла за N-донорный центр, а вторая (pKMH2L) и последующие не зависят от природы металла и обусловлены протонированием свободных O-донорных центров. Для комплексов NTP с Y первая константа pKMHL = 7.15 ± ± 0.02, а вторая pKMH2L = 5.5 ± 0.06; этот разрыв свидетельствует о высокой основности N-донорного центра. Значительное отличие от констант протонирования свободного лиганда (pKHL = 12.7 ± 0.1, pKH2L = 7.15 ± 0.02) свидетельствует о существенном сродстве иона Y3+ к донорным центрам NTP.
В настоящей работе описан синтез, строение и некоторые свойства гидрата бис-нитрило-трис-метиленфосфонатомоногидроиттриата октакалия K8[YH{N(CH2PO3)3}2] · 15H2O (II).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез [YH3{N(CH2PO3)3}] · 2H2O (I). К водному раствору 3.3 г (0.011 моль) NTP (предварительно дважды перекристаллизованной) при 70–90°С добавляли по каплям раствор 3.83 г (0.01 моль) Y(NO3)3 · 6H2O (“х. ч.”). Смесь перемешивали в течение 1 ч при 70–90°С, выпавший осадок I отделяли на фильтре, промывали дистиллированной водой до нейтральной реакции и высушивали в эксикаторе до постоянной массы. Выход I 3.96 г (94%). Количественный анализ проводили по ГОСТ 10398-76 (Y), ПНД Ф 14.1:4.248-07 (P).
Синтез K8[YH{N(CH2PO3)3}2] · 15H2O (II). К водному раствору 2.99 г (0.01 моль) NTP и 5.21 г (0.08 моль) KOH (“х. ч.”) добавляют 3.85 г (0.01 моль) I. Реакционную смесь (pH 7.8 ± 0.2) перемешивали в течение 1 ч при 60–80°С и фильтровали. Добавляли 1/3 (по объему) ДМСО, перемешивали и кристаллизовали в изотермических условиях при медленном испарении растворителя. Кристаллы II – бесцветные столбчатые призмы. Выход II 9.32 г (74%).
РСА. Первичные фрагменты структуры найдены прямым методом, положения атомов определены из разностных синтезов электронной плотности. Параметры неводородных атомов уточнены в анизотропном приближении методом наименьших квадратов по |F|2. Положения водородных атомов молекул лиганда уточнены в изотропном приближении. Положения протонов, относящихся к молекулам воды, по данным РСА локализовать не удалось. Кристаллографические характеристики, параметры эксперимента и уточнения структуры II приведены в табл. 1. Основные межатомные расстояния, валентные и торсионные углы в структуре (II) приведены в табл. 2.
Таблица 1.
Кристаллографические характеристики, данные эксперимента и уточнения структуры II
| Параметр | Значение |
|---|---|
| Брутто-формула | C6H43N2O33P6K8Y |
| M | 1258.93 |
| Сингония; пр. гр.; Z | Триклинная; P$\bar {1}$; 2 |
| a, Å | 11.0264(8) |
| b, Å | 11.3857(8) |
| c, Å | 16.6938(6) |
| α, град | 86.455(4) |
| β, град | 85.269(4) |
| γ, град | 85.319(6) |
| V, Å 3 | 2078.5(2) |
| ρ(выч.), г/см 3 | 1.963 |
| Излучение; λ, Å | MoKα; 0.71073 |
| μ, мм –1 | 2.535 |
| T, K | 100(2) |
| Размеры образца, мм | 0.179 × 0.109 × 0.058 |
| Дифрактометр | XtaLAB Pro MM003, PILATUS 200K |
| Тип сканирования | ω |
| Учет поглощения | Аналитический [39] |
| Tmin/Tmax | 0.664/0.88 |
| θmin/θmax, град | 1.797/26.372 |
| Интервалы индексов h, k, l | –13 ≤ h ≤ 13, –14 ≤ k ≤ 14, –20 ≤ l ≤ 20 |
| Число отражений измеренных/независимых (N1) | 34 366/8483 |
| Rint | 0.0716 |
| Число отражений с I > 2σ(I) (N2) | 6835 |
| Метод уточнения | Полноматричный МНК по F2 |
| Число параметров/ограничений | 534/0 |
| S | 1.215 |
| R1/wR1 по N1 | 0.1053/0.2103 |
| R1/wR1 по N2 | 0.0864/0.2035 |
| Δρmin /Δρmax, e/Å3 | –1.014/0.184 |
| Программы | CrysAlisPro [40], SHELX-2014 [41], WinGX [42], VESTA 3.0 [43] |
Таблица 2.
Основные межатомные расстояния (d), валентные (ω) и торсионные (φ) углы в структуре II
| Связь | d, Å | Связь | d, Å | Связь | d, Å |
|---|---|---|---|---|---|
| Y(1)–N(1) | 2.672(9) | C(1)–P(1) | 1.816(11) | P(3)–O(8) | 1.514(8) |
| Y(1)–O(1) | 2.234(8) | C(2)–P(2) | 1.822(11) | P(3)–O(9) | 1.504(9) |
| Y(1)–O(4) | 2.287(8) | C(3)–P(3) | 1.809(10) | P(4)–O(10)Y | 1.513(8) |
| Y(1)–O(7) | 2.295(8) | C(4)–P(4) | 1.813(12) | P(4)–O(11) | 1.518(8) |
| Y(1)–O(3)* | 2.262(7) | C(5)–P(5) | 1.844(12) | P(4)–O(12) | 1.518(9) |
| Y(1)–O(10) | 2.266(8) | C(6)–P(6) | 1.829(11) | P(5)–O(13)Y | 1.528(8) |
| Y(1)–O(13) | 2.322(8) | P(1)–O(1)Y | 1.535(8) | P(5)–O(14) | 1.509(10) |
| N(1)–C(1) | 1.465(13) | P(1)–O(2) | 1.512(8) | P(5)–O(15) | 1.521(10) |
| N(1)–C(2) | 1.484(13) | P(1)–O(3)Y | 1.533(8) | P(6)–O(16) | 1.500(9) |
| N(1)–C(3) | 1.472(14) | P(2)–O(4)Y | 1.537(9) | P(6)–O(17) | 1.521(9) |
| N(2)–C(4) | 1.516(15) | P(2)–O(5) | 1.522(8) | P(6)–O(18) | 1.515(10) |
| N(2)–C(5) | 1.490(14) | P(2)–O(6) | 1.516(8) | N(2)–H | 0.981(9) |
| N(2)–C(6) | 1.510(15) | P(3)–O(7)Y | 1.533(8) | N(2)–O(7) | 2.688(12) |
| K(1)–O | 2.672(9)–3.250(8) | K(4)–O | 2.636(9)–3.329(11) | K(7)–O | 2.744(10)–3.06(4) |
| K(2)–O | 2.613(8)–3.442(8) | K(5)–O | 2.662(11)–2.856(9) | K(8)–O | 2.631(14)–3.183(9) |
| K(3)–O | 2.610(12)–3.195(16) | K(6)–O | 2.717(9)–3.257(9) | ||
| Угол | ω, град | Угол | ω, град | Угол | ω, град |
| N(1)Y(1)O(1) | 70.23(16) | O(10)Y(1)O(13) | 81.40(17) | HN(2)C | 105.4(5) |
| N(1)Y(1)O(4) | 69.27(16) | O(13)Y(1)O(3)* | 84.94(17) | C(4)N(2)C(5) | 113.4(5) |
| N(1)Y(1)O(7) | 68.80(15) | O(1)Y(1)O(3)* | 85.88(17) | C(5)N(2)C(6) | 113.7(5) |
| N(1)Y(1)O(3)* | 132.43(16) | O(4)Y(1)O(10) | 84.28(17) | C(6)N(2)C(4) | 112.5(5) |
| N(1)Y(1)O(10) | 129.47(17) | O(7)Y(1)O(13) | 79.28(16) | N(1)C(1)P(1) | 113.2(4) |
| N(1)Y(1)O(13) | 129.90(17) | Y(1)N(1)C(1) | 106.5(3) | N(1)C(2)P(2) | 111.1(4) |
| O(1)Y(1)O(4) | 106.90(17) | Y(1)N(1)C(2) | 107.9(4) | N(1)C(3)P(3) | 113.0(4) |
| O(4)Y(1)O(7) | 111.77(17) | Y(1)N(1)C(3) | 109.0(3) | N(2)C(4)P(4) | 113.4(4) |
| O(7)Y(1)O(1) | 106.27(18) | C(1)N(1)C(2) | 110.4(4) | N(2)C(5)P(5) | 115.2(4) |
| O(3)*Y(1)O(10) | 80.04(17) | C(2)N(1)C(3) | 111.3(4) | N(2)C(6)P(6) | 120.0(4) |
| C(3)N(1)C(1) | 111.4(5) | N(2)HO(7) | 154.4(4) | ||
| Угол | φ, град | Угол | φ, град | Угол | φ, град |
| N(1)C(1)P(1)O(1) | 31.59(10) | N(1)C(3)P(3)O(7) | 33.57(10) | N(2)C(5)P(5)O(13) | 41.61(11) |
| N(1)C(2)P(2)O(4) | 34.70(10) | N(2)C(4)P(4)O(10) | 51.42(10) |
Результаты рентгеноструктурных исследований депонированы в Кембриджском банке структурных данных (CCDC № 1847628; deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk).
Рентгенофотоэлектронные (РФЭ) спектры I и II получали на отечественном рентгеноэлектронном спектрометре ЭМС-3 (УдмФИЦ УрО РАН) [44] с магнитным энергоанализатором при возбуждении AlKα-излучением (hν = 1486.6 эВ). Образцы в виде тонкоизмельченных порошков наносили слоем толщиной 1–3 мкм на подложку из пиролитического графита. В процессе регистрации спектров образцы in situ (в рабочей камере спектрометра) подвергали нагреву от комнатной температуры до 400°С при непрерывной откачке образующихся газообразных продуктов деструкции. Остаточное давление в рабочей камере не превышало 10–5 Па. Калибровку энергоанализатора проводили по спектру C1s (энергия связи Eсв = 284.5 эВ). Регистрировали спектры P2p, Y3d, N1s и валентной полосы. Коррекцию фона и неупругого рассеяния проводили по Ширли [45]. Статистическую обработку экспериментальных данных проводили в программе Fityk 0.9.8 [46].
ИК-спектры I, II и продуктов их термического разложения регистрировали в таблетках (мг: исследуемое вещество 1, KBr 250) на Фурье-спектрометре ФСМ-1201 в интервале 450–5000 см–1. Спектры комбинационного рассеяния I и II регистрировали на микроскопе-микроспектрометре Centaur U-HR в интервале 475–575 нм (возбуждением лазером с λ = 473 нм). Термогравиметрический анализ I и II проводили на автоматизированном дериватографе Shimadzu DTG-60H в интервале 30–500°С при скорости нагрева 3°С/мин в атмосфере аргона.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Строение внутренней координационной сферы комплекса II показано на рис. 1а. Атом Y координирован двумя молекулами NTP лиганда, oдна из которых полностью депротонирована. Она координирует атом Y(1) атомом N(1) и тремя атомами O (по одному от каждой PO3-группы), а также координирует атом Y(1)* двумя атомами О симметрично-эквивалентной относительно центра инверсии формульной единицы комплекса. При этом замыкаются три пятичленных внутримолекулярных цикла Y–N–C–P–O с общей связью Y–N и восьмичленный межмолекулярный цикл Y–O–P–O–Y–O–P–O. На полное депротонирование данной молекулы NTP указывают расстояния P–O (1.504(9)–1.537(9) Å, в среднем 1.523(11) Å): протонирование приводит к удлинению связи P–O до 1.55–1.56 Å [27–29, 31–33]). При этом для атомов O, координирующих атом Y, расстояния P–O (1.533(8)–1.537(9) Å, в среднем 1.534(2) Å) на 0.021 Å больше, чем для атомов O, не участвующих в координации атома Y (1.504(9)–1.522(8) Å, в среднем 1.513(6) Å). Это указывает на смещение электронной плотности от связи P–O к Y–O; последняя, таким образом, имеет существенную ковалентную составляющую. Об образовании координационной связи Y–N свидетельствуют валентные углы при атоме N(1) (106.5(3)°–111.4(5)°, в среднем 109.4(18)°), близкие к тетраэдрическому углу (109.47°). Таким образом, эта молекула лиганда пентадентатна и осуществляет как хелатную, так и мостиковую координацию атомов Y. Ее конформация близка к тригонально-псевдосимметричной, что проявляется в близости межатомных расстояний, валентных и торсионных углов между атомами трех ветвей N–C–P этой молекулы. Двугранные углы между плоскостями N(1)Y(1)C составляют 118.58(13)°–121.07(13)°, в среднем 120.0(7)°.
Рис. 1.
а – внутренняя координационная сфера комплекса II, б – кристаллическая упаковка комплекса II в координационных полиэдрах Y (темный) и K (светлые) (показана только одна из двух симметрично расположенных формульных единиц); * – симметрично эквивалентные позиции.
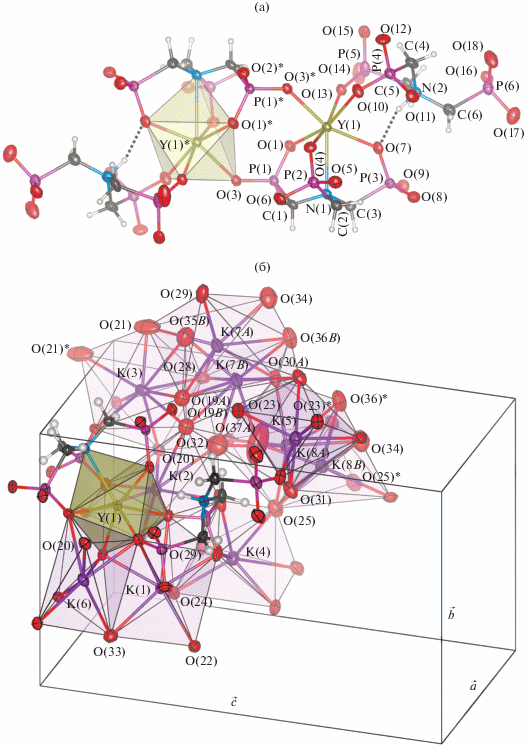
Вторая молекула NTP бидентатна; она координирует атом Y(1) двумя атомами O двух PO3-групп с замыканием восьмичленного хелатного цикла Y–O–P–C–N–C–P–O. Третья PO3-группа данной молекулы NTP не участвует в координации атомов Y. Атом азота этой молекулы NTP протонирован и образует H-связь с атомом O(7) первой молекулы лиганда. Все атомы O этой молекулы лиганда депротонированы, что подтверждается анализом расстояний P–O (1.500(9)–1.528(8) Å, в среднем 1.516(8) Å). Расстояния P–O для атомов O, участвующих в координации Y, составляют 1.513(8) и 1.528(8) Å (в среднем 1.521(8) Å), для не участвующих – 1.500(9)–1.521(10) Å (в среднем 1.515(7) Å). Конформация этой молекулы лиганда полностью асимметричная, что проявляется в резком различии межатомных расстояний, валентных и торсионных углов между атомами ее ветвей N–C–P.
Таким образом, две молекулы NTP, входящие во внутреннюю координационную сферу комплекса II, неэквивалентны по кристаллографическому положению, по химической функции и по кислотно-основному состоянию. Это резко отличает комплекс II от NTP-комплекса La [32], в котором две молекулы лиганда в координационной сфере расположены симметрично, обе полностью депротонированы и осуществляют хелатную координацию атома La, КЧ(La) 8. По-видимому, такое поведение NTP в комплексе II с Y обусловлено особенностями иттрия как комплексообразователя. В комплексе II КЧ(Y) 7, что характерно для многих элементов 5 периода. КП атома Y – искаженная тригональная антипризма, в вершинах которой расположены атомы O, с дополнительным атомом N в шапочной вершине над основанием. Расстояния Y–O составляют 2.234(8)–2.322(8) Å (в среднем 2.278(21) Å), что на 0.28(4) Å меньше ожидаемой суммы ковалентных радиусов Y и О 2.56 Å [47] (r(Y) = 1.90(7), r(O) = 0.66(2) Å). По-видимому, это объясняется значительным донированием связей Y–O электронной плотностью атомов O. Расстояние Y–N в II (2.672(9) Å), напротив, больше на 0.06(4) Å суммы ковалентных радиусов Y и N 2.61 Å (r(N) = 0.71(1) Å), что объясняется сравнительно слабой донорной способностью атома азота. По-видимому, ковалентный радиус Y, существенно меньший, чем r(La) (2.07(8) Å), и стерическая жесткость пентадентатно координированной молекулы NTP в совокупности препятствуют увеличению КЧ(Y) до 8. Конкуренция между O- и N-донорными центрами второй молекулы NTP за атом Y приводит к невозможности координации Y вторым атомом N. Таким образом, различное кислотно-основное состояние двух молекул лиганда в структуре комплекса II обусловлено стереохимическими особенностями координации Y.
Кристаллическая упаковка комплекса II изображена на рис. 1б. Формульная единица комплекса асимметрична; группа симметрии кристаллической упаковки P$\bar {1}$ обусловлена симметричным размещением формульных единиц относительно центров инверсии (на рис. 1б условно показана только одна формульная единица). Комплексные анионы [YH{N(CH2PO3)3}2]8– структурных единиц кристалла, симметрично размещенные в соседних ячейках кристаллической решетки, попарно соединены координационными связями O–Y (рис. 1а). Кристаллическая структура островная; комплексные анионы [YH{N(CH2PO3)3}2]8– окружены калий-гидратными катионами образуя непрерывную трехмерную вязь полиэдров К+–(Н2О)n. Положения двух ионов калия (K(7) и K(8)) разупорядочены. Координирующие их молекулы воды также разупорядочены, что обусловливает кажущиеся короткие контакты K–O(w). В действительности при заселении ионом K+ каждой из позиций молекулы воды заселяют только стерически подходящие позиции координационной сферы. Также, молекулы воды объединены друг с другом и с атомами кислорода PO3-групп молекул NTP водородными связями; однако из-за значительной разупорядоченности молекул воды локализовать положение большинства атомов водорода и водородных связей не удалось.
РФЭ-спектры комплексов I и II приведены на рис. 2. Спектр P2p соединения I (рис. 2, 1) включает две составляющие с шириной на половине высоты (ШПВ) 2 эВ. По литературным данным [31, 37, 48], низкоэнергетическая составляющая (Eсв = 132.2 эВ) относится к PO3-группам, координирующим атом металла, а высокоэнергетическая (Eсв = 133.9 эВ) – к свободным PO3-группам. Отношение интегральных интенсивностей 2 : 1 позволяет предположить, что в структуре I две PO3-группы координируют атом Y, а одна не участвует в координационной связи. Спектр Y3d комплекса I представляет собой спин-орбитальный дублет с Eсв = 154.7 и 157.5 эВ, ШПВ каждой составляющей 2 эВ и отношением их интегральных интенсивностей 3 : 2. Спектр N1s соединения I представлен единственной составляющей с ШПВ 2.12 эВ и максимумом при Eсв = 400.8 эВ, что характерно для азота в R3N+–H-окружении [49, 50]. В спектре валентной полосы (рис. 2б) наблюдаются занятые молекулярные состояния с Eсв ~ 5, 7 и 10 эВ, локализованные электронные состояния P3s, O2s, Y4p и Y4s.
Рис. 2.
РФЭ спектры внутренних уровней (а) и слабосвязанных электронов (б) комплексов I (1) и II (2). Интенсивность как функция энергии связи Eсв, засечками показаны 95% доверительные интервалы интенсивности.
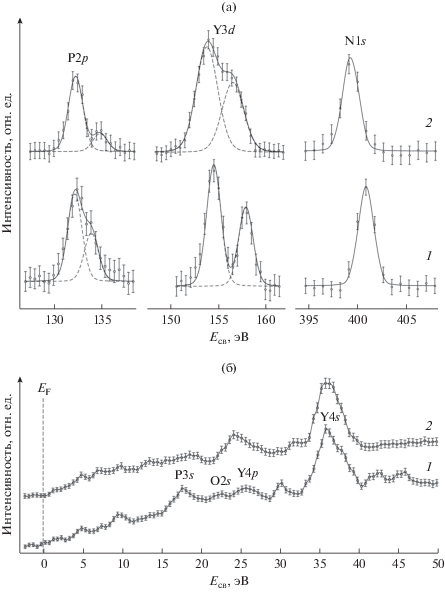
В РФЭ-спектре соединения II (рис. 2, 2) отношение интегральных интенсивностей составляющих P2p с Eсв = 132.2 и 134.7 эВ ~5 : 1, что позволяет отнести составляющую с Eсв = 132.2 эВ к атомам P(1)–P(5), а составляющую с Eсв = 134.7 эВ – к атому P(6). Спин-орбитальный дублет Y3d включает составляющие с Eсв = 153.9 и 156.6 эВ с ШПВ 3 эВ. Понижение Eсв Y3d на 0.8–0.9 эВ по сравнению с комплексом I можно объяснить обратным донированием Y электронной плотностью атомов O. Спектр N1s соединения II имеет ШПВ 2.2 эВ и Eсв = 399.2 эВ, что близко к энергии связи 1s-подуровня азота в нитридах [51–53] и подтверждает образование координационной связи Y–N. В спектре валентной полосы прослеживается сближение максимумов интенсивности состояний P3s и повышение электронной плотности в области перекрытия состояний O2s и Y4p.
Молекулярно-колебательные спектры комплексов I и II приведены на рис. 3. Колебания структурных субъединиц (комплексных ионов) как целого в структуре I представлены полосами 231, 279 и 309 см–1; для структуры II эти частоты ниже – 100, 156 и 230 см–1. Последнее объясняется значительной массой комплексного аниона [YH{N(CH2PO3)3}2]8– и низкой силовой константой ионной связи его с внешней координационной сферой. В соединении I масса координационной сферы [Y{NTP}], по-видимому, меньше, а связь между структурными единицами прочнее, на что указывает нерастворимость I в воде; возможно, эта связь имеет ковалентный характер. Полосы 480 и 550 см–1 в спектрах ИК и КР соединения I относятся к колебаниям δ(O–Y); В структуре II колебания координационной сферы представлены широкой полосой 500–640 см–1. Асимметрия КП атома Y в обеих структурах проявляется в отсутствии альтернативного запрета этих колебательных мод. Полосы 725, 760, 812, 856, 880, 910 см–1 относятся к колебаниям связей N–C–P молекул лиганда. Колебаниям ν(P–O) в комплексах I и II соответствуют полосы около 943, 1002, 1073, 1128, 1173 см–1, не подчиненные альтернативному запрету, что подтверждает асимметричную конформацию молекулы лиганда. Частоты колебаний локализованных π-связей P–O в соединении I 1234 и 1272 см–1 в соединении II смещаются к 1170 и 1225 см–1, что свидетельствует о значительной делокализации электронной плотности в PO3-группах. Также наблюдаются полосы (см–1): 1330 δ(M–O–H), 1430 δ(CH2), 2770, 2830, 2890, 2950 ν(CH2), 3050 ν(N+–H).
Рис. 3.
Спектры КР (интенсивность I как функция волнового числа ν) комплексов I (1) и II (2); ИК-спектры (пропускание T как функция волнового числа ν) комплексов I (3), II (4), продуктов термического разложения в среде аргона комплексов I (5) и II (6).
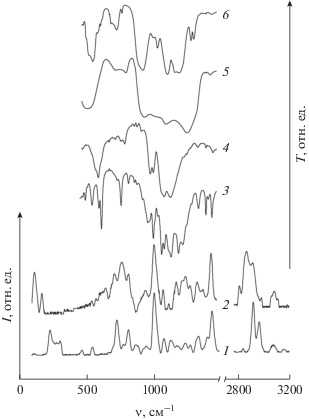
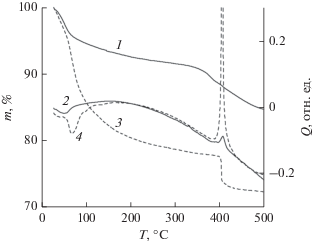
Термограммы (рис. 4) показывают, что при нагревании I одна молекула H2O отщепляется в интервале 40–80°С с заметным эндотермическим эффектом, другая – в широком интервале 80–355°С. При 375–420°С экзотермически отщепляется атом N. Дегидратация II происходит в интервалах 65–95°С (–10H2O) и 95–385°С (–5H2O). В узком интервале 405–415°С наблюдается потеря массы, соответствующая отщеплению двух молекул CH3NH2 c “взрывным” экзотермический эффектом. По-видимому, это свидетельствует о значительных механических напряжениях в хелатных циклах комплекса II. В ИК-спектрах продуктов термического разложения I и II (рис. 3, 5 и 6) обнаруживаются полосы калий-фосфатного стекла K2O · P2O5 [54] (см–1): 530, 730, 885–920, 1090; полиметафосфата калия (KPO3)n [55] (см–1): 680, 760, 1100, 1150, 1270, 1300; ортофосфата иттрия YPO4 [56, 57] (см–1): 580, 997, 1023.
Рис. 4.
Термогравиграммы I (1 и 2) и II (3 и 4) в среде аргона. Масса образца m (1 и 3) и тепловой эффект Q (2 и 4) как функции температуры Т.
Таким образом, впервые синтезированы, выделены и исследованы координационные соединения [YH3{N(CH2PO3)3}] · 2H2O (I) и K8[YH{N(CH2PO3)3}2] · 15H2O (II). Методом РСА установлена структура II; проанализированы кристаллографические особенности строения, кислотно-основное состояние и химическая функция неэквивалентных молекул лиганда. Атом Y семикоординирован в конфигурации искаженной тригональной антипризмы с дополнительной шапочной вершиной над основанием.
Предполагается возможность использования II в качестве прекурсора для получения равномерного адсорбционного Y-содержащего слоя на поверхности стали с последующим поверхностным легированием для повышения жаростойкости.
Работа выполнена в рамках государственного задания ФАНО России (номер государственной регистрации АААА-А17-117022250040-0).
Список литературы
Comprehensive Coordination Chemistry. V. 3 / Eds. Wilkinson G., Gillard R.D., McCleverty J.A. Pergamon Press, 1987. 1601 p.
Координационная химия редкоземельных элементов / Под ред. Спицына В.И., Мартыненко Л.А. М.: Изд-во МГУ, 1979. 254 с.
Comprehensive Coordination Chemistry II. V. 3 / Eds. McCleverty J.A., Meyer T.J. Elsevier, 2003. 608 p.
Rösch F., Herzog H., Plag C. et al. // Eur. J. Nucl. Med. 1996. V. 23. № 8. P. 958. doi https://doi.org/10.1007/BF01084371
Djokic´ D.Dj., Jankovic´ D.Lj., Nikolic´ N.S. // Bioorg. Med. Chem. 2008. V. 16. P. 4457. doi https://doi.org/10.1016/ j.bmc.2008.02.062
Pillis M. F., Ramanathan L. V. // Surf. Engineering. 2006. V. 22. № 2. P. 129. doi https://doi.org/10.1179/174329406X98412
McGurty J.A. US Patent № 4385934.
Wegener T., Klein F., Litnovsky A et al. // Nucl. Mater. Energy. 2016. V. 9. P. 394. doi https://doi.org/10.1016/j.nme.2016.07.011
Prajitno D.H., Soepriyanto S., Basuki E.A., Wiryolukito S. // J. Mater. Sci. Engineering. A. 2015. V. 5. № 3–4. P. 154. doi https://doi.org/10.17265/2161-6213/2015.3-4.007
Grabke H.J. // Surf. Interf. Anal. 2000. V. 30. № 1. P. 112. doi https://doi.org/10.1002/1096-9918(200008)30:1<112::AID-SIA777>3.0.CO;2-G
Wang W., Wu E., Liu S. et al. // Mater. Sci. Technol. 2016. V. 33. № 1. P. 104. doi https://doi.org/10.1179/ 1743284715Y.0000000143
Patnaik P. Handbook of Inorganic Chemicals. M-cGraw-Hill, 2002. 1086 p.
Gromov V.E., Sosnin K.V., Ivanov Yu.F. et al. // Mater. Electron. Engineering. 2015. V. 2. № 3. P. 1. doi https://doi.org/10.11605/mee-2-3
Соснин К.В., Иванов Ю.Ф., Громов В.Е. и др. // Металлург. 2015. № 9–10. С. 81. (Sosnin K.V., Ivanov Yu.F., Gromov V.E et al. // Metallurgist. 2016. V. 59. № 9–10. P. 829 . doi https://doi.org/10.1007/s11015-016-0180-3).
Wu A., Liu Q., Qin S. // J. Rare Earths. 2011. V. 29. № 10. P. 1004. doi https://doi.org/10.1016/S1002-0721(10)60586-8
Pérez F.J., Cristóbal J., Hierro M.P. et al. // Surf. Coat. Technol. 2000. V. 126. P. 116. doi https://doi.org/10.1016/S0257-8972(99)00666-0
Han B., Gu D., Yang Y. et al. // Int. J. Electrochem. Sci. 2017. V. 12. P. 374. doi https://doi.org/10.20964/2017.01.53
Soleimannejad J., Aghabozorg H., Nakhjavan B. et al. // Acta Crystallogr. E. 2007. V. 63. P. m3170. doi https://doi.org/10.1107/S1600536807060047
Lv Y.-K., Gan L.-H., Xu L et al. // Acta Crystallogr. E. 2011. V. 67. P. m837. doi https://doi.org/10.1107/S1600536811019209
Zhang C.-Y., Gao Q., Cui Y., Xie Y.-B. // Acta Crystallogr. E. 2008. V. 64. P. m1631. doi https://doi.org/10.1107/S1600536808039421
Wharmby M.T., Miller S.R., Groves J.A. et al. // Dalton Trans. 2010. V. 39. P. 6389. doi https://doi.org/10.1039/c0dt00233j
Firmino A.D.G., Mendes R.F., Antunes M.M. et al. // Inorg. Chem. 2017. V. 56. P. 1193. doi https://doi.org/10.1021/acs.inorgchem.6b02199
Cabeza A., Ouyang X., Sharma C.V.K. et al. // Inorg. Chem. 2002. V. 41. P. 2325. doi https://doi.org/10.1021/ic0110373
Demadis K.D., Katarachia S.D., Koutmos M. // Inorg. Chem. Commun. 2005. V. 8. P. 254. doi https://doi.org/10.1016/j.inoche.2004.12.019
Сомов Н.В., Чаусов Ф.Ф. // Кристаллография. 2014. Т. 59. № 1. С. 71. (Somov N.V., Chausov F.F. // Cryst. Rep. 2014. V. 59. № 1. P. 66. doi 10.1134/S1063774513050118).
Сомов Н.В., Чаусов Ф.Ф. // Кристаллография. 2015. Т. 60. № 2. С. 233. (Somov N.V., Chausov F.F. // Cryst. Rep. 2015. V. 60. № 2. P. 210. doi 10.1134/ S1063774515010228).
Сомов Н.В., Чаусов Ф.Ф., Закирова Р.М., Федотова И.В. // Коoрд. химия. 2015. Т. 41. № 12. С. 729. (Somov N.V., Chausov F.F., Zakirova R.M., Fedotova I.V. // Russ. J. Coord. Chem. 2015. V. 41. № 12. P. 798. doi 10.1134/S1070328415110081).
Сомов Н.В., Чаусов Ф.Ф., Закирова Р.М., Федотова И.В. // Кристаллография. 2016. Т. 61. № 2. С. 238. (Somov N.V., Chausov F.F., Zakirova R.M., Fedotova I.V. // Cryst. Rep. 2016. V. 61. № 2. P. 216. doi 10.1134/S1063774516020243).
Сомов Н.В., Чаусов Ф.Ф. // Кристаллография. 2016. Т. 61. С. 45–49. (Somov N.V., Chausov F.F. // Crystallogr. Repts. 2016. V. 61. P. 39–43. doi 10.1134/ S1063774516010235).
Bazaga-García M., Angeli G.K., Papathanasiou K.E. et al. // Inorg. Chem. 2016. V. 55. P. 7414. doi https://doi.org/10.1021/acs.inorgchem.6b00570
Сомов Н.В., Чаусов Ф.Ф., Закирова Р.М. и др. // Коорд. химия. 2017. Т. 43. № 12. С. 765. (Somov N.V., Chausov F.F., Zakirova R.M. et al. // Russ. J. Coord. Chem. 2017. V. 43. № 12. P. 864–873. doi 10.1134/ S1070328417120090).
Сомов Н.В., Чаусов Ф.Ф., Закирова Р.М. и др. // Коорд. химия. 2017. Т. 43. № 6. С. 369. (Somov N.V., Chausov F.F., Zakirova R.M. et al. // Russ. J. Coord. Chem. 2017. V. 43. № 6. P. 373. doi 10.1134/ S1070328417060082).
Сомов Н.В., Чаусов Ф.Ф., Закирова Р.М. и др. // Кристаллография. 2017. Т. 62. № 6. С. 896. (Somov N.V., Chausov F.F., Zakirova R.M. et al. // Cryst. Rep. 2017. V. 62. № 6. P. 857. doi 10.1134/S1063774517050224).
Чаусов Ф.Ф., Сомов Н.В., Наймушина Е.А., Шабанова И.Н. // Изв. АН. Сер. физ. 2017. Т 81. № 3. С. 312. (Chausov F.F., Somov N.V., Naimushina E.A., Shabanova I.N. // Bull. Russ. Acad. Sci.: Physics, 2017. V. 81. № 3. Р. 285. doi 10.3103/S106287381703007).
Somov N.V., Chausov F.F., Lomova N.V. et al. // Russ. J. Coord. Chem. 2017. V. 43. № 9. P. 583. doi https://doi.org/10.1134/ S1070328417090093
Чаусов Ф.Ф., Сомов Н.В., Закирова Р.М. и др. // Изв. АН. Сер. физ. 2017. Т 81. № 3. С. 394. (Chausov F.F., Somov N.V., Zakirova R.M. et al. // Bull. Russ. Acad. Sci.: Physics. 2017. V. 81. № 3. Р. 365. doi 10.3103/ S106287381703008X).
Чаусов Ф.Ф., Сомов Н.В., Наймушина Е.А. и др. // Изв. АН. Сер. физ. 2016. Т. 80. № 11. С. 1476. (Chausov F.F., Somov N.V., Naimushina E.A.et al. // Bull. Russ. Acad. Sci.: Physics. 2016. V. 80. № 11. P. 1310. doi 10.3103/S1062873816110174).
Sawada K., Kuribayashi M., Suzuki T., Miyamoto H. // J. Solution Chem. 1991. V. 20. № 8. P. 829. doi https://doi.org/10.1007/BF00675114
Clark R.C., Reid J.S. // Acta Crystalligr. A. 1995. V. 51. P. 887. doi https://doi.org/10.1107/S0108767395007367
CrysAlisPro 1.171.38.41. Rigaku Oxford Diffraction, 2015.
Sheldrick G.M. // Acta Crystallogr. A. 2008. V. 64. P. 112. doi https://doi.org/10.1107/S0108767307043930
Farrugia L.J. // J. Appl. Cryst. 1999. V. 32. P. 837. doi https://doi.org/10.1107/S0021889899006020
Momma K., Izumi F. // J. Appl. Cryst. 2011. V. 44. P. 1272. doi https://doi.org/10.1107/S0021889811038970
Trapeznikov V.A., Shabanova I.N., Kholzakov A.V., Ponomaryov A.G. // J. Electron Spectrosc. 2004. V. 137. P. 383. doi https://doi.org/10.1016/j.elspec.2004.02.115
Shirley D.A. // Phys. Rev. 1972. V. 55. P. 4709. doi https://doi.org/10.1103/PhysRevB.5.4709
Wojdyr M. // J. Appl. Cryst. 2010. V. 43. P. 1126. doi https://doi.org/10.1107/S0021889810030499
Cordero B., Gómez V., Platero-Prats A.E. et al. // Dalton Trans. 2008. P. 2832. doi https://doi.org/10.1039/b801115j
Чаусов Ф.Ф., Наймушина Е.А., Шабанова И.Н., Решетников С.М. // Изв. АН. Сер. физ. 2015. Т. 79. № 6. С. 848. doi https://doi.org/10.7868/S036767651506006X
Stevens J.S., Byard S.J., Muryn C.A., Schroeder S.L.M. // J. Phys. Chem. B. 2010. V. 114. P. 13961. doi https://doi.org/10.1021/ jp106465u
Desimoni E., Brunetti B. // Chemosensors. 2015. V. 3. P. 70. doi https://doi.org/10.3390/chemosensors3020070
Hendrickson D.N., Hollander J.M., Jolly W.L. // Inorg. Chem. 1969. V. 8. P. 2642. doi https://doi.org/10.1021/ic50082a020
Badrinarayanan S., Sinha S., Mandale A.B. // J. Electron Spectrosc. Related Phenomena. 1989. V. 49. P. 303. doi https://doi.org/10.1016/0368-2048(89)85018-2
Kawamura M., Abe Y., Yanagisawa H., Sasaki K. // Thin Solid Films. 1996. V. 287. P. 115. doi https://doi.org/10.1016/S0040-6090(96)08749-4
de Andrade J.S., Pinheiro A.G., Vasconcelos I.F. et al. // J. Phys.: Condens. Matter. 1999. V. 11. P. 4451. doi https://doi.org/10.1088/0953-8984/11/22/315
Corbridge D.E.C., Lowe E.J. // J. Chem. Soc. 1954. P. 493. doi https://doi.org/10.1039/JR9540000493
Liu Q., Su Y., Yu H., Han W. // J. Rare Earths. 2008. V. 26. № 4. P. 495. doi https://doi.org/10.1016/S1002-0721(08)60125-8
Richman I. // J. Optical Soc. Am. 1966. V. 56. № 11. P. 1589. doi https://doi.org/10.1364/JOSA.56.001589
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия


