Координационная химия, 2020, T. 46, № 12, стр. 770-776
Необычное образование парамагнитного (η4-C4Me4)CoI2(PhTeI) и особенности его электронного, молекулярного и кристаллического строения
Ю. В. Торубаев 1, И. В. Скабицкий 1, В. В. Минин 1, Е. А. Уголкова 1, П. В. Русина 1, С. С. Шаповалов 1
1 Институт общей и неорганический химии им. Н.С. Курнакова РАН
Москва, Россия
Поступила в редакцию 06.05.2020
После доработки 01.06.2020
Принята к публикации 15.06.2020
Аннотация
При длительном хранении 18-электронный (η4-C4Me4)Co(CO)2TeI2Ph не только заметно разлагается, но и необычным образом трансформируется в 17-электронный (η4-C4Me4)CoI2(PhTeI) (I). Методом РСА (CIF file CCDC № 1991837) изучено его молеклярное и кристалличесое строение, выявившее интересные параллели с молекулярным строением известных металлокомплексов с органотеллургалогенидными лигандами и с упаковкой в кристалле родственных ему однокомпонентных кристаллов (η4-C4Me4)Co(СО)2TeI2Ph, (η4-C4Me4)Co(СО)2I и двухкомпонентных (η4-C4Me4)Co(СО)2I–1,4-C6H4I2. Анализ упаковки молекул I в кристалле выявил новый супрамолекулярный синтон I···(η4-C4Me4), определяющий структурные мотивы самосборки не только в I, но и в родственных ему η4-C4Me4)Co(CO)2I, (η4-C4Me4)Co(CO)2I···1,4-C6H4I2 и (η4-C4Me4)Co(CO)2TeI2Ph. ЭПР исследование I показало, что кобальт находится в низкоспиновом состоянии с полным спином S = 1/2.
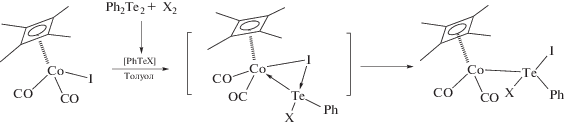
Каталитическая и магнитная активность комплексов кобальта обуслoвливает все возрастающий интерес к ним. В частности, CpCo(CO)2 успешно применяется в качестве катализатора тримеризации ацетиленов, [CpCo(CO)I2] – в функционализации связей С–Н [1] и в сочетании связей С–С [2]. Циклобутадиеновые комплексы [(C4Me4)Co(C6H6)]PF6, (C4Me4)Co(CO)2I и [(C4Me4)Co(Bipy)(MeCN)]PF6 катализируют окисление алканов и спиртов [3]. В 2012 г. мы обобщили результаты структурных и синтетических исследований органо-теллургалогенидов как нового типа лигандов в комплексах переходных металлов в обзоре [4]. Одними из наиболее интересных представителей этого класса соединений были дииодтеллурофенильный циклобутадиен-кобальтдикарбонильный комплекс (η4-C4Me4)Co(CO)2TeI2Ph и его гетерогалогенидный аналог (η4-C4Me4)Co(CO)2TeIBrPh, образующиеся при формальном внедрении PhTeX (X = Br, I) по связи Co–I в (η4-C4Me4)Co(CO)2I [5] (схема 1 ).
Схема 1.
Спустя почти 10 лет при изучении перспектив использования сэндвичевых [6] и полусэндвичевых металлокомплексов с теллурорганическими и галогенидными лигандами в дизайне кристаллов [7] мы перекристаллизовали образец (η4-C4Me4)Co(CO)2TeI2Ph, хранившийся все это время при комнатной температуре в механически поврежденной ампуле, и выделили новый парамагнитный комплекс (η4-C4Me4)CoI2(PhTeI) (I), для которого была разработана лабораторная методика получения и проведен ряд физико-химических исследований.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Коммерческий Ph2Te2 перед использованием перекристаллизовали, (η4-C4Me4)Co(CO)2TeI2Ph получили по методике [5]. Органические растворители осушали по стандартным методикам и перегоняли в атмосфере аргона.
Cинтез (η4-C4Me4)CoI2(PhTeI) (I). Кристаллический иод (0.026 г, 0.1 ммоль) добавляли небольшими порциями к интенсивно перемешиваемому магнитной мешалкой оранжевому раствору Ph2Te2 (0.041 г, 0.1 ммоль) в толуоле (7 мл) при комнатной температуре. Полученную темно-синюю реакционную смесь перемешивали еще 20 мин, затем к ней добавляли (η4-C4Me4)Co(CO)2I (0.70 г, 0.2 ммоль) в один прием. Полученный раствор интенсивно перемешивали при 40°С в течение 12 ч с обратным холодильником или кипятили 2 ч с эффективным обратным холодильником, открытым на атмосферу. Ход реакции контролировали по ИК-спектрам. После исчезновения пиков СО исходного (η4-C4Me4)-Co(CO)2I реакционную смесь охлаждали до конатной температуры, удаляли растворитель в вакууме водоструйного насоса и экстагировали остаток CH2Cl2 (10 мл). Отфильтрованный экстракт разбавляли гептаном (2 мл), концентрировали в вакууме водоструйного насоса до легкого помутнения и выдерживали несколько суток при –10°C. Образовавшиеся темно-красные призматические кристаллы отфильтровывали, промывали гексаном и высу-шивали в вакууме. Выход 0.07 г (46%).
По данным РСА, кристаллы I идентичны полученным при перекристаллизации образца (η4-C4Me4)Co(CO)2TeI2Ph, хранившегося 10 лет при комнатной температуре в поврежденной ампуле.
ИК-спектры записывали на спектрофотометре Bruker Alpha FTIR, снабженном ATR-приставкой (для твердых образцов) и в кюветах (0.1 мм) из CaF2 (для растворов). Спектры ЭПР записывали на приборе Bruker ELEXSYS E-680X в X-диапазоне при 100 и 293 K.
РСА выполнен на дифрактометре Bruker-APEXII CCD. Поглощение учтено методом множественного измерения эквивалентных отражений с использованием программы SADABS. Структура определена прямым методом и уточнена методом наименьших квадратов относительно F2 в анизотропном приближении неводородных атомов с использованием пакета программ SHELXTL и Olex2 [8, 9]. Положения атомов Н рассчитаны геометрически. Основные кристаллографические данные и параметры уточнения структуры I приведены в табл. 1, основные длины связей и углы в структуре I – в подписях к рис. 2–4.
Таблица 1.
Основные кристаллографические данные и параметры уточнения структуры I
| Параметр | Значение |
|---|---|
| Брутто формула | C14H17I3CoTe |
| М | 752.51 |
| Излучение (λ, Å) | МоKα (0.71073) |
| T, K | 150 |
| Кристаллическая система | Моноклинная |
| Пр. гр. | P21/c |
| Z | 4 |
| a, Å | 17.9930(13) |
| b, Å | 7.1900(5) |
| c, Å | 14.8942(10) |
| β, град | 93.8320(10) |
| V, Å3 | 3965.85(13) |
| ρ(выч.), г/см3 | 2.600 |
| μ, мм–1 | 7.185 |
| F(000) | 1356.0 |
| Область сбора данных по θ, град | 5.482–57.998 |
| Число измеренных отражений | 13 590 |
| Число независимых отражений | 4947 |
| Rint, Rsigma | 0.0264, 0.0340 |
| Число отражений с I > 2σ(I) | 5420 |
| Количество уточняемых параметров | 173 |
| R1, wR2 (I > 2σ(I) | 0.0376, 0.0939 |
| R1, wR2 (по всем данным) | 0.0441, 0.0976 |
| GOОF | 1.053 |
| Остаточная электронная плотность (max/min), e/Å3 | 2.92/–1.46 |
Рис. 1.
Молекулярная структура I. Длины связей и валентные углы: Co(1)–Te(1) 2.5688(6), Co(1)–I(3) 2.6260(7), Co(1)–I(2) 2.5664(7), Te(1)–I(1) 2.7769(4); Te(1)–I(3) 3.1713 Å и I(3)Te(1)I(1) 164.79(1)°, Co(1)Te(1)C(9) 111.8(1)°. Атомы водорода опущены.
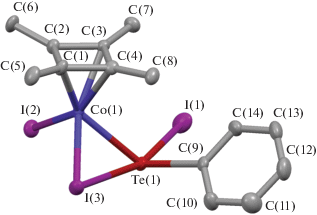
Рис. 2.
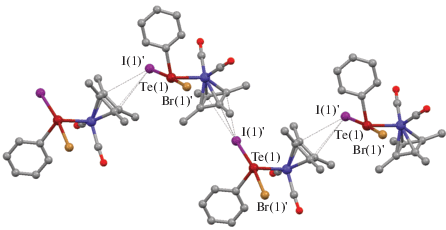
Цепочки молекул I (а), (η4-C4Me4)Co(CO)2I (б), (η4-C4Me4)Co(CO)2I···1,4-C6H4I2 (в) и (η4-C4Me4)Co(CO)2TeI2Ph (г), ассоциированных за счет взаимодействий I···(η4-C4Me4).
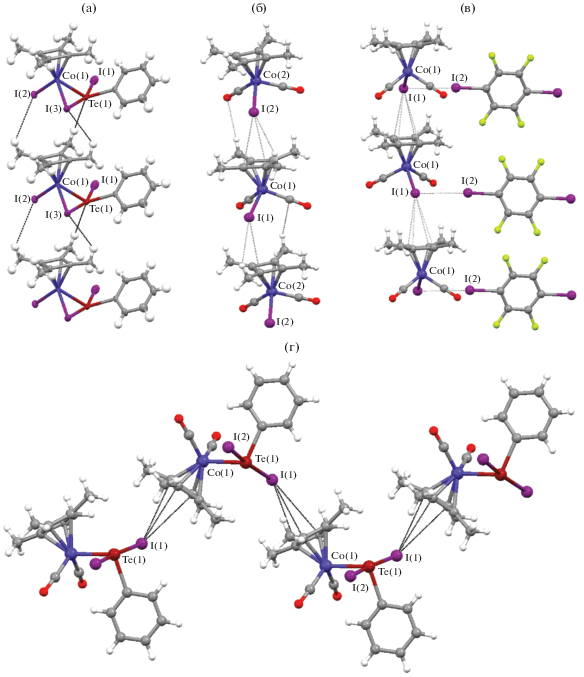
Рис. 3.
Энергетические структуры в кристаллах I (а), (η4-C4Me4)Co(CO)2I (б), (η4-C4Me4)Co(CO)2I···1,4-C6H4I2 (в) и (η4-C4Me4)Co(CO)2TeI2Ph (г), построенные на основании самых сильных межмолекулярных взаимодействий. Энергетическая структура строится из цилиндров, диаметр и направление которых отражает магнитуду энергии молекулярной упаковки в разных направлениях.
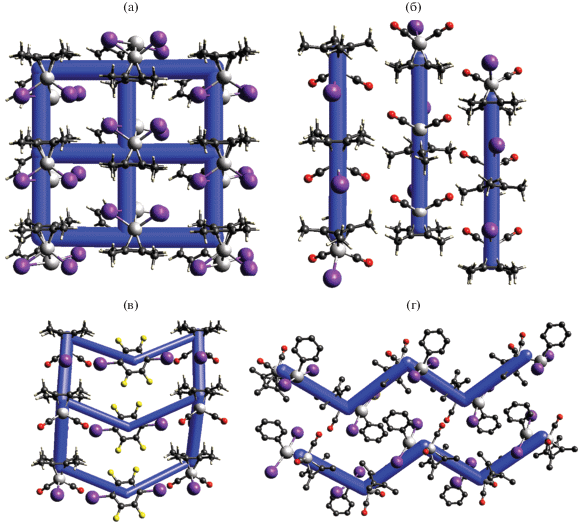
Рис. 4.
Цепочки молекул (η4-C4Me4)Co(CO)2TeIBrPh, ассоциированных преимущественно за счет взаимодействий I···(η4-C4Me4) (а не Br···(η4-C4Me4)!). Атомы водорода опущены для ясности: атомы галогенов показаны с максимальной заселенностью.
Координаты атомов и другие параметры структуры I депонированы в Кембриджском банке структурных данных (CCDC № 1991837; deposit@ccdc.cam.ac.uk или http://www.ccdc.cam.ac.uk/ data_request/cif).
Квантово-химические расчеты. Энергетическая структура в кристаллах I, (η4-C4Me4)Co(CO)2I, (η4-C4Me4)Co(CO)2I···1,4-C6H4I2 и (η4-C4Me4)- Co(CO)2TeI2Ph построена по данным межмолекулярных энергий, рассчитанных в CrystalExplorer 17.5 (TONTO, B3LYP-DGDZVP) [10] для всех уникальных молекулярных пар в первой координационной сфере молекулы, с использованием экспериментальной геометрии кристалла.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Рутинный РСА монокристаллов, полученных при перекристаллизации, показал, что за 10 лет хранения в негерметичных условиях, исходный 18-электронный комплекс (η4-C4Me4)Co(CO)2TeI2Ph не только заметно разложился, но и необычным образом трансформировался в 17-электронный (η4-C4Me4)CoI2(PhTeI) (I) (схема 2 ).
Схема 2 .
Как видно из схемы 2 , координация лиганда PhTeI в I напоминает предполагаемую структуру переходного комплекса в реакции внедрения PhTeI по связи Co–I в (η4-C4Me4)Co(CO)2TeI2Ph (схема 1 ), что можно считать косвенным доказательством возможности существования такого переходного состояния.
С целью наработки комплекса I в количествах, достаточных для изучения его физико-химических свойств, мы выяснили, что целенаправленно он может быть получен из раствора (η4-C4Me4)Co(CO)2TeI2Ph в толуоле при кипячении (без изоляции от внешней атмосферы) в течение 30 мин или интенсивном перемешивании в тех же условиях при 40°С в течение 12 ч.
Молекулярную структуру мономерного комплекса I можно представить как тетраметил-циклобутадиен-кобальтовый фрагмент, координирующий два одноэлектронных иодида и один двухэлектронный PhTeI-лиганд, стабилизированный за счет гипервалентого связывания Te···I с одним из концевых иодидных лигандов с короткими внутримолекулярными контактами Te···I (3.171 Å, рис. 1). Подсчет электронов в соответсвии с таким описанием представляет I как 17-электронный комплекс.
По сравнению с исходным (η4-C4Me4)Co(CO)2-TeI2Ph в I следует отметить небольшое увеличение растояния Со–Те (с 2.547 до 2.569 Å соответсвенно) и заметное укорочение расстояния Te–I (с ~2.95 до 2.777 Å соответсвенно). Кристаллическая структура I характеризуется отсутствием заметных межмолекулярных Te···I халькогенных связей (ХС). Характерные для кристаллов некоординированных органотеллургалогенидов межмолекулярные ХС сильно ослабляются при их координации с переходными металлами. Это происходит за счет конкуренции с внутримолекулярным галогенным связыванием Те···X (X = Br, I) и общего понижения электрофильности теллура при координации с металлом, усиленного обратным донированием M → Te) [4].
Интересно отметить общие мотивы в упаковке молекул I и (η4-C4Me4)Co(CO)2I в кристалле. В кристаллической структуре последнего, а также его сокристалла 1,4-С6F4I2 наблюдаются колонны из молекул, ассоциированных за счет межмолекулярных взаимодействий I···(η4-C4Me4) [5] (рис. 2б, 2в). Подобные колонны образуются за счет взаимодействий I…(η4-C4Me4) и Те···(η4-C4Me4) в кристалле I (рис. 2а), а в кристалле (η4-C4Me4)Co(CO)2TeI2Ph они стабилизируют зигзагообразную цепочку (рис. 2г), что позволяет говорить о супрамолекулярном синтоне [I···(η-π-лиганд)-М], определяющем дальний порядок упаковки [11].
При анализе упаковки кристалла всегда полезно помнить замечания К. Аакероя (редактора CrystEngComm c 2010 по 2019 г.) о субъективной природе видимых, но не подтвержденных расчетами мотивов упаковки [12, 13]. Другой член редколлегии CrystEngComm А. Гавецотти (c 2005 по 2008 г.) был еще более категоричен и настаивал на том, что никакой разумный журнал не должен больше принимать предложения типа “кристаллическая структура состоит из пар/цепочек/слоев, удерживаемых вместе такими-то взаимодействиями…” и аналогичные утверждения, если они не поддерживаются надежными энергетическими данными [14]. С появлением пакета программ Crystal Explorer [15], снабженного функцией Energy Framework (энергетическая структура) [16], которая позволяет эффективно рассчитать и наглядно представить энергетическую структуру кристалла, стало возможным не только находить энергетически обоснованные мотивы упаковки в кристалле, но и визуализировать супрамолекулярные синтоны [17] и супрамолекулярные реакции между ними [18]. Наши расчеты энергии парных межмолекулярных взаимодействий (TONTO/CE-B3LYP DGDZVP) в кристаллах I, (η4-C4Me4)Co(CO)2I, (η4-C4Me4)Co(CO)2I···1,4-C6H4I2 и (η4-C4Me4)Co(CO)2TeI2Ph и представление самых сильных из них в виде энергетической структуры (рис. 3а–3г) показали полное соответствие с I···(η4-C4Me4)-ассоциированными колоннами и зигзагами, предложенными выше (рис. 2).
В кристалле I энергия связывания в I···(η4-C4Me4)-ассоциированных цепочках (–9.3 ккал/моль) оказалась близка к энергии связывания между цепочками (–10.3 ккал/моль), но цепочки I···(η4-C4Me4) в (η4-C4Me4)Co(CO)2I, (η4-C4Me4)Co(CO)2I···1,4- C6H4I2 и зигзаги (η4-C4Me4)Co(CO)2TeI2Ph оказались наиболее сильно ассоциированными молекулярными агрегатами, заметно превосходящими другие. Интересно отметить, что в сокристалле (η4-C4Me4)Co(CO)2I···1,4···C6H4I2 энергия I···(η4-C4Me4)-связывания (–8 ккал/моль) даже превысила энергию межмолекулярного взаимодейтвия между галогенно-связанными (I···I) (η4-C4Me4)- Co(CO)2I и 1,4···C6H4I2 (–5.7 ккал/моль). Дисперсионные и электростатические силы вносят приблизительно равный вклад в общую энергию межмолекулярного I···(η4-C4Me4)-связывания в цепочках в I, (η4-C4Me4)Co(CO)2I, (η4-C4Me4)Co(CO)2I···1,4-C6H4I2 и зигзагах в (η4-C4Me4)Co(CO)2TeI2Ph.
Такие же зигзагообразные цепочки, как в (η4-C4Me4)Co(CO)2TeI2Ph (pис. 2г) наблюдаются и в изоструктурном ему гетерогалогенидном (η4-C4Me4)Co(CO)2TeIBrPh. Это наблюдение позволяет предположить, что в (η4-C4Me4)Co(CO)2TeIBrPh, для которого было отмечено разупорядочение позиций Br и I [5], вследствие заметной большей тенденции иода к образованию галогенных связей, должно наблюдаться преимущественное образование контактов I···(η4-C4Me4), а не Br···(η4-C4Me4). Это, в свою очередь, означает, что уточнение позиций атомов иода и брома должно проводиться со “свободной заселенностью”, а не 50/50, как в оригинальной статье [5]. И действительно, повторное уточнение структуры (η4-C4Me4)Co(CO)2TeIBrPh в таком режиме позволило понизить R1 c 3.36 до 3.01% и показало, что позиция галогена, контактирующего с (η4-C4Me4) на 80% заселена иодом, а отставшаяся (не имеющая таких контаков) – на 80% бромом (рис. 4). Это еще один важный пример того, как анализ галогенных связей может быть полезен в разрешении позиционной разупорядоченности в кристаллах [7, 19].
Наличие 17-электроного атома кобальта (S = 7/2) в окружении атомов иода (S = 5/2) в I позволяет ожидать необычное сверхтонкое расщепление сигнала в спектре ЭПР. Тем не менее измерения в растворе и твердом образце показали отсутствие разрешенной сверхтонкой структуры.
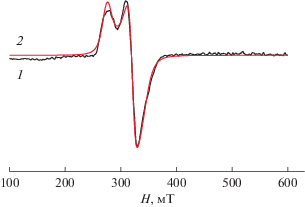
Спектр порошка соединения I при комнатной температуре представляет собой широкую неразрешенную линию с g = 2.25. Спектр раствора соединения I в толуоле при комнатной температуре представляет собой широкую неразрешенную линию с g = 2.228. Спектр раствора I в толуоле при низкой температуре (рис. 5) описывается ромбическим спиновым гамильтонианом (СГ)
Рис. 5.
Спектр раствора I в толуоле при Т = 100 К: экспериментальный спектр (1), симуляция с параметрами СГ (gz = 2.490, gx = 2.132, gy = 2.030) (2).
где gz, gx, gy – z, x, y компоненты g-тензора, Sz, Sx, Sy – проекции оператора спина на координатные оси, S = 1/2.
Параметры комплекса находили методом наилучшего приближения между экспериментальным и теоретическим спектром, который строили способом, описанным в [20]. В качестве функции формы линии использовали сумму функций Лоренца и Гаусса [21]. В ходе минимизации варьировали g-факторы, ширину и формы линий. Наилучшие параметры СГ приведены в подписи к рис. 5.
Таким образом, мы показали, что 17-электронный комплекс циклобутадиенил-кобальта I можно получить при разложении (η4-C4Me4)Co(CO)2TeI2Ph. Были определены параметры спинового гамильтониана комплекса методом наилучшего приближения между экспериментальным и теоретическим спектром. Также определены энергии связывания ассоциированных цепочек в кристалле. Учитывая важность 17-электронных комплексов кобальта в катализе, предполагается продолжить исследования в данном направлении.
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
Chirila P.G., Whiteoak C.J. // Dalton Trans. 2017. V. 46. P. 9721.
Suzuki Y., Sun B., Sakata K. et al. // Angew. Chem. Int. Ed. 2015. V. 54. P. 9944.
Shul’pin G.B., Loginov D.A., Shul’pina L.S. // Molecules. 2016. V. 21. P. 1593.
Torubaev Y., Pasynskii A., Mathur P. // Coord. Chem. Rev. 2012. V. 256. P. 709.
Torubaev Yu.V., Pasynskii A.A., Galustyan A.R. et al. // Russ. J. Coord. Chem. 2009. V. 35. № 1. P. 1. https://doi.org/10.1134/s1070328409010011
Torubaev Y.V., Lyssenko K.A., Barzilovich P.Y. et al. // CrystEngComm. 2017. V. 19. P. 5114.
Torubaev Y.V., Skabitskiy I.V., Rusina P. et al. // Cryst-EngComm. 2018. V. 20. P. 2258.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Ap-pl. Cryst. 2009. V. 42. P. 339.
Turner M.J., Thomas S.P., Shi M.W. et al. // Chem. Commun. 2015. V. 51. P. 3691.
Nangia A., Desiraju G.R. // Design of Organic Solids. Topics in Current Chemistry. Vol. 198 / Eds. Weber E. et al. Berlin, Heidelberg: Springer, 1998. P. 57–95. https://doi.org/10.1007/3-540-69178-2_2
Aakeroy C.B., Salmon D.J. // CrystEngComm. 2005. V. 7. P. 439.
Aakeroy C.B., Desper J., Elisabeth E. et al. // Z. Kristallogr. 2005. V. 220. P. 325.
Gavezzotti A. // CrystEngComm. 2013. V. 15. P. 4027.
Turner M.J., McKinnon J.J., Wolff S.K. et al. // Cryst. Explorer. 17. Univ. of Western Australia, 2017.
Turner M.J., Thomas S.P., Shi M.W. et al. // Chem. Commun. 2015. V. 51. P. 3691.
Torubaev Y.V., Skabitskiy I.V. // CrystEngComm. 2019. V. 46. P. 7057.
Torubaev Y.V., Rai D.K., Skabitsky I.V. et al. // New J. Chem. 2019. V. 43. P. 7941.
Aakeröy C.B., Chopade P.D., Desper J.et al. // Cryst. Growth Des. 2013. V. 13. P. 4145.
Ракитин Ю.В., Ларин Г.М., Минин В.В. // Интерпретация спектров ЭПР координационных соединений. М.: Наука, 1993. 339 с.
Лебедев Я.С., Муромцев В.И. // ЭПР и релаксация cтабилизированных радикалов. М.: Химия, 1972. С. 25.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия