Координационная химия, 2020, T. 46, № 7, стр. 387-401
Основные подходы к получению гетерометаллических металл-органических координационных полимеров
А. А. Сапьяник 1, 2, В. П. Федин 1, 2, *
1 Институт неорганической химии им. А.В. Николаева СО РАН
Новосибирск, Россия
2 Новосибирский национальный исследовательский государственный университет
Новосибирск, Россия
* E-mail: cluster@niic.nsc.ru
Поступила в редакцию 16.01.2020
После доработки 30.01.2020
Принята к публикации 31.01.2020
Аннотация
Химия металл-органических координационных полимеров (МОКП) интенсивно развивается в последние годы. Такие соединения образуют уникальные пористые структуры и демонстрируют интереснейшие функциональные свойства: селективная сорбция, магнитные, каталитические, люминесцентные и многие другие. Большинство изученных МОКП являются гомометаллическими. Гетерометаллические МОКП изучены гораздо меньше. Тем не менее введение гетерометалла не только позволяет направленно модифицировать свойства уже известных структур, но и позволяет получать принципиально новые структуры. Результаты исследований по изучению способов получения гетерометаллических металл-органических координационных полимеров обобщены в этом обзоре. Рассматриваются также основные структурные типы таких соединений и их функциональные свойства.
Металл-органические координационные полимеры (МОКП), представляют собой новый класс пористых материалов, состоящих из неорганических вторичных строительных элементов, которые соединены органическими лигандами (линкерами). Со времени первых сообщений о металл-органических каркасах в 1990-х гг. [1] в литературе сообщалось о многочисленных материалах на основе МОКП. Их выдающиеся и уникальные свойства привели к росту интереса к этим материалам. Пористые МОКП, сочетающие в себе несколько функций (таких как пористость и магнетизм, пористость и люминесценция), вызывают огромный интерес благодаря широким возможностям структурного дизайна и применения для “зеленой” ресурсосберегающей энергетики (например, хранение водорода или метана, а также улавливание CO2), люминесцентного сенсинга, разработки новых магнитных материалов и т.д.
Получение новых пористых каркасов с заданными свойствами является сложной задачей, поскольку функциональные свойства будут определяться тем, как неорганические и органические фрагменты взаимосвязаны в конечной структуре, что часто трудно предсказать. Поэтому ключевую роль играет выбор строительных блоков для узлов каркаса МОКП из молекулярных комплексов с уже известной геометрией узла. Помимо адсорбционных свойств, наличие других функциональных свойств гибридных пористых МОКП обычно обусловлено ионами металлов (например, для магнитных и для люминесцентных материалов). Особое место в таком случае занимают гетерометаллические строительные блоки, поскольку они позволяют более тонко варьировать функциональные особенности, обусловленные катионами металлов в структуре, например, гетерометаллические 3d–4f-МОКП могут выступать в качестве “single-molecule” магнитов или в качестве люминесцентных источников белого цвета [2].
В последние годы сочетание нескольких функциональных особенностей в одной структуре привлекает все больший интерес научного сообщества. Включение в один каркас молекул с несколькими линкерами [3, 4], нескольких различных металлов [5, 6], или сочетание этих двух подходов [7] – мощный инструмент для разработки материалов на основе МОКП. Таким образом, полученные материалы еще более специализированы для конкретных применений или могут использоваться в качестве многофункциональных материалов для одновременного выполнения различных задач. Смешивание различных металлов является важной концепцией гетерогенного катализа. Синергетический эффект дополнительных типов металлов известен на примере ферментов в природе, а гетерометаллические катализаторы широко используются в самых разнообразных каталитических реакциях [8]. Следовательно, объединение нескольких металлов в одну структуру МОКП должно улучшить свойства получаемого материала.
Термин гетерометаллические МОКП применяют к нескольким различным типам металл-органических полимерных структур: несколько катионов разных металлов входят в состав вторичного строительного блока; катионы разных металлов входят в состав разных строительных блоков, объединенных в одну структуру МОКП; катионы разных металлов входят в состав разных структурообразующих частей – катионы одних металлов в состав металлоцентра, а гетерометалла в состав металлолиганда; наконец, катионы металлов, отличных от тех, что входят в состав заряженного каркаса, могут быть включены в полости в качестве супрамолекулярных гостей. К настоящему времени реализовано несколько основных подходов для получения гетерометаллических МОКП:
1) постсинтетическая модификация МОКП за счет включения ионов других металлов в поры каркаса или постсинтетическая модификация с замещением части катионов металлов в каркасе на другие близкие по ионному радиусу катионы;
2) использование солей нескольких металлов в исходной реакционной смеси для получения гетерометаллических аналогов известных гомометаллических структур, где катионы разных металлов занимают эквивалентные структурные позиции;
3) использование металлолиганда, содержащего катион металла, отличный от структурообразующего каркас металла;
4) использование многокомпонентных смесей (содержащих источники как минимум двух разных катионов металлов) с целью включения этих катионов в структуру. В этом случае пытаются получить совершенно новые структуры в отличие от способа, указанного во втором пункте;
5) использование предсинтезированных полиядерных гетерометаллических комплексов для получения МОКП с заданной геометрией узлов.
Рассмотрим подробнее каждый из этих подходов.
ПОСТСИНТЕТИЧЕСКАЯ МОДИФИКАЦИЯ
Метод постсинтетической модификации каркасов уже успел получить достаточно широкое развитие в химии МОКП. Обычно таким способом модифицируют органические линкеры, за счет проведения реакций на функциональных группах этих лигандов для модификации функциональных свойств полимеров. Тем не менее, постсинтетически можно модифицировать и состав МОКП по катионам металлов. Здесь можно выделить несколько принципиально отличающихся друг от друга механизмов.
В первом случае катионы металла занимают определенные позиции в каналах/полостях уже полученного ранее пористых МОКП. Здесь удерживание катиона металла в определенном положении осуществляется за счет взаимодействий между донорными атомами органического линкера и введенным катионом металла. Так в работе [9] сообщается о получении гомометаллического МОКП [Ga(OH)(Btec)] ⋅ 0.5H2O, где H4Btec = = 1,2,4,5-бензолтетракарбоновая кислота (MIL-61). Поскольку исходный каркас является жесткой структурой, обладающей каналами и свободными карбоксильными группами, то оказалось возможным провести включение катионов Tb3+ и Cu2+ постсинтетической обработкой каркаса растворами солей соответствующих металлов. Получение гетерометаллического МОКП позволило существенно модифицировать функциональные свойства таких МОКП для диагностики рака простаты за счет детекции молекул саркозина. Дополнительное включение катионов Cu2+ не только регулирует люминесценцию Tb3+ за счет переноса заряда лиганд–металл, но также обеспечивает доступные участки для координации саркозина в каналах, что приводит к существенному снижению эффективности переноса заряда и тушению люминесценции при включении саркозина. В продолжении исследования включения катионов металлов в MIL-61 [10] авторы получили серию соединений включения с различными катионами лантанидов Ln-dopd-MIL-61 (Ln = Eu3+, Tb3+, Sm3+, Dy3+). Кроме характеристичной люминесценции Eu3+, Tb3+ было показано, что Sm-MIL-61 и Dy-MIL-61В проявляют очень слабые люминесцентные свойства. Тем не менее в присутствии катионов серебра в водном растворе наблюдается существенное разгорание люминесценции именно в случае Sm3+ и Dy3+, что можно использовать для создания сенсорных материалов для определения концентрации ионов серебра.
В [11] в качестве исходного МОКП использовали каркас на основе Zr4+ и 1,2,4,5-бензолтетракарбоновой кислоты. Далее по уже описанной схеме включали сначала катионы Eu3+, а затем Cu2+, которые по утверждениям авторов распределены на поверхности пор каркаса. Такая модификация позволила провести селективную детекцию мочевой тиогликолевой кислоты, биомаркера канцерогенного мономера винилхлорида в организме человека. Одной из ключевых особенностей является очень низкий предел обнаружения 89 нг/мл и высокая интенсивность люминесценции при включении аналита.
В [12] авторы модифицировали методику получения HKUST-1 ([Cu3(Btc)2], где H3Btc = 1,3,5-бензолтрикарбоновая кислота) для получения гетерометаллического аналога. В качестве допирующих реагентов использовали Zn(OAc)2 ⋅ 2H2O, RuCl3 ⋅ xH2O, Pd(OAc)2. Как было продемонстрировано, синтез без растворителя – подходящий и легкий путь для получения гетерометаллического аналога HKUST-1 таким образом, что содержание допирующего катиона металла можно контролировать согласно соотношению в смеси исходных реагентов. Все полученные соединения обладают хорошей кристалличностью и перманентной пористостью. Включение второго типа катионов металлов позволило существенно улучшить электрокаталитическую активность в реакциях восстановления CO2.
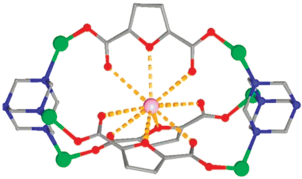
Альтернативным механизмом постсинтетической модификации для получения гетерометаллических каркасов является замещение катионов металлов в самой структуре полученных МОКП. Такое замещение обычно характерно в случае близких по размеру катионов. Частным случаем такого замещения можно считать замещение катионов гидроксония, которые компенсируют отрицательный заряд анионного каркаса. Например, в нашей работе было показано, что в анионном МОКП (H3O)2[Zn4(Ur)(HFdc)2(Fdc)4] (Ur = уротропин, H2Fdc = фуран-2,5-дикарбоновая кислота) [13] можно полностью заместить катионы гидроксония на различные катионы щелочных металлов (рис. 1). Это, в свою очередь, существенно влияет на интенсивность люминесценции образцов, а также на квантовые выходы и является основой для разработки сенсоров на щелочные металлы.
Рис. 1.
Криптандоподобная полость в структуре M2[Zn4(Ur)(HFdc)2(Fdc)4], содержащая катионы цинка – зеленым, катион щелочного металла – розовым. Adapted with permission from [13]. Copyright 2017, Wiley-VCH.
ИСПОЛЬЗОВАНИЕ СОЛЕЙ НЕСКОЛЬКИХ МЕТАЛЛОВ В ИСХОДНОЙ РЕАКЦИОННОЙ СМЕСИ
Этот способ для получения гетерометаллических МОКП – использование в исходной реакционной смеси солей разных металлов для получения гетерометаллических аналогов уже известных гомометаллических структур. Такой подход часто применяется для модификации свойств в известных МОКП, в частности для изменения магнитного поведения.
В [14] сообщается о получении биметаллических производных MOF-5 ([Zn4O(Bdc)3] (H2Bdc = = 1,4-бензолдикарбоновая кислота), для синтеза которых в исходной смеси используют нитрат цинка и ацетилацетонат железа(III). Полученная структура имеет морфологию MOF-5, в которой катионы цинка и железа занимают эквивалентные позиции и равномерно распределены в структуре. Введение ионов Fe3+ в MOF-5 создает координационно ненасыщенные центры, что приводит к преимущественной сорбции молекул воды по отношению к молекулам этанола. Пористая структура Fe(III)-MOF-5 обеспечивает свободную диффузию молекул воды. Таким образом, материалы на основе такого гетерометаллического соединения представляют интерес для создания высокоселективных мембран. Для модельной системы водного раствора этанола (90 мас. %), гибридная мембрана, содержащая Fe(III)-MOF-5, демонстрирует наивысшую эффективность разделения воды и этанола с коэффициентом разделения 3423 и потоком проникновения 1540 г/м2 ч, что намного выше, чем у гибридных мембран на основе гомометаллического MOF-5.
Смесь Co(NO3)2 ⋅ 6H2O, Zn(NO3)2 ⋅ 6H2O и метилимидазола в метаноле использовали для получения гетерометаллического МОКП с различным соотношением металлов в структуре [15]. Далее МОКП подвергался пиролизу, а полученный материал, содержащий Co3O4/ZnO, проявляет значительно лучшие каталитические характеристики при карбонилировании глицерина по сравнению с соответствующими оксидами, приготовленными из гомометаллических МОКП. В частности, выход на катализаторе Co50%Zn50% достиг 85% с конверсией 93% и селективностью ~91%. Эта каталитическая эффективность существенно выше, чем у большинства других гетерогенных катализаторов. В [16] также использовали смесь солей металлов для получения гетерометаллического МОКП. Здесь катионы Zn2+ или Cu2+ занимают место катионов Mn2+ в структуре STU-2[Mn(BIm)] (BIm = 1,2-бис((5H-имидазол-4-ил)-метилен)гидразин) [17, 18]. Допирование привело к улучшению каталитической активности реакции цианосилилирования различных ароматических альдегидов для Zn0.29-STU-2 при комнатной температуре.
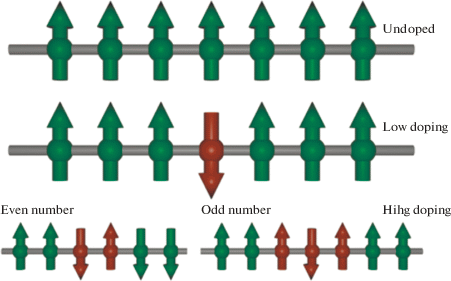
Получено [19] семейство гетерометаллических аналогов MOF-74 [M2(Dhtp)(H2O)2] (M = Mg, Mn, Fe, Co, Ni, Zn; Dhtp = 2,5-дигидрокситерефталат-анион). Co-, Fe- и Ni-MOF-74 демонстрируют слабые ферромагнитные взаимодействия между цепочками из атомов металла в структуре. Было показано, что для NiFe-MOF-74 характерно ферромагнитное упорядочение. Введение катионов Fe3+ позволяет модулировать начало спонтанной намагниченности между 10 и 16 K благодаря контролируемому появлению антиферромагнитных взаимодействий между цепочками (рис. 2).
Рис. 2.
Предлагаемые изменения спиновой конфигурации магнитных цепей в MOF-74 при легировании железом. Никель (зеленый), железо (оранжевый). Reprinted with permission from [19]. Copyright 2017, American Chemical Society.
Интересным примером является работа [20]. Исследователи пытались не просто получить гетерометаллический каркас, но гетерогенный кристалл, состоящий из двух родственных полимеров ZIF-8/67([M(2-MIm)2], где M = Zn для ZIF-8 и Co для ZIF-67, 2-MIm = 2-метилимидазол). Показано, что когда в исходном реакционном растворе присутствуют ионы Co2+ и Zn2+, гомогенное распределение двух металлов достигается только при высоком отношении Co/Zn, а при низком соотношении Co/Zn наблюдается градиент концентрации от обогащенных кобальтом ядер к оболочкам, обогащенным цинком.
ИСПОЛЬЗОВАНИЕ МЕТАЛЛОЛИГАНДОВ
Этот способ получения гетерометаллических МОКП заключается в использовании металлолиганда, содержащего катион металла, отличный от структурообразующего каркас металла.
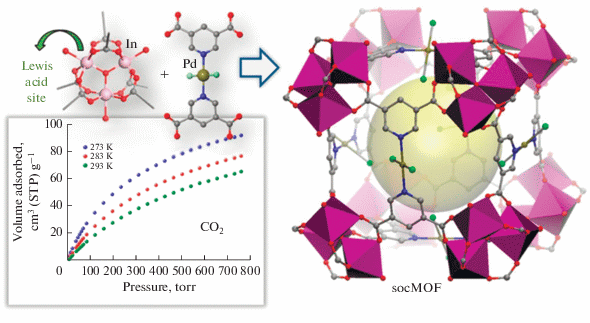
В [21] получили гетерометаллические In/Pd МОКП, в которых катионы In3+ находятся в трехядерном гексакарбоксилатном узле {In3O(COO)6}, а палладий включен в металлолиганд транс-[PdCl2(Рdc)2] (H2Рdc = пиридин-3,5-дикарбоновая кислота). Каркас [In3O(Рdc)1.5(H2O)2Cl] трехмерный и перманентно пористый, показывающий высокую гравиметрическую (92.3 см3 г–1) и объемную (120.9 см3 см–3) емкость по сорбции CO2 при 273 К и 1 бар (рис. 3), а также высокую селективность для разделения смеси CO2/CH4 (фактор селективности 15.4 для молярной смеси 50 : 50) и CO2/N2 (фактор селективности 131.7 для молярной смеси 10 : 90) с умеренной теплотой адсорбции для СО2 (29.8 кДж/моль). Второй каркас [(Me2NH2)In(Рdc)] также трехмерный с топологией сульфида платины PtS.
Рис. 3.
Узел {In3O(COO)6} и металлолиганд транс-[PdCl2(Рdc)2] в структуре МОКП и сорбция диоксида углерода при разной температуре. Reprinted with permission from [21]. Copyright 2018, American Chemical Society.
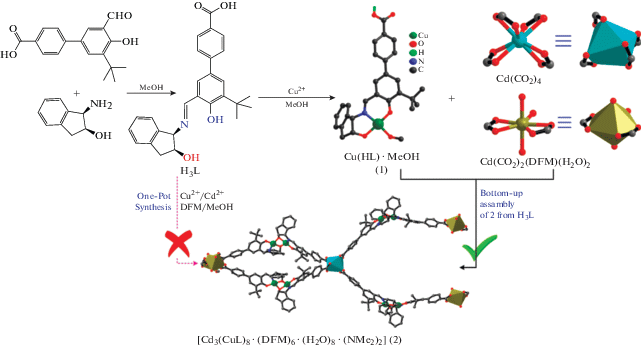
В [22] в качестве металлолиганда использовали [Cu(HL)] (рис. 4), который в реакции с бромидом кадмия дает 2D-МОКП [Cd3(CuL)8(Dmf)6 (H2O)8-(NMe2)2], служащий гетерогенным катализатором в реакциях Генри и Фриделя–Крафтса.
Рис. 4.
Схема получения МОКП [Cd3(CuL)8(Dmf)6(H2O)8(NMe2)2]. Reprinted with permission from [22]. Copyright 2018, American Chemical Society.
Работа [23] интересна с топологической точки зрения. В качестве строительных блоков в ней использовали тетра- и дикарбоксилатные лиганды на основе меди и кобальта (рис. 5). Их сочетание с кластерами [Zr6(μ3-O)4(μ3-OH)4(CO2)12] и [Hf6(μ3-O)4(μ3-OH)4(CO2)12] позволило получить восемь новых гетерометаллических МОКП со сложной топологией.
Рис. 5.
Металлолиганды из работы. Adapted with permission from [23]. Copyright 2018, American Chemical Society.
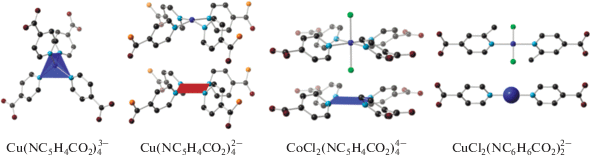
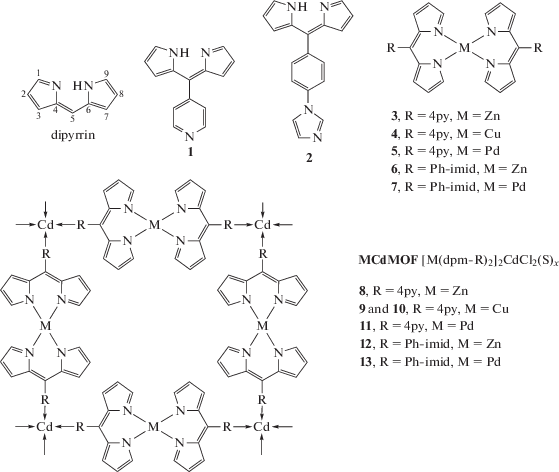
Похожие дипирриновые (Dpm) металлолиганды на основе катионов различных металлов (схема 1 ) [24] в реакциях с хлоридом кадмия позволили получить несколько гетерометаллических МОКП [{M(Dpm)2}2CdCl2(Solv)x]. Отличительной особенностью от предыдущей работы является то, что в структуре лигандов вместо карбоксильной группы присутствует N-донорный атом в ароматическом кольце и катионы цинка и кадмия связаны в трехмерном каркасе только за счет N-донорных лигандов. Также важно отметить, что полученные каркасы можно синтезировать исходя из смеси солей металлов и дипирриновых линкеров.
Схема 1 . Дипирриновые лиганды 1 и 2, металлолиганды 3−7, использованые для синтеза MCdМОКП 8−13. Reprinted with permission from [24]. Copyright 2013, American Chemical Society.
ИСПОЛЬЗОВАНИЕ МНОГОКОМПОНЕНТНЫХ СМЕСЕЙ ДЛЯ ПОЛУЧЕНИЯ НОВЫХ ГЕТЕРОМЕТАЛЛИЧЕСКИХ МОКП
Еще один способ, с помощью которого можно получить гетерометаллические МОКП – использование многокомпонентных смесей, содержащих источники как минимум двух разных катионов металлов. Этот подход не позволяет точно предсказать, будут ли образовываться гетерометаллические узлы или же катионы разных металлов будут изолированы и отделены друг от друга в структуре, образуя разные типы гомометаллических узлов. Тем не менее такой простой в исполнении способ используется наиболее часто.
Гетерометаллические МОКП [{Yb6Cu12(OH)4-(Рyc)12(H2O)36} · (NO3)14 ⋅ xS] (QUST-81) и [{Yb4O(H2O)4Cu8(OH)8/3(Рyc)8(HCOO)4} ⋅ (NO3)10/3] (QUST-82) (H2Рyc = 1H-пиразол-4-карбоновая кислота) впервые использовали для эффективного удаления гетероциклических сераорганических соединений из моторного топлива [25]. МОКП QUST-81 получен в сольвотермальных условиях нагреванием смеси нитратов Yb(III) и Cu(II) с пиразолкарбоновой кислотой в смеси диметилформамид–диметилацетамид–N-метил-2-пирролидон при 100°C. МОКП QUST-82 получен при повторном нагревании кристаллов QUST-81 в исходной реакционной смеси при 120°C. В структурах обоих координационных полимеров присутствует по два типа узлов. В случае QUST-81 – это {Yb2(COO4)4(H2O)8} и {Cu3(OH)(PyC)3}, для QUST-82 – {Yb4O(COO)8(H2O)4} и {(Cu3(OH)- (PyC)3)8(HCOO)12}. Узлы связываются с образованием трехмерных пористых каркасов.
Соединение [Zn2(L)K2(μ2-H2O)2(μ2-SCN)4] (H2L = бис(пиридин-2-альдегид) тиокарбазон) [26] было получено из смеси ацетата цинка, тиоцианата калия и H2L в метаноле при нагревании. Структура содержит два типа катионов металлов, которые не связаны друг с другом карбоксилатными мостиками, а образуют два типа гомометаллических узлов {K2(μ2-H2O)2} и катионы цинка в тетраэдрическом окружении донорных атомов лигандов.
Четыре новых гетерометаллических МОКП [Zn4Ln2(Imdc)4(SO4)(H2O)8] ⋅ 4H2O (Ln = Nd, Sm, Eu, Gd; H3Imdc = имидазол-4,5-дикарбоновая кислота) получили гидротермально в реакциях Ln2O3 с имидазол-4,5-дикарбоновой кислотой и ZnSO4 · 7H2O [27]. Как и в предыдущих случаях катионы металлов не образуют гетерометаллических узлов, а изолированы друг от друга на длину линкера. В каркасе есть два структурно независимых катиона цинка, отличающихся координационным числом (КЧ4 и 6). Катион лантанида координирован девятью атомами кислорода карбоксильных групп лиганда и координированных молекул воды. Интересной особенностью полученных гетерометаллических соединений является возможность селективной детекции I– в растворе за счет тушения люминесценции.
МОКП [H(H2O)8][DyZn4(Imdc)4(Im)4] (H3Imdc = = 4,5-имидазолдикарбоновая кислота, Im = имидазол) [28] демонстрируют возможность варьирования люминесцентных свойств в зависимости от длины волны возбуждения, в том числе показывая белую люминесценцию. Синтез вели исходя из хлорида диспрозия и ацетата цинка. Катионы металла изолированы в структуре имидазолдикарбоксилат-анионами. В [29] МОКП (Me2NH2)5-[In3Zn6(μ3-OH)2(Bptc)6] получили из нитратов индия и цинка в реакции с бифенил-3,3',5,5'-тетракарбоновой кислотой (H4Bptc). В структуре присутствует два типа вторичных строительных гомометаллических блоков {In(COO)4} и {Zn3(μ3-OH)(CO2)6}. В трехмерной структуре каркаса присутствует система полостей, обеспечивающая возможность сорбции, хранения и разделения газов. Площадь поверхности, измеренная методом БЭТ, составила 1200 м2/г, а селективность разделения газовых смесей C2H2/N2 и CO2/N2 (v : v = = 15 : 85) – 103.2 и 17.0 при 1 атм и 273 K.
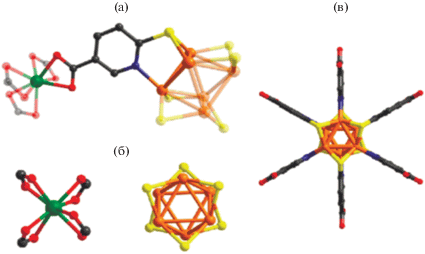
Хлорид индия(III) и иодид меди(I) использовали для получения гетерометаллического МОКП [(CH3)2NH2)InCu4L4] · MeCN · H2O (H2L = = 6-меркаптопиридин-3-карбоновая кислота) [30]. Структура содержит два типа гомометаллических узлов – моноядерный {In(COO)4} и гомоядерный {Cu6S6} (рис. 6). Благодаря своей пористой структуре и анионному типу каркаса, соединение демонстрирует возможность селективного отделения C2 углеводородов от метана, а также может сорбировать ртуть(II) из этанольного раствора.
Рис. 6.
Координационное окружение лиганда L2 (a); четырехсвязный узел In(COO)4 и кластер {Cu6S6} (б); гексадентатный металлолиганд в структуре {[(CH3)2NH2]InCu4L4 ⋅ MeCN ⋅ H2O} (в). Reprinted with permission from [30]. Copyright 2016.
МОКП (H3O)3[Gd3Mn2(Тrz)4] ⋅ 12H2O (H4Trz = = триc(1H-тетразол-5-ил)метанол) содержит в своей структуре шестиядерный кластер {Gd6O8} [31]. Кристаллы этого соединения получили смешиванием GdCl3 ⋅ 6H2O, MnCl2 ⋅ 4H2O, KC4N3, NH4F, NaN3, H2O и MeOH (v : v = 3 : 1), полученную смесь нагревали при 145°C 3 суток. Магнитные измерения показывают, что соединение является хорошим кандидатом на роль магнитных теплоносителей в низкотемпературном поле.
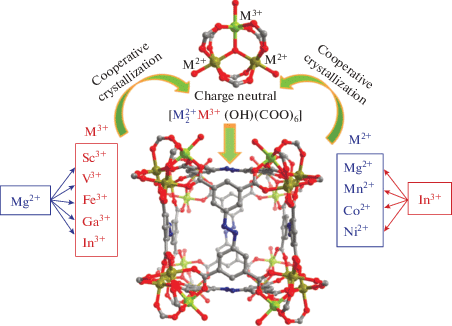
Далее рассматриваются примеры, когда в полиядерном вторичном строительном блоке содержится по крайней мере два разных катиона металлов. В [32] авторы фокусируют свое внимание на семействе гетерометаллических МОКП, которые, по их мнению, сложно получить, поскольку они состоят из ионов металлов, которые сильно отличаются по своим свойствам, например Mg2+ и V3+ или Ni2+ и In3+. Важной особенностью синтеза является использование большого избытка соли катиона M2+, так как при использовании близких к эквимолярному соотношений металлов образуется рентгеноаморфный продукт. Катионы металлов занимают кристаллографически эквивалентные места. Катионы металлов в структуре образуют трехъядерный {MII2MIII(μ3-OH)(CO2)6} узел (рис. 7), а в трехмерной структуре полученных МОКП CPM-200 есть система каналов. Соединения демонстрируют высокую пористость (БЭТ от 877 до 1459 м2/г) и могут быть использованы в качестве сорбентов для хранения CO2 и H2.
Рис. 7.
Общая схема получения узла {${\text{M}}_{{\text{2}}}^{{{\text{II}}}}$MIII(μ3-OH)(CO2)6} в структуре гетерометаллического CPM-200 МОКП. Reprinted with permission from [32]. Copyright 2016, American Chemical Society.
На основе изоструктурных гетеро- и гомометаллических МОКП [NH2(CH3)2][M3(μ3-OH)(H2O)3-(Bhb)] (M3 = Co3, Co2Ni, CoNi2, Ni3; H6Bhb = = 4,4',4"-бензол-1,3,5-триилгексабензойная кислота) [33] провели электрокаталитическое выделение кислорода в 0.1 М КОН электролите. Показано, что кинетика для биметаллических катализаторов более эффективна по сравнению с их гомометаллическими аналогами. Гетерометаллические блоки {M2M'O(COO)6} получили исходя из солей металлов, взятых в стехиометрическом соотношении.
В [34] на основе тримезат-аниона был получен ряд гомо- и гетерометаллических МОКП. Интересной структурной особенностью полученных соединений является присутствие спиральной оси вращения, соответственно все каркасы кристаллизуются в хиральной группе симметрии (рис. 8). Соединения [Zn(HBtc)(H2O)], Li4[Cd2(HBtc)- (Btc)2], [CoLi(Btc)(Dma)2], [CdLi2(Btc)4/3(H2O)3], Li2[Zn3Li5(Btc)4(Mtaz)(H2O)4] (Mtaz = 5-метилтетразол) получены при варьировании соотношения солей исходных металлов в реакции с органическими лигандами в сольвотермальных условиях. Хиральные кристаллы на основе Cd(II) и Zn(II) демонстрируют интересные нелинейные оптические свойства.
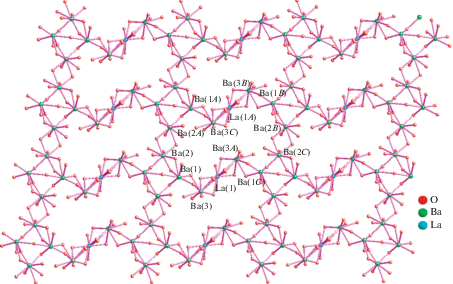
В [35] использовался жесткий асимметричный трикарбоксилатный лиганд (H3L = p-терфенил-3,4",5-трикарбоновая кислота) для получения гетерометаллического щелочноземельно-лантанидного микропористого люминесцирующего МОКП [Ba3La0.5(μ3-L)2.5(H2O)3(Dmf)] · 3DMF. Синтез вели в сольвотермальных условиях из смеси нитратов металлов с кислотой H3L в растворе DMF–H2O (1 : 1) с добавлением небольшого количества азотной кислоты. В структуре есть три типа катионов бария, отличающихся координационным окружением, а также один тип катионов лантана. Эти катионы образуют гетерометаллический остов в структуре (рис. 9). Для полученного соединения изучали люминесцентный отклик на включение различных катионов из водных растворов. Оказалось, что включение катионов Al3+ и анионов ${\text{MnO}}_{4}^{ - }$ приводит к частичному тушению люминесценции уже при достаточно низких концентрациях (10–3 и 10–4 моль/л соответственно).
Рис. 9.
Гетерометаллический остов структуры [Ba3La0.5(μ3-L)2.5(H2O)3(DMF)] · 3DMF. Reprinted with permission from [35]. Copyright 2016, American Chemical Society.
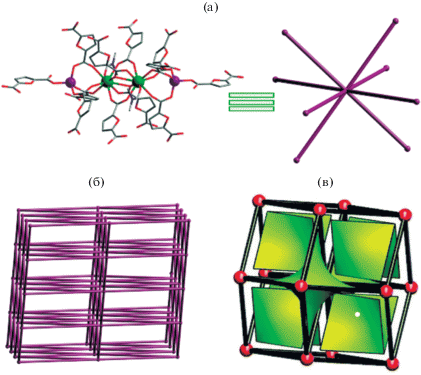
Гетерометаллические МКОП [In0.5K(3-Qlc)Cl1.5(H2O)0.5]2n и [InK(Ox)2(H2O)4] (3-HQlc = = хинолин-3-карбоновая кислота; H2Ox = щавелевая кислота) [36] получили исходя из KOH и хлорида или нитрата индия(III) соответственно. Оба МОКП содержат в своей структуре гетерометаллический узел (рис. 10). Полученные соединения демонстрируют изменение твердотельной люминесценции от синей до желтой и белой при изменении температуры.
Рис. 10.
Общая схема получения и структуры гетерометаллических МОКП. Reprinted with permission from [36]. Copyright 2016, American Chemical Society.
В серии изоструктурных МОКП [Ln2Ni(OAc)5-(HL)(L)] (H2L = 2-гидроксиимино-N-[1-(2-пиразинил)этилдиен]пропаногидразон, Ln = Dy, Tb, Gd) [37] координационный узел гетерометаллический и катионы разных металлов связаны друг с другом через мостиковый кислород. Синтез соединений вели из нитрата никеля(II) и ацетатов соответствующих Ln(III). Полученные соединения микропористые и могут обратимо сорбировать диоксид углерода, а также демонстрируют высокую селективность для разделения CO2/N2 и CO2/CH4 (фактор селективности до 98.8 и 16.8 при 298 K и 100 кПа). Антиферромагнитные взаимодействия как для МОКП на основе Dy, так и для Tb, а ферромагнитное взаимодействие для Gd наблюдаются при низкой температуре в результате конкуренции магнитной анизотропии и интерметаллического ферромагнитного суперобмена. Кроме того, МОКП на основе Dy демонстрирует медленную релаксацию намагниченности при нулевом поле постоянного тока, тогда как МОКП на основе Gd демонстрирует значительный криогенный магнитокалорический эффект с максимальным изменением энтропии 26.6 Дж кг–1 К–1 при 3.0 К.
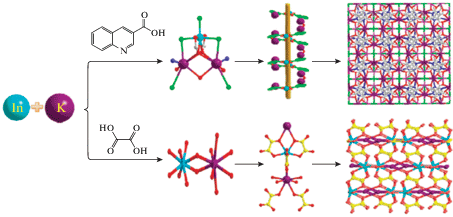
Гетерометаллический МОКП [NaEu2(Tatab)2-(DMF)3]OH (H3Tatab = 4,4',4"-s-триазин-1,3,5-триилтри-м-аминобензойная кислота) получен исходя из нитрата европия(III) и Na3Tatab [38]. Гетерометаллический узел в структуре представляет собой гексакарбоксилатный трехъядерный линейный фрагмент {NaEu2(COO)6(DMF)6} (рис. 11). Соединение проявляет высокую гидролитическую стабильность. Были проведены эксперименты по люминесцентной детекции антибиотиков и различных ароматических соединений. Показано, что происходит тушение люминесценции при включении оридазола, нитрофенола и бензилового спирта.
Рис. 11.
Гетрометаллический узел в структуре [NaEu2(Tatab)2(DMF)3] · OH. Adapted from [38] with permission from The Royal Society of Chemistry.
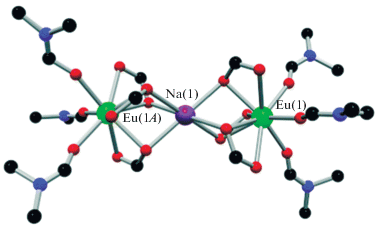
Два изоструктурных каркаса [(CH3)2NH2]2-[Zn2Ln2(Fda)6(DMF)2] ⋅ 2DMF (Ln = Eu, Tb; H2Fda = фуран-2,5-дикарбоновая кислота) в своей структуре содержат тетраядерный карбоксилатный узел [39] (рис. 12). В трехмерной структуре такие узлы связаны в Bcu-топологию. В качестве источников катионов металлов использовали соответствующие нитраты, сам синтез вели в сольвотермальных условиях в DMF. Эти МОКП демонстрируют превосходную стабильность в различных растворителях и являются перспективными материалами для создания сенсоров на быстрое и высокоселективное обнаружение анилина.
Рис. 12.
a – восьмисвязный узел {Zn2Ln2(COO)10} в Zn-Eu: Zn – фиолетовый, Eu – зеленый, O – красный, N – синий, C – черный; б – Bcu-топология структуры Zn-Eu; в – полости в структуре. Reproduced from [39] with permission from The Royal Society of Chemistry.
СИНТЕЗ НА ОСНОВЕ ПРЕДСИНТЕЗИРОВАННЫХ ГЕТЕРОМЕТАЛЛИЧЕСКИХ КОМПЛЕКСОВ
Наиболее распространенный подход к синтезу гетерометаллических координационных полимеров подразумевает использование смеси солей различных металлов, а формирование гетерометаллических строительных блоков происходит in situ в процессе роста кристаллов. Однако во многих случаях такие гетерометаллические строительные блоки известны в качестве дискретных полиядерных комплексов с монотопными лигандами; такие комплексы хорошо растворимы и достаточно стабильны, для того чтобы сохранить структуру в процессе замещения монотопного лиганда политопным для создания полимерной структуры соединения. Таким образом, синтез определенных координационных полимеров можно рационализировать посредством выбора соответствующего предсинтезированного растворимого полиядерного комплекса. Получение МОКП на основе предсинтезированных гетерометаллических комплексов, по нашему мнению, наиболее перспективно. Несмотря на очевидные преимущества, с точки зрения контроля и предсказания структуры и свойств получаемых МОКП, такой подход до сих пор используется достаточно редко. В литературе есть только единичные примеры, а систематическое изучение использования гетерометаллических молекулярных комплексов в качестве источника гетерометаллических узлов в структуре МОКП ранее не проводилось. Недавно опубликован обзор, посвященный известным примерам для такого подхода [40], в котором, однако, в основном затронуты примеры использования монометаллических полиядерных комплексов.
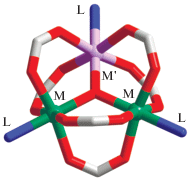
В лаборатории химии координационных полиядерных соединений ИОНХ РАН были разработаны оригинальные подходы к получению гетерометаллических пивалатных комплексов, которые в дальнейшем использовались для синтеза координационных полимеров. Один из наиболее интересных примеров – трехъядерные карбоксилатные комплексы [M3O(RCOO)6L3] (рис. 13), полученные для большого ряда металлов. Рост полимерной структуры в данном случае может осуществляться как замещением монотопных карбоксилатов на политопные, так и использованием электронейтральных политопных линкеров, способных координировать катионы металла с замещением L. Более того, ядро является хорошей платформой для получения многочисленных гетерометаллических комплексов [M'M2O(RCOO)6(L)3]), обычно на основе ряда 3d-металлов. Такие комплексы – очень удобные исходные материалы для рационального дизайна гетерометаллических координационных полимеров, и многие такие примеры были успешно продемонстрированы в ИОНХ РАН.
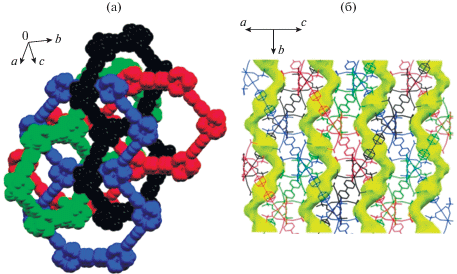
Было предложено использовать политопные донорные мостиковые линкеры различной геометрии для соединения гетерометаллических пивалатных комплексов [M'M2O(Рiv)6(HРiv)3] (Рiv = = ButCOO–) при направленном синтезе МОКП. Так, в [41] два изоструктурных координационных полимера [Fe2MO(Piv)6(Bpy)3/2] (M = Ni2+ или Co2+) были получены за счет связывания соответствующих трехъядерных гетерометаллических пивалатов с линейными линкерами Bpy. Полученные слои с топологией hcb упакованы в пористую взаимопроросшую структуру с зигзагообразными каналами (рис. 14). Микропористая природа этих МОКП была подтверждена измерениями изотерм адсорбции N2 и H2 (SBET = 520 м2 г–1 для M = Ni, SBET = 273 м2 г–1 для M = Co).
Рис. 14.
a – взаимопрорастание 2D-слоев (t-Bu группы пивалат-анионов и атомы водорода не показаны); б – визуализация каналов. Adapted with permission from [41]. Copyright 2017, Wiley-VCH.
Структуры трехъядерных гетерометаллических пивалатных комплексов сохраняются в координационных полимерах. Магнитное поведение [Fe2MO(Piv)6(Bpy)3/2] определяется обменными взаимодействиями в трехъядерных блоках [42]. Кроме того, кристаллические структуры пористых координационных полимеров [Fe2MO(Piv)6(Bpy)3/2] оказались гибкими с точки зрения изменения расстояний между слоями, что привело к изменению объема пор. Такие изменения полностью обратимы и вызваны заменой растворителя. Было обнаружено сильное различие между сорбцией алканов и спиртов: хотя изотермы сорбции алканов (н-гексан и н-октан) типичны для микропористых сорбентов, адсорбция спиртов (метанол и этанол), вероятно, была связана со структурными перегруппировками. Более высокая сорбционная емкость для этанола по сравнению с метанолом согласуется с гидрофобной природой каналов.
[Fe2NiO(Piv)6(Bpy)3/2] комплекс использовали для получения обширной серии полимерных структур с использованием различных тритопных азотсодержащих линкеров [43, 44]. Для полученных соединений продемонстрирована перманентная пористость по изотермам сорбции азота и водорода при 78 K. Кроме того, пористый координационный полимер [Fe2NiO(Piv)6(L2)] (L2 = 4-(4-N,N-диметиламинофенил)-2,6-бис(4-пиридил) пиридин) использовали в качестве гетерогенного катализатора для конденсации салицилового альдегида или 9-антраценкарбальдегида с малононитрилом. Наилучшая активность наблюдалась в случае салицилового альдегида, что приводило к его превращению в 2-имино-2Н-хромен-3-карбонитрил с высоким выходом.
Связывание фрагмента трехъядерного комплекса [Fe2CoO(Piv)6] редокс-активным мостиком [Ni(L6)2] (L6H представляет собой основание Шиффа, полученного из гидразида 4-пиридинкарбоновой кислоты и 2-пиридинкарбальдегида) дает новый пористый координационный полимер [{Fe2CoO(Piv)6}Ni(L6)2}]+ [45]. Кристаллическая решетка этого соединения построена из 2D-слоев, где каждый лиганд [Ni(L6)2] связывает два слоя [Fe2CoO(Piv)6]. Магнитные свойства координационного полимера в основном зависят от магнетизма отдельных компонентов: трехъядерного пивалата и мостика [Ni(L6)2], поскольку взаимодействия между этими компонентами незначительны
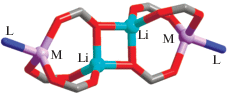
В кристаллической структуре [Li2M2(RCOO)6L2] каждый катион Li+ находится в тетраэдрическом окружении, в то время как каждый более тяжелый металл может иметь КЧ 4 или 5 в зависимости от природы этого металла и аксиальных лигандов L (рис. 15). Хорошо развитая координационная химия таких четырехъядерных молекулярных комплексов делаeт их привлекательным строительным блоком для рационального получения гетерометаллических координационных полимеров.
На основе таких пивалатных комплексов была получена обширная серия новых гетерометаллических МОКП. Наиболее яркими представителями полученного класса соединений являются две серии изоретикулярных каркасов [LiM(Btb)(Solv)2] (M = Zn2+ или Co2+, H3Btb = 1,3,5-трискарбоксифенилбензол) [46] и [Li2Zn2(R-Bdc)3(Bpy)] (R-заместитель в терефталатномлиганде) [47].
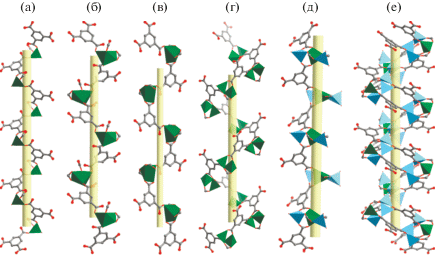
Был получен ряд слоистых и трехмерных координационных полимеров, где четырехъядерный фрагмент распадается на два идентичных гетерометаллических трикарбоксилатных фрагмента {LiM(RCOO)3} [46, 48]. Использование трикарбоксилатных органических линкеров различной геометрии позволило тонко варьировать размерность полученных координационных полимеров. В случае слоистых соединений их структурная устойчивость существенно увеличивается благодаря дополнительным взаимодействиям между ароматическими системам линкеров соседних слоев, образуя так называемую супрамолекулярную 3D-структуру с одномерными каналами (рис. 16).
Рис. 16.
Вторичный строительный блок в [LiZn(Btb)(DMF)2] (a); стабилизация слоев (б); визуализация каналов в структуре (в).
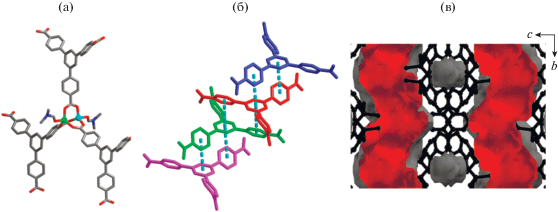
Благодаря такой стабилизации соединения [LiM(Btb)(Solv)2] достаточно стабильны при удалении гостевых молекул и демонстрируют перманентную пористость, показанную по изотермам сорбции CO2 при 195 K. Поскольку каналы оказались узкими, то соединения также представляют интерес для разделения таких газовых смесей, как CO2/N2 и CO2/CH4, поскольку не сорбируют азот и метан. В структуре соединений [Li2Zn2(R-Bdc)3-(Bpy)] важно отметить, что это один из немногих уникальных примеров, когда при синтезе сохраняется не только геометрия изначального тетраядерного фрагмента, но также удается заместить все карбоксилатные линкеры и монотопные донорные пиридиновые линкеры на дитопный Bpy (рис. 17). В трехмерной структуре присутствует система широких каналов, диаметр которых зависит от размера заместителя в бензольном кольце терефталат-аниона. В случае наибольшего заместителя – нитро группы – некоторые боковые каналы оказываются полностью блокированными, превращая систему каналов в изолированные одномерные каналы. Соединения перманентно пористы и обладают площадью поверхности от 450 до 1200 м2/г (измерено методом BET). Благодаря функционализации внутренней поверхности пор за счет использования терефталат-аниона с заместителями в бензольном кольце, соединения могут быть использованы для разделения различных смесей, включая промышленно важное разделение бензола и циклогексана.
Рис. 17.
Вторичный строительный блок в структуре [Li2Zn2(Bdc)3(Bpy)] [47] (a); проекция структуры перпендикулярно каналам (б).
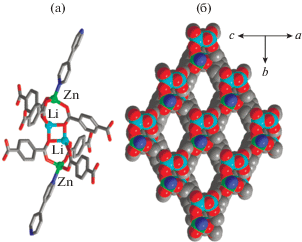
Работа с гетерометаллическими комплексами продолжается. Показана возможность использования и других исходных фрагментов {M2Ln} [49]. Данная область исследований выглядит впечатляюще перспективной, поскольку предоставляет возможность для структурного дизайна нового класса координационных полимеров.
В заключение необходимо отметить, что химия гетерометаллических металл-органических координационных полимеров открывает возможности не только для модификации свойств уже известных гомометаллических координационных полимеров, но и позволяет получить новые уникальные серии соединений с интересными сорбционными, оптическими, магнитными и другими функциональными свойствами. При использовании предсинтезированных гетерометаллических комплексов можно вести направленный синтез МОКП с заданной структурой гетерометаллического ядра, что существенно упрощает процесс получения новых гетерометаллических МОКП.
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
Hoskins B.F., Robson R. // J. Am. Chem. Soc. 1990. V. 112. № 4. P. 1546.
Barsukova M.O., Sapchenko S.A., Dybtsev D.N., Fedin V.P. // Russ. Chem. Rev. 2018. V. 87. № 11. P. 1139.
Qin J.-S., Yuan S., Wang Q. et al. // J. Mater. Chem. A. 2017. V. 5. № 9. P. 4280.
Bunck D.N., Dichtel W.R. // Chem. Eur. J. 2013. V. 19. № 3. P. 818.
Burrows A.D. // CrystEngComm. 2011. V. 13. № 11. P. 3623.
Dhakshinamoorthy A., Asiri A.M., Garcia H. // Catal. Sci. Technol. 2016. V. 6. № 14. P. 5238.
Fei H., Cahill J.F., Prather K.A., Cohen S.M. // Inorg. Chem. 2013. V. 52. № 7. P. 4011.
Yu W., Porosoff M.D., Chen J.G. // Chem. Rev. 2012. V. 112. № 11. P. 5780.
Sun N.-N., Yan B. // Analyst. 2018. V. 143. P. 2349.
Sun N., Yan B. // Phys. Chem. Chem. Phys. 2017. V. 19. P. 9174.
Hao J.-N., Xu X.-Y., Lian X. et al. // Inorg. Chem. 2017. V. 56. № 18. P. 11176.
Perfecto-Irigaray M., Albo J., Beobide G. et al. // RSC Adv. 2018. V. 8. № 38. P. 21092.
Sapchenko S.A., Demakov P.A., Samsonenko D.G. et al. // Chem. Eur. J. 2017. V. 23. № 10. P. 2286.
Cheng X., Jiang Z., Cheng X. et al. // J. Memb. Sci. 2018. V. 545. P. 19.
Lü Y., Jiang Y., Zhou Q. et al. // J. Solid State Chem. 2017. V. 256. P. 93.
Du J.-J., Zhang X., Zhou X.-P., Li D. // Inorg. Chem. Front. 2018. V. 5. № 11. P. 2772.
Zhou X.-P., Li M., Liu J., Li D. // J. Am. Chem. Soc. 2012. V. 134. № 1. P. 67.
Wu Y., Zhou X.-P., Yang J.-R., Li D. // Chem. Commun. 2013. V. 49. № 33. P. 3413.
Rubio-Giménez V., Waerenborgh J.C., Clemente-Juan J.M., Martí-Gastaldo C. // Chem. Mater. 2017. V. 29. № 15. P. 6181.
Guo W., Xia W., Cai K. et al. // Nano Micro Small. 2017. V. 13. № 41. P. 1.
Bratsos I., Tampaxis C., Spanopoulos I. et al. // Inorg. Chem. 2018. V. 57. № 12. P. 7244.
Li C., Tang H., Fang Y. et al. // Inorg. Chem. 2018. V. 57. № 21. P. 13912.
Muldoon P.F., Liu C., Miller C.C. et al. // J. Am. Chem. Soc. 2018. V. 140. № 20. P. 6194.
Béziau A., Baudron S.A., Fluck A., HosseiniM.W. // Inorg. Chem. 2013. V. 52. № 24. P. 14439.
Han Y., Sinnwell M.A., Teat S.J. et al. // Adv. Sci. 2019. V. 6. № 7. 1802056.
Abedi M., Mahmoudi G., Kirillov A.M., Kaminsky W. // Polyhedron. 2018. V. 142. P. 110.
Ding Y.-J., Li T., Hong X.-J. et al. // CrystEngComm. 2015. V. 17. № 21. P. 3945.
Li Y.-F., Wang D., Liao Z. et al. // J. Mater. Chem. C. 2016. V. 4. № 19. P. 4211.
Li Q., Zhu Z., Qian J. // Polyhedron. 2018. V. 155. P. 218.
Han Y., Zheng H., Liu K. et al. // ACS Appl. Mater. Interfaces. 2016. V. 8. № 35. P. 23331.
Hu H.-C., Kang X.-M., Cao C.-S. et al. // Chem. Commun. 2015. V. 51. № 54. P. 10850.
Zhai Q.-G., Bu X., Mao C. et al. // J. Am. Chem. Soc. 2016. V. 138. № 8. P. 2524.
Zhou W., Huang D.-D., Wu Y.-P. et al. // Angew. Chem. Int. Ed. 2019. V. 51. № 13. P. 4227.
Li Y.-P., Wang X.-X., Li S.-N. et al. // Cryst. Growth Des. 2017. V. 17. № 11. P. 5634.
Ding B., Liu S.X., Cheng Y. et al. // Inorg. Chem. 2016. V. 55. № 9. P. 4391.
Du X., Fan R., Wang X. et al. // Cryst. Growth Des. 2016. V. 16. № 3. P. 1737.
Feng D.-D., Dong H.-M., Liu Z.-Y. et al. // Dalton Trans. 2018. V. 47. № 43. P. 15344.
Han M.-L., Wen G.-X., Dong W.-W. et al. // J. Mater. Chem. C. 2017. V. 5. № 33. P. 8469.
Li L., Zou J.-Y., You S.-Y. et al. // Dalton Trans. 2017. V. 46. № 47. P. 16432.
Dybtsev D.N., Sapianik A.A., Fedin V.P. // Mendeleev Commun. 2017. V. 27. № 4. P. 321.
Polunin R.A., Kolotilov S.V., Kiskin M.A. et al. // Eur. J. Inorg. Chem. 2010. V. 32. P. 5055.
Polunin R.A., Kolotilov S.V., Kiskin M.A. et al. // Eur. J. Inorg. Chem. 2011. V. 32. P. 4985.
Dorofeeva V.N., Kolotilov S.V., Kiskin M.A. et al. // Chem. Eur. J. 2012. V. 18. P. 5006.
Sotnik S.A., Polunin R.A., Kiskin M.A. et al. // Inorg. Chem. 2015. V. 54. P. 5169.
Lytvynenko A.S., Kolotilov S.V., Kiskin M.A. et al. // Inorg. Chem. 2014. V. 53. P. 4970.
Sapianik A.A., Kiskin M.A., Kovalenko K.A. et al. // Dalton Trans. 2019. V. 48. P. 3676.
Sapianik A.A., Zorina-Tikhonova E.N., Kiskin M.A. et al. // Inorg. Chem. 2017. V. 56. № 3. P. 1599.
Sapianik A.A., Kiskin M.A., Samsonenko D.G. et al. // Polyhedron 2018. V. 145. P. 147.
Sapianik A.A., Lutsenko I.A., Kiskin M.A. et al. // Russ. Chem. Bull. 2016. V. 65. № 11. P. 2601.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия