Координационная химия, 2022, T. 48, № 11, стр. 669-676
Необычная координация нафталина в полиядерном гетеролигандном иттербий-эрбиевом комплексе
Т. В. Балашова 1, *, С. К. Полякова 1, Р. В. Румянцев 1, Г. К. Фукин 1, М. Н. Бочкарев 1
1 Институт металлоорганической химии им. Г.А. Разуваева РАН
Нижний Новгород, Россия
* E-mail: petrovsk@iomc.ras.ru
Поступила в редакцию 14.04.2022
После доработки 18.05.2022
Принята к публикации 24.05.2022
- EDN: TAEEVT
- DOI: 10.31857/S0132344X22110019
Аннотация
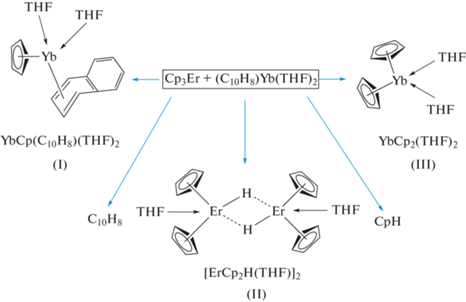
Реакцией Cp3Er и Yb(C10H8)(THF)2 в тетрагидрофуране получены гетеро- и гомолептические комплексы CpYb(C10H8)(THF)2 (I) [Er(Cp)H(THF)]2 (II) Cp2Yb(THF)2 (III), строение которых установлено методом РСА (CCDC № 2165047 (I), 2165048 (II), 2165049 (III)). При проведении реакции в диметоксиэтане впервые получен и структурно охарактеризован нафтильный комплекс [Yb-Cp(DME)]2(C10H6)ErCp2 (IV) (CCDC № 2165050) с необычной координацией нафталинового лиганда, содержащий в своем составе два разных иона лантанoида, находящихся при этом в разных степенях окисления (Yb2+, Yb3+ и Er3+).
Ареновые комплексы редкоземельных металлов – это один из самых интересных и сложных классов металлоорганических соединений. Способность принимать один или два электрона, превращаясь при этом в анион-радикалы и дианионы, разнообразие возможностей для π-координации от η2 до η6 делает эти лиганды весьма перспективными для изучения химии органолантанидных соединений. Нафталиновые производные лантанoидов привлекли значительное внимание исследователей благодаря их высокой реакционной способности и стали хорошо изученным классом лантанoид-ареновых комплексов [1, 2]. Высокая электроположительность лантанoидов [3] обусловливает ионный характер связи металл-лиганд в нафталиновых комплексах. Большинство полученных на сегодняшний день соединений составляют производные Ln(III): смешанные нафталин-иодные комплексы [LnI2(THF)3]2(μ-C10H8) [4, 5], комплексы, не содержащие иод, например трехпалубный тулиевый комплекс [C10H8Tm(DME)]2(μ-C10H8) [6] и различные гетеролигандные нафталин-циклопентадиенильные комплексы [7–9]. В то же время круг соединений двухвалентных лантанoидов значительно уже. Были получены комплексы Eu и Yb состава [ILn(DME)2]2(μ-C10H8) [4], трехпалубный комплекс [CpBn5Yb(DME)]2(μ-η4:η4-C10H8) [10]. Синтезированный в самом начале исследований нафталинид иттербия (C10H8)-Yb(THF)3 [11], сочетающий в одной молекуле два сильных восстановительных центра (ион Yb2+ и дианион (C10H8)2–, обладает удивительно высокой для органолантанoидов реакционной способностью. Все полученные соединения содержат либо один, либо несколько одинаковых ионов редкоземельных металлов. Гетеробиметаллических нафталиновых комплексов, содержащих в своем составе разные лантанoиды, получено не было. Вместе с тем известно, что гетеробиметаллические комплексы Yb–Er способны проявлять ап-конверсионные свойства [12]. Ион иттербия, обладая высоким эффективным сечением поглощения в ИК-области, является перспективным для использования в качестве сенсибилизирующего иона [13–15]. Ион эрбия, имеющий длительное время жизни возбужденных метастабильных состояний, на которые происходит передача энергии, часто используется в качестве излучающего центра [16–18]. Несмотря на преимущества ап-конверсионных материалов с органическими лигандами, число таких систем крайне ограничено [12, 19] из-за трудности их получения. С целью создания подобного рода материалов, была предпринята попытка получения комплексов Yb–Er с мостиковым дианионом нафталина (${{{\text{C}}}_{{{\text{10}}}}}{\text{H}}_{8}^{{2 - }}$).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез проводили в условиях, исключающих контакт с кислородом и влагой воздуха, с использованием стандартной техники Шленка. Тетрагидрофуран (ТГФ), диметоксиэтан (ДМЭ) сушили натрий-бензофенонкетилом по стандартной методике и отбирали в вакууме непосредственно перед использованием. Yb(C10H8)(THF)2 и Cp3Er получали по известным методикам [11, 20]. ИК-спектры записывали на Фурье-спектрометре ФСМ-1201 в диапазоне 4000–400 см–1. Образцы готовили в виде суспензии в вазелиновом масле. С, Н-элементный анализ выполняли на анализаторе Elementar Vario ELcube Analyzer.
Cинтез комплексов CpYb(C10H8)(THF)2 (I), [Er(Cp)H(THF)]2 (II), Cp2Yb(THF)2 (III). К смеси порошков ErCp3 (214 мг, 0.59 ммоль) и Yb(C10H8)- (THF)2 (262 мг, 0.59 ммоль) наконденсировали 7 мл ТГФ. Реакционную смесь перемешивали в течение 4 ч при –10°С до растворения нафталиниттербия. Из бордово-фиолетового раствора постепенно выпадали кристаллы комплекса I, которые отделили декантацией, промывали холодным ТГФ и высушивали в вакууме. Выход I 31 мг (62%).
ИК I (KBr; ν, см–1): 1595 сл, 1254 ср, 1191 ср, 1108 ср, 1059 ср, 1010 ср, 981 пл, 854 с, 827 сл, 778 с, 756 с, 747 с, 720 с, 661 сл, 476 ср (совпадает с описанными ранее [8, 21]).
При концентрировании и последующем охлаждении маточного раствора выпадают розовые кристаллы комплекса II и изумрудно-зеленые кристаллы комплекса III, которые промывали холодным ТГФ и высушивали в вакууме.
Выход II 38 мг (26%).
ИК-спектр комплекса II совпадает с описанным ранее [22].
Выход III 7 мг (16%).
ИК-спектры комплексов II и III совпадают с описанными ранее [8, 23].
В летучих продуктах реакции методом ВЭЖХ были обнаружены С10Н8 и следовые количества СрН. Из оставшегося после удаления летучих продуктов аморфного порошка индивидуальных соединений выделить не удалось.
Cинтез комплекса [YbCp(DME)]2(C10H6)ErCp2 (IV). К смеси порошков ErCp3 (104 мг, 0.29 ммоль) и Yb(C10H8)(THF)2 (128 мг, 0.29 ммоль) наконденсировали 10 мл ДМЭ. Реакционную смесь перемешивали в течение 6 ч при –10°С до полного растворения исходных соединений. Образовавшийся фиолетовый раствор концентрировали и охлаждали до –17°С. Выпавшие кристаллы комплекса IV отделяли декантацией, промывали холодным ДМЭ и высушивали в вакууме. Выход 21 мг, 20%. μэфф = 5.7 М.Б.
| Найдено, %: | C 42.31; | H 4.49; | Er Yb, 47.39. |
| Для C38H46ErO4Yb2 | |||
| вычислено, %: | C 42.26; | H 4.29; | Er Yb, 47.53. |
ИК (KBr; ν, cм–1): 1259 ср, 1069 ср, 1010 с, 959 сл, 915 сл, 871 ср, 781 с, 761 с, 664 сл, 617 сл, 498 сл, 473 сл.
Разделить остальные продукты и выделить их в индивидуальном состоянии не удалось.
РСА комплексов I–IV проведены на автоматическом дифрактометре Bruker D8 Quest (графитовый монохроматор, МоКα-излучение, φ- и ω-сканирование, λ = 0.71073 Å). Экспериментальные наборы интенсивностей интегрированы с помощью программы SAINT [24]. Программы SADABS [25] (I, III и IV) и TWINABS (II) [26] использованы для введения поправок на поглощение. Структуры расшифрованы методом “dual-space”в программе SHELXT [27]. Неводородные атомы уточнены полноматричным МНК по $F_{{hkl}}^{2}$ в анизотропном приближении с помощью программного пакета SHELXTL [28]. Атомы водорода, за исключением H(1) в комплексе II, помещены в геометрически рассчитанные положения и уточнены в модели наездника (Uiso(H) = 1.5Ueq(C) для CH3-групп, Uiso(H) = 1.2Ueq(C) для остальных групп). В свою очередь, атом H(1) в комплексе II локализован объективно из разностного Фурье-синтеза и уточнен в изотропном приближении. Кристаллы комплексов I и II представляют собой двухкомпонентные двойники. Соотношение доменов составляет ~0.969 : 0.031 и ~0.937 : 0.063 в I и II соответственно. Одна некоординированная молекула ТГФ приходится на одну молекулу комплекса I в кристалле. Основные кристаллографические характеристики и параметры рентгеноструктурного эксперимента для I–IV приведены в табл. 1.
Таблица 1.
Кристаллографические данные и параметры эксперимента и уточнения для комплексов I–IV
| Комплекс | Значение | |||
|---|---|---|---|---|
| I | II | III | IV | |
| Брутто-формула | C27H37O3Yb | C28H38O2Er2 | C18H26O2Yb | C38H46O4Yb2Er |
| М | 582.60 | 741.10 | 447.43 | 1080.09 |
| Температура, K | 100(2) | 100(2) | 100(2) | 100(2) |
| Сингония | Моноклинная | Триклинная | Моноклинная | Моноклинная |
| Пр. группа | P21/n | $P\bar {1}$ | P21/n | C2/c |
| a, Å | 12.1911(7) | 7.9355(7) | 13.2741(4) | 15.1929(6) |
| b, Å | 11.9207(7) | 7.9913(7) | 9.9058(3) | 18.0544(7) |
| c, Å | 16.7649(9) | 10.8018(9) | 13.6177(4) | 13.7795(5) |
| α, град | 90 | 90.973(2) | 90 | 90 |
| β, град | 100.9173(17) | 108.514(2) | 110.1525(10) | 111.0302(12) |
| γ, град | 90 | 103.344(2) | 90 | 90 |
| V, Å3 | 2392.3(2) | 628.98(9) | 1680.98(9) | 3527.9(2) |
| Z | 4 | 1 | 4 | 4 |
| ρ(выч.), мг/см3 | 1.618 | 1.957 | 1.768 | 2.034 |
| μ, мм–1 | 3.934 | 6.647 | 5.565 | 7.653 |
| Размер кристалла, мм | 0.27 × 0.09 × 0.03 | 0.30 × 0.22 × 0.17 | 0.19 × 0.12 × 0.06 | 0.09 × 0.06 × 0.03 |
| F(000) | 1172 | 358 | 880 | 2056 |
| Интервал 2θ, град | 2.285–26.022 | 2.632–38.421 | 2.601–29.129 | 2.256–26.367 |
| Число отражений собранных/независимых | 30 698/4764 | 10 865/10 865 | 23 343/4519 | 26 097/3611 |
| Rint | 0.0691 | 0.0277 | 0.0387 | 0.0856 |
| R1, wR2 (I > 2σ(I)) | 0.0485, 0.1404 | 0.0284, 0.0654 | 0.0266, 0.0465 | 0.0323, 0.0558 |
| R1, wR2 (по всем данным) | 0.0732, 0.1602 | 0.0367, 0.0676 | 0.0496, 0.0512 | 0.0648, 0.0635 |
| S | 1.043 | 1.039 | 1.069 | 1.015 |
| Остаточная электронная плотность (max/min), e/Å3 | 1.167/–1.410 | 1.811/–3.295 | 1.075/–0.884 | 1.310/–1.071 |
Структуры депонированы в Кембриджском банке структурных данных (CCDC № 2165047 (I), 2165048 (II), 2165049 (III) и 2165050 (IV); http://ccdc.cam.ac.uk/structures/).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Ранее явление ап-конверсии наблюдалось на иттербий-эрбиевом гексафторизопропоксидном комплексе Er0.67Yb1.33[(CF3)2CHO]9 [12]. С целью получения новых ап-конверсионных материалов в данной работе предприняты попытки синтеза гетеролигандных биметаллических комплексов Yb–Er с мостиковым дианионом нафталина. В качестве синтетического подхода была выбрана реакция Cp3Er с Yb(C10H8)(THF)2 в молярном соотношении 1 : 1 в среде тетрагидрофурана, которая легко протекает при пониженных температурах (–10°С). Продукты реакции Cp3Er с нафталинидом иттербия представлены на схеме 1 .
Схема 1 .
Комплекс I был выделен в виде темно-фиолетовых кристаллов в форме иголок, чрезвычайно чувствительных к кислороду и влаге воздуха, с выходом 60%. По данным РСА, молекулярное строение комплекса I аналогично строению CpYC10H8(DME) [8] и CpLuC10H8(DME) [21]. Атом Yb связан с η5-Ср-лигандом, η4-нафталином и двумя молекулами ТГФ (рис. 1). Координированное с атомом Yb шестичленное кольцо нафталина неплоское. Перегиб по линии С(2)–С(5) в молекуле нафталина составляет 30.3° (26.1° в комплексе Y [8] и 31.5° в комплексе Lu [21]). Как и в аналогах Y и Lu, в молекуле комплекса I наблюдается перераспределение значений длин связей С–С в координированном кольце нафталина по сравнению с их значениями в свободном нафталине. Расстояния С(1)–С(2), С(2)–С(3) и С(4)–С(5), С(5)–С(6), равные 1.465(15), 1.458(14) и 1.464(14), 1.473(14) Å соответственно, существенно превышают длину связи С(3)–С(4) 1.363(14) Å. Средние расстояния в одном ароматическом кольце свободного нафталина С(1)–С(6) составляют: 1.415, 1.363, 1.378, 1.363 и 1.415 Å (Mogul 2020.2.0) [29, 30]. Расстояния С–С в кольце нафталина, не связанном с атомом Yb, лежат в интервале 1.362(15)–1.424(13) Å. Таким образом, нафталин в I может быть представлен в виде диа-ниона.
Рис. 1.
Молекулярная структура комплекса I. Избранные длины связей и углы: Yb(1)–O(1) 2.358(6), Yb(1)–O(2) 2.385(6), Yb(1)–C(2) 2.459(11), Yb(1)–C(3) 2.555(10), Yb(1)–C(4) 2.576(9), Yb(1)–C(5) 2.453(10), Yb(1)–CCp 2.604(9)–2.694(9), C(1)–C(2) 1.465(15), C(2)–C(3) 1.458(14), C(3)–C(4) 1.363(14), C(4)–C(5) 1.464(14), C(5)–C(6) 1.473(14), C(1)–C(6) 1.424(13) Å и O(1)Yb(1)O(2) 76.4(2)°, C(1)C(2)C(3) 115.1(8)°, C(2)C(3)C(4) 119.9(9)°, C(3)C(4)C(5) 118.1(9)°, C(4)C(5)C(6) 115.7(9)°. Тепловые эллипсоиды приведены с 30%-ной вероятностью. Атомы водородa не показаны.

Такое представление отлично согласуется с распределением длин связей Yb–C(C10H8). Межатомные расстояния Yb–С(2) и Yb–С(5) в I (2.459(11) и 2.453(10) Å соответственно) существенно короче, чем Yb–С(3) и Yb–С(4) (2.555(10) и 2.576(9) Å). Расстояния Yb(1)–C(1) и Yb(1)–C(6) (2.983 и 2.958 Å) значительно превышают сумму ионного радиуса катиона иттербия (0.985 Å) [31] и ван-дер-ваальсового радиуса углерода (1.7 Å) [32]. Аналогичное распределение длин связей наблюдалось в подобных комплексах Y и Lu [8, 21]. Исходя из этого, связь нафталина с атомом Yb в I более корректно можно представить как 2η1:η2 (2σ,π)-взаимодействие.
Расстояния Yb–CCp в комплексе I несколько превышают расстояния Yb–C(C10H8) и варьируются в диапазоне 2.604(9)–2.694(9) Å. Расстояние между атомом иттербия и центром циклопентадиенильного лиганда в I (2.363 Å) находится в хорошем согласии с ранее опубликованными родственными комплексами Yb3+ [33–35].
Образование трехъядерного гидридного комплекса лютеция наблюдалось ранее в реакции Cp2LuCl и C10H8Na [7]. Реакция проходит через стадию образования интермедиата с дианионом нафталина с последующим расщеплением связи С–Н и образованием гидридного и нафтильного фрагмента. Венлиангом Хуангом с соавторами подробно рассмотрен новый тип активации связи С–Н на комплексах редкоземельных металлов в присутствии восстановителя [36]. Эти условия позволяют расщеплять неактивированные ароматические связи С–Н, что приводит к образованию гидрида соответствующего металла и его фенильного (или нафтильного) комплекса. Предлагаемый механизм включает стадию образования аренового биметаллического промежуточного продукта. Образование гидридного комплекса II и нафтильного комплекса IV, по-видимому, протекает по такому же механизму: через активацию С–Н с последующим β-элиминированием атома водорода.
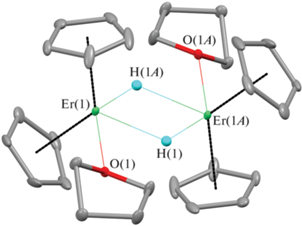
Соединение II, по данным РСА, представляет собой центросимметричный димер, в котором каждый атом эрбия связан с двумя η5-Ср-лигандами, одной терминальной молекулой ТГФ и двумя μ2-мостиковыми атомами водорода (рис. 2). Комплекс II изоструктурен ранее опубликованному лютециевому димеру [37]. Четырeхчленный металлоцикл ErHErH плоский, что характерно для родственных димерных гидридных комплексов Lu [37] и Sm [38], полученных по реакциям алкил- или арилпроизводных лантанoидов с водородом. Атомы кислорода ТГФ молекул незначительно отклоняются от плоскости металлоцикла (0.167 Å). Расстояние Ln–Ln в II (3.5721(4) Å) больше, чем в комплексе [Lu(Cp)H(THF)]2 (3.5216(6) Å) [25] в отличном соответствии с разницей в ионных радиусах эрбия (1.062 Å) и лютеция (1.032 Å) [31].
Рис. 2.
Молекулярная структура комплекса II. Избранные длины связей и углы: Er(1)–O(1) 2.417(4), Er(1)–CCp 2.634(3)–2.665(3), Er(1)–H(1) 2.15(3), Er(1)–H(1A*) 2.10(4), Er(1)…Er(1A) 3.5721(4) Å и O(1)Er(1)H(1) 70.5(9)°, H(1A)Er(1)O(1) 135.9(10)°, H(1)Er(1)H(1A) 65.6(16)°. Тепловые эллипсоиды приведены с 30%-ной вероятностью. Атомы водороды не показаны. * Операция симметрии, используемая для генерации эквивалентных атомов в комплексе II (А): –x, –y, –z.
Расстояния Er–CCp в комплексе II варьируются в узком диапазоне 2.634(3)–2.665(3) Å. Расстояния между атомом иттербия и центрами циклопентадиенильных лигандов в II (2.359 и 2.365 Å) находятся в хорошем согласии с ранее опубликованными родственными комплексами Er3+ [39, 40]. Расстояния Er–O в комплексе II систематически превышают расстояния Yb–O в комплексе I, что хорошо согласуется с разницей в ионных радиусах этих элементов [31].
В качестве побочного продукта реакции также образуется Cp2Yb(THF)2 в виде изумрудно-зеленых кристаллов. Атом иттербия в комплексе III связан с двумя η5-Ср-лигандами и двумя молекулами ТГФ (рис. 3). Геометрия ближайшего окружения атома Yb(1) в III схожа с родственными циклопентадиенильными комплексами с ДМЭ [41, 42] и TPPO (трифенилфосфиноксидом) [43, 44]. Расстояния Yb(1)–CCp в III (2.691(3)–2.741(3) Å) систематически больше по сравнению с комплексом I (2.604(9)–2.694(9) Å), что хорошо согласуется с разницей в ионных радиусах для Yb2+ (1.140 Å) и Yb3+ (0.985 Å) [31]. Аналогичная тенденция наблюдается для связей Yb–O.
Рис. 3.
Молекулярная структура комплекса III. Избранные длины связей и углы: Yb(1)–O(1) 2.422(2), Yb(1)–O(2) 2.427(2), Yb(1)–CCp 2.691(3)–2.741(3) Å и O(1)Yb(1)O(2) 81.90(8)°. Тепловые эллипсоиды приведены с 30%-ной вероятностью. Атомы водородa не показаны.

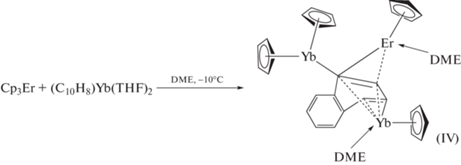
Гетерометаллический комплекс IV в виде кристаллов, пригодных для РСА, выделить не удалось ввиду его высокой лабильности и низкой устойчивости. Известно, что смешанные Ср-нафталиновые комплексы лантанoидов с ТГФ-лигандами менее стабильны, чем с ДМЭ [21]. При проведении реакции Cp3Er с нафталинидом иттербия в ДМЭ в тех же условиях удалось выделить соединение IV (схема 2 ), являющееся промежуточным продуктом, распад которого и дальнейшие превращения дают уже описанные выше комплексы I–III.
Схема 2 .
Все полученные до сих пор нафтильные комплексы редкоземельных металлов [7, 24] являются одноядерными соединениями. Комплекс IV, по данным РСА, представляет собой трехъядерный гетеробиметаллический комплекс.
В независимой области ячейки кристалла IV находится только половинка молекулы. Атомы Yb(1) и Er(1) вместе с координированными на них циклопентадиенильными лигандами и молекулами ДМЭ, а также молекула нафталина при этом разупорядочены по двум положениям с заселенностью 50 : 50. В результате комплекс имеет асимметричное строение (рис. 4).
Рис. 4.
Молекулярная структура комплекса IV. Избранные длины связей и углы: Yb(2)–C(15) 2.481(10), Yb(2)–CCp 2.631(6)–2.657(6), Er(1)–O(1) 2.48(3), Er(1)–O(2) 2.354(16), Er(1)–C(15) 2.409(15), Er(1)–C(16) 2.577(13), Er(1)–CCp 2.635(13)–2.658(13), Yb(1)–O(1A) 2.43(3), Yb(1)–O(2A) 2.428(16), Yb(1)–C(15) 2.522(15), Yb(1)–C(16) 2.683(14), Yb(1)–C(23) 2.719(12), Yb(1)–C(24) 2.605(13), Yb(1)–CCp 2.679(13)–2.701(13), C(15)–C(24) 1.416(15), C(15)–C(16) 1.508(15), C(16)–C(17) 1.509(18), C(22)–C(23) 1.471(17), C(23)–C(24) 1.426(16), Yb(1)–Yb(2) 3.633, Yb(1)–Er(1) 4.830, Yb(2)–Er(1) 3.832 Å и O(2)Er(1)O(1) 65.3(8)°, O(2A)Yb(1)O(1A) 65.4(8)°, C(24)C(15)C(16) 115.2(11)°, C(17)C(16)C(15) 118.6(11)°, C(24)C(23)C(22) 118.1(11)°, C(15)C(24)C(23) 119.6(11)°. Тепловые эллипсоиды приведены с 30%-ной вероятностью. Атомы водородa не показаны.

Расстояния C–C в некоординированном кольце нафталина варьируются от 1.35(2) до 1.434(19) Å. Усредненное значение C–C в этом шестичленном кольце составляет 1.396 Å и отлично согласуется с ароматической структурой [45]. Расстояния C(16)–C(17) (1.509(18) Å) и C(22)–C(23) (1.471(17) Å), как и в комплексе I, соответствуют одинарной связи C–C. В отличие от комплекса I, в молекуле нафталина в комплексе IV отсутствуют два атома водорода на атомах C(15) и C(16). Подобная ситуация наблюдалась ранее в тетраядерном комплексе рения [46]. Таким образом, молекула нафталина несет общий, что соответствует наличию в молекуле трех различных ионов Yb3+, Yb2+ и Er3+. Фрагмент C(16)–C(15)=C(24)–C(23) в IV более искажен по сравнению с комплексом I и литературным комплексом рения [46], что, вероятно, связано со стерическими факторами. Расстояние C(15)–C(16) (1.508(15) Å) хорошо соответствует одинарной связи C–C. В свою очередь, расстояние C(15)–C(24) (1.416(15) Å) несколько превышает двойную связь C=C, а расстояние C(23)–C(24) (1.426(16) Å), напротив, несколько короче, чем одинарная связь C–C [29, 30]. Однако предположение о том, что атомы Er(1), Yb(1) и Yb(2) в IV представляют собой соответственно трехвалентный эрбий и атомы двух- и трехвалентного иттербия хорошо согласуются с расстояниями Ln–O и Ln–CCp в комплексах I–III.
Расстояние Yb(2)–C(15) (2.481(10) Å) можно трактовать как σ-связь Yb–C. Это значение хорошо согласуется с длинами связей Yb(III)–арен [47, 48]. Атом эрбия связан с молекулой нафталина посредством взаимодействий Er(1)–C(15) и Er(1)–C(16) (2.409(15) и 2.577(13) Å). Как и в комплексе I атом Yb(1) в IV связан сразу с четырьмя атомами углерода молекулы нафталина. Однако в случае комплекса IV расстояния Yb–C варьируются в более широком диапазоне (2.522(15)–2.719(12) Å). Как и в случае перераспределения длин связей в нафталиновом кольце, такая ассиметричная координация, по всей видимости, определяется стерическими факторами. Кроме того, отметим, что расстояния Yb–C(C10H8) в IV систематически больше по сравнению с комплексом I, что хорошо согласуется с разницей в ионных радиусах атомов Yb(II) и Yb(III) [31].
Данные РСА подтверждаются данными магнитных измерений. Магнитный момент комплекса IV составляет 5.7 М.Б., что соответствует наличию в составе молекулы Yb2+, Yb3+ и Er3+. Значения эффективных магнитных моментов для органических соединений соответствующих ионов лантанoидов составляют 0 М.Б., 3.8–4.3 и 9.0–9.6 М.Б. [49]. Расчетное значение магнитного момента соединения, где все три иона присутствуют в соотношении 1 : 1 : 1, находится в интервале 5.6–6.0 М.Б.
Вопреки ожидаемым результатам, комплекс IV оказался люминесцентно неактивным, что не позволило наблюдать в этой системе явление ап-конверсии.
Таким образом, реакция ErCp3 с нафталинидом иттербия – сложный, многостадийный и многовекторный процесс, в результате которого были выделены и структурно охарактеризованы комплексы CpYb(C10H8)(THF)2 (I), [Er(Cp)H(THF)]2 (II), Cp2Yb(THF)2 (III), [YbCp(DME)ErCp(DME)]- (C10H6)YbCp2 (IV). Гетеролигандный гетерометаллический Yb−Er нафтильный комплекс получен впервые. Предложен путь его синтеза, включающий стадию образования неустойчивого комплекса, содержащего фрагмент [(Cp2Er+)2(${{{\text{C}}}_{{{\text{10}}}}}{\text{H}}_{8}^{{2 - }}$)], и его распад с образованием гидридного и σ-нафтильного продуктов. Нафтильный комплекс, который можно считать интермедиатом, содержит Er3+, Yb2+ и Yb3+, о чем свидетельствуют данные РСА и магнитных измерений. Соединение оказалось люминесцентно неактивным. Однако все полученные комплексы являются чрезвычайно реакционноспособными, тем самым открывая богатые возможности получения различных соединений Er и Yb, недоступных другими синтетическими методами.
Авторы заявляют, что у них нет конфликта интересов.
Список литературы
Bochkarev M.N. // Chem. Rev. 2002. V. 102. P. 2089.
Huang W., Diaconescu P.D. // Dalton Trans. 2015. V. 44. P. 15360.
Morss L.R. // Chem. Rev. 1976. V. 76. P. 827.
Fedushckin I.L., Bochkarev M.N., Schumann H. et al. // J. Organomet. Chem. 1995. V. 489. P. 145.
Bochkarev M.N., Fedushkin I.L., Larichev R.B. // Russ. Chem. Bull. 1996. V. 45. № 10. P. 2443.
Bochkarev M.N., Fedushkin I.L., Fagin A.A. et al. // Chem. Commun. 1997. № 18. P. 1783.
Protchenko A.V., Fedorova E.A., Bochkarev M.N. et al. // Russ. Chem. Bull. 1994. V. 43. P. 1916.
Protchenko A.V., Zakharov L.N., Fukin G.K. et al. // Russ. Chem. Bull. 1996. V. 45. P. 950.
Protchenko A.V., Almazova O.G., Zakharov L.N. et al. // J. Organomet. Chem. 1997. V. 536–537. P. 457.
Selikhov A.N., Mahrova T.V., Cherkasov A.V. et al. // Organomet. 2016. V. 35. P. 2401.
Bochkarev M.N., Trifonov A.A., Fedorova E.A. et al. // J. Organomet. Chem. 1989. V. 372. P. 217.
Balashova T.V., Pushkarev A.P., Yablonskiy A.N. et al. // J. Lumin. 2017. V. 192. P. 208.
Oliveira A.S., de Araujo M.T., Gouveia-Neto A.S. et al. // Appl. Phys. Lett. 1998. V. 72. P. 753.
Xu S., Yang Z., Zhang J. et al. // Chem. Phys. Lett. 2004. V. 385. P. 263.
Martin I.R., Rodriguez V.D., Lavin V., Rodriguez-Mendoza U.R. // Spectrochim. Acta. A. 1999. V. 55. P. 941.
Kanoun A., Jaba N., Mejri H. et al. // Phys. Status Solidi. A. 2001. V. 188. P. 1145.
Vetrone F., Boyer J.C., Capobianco J.A. et al. // Chem. Mater. 2003. V. 15. P. 2737.
Patra A., Friend C.S., Kapoor R., Prasad P.N. // Appl. Phys. Lett. 2003. V. 83. P. 284.
Sorgho L.A., Besnard C., Pattison P. et al. // Angew. Chem. Int. Ed. 2011. V. 50. P. 4108.
Birmingham J.M., Wilkinson G. // J. Am. Chem. Soc. 1956. V. 78. P. 42.
Protchenko A.V., Zakharov L.N., Bochkarev M.N., Struchkov Yu.T. // J. Organomet. Chem. 1993. V. 447. P. 209.
Schumann H., Genthe W., Hahn E., Hossain M.B., Van Der Helm D. J. Organomet. Chem. 1986. V. 299(1). P. 67.
Calderazzo F., Pappalardo R., Losi S. // J. Inorg. Nucl. Chem. 1966. V. 28. № 4. P. 987.
SAINT. Data Reduction and Correction Program. Madison (WI, USA): Bruker AXS, 2014.
Krause L., Herbst-Irmer R., Sheldrick G.M., Stalke D. // J. Appl. Crystallogr. 2015. V. 48. № 1. P. 3.
Sheldrick G.M. TWINABS. Version 2012/1. Göttingen (Germany): Georg-August-Univ. Göttingen, 2012.
Sheldrick G.M. // Acta Crystallogr. A. 2015. V. 71. № 1. P. 3.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3.
Bruno I.J., Cole J.C., Kessler M. et al. // J. Chem. Inf. Comput. Sci. 2004 . V. 44. P. 2133.
Cottrell S.J., Olsson T.S.G., Taylor R. // J. Chem. Inf. Model. 2012. V. 52. P. 956.
Shannon R.D. // Acta Crystallogr. A. 1976. V. 32. P. 751.
Batsanov S.S. // Inorg. Mater. 2001. V. 37. № 9. P. 871.
Zhang Z., Zhang L., Li Y., Hong L., Chen Z., Zhou X. // Inorg. Chem. 2010. V. 49. P. 5715.
Liu R., Zheng P., Weng L., Zhou X., Liu C. // J. Organomet. Chem. 2008. V. 693. P. 1614.
Trifonov A.A., Kurskii Yu.A., Bochkarev M.N., Muehle S., Dechert S., Schumann H. // Russ. Chem. Bull. 2003. V. 52. P. 601.
Huang W., Dulong F., Khan S.I., Cantat T., Diaconescu P.L. // J. Am. Chem. Soc. 2014. V. 136. P. 17410.
Schumann H., Genthe W., Hahn E. // J. Organomet. Chem. 1986. V. 299. P. 61.
Evans W.J., Bloom I., Hunter W.E., Atwood J.L. // J. Am. Chem. Soc. 1983. V. 105. P. 1401.
Sun Y., Zhang Z., Wang X. et al. // Dalton Trans. 2010. V. 39. P. 221.
Evans W.J., Meadows J.H., Wayda A.L. et al. // J. Am. Chem. Soc. 1982. V. 104. P. 2015.
Deacon G.B., Mackinnon P.I., Hambley T.W., Taylor J.C. // J. Organomet. Chem. 1983. V. 259. P. 91.
Jin J., Jin S., Chen W. // J. Organomet. Chem. 1991. V. 412. P. 71.
Deacon G.B., Gatehouse B.M., White P.A. // Polyhedron. 1989. V. 8. P. 1983.
Zhou X.-G., Wu Z.-Z., Jin Z.-S. // J. Organomet. Chem. 1992. V. 431. P. 289.
Lonsdale K. // Nature. 1928. V. 122. P. 810.
Adams R.D., Dhull P., Smith M.D., Tedder J.D. // Inorg. Chem. 2019. V. 58. P. 2109.
Petrov A.R., Rufanov K.A., Harms K., Sundermeyer J. // J. Organomet. Chem. 2009. V. 694. P. 1212.
Bochkarev M.N., Khramenkov V.V., Rad’kov Yu.F. et al. // J. Organomet. Chem. 1992. V. 429. P. 27.
Evans W.J., Hozbor M.A. // J. Organomet. Chem. 1987. V. 326. P. 299.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия