Кристаллография, 2020, T. 65, № 4, стр. 593-596
Синтез, кристаллическая и молекулярная структура сольватированного комплекса [МоО2(L) · С5Н5N] (L2– = анион 2-[N-(2-гидроксинафтилиден)амино]пропан-1,2,3-триола)
В. С. Сергиенко 1, 2, *, В. Л. Абраменко 3, М. Д. Суражская 1
1 Институт общей и неорганической химии им. Н.С. Курнакова РАН
Москва, Россия
2 Всероссийский институт научной и технической информации РАН
Москва, Россия
3 Луганский национальный университет им. Владимира Даля
Луганск, Украина
* E-mail: sergienko@igic.ras.ru
Поступила в редакцию 30.07.2019
После доработки 03.09.2019
Принята к публикации 03.09.2019
Аннотация
Синтезировано новое соединение диоксомолибдена (VI), [MoO2(L) · С5Н5N], где L2– = 2-[N-2-гидроксинафтилиден)амино]пропан-1,2,3-триол. Его строение определено методом ИК-спектроскопии и рентгеноструктурного анализа. Атом Мо имеет октаэдрическую координацию – он окружен двумя оксолигандами в цис-позициях друг относительно друга, двумя атомами О и атомом N(2) тридентатного бис(хелатного) лиганда L, а также атомом N(1) молекулы пиридина (Pу). В транс-позициях по отношению к лигандам О(оксо) расположены атомы N(2)(L) и N(1)(Py) на увеличенных вследствие структурного проявления транс-влияния кратносвязанных оксолигандов расстояниях (Мо–N(1) 2.476, Mo–N(2) 2.272 Å).
ВВЕДЕНИЕ
Алкогольимины, производные замещенных ароматических о-оксиальдегидов и аминоспиртов, при взаимодействии с солями переходных металлов образуют комплексы различного типа и строения, проявляя би- или тридентатную функцию [1–5]. Для диоксомолибдена (VI) с алкоголь-иминами получены внутрикомплексные соединения (ВКС) состава [МоО2(L)] и [МоО2(L) · Solv], где L2– – анионы тридентатных, дважды депротонированных молекул алкогольиминов, производных замещенных ароматических о-оксиальдегидов или о-оксиацетофенона, Solv – нейтральная N- или О-донорная молекула [1–4]. По данным ИК-спектроскопических исследований комплексы [МоО2(L)] являются олигомерами с мостиковой связью Мо=О → Мо [6], тогда как сольватированные мономерные комплексы [МоО2(L) · Solv], согласно данным рентгеноструктурного анализа (РСА) [1–3], объединены в псевдодимеры межмолекулярными водородными связями.
Увеличение количества спиртовых ветвей в аминном фрагменте молекул алкогольиминов по результатам ИК-спектроскопических и рентгеноструктурных исследований комплексов [МоО2(L) · Solv] (L2– – дважды депротонированные молекулы азометинов, производных салициловых альдегидов и трис(гидроксиметил)аминометана) не оказывает влияния на характер координации лигандов: в донорно-акцепторном взаимодействии принимает участие лишь одна из трех спиртовых ветвей аминного фрагмента. Две другие спиртовые группы участвуют в межмолекулярных водородных связях, объединяющих мономерные молекулы в полимер [2]. Данные РСА свидетельствуют о том, что связи донорных молекул Solv (в частности, метанола) с атомом молибдена существенно удлинены (ослаблены) вследствие статистического транс-влияния кратносвязанных оксолигандов цис-МоО2-группы, что объясняет легкость десольватации комплексов с образованием олигомеров, разрушаемых при добавлении донорных растворителей.
В целях продолжения работ по изучению строения и свойств ВКС диоксомолибдена (VI) с алкогольиминами о-оксиальдегидов проведен синтез, ИК-спектроскопическое и рентгеноструктурное исследование комплекса [МоО2(L) · С5Н5N] (I) (L2– – анион дважды депротонированной молекулы 2-[N-(2-гидроксинафтилиден)амино]пропан-1,2,3-триола (H2L)).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез H2L, его характеристики и ИК-спектр описаны в [2].
Синтез I. Комплекс получали кипячением метанольных растворов эквимолярных количеств ацетилацетоната молибденила и азометина в течение получаса с последующим добавлением 2–3 мл пиридина и выдерживанием в реакционной смеси в течение суток при 0°С. Выход мелкокристаллического вещества составлял ∼80%. Кристаллы для РСА получали следующим образом. 0.326 г (0.001 моль) МоО2(Асас)2 растворяли при кипячении в 20 мл метанола и прибавляли при перемешивании 20 мл метанольного раствора, содержащего 0.275 г (0.001 моль) лиганда. Смесь кипятили в течение 10 мин, добавляли 3 мл пиридина и раствор упаривали до объема ∼10 мл. После выдерживания в холодильнике реакционной смеси в течение суток выпавшие кристаллы отделяли с помощью фильтра, промывали холодным метанолом и сушили в токе сухого аргона. Выход комплекса в виде игольчатых кристаллов лимонного цвета составлял ∼82%. При 140°С комплекс десольватируется, его заметное разложение без плавления начинается при нагревании свыше 300°С.
Элементный анализ комплекса на содержание углерода, водорода и азота проводили с использованием анализатора Carlo-Erba 1106 Elemental Analyzer CHN. Содержание молибдена определяли путем прокаливания навески комплекса до массовой формы МоО3 [7]. В работе использовали реактивы зарубежных фирм Lancaster, Merk, Fluka без дополнительной очистки. Содержание элементов: С 49.84, Н 4.38, Мо 20.10, N 5.75, О 20.15 мас. %. Для C20H20MoN2O6 вычислено: С 50.01, Н 4.20, Мо 19.97, N 5.83, О 19.99 мас. %.
ИК-спектр I регистрировали на спектрометре ИКС-29 в области 3600–400 см–1 в суспензии вазелинового масла. ИК-спектры [МоО2(L) · С5Н5N]: 3300 ш., 1650, 1620, 1605, 1550, 1340, 1300, 1255, 1170, 1142, 1110, 1080, 1055, 1040, 980, 930, 907, 875, 770, 745, 720, 675, 580, 562, 550, 512, 430 см–1.
Рентгеноструктурный анализ соединения I выполнен на автоматическом дифрактометре Enraf-Nonius CAD4 при комнатной температуре (СuKα-излучение, λ = 1.5418 Å, графитовый монохроматор). Кристаллы I (M = 480.32) моноклинные, пр. гр. P21/c, a = 15.791(3), b = 9.334(3), c = = 14.012(2) Å, β = 108.69(1)°, V = 1956.4(8) Å3, Z = = 4, ρвыч = 1.631 г/см3, μ(CuKα) = 5.844 мм–1, F(000) = 976. Размер кристалла 0.20 × 0.08 × × 0.03 мм. Интенсивности 12334 отражений (из них 3326 независимых, Rint = 0.0524) измерены методом ω-сканирования в интервале 4.24° < θ < < 24.96°, (–18 ≤ h ≤ 18, –10 ≤ k ≤ 10, –16 ≤ l ≤ 16); параметры Тmax/Tmin = 0.8442/0.3878. Структура расшифрована прямым методом и уточнена полноматричным анизотропным методом наименьших квадратов по F2 для всех неводородных атомов (SHELXL-97 [8]). Все атомы водорода помещены в рассчитанные позиции и уточнены по схеме “наездника”. Окончательное значение факторов расходимости составило R1 = 0.0410, wR2 = 0.0982 для отражений с I > 2σ(I) и 336 параметров уточнения, R1 = 0.0445, wR2 = 0.1010 для всех рефлексов; GooF(F2) = 1.062, Δρmax, Δρmin = = 0.779, –0.745 э/Å3. Основные длины связей и валентные углы приведены в табл. 1. Структура депонирована в Кембриджский банк структурных данных (CCDC № 1940964).
Таблица 1.
Межатомные расстояния и основные валентные углы в структуре соединения I
| Связь | d, Å | Угол | ω, град |
|---|---|---|---|
| Mo(1)–O(1) | 1.688(2) | O(1)Mo(1)O(2) | 105.96(11) |
| Mo(1)–O(2) | 1.691(2) | O(1)Mo(1)O(4) | 97.09(9) |
| Mo(1)–O(4) | 1.950(2) | O(2)Mo(1)O(4) | 99.18(1) |
| Mo(1)–O(3) | 1.956(2) | O(1)Mo(1)O(3) | 101.91(10) |
| Mo(1)–N(2) | 2.272(2) | O(2)Mo(1)O(3) | 98.32(10) |
| Mo(1)–N(1) | 2.476(3) | O(4)Mo(1)O(3) | 149.44(9) |
| O(1)Mo(1)N(2) | 161.62(10) | ||
| O(2)Mo(1)N(2) | 91.66(10) | ||
| O(4)Mo(1)N(2) | 74.50(7) | ||
| O(3)Mo(1)N(2) | 80.15(8) | ||
| O(1)Mo(1)N(1) | 80.89(10) | ||
| O(2)Mo(1)N(1) | 172.87(10) | ||
| O(4)Mo(1)N(1) | 81.63(9) | ||
| O(3)Mo(1)N(1) | 78.05(9) | ||
| N(2)Mo(1)N(1) | 81.71(8) |
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В ИК-спектре ВКС I наблюдается характерное для внутрикомплексных соединений металлов с азометинами низкочастотное смещение полосы валентных колебаний связи С=N на 8 см–1 по сравнению с ее положением в спектре свободного лиганда (1640 см–1). В области 3100–3600 см–1 в спектре I сохраняется широкая интенсивная полоса поглощения валентных колебаний ОН-групп спиртовых фрагментов с максимумом при ∼3300 см–1, что с учетом результатов элементного анализа указывает на участие в координации лишь одной из трех спиртовых гидроксогрупп. В спектрах I наблюдается смещение серии полос в области ∼1000–1605 см–1, отвечающих колебаниям связей гетерокольца координированной молекулы пиридина [9]. Интенсивные полосы 930 и 907 см–1 относятся к симметричным и антисимметричным валентным колебаниям связей Мо=О цис-МоО2-групп. В области низких частот в ИК-спектрах комплексов появляются новые полосы поглощения при 675 и 550–580 см–1, которые следует отнести к валентным колебаниям связей Мо–NL и Мо–ОL соответственно [2].
На основании полученных экспериментальных и с учетом литературных данных можно предположить, что исследуемый комплекс [МоО2(L) · С5Н5N] имеет типичное для оксо- и диоксокатионов группы VIВ октаэдрическое строение с двумя кратносвязанными оксолигандами в цис-положении друг относительно друга. В транс-позициях к оксолигандам в соответствии с “правилом самосогласованности” [10] располагаются донорный атом N азометиновой группы и атом азота координированной молекулы пиридина. Остальные две вершины октаэдра в ВКС занимают два атома О депротонированных гидроксогрупп альдегидного и спиртового фрагментов в цис-позициях по отношению к оксолигандам.
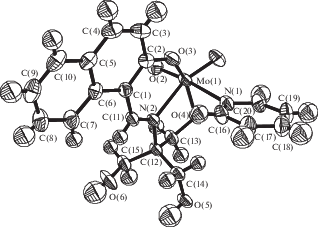
Строение ВКС I подтверждено методом РСА. В моноядерной молекуле (рис. 1) атом молибдена находится внутри октаэдра – он координирован двумя оксолигандами О(1), О(2), двумя атомами кислорода О(3), О(4) и атомом азота N(2) тридентатного бис(хелатного) двухзарядного лиганда (L)2–, атомом N(1) молекулы пиридина (Pу). В транс-позициях по отношению к лигандам О(оксо) располагаются, в соответствии с “правилом самосогласованности” [10], нейтральные атомы N(2), N(1), лигандов L, Py соответственно. Длины связей Mo–N(2) 2.272 и Мо–N(1) 2.476 Å существенно увеличены вследствие структурного проявления транс-влияния кратносвязанных оксолигандов. Эти связи также заметно длиннее стандартного расстояния Мо–N 2.10 Å [10]. Связи атомов Мо с атомами азота пиридина N(1) и лиганда L1 N(2) существенно (на 0.204 Å) различаются по длине. Связи Мо–О(оксо) (1.688, 1.691 Å) типичны по длине и соответствуют увеличенной кратности. Связи Мо–О(3,4)(L1)цис достаточно короткие – 1.950, 1.956 Å – и меньше стандартного расстояния Мо–О 2.04 Å [10]. Атом Мо смещен из центра октаэдра МоО4N2 к ребру О(1)(оксо)–О(2)(оксо): валентные углы О(оксо)Мо–О,Nцис, за одним исключением (О(1)МоN(1) = 80.9°), больше идеальной величины 90° (91.7°–101.9°), а противолежащие углы (О,N)Mo(O,N) – заметно меньше 90° (74.5°–81.70°). Самый большой валентный угол в структуре I – О(1)МоО(2) 106.0° – увеличен из-за отталкивания кратносвязанных оксолигандов. Углы между противолежащими донорными атомами лигандов (О(2)МоN(1) = = 172.9°, О(1)МоN(2) = 161.6°, O(3)MoO(4) = = 149.4°) в разной степени отклоняются от идеального значения 180°. При координации тридентатного лиганда L1 с атомом металла замыкаются два сопряженных по связи Мо–N(2) хелатных цикла: шестичленный МоNC3O (А) и пятичленный MoNC2O (Б). Металлоцикл А имеет несимметричную твист-конформацию с отклонением в разные стороны от четырех копланарных атомов NC3 (±0.016–0.036 Å) атомов Мо на 0.299 Å, О(3) – на –0.088 Å. Хелатный цикл Б имеет несимметричную конформацию с отклонением в одну сторону атомов Мо на 0.211 Å, С(13) – на –0.560 Å от плоскости атомов N(2), O(4), С(12). Двугранный угол между копланарными атомами плоскостей А [N(2), С(1), С(2), C(11)] и Б [N(2), O(4), С(12)] составляет всего 2.5°.
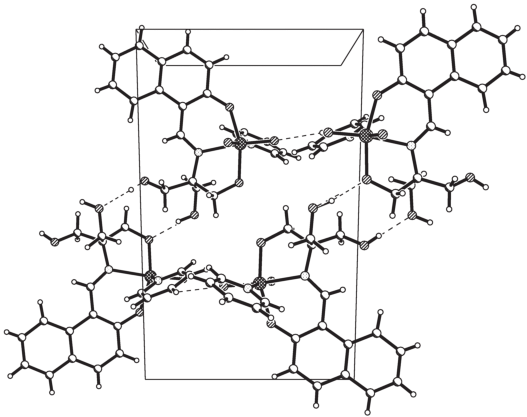
Молекулы I объединены двумя типами водородных связей О–Н···О с участием трех (из четырех) атомов кислорода лигандов L: одного хелатного О(4) и двух концевых О(5), О(6). Геометрические параметры водородных связей О(5)–Н(5А)···О(4А#1) (–х + 1, у + 1/2, z + 3/2): H···O = = 1.85, O···O = 2.723(3) Å, угол ОНО = 167°; О(6)–Н(6А)···О(5#1) (–х + 1, у + 1/2, z + 3/2): H···O = = 1.85, O···O = 2.670(3) Å, угол ОНО = 177°). За счет этих водордных связей формируются одномерные цепочки вдоль оси с кристалла (рис. 2).
Рентгеноструктурный анализ проведен в ЦКП ФМИ ИОНХ РАН. Работа выполнена в рамках государственного задания ИОНХ РАН в области фундаментальных научных исследований.
Список литературы
Сергиенко В.С., Абраменко В.Л., Порай-Кошиц М.А., Гарновский А.Д. // Журн. структур. химии. 1990. Т. 31. № 5. С. 54.
Сергиенко В.С., Абраменко В.Л., Сокол В.И. // Журн. неорган. химии. 2013. Т. 58. № 9. С. 1172.
Сергиенко В.С., Абраменко В.Л., Чураков А.В. и др. // Кристаллография. 2014. Т. 59. № 4. С. 589.
Гарновский А.Д., Васильченко И.С., Гарновский Д.А. // Современные аспекты синтеза металлокомплексов. Основные лиганды и методы. Ростов-на-Дону: ЛаПО, 2000. 355 с.
Zabierowski P., Szklarzewicz J., Kurpiewska K. et al. // Polyhedron. 2013. V. 49. № 1. P. 74.
Sui Y., Zeng X., Fang X. et al. // J. Mol. Catal. A. 2007. V. 270. № 1–2. P. 61.
Сергиенко В.С., Абраменко В.Л., Горбунова Ю.Е. // Журн. неорган. химии. 2018. Т. 63. № 1. С. 32.
Sheldrick G.M. // Acta Cryst. A. 2008. V. 64. № 1. P. 112.
Накамото К. ИК-спектры и спектры КР неорганических и координационных соединений. М: Мир, 1991. 536 с.
Пopaй-Koшиц M.A. // Izv. Jugosl. Cent. Kristallogr. (Zagreb). 1974. № 1. P. 19.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография