Кристаллография, 2020, T. 65, № 5, стр. 740-744
Силикат-германат Ba2K2In2[(Si0.8Ge0.2)6O18] · 2H2O – аналог природного цирконосиликата костылевита K4Zr2[Si6O18] · 2H2O
О. В. Реутова 1, Е. Л. Белоконева 1, *, О. В. Димитрова 1, А. С. Волков 1
1 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
* E-mail: elbel@geol.msu.ru
Поступила в редакцию 25.03.2020
После доработки 25.03.2020
Принята к публикации 16.04.2020
Аннотация
Методом гидротермального синтеза получены кристаллы нового силиката-германата Ba2K2In2[(Si0.8Ge0.2)6O18] · 2H2O, пр. гр. P21/n, a = 6.5548(6), b = 11.6946(10), c = 13.0203(11) Å, β = = 102.774(1)°. Структура аналогична структуре природного цирконосиликата костылевита K4Zr2[Si6O18] · 2H2O (пр. гр. P21/c) при замене атомов Zr на In, части K на Ba и вхождении в SiО4-тетраэдры изоморфной примеси атомов Ge. Шестерные тетраэдрические кольца из (Si,Ge)О4-тетраэдров соединены InО6-октаэдрами в смешанный каркас, в пустотах которого располагаются крупные катионы. Различие в записи групп связано лишь с выбором координатных осей и, соответственно, установки той же моноклинной группы.
ВВЕДЕНИЕ
Силикаты – самые распространенные в земной коре минералы, они хорошо изучены. Структурная кристаллохимия и систематика данного класса изложены в [1, 2], где проанализированы разнообразные комбинации кремнекислородных тетраэдров – от простейших изолированных группировок до сложнейших каркасов. Силикаты не только известны в природе, но и синтезированы с добавлением различных металлов. Важные в приложении свойства кристаллов обусловливают к ним большой интерес. Элемент германий представляет собой аналог кремния, однако как более крупный катион демонстрирует двоякую координацию: тетраэдрическую и октаэдрическую, которая для кремния достижима лишь при высоких давлениях. Для обоих элементов возможны как индивидуальные химические соединения, так и соединения с изоморфными замещениями в общей тетраэдрической позиции. Это силикаты-германаты, среди которых известны аналоги минералов санборнита, миларита, альбита, перриерита, фармакосидерита, рихтерита, апатита, граната, сфена, а также разнообразных цеолитов [3]. Недавно были синтезированы и структурно изучены новые представители силикатов-германатов: Cs2Pb2[(Si0.6Ge0.4)2O7] [4], Pb8K1.68Na0.32[(Ge0.65Si0.35)2О7]3 – силикато-германатный аналог минерала назонита [5], полярный германато-силикат K1.46Pb1.54Сa[(Ge0.23Si0.77)3O9] (ОН)0.54 · · 0.46Н2О с волластонитовой цепочкой и широким изоморфизмом [6], а также Cs2In2[(Si2.1Ge0.9)2O15](OH)2 · H2O [7]. Данное соединение обладает оригинальным строением, оно включает в себя новый тетраэдрический силикато-германатный слой, что определяет интерес к продолжению исследований силикатов-германатов индия. В настоящей работе приведены результаты гидротермального синтеза и исследования кристаллической структуры нового силиката-германата Ba2K2In2[(Si0.8Ge0.2)6O18] · 2H2O (I). Проведено сопоставление с изоструктурным минералом костылевитом K4Zr2[Si6O18] · 2H2O, а также минералом петараситом Na5Zr2[Si6O18] (Cl,OH) · · 2H2O.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез и свойства кристаллов. Кристаллы Ba2K2In2[(Si0.8Ge0.2)6O18] · 2H2O (I) получены в гидротермальных условиях из исходных компонентов Ba(OH)2 : In(NO3)3 : SiO2 : GeO2, взятых в массовых соотношениях 1 : 1 : 2 : 1. Шихту заливали водой, массовое отношение жидкой и твердой фазы составляло 1 : 5. В качестве минерализаторов в растворе присутствовали ионы K+, Cl– за счет добавления хлорида калия в концентрации 15 мас. %. Синтез проводили в стандартных автоклавах объемом 5–6 см3, футерованных фторопластом, при T = 280°С и P ∼ 100 атм. Нижний предел температуры был ограничен кинетикой гидротермальных реакций, верхний – возможностями аппаратуры. Коэффициент заполнения автоклава выбирали таким образом, чтобы давление оставалось постоянным. Время взаимодействия составляло 18–20 сут, что было необходимо для полного завершения реакции, после чего кристаллы промывали водой.
В опыте присутствовало большое количество белой рыхлой шихты, в которой были обнаружены бесцветные прозрачные призматические кристаллы, веерообразные сростки вплоть до мутноватых белесых сферолитов. Выход кристаллов составлял ∼50%. Их состав был определен на двух образцах – призматических сростках и сферолитах – с помощью рентгеноспектрального анализа, выполненного в лаборатории локальных методов исследования вещества МГУ на микрозондовом комплексе на базе растрового электронного микроскопа Jeol JSM-6480LV. Он показал присутствие в обеих разновидностях атомов In, Ba, K, Ge и Si, что подтвердило однофазность образцов.
Параметры ячейки монокристалла, представлявшего собой уплощенную призму (0.2 × 0.1 × × 0.05 мм), определены на дифрактометре XСalibur S c CCD-детектором. В базе данных ICSD [3] был найден минерал костылевит K4Zr2[Si6O18] · · 2H2O с близкими параметрами моноклинной ячейки. С учетом различия составов представляло интерес провести уточнение структуры и подтвердить структурную аналогию.
Рентгеноструктурное исследование. Трехмерный экспериментальный набор интенсивностей для исследования структуры I получен в полной сфере обратного пространства на дифрактометре Brucker SMART APEX II с CCD-детектором, графитовым монохроматором (излучение MoKα) и низкотемпературной приставкой для сбора данных при T = 180 K. Обработка данных выполнена с использованием программ APEX2. Была выбрана пр. гр. P21/n – нестандартная установка пр. гр. Р21/b центросимметричного минерала-аналога костылевита.
По программе SHELXS [8] прямыми методами найдены позиции тяжелых атомов: двух атомов Ba, трех атомов K и одного атома Si. Координационное окружение катионов атомами О, выявленными из разностных синтезов (всего было выявлено 10 позиций), показало, что Ва2 представляет собой атом In, K1, K2, K3 оказались атомами Si, а позиция Si отвечала атому K. Тепловые атомные смещения Si в тетраэдрических позициях различались, были занижены, а межатомные расстояния завышены, что указывало на изоморфное вхождение в них атомов Ge, выявленных при определении состава. Различались также межатомные расстояния. Для каждой из позиций последовательно определено соотношение атомов Si : Ge путем варьирования с шагом 0.05. Минимальному фактору расходимости, полученному при уточнении моделей, отвечали составы Si1 – (Si0.7Ge0.3), Si2 – (Si0.8Ge0.2), Si3 – (Si0.9Ge0.1). Однако формула обладала избыточным отрицательным зарядом. Оценка баланса валентных усилий показала, что большинство атомов входит в координацию тетраэдров, являясь мостиковыми или не мостиковыми атомами О, атом О10 входил в координацию лишь двух атомов Ва, т.е. был молекулой воды. Формула KBaIn(Si0.8Ge0.2)3O9 · Н2О подобна формуле костылевита K4Zr2[Si6O18] · · 2H2O и идентична ему при удвоении количества атомов. Итоговая формула Ba2K2In2[(Si0.8Ge0.2)6 O18] · · 2H2O, Z = 2.
Поглощение в кристалле с учетом его малых размеров было пренебрежимо мало. Заключительное уточнение позиционных и анизотропных тепловых смещений атомов выполнено методом наименьших квадратов с использованием комплекса программ SHELXL [8] с учетом аномального рассеяния Мо-излучения и путем варьирования весовой схемы. Все тепловые эллипсоиды имели положительные полуоси, а межатомные расстояния отвечали стандартным для найденных сортов атомов с учетом изоморфизма. Параметры эксперимента и результаты уточнения приведены в табл. 1, координаты атомов – в табл. 2, основные межатомные расстояния – в табл. 3. Информация о структуре имеется в Кембриджском банке данных (CSD № 1992423).
Таблица 1.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структуры Ba2K2In2[(Si0.8Ge0.2)6O18] · 2H2O
| Химическая формула | Ba2K2In2[(Si0.8Ge0.2)6O18] · 2H2O |
|---|---|
| М | 1124.46 |
| Сингония, пр. гр., Z | Моноклинная, P21/n, 2 |
| а, b, c, Å | 6.5548(6), 11.6946(10), 13.0203(11) |
| β, град | 102.774(1) |
| V, Å3 | 973.38(15) |
| Dx, г/см3 | 3.837 |
| Излучение; λ, Å | МоKα; 0.71073 |
| μ, мм–1 | 8.970 |
| Т, K | 293 |
| Размер образца, мм | 0.2 × 0.1 × 0.05 |
| Дифрактометр | Brucker SMART APEX II |
| Тип сканирования | Ω |
| θmах, град | 28.883 |
| Пределы h, k, l | –8 ≤ h ≤ 8, –15 ≤ k ≤ 15, –16 ≤ l ≤ 16 |
| Количество рефлексов измеренных/независимых с I ≥ 1.96σ/Rуср | 11 493/2347/0.0208 |
| Метод уточнения | МНК по F2(hkl) |
| Весовая схема | 1/[σ2(Fo)2 + (0.0177P)2], P = [max(Fo)2 + 2(Fc)2]/3 |
| Число параметров | 145 |
| Rall | 0.0245 |
| Rgt, Rwgt | 0.0236, 0.0727 |
| S | 2.579 |
| Δρmin/Δρmax, э/Å3 | –1.829/1.065 |
| Программы | SHELX |
Таблица 2.
Координаты базисных атомов и эквивалентные изотропные параметры в структуре Ba2K2In2[(Si0.8Ge0.2)6O18] · 2H2O
| Атом | x/a | y/b | z/c | Uэкв, Å2 |
|---|---|---|---|---|
| Ba | 0.20149(4) | 0.56151(2) | 0.40376(2) | 0.01256(9) |
| K | 0.70694(15) | 0.10891(11) | 0.39879(8) | 0.0210(2) |
| In | 0.10128(4) | 0.29292(2) | 0.22921(2) | 0.00486(9) |
| Si1* | 0.28797(11) | 0.24446(6) | 0.21648(4) | 0.00414(15) |
| Si2** | –0.07216(13) | 0.81430(7) | 0.33353(7) | 0.00622(17) |
| Si3*** | 0.31804(15) | 0.53397(8) | 0.15802(7) | 0.00557(19) |
| O1 | 0.0872(4) | 0.7408(3) | 0.2803(2) | 0.0089(6) |
| O2 | 0.1360(5) | 0.4719(3) | 0.2028(2) | 0.0098(6) |
| O3 | –0.0966(5) | 0.7438(3) | 0.4419(2) | 0.0106(6) |
| O4 | 0.0299(5) | 0.9386(2) | 0.3821(3) | 0.0117(6) |
| O5 | 0.5204(5) | 0.2632(3) | 0.5652(2) | 0.0109(6) |
| O6 | 0.4644(5) | 0.6152(2) | 0.2452(2) | 0.0111(6) |
| O7 | 0.2158(5) | 0.6074(3) | 0.0519(2) | 0.0117(6) |
| O8 | 0.2255(4) | 0.3350(3) | 0.3917(2) | 0.0092(6) |
| O9 | –0.2959(5) | 0.8345(3) | 0.2538(3) | 0.0146(7) |
| O10 (H2O) | 0.2264(5) | 0.5064(3) | 0.6156(3) | 0.0196(7) |
Таблица 3.
Основные межатомные расстояния d между катионами и анионами в структуре Ba2K2In2 [(Si0.8Ge0.2)6O18] · 2H2O
| Связь | Рассто-яние, Å | Связь | Рассто-яние, Å |
|---|---|---|---|
| Ba–O1 | 2.647(3) | K–O2 | 2.838(3) |
| Ba–O8 | 2.661(3) | K–O4 | 2.949(3) |
| Ba–O5 | 2.714(3) | K–O7 | 2.979(3) |
| Ba–O2 | 2.762(3) | K–O4 | 3.041(3) |
| Ba–O10 | 2.802(3) | K–O1 | 3.090(3) |
| Ba–O10 | 2.872(4) | K–O6 | 3.153(3) |
| Ba–O3 | 3.006(3) | K–O7 | 3.213(3) |
| Ba–O6 | 3.034(3) | K–O5 | 3.038(3) |
| Среднее Ba–O | 2.812 | Среднее K–O | 3.038 |
| In–O9 | 2.118(3) | Si2–O9 | 1.616(3) |
| In–O2 | 2.142(3) | Si2–O1 | 1.621(3) |
| In–O8 | 2.149(3) | Si2–O4 | 1.665(3) |
| In–O1 | 2.161(3) | Si2–O3 | 1.672(3) |
| In–O6 | 2.164(3) | Среднее Si2–O | 1.644 |
| In–O5 | 2.185(3) | ||
| Среднее In–O | 2.153 | ||
| Si1–O8 | 1.636(3) | Si3–O2 | 1.612(3) |
| Si1–O5 | 1.636(3) | Si3–O6 | 1.621(3) |
| Si1–O7 | 1.690(3) | Si3–O7 | 1.639(3) |
| Si1–O3 | 1.699(3) | Si3–O4 | 1.655(3) |
| Среднее Si1–O | 1.665 | Среднее Si3–O | 1.632 |
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Структура. Анионный радикал – шестерное кольцо в новом силикате-германате Ba2K2In2 [{(Si0.7Ge0.3)(Si0.8Ge0.2)(Si0.9Ge0.1)}2O18] · 2H2O – сформирован тремя независимыми тетраэдрами, которые слегка различаются заполнением позиций атомами Ge и Si с расстояниями, стандартными для данных сортов (табл. 2, 3). Далее они объединены вершинами изолированных InО6-октаэдров в каркас (рис. 1а) (расстояния In–O равны 2.119–2.185 Å). В крупных овальных каналах структуры с поперечными сечениями ∼6 × 4.8 Å, сформированных тетраэдрами и октаэдрами, располагаются катионы Ва, координированные атомами О на расстояниях до 3.034 Å (координационные числа 8 и 6), причем в координацию входят две молекулы воды, находящиеся в тех же полостях (рис. 1а). Атомы K находятся на стенках более узких каналов второго типа, обрамленных кремнекислородными кольцами. В проекции вдоль самой короткой оси а ячейки хорошо видно, что новый силикат-германат подобен костылевиту K4Zr2[Si6O18] · 2H2O [9] (рис. 1б) с учетом замены Zr на In, изоморфизма в тетраэдрах (Si,Ge)О4, а также заполнения более крупных каналов атомами Ва вместо части атомов K и молекулами воды. Меньшие в сечении каналы заняты атомами K в обеих структурах. Различие в установках пространственных групп связано с выбором координатных осей (рис. 2а). При выборе в качестве координатной оси с новой фазы диагонали ячейки костылевита и смене оси моноклинности с костылевита на b исследуемой фазы (в обоих случаях правые тройки координатных осей) группа меняется от P1121/b у костылевита до P121/n1 для силиката-германата. Параметры костылевита a = 6.565, b = 13.171, c = 11.727 Å, γ = = 105.3° отвечают параметрам новой фазы а = = ‒акост, b = cкост и с = aкост + bкост (табл. 1) с соответствующей сменой угла моноклинности γ на β.
Рис. 1.
Кристаллические структуры Ba2K2In2[(Si0.8Ge0.2)6O18] · 2H2O (а) и костылевита K4Zr2[Si6O18] · 2H2O (б) в аналогичных проекциях, показывающих идентичность смешанных каркасов. Показаны InО6- и ZrО6-октаэдры; SiО4-, (Si,Ge)О4-тетраэдры; шариками обозначены атомы K, Ba и молекулы воды.
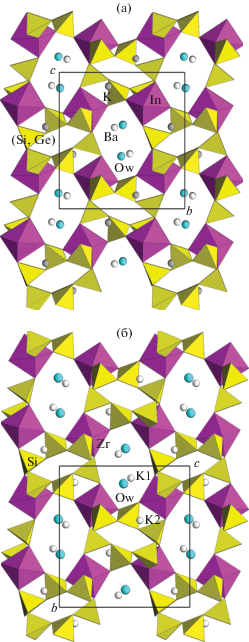
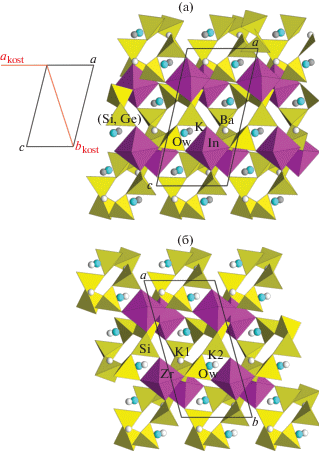
Рис. 2.
Проекции вдоль осей моноклинности в структурах Ba2K2In2[(Si0.8Ge0.2)6O18] · 2H2O (а) и костылевита K4Zr2[Si6O18] · 2H2O (б). Показаны InО6- и ZrО6-октаэдры, SiО4-, (Si,Ge)О4-тетраэдры; шариками обозначены атомы K, Ba и молекулы воды. Показана связь ячеек в двух установках одинаковой моноклинной пространственной группы.
Сопоставление с близким по составу и исследованным недавно силикат-германатом Cs2In2[(Si2.1Ge0.9)2O15](OH)2 · H2O [7] показывает, что в его структуре также имеется смешанный каркас, однако он образован InО6-октаэдрами и гофрированными слоями (Si,Ge)О4-тетраэдров. Атомы Cs и молекулы воды заполняют более крупные по сравнению с новым соединением каналы каркаса. К данной группе можно также отнести близкий по химической формуле минерал петарасит Na5Zr2[Si6O18](Cl,OH) · 2H2O [10 ] . Он, как и рассмотренный минерал костылевит и его новый аналог синтетический силикат-германат, имеет в структуре тот же анионный радикал: шестерное кольцо [Si6O18], соединенное ZrО6-октаэдрами в смешанный каркас. Однако параметры ячейки заметно отличаются: a = 10.796, b = 14.493, c = 6.623 Å, β = 113.2°, пр. гр. P121/m1. Замена крупных атомов K (Ва) на более мелкий Na, по-видимому, играет важную роль и приводит к структурной перестройке: кольца обладают зеркальной плоскостью m, расположение связывающих октаэдров также ей подчиняется, и итоговый смешанный каркас иной.
ЗАКЛЮЧЕНИЕ
Синтезирован и структурно исследован новый силикат-германат KBaIn(Si0.8Ge0.2)3O9 · Н2О. Анионный радикал представлен шестерными кольцами, объединенными в смешанный каркас InО6-октаэдрами, структура аналогична структуре минерала костылевита K4Zr2[Si6O18] · 2H2O. Новый член данного структурного типа иллюстрирует его достаточно широкие возможности в отношении гетеровалентного изоморфизма, причем несколько более крупный In3+, нежели Zr4+, коррелирует в структуре с вхождением более крупного Ge в SiО4-тетраэдр, что позволяет сохранить устойчивость каркаса с крупными атомами Ba и K в пустотах. Вхождение Na в петарасит Na5Zr2[Si6O18](Cl,OH) · 2H2O с аналогичной формулой заметно меняет структуру и топологию каркаса.
Авторы выражают благодарность С.М. Аксенову за помощь в получении экспериментальных данных, а также сотрудникам лаборатории локальных методов исследования вещества МГУ за определение состава кристаллов.
Список литературы
Liebau F. Structural Chemistry of Silicates. Structure, Bonding, and Classification. Berlin; Heidelberg: Springer-Verlag, 1985. 410 p.
Пущаровский Д.Ю. // Структурная минералогия силикатов и их синтетичексих аналогов. М: Недра, 1986. 160 с.
Inorganic Crystal Structure Data Base – ICSD. Fachinformationzentrum (FIZ) Karlsruhe. 2011. I version.
Belokoneva E.L., Morozov I.A., Volkov A.S. et al. // Solid. State Sci. 2018. V. 78. P. 69.
Белоконева Е.Л., Морозов И.А., Димитрова О.В., Волков A.С. // Кристаллография. 2018. Т. 63. № 6. С. 884.
Белоконева Е.Л., Морозов И.А., Димитрова О.В., Волков A.С. // Кристаллография. 2019 Т. 64. № 2. С. 228.
Белоконева Е.Л., Реутова О.В., Димитрова О.В., Волков А.С. // Кристаллография. 2020. Т. 65. № 4. С. 575.
Sheldrick G.M. // Acta Cryst. A. 2008. V. 64. P. 112.
Илюшин Г.Д., Хомяков А.П., Шумяцкая Н.С. и др. // Докл. АН СССР. 1981. Т. 256. С. 860.
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография


