Кристаллография, 2022, T. 67, № 3, стр. 376-383
Полиморфизм Li4P2O7: новая модификация и выделение структурных подсемейств тополого-симметрийным анализом
Е. Л. Белоконева 1, *, А. А. Гаганина 1, О. В. Димитрова 1, А. С. Волков 1
1 Московский государственный университет им. М.В. Ломоносова
Москва, Россия
* E-mail: elbel@geol.msu.ru
Поступила в редакцию 19.08.2021
После доработки 10.01.2022
Принята к публикации 10.01.2022
- EDN: LJFWPU
- DOI: 10.31857/S0023476122030055
Аннотация
В гидротермальных условиях получены кристаллы новой полиморфной разновидности пирофосфата Li4P2O7 как результат влияния минерализаторов. Традиционный кристаллохимический и тополого-симметрийный анализ строения нового полиморфа и исследованных ранее соединений позволили выделить два структурных подсемейства. Для первого характерны каркасы с вершинным сочленением LiO4-тетраэдров, для второго – с реберным сочленением, степень которого возрастает с повышением температуры и коррелирует с катионной проводимостью. Установлено, что условия получения кристаллов непосредственно влияют на структуру и их свойства. Для второго подсемейства, в котором структуры различаются лишь элементами симметрии, связывающими в каркас идентичные слои, содержащие LiO4-тетраэдры, из-за более высокой локальной симметрии промежуточных слоев из пирогрупп Р2О7, предложен группоид симметрии и предсказаны сложные и разупорядоченные варианты.
ВВЕДЕНИЕ
Силикаты обладают высокой термической устойчивостью, механической прочностью, разнообразными структурами, широко применяются в качестве материалов в технике. Германаты в природе практически не встречаются, однако известно немало синтетических соединений. Для пары элементов Si и Ge типичны изоморфные замещения в общей тетраэдрической позиции, такие соединения относятся к силикатам-германатам. С целью поиска новых силикатно-германатных фаз систематически проводили гидротермальный синтез в системах: PbO(Bi2O3)–SiO2–GeO2–Me2O–Z–H2O, Me = Li+, K+, Cs+, Rb+, Ba+, Cs+; Z = Cl–, F–, ${\text{CO}}_{3}^{{2 - }}$, P2O5, ${\text{NO}}_{3}^{ - }$, B2O3, где Mе и Z – минерализаторы, важная роль которых является предметом исследования. Выбор ионов свинца и висмута определен их сложными электронными оболочками и присутствием неподеленных электронных пар, что позволяет ожидать проявления нелинейно-оптических свойств у кристаллов с нецентросимметричными структурами.
В настоящей работе приведены достаточно неожиданные результаты синтеза новой модификации пирофосфата лития Li4P2O7 в системе, содержащей PbO, SiO2, GeO2, P2O5 и минерализатор LiNO3. Новая модификация была получена в результате влияния на кристаллизацию указанного минерализатора. Проведен традиционный кристаллохимический, а также тополого-симметрийный анализ как новой разновидности, так и известных соединений. Выявлены особенности строения всех модификаций, не установленные ранее, и показано существование двух структурных подсемейств Li4P2O7. Рассмотрено соотношение структура–проводимость, связанная с ионами лития.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез и состав кристаллов. Кристаллы нового пирофосфата лития получены в гидротермальных условиях в области средних температур в системе PbO : SiO2 : GeO2 : Р2О5 при массовом соотношении компонентов 1 : 1 : 1 : 2. LiNO3 в концентрации более 20 мас. % добавляли в раствор, обеспечивая высокую концентрацию ионов Li+ и ${\text{NO}}_{3}^{ - }$ как минерализаторов. Шихту заливали водой, массовое отношение жидкой и твердой фаз составляло 1 : 5. Синтез проводили в стандартном автоклаве объемом 5 см3, футерованном фторопластом, при T = 280°С и P ∼ 100 атм. Коэффициент заполнения автоклава выбран так, чтобы давление оставалось постоянным. Длительность эксперимента составила 21 день. В опыте были обнаружены тонкие бесцветные призматические кристаллы, а также их сростки. Выход кристаллов был небольшим и составлял ∼10%.
Определенные на дифрактометре XCalibur S с CCD-детектором параметры элементарной ячейки не имели аналогов в базе данных ICSD [1]. Состав кристаллов был определен с помощью рентгеноспектрального анализа, выполненного в лаборатории локальных методов исследования вещества МГУ на микрозондовом комплексе на базе растрового электронного микроскопа Jeol JSM-6480LV, который показал присутствие атомов P. По-видимому, полученная фаза является новым фосфатом лития и образовалась благодаря высокой концентрации минерализаторов.
Рентгеноструктурное исследование. Для рентгеноструктурного анализа был выбран небольшой и наиболее совершенный прозрачный тонкий уплощенный монокристалл размером 0.15 × × 0.75 × 0.05 мм. Экспериментальный набор дифракционных отражений получен в полной сфере обратного пространства на том же дифрактометре. Обработка данных выполнена по программе CrysAlis [2]. В качестве возможной пространственной группы рассматривали P$\bar {1}$, которая была подтверждена в ходе структурной расшифровки прямыми методами с использованием программы SHELXS [3] без предварительного знания химической формулы. Первоначально были определены позиции наиболее тяжелых атомов P. Из разностных синтезов найдены семь позиций для атомов О, входящих в координацию PО4-тетраэдров. На картах разностных синтезов электронной плотности также выявлены дополнительные позиции в структуре, координированные четырьмя атомами О. По межатомным расстояниям они отвечали атомам Li. Они были учтены в модели структуры, что согласовывалось с условиями получения кристаллов. Оценка баланса валентных усилий подтвердила присутствие атомов Li, P и О во всех локализованных позициях. Заключительная формула нового фосфата, определенная в ходе структурной расшифровки, Li4P2O7, Z = 2. Завышенный фактор расходимости, некоторый разброс параметров тепловых смещений и параметр Флэка показывали на необходимость учета двойникования. Полученная модель структуры включала слои, параллельные bc. Вероятно, существование двойникующей зеркальной плоскости mx, введение которой в виде матрицы (–1 0 0/0 1 0/0 0 1) в программе SHELXL [3] в изотропном приближении атомных смещений, позволило заметно снизить значение R-фактора с 7 до 4.5%, а также скорректировать параметры тепловых смещений атомов. Объем двойниковой компоненты составил BASF = 0.25. Уточнение в анизотропном приближении атомных смещений с варьированием весовой схемы и отбраковкой шести слабых “неудовлетворительных” рефлексов дало R = 3.56% при S = 1.063. Отметим низкие величины остаточных пиков электронной плотности, что говорит о достоверности структурного определения. Условия эксперимента и результаты уточнения структуры, координаты полученных атомов и межатомные расстояния даны в табл. 1, 2, 3. Информация о структуре имеется в Кембриджском банке структурных данных (CCDC № 2098880).
Таблица 1.
Кристаллографические характеристики, данные эксперимента и результаты уточнения структуры I
| Химическая формула | Li4P2O7 |
|---|---|
| М | 201.70 |
| Сингония, пр. гр., Z | Триклинная, P$\bar {1}$, 2 |
| a, b, c, Å | 5.1625(3), 7.5598(5), 7.8922(5) |
| α, β, γ, град | 64.674(6), 89.881(5), 89.888(5) |
| V, Å3 | 278.41(3) |
| Dx, г/см3 | 2.406 |
| Излучение | МоKα, 0.71073 |
| μ, мм–1 | 0.759 |
| T, K | 293 |
| Размер образца, мм | 0.15 × 0.075 × 0.05 |
| Дифрактометр | XCalibur S |
| Тип сканирования | Ω |
| θmax | 30.77 |
| Пределы hkl | –7 ≤ h ≤ 7, –10 ≤ k ≤ 10, –11 ≤ l ≤ 11 |
| Количество рефлексов измеренных/независимых/с I ≥ 1.96 σ(I)/Rуср | 4489/1550/1399/0.0402 |
| Метод уточнения | МНК по F2(hkl) |
| Весовая схема | 1/[σ2(Fo)2 + (0.0263P)2 + + 0.0547P], где P = ((Fo)2 + 2(Fc)2)/3 |
| Число параметров | 119 |
| Rall | 0.0422 |
| Rgt, Rwgt | 0.0356, 0.074 |
| S | 1.063 |
| Δρmin/Δρmax, э/Å3 | –0.46/0.43 |
| Программы | SHELX |
Таблица 2.
Координаты базисных атомов и эквивалентные изотропные параметры для структуры I
| Атом | x/a | y/b | z/c | Uэкв, Å2 |
|---|---|---|---|---|
| P1 | 0.31382(15) | 0.14604(9) | 0.68033(9) | 0.0085(2) |
| P2 | 0.18848(15) | 0.43453(9) | 0.82252(9) | 0.0090(2) |
| O1 | 0.3191(4) | 0.2924(3) | 1.0036(2) | 0.0121(4) |
| O2 | 0.1940(4) | 0.1416(2) | 0.5062(2) | 0.0119(4) |
| O3 | 0.1808(4) | 0.0001(3) | 0.8584(2) | 0.0117(4) |
| O4 | –0.1024(4) | 0.4341(3) | 0.8390(3) | 0.0138(4) |
| O5 | 0.6016(4) | 0.1149(3) | 0.6892(2) | 0.0146(4) |
| O6 | 0.3042(4) | 0.6397(2) | 0.7504(2) | 0.0118(4) |
| O7 | 0.2585(4) | 0.3620(2) | 0.6633(2) | 0.0140(4) |
| Li1 | –0.3086(10) | 0.2691(7) | 1.0431(6) | 0.0160(10) |
| Li2 | 0.1869(10) | 0.8584(6) | 0.5192(6) | 0.0158(9) |
| Li3 | 0.8043(10) | –0.0234(6) | 0.9012(6) | 0.0141(9) |
| Li4 | 0.3094(11) | 0.3320(7) | 0.2523(6) | 0.0180(10) |
Таблица 3.
Основные межатомные расстояния между катионами и анионами в тетраэдрах в структуре I
| Связь | Расстояние, Å | Связь | Расстояние, Å |
|---|---|---|---|
| P1–O5 | 1.501(2) | P2–O4 | 1.507(2) |
| P1–O2 | 1.522(2) | P2–O6 | 1.527(2) |
| P1–O3 | 1.529(2) | P2–O1 | 1.530(2) |
| P1–O7 | 1.605(2) | P2–O7 | 1.612(2) |
| Среднее | 1.539 | Среднее | 1.544 |
| Угол Р1–О7–Р2 130.31° | |||
| Li1–O1 | 1.943(6) | Li2–O2 | 2.099(5) |
| Li1–O3 | 1.956(5) | Li2–O5 | 1.910(5) |
| Li1–O6 | 2.023(5) | Li2–O6 | 1.962(5) |
| Li1–O4 | 1.888(5) | Li2–O2' | 1.977(5) |
| Среднее | 1.955 | Среднее | 1.987 |
| Li3–O1 | 1.950(5) | Li4–O1 | 2.109(5) |
| Li3–O3 | 1.968(6) | Li4–O2 | 1.993(5) |
| Li3–O3' | 1.980(5) | Li4–O4 | 1.922(5) |
| Li3–O5 | 1.869(5) | Li4–O6 | 2.006(6) |
| Среднее | 1.942 | Среднее | 2.008 |
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В кристаллической структуре новой модификации Li4P2O7 (I) имеются пирофосфатные сдвоенные тетраэдры [P2O7]4–, а вся структура составлена из тетраэдров, характерных как для атомов фосфора, так и для атомов лития, совместно образующих каркас. Расстояния в РО4-тетраэдрах стандартные и, как это известно для фосфатов, расстояния до мостикового атома кислорода О7 увеличены (табл. 3). Все четыре базисных атома Li находятся в достаточно правильных тетраэдрах со средними расстояниями ∼1.97 Å. В силу низкой валентности ионов лития Li+ наличие одной общей вершины – атома О – более чем у двух тетраэдров не противоречит правилу Полинга. Так, атомы О1 и О2 являются общими для трех LiО4-тетраэдров и одного РО4-тетраэдра, что отвечает идеальной сумме валентностей на ионе О2–. Каждый из атомов О4, О5 и О6 объединяет два LiО4-тетраэдра и один РО4-тетраэдр. Атом О3 принадлежит одному LiО4-тетраэдру и одному РО4-тетраэдру. Наиболее четко особенность каркаса прослеживается в проекции на плоскость bc, а угол моноклинности α, близкий к 60°, обусловливает определенную псевдогексагональность каркаса и структуры в целом (рис. 1). Подобное сочленение сразу нескольких тетраэдров в одной вершине известно для бора согласно базе данных ICSD [1], например в CaBO2, где имеется двойной слой B3+О4-тетраэдров, или в PbB4O7, или в минерале клиноэдрите CaZnSiO4·H2O, где тетраэдрический слой сформирован Si4+О4- и Zn2+О4-тетраэдрами.
Рис. 1.
Проекция кристаллической структуры Li4P2O7 (I) на плоскость bc, показаны РО4- и LiO4-тетраэдры.

В каркасе новой модификации I можно отметить слой, перпендикулярный оси а (рис. 2). Все тетраэдры, фосфорные и литиевые, ориентированы вверх и вниз относительно слоя. Выделяются тригональные окна-кольца, сформированные шестью тетраэдрами: четырьмя LiО4-тетраэдрами, обращенными попарно вверх и вниз относительно слоя, и двумя PО4-тетраэдрами, также обращенными вверх и вниз относительно слоя. Треугольные основания тетраэдров формируют слегка искаженный плотноупакованный слой из атомов O с вакансиями в центрах колец. Как отмечалось выше, большинство атомов О принадлежит одновременно трем тетраэдрам с учетом выше- и нижерасположенных атомов и лишь мостиковый атом О7 относится к двум РО4-тетраэдрам.
Рис. 2.
Проекция одного слоя каркаса кристаллической структуры Li4P2O7 (I) на плоскости bc (а) и ab (б). Показаны РO4- и LiO4-тетраэдры.

Пирофосфаты различных металлов отличаются большим количеством полиморфов [1]. Известны несколько полиморфных модификаций и Li4P2O7, которые будут рассмотрены ниже. Исследованная структура наиболее близка к метастабильному “псевдомоноклинному” полиморфу Li4P2O7 [4], отличающемуся от I удвоенным параметром b (параметр а для I). Кристаллы этого соединения получены первоначально из раствора, а затем подвергнуты выпариванию и высушиванию, образовалась монофаза в виде кристаллического порошка. Для получения монокристаллов образец был доведен до плавления, и затем расплав был закален на воздухе. Это привело к образованию одновременно двух метастабильных полиморфов Li4P2O7: “псевдомоноклинного”, наиболее близкого к I, и нового тригонального (пр. гр. P3212). Получены монокристаллы тригонального полиморфа и исследована их структура, монокристаллы триклинной “псевдомоноклинной” модификации для исследования получить не удалось. Структура расшифрована методом Ритвельда (R = 7.62%) прямыми методами (программа ENDEAVOUR [5]). В проекции аb можно выявить слабое расщепление перекрывающихся О-вершин тетраэдров (рис. 3) по сравнению с исследованной структурой (рис. 1). Структура новой модификации I определена на монокристалле, что гарантирует ее надежность. Если бы двойникование осуществлялось в соотношении 1 : 1 (BASF = 0.5), то имелся бы новый полиморф с удвоенным плоскостью mz параметром а вдоль направления чередования слоев и иной группой симметрии. Он отличался бы от метастабильной “псевдомоноклинной” фазы, где удваивание обусловлено практически трансляционным повтором, но с небольшим нарушением. Стабильные условия роста в рассматриваемом случае позволили получить в кристаллах почти правильное расположение слоев с разупорядочением на четверть (BASF = 0.25). Новая тригональная модификация принципиально отличается от рассмотренных ранее сочленением LiО4-тетраэдров в цепочки и далее в слои, которые затем соединяются в каркас пирогруппами, так что LiО4- и РО4-тетраэдры находятся в разных относительно оси с слоях. В [4] известные полиморфы Li4P2O7 сопоставлены по расположению пирофосфатных групп. Отмечено их “колеблющееся” расположение в структурах фаз, полученных в метастабильных условиях.
Рис. 3.
Проекция кристаллической структуры метастабильной “псевдомоноклинной” модификации Li4P2O7 на плоскость аb.

Намного раньше были синтезированы и исследованы два других полиморфа. Моноклинная модификация Li4P2O7 [6] получена методом гидротермального синтеза при высоком давлении Р = 1000 атм и температуре выше 600°С. Она построена, как и все полиморфы, из LiО4- и РО4-тетраэдров, связанных между собой в каркас. По сравнению с различной ориентацией тетраэдров в пирогруппах Р2О7 в I (рис. 1) и в метастабильной фазе (рис. 3) наблюдается их одинаковая ориентация в моноклинной фазе [6]. Высокотемпературная триклинная модификация Li4P2O7 [7] синтезирована путем нагревания смеси исходных компонентов, растирания и расплавления в платиновом тигле при 650°С и закалки до комнатной температуры. Как и в моноклинной фазе, в триклинной модификации одинаковая ориентация РО4-тетраэдров в диортогруппе. В обеих структурах отсутствуют также мостиковые атомы кислорода, принадлежащие только РО4-тетраэдрам, поскольку с этой вершиной сочленен и LiO4-тетраэдр в отличие от I и метастабильной “псевдомоноклинной” фазы. Принципиальное отличие двух данных структур от I и метастабильной “псевдомоноклинной” фазы состоит в наличии реберной связи между LiО4-тетраэдрами. Общая симметрия каркаса и структур заметно отклоняется от псевдогексагональной симметрии, описанной выше.
Анализ строения моноклинной и триклинной модификаций показывает, что в каркасах имеются одинаковые структурные фрагменты. Это четверки связанных ребрами LiО4-тетраэдров, объединенных в ленты парами связанных ребрами LiО4-тетраэдров с формулой [Li8О18]∞ (число атомов О дано без учета поделенных вершин с РО4-тетраэдрами). В моноклинной структуре ленты вытянуты вдоль оси а, а в триклинной – вдоль оси с. Ракурсы, представленные на рис. 4а, 4б, позволяют определить “слои” L1, в которых ленты (рис. 4в), располагающиеся в данных проекциях в торце, выделены овалами. Симметрия каждого такого “Li-слоя” = L1 отвечает группе Р$\bar {1}$: центры инверсии обеих структур расположены в этих “Li-слоях”. Отличаются элементы симметрии, связывающие эти слои в каркас каждой из структур: оси 21 в моноклинной (рис. 4а) и центры инверсии $\bar {1}$ в триклинной модификациях (рис. 4б). В [7] подобная связь не установлена, и соотношение осей двух модификаций иное: aмон= стрикл, bмон= атрикл + 2bтрикл, смон= атрикл – bтрикл (рис. 4а, 4б) (оптимально структуры сопоставляются при повороте на 180° триклинной ячейки вдоль оси смон).
Рис. 4.
Проекции двух высокотемпературных полиморфов Li4P2O7 второго семейства и общего фрагмента структур: а – моноклинного полиморфа на плоскость bc, б – триклинного полиморфа на плоскость ab, в – лента из LiO4-тетраэдров в проекции на плоскость bc. Обозначены элементы симметрии пр. гр. P21/n и элементы симметрии групп “слоев” L1 и L2, локальные центры инверсии и оси 21 “слоя” L2 находятся на высоте 1/4. Показаны LiO4-тетраэдры, РО4-тетраэдры показаны только в слое L2, атомы Р обозначены шарами. Овалом выделена лента из LiO4-тетраэдров.
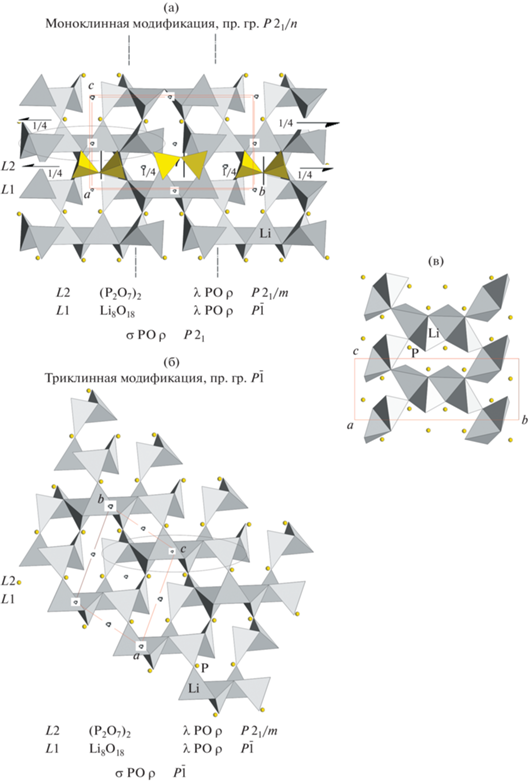
Причиной подобного двойного варианта симметрийной связи слоев L1 и существования двух структурных модификаций является более высокая симметрия второго “слоя” L2, представленного пирогруппами Р2О7. Отметим, что “слой” L2 – двумерная периодическая единица, которая в кристаллохимическом смысле не является слоем. То же справедливо для слоя L1. Собственная симметрия L2 отвечает группе P21/m, в которой зеркальная плоскость m (рис. 4а) носит локальный характер, является элементом симметрии только этого слоя, а вся группа характеризуется частичными операциями λPO (Partial Operation) [8], не справедливыми для соседних слоев. Оба элемента симметрии – центр инверсии и винтовая ось – равноправные в группе, представляют собой ее минимальные подгруппы и дают два варианта сочленения “слоев”. Поскольку симметрия “слоя” L2 выше (N = 4) по сравнению со “слоем” L1 (F = = 2), согласно теореме Дорнбергер–Шифф в ее теории OD-структур [8] число вариантов Z = N/F определяется отношением порядков симметрии групп слоев, и здесь Z = 4/2 = 2. Каждая из двух структур, представленных на рис. 4, является MDO-политипом (MDO – Maximal Degree of Order) с максимальной степенью порядка, поскольку все “слои” сочленены в пары одинаково: либо центрами инверсии $\bar {1}$, либо винтовыми осями 21, и данные операции обозначаются как σРО [8]. При упорядоченном чередовании операций, например $\bar {1}$, 21, $\bar {1}$, 21, …, будет существовать другая, так называемая периодическая структура с бóльшим периодом вдоль направления чередования слоев и иной симметрией. Таким образом, разнообразие возможных политипных модификаций обусловливается различным чередованием слоев в тройках вдоль оси а моноклинной структуры или диагонали триклинной, что характеризуется как одномерный полиморфизм. При отсутствии порядка в расположении слоев будут образовываться разупорядоченные структуры. Данное семейство описывается группоидом симметрии согласно [8]:
Два последних полиморфа получены в условиях высоких температур и давлений. В силу этого они близки друг другу, имеют существенную долю реберных связей LiO4-тетраэдров и отличаются от исследованного соединения I, полученного в условиях мягкого гидротермального синтеза, в котором соединение по ребрам отсутствует. Таким образом, исследованная структура I, так же как и родственная ей метастабильная фаза, принадлежит одному подсемейству, а моноклинная и триклинная разновидности – другому.
Литиевые фосфаты привлекают интерес в силу их катионной проводимости. Проводимость Li4P2O7 исследована в [10], где была повторно получена триклинная модификация [7]. Она была нагрета in situ от комнатной температуры до 950 K, был зафиксирован переход в моноклинную фазу, которая, однако, отличается от всех исследованных. Два LiО4-тетраэдра из четырех независимых сильно искажены, что можно объяснить возможными смещениями атомов за счет проводимости при высокой температуре. В [10] выявлены каналы, которые проходят через тетраэдры и между ними. Рассмотрение структуры новой высокотемпературной моноклинной фазы [10] показало, что произошла существенная перестройка: образовались сплошные, связанные ребрами цепочки LiО4-тетраэдров, чередующиеся с цепочками из четверок LiО4-тетраэдров, связанных ребрами (рис. 5). Вероятно, такие структурные изменения способствуют проводимости по литию, что не отмечено в [10].
Рис. 5.
Проекция на плоскость ас высокотемпературной моноклинной модификации (пр. гр. P21/n), полученной in situ в [10], даны LiO4-тетраэдры, атомы Р обозначены шарами.

В структуре новой тригональной модификации – второй метастабильной фазы [4] – LiO4-тетраэдры связаны в цепочки наподобие пироксеновых с симметрией g. Далее они образуют на том же уровне слой тетраэдров одной ориентации зеркальными псевдоплоскостями m и затем путем сочленения по ребрам удваиваются горизонтальными осями 2 пр. гр. Р3212 в плотный двойной неполярный слой. Отличие тригонального полиморфа от всех рассмотренных выше, как отмечалось, состоит в слоистом строении, проводимость по ионам лития в нем не исследована.
ВЫВОДЫ
В гидротермальных условиях синтезированы монокристаллы нового полиморфа Li4P2O7 (I) и изучена их структура. Выявлен закон двойникования кристаллов с долей компоненты BASF = = 0.25. Кристаллохимическое сопоставление I с недавно полученным и исследованным метастабильным полиморфом показало, что он отличается одним из параметров триклинной ячейки. Показано, что соединение I и метастабильный “псевдомоноклинный” полиморф, в которых все тетраэдры связаны вершинами, образуют подсемейство, отличающееся своим строением от исследованных ранее других разновидностей, составляющих второе подсемейство, в которых LiO4-тетраэдры связаны и по ребрам. Закон его строения определен в рамках тополого-симметрийного анализа OD-теории, где решающую роль играют выделение структурных единиц (слоев) и анализ их симметрии. Так, моноклинная и триклинная структуры отличаются друг от друга лишь симметрийным способом связи одинаковых “слоев” L1 в каркасах за счет более высокой локальной симметрии промежуточных “слоев” из пирогрупп Р2О7. Записан группоид симметрии для второго подсемейства. Наличие двух подсемейств определяется различными условиями ростовых экспериментов: мягкого гидротермального синтеза для первого подсемейства и высокотемпературного для второго. Детально описано реберное сочленение тетраэдров во втором подсемействе, которое рассматривается как результат условий получения кристаллов, усиливается при повышении температуры и влияет на катионную проводимость.
Авторы выражают благодарность Н.В. Зубковой за помощь в получении экспериментальных данных, а также сотрудникам лаборатории локальных методов исследования вещества МГУ за определение состава кристаллов.
Список литературы
Inorganic Crystal Structure Data Base – ICSD. Fachinformationzentrum (FIZ) Karlsruhe. 2011. I version.
Agilent Technologies, CrysAlisPro Software System, version 1.171.3735. Agilent Technoligies UK Ltd. Oxford, UK, 2014.
Sheldrick G.M. // Acta Cryst. A. 2008. V. 64. P. 112.
Raguz B., Wittich K., Glaum R. // Eur. J. Inorg. Chem. 2019. V. 2019. № 11–12. P. 1688. https://doi.org/10.1002/ejic.201801100
Putz H., Schoen J.C. Endeavour 1.7, Crystal Impact GbR, Bonn, Germany. 2009.
Якубович О.В., Мельников О.К. // Кристаллография. 1994. Т. 39. № 5. С. 815.
Daidouh A., Veiga M.L., Pico C., Martinez-Ripoll I.M. // Acta Cryst. C. 1997. V. 53. P. 167.
Dornberger-Schiff K. // Abh. Deutsch. Akad. Wiss. Berlin. 1964. B. 3. S. 1.
Grell H., Dornberger-Schiff K. // Acta Cryst. A. 1982. V. 38. P. 49.
Voronin V.I., Sherstobitova E.A., Blatov V.A., Shekhtman G.S. // J. Solid State Chem. 2014. V. 211. P. 170. https://doi.org/10.1016/j.jssc.2013.12.015
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография


