Кристаллография, 2023, T. 68, № 1, стр. 86-93
Развитие рентгеновских методов исследования белковых планарных систем на поверхности жидкости с использованием синхротронного излучения
М. С. Фоломешкин 1, 2, *, А. Е. Благов 1, 2, А. С. Бойкова 2, Ю. А. Волковский 1, 2, Ю. А. Дьякова 1, 2, К. Б. Ильина 1, 2, М. А. Марченкова 1, 2, Ю. В. Писаревский 1, 2, П. А. Просеков 1, А. В. Рогачев 2, А. Ю. Серегин 1, 2, М. В. Ковальчук 1, 2, 3
1 Институт кристаллографии им. А.В. Шубникова ФНИЦ “Кристаллография и фотоника” РАН
Москва, Россия
2 Национальный исследовательский центр “Курчатовский институт”
Москва, Россия
3 Санкт-Петербургский государственный университет
Санкт-Петербург, Россия
* E-mail: folmaxim@gmail.com
Поступила в редакцию 15.02.2022
После доработки 13.03.2022
Принята к публикации 15.03.2022
- EDN: DOLMPH
- DOI: 10.31857/S0023476123010083
Аннотация
Представлены результаты исследования структуры ленгмюровских пленок лизоцима на поверхности жидкости, сформированных из кристаллизационных растворов с добавлением в качестве осадителя ряда хлоридов металлов. Методом рентгеновской рефлектометрии определены толщины и плотности исследуемых пленок, а методом стоячих рентгеновских волн в области полного внешнего отражения получены профили распределения концентрации атомов серы, содержащихся в молекулах белка, и ионов осадителей в приповерхностной области субфазы. На основе полученных результатов проведен анализ зависимости структуры формируемых пленок от использованного осадителя и некоторых особенностей применения методов рентгеновской рефлектометрии и стоячих рентгеновских волн в исследовании ленгмюровских пленок глобулярных белков на поверхности жидкости.
ВВЕДЕНИЕ
В настоящее время все больший интерес вызывает возможность использования молекул белков в качестве функциональных элементов различных биоэлектронных гибридных систем, например высокочувствительных сенсорных устройств [1–3]. Перспективными представляются планарные системы, в которых молекулы белков образуют упорядоченные ансамбли с контролируемыми параметрами структуры: толщиной, плотностью, ориентацией молекул. Необходимость контроля параметров структуры с нанометровой точностью накладывает высокие требования как на технологии формирования, так и на методы исследования подобных систем.
Ленгмюровская технология является одним из наиболее эффективных методов получения упорядоченных молекулярных белковых слоев с возможностью сохранения конформационного состояния молекул белка. В [4–9] была предложена и на примере модельного белка лизоцима апробирована принципиально новая методика формирования ленгмюровских пленок, заключающаяся в использовании кристаллизационного раствора белка с добавлением различных осадителей. Хорошо известно, что добавление осадителей в растворы глобулярных белков может способствовать перераспределению поверхностного заряда молекул белка и изменению межмолекулярного взаимодействия – возникновению притяжения вместо отталкивания [10]. Кроме того, как было показано в предыдущих работах по исследованию кристаллизационных растворов белков [11–22], добавление осадителей приводит к образованию определенных олигомеров белков, служащих кластерами-прекурсорами в процессе дальнейшей кристаллизации. Так, добавление хлоридов одно- и двухвалентных металлов в раствор белка лизоцима приводит к образованию стабильных олигомеров – димеров и октамеров, участвующих в формировании структуры кристаллов лизоцима тетрагональной сингонии [11–16, 18, 21, 22]. Было выдвинуто предположение, что использование кристаллизационного раствора белка с осадителем должно приводить к изменению структуры формируемой ленгмюровской пленки, так как образующиеся в растворе олигомеры могут участвовать в процессе образования монослоя. Для подтверждения данного предположения был проведен ряд исследований пленок белка лизоцима, сформированных из растворов с различными осадителями как на поверхности жидкости, так и на твердых подложках [4–9].
Исследования на поверхности жидкости представляют особый интерес при изучении взаимодействия ионов осадителя с молекулами белка. Данная информация необходима для понимания механизмов образования предкристаллизационной фазы в белковых растворах и участия образующихся олигомеров как в процессе кристаллизации, так и при формировании ленгмюровских пленок. Ранее [7] с применением метода стоячих рентгеновских волн (СРВ) исследовали пленки лизоцима, сформированные на поверхности жидкости из кристаллизационного раствора с добавлением хлорида калия. Было продемонстрировано увеличение толщины при получении пленки из кристаллизационного раствора с осадителем, а также ее стабильность в течение более 10 ч после формирования; кроме того, определены профили распределения ионов осадителя. Однако исследования методом рентгеновской рефлектометрии (РР) в данной работе не проводились из-за ограниченного углового диапазона сканирования, доступного на экспериментальной установке. В то же время РР является прямым методом восстановления профиля распределения электронной плотности, что позволяет повысить точность определения толщины пленки и интерпретации экспериментальных данных, полученных методом СРВ.
В настоящей работе представлены результаты исследования структуры ленгмюровских пленок лизоцима на поверхности жидкости с проведением измерений методами РР и СРВ в рамках одного эксперимента на станции P08 EMBL (DESY, Гамбург, Германия). Исследовали пленки, сформированные из кристаллизационных растворов белка без осадителя и с осадителями KCl, NiCl2, CuCl2.
ТЕОРИЯ
Метод РР. Этот метод применяется для изучения структуры многослойных систем с толщинами слоев от единиц до сотен нанометров. Метод чувствителен к градиенту электронной плотности ρe по нормали к поверхности исследуемой системы и дает усредненную вдоль слоев информацию, что некритично для гомогенных слоев. В методе используют так называемую скользящую геометрию падения рентгеновского пучка и анализируют угловые зависимости интенсивности зеркальной компоненты отраженного излучения. Интерференция отраженных от разных границ многослойной системы волн приводит к возникновению на кривой зеркального отражения характерных осцилляций. Анализ кривых отражения позволяет восстановить профиль распределения электронной плотности по глубине исследуемой системы и определить такие параметры, как толщины и плотности слоев, а также охарактеризовать межслоевые границы.
Для анализа кривых зеркального отражения необходимо решить задачу об отражении рентгеновского излучения от исследуемой многослойной системы. Для этого рассмотрим идеальную систему, состоящую из произвольного числа N параллельных слоев с резкими границами, каждый из которых характеризуется толщиной dn и комплексной поляризуемостью [23] χn: Re(χn) ~ ~ ρe. Будем считать слои гомогенными и определим систему координат таким образом, чтобы координата x была направлена вдоль поверхности, а координата z – от верхней границы вглубь слоя; нумерацию n слоев будем вести сверху вниз. Отсчет координаты от верхних границ слоев обусловлен в данном случае более компактной формой записи некоторых представленных далее формул по сравнению с другими системами координат.
Пусть теперь плоская монохроматическая волна длиной λ падает из вакуума на поверхность многослойной системы под скользящим углом θ. На каждой межслоевой границе излучение претерпевает преломление и отражение, причем зависимость электрического поля от координаты x можно считать постоянной по глубине системы ввиду гомогенности слоев и малости угла θ. Тогда поле в произвольном слое n записывается в виде
где Tn и Rn – амплитуды отраженной и преломленной волн на нижней границе слоя, kn = k(χn + + ${{\sin }^{2}}\theta $)1/2 – проекции волновых векторов на ось z, k = 2π/λ, λ – длина волны излучения.Интенсивность зеркального отражения найдем из условий непрерывности тангенциальных компонент электрического и магнитного полей на границе между двумя слоями. Малое значение θ позволяет рассмотреть только более простой случай σ-поляризации, когда амплитуды электрического поля перпендикулярны плоскости отражения (x, z):
(2)
$\begin{gathered} {{T}_{n}}({{c}_{n}} + {{X}_{n}}c_{n}^{{--1}}) = {{T}_{{n + 1}}}(1 + {{X}_{{n + 1}}}), \\ {{k}_{n}}{{T}_{n}}({{c}_{n}}--{{X}_{n}}c_{n}^{{ - 1}}) = {{k}_{{n + 1}}}{{T}_{{n + 1}}}(1--{{X}_{{n + 1}}}), \\ \end{gathered} $Отметим, что в реальных тонкопленочных мономолекулярных системах на основе глобулярных белков отсутствуют резкие границы между слоями, что обусловлено неравномерным распределением электронной плотности в молекулах белка. Для расчета отражения от таких систем удобно представить поляризуемость в виде плавно меняющейся функции χ(z), которую необходимо разбить на достаточно тонкие слои, в пределах которых изменением χ(z) можно пренебречь. В результате расчет для такой структуры можно проводить как для обычной многослойной системы с большим количеством слоев с резкими границами.
Метод СРВ. С помощью данного метода [25–27] анализируют экспериментальные кривые интенсивности вторичных процессов (например, рентгеновской флуоресценции) в зависимости от угла θ падения рентгеновского излучения на исследуемую многослойную систему. В окрестности критического угла θcr = [Re(χ)]1/2 интенсивность отраженного от границы системы пучка сравнима с интенсивностью падающего излучения. В области перекрытия падающего и отраженного пучков в результате конструктивной и деструктивной интерференции формируется СРВ, период пучностей и узлов которой зависит от угла θ. Это позволяет буквально просканировать исследуемую многослойную систему и получить характерную угловую зависимость интенсивности выхода рентгеновской флуоресценции, определяемую распределением концентрации флуоресцирующих атомов по глубине структуры.
Для расчета интенсивности поля СРВ в многослойной системе необходимо определить амплитуды отраженной Tn и преломленной Rn волн в каждом слое. Для этого еще раз воспользуемся системой (2), решение которой для амплитуд преломленных волн Tn приводит к следующей рекуррентной формуле:
(5)
${{T}_{{n + 1}}} = {{T}_{n}}({{c}_{n}} + {{X}_{n}}c_{n}^{{--1}}){\text{/}}(1 + {{X}_{{n + 1}}}).$В дипольном приближении интенсивность выхода рентгеновской флуоресценции атомов определенного сорта пропорциональна интенсивности поля рентгеновского излучения в данной точке. В этом случае угловую зависимость интенсивности флуоресценции многослойной системы можно записать в следующем виде:
где I(z, qz) – распределение интенсивности поля СРВ по глубине системы; Ca(z) – распределение концентрации атомов данного сорта; μ(z) – функция, учитывающая поглощение флуоресцентного сигнала в многослойной системе.МАТЕРИАЛЫ И МЕТОДЫ
Реагенты. В работе использовали белок лизоцим из куриного яйца производства Sigma-Aldrich (CAS № 12650-88-3), KCl (CAS № 7447-40-7, abcr GmbH), LiCl (ТУ 6-09-3751-83, Лаверна Стройинжиниринг), NiCl2 (CAS № 7791-20-0, Alta Aesar) и CuCl2 (CAS № 7447-39-4, Acros Organics). Растворы веществ были приготовлены с использованием ультрачистой воды Millipore (сопротивление воды 18 МОм см). Белок и соли растворяли в натрий-ацетатном буфере концентрацией 0.2 М, рН 4.5. Растворы солей фильтровали с помощью мембранных шприцевых фильтров Millex с размером пор 0.22 мкм, раствор белка центрифугировали в течение 10 мин с частотой 10 000 об./мин. Начальная концентрация в маточном растворе белка – 80 мг/мл, начальные концентрации всех солей в маточных растворах – 0.8 М.
Образцы. Пленки лизоцима формировали с помощью однобарьерной ленгмюровской ванны (36 × 11.5 × 0.5 см), входящей в состав жидкостного дифрактометра LISA. Перед каждым экспериментом ванну очищали этанолом и промывали большим количеством ультрачистой воды. Поверхностное давление измеряли с помощью весов Вильгельми (3 × 1.5 см, фильтровальная бумага).
На поверхность субфазы (ультрачистая вода) наносили белковый раствор с буфером/солью в объемном отношении 1 : 1. Скорость сжатия монослоя составляла 23 см2/мин. Сформированные монослои исследовали при поверхностном давлении 10–20 мН/м.
Описание эксперимента. Измерения методом РР и СРВ проводили на станции P08 (PETRA III, DESY, Германия) с использованием жидкостного дифрактометра LISA [28].
Размер рентгеновского пучка c энергией 18 кэВ составлял 400 × 100 мкм в месте расположения образца. В целях уменьшения рассеяния излучения на воздухе, а также предотвращения испарения жидкости из ленгмюровской ванны все измерения проводили в атмосфере гелия. После каждого измерения для уменьшения влияния радиационного повреждения образца ленгмюровскую ванну сдвигали на 2 мм перпендикулярно линии пучка; для каждого образца проводили по пять–восемь измерений.
Данные РР регистрировали в диапазоне 0–10 нм–1 двумерным детектором LAMBDA. В случае метода СРВ данные получали в диапазоне от 0–0.3 нм–1, сбор флуоресцентного сигнала осуществляли с помощью энергодисперсионного детектора Amptek PX5, рассеянный сигнал регистрировали с использованием линейного детектора Mythen1K.
Обработка экспериментальных данных. Для обработки данных РР использовали модель пленки, в которой плавное распределение поляризуемости задавали в виде суммы функций ошибок erf(z), описывающих переходные слои пленка–вакуум, пленка–субфаза. Это распределение разбивали на достаточно тонкие подслои, в пределах которых изменением электронной плотности можно пренебречь, и для полученной слоистой системы вычисляли теоретическую кривую зеркального отражения в соответствии с уравнениями (3), (4). Модельный профиль распределения электронной плотности уточняли путем минимизации расхождения экспериментальной и расчетной кривых зеркального отражения методом наименьших квадратов.
Для обработки данных, полученных методом СРВ, сначала рассчитывали угловую зависимость распределения интенсивности поля СРВ в соответствии с уравнением (6) с учетом уточненного при обработке данных РР профиля распределения электронной плотности. Далее задавали распределение концентрации интересующего химического элемента по глубине структуры в виде экспоненциально-модифицированной функции Гаусса и в дипольном приближении вычисляли угловые зависимости выхода рентгеновской флуоресценции в соответствии с (7). Профиль распределения концентрации элемента также уточняли путем минимизации расхождения экспериментальной и расчетной кривых методом наименьших квадратов. Обработку экспериментальных спектров рентгеновской флуоресценции проводили с использованием программы PyMca [29].
Для реализации нелинейного метода наименьших квадратов применяли алгоритм последовательных приближений Левенберга–Марквардта; ошибку уточненных профилей и соответствующих им параметров оценивали с применением подхода, описанного в [30].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Исследовали четыре серии образцов: пленки, сформированные из раствора белка без осадителя; пленки, сформированные из кристаллизационных растворов при добавлении ряда осадителей (KCl, NiCl2, CuCl2). Для каждой системы измерения проводили при нескольких значениях поверхностного давления (пять–восемь измерений для одного образца). Эксперименты показали нечувствительность образцов к изменениям поверхностного давления и высокую воспроизводимость экспериментальных данных, что позволило провести их усреднение. Кроме того, наблюдалась временная стабильность – несколько измерений одного образца со сдвигом ленгмюровской ванны после каждого измерения занимали в общей сложности более 1 ч.
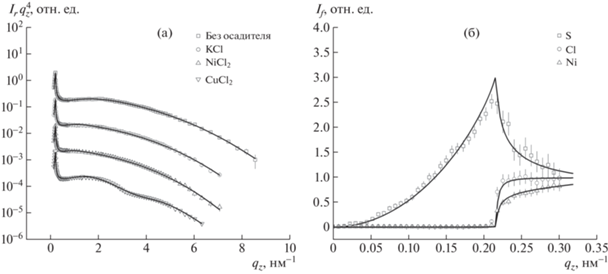
На рис. 1 представлены экспериментальные и теоретические данные для методов РР и СРВ. В случае метода СРВ приведены данные только для серии образцов, полученных с использованием осадителя NiCl2, так как для остальных образцов наблюдался схожий характер угловых зависимостей выхода рентгеновской флуоресценции. Все кривые выхода флуоресценции атомов серы были практически идентичны. Видно, что кривые зеркального отражения хорошо моделируются при использовании суммы функций ошибок в качестве функции распределения электронной плотности в образце. Теоретические угловые зависимости выхода флуоресценции также достаточно точно соответствуют экспериментальным данным, поэтому можно говорить об адекватности используемой в расчетах модели распределения концентрации элементов в виде экспоненциально-модифицированных функций Гаусса.
Рис. 1.
Экспериментальные (точки) и расчетные (линии) кривые: а – интенсивности зеркального отражения для образцов пленок без осадителя и с осадителями KCl, NiCl2, CuCl2 (кривые смещены друг относительно друга по оси ординат для наглядности); б – выхода рентгеновской флуоресценции атомов S, Cl, Ni для образца с осадителем NiCl2 (в случае образцов с осадителями KCl и CuCl2 наблюдался схожий характер кривых).
На рис. 2а представлены уточненные в ходе обработки профили распределения электронной плотности по данным РР и профили распределения атомов серы по данным, полученным методом СРВ. Атомы серы равномерно распределены внутри молекулы лизоцима (содержатся в аминокислотах Cys-6, Met-12, Cys-30, Cys-64, Cys-76, Cys-80, Cys-94, Met-105, Cys-115, Cys-127), поэтому по распределению концентрации серы можно достаточно точно судить о положении пленки в приповерхностной области субфазы. Однако нахождение толщины пленки по распределению серы является менее точной оценкой по сравнению с данными РР, так как выход флуоресценции слабо чувствителен к толщине слоя серы в пределах монослоя. Кроме того, атомы серы, несмотря на равномерное распределение внутри молекулы, занимают не весь ее объем. Соответственно, полуширина профиля распределения в любом случае будет меньше диаметра мономера лизоцима, равного приблизительно 3 нм. Тем не менее еще раз отметим, что положение максимума профиля по экспериментальным данным определяется с высокой точностью.
Рис. 2.
Профили распределения: а – электронной плотности и концентрации атомов серы для пленок, полученных без использования осадителя и с осадителями KCl, NiCl2, CuCl2; б – концентрации ионов Cl, K, Ni, Cu осадителя.

Из приведенных данных РР видно, что использование при формировании ленгмюровской пленки кристаллизационного раствора приводит к изменению распределения электронной плотности: при добавлении осадителя в раствор белка наблюдается увеличение толщины пленки. Толщины пленок определяли по полученным профилям распределения плотности – по положению полувысот функций ошибок, задающих переходные слои; рассчитанные значения толщины представлены в табл. 1. Полученные таким образом толщины всех пленок меньше теоретического значения диаметра мономера лизоцима (около 3 нм), что объясняется близкими значениями электронной плотности субфазы и молекулы белка. Так, максимальная относительная плотность мономера (относительно плотности воды) составляет ~1.3 отн. ед. и уменьшается ближе к краям молекулы. В результате наблюдается эффективное уменьшение толщины монослоя на поверхности субфазы, если анализировать контраст электронной плотности. Кроме того, “затянутость” межфазной границы пленка–субфаза несколько затрудняет однозначное определение реальной толщины пленки. Увеличение толщины при добавлении осадителя может быть объяснено участием в формировании пленки октамеров белка, образующихся в кристаллизационных растворах в концентрациях порядка нескольких процентов, что согласуется с результатами исследований [4–9, 21, 22]. Имеет место следующая зависимость: увеличение толщины пленок, сформированных из растворов с наибольшей концентрацией октамеров, по данным [21, 22] также максимально. Так, толщина пленок с осадителями NiCl2, KCl и CuCl2 увеличена приблизительно на 75, 56 и 45% соответственно по сравнению с толщиной пленки, сформированной из раствора без осадителя.
Таблица 1.
Параметры образцов по данным, полученным методами РР и СРВ
| Образец | d, нм | ρe, отн. ед. | zCl, мкм | zMe, мкм |
|---|---|---|---|---|
| Без осадителя | 1.21(4) | 1.198(8) | – | – |
| KCl | 1.89(3) | 1.209(5) | 7.2(5) | 10.8(6) |
| NiCl2 | 2.120(26) | 1.208(5) | 7.8(9) | 36.9(28) |
| CuCl2 | 1.76(4) | 1.234(9) | 8.3(13) | 89(7) |
Полученные профили распределения серы во всех образцах полушириной ~1 нм показывают, что пиковая плотность пленки (по данным РР) приходится именно на молекулы белка. При этом пленка остается стабильной, и белок не тонет в воде, о чем свидетельствует отсутствие флуоресцентного сигнала от атомов серы из объема субфазы. Уменьшение пикового значения относительной электронной плотности (табл. 1) по сравнению с теоретическим (1.3 отн. ед.) свидетельствует о незначительной разреженности (неплотности упаковки) молекул на поверхности субфазы. Увеличенная приблизительно на 3% плотность и более резкая межфазная граница пленки с осадителем CuCl2 могут быть объяснены встраиванием тяжелых ионов меди в структуру молекулы лизоцима [31].
На рис. 2б показаны профили распределения концентрации ионов осадителей по данным, полученным методом СРВ, для всех образцов, приготовленных из растворов с добавлением осадителя. Представленные распределения ионов принципиально отличаются от профиля распределения атомов серы, так как ионы осадителя диффундируют в приповерхностную область субфазы. Глубины проникновения в субфазу разных ионов заметно различаются, и наблюдается характерная зависимость: более тяжелые элементы проникают в субфазу на бóльшую глубину. В табл. 1 приведены глубины проникновения ионов осадителя в субфазу, на которых концентрация уменьшается в e раз. Интересно, что распределение концентрации всех ионов имеет максимум около поверхности субфазы, следовательно, белковая пленка препятствует процессу диффузии и “удерживает” ионы осадителя. В то же время различия между глубинами проникновения ионов с близкой атомной массой (Cl, K и Ni, Cu соответственно) свидетельствуют о различной специфике взаимодействия этих ионов с молекулами белка. Так, более затянутый профиль распределения ионов меди говорит о более слабом межмолекулярном взаимодействии мономеров белка при формировании пленки из раствора с осадителем CuCl2 по сравнению с осадителем NiCl2, что также согласуется с данными о концентрации образующихся в этих растворах олигомеров [21, 22].
Отметим, что по экспериментальным данным, полученным методом СРВ в геометрии скользящего падения пучка, сложно судить о распределении концентрации ионов осадителя в нанометровом масштабе непосредственно у нижней границы монослоя белка. Проблема заключается в усилении флуоресцентного сигнала от ионов, находящихся в объеме субфазы при увеличении угла падения пучка выше критического, что хорошо видно по форме кривых флуоресценции (рис. 1б). Так как угловая зависимость выхода флуоресценции определяется интегральным распределением концентрации ионов по глубине, локальные изменения концентрации вблизи поверхности практически не влияют на форму кривой.
ЗАКЛЮЧЕНИЕ
С применением метода РР показано, что использование кристаллизационных растворов с добавлением хлоридов металлов (KCl, NiCl2, CuCl2) в качестве осадителя при формировании ленгмюровской пленки лизоцима на жидкости приводит к увеличению ее толщины по сравнению с раствором без добавления осадителя. Выявлена следующая зависимость: увеличение толщины пленки (приблизительно на 75, 56 и 45% в случае осадителей NiCl2, KCl и CuCl2 соответственно) пропорционально концентрации олигомеров (димеров и октамеров) белка в кристаллизационных растворах по данным проведенных ранее исследований. Полученные абсолютные толщины пленок оказались занижены по сравнению с теоретическим значением, соответствующим диаметру мономера лизоцима (~3 нм), что объясняется слабым контрастом между электронной плотностью лизоцима и воды. Эту особенность необходимо учитывать для более точной интерпретации экспериментальных данных метода РР при исследовании подобных систем.
Полученные методом РР результаты подтверждают выдвинутую ранее теорию об участии образующихся в кристаллизационных растворах олигомеров белка в качестве структурных элементов формируемой ленгмюровской пленки. Также установлено увеличение электронной плотности (~3%) и контрастности межфазной границы пленка–субфаза для пленок с осадителем CuCl2, что может быть объяснено встраиванием относительно тяжелых ионов меди в структуру мономера лизоцима.
Методом СРВ определены профили распределения концентрации атомов серы и ионов-осадителей в исследованных пленках и в приповерхностной области субфазы. Полученные профили для атомов серы во всех образцах показали, что пик электронной плотности (определенный по данным РР) соответствует молекулам лизоцима, т.е. пленки находятся на поверхности субфазы, и молекулы белка не тонут. Однако точное определение толщины пленок с помощью метода СРВ оказалось затруднено ввиду слабой чувствительности кривой выхода флуоресценции к полуширине распределения атомов серы в таких тонких пленках. Таким образом, метод РР, чувствительный к контрасту электронной плотности, оказывается более точным при определении толщины подобных тонкопленочных систем на основе глобулярных белков.
Точное выявление специфики распределения ионов-осадителей в нанометровом масштабе относительно ленгмюровской пленки по полученным экспериментальным данным оказалось невозможным из-за сильного сигнала выхода флуоресценции из объема субфазы. Тем не менее данные о распределении ионов в микромасштабе в приповерхностной области субфазы позволили получить косвенную информацию об их взаимодействии с молекулами лизоцима. Показано, что белковая пленка “удерживает” ионы осадителя в приповерхностном слое толщиной ~10–100 мкм, зависящей от атомной массы иона. По разнице глубин проникновения ионов меди и никеля (с приблизительно одинаковой атомной массой) установлено, что осадитель NiCl2 оказывает большее влияние на межмолекулярное взаимодействие мономеров лизоцима при формировании пленки, что согласуется с результатами предыдущих работ по исследованию кристаллизационных растворов лизоцима.
Работа выполнена при поддержке Министерства науки и высшего образования (Государственное задание ФНИЦ “Кристаллография и фотоника” РАН, подготовка образцов), (Соглашение № 075-15-2021-1362 от 12.10.2021 г., обработка экспериментальных данных); при поддержке НИЦ “Курчатовский институт” (приказ № 1360, подготовка и проведение рентгеноструктурных исследований).
Список литературы
Fraden J. Handbook of Modern Sensors. Cham: Springer International Publishing, 2016. 758 p.
Mir S.H., Nagahara L.A., Thundat T. et al. // J. Electrochem. Soc. 2018. V. 165. № 8. P. B3137. https://doi.org/10.1149/2.0191808jes
Liu R. // Materials. 2014. V. 7. № 4. P. 2747. https://doi.org/10.3390/ma7042747
Ковальчук М.В., Бойкова А.С., Дьякова Ю.А. и др. // Кристаллография. 2017. Т. 62. № 4. С. 650. https://doi.org/10.7868/S0023476117040129
Marchenkova M., Boikova A., Dyakova Y. et al. // Acta Cryst. A. 2017. V. 70. P. C1182. https://doi.org/10.1107/S2053273317083929
Бойкова А.С., Дьякова Ю.А., Ильина К.Б. и др. // Кристаллография. 2018. Т. 63. № 5. С. 703. https://doi.org/10.1134/S0023476118050065
Kovalchuk M.V., Boikova A.S., Dyakova Y.A. et al. // Thin Solid Films. 2019. V. 677. P. 13. https://doi.org/10.1016/j.tsf.2019.02.051
Фоломешкин М.С., Бойкова А.С., Волковский Ю.А. и др. // Кристаллография. 2020. Т. 65. № 6. С. 851. https://doi.org/10.31857/S0023476120060156
Folomeshkin M.S., Marchenkova M.A., Boikova A.S. et al. // J. Phys.: Conf. Ser. 2020. V. 1560. P. 012033. https://doi.org/10.1088/1742-6596/1560/1/012033
Ducruix A., Guilloteau J.P., Riès-Kautt M. et al. // J. Cryst. Growth. 1996. V. 168 P. 28. https://doi.org/10.1016/0022-0248(96)00359-4
Марченкова М.А., Волков В.В., Благов А.Е. и др. // Кристаллография. 2016. Т. 61. № 1. С. 10. https://doi.org/10.7868/S0023476116010148
Kovalchuk M.V., Blagov A.E., Dyakova Yu.A. et al. // Cryst. Growth Des. 2016. V. 16. № 4. P. 1792. https://doi.org/10.1021/acs.cgd.5b01662
Дьякова Ю.А., Ильина К.Б., Конарев П.В. и др. // Кристаллография. 2017. Т. 62. № 3. С. 364. https://doi.org/10.7868/S0023476117030055
Бойкова А.С., Дьякова Ю.А., Ильина К.Б. и др. // Кристаллография. 2017. Т. 62. № 6. С. 876. https://doi.org/10.7868/S0023476117060078
Boikova A.S., Dyakova Y.A., Ilina K.B. et al. // Acta Cryst. D. 2017. 73. P. 591. https://doi.org/10.1107/S2059798317007422
Кордонская Ю.В., Тимофеев В.И., Дьякова Ю.А. и др. // Кристаллография. 2018. Т. 63. № 6. С. 902. https://doi.org/10.1134/S002347611806019X
Ковальчук М.В., Бойкова А.С., Дьякова Ю.А. и др. // Кристаллография. 2018. Т. 63. № 6. С. 857. https://doi.org/10.1134/S0023476118060061
Дьякова Ю.А., Бойкова A.С., Ильина К.Б. и др. // Кристаллография. 2019. Т. 64. № 1. С. 15. https://doi.org/10.1134/S0023476119010065
Kovalchuk M.V., Boikova A.S., Dyakova Y.A. et al. // J. Biomol. Struct. Dynamics. 2019. V. 37. № 12. P. 3058. https://doi.org/10.1080/07391102.2018.1507839
Marchenkova M.A., Konarev P.V., Rakitina T.V. et al. // J. Biomol. Struct. Dynamics. 2020. V. 38. № 10. P. 2939. https://doi.org/10.1080/07391102.2019.1649195
Kordonskaya Y.V., Marchenkova M.A., Timofeev V.I. et al. // J. Biomol. Struct. Dynamics. 2020. V. 39. № 18. P. 7223. https://doi.org/10.1080/07391102.2020.1803138
Марченкова М.А., Конарев П.В., Бойкова А.С. и др. // Кристаллография. 2021. Т. 66. № 5. С. 723. https://doi.org/10.31857/S0023476121050131
Кон В.Г. // Кристаллография. 2006. Т. 51. № 5. С. 1001.
Parratt L.G. // Phys. Rev. 1954. V. 95. № 2. P. 359. https://doi.org/10.1103/PhysRev.95.359
Ковальчук М.В., Кон В.Г. // Успехи физ. наук. 1986. Т. 149. № 1. С. 69.
Bedzyk M.J., Bommarito G.M., Schildkraut J.S. // Phys. Rev. Lett. V. 69. № 12. P. 1376. https://doi.org/10.1103/PhysRevLett.62.1376
Zheludeva S.I., Kovalchuk M.V., Novikova N.N et al. // J. Appl. Cryst. 1997. V. 30. P. 833. https://doi.org/10.1107/S0021889897001167
Murphy B.M., Greve M., Runge B. et al. // J. Synchr. Radiat. 2014. V. 21. P. 45. https://doi.org/10.1107/S1600577513026192
PyMca. http://pymca.sourceforge.net/
Press W., Teukolsky S., Vatterling W. et al. Numerical Recipes, The Art of Scientific Computing. Cambridge: Cambridge University Press, 2007. 1256 p.
Marchenkova M.A., Kuranova I.P., Timofeev V.I. // J. Biomol. Struct. Dynamics. 2020. V. 38. № 17. P. 5159. https://doi.org/10.1080/07391102.2019.1696706
Дополнительные материалы отсутствуют.
Инструменты
Кристаллография


