Мембраны и мембранные технологии, 2022, T. 12, № 1, стр. 29-37
Изучение деградации перфторированной мембраны в процессе работы в водородном топливном элементе
Д. С. Кудашова a, Н. А. Кононенко a, М. А. Бровкина a, И. В. Фалина a, *
a Федеральное государственное бюджетное образовательное учреждение высшего образования “Кубанский государственный университет”
350040 Краснодар, ул. Ставропольская, 149, Россия
* E-mail: irina_falina@mail.ru
Поступила в редакцию 07.09.2021
После доработки 01.10.2021
Принята к публикации 08.10.2021
- EDN: HPQWOR
- DOI: 10.1134/S2218117222010059
Аннотация
Представлены результаты исследования транспортных и структурных характеристик мембраны МФ-4СК на разных этапах ее работы в составе мембранно-электродного блока водородного топливного элемента. Для оценки деградации мембраны использованы методы мембранной кондуктометрии и вольтамперометрии, контактной эталонной порометрии и оптической микроскопии. Выполнена количественная оценка влияния термомеханического воздействия в процессе прессования мембранно-электродного блока и различных условий его эксплуатации на толщину мембраны, ее обменную емкость, влагосодержание, характеристики пористой структуры, удельную электропроводность и параметры вольтамперной кривой. Выявлены основные факторы, оказывающие наибольшее влияние на деградацию перфторированной мембраны.
ВВЕДЕНИЕ
Одними из наиболее перспективных альтернативных источников электрической энергии являются низкотемпературные водородные топливные элементы [1]. Их несомненным преимуществом является высокий КПД, отсутствие вредных и опасных выбросов в атмосферу. Однако их широкое внедрение осложняется как стоимостью вырабатываемой электроэнергии, так и отсутствием стабильных и высоко эффективных материалов [2, 3]. Одним из ключевых компонентов водородного топливного элемента является протонообменная мембрана, в качестве которой традиционно используют перфторированные сульфокатионитовые полимеры типа Nafion (DuPont, США) или российский аналог мембрана МФ-4СК. В настоящее время исследования в области низкотемпературных топливных элементов направлены на усовершенствование всех компонентов мембранно-электродного блока (МЭБ) – протонообменной мембраны и каталитического слоя, непосредственно контактирующего с ней.
Основными причинами снижения характеристик водородных топливных элементов являются изменение свойств катализатора [1, 4–7], в первую очередь на катоде [2]. Причиной деградации катализатора является снижение его активности вследствие уменьшения его поверхности из-за укрупнения наночастиц, необратимого окисления части активных центров, а также разрушения углеродного носителя [4, 5, 8]. Изучение механизмов этих процессов в настоящее время является актуальным научным направлением.
Помимо негативных процессов, протекающих с катализатором, может происходить ухудшение свойств полимерного электролита [7, 9–13], что также необходимо учитывать при разработке топливного элемента. Протекающие в мембране деградационные процессы можно разделить на две группы: разрушение самого полимера и появление примесей, снижающих транспортные характеристики мембраны. В настоящее время в литературе рассматривается несколько причин деградации мембраны. С одной стороны, возможно загрязнение протонообменной мембраны посторонними катионами, которые попадают в МЭБ с потоком воздуха или топлива [14, 15] или образуются за счет частичного окисления его конструктивных элементов [16–18]. В качестве источника посторонних катионов также могут выступать катализаторы на основе сплавов платины с d-элементами, легирование которыми интенсивно проводится в последнее время с целью повышения их удельной активности в токообразующих реакциях и снижения стоимости электрокатализаторов [19–21]. Авторы [18] отмечают возможность загрязнения мембран наночастицами таких элементов как Pt, Ir, Ti, Fe, Ni, катионы которых образуются в процессе окисления частей МЭБ, мигрируют внутрь мембраны и восстанавливаются водородом, который попадает в мембрану по механизму кроссовера. Так, в процессе коррозии платины в составе катодного катализатора катионы Pt2+ и Pt4+ могут мигрировать в мембрану, и, восстанавливаясь водородом, формировать платиновую полосу в мембране со стороны катода [6, 9]. Другая причина – разрушение полимерных цепей пероксо-соединениями, образующимися в реакции электровосстановления кислорода [9, 22–24], вследствие чего происходит уменьшение толщины мембраны [25] и ее обменной емкости [2]. Однако вклад каждого из механизмов деградации МЭБ и в частности протонообменной мембраны, до сих пор до конца не выявлены. Целью данной работы являлось изучение деградации протонообменной мембраны МФ-4СК на основании исследования ряда ее физико-химических характеристик на разных этапах работы мембранно-электродного блока водородного топливного элемента. В задачу работы входило комплексное изучение электротранспортных и структурных свойств протонообменной мембраны методами мембранной кондуктометрии и вольтамперометрии, контактной эталонной порометрии (КЭП), оптической микроскопии.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Объекты исследования
Объектом исследования являлась перфторированная мембрана МФ-4СК (ООО “Пластполимер”, Санкт-Петербург), которая выступала в качестве полимерного электролита МЭБ. Для исследования были взяты исходная мембрана (МФ-4СК), мембрана после прессования при изготовлении МЭБ (образец МФ-4СК-П), а также мембраны после ресурсных испытаний в двух режимах: потенциостатическом в течение 100 ч (далее режим 1, образец МФ-4СК-Р1) и потенциодинамическом (режим 2, образец МФ-4СК-Р2). Изучение транспортных и структурных характеристик мембран проводилось на каждом этапе формирования и эксплуатации МЭБ: непосредственно после его прессования, а также после ресурсных испытаний в режимах 1 и 2. Перед изготовлением МЭБ мембраны кипятили в дистиллированной воде в течение 3 ч, затем погружали в 1 М раствор серной кислоты для перевода в протонную форму и отмывали дистиллированной водой с контролем сопротивления воды над мембраной.
Изготовление и испытание мембранно-электродного блока топливного элемента
Для приготовления каталитических чернил во всех случаях использовали коммерческий катализатор E-TEK-C1-40 (40% Pt на саже Vulkan XC-72). Каталитическая смесь для нанесения на электроды состояла из навески катализатора, 10% дисперсии Nafion в изопропаноле (содержание Nafion составляло 12.5% от массы катализатора), дистиллированной воды и изопропанола в соотношении 8 : 1. Полученную смесь диспергировали в ультразвуковой ванне в течение 60 минут. Далее углеродную бумагу “Toray EC-TP1-090T” толщиной 280 мкм помещали на предварительно обезжиренную плитку, поверхность которой нагрета до 60°С, и равномерно наносили каталитические чернила на одну из ее поверхностей. Площадь каждого электрода составляла 5 см2. Мембранно-электродные блоки получали путем горячего прессования газодиффузионных слоев, с предварительно нанесенными на них каталитическим слоем, и воздушно-сухой протонообменной мембраны МФ-4СК при температуре 117–120°С. Прессование осуществлялось в течение 3 мин при давлении 80 атм. Загрузка обоих электродов платиной составляла 0.3 мг/см2.
Ресурсные испытания МЭБ проводились при 25°С без дополнительного увлажнения газов в двух режимах: режим 1 – 100 ч при нагрузочном напряжении 0.5 В и режим 2 – ускоренное стресс-тестирование треугольными импульсами в интервале напряжений 0.6–1.2 В со скоростью развертки потенциала 0.1 В/с в течение 10 000 циклов. Режим 1 обеспечивал мягкие условия тестирования, позволяющие частично регенерировать мембрану после стадии прессования. Режим 2 предполагал стресс-тестирование в жестких условиях, позволяющих подвергнуть все компоненты МЭБ ощутимому негативному воздействию. Наложение 2500 циклов в выбранном режиме стресс-тестирования эквивалентно проведению ресурсных испытаний в течение 1010 ч [2]. Измерение спектров электрохимического импеданса проводили в диапазоне частот 0.1 Гц–500 кГц до начала тестирования и каждые 2000 циклов. На основании спектров импеданса определяли омическое сопротивление МЭБ. Скорость подачи водорода и воздуха в ячейку при исследовании всех электрохимических характеристик МЭБ поддерживалась постоянной и составляла 20 и 180 л/ч соответственно. Электрохимические характеристики МЭБ изучали с помощью Potentiostat-galvanostat P-45X c модулем частотного анализатора “FRA-24M” (Electrochemical Instruments, Черноголовка, Россия).
После проведения ресурсных испытаний МЭБ разбирали, мембрану помещали в дистиллированную воду, удаляли катализатор с ее поверхности и далее проводили исследование свойств полимерного электролита.
Физико-химические характеристики мембраны
Определение обменной емкости образцов мембран (Q, ммоль/г) проводили по стандартной методике методом смещения равновесия с избытком титранта. Экспериментально полученное значение Q пересчитывалось на 1 г сухой мембраны. Толщина мембраны (l, мм) измерялась микрометром МК-25 0.01.
Для оценки проводящих свойств перфторированных мембран использован ртутно-контактный метод, описанный в работе [26]. Для измерения концентрационных зависимостей удельной электропроводности проводили подготовку образцов, которая заключалась в их приведении в равновесие с растворами серной кислоты различных концентраций. Сопротивление мембран определяли по активной части импеданса в диапазоне частот 0.1 Гц–500 кГц. Погрешность определения сопротивления образцов не превышала 5%.
Измерение вольтамперных характеристик мембран проводили в проточной четырехкамерной электродиализной ячейке. При проведении эксперимента исследуемая мембрана была отделена от электродных камер вспомогательной катионообменной (МК-40) и анионобменной (МА-41) мембранами. Раствор серной кислоты с концентрацией 0.05 моль-экв/л прокачивался через все камеры электродиализной ячейки со скоростью 10 мл/мин. Межмембранное расстояние составляло 0.73 см, поляризуемая площадь мембран составляла 2.38 см2. На платиновые поляризующие электроды подавался постоянный ток. Мембранный потенциал измерялся при помощи капилляров Луггина, соединенных с хлоридсеребряными электродами, подведенными к геометрическим центрам поляризуемых участков исследуемой мембраны и находившимися на расстоянии около 0.8 мм от ее поверхности. Вольтамперные характеристики были получены из хронопотенциограмм, как зависимости среднего во времени скачка потенциала в стационарном состоянии от плотности тока. Методика получения вольтамперных характеристик и хронопотенциограмм подробно описана в работе [27].
Для изучения распределения воды по энергиям связи и эффективным радиусам пор в мембранах использован метод контактной-эталонной порометрии [28, 29]. С помощью данного метода можно исследовать пористую структуру материалов в более широком диапазоне радиусов пор от 1 нм до 300 мкм по сравнению с другими структурно-чувствительными методами. Сущность метода заключается в измерении равновесной кривой относительного влагосодержания для образца, находящегося в контакте с эталоном, для которого порометрическая кривая предварительно получена независимым методом. Методика проведения эксперимента подробно описана в работах [30, 31].
Из полученных порометрических кривых в интегральном и дифференциальном виде определялся ряд характеристик пористой структуры. Величина максимального влагосодержания (V0, см3/г) характеризует общий объем порового пространства в мембране. С использованием найденного значения V0 и величины обменной емкости мембраны рассчитывалось удельное влагосодержание как количество молей воды, приходящееся на 1 моль сульфогрупп мембраны (n, ${{{\text{мол}}{{{\text{ь}}}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}} \mathord{\left/ {\vphantom {{{\text{мол}}{{{\text{ь}}}_{{{{{\text{H}}}_{{\text{2}}}}{\text{O}}}}}} {{\text{мол}}{{{\text{ь}}}_{{{\text{SO}}_{{\text{3}}}^{ - }}}}}}} \right. \kern-0em} {{\text{мол}}{{{\text{ь}}}_{{{\text{SO}}_{{\text{3}}}^{ - }}}}}}$):
где Vm – мольный объем воды, равный 18 см3/моль.Площадь внутренней удельной поверхности макро- и мезопор с эффективным радиусом более 1 нм (S1) рассчитывалась по формуле [31]:
(2)
${{S}_{{1~}}} = 2\mathop \smallint \limits_{r = 1}^{{{r}_{{{\text{max}}}}}} \frac{1}{{{{r}^{2}}}}\left( {\frac{{dV}}{{d\ln r}}} \right)dr = 2\mathop \smallint \limits_{r = 1}^{{{r}_{{{\text{max}}}}}} \frac{{dV}}{r}.$Общая площадь внутренней удельной поверхности (S) складывалась из этих двух слагаемых: S = S1+ S2.
С привлечением данных по обменной емкости мембраны рассчитывалось также среднее расстояние между фиксированными группами (L) и величина плотности заряда на внутренней межфазной поверхности раздела (q):
где NA – число Авогадро.Для получения изображений поверхностей мембран в набухшем состоянии использован оптический микроскоп Альтами БИО 2 с 10-кратным увеличением, снабженный цифровой окулярной USB-камерой.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Характеристики МЭБ
Результаты ресурсных испытаний МЭБ в мягких условиях тестирования (режим 1), позволяющих частично регенерировать мембрану после стадии прессования, и более жестких (режим 2), эквивалентным длительным ресурсным испытаниям, представлены на рис. 1а, 1б. Для режима 2 представлена плотность тока при наложенной разности потенциалов 0.6 В. Как видно из рис. 1а, в режиме тестирования 1 наблюдается увеличение плотности тока в процессе работы МЭБ до величины 70 мА/см2. В то же время при работе МЭБ в режиме 2 плотность тока существенно снижается уже после 1000 циклов и при дальнейшей работе остается практически постоянной.
Результаты измерения сопротивления МЭБ в процессе тестирования в различных условиях представлены на рис. 2 с учетом реального времени проведения эксперимента в режиме стресс-тестирования. Как видно из рисунка, сопротивление МЭБ существенно выше при его работе в потенциодинамическом режиме по сравнению с потенциостатическим режимом.
Физико-химические и структурные характеристики полимерного электролита
Физико-химические характеристики мембраны определялись на каждом этапе формирования и эксплуатации МЭБ. В табл. 1 представлены значения толщины четырех образцов исходной мембраны МФ-4СК в набухшем состоянии (l0). Несмотря на то, что образцы были вырезаны из одного листа, их толщина варьируется от 0.20 до 0.23 мм. Толщина мембраны после ее использования в МЭБ (l1) в набухшем состоянии также представлена в табл. 1. Как видно из таблицы, термическое и механическое воздействие на мембрану в процессе прессования при изготовлении МЭБ приводит к уменьшению толщины мембраны примерно на 10%. При дальнейшей эксплуатации мембраны в составе МЭБ ее толщина практически не изменяется. В то же время на обменную емкость мембраны стадия прессования МЭБ влияния не оказывает (табл. 1). Снижение обменной емкости на 8% отмечено для мембраны МФ-4СК-Р2 после эксплуатации ее в жестких условиях стресс-тестирования. Причиной этого может быть отщепление части функциональных SO3-групп пероксо-соединениями, образующимися в реакции электровосстановления кислорода.
Таблица 1.
Физико-химические и структурные характеристики мембраны МФ-4СК на различных этапах ее работы в топливном элементе
| № | Мембрана | l0, мм | l1, мм | Q, ммоль/гсух | V0, см3/г | n, моль H2O/моль S${\text{O}}_{3}^{ - }$ | S, м2/г | L, нм | q, Кл/м2 |
|---|---|---|---|---|---|---|---|---|---|
| 1 | МФ-4СК | 0.235 ± 0.003 | 0.235 ± 0.003 | 0.87 | 0.36 | 23.0 | 236 | 0.65 | 0.38 |
| 2 | МФ-4СК-П | 0.204 ± 0.007 | 0.183 ± 0.006 | 0.86 | 0.26 | 16.8 | 195 | 0.61 | 0.43 |
| 3 | МФ-4СК-Р1 | 0.211 ± 0.007 | 0.202 ± 0.004 | 0.87 | 0.24 | 15.3 | 198 | 0.61 | 0.42 |
| 4 | МФ-4СК-Р2 | 0.207 ± 0.006 | 0.182 ± 0.004 | 0.80 | 0.24 | 16.7 | 188 | 0.63 | 0.41 |
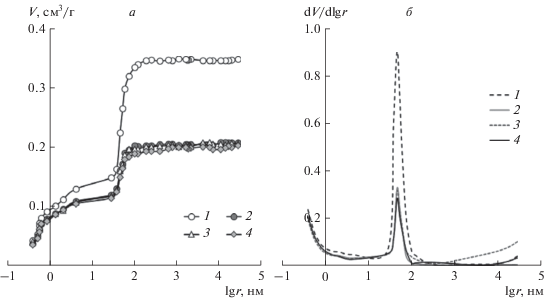
На рис. 3 для всех исследованных образцов мембраны представлены кривые распределения воды по эффективным радиусам пор, рассчитанные из них структурные характеристики приведены в табл. 1. Как видно из приведенных результатов, наиболее существенные изменения в структуре мембраны МФ-4СК происходят в процессе прессования при изготовлении МЭБ. Оказываемое при этом термическое и механическое воздействие на мембрану приводит к снижению общего объема пор на 28%. В результате этого удельное влагосодержание мембраны снижается также на 28%. Происходящее при этом уменьшение площади внутренней удельной поверхности сопровождается закономерным уменьшением расстояния между функциональными группами и увеличением плотности заряда на внутренней межфазной поверхности раздела. Дальнейшего изменения структурных характеристик мембраны в процессе ее работы в топливном элементе практически уже не происходит.
Рис. 3.
Интегральные (а) и дифференциальные (б) кривые распределения воды по радиусам пор. 1 – МФ-4СК, 2 – МФ-4СК-П, 3 – МФ-4СК-Р1, 4 – МФ-4СК-Р2.
На рис. 4 представлены концентрационные зависимости удельной электропроводности мембран в растворе серной кислоты. Анализ полученных зависимостей показал, что электропроводность всех образцов снижается примерно в 2 раза во всем диапазоне концентраций по сравнению с электропроводностью исходной мембраны, что связано со снижением как максимального, так и удельного влагосодержания мембран.
Рис. 4.
Концентрационные зависимости удельной электропроводности образцов мембран в растворе серной кислоты. 1 – МФ-4СК, 2 – МФ-4СК-Р1, 3 – МФ-4СК-П, 4 – МФ-4СК-Р2, 5 – раствор H2SO4.

На основании концентрационных зависимостей удельной электропроводности рассчитаны транспортно-структурные параметры микрогетерогенной модели ионообменной мембраны. Согласно указанной модели [26], структура ионообменной мембраны рассматривается как двухфазная проводящая система, содержащая гелевую фазу и фазу межгелевого раствора. В гелевой фазе, в состав которой условно включены все компоненты ионообменной мембраны за исключением равновесного раствора, перенос тока осуществляется только противоионами. В межгелевых промежутках, заполненных электронейтральным раствором, ток переносят как катионы, так и анионы. Электропроводность такой системы описывается уравнением [32]:
(6)
${{k}_{{m~}}} = k_{{{\text{iso}}}}^{{{{f}_{1}}}}{\text{\;}}k_{{{\text{sol}}}}^{{1 - {{f}_{1}}}},$Таблица 2.
Транспортно-структурные параметры, рассчитанные в рамках микрогетерогенной модели проводимости
| № | Мембрана | f1 | f2 | κiso, См/м |
|---|---|---|---|---|
| 1 | МФ-4СК | 0.87 | 0.13 | 4.08 |
| 2 | МФ-4СК-П | 0.86 | 0.14 | 2.00 |
| 3 | МФ-4СК-Р1 | 0.88 | 0.12 | 2.29 |
| 4 | МФ-4СК-Р2 | 0.87 | 0.13 | 1.83 |
Как видно из табл. 2, электропроводность гелевой фазы мембраны уменьшается примерно в 2 раза уже после прессования. Указанное снижение κiso обусловлено снижением влагосодержания образцов, в том числе гидратной емкости гелевой фазы, и, как следствие, уменьшением подвижности противоионов в геле. Наиболее существенное уменьшение проводимости геля наблюдается для образца МФ-4СК-Р2, и может быть обусловлено его более низкой обменной емкостью по сравнению с другими образцами. Несмотря на это, объемные доли проводящих фаз изменяются пропорционально и соотношение между ними остается постоянным. Это позволяет сделать вывод о равномерном сжатии мембраны в процессе прессования. Ранее авторами [33] при исследовании широкого круга мембран различных структурных типов отмечался аналогичный эффект неизменности значений параметров f1 и f2 с увеличением концентрации раствора несмотря на уменьшение влагосодержания мембран.
На рис. 5 представлены вольтамперные характеристики мембран в 0.05 моль-экв/л растворе серной кислоты. Как видно из рисунка, кривые имеют классический вид и содержат три области: омический участок, плато предельного тока и сверхпредельную область. На рисунке представлены приведенные вольтамперные характеристики за вычетом омического участка.
Рис. 5.
Вольтамперные характеристики образцов мембран. 1 – МФ-4СК, 2 – МФ-4СК-П, 3 – МФ-4СК-Р1, 4, 4 ' – МФ-4СК-Р2 (к потоку противоионов обращена поверхность, контактировавшая в МЭБ с катодом (4) и анодом (4')).

Отмечено, что наиболее существенные эффекты наблюдаются в изменении величины (ilim) и протяженности плато (Δ) предельного тока, значения которых представлены в табл. 3. Можно видеть, что для мембран, которые подвергались термическому и механическому воздействию в процессе прессования, наблюдается увеличение протяженности плато предельного тока примерно на 50%. Аналогичный эффект отмечался рядом авторов при изучении влияние масштабов геометрической неоднородности поверхности на параметры вольтамперной характеристики ионообменной мембраны [34].
Таблица 3.
Параметры вольтамперных кривых
| № | Мембрана | ilim, A/м2 | ∆, В |
|---|---|---|---|
| 1 | МФ-4СК | 179 | 0.60 |
| 2 | МФ-4СК-П | 174 | 0.92 |
| 3 | МФ-4СК-Р1 | 170 | 0.93 |
| 4 ориентация к катоду | МФ-4СК-Р2 | 164 | 1.21 |
| 4 ориентация к аноду | 177 | 0.90 |
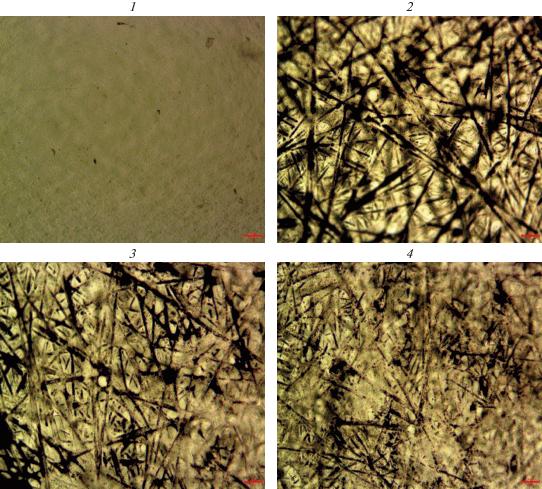
Анализ оптических изображений поверхности исследованных образцов, представленных на рис. 6, показывает возникновение геометрических неоднородностей на поверхности мембраны после прессования, рисунок которых повторяет плетение волокон углеродной бумаги. Это является причиной задержки в наступлении сверхпредельного состояния в электромембранной системе. Однако необходимо отметить, что появление неоднородностей такого масштаба не оказывает влияние на величину предельного тока (табл. 3).
Рис. 6.
Оптические изображения поверхности исследованных мембран. 1 – МФ-4СК, 2 – МФ-4СК-П, 3 – МФ-4СК-Р1, 4 – МФ-4СК-Р2.
Для образца МФ-4СК-Р2 после стресс-тестирования обнаружена асимметрия вольтамперной характеристики, которая не наблюдалась для остальных образцов. В случае, когда поверхность, контактировавшая в МЭБ с катодом, встречает поток противоионов, плотность предельного тока ниже, а плато предельного тока более протяженное по сравнению с обратной ориентацией образца. Причиной наблюдаемого эффекта более позднего перехода электромембранной системы в сверхпредельное состояние может являться частичное разрушение структуры поверхности за счет появления перекисных соединений на катоде и снижение обменной емкости в приповерхностном слое, которое в случае кластерных перфторированных мембран приводит к усилению электрической неоднородности их поверхности [35].
ЗАКЛЮЧЕНИЕ
Проведено комплексное исследование транспортных и структурных свойств полимерного электролита на разных этапах его работы в составе мембранно-электродного блока водородного топливного элемента. Показано, что после термического и механического воздействия на мембрану в процессе прессования МЭБ происходит существенное уменьшение ее толщины, суммарного объема пор и удельного влагосодержания на 28%. При этом удельная электропроводность мембраны в целом и ее гелевой фазы снижается в 2 раза, однако соотношение объемных долей проводящих фаз сохраняется постоянным. Дальнейшего ухудшения физико-химических характеристик мембран после работы в составе МЭБ водородного топливного элемента в мягких условиях потенциостатического режима не происходит. Однако при работе в режиме стресс-тестирования снижается обменная емкость мембраны на 8% и появляется асимметрия вольтамперной характеристики.
Список литературы
Okonkwo P.C., Ige O.O., Barhoumi E.M., Uzoma P.C., Emori W., Benamor A., Abdullah A.M. // International J. Hydrogen Energy. 2021. V. 46. № 29. P. 15850.
Аваков В.Б., Алиев А.Д., Бекетаева Л.А., Богдановская В.А., и др. // Электрохимия. 2014. Т. 50. № 8. С. 858.
Gatto I., Carbone A., Sacca A., Passalacqua E., Oldani C., Merlo L., Sebastian D., Arico A.S., Baglio V. // J. Electroanalytical Chemistry. 2019. V. 842. P. 59.
Pivac I., Bezmalinovic D., Barbir F. // International J. Hydrogen Energy. 2018. V. 43. P. 13512.
Meyer Q., Zeng Y., Zhao C. // J. Power Sources. 2019. V. 437. P. 226922.
Ferreira P.J., la O’ G.J., Shao-Horn Y., Morgan D., Makharia R., Kocha S., Gasteiger H. A. // J. Electrochem. Soc. 2005. V. 152. № 11. P. A2256.
Xiao-Zi Y., Hui L., Shengsheng Z., Jonathan M., Haijiang W. // J. Power Sources. 2011. V. 196. P. 9107.
Martínez-Huerta M.V., Lázaro M.J. // Catalysis Today. 2017. V. 285. P. 3.
El-kharouf A., Chandan A., Hattenberger M., Pollet B.G. // J. Energy Institute. 2012. V. 85. № 4. P. 188.
Wu J., Yuan X.Z., Martin J.J., Wang H., Zhang J., Shen J., Shaohong W., Merida W. // J. Power Sources. 2008. V. 184. № 1. P. 104.
Borup R., Meyers J., Pivovar B., Kim Y.S. et al. // Chem. Rev. 2007. V. 107. P. 3904.
Haolin T., Shen P., San P.J., Fang W., Mu P. // J. Power Sources. 2007. V. 170. № 1. P. 85.
Sorrentino A., Sundmacher K., Vidakovic-Koch T. // Energies. 2020. V. 13. P. 5825.
Park J., Uddin M.A., Pasaogullari U., Bonville L. // International J. Hydrogen Energy. 2017. V. 42. № 33. P. 21146.
Uddin M.A., Qi J., Wang X., Pasaogullari U., Bonville L. // International J. Hydrogen Energy. 2015. V. 40. P. 13 099.
Sulek M., Adams J., Kaberline S., Ricketts M., Waldecker J.R. // J. Power Sources. 2011. V. 196. № 21. P. 8967.
Pozio A., Silva R.F., Francesco M.D., Giorgi L. // Electrochim. Acta. 2003. V. 48. № 11. P. 1543.
Григорьев С. А., Бессарабов Д.Г., Фатеев В.Н. // Электрохимия. 2017. Т. 53. № 3. С. 359.
Min M., Kim H. // International J. Hydrogen Energy. 2016. V. 41. №. 39. P. 17557.
Alekseenko A.A., Guterman V.E., Belenov S.V., Menshikov V.S., Tabachkova N.Yu., Safronenko O.I., Moguchikh E.A. // Int. J. Hydrogen Energy. 2018. V. 43. P. 3676.
Zhang S., Yuan X., Wang H., Me’rida W., Zhu H., Shen J., Wu S., Zhang J. // International J. Hydrogen Energy. 2009. V. 34. № 1. P. 388.
Chandesris M., Vincent R., Guetaz L., Roch J.-S., Thoby D., Quinaud M. // International J. Hydrogen Energy. 2017. V. 42. № 12. P. 8139.
Hongsirikarn K., Mo X., Goodwin J.G., Creager S. // J. Power Sources. 2011. V. 196. № 6. P. 3060.
Teranishi K., Kawata K., Tsushima S., Hirai S. // Electrochem. Solid-State Lett. 2006. V. 9. № 10. P. A475.
Григорьев С.А., Джусь К.А., Бессарабов Д.Г., Маркелов В.В., Фатеев В.Н. // Электрохимическая энергетика. 2014. Т. 14. № 4. С. 187.
Berezina N.P., Kononenko N.A., Gnusin N.P., Dyomina O.A. // Adv. Colloid and Interface Sci. 2008. V. 139. P. 3.
Belashova E.D., Melnik N.A., Pismenskaya N.D., Shevtsova K.A., Nebavsky A.V., Lebedev K.A., Nikonenko V.V. // Electrochim. Acta. 2012. V. 59. P. 412.
Volfkovich Y.M., Filippov A.N., Bagotsky V.S. Structural Properties of Porous Materials and Powders Used in Different Fields of Science and Technology. Springer-Verlag London. 2014. 328 p.
Volfkovich Y.M., Bagotzky V.S., Sosenkin V.E., Blinov I.A. // Colloids and Surfaces A: Physicochemical and Engineering Aspects. 2001. V. 187–188. P. 349.
Kononenko N., Nikonenko V., Grande D., Larchet C., Dammak L., Fomenko M., Volfkovich Yu. // Advances in Colloid and Interface Science. 2017. V. 246 P. 196.
Kononenko N.A., Fomenko M.A., Volfkovich Yu. M. // Adv. Colloid and Interface Sci. 2015. V. 222. P. 425.
Zabolotsky V.I., Nikonenko V.V. // J. Membr. Sci. 1993. V. 79. P. 181.
Демина О.А., Фалина И.В., Кононенко Н.А. // Электрохимия. 2015. Т. 51. № 6. С. 641.
Balster J., Yildirim M. H., Stamatialis D. F., Ibanez R. et al. // J. Phys. Chem. B. 2007. V. 111. № 9. P. 2152.
Pis’menskayaa N.D., Nikonenko V.V., Mel’nik N.A., Pourcelli G., Larchet G. // Russ. J. Electrochem. 2012. V. 48. № 6. P. 610.
Дополнительные материалы отсутствуют.
Инструменты
Мембраны и мембранные технологии




