Микология и фитопатология, 2019, T. 53, № 1, стр. 46-48
Новый способ получения культуры Venturia inaequalis из аскоспор
А. И. Насонов *
Северо-Кавказский федеральный научный центр садоводства, виноградарства, виноделия
350901 Краснодар, Россия
* E-mail: nasoan@mail.ru
Поступила в редакцию 05.05.2018
После доработки 10.05.2018
Принята к публикации 29.05.2018
Аннотация
Аскомицет Venturia inaequalis является возбудителем одной из самых экономически значимых болезней яблони. Выделение патогена в чистую культуру является важным этапом его популяционных исследований. Предложена модификация метода получения изолятов гриба из аскоспор, отличающаяся простотой и эффективностью. В качестве ловушки спор использовалась перевернутая вверх дном полистирольная чашка Петри с предварительно залитым 3–6-миллиметровым слоем 2%-го водного агара. Перезимовавший лист яблони закладывался в крышку чашки Петри выводными отверстиями псевдотециев наверх. Ловушка инкубировалась при комнатной температуре в течение 15 ч. Попадание аско-спор V. inaequalis на поверхность агара происходило за счет специфического механизма разгрузки аска, называемого водяной пушкой. Одиночные проросшие аскоспоры изолировали в новые чашки Петри. Используемая ловушка позволяла получать чистый инокулюм проросших аскоспор для дальнейшего моноспорового посева.
Выделение возбудителя парши яблони в чистую культуру является важным этапом популяционно-генетических исследований патогена. Достаточно сложный метод получения аскоспоровой культуры был описан американскими учеными в начале прошлого столетия. Он заключался в препарировании перитециев парши яблони с извлечением отдельных сумок, с последующим захватом аскоспор выделенного аска микрокапилляром (Keitt, Palmiter 1938; Keitt, Langford, 1941). Такой подход отвечал научным задачам того времени по изучению механизмов наследования отдельных признаков Venturia inaequalis (Cooke) G. Winter. В современных популяционных исследованиях требуется получение как можно большего количества изолятов вида. Оценка популяции патогенного гриба сразу после прохождения полового процесса (на аскоспоровой стадии) позволяет максимально оценить его разнообразие (Nasonov, Suprun, 2016). В этом случае необходим простой и хорошо воспроизводимый метод получения изолятов микромицета из аскоспор.
Относительно несложный подход для получения чистого инокулюма аскоспор в целом для сухоспоровых аскомицетов был описан в справочнике “Методы экспериментальной микологии” (Bilay, 1982). Внутрь чашки Петри вкладывалась культуральная чашка меньшего размера или стеклянные палочки, на которую/которые помещался лист отверстиями плодовых тел вниз. После инкубирования ловушки в течении 3 ч и более дно большой чашки микроскопировали под стереомикроскопом для поиска и переноса спор на питательный агар. Существенным недостатком данной методики является расположение собирающей поверхности под листом, что приводит к случайному заносу нецелевых спор других микроорганизмов путем осыпания. В недавно предложенном методе получения аскоспоровой культуры парши яблони (Nasonov et al., 2016) данный недостаток был преодолен помещением листа прошлогоднего опада отверстиями перитециев наверх в чашке Петри в условиях влажной камеры. Ловчей поверхностью выступала нижняя сторона предметного стекла, помещенного над дезинфицированным листовым опадом на стеклянные палочки. Метод включал этапы посева вазелина с поверхности предметного стекла в чашку Петри с водным агаром и перенесение единичных проросших аскоспор на питательный агар. Предложенный авторами метод основан на баллистическом механизме эмиссии аскоспор псевдотециями V. inaequalis. Он позволяет получать чистый инокулюм аскоспор для моноспорового посева, но требует более чем двое суток.
Предлагается модификация вышеописанной методики, которая позволяет значительно ее упростить и снизить времязатратность. Принцип новой ловушки очень прост и исключает установку ловчего предметного стекла, сочетая сразу все этапы предыдущего подхода в одном. Чашку Петри 90 мм диам. с предварительно залитым 2%-м водным агаром переворачивают вверх дном. Толщина агара составляет 3–6 мм – так, чтобы расстояние между листом с псевдотециями и поверхностью агара в полистирольной чашке Петри оказывалось 7–10 мм. В крышку перевернутой чашки Петри 90 мм диам. закладывают стерильный смоченный дистиллированной водой лист фильтровальной бумаги, например марки “Белая” или “Желтая лента”. На фильтровальную бумагу помещают хорошо промытый в проточной водопроводной воде и дезинфицированный лист опада яблони с созревшими псевдотециями гриба (рис. 1). Листья дезинфицируют 10 с в 70%-м растворе спирта, затем 10 с в 3%-м растворе перекиси водорода и промывают в стерильной дистиллированной воде. Выводные отверстия плодовых тел должны быть ориентированы вверх. Определение их положения относительно нижней или верхней стороны листа может осуществляться микроскопированием при малом увеличении стереомикроскопа, либо закладкой двух частей одного листа разными сторонами вверх.
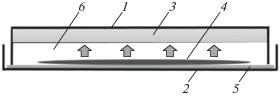
Рис. 1.
Схема спороловушки: 1 – дно чашки Петри; 2 – верхняя створка чашки Петри; 3 – 2%-й водный агар; 4 – лист опада яблони; 5 – фильтровальная бумага; 6 – внутреннее пространство чашки Петри. Широкими стрелками показано направление движения аскоспор внутри спороловушки.
Ловушку инкубируют при комнатной температуре в течение ночи (около 15 ч), после чего снимают нижнюю часть чашки Петри, переворачивают и микроскопируют поверхность водного агара при малом увеличении стереомикроскопа (40×). Проросшие одиночные аскоспоры вырезают вместе с агаровым блоком и переносят на питательный агар.
Данная методика была апробирована при получении 50 моноспоровых изолятов V. inaequalis и показала свою высокую эффективность. Методика практически исключает контаминацию спорового материала пропагулами других грибов, а также бактерий или их пассивный занос под действием сил гравитации. Попадание аскоспор V. inaequalis на поверхность агара происходит за счет специфического механизма разгрузки аска, называемого водяной пушкой, позволяющего выбрасывать споры под давлением на высоту 5–13 мм (Aylor, Anagnostakis, 1991), а по некоторым данным – до 50 мм (Fedorova, 1977). Разгрузка асков может происходить в течение суток (Fedorova, 1977). Попадание аскоспор на поверхность агара запускает процесс их прорастания. Оптимальной для прорастания аскоспор является температура 15–25°C. При этих значениях прорастание начинается через 2–3 часа (Louw, 1948; Boric, 1985).
Список литературы
Aylor D.E., Anagnostakis S.L. Active discharge of ascospores of Venturia inaequalis. Phytopathology. 1991. V. 81. P. 548–551.
Bilay V.I. (ed.). Methods of experimental mycology. Naukova Dumka, Kyev, 1982 (in Russ.).
Boric B. Influence of temperature on germability of spores of Venturia inaequalis (Cooke) Winter, and their viability as affected by age. Zast Bilja. 1985. V. 36. P. 295–302.
Fedorova R.N. Apple scab. Kolos, Leningrad, 1977 (in Russ.).
Keitt G.W., Langford M.H. Venturia inaequalis (Cke.) Wint. I. A groundwork for genetic studies. Amer. J. Bot. 1941. V. 28 (9). P. 805–820.
Keitt G.W., Palmiter D.H. Heterothallism and variability in Venturia inaequalis. Amer. J. Bot. 1938. V. 25 (5). P. 338–345.
Louw A.J. The germination and longevity of spores of the apple-scab fungus, Venturia inaequalis (Cke.) Wint. Union S. Afric. Sci. Bull. 1948. V. 285. P. 19.
Nasonov A.I., Suprun I.I. Use monoascosporic isolates in population studies Venturia inaequalis. In: Modern solutions in the development of agricultural science and production. Krasnodar, 2016. P. 124–128 (in Russ.).
Nasonov A.I., Yakuba G.V., Suprun I.I. Obtaining of Venturia inaequalis ascospore culture under laboratory conditions. Mikologiya i fitopatologiya. 2016. V. 50 (2). P. 130–131 (in Russ.).
Билай В.И. (ред.) (Bilay) Методы экспериментальной микологии. Киев: Наукова думка, 1982. 550 с.
Насонов А.И., Супрун И.И. (Nasonov, Suprun) Использование моноаскоспоровых изолятов в популяционных исследованиях Venturia inaequalis. Современные решения в развитии сельскохозяйственной науки и производства: Международный саммит молодых ученых: материалы конф. Краснодар, 2016. С. 124–128.
Насонов А.И., Якуба Г.В., Супрун И.И. (Nasonov et al.) Получение аскоспоровой культуры гриба Venturia inaequalis в лабораторных условиях // Микология и фитопатология. 2016. Т. 5. Вып. 2. С. 131–132.
Федорова Р.Н. (Fedorova) Парша яблони. Л.: Колос, 1977. 64 с.
Дополнительные материалы отсутствуют.
Инструменты
Микология и фитопатология


