Российские нанотехнологии, 2020, T. 15, № 3, стр. 280-308
ГРАФЕН И ГРАФЕНОПОДОБНЫЕ МАТЕРИАЛЫ ДЛЯ ВОДОРОДНОЙ ЭНЕРГЕТИКИ
О. К. Алексеева 1, И. В. Пушкарева 1, *, А. С. Пушкарев 1, В. Н. Фатеев 1
1 Национальный исследовательский центр “Курчатовский институт”
Москва, Россия
* E-mail: pushkareva_iv@nrcki.ru
Поступила в редакцию 10.06.2020
После доработки 10.06.2020
Принята к публикации 22.06.2020
Аннотация
В обзоре рассмотрены актуальные и перспективные области применения графена и материалов на его основе для целей экологически чистой водородной энергетики. Анализ результатов теоретических и экспериментальных исследований аккумулирования водорода в графеновых материалах подтверждает возможность создания на их основе систем обратимого хранения водорода, сочетающих высокую емкость, стабильность и возможность быстрого выделения водорода при приемлемых для практического использования условиях. Благодаря достижениям в области разработки химически- и термостойких мембранных материалов на основе графена могут быть созданы новые газоразделительные мембраны, обеспечивающие высокие проницаемость и селективность и перспективные для очистки водорода в процессах его получения из природного газа. Характеристики полимерных мембран, которые в основном используются в промышленности в настоящее время, могут быть существенно улучшены с помощью небольших добавок графеновых материалов. Применение графеноподобных материалов в качестве носителя наночастиц или функциональных добавок в составе электрокаталитического слоя в топливных элементах с твердым полимерным электролитом позволяет добиться улучшения их характеристик, повышения активности и стабильности электрокатализатора в реакции выделения кислорода.
ОГЛАВЛЕНИЕ
Введение
1. Системы хранения водорода на основе графена
2. Мембраны на основе графена для очистки и концентрирования водорода
3. Применение графена в электрокаталитических слоях топливных элементов с твердым полимерным электролитом
Заключение
ВВЕДЕНИЕ
В последние годы графену уделяется большое внимание со стороны научного сообщества. Огромным импульсом к активному исследованию и внедрению графена и графеноподобных материалов в различные области науки и техники послужили новаторские эксперименты А.К. Гейма и К.С. Новосёлова, за которые они были удостоены Нобелевской премии по физике в 2010 г. [1]. Графен представляет собой один слой (монослой) атомов углерода, плотно связанных в гексагональной кристаллической решетке. Это аллотроп углерода в форме плоскости sp2-связанных атомов с длиной молекулярной связи 0.142 нм [2]. Известно, что графен обладает рядом уникальных свойств, таких как очень высокие тепло- и электропроводность, высокая удельная площадь поверхности, механическая прочность, а также стойкость в агрессивных средах [2, 3]. Все эти свойства делают его крайне перспективным для наноэлектроники, электрохимической энергетики, в области мембранных материалов, опреснения и очистки воды; также ведутся исследования в области противораковых свойств графена. В представленном обзоре рассмотрены новые актуальные и перспективные области применения графена и материалов на его основе для целей экологически чистой водородной энергетики – для очистки и хранения водорода, а также для электрохимических систем его производства и применения.
1. СИСТЕМЫ ХРАНЕНИЯ ВОДОРОДА НА ОСНОВЕ ГРАФЕНА
Для развития водородной энергетики необходимо создание безопасных эффективных систем обратимого хранения водорода, сочетающих высокую емкость, стабильность и возможность быстрого выделения водорода [4–8]. Большое внимание уделяется наноматериалам на основе графена, двумерного (2D) кристалла, состоящего из монослоя sp2-гибридизованных атомов углерода, образующих “сотовую” структуру. Такая конфигурация атомов углерода может обеспечить эффективную связь с атомами водорода. С точки зрения хранения водорода графен обладает и другими полезными качествами. Он экологичный, легкий, термо- и химически стабильный, имеет высокую механическую прочность и его можно транспортировать на большие расстояния. В то же время графен – гибкий материал, что важно для использования в различных устройствах. Графен может быть синтезирован в больших количествах, разными методами, и его производство с каждым годом дешевеет. Удельная поверхность графена по теоретическим оценкам составляет 2630 м2/г [9, 10]. Конечно, при синтезе графена отдельные листки образуют агломераты и/или имеют дефекты, и реальная поверхность обычно составляет 150–600 м2/г (реже ~2000 м2/г). Заметим, что для трехмерных (3D) графеновых материалов удельная поверхность может достигать 3500 м2/г [11, 12]. Об этих материалах будет ниже рассказано отдельно.
Водород может адсорбироваться на графене двумя разными способами. Это физическая сорбция (обычно водород в молекулярном виде) и хемосорбция (атомарный водород).
Физическая сорбция обусловлена физическими взаимодействиями в основном силами Ван-дер-Ваальса. Этот процесс отличается быстрой кинетикой, но для обеспечения стабильности требуются высокие давления и низкие температуры. Энергия связи по разным оценкам составляет всего 0.01–0.06 эВ на расстоянии ~0.3 нм от графенового слоя [13, 14]. Первые теоретические оценки гравиметрической емкости хранения водорода дали для графена очень низкие значения, однако в 2005 г. авторы [15] учли в своей модели квантовые эффекты и получили обнадеживающие результаты. Отметим, что речь не идет об отдельном листе графена. В этой работе представлены данные для двух графеновых слоев, разделенных межслоевым промежутком d = 0.4–1.4 нм (рис. 1). Расчеты проведены для давлений 5 и 10 МПа и температур в диапазоне 200–300 К. Наилучшие результаты получены для межслоевого расстояния ~0.7 нм (в природном графите расстояние между слоями ~0.335 нм). При температуре 300 К и давлениях 5 и 10 МПа гравиметрическая емкость составляет 3.32 и 4.54 мас. % соответственно, а при 250 К и давлениях 5 и 10 МПа – 5.11 и 6.43 мас. % соответственно. При межслоевом расстоянии меньше 0.6 нм и больше 0.8 нм наблюдается существенное снижение значений емкости. По мнению Patchakovskii и соавт., только система из слоев с увеличенным по сравнению с графитом расстоянием может представлять интерес для практического применения. Создать такие системы можно, например, путем внедрения других атомов (подробнее об этом будет рассказано ниже).
Рис. 1.
Гравиметрическая (а) и объемная (б) емкости хранения водорода в зависимости от межслоевого расстояния. Сплошная горизонтальная линия – 6.5 мас. % и 31.2 см3/моль – ориентиры для хранения на борту транспортных средств [15].

В большинстве экспериментов значения сорбционной емкости графена оказались довольно низкими – меньше 1 мас. % при комнатной температуре и давлениях 0.1–10 МПа и чуть больше 1 мас. % при 77 К (например, [14, 16, 17]). Одни из лучших экспериментальных данных получены в [18] – 3.1 мас. % при 300 К и 10 МПа. Образец графена с удельной поверхностью 925 м2/г был получен эксфолиацией оксида графита и состоял из 3–6 слоев (рис. 2). Величина гравиметрической емкости близка к расчетам [15], однако надо учесть, что авторы [18] не исключают присутствия функциональных групп, возникших при синтезе и обработке.
Авторы [19] использовали модифицированную версию модели расширенного графита и продемонстрировали возможность хранения водорода между слоями нанопластинок графена. Эксперименты подтвердили их выводы о заметной физической сорбции. При давлении 0.2 МПа и температуре 99 К гравиметрическая емкость такой системы равна 2.47 мас. %.
Отдельного упоминания заслуживает графен с наноблистерами. Эта структура представляет собой графеновый слой с островками различной формы, в которых может накапливаться газ. Блистеринг, один из опаснейших механизмов разрушения металлов вследствие образования наполненных газом (водородом, гелием) пузырей, активно изучается уже более 50 лет, особенно в связи с проблемой создания термоядерного реактора [20]. В противоположность этому блистерная структура, обнаруженная у графеновых материалов, может быть использована для разработок систем хранения и транспортировки водорода [21–23]. Блистеры разных размеров возникают в процессе синтеза графеновых материалов или их специально формируют для получения определенных электронных свойств [24]. При воздействии атомарного водорода такие структуры образуются на поверхности высокоориентированного пиролитического графита (ВОПГ) или графена [21–23]. В [21] образцы ВОПГ подвергли воздействию атомарного водорода (5 × 1013 Н/см2). В результате поверхность образцов покрылась выпуклостями, в которых обнаружили молекулярный водород различными методами, включая метод сканирующей электронной микроскопии (СЭМ), причем его давление по оценкам ~2.7 МПа. Блистеры были стабильны в течение нескольких месяцев. Автор [21] полагает, что произошла интеркаляция атомарного водорода, который имеет достаточно маленький размер, чтобы проникнуть в слои графита. Затем он превратился в молекулярный газообразный водород, деформировал слой графита (графен) и оказался заперт в блистере. В [23] изучена сорбция водорода в систему из нескольких слоев графена с блистерами в верхнем монослое (рис. 3). В соответствии с экспериментальными результатами [21] рассмотрено заполнение атомарным водородом. Моделирование показало, что максимальная плотность водорода в блистере размером ~7 нм при 77 К и нормальном давлении составляет 6.86 мас. %, причем 6.66 мас. % – доля молекулярного водорода и только 0.2 мас. % остается в виде атомов, образовавших химические связи с решеткой на периферии блистера. Блистеры механически стабильны даже при наличии дефектов в структуре, но водород можно выделить при повышении температуры или давления. Конечно, перспективы практического применения пока не ясны, но ведь еще несколько лет назад было трудно представить, что графеновые блистеры будут использовать при разработке различных наномеханических устройств [23].
Объемная емкость хранения водорода при физической сорбции в графеновых материалах зависит от степени компактирования графеновых пластинок-чешуек. Достаточные величины могут быть достигнуты при комнатной температуре и давлении 10 МПа [15].
При хемосорбции (химической адсорбции) водорода между атомами водорода и графена образуется химическая связь (в основном ковалентная). Гибридизация атомов углерода изменяется с sp2 на sp3. Для хемосорбции молекулярного водорода требуется диссоциация (диссоциативная хемосорбция). Хемосорбция атомарного водорода является более благоприятным процессом. Считается, что энергия связи и барьер хемосорбции для атомарного водорода равны ~0.7 и ~0.3 эВ [13]. Однако здесь возникает проблема обратимости процесса адсорбции.
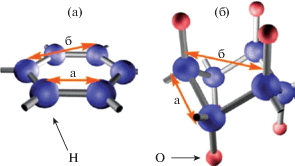
Максимальная достижимая емкость при хемосорбции, соответствующая заполненной поверхности графена, равна 8.3% (1 : 12). Для водородной энергетики с точки зрения хранения водорода представляет интерес и “гидрированный” графен – графан. Графан – 2D-материал, в котором каждый атом углерода связан с атомом водорода и тремя атомами углерода. В 2003 г. авторы [25] теоретически рассмотрели возможность хемосорбции водорода с двух сторон листа графена. Свое название “графан” материал получил в 2006 г. от авторов [26], которые, пользуясь расчетами из первых принципов, продемонстрировали его стабильность при комнатной температуре. В 2009 г. графан был получен экспериментально [27], его схема представлена на рис. 4.
Чтобы обеспечить хемосорбцию водорода с двух сторон, авторы [27] использовали образцы графена в виде свободных мембран. Обработку проводили холодной водородной плазмой. Заметим, что и в этом случае для систем хранения водорода проблемой является десорбция.
Как видно из приведенных выше данных, идеальный графен (а также графан) не перспективен для практического хранения водорода. Рассмотрим подробнее основные направления экспериментальных и теоретических исследований, нацеленных на повышение сорбционной емкости и кинетики сорбции/десорбции водорода на графене.
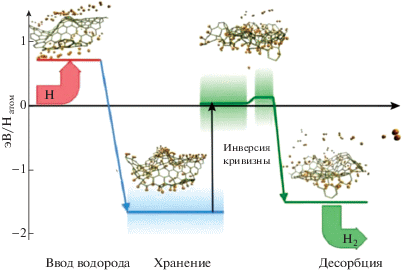
Одно из таких направлений – изучение влияния кривизны поверхности графеновых материалов на хемосорбцию водорода [14, 28–30]. Расчеты на основе теории функционала плотности продемонстрировали зависимость энергии связи и барьера адсорбции от кривизны. На выпуклых поверхностях, например на гребнях “гофрированного” графена, энергия связи на 1–2 эВ больше, чем во впадинах [28, 29], и барьер адсорбции значительно снижается. Экспериментальные результаты, полученные с помощью сканирующей туннельной микроскопии, подтвердили эти выводы [30]. Авторы [30] изучали адсорбцию водорода и обнаружили атомарный водород именно на выпуклых областях монослоя графена. Кривизна графена была обусловлена взаимодействием с SiC (0001) подложкой (заметим, что существуют и другие методы получения гофрированного, складчатого графена и т.п., например, [31]). Расчеты показали, что для десорбции водорода нужна инверсия кривизны (рис. 5).
Рис. 5.
Атомарный водород адсорбирован на гребнях поверхности. Инверсия кривизны приводит к десорбции водорода в молекулярном виде [28].

Инверсия кривизны приводит к десорбции водорода в молекулярном виде [28].
Зависимость хемосорбции от кривизны в сочетании с гибкостью графена позволяет надеяться на создание обратимых систем хранения водорода с контролируемым выделением водорода при комнатной температуре. По мнению авторов [29], гравиметрическая емкость может достигать 8 мас. %. Ассоциативная десорбция водорода происходит при инверсии кривизны без изменения температуры и давления, например, под действием внешних полей (рис. 6).
Рис. 6.
Схема устройства для хранения водорода. Можно выделить три фазы. Атомарный водород вводится в устройство, хемосорбируется на выпуклостях (гребнях) – начинается фаза хранения. Инверсия кривизны приводит к ассоциативной десорбции Н2 [29].
Для практического применения важно, что складки и волны, которые практически всегда присутствуют на поверхности графена, являются химически активными областями и, как показывают расчеты теории функционала плотности [32], могут в 6 раз снижать энергию диссоциации молекулярного водорода. Авторы [33] в своих экспериментах продемонстрировали, что водород в отличие от всех других газов проникает через монослой графена. Причиной этого является именно наличие областей с локальной кривизной и напряженным состоянием, на которых происходят адсорбция и диссоциация молекулярного водорода (барьер для достижения этого состояния снижается до 1 эВ). Образуется sp3-связь. Проникшие через монослой графена атомы водорода десорбируются с вогнутой поверхности, что и позволило авторам [33] их зарегистрировать.
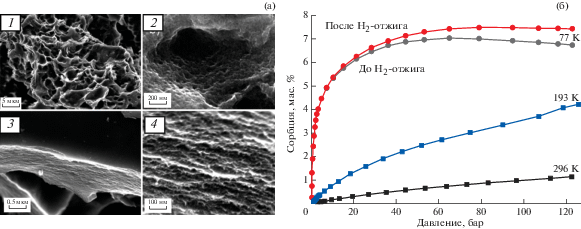
Это направление исследований относится к изменению конфигурации поверхности графена, а для практического применения необходимо создание объемных систем, которые по возможности сохраняли бы необходимые свойства при переходе от 2D к 3D. Очень трудно упаковать графеновые листки в многослойную 3D-структуру, сохранив между ними расстояние ~0.7 нм, оптимальное для физической сорбции [15, 34]. В настоящее время исследователи в основном используют два подхода – создание разупорядоченных пористых каркасов или встраивание между листками молекулярных столбиков-распорок [9, 11, 12]. Прекурсорами в обоих вариантах являются графеновые чешуйки или чешуйки восстановленного оксида графена (ВОГ). Восстановленный оксид графена, в отличие от графена, содержит остаточный кислород и другие гетероатомы, а также структурные дефекты. Восстановленный оксид графена получают из оксида графена (ОГ) ультразвуковым, химическим или термическим восстановлением, а также из оксида графита после предварительного восстановления этого материала щелочами до ОГ. Авторы [11] в своих экспериментах использовали чешуйки ВОГ, полученные из оксида графита и дополнительно активированные в КОН. В результате сформировалась иерархическая трехмерная каркасная структура (3D “scaffolds”) из частиц размером до 10 мкм, состоящих из дефектных и связанных между собой графеновых слоев (рис. 7). Удельная поверхность и объем пор равны 3200–3400 м2/г и 2.2 см3/г соответственно. Гравиметрическая емкость для 77 К достигает максимума при 4 МПа и составляет 7.04 мас. %; для 193 и 296 К сорбция водорода растет с увеличением давления и при 12 МПа равна 4 и 1.13 мас. % для 193 и 296 К соответственно (рис. 7). Дополнительная активация в атмосфере водорода в течение двух часов при 450°С увеличивает сорбцию водорода на ~10% для всех трех температур.
Рис. 7.
СЭМ-изображения образца с удельной поверхностью по БЭТ ~3300 м2/г. Видна иерархическая пористая структура (1, 2), а также слоистая структура на краях микрочастиц (3, 4) (а). Изотермы адсорбции при 77 К (до и после отжига в водороде), 193 и 296 К для образца с удельной поверхностью 3230 м2/г (б) [11].
Во втором варианте формирования 3D-графеновых структур для разделения слоев часто используют молекулярные столбики из органических молекул, например полианилина, диаминов (рис. 8) [35]. Моделирование дает неплохие результаты, около 4 мас. %, но в различных экспериментах гравиметрическая емкость достигает всего 1.5% [12].
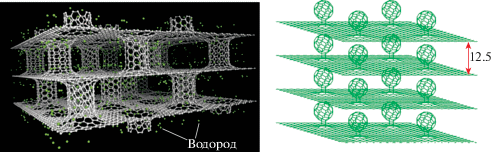
Исследователи предлагают и более экзотические варианты, когда “несущими опорами” между графеновыми “перекрытиями” являются углеродные нанотрубки (УНТ) [36, 37] или фуллерены (рис. 9) [38]. Сначала появились результаты компьютерного моделирования таких систем, в которых были предсказаны неплохие параметры сорбции водорода (например, по данным [36] 4 мас. % при 77 К и 1 МПа, а при добавках Li – 6.1 мас. % и 41 г/л при нормальных условиях). Позже 3D-системы с колоннами из нанотрубок были синтезированы, но довольно сложными способами [37, 39], и пока трудно представить возможность их практического применения.
Авторы исследований, о которых было рассказано выше, искали возможности повышения сорбционной емкости и улучшения кинетики сорбции/десорбции водорода на графеновых материалах путем изменения кривизны поверхности, увеличения расстояния между слоями, создания каркасных 3D-систем. Результаты теоретических рассмотрений и моделирования довольно оптимистичны, но в экспериментах, как в случаях физической сорбции, так и для хемосорбции, не удалось достичь нужных значений емкости при приемлемых для практического применения температурах и давлениях. Возможно, это связано с тем, что синтезированные образцы не могут в полной мере воспроизводить идеальные модельные системы.
Другой подход, направленный на повышение сорбции водорода при нормальных условиях, – функционализация графена гетероатомами [13, 14, 17, 40–43]. Сюда входит присоединение к поверхности графена атомов щелочных (Li, Na) [44, 45] и переходных металлов Ti, Ni, Pd, Pt (так называемое “декорирование”) [16, 46, 47], замещение графена атомами B, S, N, P (допирование) [48, 49], а также одновременное декорирование/допирование [17, 40, 50, 51]. Атомы переходных металлов на поверхности графена действуют как каталитические центры диссоциативной хемосорбции водорода. Благодаря их наличию возникает спилловер-эффект, т.е. миграция образовавшихся атомов водорода на графен, что повышает эффективность сорбции [6, 9, 52]. Кроме того, сторонники этого направления исследований считают, что декорированные-допированные системы позволят устранить недостатки как хемо-, так и физической сорбции, обеспечив “промежуточные” значения энергии связи. Это поможет улучшить как стабильность системы, так и кинетику сорбции-десорбции даже при комнатной температуре. Приведем некоторые результаты теоретических и экспериментальных исследований. Выше был рассмотрен пример эффективного действия добавок Li к 3D-системе графена с колоннами из УНТ [36]. Теоретические исследования [44] показали, что гравиметрическая плотность системы графен–2(Li–3H2) может достигать 10.2 мас. %. Авторы [44] рассматривали структуру графен–2Li–графен (два слоя графена с атомами лития в промежутке, декорирующими “пол” и “потолок”) (рис. 10). Средняя энергия адсорбции молекул водорода на атоме Li равна 0.37, 0.17 и 0.12 эВ для 1–3 молекул H2 соответственно, что находится между значениями для физической и химической сорбции (0.06–0.8 эВ). Таким образом, может быть реализована обратимая адсорбция водорода.
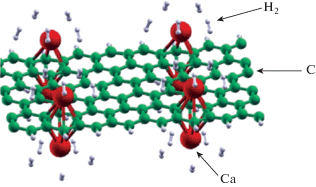
Расчеты из первых принципов для графена, декорированного атомами Ca, показали, что до шести молекул водорода могут адсорбироваться на атоме Сa с энергией связи 0.2 эВ/H2, и гравиметрическая емкость достигает ~5 мас. % (рис. 11) [53].
Рис. 11.
Оптимизированная структура графена с атомами Са, адсорбирующая максимальное количество молекул водорода [53].
Декорирование переходными металлами, как показывают результаты теоретических оценок и моделирования, а также экспериментов, приводит к формированию стабильных, но обладающих обратимостью систем. В [47] методом расчетов ab initio, основанных на использовании теории функционала плотности, продемонстрировано, что адсорбция атомов Pt приводит к повышению энергии связи молекул водорода в сравнении с величиной для исходного графена, равной ~0.07 эВ. В зависимости от числа адсорбированных молекул водорода, от одной до восьми, энергия связи меняется от 1.84 до 0.13 эВ соответственно. Гравиметрическая емкость графена при адсорбции восьми молекул H2 на атом Pt, равна 3.74 мас. %. Экспериментальные данные подтверждают, что гравиметрическая емкость графена при декорировании переходными металлами возрастает, но величины не превышают 1.5 мас. % [16, 46, 54]. Так, авторы [54] после декорирования платиной образца графеновых пластинок, состоящих из нескольких слоев, получили 1.4 мас. % при 298 К и 3 МПа. В [46] декорирование Pt и Pd привело к двукратному увеличению сорбционной емкости графена при 303 К и 5.7 МПа – с 0.067 до 0.15 и 0.156 мас. % соответственно. Возможно, спилловер-эффект, который должен способствовать повышению сорбции, подавляется при агломерации частиц. По-видимому, единственным исключением являются отличные результаты [55]. Авторы [44] синтезировали нанокомпозит Pd-графен. Сферические наночастицы Pd размером 5–45 нм были равномерно распределены в графеновой матрице, состоящей из пластинок графена со сморщенной поверхностью. При давлении 5 МПа и комнатной температуре гравиметрическая емкость достигла 6.7 мас. % при 1% Pd в нанокомпозите, при 6 МПа – 8.67 мас. % при 1% Pd и 7.16 мас. % в нанокомпозите.
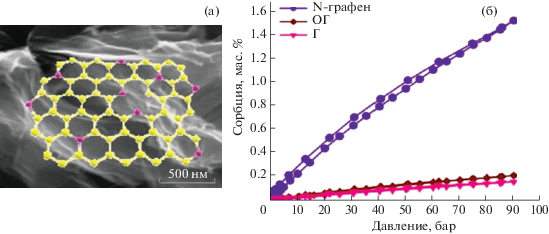
Допирование (замещение углерода в решетке) N, P, S и некоторыми другими атомами в зависимости от их свойств приводит к перераспределению зарядов у соседних атомов, структурной деформации, образованию вакансий. Гетероатомы могут быть центрами активации водорода, который затем путем спилловера перейдет на поверхность углеродной матрицы. В [49] показано, что в результате P-допирования гравиметрическая емкость материала из многослойных листков графена повышается и достигает ~2.2 мас. % при 298 К и 10 МПа (рис. 12).
Рис. 12.
СЭМ-изображение материала из многослойных графеновых листов, допированных фосфором (а). Сорбция водорода этим материалом и недопированными порошком графита (Г), оксидом графена (ОГ), ВОГ (б) [49].

Слоистый графеновый материал, допированный азотом (7.5 ат. %), был исследован в [48]. При комнатной температуре и давлении 9 МПа гравиметрическая емкость равна ~1.5 мас. % (рис. 13).
Рис. 13.
N-допированный графеновый материал (а) и изотермы адсорбции/десорбции при 298 К для этого материала и недопированных порошка графита (Г) и оксида графита (ОГ) (б) [48].
Отметим, что допирование азотом активно используется при разработке эффективных электрокатализаторов водородных топливных элементов (ТЭ) [56–59]. Графен, как и другие углеродные наноматериалы, сам по себе не может являться катализатором из-за отсутствия активных центров. Образование различных азотных конфигураций (графитоподобный, или замещающий N, пиридиновый N и пиррольный N) приводит к созданию таких центров, а также играет важную роль в стабилизации наночастиц каталитического металла (Pt, Pd). Существуют различные методы допирования азотом, например при синтезе графеновых материалов или при последующей обработке. Как показывают недавние исследования, эффективным является метод азотирования в плазме газового разряда (плазмообразующими газами являются азот или смесь азот/аргон) [60].
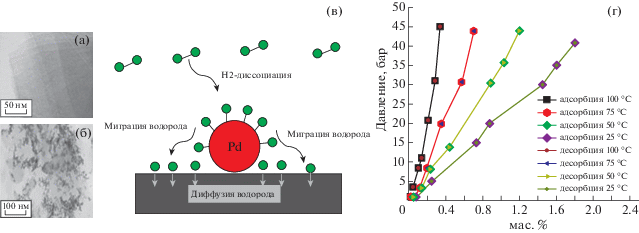
Наиболее перспективные исследования сорбции водорода в графеновых материалах с гетероатомами, по-видимому, относятся к совместному декорированию-допированию, особенно при допировании азотом и декорировании металлами Pt, Pd. Атомы этих и некоторых других переходных металлов на поверхности графена действуют как каталитические центры диссоциации молекул водорода. Внедрение атомов азота, как уже говорилось выше, образуют центры стабилизации наночастиц этих металлов, предотвращают их агломерацию, что могло бы снизить спилловер-эффект. Однако экспериментальных работ такого рода пока на удивление мало. Один из примеров – допирование азотом нанопластинок графена (10–20 одноатомных слоев), декорированных палладием [51]. При комнатной температуре и давлении 3.2 МПа гравиметрическая емкость для нанопластинок графена, N-нанопластинок графена и Pd-декорированных N-нанопластинок графена равна 0.27, 0.42 и 1.25 мас. % соответственно (рис. 14, изображения получены с помощью просвечивающей электронной микроскопии (ПЭМ)). Авторы [51] подчеркивают, что допирование азотом обеспечило сильную связь Pt–графен и высокую дисперсию наночастиц Pt.
Рис. 14.
ПЭМ-изображение N-графена (а) и Pd–N-графена (б). Схема спилловер-эффекта на Pd–N–графене (в). Изотермы адсорбции-десорбции водорода для образца Pd–N–графен при температурах 25–100°С и давлениях до 4.5 МПа (45 бар) (г) [51].
В заключение этого раздела расскажем еще об одном подходе к созданию 3D-систем хранения водорода. Графен в них не является основным компонентом, однако играет важную роль. Речь идет о композитах из наноструктурных гидридов, “завернутых” в графен [61]. Комплексный гидрид LiBH4 имеет высокие расчетные гравиметрическую (18.5 мас. %) и объемную плотность (121 кг/м3), но температура десорбции высокая [6]. Термодинамические параметры можно несколько улучшить путем добавления дестабилизирующего агента MgH2. Гравиметрическая емкость системы 2LiBH4–MgH2 равна 11.4 мас. %. Для приемлемой скорости десорбции все равно требуется температура выше 400°С. Кроме того, возникают проблемы при циклировании – рост зерен, разделение фаз, агломерация частиц. Авторы [61] создали уникальный композит из наночастиц 2LiBH4–MgH2 размером ~10.5 нм, равномерно распределенных на гибких, но прочных графеновых подложках. Схема синтеза представлена на рис. 15.
Рис. 15.
Схема синтеза нанокомпозита 2LiBH4–MgH2–графен: 1 – самосборка наночастиц MgH2 на графене при сольвотермическом синтезе в атмосфере водорода; 2 – пропитка раствором LiBH4; 3 – удаление растворителя и гетерогенная нуклеация LiBH4 на наночастицах MgH2 [61].

Изображения наночастиц MgH2 на графене и 2LiBH4–MgH2 на графене, полученные методом СЭМ, показаны на рис. 16.
Рис. 16.
СЭМ-изображения наночастицы MgH2 на графене (а) и нанокомпозита 2LiBH4–MgH2–графен (б, в) [61].

Нанокомпозит имеет высокую емкость (9.1 мас. %) и хорошую стабильность при циклировании (после 25 циклов при 350°С емкость равна 8.9 мас. %).
Рассмотренные выше результаты теоретических и экспериментальных исследований аккумулирования водорода в графеновых материалах подтверждают возможность создания на их основе эффективных систем обратимого хранения водорода.
2. МЕМБРАНЫ НА ОСНОВЕ ГРАФЕНА ДЛЯ ОЧИСТКИ И КОНЦЕНТРИРОВАНИЯ ВОДОРОДА
Для водородной энергетики первостепенное значение имеют задачи концентрирования водорода и очистки его от примесей. Существуют различные методы промышленного производства водорода: паровая конверсия метана или природного газа, газификация угля, электролиз воды, термохимические методы [62]. Используют также паровую конверсию в водород этанола, получаемого в больших количествах из возобновляемой биомассы [63]. Во всех случаях требуется дополнительная очистка целевого продукта. Например, водород, полученный при паровой конверсии метана, одной из наиболее распространенных в настоящее время технологий, неизбежно содержит примеси метана.
Для концентрирования и очистки водорода применяют мембранное разделение газовых смесей, короткоцикловую адсорбцию с переменным давлением, криогенную дистилляцию. Последние два способа, хотя и позволяют получить чистый водород, но имеют высокую стоимость и значительное энергопотребление. В настоящее время мембранные методы очистки считаются наиболее перспективными, так как обеспечивают оптимальное соотношение затраты–эффективность [64]. Важнейшие характеристики мембран – проницаемость и селективность – зависят от физических и химических свойств мембранных материалов. В промышленности в основном используют полимерные мембраны [65–67]. К сожалению, при этом приходится жертвовать проницаемостью ради селективности или наоборот. Активно продолжаются исследования и разработки в других направлениях; большое внимание уделяется мембранам с наноструктурным углеродным селективным слоем, а также со смешанной матрицей (mixed matrix membranes), включающей в себя углеродные наноматериалы [68–76]). Особый интерес вызывает графен. Действительно, это очень перспективный мембранный материал с минимально возможной толщиной (в один атом), при этом прочный, гибкий, химически- и термостабильный. В последнее время были разработаны различные методы его синтеза в довольно больших объемах. Конечно, идеальный графен непроницаем для газов. Заметим, что недавно было экспериментально показано, что Н2, в отличие от всех других газов, в некотором количестве проникает через монослой графена [33] (разд. 1). Тем не менее причиной этого является наличие складок, волн на поверхности (эффект кривизны поверхности), т.е. именно “неидеальность” графена.
Основные направления при разработке мембран на основе графена: создание пор в плоскости графена, конструирование каналов в графеновых слоях (с использованием ОГ) [65–67, 77–79].
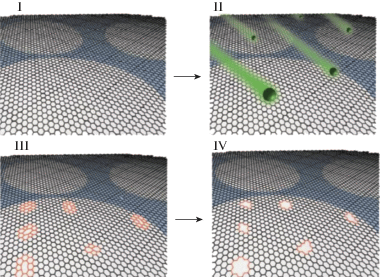
Нанопористый графен и по теоретическим оценкам, и по некоторым экспериментальным данным является материалом, который может обеспечить высокие проницаемость и селективность при разделении газовых смесей, содержащих водород. Сложность заключается в создании необходимого количества пор нужного размера. Используют ионные, электронные пучки, плазменную обработку [80–84]. Например, с помощью сфокусированного пучка ионов Ga и He в двухслойном графене сформировали поры диаметром в интервале от 10 нм до 1 мкм [81]. Авторы [80] показали, что бомбардировка монослоя графена ионами галлия (6 × 1012 см–2) приводит к возникновению дефектов, которые при довольно длительном химическом травлении с использованием окислителя превращаются в поры диаметром 0.4 нм, при этом плотность пор ~1012 см–2 (рис. 17).
Рис. 17.
Процесс создания контролируемых субнанометровых пор в графене: I – графен на сетке для ПЭМ, II – бомбардировка ионами галлия, III – бомбардировка создает дефекты, IV – химическое травление превращает дефекты в поры [80].
Авторы [83, 84] продемонстрировали, что нанопористый графен действительно обеспечивает рекордное разделение смеси H2/CH4 при высокой проницаемости. Они разработали метод формирования пор строго контролируемого размера (с точностью до десятых долей нанометра). При обработке монослоя графена кислородной плазмой (1–2 с) возникают дефекты (в основном sp3-типа), из которых в результате последующего травления в газообразном озоне (2–10 с) развиваются поры, пропускающие H2 и не пропускающие CH4 и C3H8, т.е. размером не более 0.38 нм (размеры молекул H2, CH4 и C3H8 равны 0.259, 0.38 и 0.43 нм соответственно) (рис. 18). Плотность этих пор составляет 2.1 × 1012 см–2, что достаточно для обеспечения высокой проницаемости. Доля более крупных пор менее 0.002%. Фактор разделения равен 15–25 для смеси H2/CH4 и 38–58 для смеси H2/C3H8. Если рассматривать процесс выделения водорода из смеси, содержащей 35% водорода, то при факторе разделения 20 будет восстановлено 90% водорода 90% чистоты.
Рис. 18.
Схема формирования пор в монослое графена [84]. Зарождение дефектов под воздействием О2-плазмы. Развитие пор при травлении озоном.

Авторы исследований [83, 84] также разработали способ переноса без повреждений монослоя графена, синтезированного методом химического осаждения из газовой фазы, на микропористую подложку, что важно для практического использования этого мембранного материала.
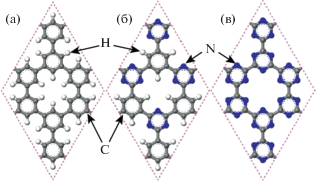
Теоретические исследования предсказывают, что мембраны на основе нанопористого графена могут иметь даже более высокую эффективность, чем обнаружено в экспериментах, особенно при модификации пор азотом. В [85] с использованием метода функционала плотности показано, что пористый графен и пористый графен, в разной степени модифицированный азотом (рис. 19), обеспечивают проницаемость водорода, требуемую для применения в промышленности, при 350, 275 и 125 К для конфигураций а, б, в соответственно. Энергетические барьеры для прохождения газов через поры тем выше, чем мельче поры и крупнее молекулы газов. Соответственно, проницаемость для изученных в работе газов имеет зависимость, противоположную величине барьера: He > H2 > Ne > CO > N2 > Ar > CH4. Селективность, необходимая для очистки водорода, очень высока, при этом H2/CH4 > H2/N2 > H2/CO.
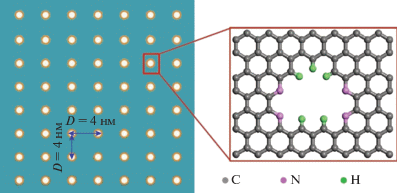
Авторы [77] сравнили проницаемость и селективность графеновых и полимерных мембран при разделении смеси H2/CH4. Для моделирования методами молекулярной динамики использована конфигурация графеновой мембраны, показанная на рис. 20. Часть атомов углерода заменена модифицирующими атомами водорода и азота. Расстояние между порами (4 нм) и плотность пор (~6 × 1012 см–2) близки к приведенным выше экспериментальным данным.
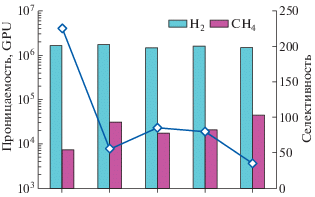
Проницаемость нанопористых графеновых мембран по расчетам [77] на порядок величины больше, чем у полимерных мембран, а селективность немного ниже, но того же порядка величины (она достигает 225, а у некоторых полимерных может быть 300–400) (рис. 21). С точки зрения энергозатрат на сжатие и на требуемую площадь мембраны может быть достигнут значительный экономический эффект – потребление энергии на сжатие не зависит от селективности, если ее значение выше 200, а выигрыш в площади мембраны будет существенным.
Рис. 21.
Проницаемость (гистограмма) и селективность (линия) для разного соотношения водород–метан в смеси (5:1, 5:2, 5:3, 5:4, 5:5) [77].
Мембраны на основе оксида графена (ОГ-мембраны) благодаря своей уникальной тонкой слоистой структуре и наличию функциональных групп также могут обеспечить высокие проницаемость и селективность и найти практическое применение для очистки или выделения водорода [66, 67, 73, 79, 86–93]. Однородные слоистые структуры, необходимые для создания мембран, можно получить из дисперсий чешуек ОГ, используя покрытие окунанием, вакуумную фильтрацию, покрытие распылением, послойное осаждение и другие методы. Важно оптимизировать размеры чешуек, конфигурацию упаковки, общую толщину, межслоевое расстояние. Без этого диффузионный путь для молекул газа будет слишком извилистым, длинным, что скажется на проницаемости. В настоящее время синтезируют и исследуют различные типы ОГ-мембран – свободные (без подложки), осажденные на пористые полимеры, керамику и другие пористые материалы, и композитные. Мембраны без подложки имеют преимущества за счет минимальной толщины. Даже при общей толщине мембраны в несколько микрон при малых горизонтальных размерах чешуек получали значительные проницаемость и селективность для смеси Н2/CO2 [86]. Методом молекулярной динамики авторы [88] показали, что ОГ-мембрана эффективно разделяет водород и метан. В [93] этим же методом изучили смесь Н2/CO2 и выяснили, что селективность зависит от межслоевого расстояния и расстояния между порами, находящимися в разных слоях. Как экспериментальные, так и теоретические данные говорят о том, что вопрос о механизме транспорта молекул газа не до конца ясен. По-видимому, основным механизмом для крупных молекул (CH4, N2, CO2) является кнудсеновская диффузия, поскольку межслоевое расстояние довольно большое. Это подтверждают экспериментальные данные: проницаемость для этих газов обратно пропорциональна квадратному корню из молекулярной массы [89, 90, 92]. Однако существенно более высокая проницаемость для водорода и гелия говорит о том, что дополнительный вклад дает другой путь. По мнению авторов [89, 90], это прямой узкий канал, образованный дефектами (рис. 22). Конечно, на структуру слоев, пористость влияет метод синтеза чешуек ОГ и самой мембраны. На рис. 23 приведены СЭМ-изображения поверхности и сечения ОГ-мембраны, полученной вакуумной фильтрацией на макропористую полимерную подложку [90].
Рис. 23.
СЭМ-изображения поверхности и сечения ОГ-мембраны, полученной вакуумной фильтрацией на макропористую полимерную подложку [90].

Для очистки водорода также представляют интерес нанокомпозитные и гибридные мембраны, состоящие из пластинок графена или ОГ и полимерного или неорганического мембранного материала [65, 66, 73]. Как показали работы, проведенные в НИЦ “Курчатовский институт”, микропористые керамические трубки из оксида алюминия являются хорошей подложкой для получения нанокомпозитных мембран с наноуглеродным селективным слоем [68–70]. Авторы [94] синтезировали новый тип таких мембран с нанесенным из раствора монослоем ОГ. Мембраны продемонстрировали стабильность, высокую проницаемость для водорода и хорошую селективность H2/CO2 (фактор разделения >57). Авторы [73] разработали метод получения гибких 2D-мембран со смешанной матрицей, основным материалом которых является ОГ, а металл-органические каркасные (МОК) структуры представляют собой наноразмерные микропористые включения, повышающие проницаемость. Для этого сначала методом последовательного осаждения из растворов создали ультратонкую смешанную мембрану из ОГ и нанопластинок СuO, затем ввели в растворе органические лиганды и преобразовали CuO в каркасные структуры (рис. 24). Проницаемость синтезированных мембран высокая, фактор разделения H2/CO2 равен 73.2.
Рис. 24.
Схема синтеза гибкой ОГ-мембраны. Нанопластинки CuO внедрены в матрицу ОГ. В результате реакции CuO с органических лигандами в растворе in situ формируются МОК-структуры (а). СЭМ-изображения сечения мембраны (б) [73].

Методом вакуумной фильтрации были синтезированы стабильные гибридные мембраны ОГ–MoS2 (рис. 25) [95]. Мембрана толщиной 60 нм, содержащая ~75 мас. % MoS2, обеспечила высокую проницаемость для водорода и селективность H2/CO2, равную 26.7, а мембрана толщиной 150 нм, содержащая ~29 мас. % MoS2, оказалась более селективной (44.2), но проницаемость была в ~2.6 раза ниже. В целом ОГ–MoS2 имеет проницаемость и селективность лучше, чем ОГ-мембрана и MoS2-мембрана, т.е. имеется синергетический эффект. В гибридной мембране упаковка слоев была такой же, как в чистой ОГ-мембране, но добавление нанопластинок MoS2 привело к образованию пор (плотность пор тем выше, чем больше концентрация MoS2). С точки зрения практического применения важно, что гибридная мембрана имеет высокую стабильность.
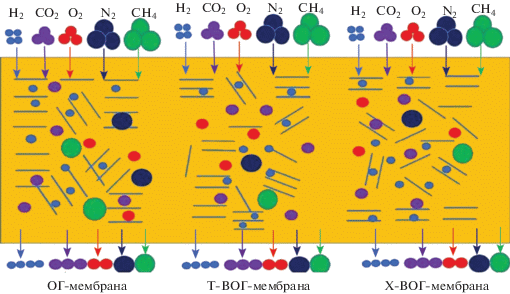
Как было сказано выше, в промышленности в настоящее время в основном используют полимерные мембраны, при этом приходится жертвовать либо проницаемостью, либо селективностью. Исследователи пытаются преодолеть эти проблемы, добавляя в полимер графеновые материалы. Разрабатывают разные варианты мембран со смешанной матрицей. По мнению авторов [65], наилучшим полимером является полиимид Matrimid. Это термостабильный материал, имеющий достаточную механическую прочность и хорошие газотранспортные свойства, особенно для целей очистки и концентрирования водорода. Из смеси раствора порошка этого полимера и суспензий нанопластинок ОГ было синтезировано три типа пленок – мембранных материалов. Использовали ОГ, полученные из оксида графита методами ультразвуковой эксфолиации, термического восстановления (Т-ВОГ) и химического восстановления (Х-ВОГ). По данным рентгеновской дифракции толщина нанопластинок ОГ составляет 5.62, 0.92 и 0.97 нм для ОГ, Т-ВОГ и Х-ВОГ, при этом количество слоев соответственно равно 6, 3 и 2, а межслоевые расстояния – 0.89, 0.31 и 0.41 нм. СЭМ-изображения сечений трех мембран, содержащих 0.4 мас. % ОГ, и исходного полимера представлены на рис. 26. Видно, что графеновые наночастицы распределены равномерно и каждая находится в окружении полимерной ячейки.
Рис. 26.
СЭМ-изображения сечений трех композитных мембран, содержащих 0.4 мас. % оксида графена: ОГ (а), Т‑ВОГ (б), Х-ВОГ (в) и исходного полимера (г) [65].

Транспорт газов в полимерных мембранах подчиняется механизму “растворение–диффузия”. В композитных мембранах графеновые включения влияют на диффузию. Когда молекулы газа встречают препятствие в виде графеновых нанопластинок, они могут либо вернуться в полимерную матрицу, либо проникнуть между слоями. Механизм – кнудсеновская диффузия или молекулярно-ситовой эффект – зависит от промежутка между слоями. Так, в случае мембраны с ОГ молекулы всех исследованных газов (H2, CO2, O2, N2 и CH4) могут проходить не только через полимерную, но и через графеновую фазу с межслоевым расстоянием 0.89 нм (рис. 27). Газотранспортные свойства лишь немного улучшаются по сравнению с полимерной мембраной. В отличие от этого мембраны с Т-ВОГ и Х-ВОГ, имеющие межслоевое расстояние 0.39 и 0.41 нм, проявляют исключительно высокую селективность в процессах с водородом. Селективность H2/CH4 при концентрации 0.2 мас. % ОГ достигает 226 для мембраны с Т-ВОГ и 231 для мембраны с Х-ВОГ (для полимерной мембраны она равна 50). Селективность H2/N2 для этих мембран возрастает примерно в 2 раза по сравнению с исходной полимерной мембраной. Таким образом, новые мембраны перспективны для очистки водорода в процессах его получения из природного газа, а также для извлечения водорода из продувочных газов синтеза аммиака.
Разработка химически- и термостойких мембранных материалов на основе графена, обеспечивающих высокие проницаемость и селективность, может привести к значительному прогрессу в мембранных технологиях, что важно для задач водородной энергетики. Такой уникальный материал, как графен, находит множество других применений, в том числе для борьбы с инфекциями. Ученые во многих странах полагают, что он сыграет важную роль в победе над коронaвирусной инфекцией COVID-19 и будет использован как для диагностики (сенсоры), так и для защиты (фильтры, маски (рис. 28)) [96]. Китайские исследователи уже предложили метод функционализации обычных хирургических масок путем нанесения графеновых покрытий. Новые маски супергидрофобные, их можно стерилизовать просто на солнце и использовать многократно [97].
3. ПРИМЕНЕНИЕ ГРАФЕНА В ЭЛЕКТРОКАТАЛИТИЧЕСКИХ СЛОЯХ ТОПЛИВНЫХ ЭЛЕМЕНТОВ С ТВЕРДЫМ ПОЛИМЕРНЫМ ЭЛЕКТРОЛИТОМ
Энергоустановки на основе ТЭ с твердым полимерным электролитом (ТПЭ) являются одними из наиболее перспективных благодаря низкой рабочей температуре, низкому уровню шума, способности к быстрому запуску, высокой удельной мощности и экологичности. Топливные элементы с ТПЭ были разработаны для использования в небольших генераторах энергии (мощностью от 1 кВт до 5 МВт), установленных в местах непосредственного потребления: в больницах, отелях и офисных зданиях, благодаря их компактной конструкции. Они также могут использоваться в портативных электронных устройствах (20–100 мВт), таких как ноутбуки, мобильные телефоны, видеокамеры, потому что они легче и меньше батарей, а также имеют более длительное время непрерывной работы, более быстрое время отклика и не требуют перезарядки от сети (в отличие от аккумуляторных батарей). Другой важнейшей нишей применения ТЭ с ТПЭ (мощностью 5–500 кВт) является транспорт, например автобусы, автомобили, мотоциклы, беспилотные летательные аппараты. Развитию данного направления способствует постоянный рост цен на ископаемое топливо, вызванный его ограниченной доступностью и ужесточением “экологического” законодательства во многих странах мира с целью снижения интенсивности выбросов парниковых газов [98]. Кроме того, благодаря таким своим свойствам, как низкая инерционность, высокий уровень взрывопожаробезопасности, малое время отклика на изменение мощности нагрузки, ТЭ с ТПЭ играет немаловажную роль в энергоустановках и энергосистемах на основе возобновляемых источников энергии, которые в настоящее время активно внедряются мировую энергетику.
Важнейшим сдерживающим фактором является ограничение ресурса ТЭ с ТПЭ, которое связано главным образом с деградацией электродов, мембраны и влиянием примесей, содержащихся в подаваемых газах. Отравление поверхности электрокатализатора (например, молекулами СО) приводит к ухудшению характеристик ТЭ за счет снижения числа активных центров [99]. Одним из основных компонентов ТЭ с ТПЭ являются электрокаталитические слои, в которых протекают полуреакции, в сумме представляющие собой токообразующую реакцию. Протекание полуреакций с высокой скоростью обеспечивается использованием электрокатализаторов, которые традиционно представляют собой наночастицы Pt на углеродном носителе [100].
В настоящее время в качестве носителей электрокатализаторов наиболее широкое распространение получили различные сажи (марок Vulcan XC-72, Ketjen Black и др.). Свойства этих углеродных носителей, в том числе их относительно высокая удельная поверхность (до 250 м2/г для XC-72 [101]), пористая структура, электропроводность, механическая прочность и устойчивость к коррозии, во многом определяют эффективность катализаторов и, соответственно, эффективность работы электрохимической системы. К наиболее важным недостаткам сажи относятся наличие сероорганических примесей, глубоких микропор (доля микропор составляет до 47% [100]) на поверхности материала, а также все-таки недостаточно высокая стабильность. Наночастицы катализатора оказываются в ловушке в микропорах и не имеют доступа к реагентам и электролиту, в результате чего снижается каталитическая активность [101, 102]. Сажа также нестабильна в сильнокислых/щелочных условиях в ТЭ, что выражается в виде коррозии углеродного носителя и отрыва наночастиц катализатора [101], что в свою очередь приводит к значительному ухудшению характеристик ТЭ с ТПЭ.
В целом ключевыми отличиями графена и его производных от углеродной сажи, традиционно используемой в качестве носителя электрокаталитически активных наночастиц Pt (например, Vulcan XC-72 [103]), является его высокая удельная поверхность, химическая стабильность, графитоподобная структура [104], которая обеспечивает более высокую электрохимическую коррозионную стойкость носителя, а также сильное взаимодействие металл–носитель, предохраняющее каталитически активные наночастицы Pt от укрупнения и растворения [105, 106]. Также к преимуществам графеноподобных материалов можно отнести их слоистую структуру, которая может облегчить массоперенос реагентов [107] и повышение толерантности анодного катализатора ТЭ с ТПЭ на основе Pt к СО [107]. С другой стороны, графеноподобные материалы при их использовании в качестве носителей обладают рядом недостатков, сдерживающих внедрение этих материалов в качестве носителей. К таким недостаткам можно отнести сильную агломерацию наночастиц Pt при синтезе катализаторов; “рестекинг” нанолистов графена вследствие ван-дер-ваальсова взаимодейсвтия; склонность нанолистов графена к агломерированию в водных растворах [108]. На свойства катализаторов на основе графеноподобных материалов влияют различные факторы, такие как методы синтеза и сушки, методики приготовления “каталитических чернил”, механическая, химическая, физическая обработка катализатора и т.п. [109–112].
В [109] был исследован катализатор Pt/ВОГ, приготовленный путем одновременного восстановления оксида графена и H2PtCl6 с помощью NaBH4 в качестве восстановителя. Содержание Pt в катализаторе составило 45 мас. %, а площадь удельной электрохимически активной поверхности (ЭАП) – 44.6 м2/г Pt. Исследования электрохимической активности катализатора в реакции окисления метанола методом циклической вольтамперометрии показали, что полученный электрокатализатор Pt/ВОГ существенно активнее по сравнению с Pt/Vulcan, приготовленным аналогично. Максимальная плотность тока Pt/ВОГ составила около 200 мА/мг Pt при 0.652 В (относительно хлорсеребряного электрода сравнения), что почти вдвое выше, чем у Pt/Vulcan. В [111] авторы показали влияние процедуры сушки катализатора Pt/ВОГ, синтезированного тем же методом, что и в [109, 110], на свойства каталитических чернил. В случае традиционной сушки катализатор сильно агрегируется, поэтому повторное диспергирование чернил для их нанесения практически невозможно даже с помощью мощной ультразвуковой обработки. Большое внимание уделяется диспергированию графеновых листов в воде или других растворителях с помощью добавки поверхностно-активных веществ или функционализации поверхности графена. Однако поверхностно-активные вещества негативно влияют на протекание реакций в ТЭ, а также могут привести к ухудшению электронной проводимости [112]. Для стабилизации графена и предотвращения необратимой агрегации и сворачивания плоскостей во время сушки и термообработки в [111] предложено применить лиофилизацию, которая позволила предотвратить сильное агрегирование Pt/ВОГ. Максимальная плотность тока Pt/ВОГ в реакции окисления метанола составила 182.6 А/г, в то время как для Pt/Vulcan XC-72 она составила лишь 77.9 А/г. Отжиг катализатора Pt/ВОГ (Pt/ВОГ-O) при 300°С в течение 2 ч в атмосфере N2 позволил повысить максимальную плотность тока до 261.6 А/г за счет таких факторов, как усиление взаимодействия между Pt и носителем (ВОГ), возникновение дополнительных активных центров Pt, частичное разрушение поверхностных функциональных групп, ведущее к уменьшению количества дефектов на поверхности ВОГ и повышению его стабильности, а также повышение кристалличности наночастиц Pt.
В [110] синтез электрокатализатора Pt/ВОГ осуществлялся полиольным методом, однако двумя разными способами. В одном случае восстановление оксида графена и H2PtCl6 осуществлялось в этиленгликоле одновременно, тогда как во втором случае ОГ предварительно восстанавливался с помощью NaBH4, а затем помещался в этиленгликоль, и на его поверхность высаживались наночастицы Pt. Вольтамперометрические измерения, а также результаты тестирования электрокатализаторов в составе ТЭ с ТПЭ показали, что катализатор, полученный в двухстадийном процессе, оказался более активным в реакции окислении метанола.
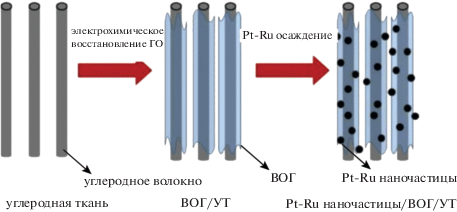
В [113] авторам удалось синтезировать биметаллические наночастицы Pt–Ru на волокнах углеродной ткани, обернутых нанолистами ВОГ (рис. 29). Необходимость такой модификации углеродной ткани объясняется тем, что, несмотря на высокую площадь поверхности ткани, наночастицы слабо взаимодействуют с поверхностью волокон и их дисперсность остается невысокой [114]. Модификация способствует образованию равномерно распределенных наночастиц электрокатализатора малого размера с высокой площадью поверхности. В [115] синтезирован многослойный электрокатализатор, представляющий собой углеродные нановолокна (УНВ), обернутые листами ВОГ, на поверхность которых высажены наночастицы Pt. Эти частицы играют роль спейсера для следующего слоя ВОГ, на который вновь восстанавливаются наночастицы Pt и т.д. Циклические вольтамперометрические исследования катализатора в растворе 1 M KOH и 1 M CH3OH показали, что многослойный электрод обладает более высокой каталитической активностью в реакции окисления метанола по сравнению с Pt/ВОГ/УНВ и Pt/УНВ.
Рис. 29.
Схема синтеза наночастиц Pt–Ru на волокнах углеродной ткани, обернутых ВОГ (УТ – углеродная ткань, ГО – оксид графита) [113].
Графен привлекает большое внимание и как носитель электрокатализаторов для водородно-кислородных (-воздушных) ТЭ [116–119].
В [116] удалось синтезировать ряд платиновых катализаторов на ВОГ в качестве носителя с величиной ЭАП более 70 м2/г Pt. В частности, исследовались катализаторы Pt/ВОГ, модифицированные полидиаллилдиметиламмонием (ПДДА), который используется для функционализации поверхности графена с целью улучшения дисперсии наночастиц Pt на поверхности ВОГ. Так, величина ЭАП электрокаталитического слоя на основе ПДДА-модифицированного ВОГ оказалась равной 78.6 м2/г Pt против 72.5 м2/г Pt у катализатора на основе немодифицированного ВОГ. В ходе исследований в составе воздушно-водородного ТЭ удалось достичь величины максимальной плотности мощности более 700 мВт/см2. Величина ЭАП катализатора Pt/ВОГ после проведения ускоренного стресс-тестирования (УСТ) составила 23.5% от исходной, а Pt/ВОГ-ПДДА – 43%.
В [120] показано, что использование этиленгликоля в качестве восстановительного агента позволяет получать электрокатализаторы на основе Pt и ВОГ или графеновых нанопластинок (ГНП) с наиболее высокой ЭАП и активностью в реакции восстановления кислорода (РВК) с равномерным распределением наночастиц по поверхности носителя. Кроме того, показано, что в качестве прекурсора наночастиц Pt H2PtCl6 оказалась более эффективной, чем K2PtCl4. В [121] авторы представили два различных и эффективных метода синтеза наночастиц Pt на ГНП в качестве носителя. Первый метод – осаждение в среде сверхкритического CO2, а второй – метод микроволнового облучения. Преимущество первого заключается в уменьшении степени агломерации наночастиц Pt в процессе восстановления благодаря сильному взаимодействию между адсорбированными ионами-предшественниками и поверхностью ГНП, которое позволяет получить наночастицы Pt со средним размером менее 1.5 нм и повысить коррозионную стойкость катализатора в целом (против коррозии носителя). Также авторами [122] предложен гибкий одноступенчатый метод нанесения наночастиц Pt на поверхность ВОГ путем плазмоструйной обработки раствора H2PtCl6. Полученный электрокатализатор продемонстрировал высокую активность в РВК как в кислых, так и в щелочных растворах [122].
Результаты [123, 124] показали, что ВОГ и оксид графита также могут быть использованы в качестве носителя электрокатализатора для высокотемпературных ТЭ с ТПЭ на основе полибензимидазольной мембраны.
При синтезе электрокатализаторов на основе ВОГ полиольным методом большое значение также имеют pH среды, прекурсор Pt, соотношение OH–/Pt, а также свойства исходного оксида графита. Наилучшего результата с точки зрения морфологии (размер частиц, равномерность их распределения по поверхности носителя и т.п.) удалось достичь при использовании H2PtCl6, лиофильно высушенного ОГ, приготовленного по методу Хаммерса с соотношением графит:окислитель – 1:6 и рН, равного 12 [125].
Оригинальный способ использования графена в качестве носителя молекулярных электрокатализаторов выделения водорода продемонстрирован в работах российских исследователей, проводимых, в том числе, в НИЦ “Курчатовский институт” [126]. Клатрохелатные комплексы Fe, Co и Ru могут адсорбироваться на развитой поверхности ВОГ, что позволяет существенно повысить эффективность и производительность катода электролизера воды с ТПЭ [127, 128]. Аналогичный подход может быть использован в случае молекулярных электрокатализаторов РВК и т.д. [129].
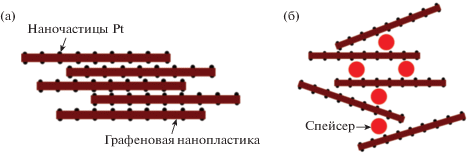
Удачным признано сочетание графена и традиционно используемой в качестве носителя элетрокатализаторов углеродной сажи [130, 131]. В [132] авторами разработан электрокатализатор на смешанном носителе на основе графена и сажи, в котором оптимальное содержание сажи составило 25%. Указанный электрокатализатор продемонстрировал существенное улучшение характеристик ТЭ при высокой плотности тока. Максимальная удельная мощность ТЭ составила 2.58 кВт/г Pt или 645 мВт/см2. Кроме того, показано, что интеркалирование сажи между листами ВОГ предотвращает сильное “сворачивание” и агломерацию нанолистов ВОГ [133]. В [117] авторы также предположили, что сферические частицы сажи будут выступать в качестве спейсеров между листами графена (рис. 30). Показано, что присутствие частиц сажи способствует эксфолиации графена, декорированного наночастицами Pt, а также способствуeт увеличению расстояния между листами ВОГ и повышению проницаемости каталитического слоя для реагентов. Оптимальное содержание сажи составило 25%. Площадь ЭАП за счет добавления сажи увеличилась примерно на 50%, хотя ее значение нельзя считать достаточно высоким (48 м2/г Pt для композитного носителя). В [134] показано, что использование сажи в качестве спейсера между наночешуйками ВОГ, допированного В, приводит к снижению как омического, так и поляризационного сопротивления мембранно-электродного блока. Аналогично добавление многостенных УНТ в электрокаталитический слой на основе электрокатализатора Pt/графен способствует лучшему транспорту реагентов и продуктов реакции (за счет изменения структуры пор), обеспечивает лучший электрический контакт между частицами катализатора и приводит к повышению степени использования Pt [135].
Рис. 30.
Условная схема электрокаталитического слоя, образованного с помощью электрокатализатора с ВОГ в качестве носителя без использования спейсера (а) и при использовании углеродной сажи в качестве спейсера между чешуйками ВОГ (б) [117].
В [136] показано, что противоположно заряженные листы Pt/ВОГ и УНТ самопроизвольно формируют структуру типа “сендвич”, т.е. находясь в растворе, отрицательно заряженные УНТ встраиваются между листами предварительно синтезированного положительно заряженного композита Pt/ВОГ. Углеродные нанотрубки, будучи зажатыми между листами Pt/ВОГ, способствуют массопереносу в электрокаталитическом слое ТЭ и препятствуют рестекингу Pt/ВОГ. После УСТ электрохимически активная поверхность катализатора Pt/ВОГ-УНТ(10) составила 61% от исходной, а ЭАП электрокатализаторов Pt/ВОГ и Pt/C упала до ∼20%.
Оригинальный подход продемонстрирован в [137–139], который заключается во введении в катод наряду с платиновым катализатором на носителе модифицированных кислородом УНВ. Авторы [137] полагают, что механизм влияния модифицированных кислородом УНТ на кинетику электровосстановления кислорода на платине заключается во включении хинон-гидрохинонного Red–Ox-перехода в процесс восстановления кислорода. Электрически связанные с платиной УНТ восстанавливают (за счет гидрохинонных групп) адсорбированный на ней кислород.
Как было указано выше, электрокатализаторы, в которых носителем являются наночешуйки графена или ВОГ, страдают от склонности к агломерации под действием ван-дер-ваальсовых сил [104]. В [135] пористая структура, образованная многостенными УНТ, действовала как в качестве среды для эффективного переноса реагентов и продуктов реакции, так и в качестве электронпроводящей сети.
В [140–142] показаны функциональные возможности использования терморасширенного графита в электродах химических источников тока. Показана эффективность использования терморасширенного графита в составе электрода для различных химических источников тока в качестве связующего вместо полимерных растворов и одновременно токопроводящего компонента. Добавление 1 мас. % ВОГ в состав композитной биполярной пластины позволяет повысить ее проводимость (как продольную, так и поперечную), также увеличить максимальную плотность мощности ТЭ с ТПЭ на 10% [143].
Восстановленный ОГ может выступать в роли функциональной добавки в электрокаталитический слой на основе традиционного платинового катализатора, что позволяет повысить эффективность работы ТЭ в области высоких плотностей тока [134, 144–146]. В этом случае нанолисты ВОГ в электрокаталитическом слое выступают в качестве спейсеров между агломератами частиц носителя Vulcan XC-72, покрытых наночастицами Pt [147]. При этом благодаря высокому аспектному числу (отношению длины к толщине) нанолистов ВОГ понижается перколяционный предел активного слоя по электронной проводимости, что подтверждается моделированием (метод Монте-Карло) и экспериментальными результатами. Показано, что использование в электрокаталитическом слое частиц, образующих агломераты большого размера (УНВ) (до 4 мкм), способствуeт снижению перколяционного предела по электронной проводимости слоя, позволяет повысить содержание иономера и облегчить массоперенос реагентов и продуктов реакции [147]. В силу пространственно-развитой структуры и высокой электропроводности ВОГ в структуре каталитического слоя формируется высокопроводящая сеть (матрица), что подтверждается результатами импедансометрических исследований [144]. Кроме того, увеличиваются пористость активного слоя и его проницаемость для реагентов (водорода и кислорода) и продукта электрохимической реакции (воды), что способствует не только некоторому снижению транспортных ограничений [134], но и повышению степени использования наночастиц Pt [136]. Согласно результатам [148, 149] терморасширенный графит может использоваться в качестве термостабилизирующей функциональной добавки, что позволит повысить рабочую температуру функционирования электродов ТЭ на основе протонпроводящего полимера Nafion с целью увеличения плотности рабочего тока, снижения загрузки платины и повышения их долговечности.
Восстановленный оксид графена обладает богатыми возможностями модификации свойств своей поверхности. Для придания ВОГ обратимых окислительно-восстановительных свойств существует несколько подходов. Одним из простых и очевидных методов является модифицирование поверхности за счет адсорбции органических молекул, заведомо обладающих обратимыми окислительно-восстановительными свойствами, подобно хинон-гидрохинонным циклам [150]. В некоторых случаях возможно закрепление таких органических молекул на поверхности графеновых частиц за счет прочных химических связей. Другим методом является функционализация ВОГ с приданием обратимых окислительно-восстановительных свойств непосредственно частицам самого ВОГ, где ансамбли кислородсодержащих функциональных групп приобретают способность к обратимым окислительно-восстановительным реакциям [151]. Кроме того, препаративные методы позволяют получать ВОГ с различной электропроводностью, гидрофильностью, донорно-акцепторными свойствами. Восстановленный оксид графена, допированный различными элементами (N, B, Р, S, O, F), представляется перспективным компонентом электрокатализаторов [152, 153] воздушно-водородных ТЭ и электролизеров, в частности, за счет существенного увеличения локальной плотности состояний ферми-энергии, что способствует переносу электрона с углерода графена на хемосорбированный кислород, облегчая процесс электровосстановления кислорода [154].
Ниже будет рассмотрено несколько примеров применения модифицированных графеновых материалов как в качестве носителей активных наночастиц Pt, так и в качестве электрокатализаторов РВК.
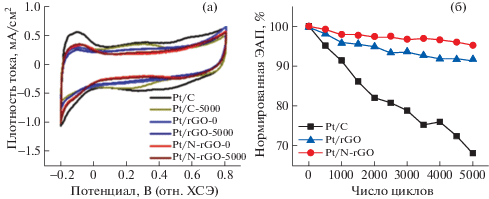
Зачастую промежуточным веществом при получении графена является ОГ (эксфолиированный оксид графита), поверхность которого содержит большое количество кислородсодержащих функциональных групп, в том числе эпоксидных, карбоксильных и гидроксильных, которые затем можно функционализировать на каждой стороне листа [155]. Например, в [156] во время процесса восстановления оксида графита до ВОГ одновременно проходило азотирование (модифицирование носителя азотом). Допированный азотом ОГ оказался более стойким носителем по сравнению с сажей Vulcan XC-72 (после УСТ электрокатализатор Pt/ВОГ-N потерял 60% ЭАП, тогда как Pt/Vulcan XC-72 – 96%). Электрокатализатор Pt/ВОГ-N, в котором наночастицы Pt наносились на поверхность ВОГ, допированного N (атомы N выступали в качестве “мостов” между Pt и носителем), продемонстрировал существенно более высокую удельную активность в реакции РВК по сравнению с коммерческим аналогом за счет взаимно усиливающего влияния наночастиц Pt и допированной гетероатомами матрицы ВОГ, а также за счет малого размера (2.8 нм) и структуры частиц Pt (111). Атомы азота обеспечивают транспорт электронов, что приводит к снижению сопротивления и предотвращает отрыв, растворение, миграцию и агрегацию наночастиц на поверхности ВОГ в ходе ускоренного стресс-тестирования (рис. 31) [157].
Рис. 31.
Результаты ускоренного стресс-тестирования электрокатализаторов Pt/N–rGO, Pt/rGO и Pt/C. Циклические вольтамперограммы электродов с Pt/N–rGO, Pt/rGO и Pt/C до и после стресс-тестирования в течение 5000 циклов в деаэриированном 0.1 М растворе HClO4 (а), сравнение величины ЭАП электрокатализаторов до и после стресс-тестирования (б) [157].
В [158] разработан высокоустойчивый электрокатализатор Pt/FeNGnPs, в котором наночастицы Pt закреплены на поверхности графеноподобных нанопластин, допированных N и Fe. Кроме повышения стабильности, функциональные группы Fe–N–C выступают в качестве дополнительных активных центров РВК, что позволяет снизить загрузку Pt.
В [159] предложен простой и экологичный метод допирования графена бором, а также показано, что именно модифицированный полиольный метод синтеза катализатора позволяет получить катализатор с высокой активностью и оптимальной морфологией. Также на ВОГ, допированном B, удалось синтезировать наночастицы Pt с практически нулевой степенью агломерации (рис. 32). Размер частиц лежит в диапазоне 9–16 нм для образца Pt-BG-3 с достаточно высоким содержанием Pt (4–4.7 ат. % Pt) [160].
Рис. 32.
Схема получения электрокатализатора Pt–BG (а), СЭМ- (б) и ПЭМ-изображения (в) электрокатализатора Pt-BG-3 (4–4.7 ат. % Pt) [160].

Относительно малоизученной является модификация кислородом углеродных материалов, таких как активированный уголь, углеродная сажа, УНВ, графит и графеноподобные материалы, с помощью обработки озоном [161–163] для управляемого формирования на их поверхности кислородосодержащих функциональных групп. Преимуществами такого метода перед, например, жидкофазным окислением или обработкой кислородной плазмой являются относительная простота конструкции установки, простой принцип действия и низкая стоимость. Кроме того, такой подход легко масштабируется для массового производства и может быть дополнен такими воздействиями, как повышение температуры процесса, добавка водяного пара или обработка ультрафиолетом [164] для повышения степени окисления. Согласно [165] обработка озоном графеноподобных материалов позволила повысить удельную поверхность расширенного графита и сформировать на его поверхности дополнительные функциональные группы, а соотношение O/C достигло 0.2 при проведении процесса при комнатной температуре. Озонирование при повышенных температурах (около 140°С) вызывает частичное разложение графита, сопровождающееся выделением СО и СО2. С другой стороны, согласно результатам [164] однослойные и многослойные графеноподобные пластинки, подвергнутые обработке озоном, претерпевают изменение своей структуры в сторону аморфного состояния. В [163] при озонировании нанолистов ВОГ при 80°С также удалось достичь значения O/C, равного 0.503, и на порядок увеличить число карбоксильных групп до более чем 14%. В [166] графит был предварительно окислен электрохимическим способом, эксфолиирован и далее использовался в качестве носителя наночастиц Pt. Полученный электрокатализатор продемонстрировал высокую активность в РВК как при исследованиях методом вращающегося дискового электрода, так и в мембранно-электродном блоке ТЭ. Методами рамановской и фотоэлектронной спектроскопии подтверждено наличие в графите дефектов и функциональных групп (C=O и OH) в результате электрохимической окислительной обработки. Результаты экспериментальных исследований [167, 168] показали, что обработка ВОГ озоном позволяет сформировать на его поверхности дополнительные кислородные функциональные группы, однако он окисляет наиболее химически активные участки поверхности, которые уже могут выступать в качестве центров зарождения наночастиц. Поэтому существенного роста числа центров зарождения частиц и соответствующего снижения размера наночастиц Pt (и роста ЭАП катализатора) не наблюдается. Модификация ВОГ фтором, напротив, привела к увеличению среднего размера наночастиц Pt и резкому снижению ЭАП электрокатализатора, что объясняется сильными акцепторными свойствами фтора и низкой доступностью поверхности фторированного носителя для сорбции прекурсора.
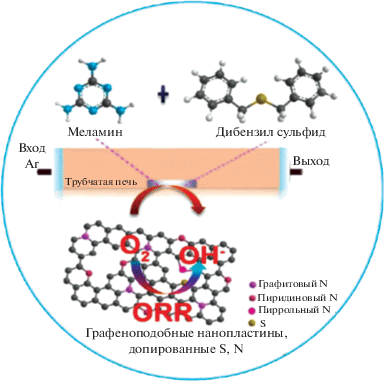
Углеродные материалы, допированные гетероатомами, сами по себе являются многообещающими неметаллическими электрокатализаторами, которые могут использоваться в приложениях по электрохимическому хранению и преобразованию энергии [169–172]. Механизм заключается в разнице между электроотрицательностью допирующих гетероатомов и атомов углерода самого носителя, что приводит к изменению распределения плотности атомного заряда/спиновой плотности на соседних атомах углерода, выступающих в роли активных центров РВК [173]. Такая большая разница в электроотрицательности атомов в матрице носителя также усиливает взаимодействие между металлическими наночастицами (например, Pt) и носителем, которое способствует повышению стабильности наночастиц. Например, в [174] показано, что электроды на основе ВОГ, допированном N, продемонстрировали высокую активность, стабильность и толерантность в РВК. Причем активность можно регулировать с помощью концентрации и конфигурации атомов N. Согласно последним исследованиям, за активность допированных азотом углеродных наноматериалов ответственны главным образом атомы N в пиридиновой и графитовой форме [175]. В [172] электрокатализатор в виде графеноподобных пластин, допированных атомами S и N (рис. 33), показал высокую активность в РВК по сравнению с монодопированными аналогами и существенно более высокую стабильность по сравнению с традиционным электрокатализатором РВК – Pt/C как в кислой, так и в щелочной среде. За высокую активность в РВК отвечает высокое содержание азота в графитовой и пиридиновой форме, однако атомы S позволяют вызывать поляризацию соседних атомов C и N, что приводит к растяжению и возникновению дефектов в углеродном каркасе, которые в конечном итоге способствуют хемосорбции кислорода [176].
Рис. 33.
Схема процедуры синтеза электрокатализатора РВК – графеноподобных пластин, допированных S, N [171].
Атомы P слишком велики, чтобы встроиться в плоскость графита и могут эффективно занимать лишь краевые дефекты. Активные центры P наиболее активны в случае неокисленного электрокатализатора и могут быть легко окислены кислородосодержащими частицами и теряют свою активность. Однако окисленный активный центр Р, связанный с N, стабилизирует графитовое состояние N и активирует соседний центр С в реакции выделения кислорода [170].
Неплатиновые электрокатализаторы, несмотря на достаточно высокие значения активности, достигаемые в лабораторных условиях, пока не продемонстрировали достаточно высокий доказанный ресурс работы в составе ТЭ, чтобы конкурировать с электрокатализаторами на основе Pt.
ЗАКЛЮЧЕНИЕ
Представленный обзор показывает, что открытие и изучение свойств графена и графеноподобных материалов (ОГ, ВОГ, УНТ, УНВ и др.), а также развитие доступных методов синтеза указанных материалов вызывают огромный интерес с целью их широкого применения в эффективных системах очистки и обратимого хранения водорода, а также в качестве носителей электрокатализаторов топливных элементов.
Результаты теоретических и экспериментальных исследований подтверждают возможность создания на основе графеновых материалов эффективных систем обратимого хранения водорода. Работы ведутся в нескольких направлениях. Показана возможность повышения сорбционной емкости и улучшения кинетики сорбции/десорбции водорода путем изменения кривизны поверхности графена, увеличения расстояния между слоями, создания каркасных 3D-систем на основе графена или ВОГ. Другое важное направление – функционализация графена гетероатомами (декорирование поверхности или допирование путем замещения атомов углерода). Атомы переходных металлов на поверхности графена действуют как каталитические центры диссоциативной хемосорбции водорода, что приводит к возникновению спилловер-эффекта, повышающего эффективность сорбции. Наиболее перспективно, видимо, совместное декорирование-допирование, особенно при допировании азотом и декорировании металлами Pt, Pd. Также вызывает интерес разработка композитов из наноструктурных гидридов, “завернутых” в графен. Например, композит из наночастиц 2LiBH4–MgH2, равномерно распределенных на гибких, но прочных графеновых подложках, имеет емкость 9.1 мас. % и хорошую стабильность при циклировании.
Разработка химически- и термостойких мембранных материалов на основе графена, обеспечивающих высокие проницаемость и селективность, может привести к значительному прогрессу в мембранных технологиях концентрирования водорода и очистки его от примесей. Основные направления работ – формирование нужных пор в плоскости графена, конструирование каналов в графеновых слоях (с использованием оксида графена), создание нанокомпозитных и гибридных мембран, состоящих из пластинок графена или оксида графена и неорганического мембранного материала. Для улучшения характеристик полимерных мембран, которые в основном используют в настоящее время в промышленности, предлагаются добавки графеновых материалов. Например, для полимерных мембран с добавками 0.2 мас. % ВОГ продемонстрирована исключительно высокая селективность H2/CH4. Новые мембраны перспективны для очистки водорода в процессах его получения из природного газа.
Применение ВОГ в качестве носителя для наночастиц Pt позволяет добиться улучшения транспортных характеристик электрокаталитического слоя ТЭ с ТПЭ, повышения его стабильности (как за счет более высокой стабильности носителя, так и за счет специфического взаимодействия между наночастицами и носителем), повышения активности электрокатализатора в РВК (что способствует снижению содержания Pt). Проблема “рестекинга” (агломерации) плоских (листовых) частиц графеноподобных материалов может быть решена путем внедрения (интеркаляции) функциональных добавок, например частиц сажи или нанотрубок между листовыми частицами ВОГ (в том числе с уже нанесенными наночастицами Pt), внедрением функциональных групп или нанесением на их поверхность металлических наночастиц, препятствующих агломерации под действием ван-дер-ваальсовых сил. Графеноподобные материалы сами могут выступать в роли функциональной добавки в электрокаталитический слой на основе традиционного катализатора, что позволяет повысить эффективность работы топливного элемента в области высоких плотностей тока за счет улучшения транспортных характеристик слоя (повышения пористости, ускорения диффузии кислорода и др.), повышения электропроводности и степени использования благородного металла. Допирование графеноподобных материалов гетероатомами (N, O, B, P, S) возможно различными методами в одну или несколько стадий и позволяет в той или иной степени влиять на электрокаталитические свойства самого ВОГ или наночастиц Pt на его поверхности, а также их морфологию. Плазменные методы модификации поверхности графеноподобных материалов являются одними из наиболее перспективных, так как они позволяют отказаться от использования высоких температур, растворителей и связанного с этими факторами загрязнения конечного продукта.
Исследование выполнено при финансовой поддержке Российского фонда фундаментальных исследований в рамках научного проекта № 18-53-53025.
Список литературы
Dresselhaus M.S., Araujo P.T. // ACS Nano. 2010. V. 4. № 11. P. 6297. https://doi.org/10.1021/nn1029789
Ivanovskii A.L. // Russ. Chem. Rev. 2012. V. 81. № 7. P. 571. https://doi.org/10.1070/RC2012v081n07ABEH004302
Губин С.П., Ткачев С.В. Графен и родственные наноформы углерода. М.: Книжный дом “ЛИБРИКОМ”, 2012. 104 с.
Алексеева О.К., Козлов С.И., Самсонов Р.О., Фатеев В.Н. // Транспорт на альтернативном топливе. 2009. № 4 (10). С. 68.
Алексеева О.К., Козлов С.И., Самсонов Р.О., Фатеев В.Н. // Транспорт на альтернативном топливе. 2009. № 5 (11). С. 72.
Фатеев В.Н., Алексеева О.К., Коробцев С.В. и др. // Chemical Problems. 2018. № 4 (16). С. 453.
Нечаев Ю.С., Алексеева О.К. // Успехи химии. 2004. Т. 73. С. 1308.
Nechaev Yu.S., Alexeeva O.K., Öchsner A. // J. Nanosci. Nanotechnol. 2009. V. 9. № 6. P. 3949. https://doi.org/10.1166/jnn.2009.NS95
Yu X., Tang Z., Sun D. et al. // Prog. Mater. Sci. 2017. V. 88. P. 1. https://doi.org/10.1016/j.pmatsci.2017.03.001
Stoller M.D., Park S., Zhu Y. et al. // Nano Lett. 2008. V. 8. № 10. P. 3498. https://doi.org/10.1021/nl802558y
Klechikov A., Mercier G., Sharifi T. et al. // Chem. Commun. 2015. V. 51. № 83. P. 15280. https://doi.org/10.1039/C5CC05474E
Bellucci L., Tozzini V. // Molecules. 2020. V. 25. № 2. P. 339. https://doi.org/10.3390/molecules25020339
Tozzini V., Pellegrini V. // Phys. Chem. Chem. Phys. 2013. V. 15. № 1. P. 80. https://doi.org/10.1039/C2CP42538F
Jain V., Kandasubramanian B. // J. Mater. Sci. 2019. V. 55. № 5. P. 1865. https://doi.org/10.1007/s10853-019-04150-y
Patchkovskii S., Tse J.S., Yurchenko S.N. et al. // Proc. Natl. Acad. Sci. 2005. V. 102. № 30. P. 10439. https://doi.org/10.1073/pnas.0501030102
Hudson M.S.L., Raghubanshi H., Awasthi S. et al. // Int. J. Hydrogen Energy. 2014. V. 39. № 16. P. 8311. https://doi.org/10.1016/j.ijhydene.2014.03.118
Boateng E., Chen A. // Mater. Today Adv. 2020. V. 6. P. 100022. https://doi.org/10.1016/j.mtadv.2019.100022
Subrahmanyam K.S., Vivekchand S.R.C., Govindaraj A., Rao C.N.R. // J. Mater. Chem. 2008. V. 18. № 13. P. 1517. https://doi.org/10.1039/b716536f
Chauhan P.K., Vidhukiran V., Sujith R., Parameshwaran R. // Mater. Res. Express. 2019. V. 6. P. 105617. https://doi.org/10.1088/2053-1591/ab3cdc
Голубева А.В., Черкез Д.И. // ВАНТ. Сер. Термоядерный синтез. 2018. Т. 41. № 4. С. 26. https://doi.org/10.21517/0202-3822-2018-41-4-26-37
Waqar Z. // J. Mater. Sci. 2007. V. 42. № 4. P. 1169. https://doi.org/10.1007/s10853-006-1453-1
Nechaev Y.S., Veziroglu T.N. // Adv. Mater. Phys. Chem. 2013. V. 3. № 5. P. 255. https://doi.org/10.4236/ampc.2013.35037
Slepchenkov M.M., Barkov P.V., Glukhova O.E. // Crystals. 2018. V. 8. № 4. P. 161. https://doi.org/10.3390/cryst8040161
Boddeti N.G., Koenig S.P., Long R. et al. // J. Appl. Mech. 2013. V. 80. № 4. P. 040909. https://doi.org/10.1115/1.4024255
Sluiter M.H.F., Kawazoe Y. // Phys. Rev. B. 2003. V. 68. № 8. P. 085410. https://doi.org/10.1103/PhysRevB.68.085410
Sofo J.O., Chaudhari A.S., Barber G.D. // Phys. Rev. B. 2007. V. 75. P. 153401. https://doi.org/10.1103/PhysRevB.75.153401
Elias D.C., Nair R.R., Mohiuddin T.M.G. et al. // Science. 2009. V. 323. № 5914. P. 610. https://doi.org/10.1126/science.1167130
Camiola V.D., Farchioni R., Cavallucci T. et al. // Front. Mater. 2015. V. 2. № 3. P. 1. https://doi.org/10.3389/fmats.2015.00003
Tozzini V., Pellegrini V. // J. Phys. Chem. C. 2011. V. 115. № 51. P. 25523. https://doi.org/10.1021/jp208262r
Goler S., Coletti C., Tozzini V. et al. // J. Phys. Chem. C. 2013. V. 117. № 22. P. 11506. https://doi.org/10.1021/jp4017536
Deng S., Berry V. // Mater. Today. 2016. V. 19. № 4. P. 197. https://doi.org/10.1016/j.mattod.2015.10.002
McKay H., Wales D.J., Jenkins S.J. et al. // Phys. Rev. B. 2010. V. 81. № 7. P. 075425. https://doi.org/10.1103/PhysRevB.81.075425
Sun P.Z., Yang Q., Kuang W.J. et al. // Nature. 2020. V. 579. № 7798. P. 229. https://doi.org/10.1038/s41586-020-2070-x
Baburin I.A., Klechikov A., Mercier G. et al. // Int. J. Hydrogen Energy. 2015. V. 40. № 20. P. 6594. https://doi.org/10.1016/j.ijhydene.2015.03.139
Pedrielli A., Taioli S., Garberoglio G., Pugno N.M. // Microporous Mesoporous Mater. 2018. V. 257. P. 222. https://doi.org/10.1016/j.micromeso.2017.08.034
Dimitrakakis G.K., Tylianakis E., Froudakis G.E. // Nano Lett. 2008. V. 8. № 10. P. 3166. https://doi.org/10.1021/nl801417w
Klontzas E., Tylianakis E., Varshney V. et al. // Sci. Rep. 2019. V. 9. № 1. P. 13676. https://doi.org/10.1038/s41598-019-50037-y
Wu X., Zeng X.C. // Nano Lett. 2009. V. 9. № 1. P. 250. https://doi.org/10.1021/nl802832m
Xia K., Zhan H., Gu Y. // Procedia IUTAM. 2017. V. 21. P. 94. https://doi.org/10.1016/j.piutam.2017.03.042
Shiraz H.G., Tavakoli O. // Renew. Sustain. Energy Rev. 2017. V. 74. P. 104. https://doi.org/10.1016/j.rser.2017.02.052
Bonaccorso F., Colombo L., Yu G. et al. // Science. 2015. V. 347. № 6217. P. 1246501. https://doi.org/10.1126/science.1246501
Mohan M., Sharma V.K., Kumar E.A., Gayathri V. // Energy Storage. 2019. V. 1. № 2. P. 35. https://doi.org/10.1002/est2.35
Spyrou K., Gournis D., Rudolf P. // ECS J. Solid State Sci. Technol. 2013. V. 2. № 10. P. M3160. https://doi.org/10.1149/2.018310jss
Zhou X.F., Fang H.Y., Tang C.M. // Acta Phys. Sin. 2019. V. 68. № 5. P. 053601. https://doi.org/10.7498/aps.68.20181497
Tachikawa H., Iyama T. // J. Phys. Chem. C. 2019. V. 123. № 14. P. 8709. https://doi.org/10.1021/acs.jpcc.9b01152
Huang C.-C., Pu N.-W., Wang C.-A. et al. // Sep. Purif. Technol. 2011. V. 82. P. 210. https://doi.org/10.1016/j.seppur.2011.09.020
Lamichhane S., Pantha N., Adhikari N. // Bibechana. 2014. V. 11. № 1. P. 113. https://doi.org/10.3126/bibechana.v11i0.10389
Ariharan A., Viswanathan B., Nandhakumar V. // Graphene. 2017. V. 6. № 2. P. 41. https://doi.org/10.4236/graphene.2017.62004
Ariharan A., Viswanathan B., Nandhakumar V. // Graphene. 2016. V. 5. № 2. P. 39. https://doi.org/10.4236/graphene.2016.52005
Gueye E.H.O., Dione A.N., Dioum A. et al. // Am. J. Nanomaterials. 2019. V. 7. № 1. P. 30. https://doi.org/10.12691/ajn-7-1-4
Vinayan B.P., Sethupathi K., Ramaprabhu S. // J. Nanosci. Nanotechnol. 2012. V. 12. № 8. P. 6608. https://doi.org/10.1166/jnn.2012.4539
Nechaev Y.S., Filippova V.P., Tomchuk A.A. et al. // Nanosyst. Physics, Chem. Math. 2016. V. 7. № 1. P. 204. https://doi.org/10.17586/2220-8054-2016-7-1-204-209
Lee H., Ihm J., Cohen M.L., Louie S.G. // Nano Lett. 2010. V. 10. № 3. P. 793. https://doi.org/10.1021/nl902822s
Divya P., Ramaprabhu S. // Phys. Chem. Chem. Phys. 2014. V. 16. № 48. P. 26725. https://doi.org/10.1039/C4CP04214J
Zhou C., Szpunar J.A. // ACS Appl. Mater. Interfaces. 2016. V. 8. № 39. P. 25933. https://doi.org/10.1021/acsami.6b07122
Wang H., Maiyalagan T., Wang X. // ACS Catal. 2012. V. 2. № 5. P. 781. https://doi.org/10.1021/cs200652y
Scardamaglia M., Bittencourt C. // Beilstein J. Nanotechnol. 2018. V. 9. P. 2015. https://doi.org/10.3762/bjnano.9.191
Paul R., Dai Q., Hu C., Dai L. // Carbon Energy. 2019. V. 1. № 1. P. 19. https://doi.org/10.1002/cey2.5
Gao K., Wang B., Tao L. et al. // Adv. Mater. 2019. V. 31. № 13. P. 1805121. https://doi.org/10.1002/adma.201805121
Пушкарев А.С., Алексеева О.К., Пушкарева И.В. и др. // Российские нанотехнологии. 2020. Т. 15. В печати.
Xia G., Tan Y., Wu F. et al. // Nano Energy. 2016. V. 26. P. 488. https://doi.org/10.1016/j.nanoen.2016.06.016
Козлов С.И., Фатеев В.Н. Водородная энергетика: современное состояние, проблемы, перспективы. М.: Газпром ВНИИГАЗ, 2009. 518 с.
Миронова Е.Ю., Ермилова М.М., Орехова Н.В. и др. // Российские нанотехнологии. 2017. Т. 12. № 11–12. С. 23.
Ockwig N.W., Nenoff T.M. // Chem. Rev. 2007. V. 107. № 10. P. 4078. https://doi.org/10.1021/cr0501792
Chen X.Y., Tien-Binh N., Romero A. et al. // J. Membr. Sci. Res. 2020. V. 6. № 1. P. 58. https://doi.org/10.22079/JMSR.2019.100069.1244
Alen S.K., Nam S., Dastgheib S.A. // Int. J. Mol. Sci. 2019. V. 20. № 22. P. 5609. https://doi.org/10.3390/ijms20225609
Yoon H.W., Cho Y.H., Park H.B. // Philos. Trans. R. Soc. A. 2016. V. 374. P. 20150024. https://doi.org/10.1098/rsta.2015.0024
Алексеева О.К., Амирханов Д.М. // Рос. хим. журн. 2004. Т. XLVIII. № 5. С. 82.
Амирханов Д.М., Алексеева О.К., Котенко А.А. и др. // Мембраны. 2006. № 4 (32). С. 19.
Алексеева О.К., Котенко А.А., Челяк М.М. // Мембраны. 2007. № 4 (36). С. 3.
Alexeeva O.K., Nechaev Y.S., Shapir B.L., Öchsner A. // Int. Sci. J. Altern. Energy Ecol. 2009. № 1 (69). P. 131.
Shen J., Zhang M., Liu G. et al. // AIChE J. 2016. V. 62. № 8. P. 2843. https://doi.org/10.1002/aic.15260
Kang Z., Wang S., Fan L. et al. // Commun. Chem. 2018. V. 1. № 1. P. 3. https://doi.org/10.1038/s42004-017-0002-y
Hyun T., Jeong J., Chae A. et al. // BMC Chem. Eng. 2019. V. 1. № 1. P. 12. https://doi.org/10.1186/s42480-019-0012-x
Kim S., Wang H., Lee Y.M. // Angew. Chemie Int. Ed. 2019. V. 58. № 49. P. 17512. https://doi.org/10.1002/anie.201814349
Hamid M.R.A., Jeong H.-K. // Korean J. Chem. Eng. 2018. V. 35. № 8. P. 1577. https://doi.org/10.1007/s11814-018-0081-1
Sun C., Zheng X., Bai B. // Chem. Eng. Sci. 2019. V. 208. P. 115141. https://doi.org/10.1016/j.ces.2019.07.059
Алексеева О.К. // Вода magazine. 2014. № 6 (82). С. 30.
Huang L., Lin H. // Membranes. 2018. V. 8. № 4. P. 100. https://doi.org/10.3390/membranes8040100
O’Hern S.C., Boutilier M.S.H., Idrobo J.-C. et al. // Nano Lett. 2014. V. 14. № 3. P. 1234. https://doi.org/10.1021/nl404118f
Celebi K., Buchheim J., Wyss R.M. et al. // Science. 2014. V. 344. № 6181. P. 289. https://doi.org/10.1126/science.1249097
Gilboa T., Zrehen A., Girsault A., Meller A. // Sci. Rep. 2018. V. 8. № 1. P. 9765. https://doi.org/10.1038/s41598-018-28136-z
Huang S., Dakhchoune M., Luo W. et al. // Nat. Commun. 2018. V. 9. № 1. P. 2632. https://doi.org/10.1038/s41467-018-04904-3
Zhao J., He G., Huang S. et al. // Sci. Adv. 2019. V. 5. № 1. P. 1851. https://doi.org/10.1126/sciadv.aav1851
Wei S., Zhou S., Wu Z. et al. // Appl. Surf. Sci. 2018. V. 441. P. 631. https://doi.org/10.1016/j.apsusc.2018.02.111
Kim H.W., Yoon H.W., Yoon S.-M. et al. // Science. 2013. V. 342. № 6154. P. 91. https://doi.org/10.1126/science.1236098
Bouša D., Friess K., Pilnáček K. et al. // Chem. - A Eur. J. 2017. V. 23. № 47. P. 11416. https://doi.org/10.1002/chem.201702233
Zheng H., Zhu L., He D. et al. // Int. J. Hydrogen Energy. 2017. V. 42. № 52. P. 30653. https://doi.org/10.1016/j.ijhydene.2017.10.134
Ibrahim A., Lin Y.S. // J. Membr. Sci. 2018. V. 550. P. 238. https://doi.org/10.1016/j.memsci.2017.12.081
Ibrahim A.F.M., Lin Y.S. // Chem. Eng. Sci. 2018. V. 190. P. 312. https://doi.org/10.1016/j.ces.2018.06.031
Lyu J., Wen X., Kumar U. et al. // RSC Adv. 2018. V. 8. № 41. P. 23130. https://doi.org/10.1039/C8RA03156H
Ibrahim A.F.M., Banihashemi F., Lin Y.S. // Chem. Commun. 2019. V. 55. № 21. P. 3077. https://doi.org/10.1039/C8CC10283J
Liu Q., Gupta K.M., Xu Q. et al. // Sep. Purif. Technol. 2019. V. 209. P. 419. https://doi.org/10.1016/j.seppur.2018.07.044
Zeynali R., Ghasemzadeh K., Sarand A.B. et al. // Catal. Today. 2019. V. 330. P. 16. https://doi.org/10.1016/j.cattod.2018.05.047
Ostwal M., Shinde D.B., Wang X. et al. // J. Memb. Sci. 2018. V. 550. P. 145. https://doi.org/10.1016/j.memsci.2017.12.063
Palmieri V., Papi M. // Nano Today. 2020. V. 33. P. 100883. https://doi.org/10.1016/j.nantod.2020.100883
Zhong H., Zhu Z., Lin J. et al. // ACS Nano. 2020. V. 14. № 5. P. 6213. https://doi.org/10.1021/acsnano.0c02250
Daud W.R.W., Rosli R.E., Majlan E.H. et al. // Renew. Energy. 2017. V. 113. P. 620. https://doi.org/10.1016/j.renene.2017.06.027
Bodner M., Senn J., Hacker V. Fuel Cells and Hydrogen: From Fundamentals to Applied Research. Amsterdam: Elsevier, 2018. 267 p. https://doi.org/10.1016/B978-0-12-811459-9.00007-4
Dai L., Chang D.W., Baek J.B., Lu W. // Small. 2012. V. 8. № 8. P. 1130. https://doi.org/10.1002/smll.201101594
Trogadas P., Fuller T.F., Strasser P. // Carbon N. Y. 2014. V. 75. P. 5. https://doi.org/10.1016/j.carbon.2014.04.005
Sharma S., Pollet B.G. // J. Power Sources. 2012. V. 208. P. 96. https://doi.org/10.1016/j.jpowsour.2012.02.011
Antolini E. // Appl. Catal. B. 2009. V. 88. № 1–2. P. 1. https://doi.org/10.1016/j.apcatb.2008.09.030
Antolini E. // Appl. Catal. B. 2012. V. 123–124. P. 52. https://doi.org/10.1016/j.apcatb.2012.04.022
Liu M., Zhang R., Chen W. // Chem. Rev. 2014. V. 114. № 10. P. 5117. https://doi.org/10.1021/cr400523y
Du L., Shao Y., Sun J. et al. // Nano Energy. 2016. V. 29. P. 314. https://doi.org/10.1016/j.nanoen.2016.03.016
Pandey R.P., Shukla G., Manohar M., Shahi V.K. // Adv. Colloid Interface Sci. 2017. V. 240. P. 15. https://doi.org/10.1016/j.cis.2016.12.003
Sui S., Wang X., Zhou X. et al. // J. Mater. Chem. A. 2017. V. 5. № 5. P. 1808. https://doi.org/10.1039/C6TA08580F
Li Y., Tang L., Li J. // Electrochem. Commun. 2009. V. 11. № 4. P. 846. https://doi.org/10.1016/j.elecom.2009.02.009
Hsieh S.H., Hsu M.C., Liu W.L., Chen W.J. // Appl. Surf. Sci. 2013. V. 277. P. 223. https://doi.org/10.1016/j.apsusc.2013.04.029
Xin Y., Liu J., Zhou Y. et al. // J. Power Sources. 2011. V. 196. № 3. P. 1012. https://doi.org/10.1016/j.jpowsour.2010.08.051
Liang Y., Wu D., Feng X., Müllen K. // Adv. Mater. 2009. V. 21. № 17. P. 1679. https://doi.org/10.1002/adma.200803160
Wang H., Du J., Yao Z. et al. // Colloids Surf. A. 2013. V. 436. P. 57. https://doi.org/10.1016/j.colsurfa.2013.06.020
Yao Z., Zhu M., Jiang F. et al. // J. Mater. Chem. 2012. V. 22. № 27. P. 13707. https://doi.org/10.1039/c2jm31683h
Yao Z., Yue R., Zhai C. et al. // Int. J. Hydrogen Energy. 2013. V. 38. № 15. P. 6368. https://doi.org/10.1016/j.ijhydene.2013.02.140
Lei M., Liang C., Wang Y.J. et al. // Electrochim. Acta. 2013. V. 113. P. 366. https://doi.org/10.1016/j.electacta.2013.09.119
Park S., Shao Y., Wan H. et al. // Electrochem. Commun. 2011. V. 13. № 3. P. 258. https://doi.org/10.1016/j.elecom.2010.12.028
Cheng K., He D., Peng T. et al. // Electrochim. Acta. 2014. V. 132. P. 356. https://doi.org/10.1016/j.electacta.2014.03.181
Baranov I.E., Porembskii V.I., Lyutikova E.K. et al. // Chemical Problems. 2019. № 4 (17). P. 489. https://doi.org/10.32737/2221-8688-2019-4-489-499
Şanli L.I., Bayram V., Yarar B. et al. // Int. J. Hydrogen Energy. 2016. V. 41. № 5. P. 3414. https://doi.org/10.1016/j.ijhydene.2015.12.166
Daş E., Alkan Gürsel S., Işikel Şanli L., Bayrakçe-ken Yurtcan A. // Int. J. Hydrogen Energy. 2016. V. 41. № 23. P. 9755. https://doi.org/10.1016/j.ijhydene.2016.01.111
Hussain S., Erikson H., Kongi N. et al. // ChemElectroChem. 2018. V. 5. № 19. P. 2902. https://doi.org/10.1002/celc.201800582
Devrim Y., Arıca E.D., Albostan A. // Int. J. Hydrogen Energy. 2018. V. 43. № 26. P. 11820. https://doi.org/10.1016/j.ijhydene.2018.03.047
Alpaydin G.U., Devrim Y., Colpan C.O. // Int. J. Energy Res. 2019. V. 43. № 8. P. 3578. https://doi.org/10.1002/er.4504
Pak Hoe L., Boaventura M., Lagarteira T. et al. // Int. J. Hydrogen Energy. 2018. V. 43. № 35. P. 16998. https://doi.org/10.1016/j.ijhydene.2018.05.147
Pushkarev A.S., Solovyev M.A., Grigoriev S.A. et al. // Int. J. Hydrogen Energy. 2020. https://doi.org/10.1016/j.ijhydene.2020.02.098
Voloshin Y.Z., Chornenka N.V., Varzatskii O.A. et al. // Electrochim. Acta. 2018. V. 269. P. 590. https://doi.org/10.1016/j.electacta.2018.03.030
Voloshin Y.Z., Chornenka N.V., Belov A.S. et al. // J. Electrochem. Soc. 2019. V. 166. № 13. P. H598. https://doi.org/10.1149/2.0391913jes
Dey S., Mondal B., Chatterjee S. et al. // Nat. Rev. Chem. 2017. V. 1. № 12. P. 0098. https://doi.org/10.1038/s41570-017-0098
Şanlı L.I., Yarar B., Bayram V., Gürsel S.A. // J. Mater. Sci. 2017. V. 52. № 4. P. 2091. https://doi.org/10.1007/s10853-016-0497-0
Yılmaz M.S., Kaplan B.Y., Metin Ö., Gürsel S.A. // Mater. Des. 2018. V. 151. P. 29. https://doi.org/10.1016/j.matdes.2018.04.041
Şanlı L.I., Bayram V., Ghobadi S. et al. // Int. J. Hydrogen Energy. 2017. V. 42. № 2. P. 1085. https://doi.org/10.1016/j.ijhydene.2016.08.210
Yurtcan A.B., Daş E. // Int. J. Hydrogen Energy. 2018. V. 43. № 40. P. 18691. https://doi.org/10.1016/j.ijhydene.2018.06.186
Yang H.N., Lee D.C., Park K.W., Kim W.J. // Energy. 2015. V. 89. P. 500. https://doi.org/10.1016/j.energy.2015.06.019
Yun Y.S., Kim D., Tak Y., Jin H.-J. // Synth. Met. 2011. V. 161. № 21–22. P. 2460. https://doi.org/10.1016/j.synthmet.2011.09.030
Liu Z., Abdelhafiz A.A., Jiang Y. et al. // Mater. Chem. Phys. 2019. V. 225. P. 371. https://doi.org/10.1016/j.matchemphys.2018.12.100
Глебова Н.В., Нечитайлов А.А., Гурин В.Н. // Письма в ЖТФ. 2011. Т. 37. С. 32.
Нечитайлов А.А., Глебова Н.В., Кошкина Д.В. и др. // Письма в ЖТФ. 2013. Т. 39. С. 15.
Нечитайлов А.А., Глебова Н.В. // Электрохимия. 2014. Т. 50. С. 835.
Lee J.Y., Lee J.J., Rhim H.R. et al. // Adv. Mater. Res. 2010. V. 123–125. P. 1107. https://doi.org/110.4028/www.scientific.net/AMR.123-125.1107
Финаенов А.И., Шпак И.Е., Афонина А.В. и др. // Вестн. СГТУ. 2012. № 4 (68). С. 107.
Яковлев А.В., Финаенов А.И., Забудьков С.Л., Яковлева Е.В. // Журн. прикл. химии. 2006. Т. 79. С. 1761.
Kakati B.K., Ghosh A., Verma A. // Int. J. Hydrogen Energy. 2013. V. 38. № 22. P. 9362. https://doi.org/10.1016/j.ijhydene.2012.11.075
Sung C.-C., Liu C.-Y., Cheng C.C.J. // Int. J. Hydrogen Energy. 2014. V. 39. № 22. P. 11706. https://doi.org/10.1016/j.ijhydene.2014.05.154
Pushkarev A.S., Pushkareva I.V., Grigoriev S.A. et al. // Int. J. Hydrogen Energy. 2015. V. 40. № 42. P. 14492. https://doi.org/10.1016/j.ijhydene.2015.05.093
Григорьев С.А., Пушкарев А.С., Калиниченко В.Н. и др. // Кинетика и катализ. 2015. Т. 56. № 5. С. 698.
Baranov I.E., Nikolaev I.I., Pushkarev A.S. et al. // Int. J. Electrochem. Sci. 2018. V. 13. P. 8673. https://doi.org/10.20964/2018.09.48
Глебова Н.В., Краснова А.О., Нечитайлов А.А. // Журн. прикл. химии. 2018. Т. 91. № 8. С. 1111.
Краснова А.О., Глебова Н.В., Жилина Д.В., Нечитайлов А.А. // Журн. прикл. химии. 2017. Т. 90. № 3. С. 299. https://doi.org/10.1134/S1070427217030065
Игнатова А.А., Ярмоленко О.В. // Международный научный журнал “Альтернативная энергетика и экология”. 2015. Т. 172–173. № 8–9. С. 112. https://doi.org/10.15518/isjaee.2015.08-09.014
Dreyer D.R., Park S., Bielawski C.W., Ruoff R.S. // Chem. Soc. Rev. 2010. V. 39. № 1. P. 228. https://doi.org/10.1039/B917103G
Wang X., Sun G., Routh P. et al. // Chem. Soc. Rev. 2014. V. 43. № 20. P. 7067. https://doi.org/10.1039/C4CS00141A
Vikkisk M., Kruusenberg I., Joost U. et al. // Appl. Catal. B. 2014. V. 147. P. 369. https://doi.org/10.1016/j.apcatb.2013.09.011
Maiti U.N., Lee W.J., Lee J.M. et al. // Adv. Mater. 2014. V. 26. № 1. P. 40. https://doi.org/10.1002/adma.201303265
Martínez-Huerta M.V., Lázaro M.J. // Catal. Today. 2017. V. 285. P. 3. https://doi.org/10.1016/j.cattod.2017.02.015
Heydari A., Gharibi H. // J. Power Sources. 2016. V. 325. P. 808. https://doi.org/10.1016/j.jpowsour.2016.06.039
Li Z., Gao Q., Zhang H. et al. // Sci. Rep. 2017. V. 7. № 1. P. 43352. https://doi.org/10.1038/srep43352
Kim J., Kim C., Jeon I.-Y. et al. // ChemElectroChem. 2018. V. 5. № 19. P. 2857. https://doi.org/10.1002/celc.201800674
Pullamsetty A., Subbiah M., Sundara R. // Int. J. Hydrogen Energy. 2015. V. 40. № 32. P. 10251. https://doi.org/10.1016/j.ijhydene.2015.06.020
Lim D., Shim Y., Oh J. et al. // J. Solid State Chem. 2019. V. 271. P. 168. https://doi.org/10.1016/j.jssc.2018.12.058
Razumovskii S.D., Gorshenev V.N., Kovarskii A.L. et al. // Fullerenes, Nanotub. Carbon Nanostructures. 2007. V. 15. № 1. P. 53. https://doi.org/10.1080/15363830600812423
Álvarez P.M., García-Araya J.F., Beltrán F.J. et al. // J. Colloid Interface Sci. 2005. V. 283. № 2. P. 503. https://doi.org/10.1016/j.jcis.2004.09.014
Xu Z., Yue M., Chen L. et al. // Chem. Eng. J. 2014. V. 240. P. 187. https://doi.org/10.1016/j.cej.2013.11.045
Tao H., Moser J., Alzina F. et al. // J. Phys. Chem. C. 2011. V. 115. № 37. P. 18257. https://doi.org/10.1021/jp2050756
Krawczyk P. // Chem. Eng. J. 2011. V. 172. № 2–3. P. 1096. https://doi.org/10.1016/j.cej.2011.06.005
Teran-Salgado E., Bahena-Uribe D., Márquez-Aguilar P.A. et al. // Electrochim. Acta. 2019. V. 298. P. 172. https://doi.org/10.1016/j.electacta.2018.12.057
Grigoriev S.A., Fateev V.N., Pushkarev A.S. et al. // Materials. 2018. V. 11. P. 1405. https://doi.org/10.3390/ma11081405
Пушкарева И.В. Дис. “Разработка и исследование электрокаталитических материалов для топливных элементов с твердым полимерным электролитом” … канд. тех. наук. М.: МЭИ, 2019.
Gaidukevič J., Razumienė J., Šakinytė I. et al. // Carbon N. Y. 2017. V. 118. P. 156. https://doi.org/10.1016/j.carbon.2017.03.049
Chai G.-L., Qiu K., Qiao M. et al. // Energy Environ. Sci. 2017. V. 10. № 5. P. 1186. https://doi.org/10.1039/C6EE03446B
Zhang J., Wang J., Wu Z. et al. // Catalysts. 2018. V. 8. № 10. P. 475. https://doi.org/10.3390/catal8100475
Li J., Zhang Y., Zhang X. et al. // ACS Appl. Mater. Interfaces. 2017. V. 9. № 1. P. 398. https://doi.org/10.1021/acsami.6b12547
Gong K., Du F., Xia Z. et al. // Science. 2009. V. 323. № 5915. P. 760. https://doi.org/10.1126/science.1168049
Wu J., Ma L., Yadav R.M. et al. // ACS Appl. Mater. Interfaces. 2015. V. 7. № 27. P. 14763. https://doi.org/10.1021/acsami.5b02902
Wu Z., Song M., Wang J., Liu X. // Catalysts. 2018. V. 8. № 5. P. 196. https://doi.org/10.3390/catal8050196
Wang D.-W., Su D. // Energy Environ. Sci. 2014. V. 7. № 2. P. 576. https://doi.org/10.1039/c3ee43463j
Дополнительные материалы отсутствуют.
Инструменты
Российские нанотехнологии