Нефтехимия, 2019, T. 59, № 3, стр. 357-364
Исследование состава жидких продуктов каталитического гидроожижения сапропелей
Е. Н. Терехова 1, *, О. Б. Бельская 1
1 Институт проблем переработки углеводородов СО РАН
Омск, Россия
* E-mail: m.lena.n@mail.ru
Поступила в редакцию 29.08.2018
После доработки 27.10.2018
Принята к публикации 10.12.2018
Аннотация
Исследован состав жидких продуктов, полученных при каталитическом гидроожижении сапропеля. В качестве методики анализа предложена комбинация известных на сегодняшний день методик анализа нефтепродуктов с учетом особенностей исходного сырья (сапропеля). Установлены закономерности, связывающие состав жидких продуктов с природой растворителя (декалин, этанол) и катализатора (CoMo/Al2O3, FeNi/Al2O3). Показано, что при использовании этанола в качестве растворителя, в составе жидких продуктов преобладают карбоиды и асфальтены, а при применении декалина наблюдается увеличение содержания парафинов и кислородсодержащих соединений.
Сапропели – донные органические отложения, состоящие из отмершей водной растительности и остатков живых организмов, планктона. Сапропель широко распространен на Земле и является возобновляемым природным органическим сырьем. Следует отличать сапропель от торфа и ила, которые находятся в водоемах со стоячей водой или болотах. Особенностью сапропеля является более низкое содержание органического вещества [1, 2]. Количество и состав минеральных компонентов сапропелей зависит от условий образования, химического состава питающих водоемы вод и эрозийных процессов.
Нативный сапропель широко применяется в сельском хозяйстве и ветеринарии, а также как сырье в химической промышленности, при производстве сорбентов для очистки вод, почв и грунтов от нефтепродуктов, для получения аммиака, воска, парафина [3].
Среди технологических направлений переработки сапропелей традиционными являются термические и термохимические методы [4, 5]. Кроме того, в настоящее время актуальным направлением является поиск нового энергетического сырья и вовлечение в глубокую переработку альтернативных источников органического сырья (уголь, горючие сланцы, биомасса) с целью получения искусственного жидкого топлива (так называемой бионефти) и сырья для химической промышленности [6], в связи с чем ресурсы сапропелей заслуживают особого внимания.
Для превращения органической массы в продукты топливного назначения применяется процесс каталитического гидроожижения, сопровождающийся реакциями гидрирования, гидрогенолиза, изомеризации [4]. В настоящее время основным сырьем для данного процесса являются бурые угли [7, 8], для которых хорошо изучены условия и параметры гидроожижения. Хотя химический состав сапропелей незначительно отличается от состава бурых углей, в качестве сырья его используют реже [9–11]. Так, в работе [11] изучено термическое растворение в этаноле сапропелей различных озер Новосибирской области. Показано влияние температуры на конверсию органического вещества, жидкие продукты изучены методом хромато-мас-спектрометрии (ХМС).
Ряд экспериментов по каталитическому гидроожижению сапропелей был ранее проведен сотрудниками нашего института [4]. Для проведения процесса использовали сапропели с различным содержанием органического вещества, в качестве растворителя применяли декалин. Установлено, что наибольшее влияние на протекание процесса оказывает температура: максимальная конверсия органического вещества (ОВ) достигается при 450°С, однако выход жидких продуктов (ЖП) выше при 370–400°С. Определены технологические параметры, обеспечивающие максимальный выход ЖП и максимальную степень превращения органической массы сапропеля.
Сложный состав продуктов, образующихся при гидроожижении сапропелей, обусловлен природой исходного сырья и представляет определенные трудности при анализе. В отличие от ЖП, полученных при гидроожижении бурых углей, в составе продуктов гидроожижения сапропелей содержится значительное количество кислород- и азотсодержащих соединений, нафталины [4]. Это приводит к тому, что, несмотря на наличие работ по гидроожижению сапропелей, состав ЖП до конца не изучен. Однако известно, что физико-химические свойства (фракционный и групповой состав и т.д.) жидких продуктов растворения сапропеля определяются химическими свойствами применяемого растворителя, что дает возможность путем подбора соответствующего растворителя и условий растворения получить из сапропеля жидкие продукты с различными выходом и составом [12].
Следует отметить, что методы анализа продуктов термохимической переработки сапропелей имеют много общего с соответствующими методами анализа ЖП термической переработки бурых углей, а также сланцевых смол, нефтей и нефтепродуктов. В настоящее время использование физико-химических методов разделения сложных смесей совместно с применением современных методов анализа сделало возможным не только достоверное определение групповых компонентов природного органического сырья и продуктов его переработки, но и идентификацию значительного количества составляющих его соединений. Однако вопрос остается не разрешенным, особенно в приложении к сложным смесям высококипящих органических веществ.
В связи с этим целью данной работы являлось исследование состава жидких продуктов гидроожижения сапропеля и установление связи состава жидких продуктов с природой растворителя и применяемой каталитической системой.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве объекта анализа использовали сапропель озера Жилой Рям Омской области. Выбор данного сапропеля определяется доступностью для добычи, большим запасом ископаемого, высоким содержанием органического вещества (ОВ). Исходный сапропель относится к органо-кремнеземистому типу; содержание золы 30.93%, содержание органического вещества 69.07%.
Процесс гидроожижения сапропеля проводили на установке, показанной на рис. 1 при давлении водорода 6 МПа в течение 60 мин. Условия проведения эксперимента были подобраны нами ранее [4].
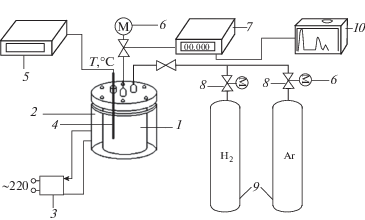
Рис. 1.
Установка для гидроожижения сапропеля: 1 – реактор, 2 – электронагреватель, 3 – регулируемый источник питания, 4 – термопара, 5 – регистратор температуры, 6 – регистратор давления, 7 – газовый счетчик, 8– игольчатый вентиль, 9 – баллоны с газом, 10 – газовый хроматограф.
В качестве растворителя использовали неполярный растворитель декалин и полярный - этанол. Декалин является модельным представителем протонододонорных растворителей, обладающим высокой растворяющей способностью по отношению к ароматическим и циклическим углеводородам [13]. Температуру проведения процесса поддерживали равной 350оС, согласно работе [4]. Этанол также является хорошим растворителем большинства продуктов термических превращений, легко отделяется от них и широко доступен [14]. При использовании этанола процесс проводили при температуре 200°С, как было предложено авторами [11].
В реактор объемом 0.16 дм3 загружали образец сапропеля и растворитель в массовом отношении 1 : 1, содержание катализатора составляло 5 мас. % от сухого сапропеля. Далее систему продували инертным газом (Аr) в течение 5 мин при расходе 0.5 л/ч и опрессовывали инертным газом при давлении 6 МПа в течение 10 мин. Затем подавали водород при заданном давлении, реактор помещали в печь, разогревали до заданной температуры со скоростью 2 град/мин и выдерживали при рабочей температуре необходимое время. После этого реактор охлаждали, продукты выгружали с последующим отделением жидкой фазы от твердого остатка фильтрованием через воронку Бюхнера, а затем отгоняли растворитель под вакуумом. Определение количества и состава газообразных продуктов в данной работе не проводилось.
В качестве катализаторов применяли CoMo/ Al2O3 и FeNi/Al2O3. Перед началом реакции образцы катализаторов подвергали восстановлению в токе водорода при 650°С в течение 5 ч, либо предварительно сульфидировали смесью H2S + H2 в интервале температур 280–420°С в течение 4 ч.
Исследование состава жидких продуктов и отдельных фракций проводили на хромато-масс-спектрометре 6890/5973N фирмы Agilent Technologies с неполярной хроматографической колонкой HP-5ms (ХМС). Для дополнительной очистки углеводородных фракций от полярных соединений применяли метод твердофазной экстракции (ТФЭ). Использовали патрон “Диапак С-16”, представляющий собой пластиковую колонку, содержащую 3 см3 герметично упакованного сорбента (гидрофобный сорбент с привитыми гексадецильными группами). Образец ЖП объемом 0.1 мл помещали в патрон и последовательно обрабатывали выбранными растворителями (бензол, ацетон).
Зольность исходного сапропеля и твердых остатков после гидроожижения (Аdaf) определяли по ГОСТ 11022–95 “Топливо твердое минеральное. Методы определения зольности”. Навеску образца сжигают в муфельной печи, нагретой до температуры (815 ± 10)°С, и выдерживают при этой температуры до постоянной массы. Зольность в процентах рассчитывают по массе остатка после прокаливания.
Элементный состав исследуемых образцов определяли на элементном анализаторе Vario El Cubе (содержание C, H, N, S).
Расчет t-критерия Стьюдента при сравнении средних величин проводили в соответствии с общепринятыми алгоритмами [15] и с использованием онлайн-калькулятора medstatistic.ru/calculators/averagestudent.html.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Среди современных методов анализа несомненным лидером при анализе сложных неразделенных смесей ОВ является ХМС. Однако применительно к образцам ЖП гидроожижения сапропеля без предварительного разделения данный метод оказался малоинформативным – в среднем хроматограмма такого образца содержала около 220 пиков, что не позволило провести идентификацию отдельных компонентов.
В качестве основных способов разделения смесей ОВ можно выделить: разделение по температурам кипения; по растворимости (с использованием методов осаждения или экстракции [12]), адсорбционные методы (твердофазная экстракция).
Для группового анализа ЖП переработки сапропелей применяется, как правило, методика Казакова, разработанная в 1953 г. [16]. Данная методика основана на последовательном осаждении определенных групп соединений вследствие разной растворимости классов соединений в различных растворителях. Для количественного определения содержания фенолов, карбоновых кислот, органических оснований и нейтральных кислородных соединений применяются, в основном, экстракционно-весовые методы [12]. К недостаткам указанных методов относятся их продолжительность, невозможность идентификации отдельных компонентов (количественно выделяются только определенные классы веществ), а также недостаточно четкое выделение групп компонентов.
В данной работе разделение по температурам кипения применительно к смеси ЖП гидроожижения сапропеля не дало существенных результатов – при отгонке удалось выделить всего две фракции – фракцию, кипящую до 220°С и маслянистый остаток. Первая фракция представляла собой растворитель (в данном случае декалин) со следовым содержанием продуктов его деструкции. Таким образом, нам удалось только удалить растворитель, тем самым сконцентрировав ЖП. Разделить сами ЖП, по-видимому, не позволило межмолекулярное взаимодействие между компонентами полученного продукта, либо содержание в смеси большого числа компонентов с близкими температурными интервалами кипения, что не позволило провести дробную конденсацию образовавшихся паров. Поскольку продукты деструкции ОВ сапропеля остались в “тяжелой” фракции, можно предположить, что основная масса ЖП представлена тяжелыми соединениями, возможно, конденсированными структурами, полиароматикой. Вероятно, в процессе деструкции ОВ сапропеля наряду с крекингом и гидрированием, также преобладают процессы полициклизации.
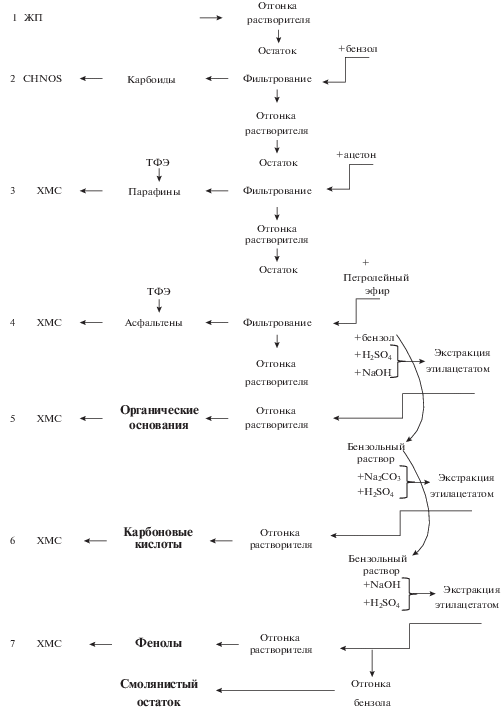
Поэтому после удаления растворителя была предложена методика, включающая разделение ЖП по растворимости (согласно методике Казакова и экстракционным методам выделения отдельных классов кислородсодержащих соединений), ТФЭ, анализ полученных групп методом ХМС. Предложенная схема исследования ЖП представлена на рис. 2.
На стадии (1) проводили вакуумную отгонку растворителя при температуре 180–200°С в случае использования декалина, и при 65–75°С при применении этанола. Остаток ЖП на стадии (2) растворяли в бензоле. Выделившиеся в виде твердого осадка карбоиды [5] отделяли фильтрованием и взвешивали после высушивания. Поскольку карбоиды – группа высокоассоциированных веществ, которые характеризуются полной нерастворимостью во всех органических растворителях, для более детального их анализа применяли элементный анализ (CHNOS-метод). Далее на стадии (3) отгоняли бензол под вакуумом, остаток растворяли в ацетоне. Твердый осадок – парафины [5] – отделяли фильтрованием, высушивали и взвешивали. Затем, на стадии (4), отгоняли ацетон, остаток растворяли в петролейном эфире. Выделившийся осадок – асфальтены – отделяли фильтрованием, высушивали и взвешивали. На следующем этапе (5) определяли содержание кислородсодержащих соединений. Для этого отгоняли петролейный эфир, остаток растворяли в пятикратном объеме бензола, дважды последовательно взбалтывали в делительной воронке с 10%-м водным раствором Н2SO4 в объемном соотношении 3 : 1. Сернокислый раствор отделяли и разлагали органические основания избытком NaOH. Выделившиеся в свободном виде органические основания извлекали этилацетатом (5 : 1), эфирную вытяжку отделяли, растворитель отгоняли, и остаток взвешивали. После удаления оснований бензольный раствор взбалтывали с 3%-м раствором бикарбоната натрия (3 : 1), затем обрабатывали избытком 10%-й H2SO4 (стадия (6)). Выделившиеся органические кислоты извлекали этилацетатом (5 : 1), отфильтровывали, и этилацетат отгоняли. Остаток в колбе высушивали до постоянного веса и взвешивали. Бензольный раствор со стадии (6) взбалтывали с 5%-м NaOH (3 : 1), а после разлагали избытком 10%-й H2SO4. Выделившиеся фенолы (7) извлекали этилацетатом (5 : 1), отфильтровывали и отгоняли растворитель. Содержание отдельных групп органических соединений в исследуемом образце рассчитывали по формуле:
Для более детального анализа и определения индивидуальных компонентов, выделенные группы соединений после взвешивания растворяли в растворителе с предыдущей ступени и анализировали методом ХМС. Углеводородные фракции перед анализом были дополнительно очищены от полярных соединений методом ТФЭ.
По предложенной схеме были проанализированы ЖП гидроожижения. Показано, что при использовании обоих типов катализаторов в составе ЖП, полученных при проведении процесса в этаноле (табл. 1), преобладают карбоиды и асфальтены, т.е. наиболее высокомолекулярные компоненты. Различия в средних значениях по критерию Стьюдента статистически значимы при уровне значимости 0.05.
Таблица 1.
Групповой состав жидких продуктов (растворитель этанол)
| Катализатор | Групповой состав, мас. % | ||||||
|---|---|---|---|---|---|---|---|
| парафины | асфальтены | карбоиды | карб. к-ты | орг. осн. | фенолы | неидент. остаток | |
| СоМо восст. | 6.56 ± 1.02 | 29.57 ± 4.12 | 43.89 ± 1.15 | 0.44 ± 0.21 | 0.24 ± 0.11 | 0.10 ± 0.02 | 19.2 ± 2.11 |
| СоМо осерн. | 3.27 ± 0.95 | 21.23 ± 5.01 | 71.97 ± 2.24 | 1.41 ± 0.18 | 1.20 ± 0.23 | 0.35 ± 0.11 | 0.57 ± 0.20 |
| FeNi восст. | 6.35 ± 1.29 | 26.87 ± 2.33 | 38.12 ± 2.11 | 1.65 ± 0.48 | 0.89 ± 0.22 | 0.24 ± 0.05 | 25.88 ± 5.11 |
| FeNi осерн. | 11.41 ± 2.55 | 30.30 ± 2.27 | 55.67 ± 4.32 | 0.87 ± 0.11 | 0.36 ± 0.09 | 0.25 ± 0.08 | 1.14 ± 0.93 |
В тех образцах, где активная форма катализатора – сульфидная, это преобладание существеннее, чем для восстановленных активных центров. Преобладание высокомолекулярных соединений можно объяснить тем, что в случае осерненного катализатора, наряду с крекингом связей ОВ, происходит и превращение растворителя с образованием высокомолекулярных продуктов. Возможно также, что радикалы, образующиеся при деструкции ОВ сапропеля, вступают в реакцию с продуктами превращения растворителей. Кроме того, интересен тот факт, что в составе жидких продуктов очень мало кислородсодержащих соединений, несмотря на то, что сам растворитель содержит кислород. По-видимому, в данном случае кислород и из растворителя, и из ОВ переходит в газообразные продукты. Как было показано ранее [4], кислород удаляется в виде СО2, NO2 и чистом молекулярном виде.
При анализе ЖП, полученных в декалине (табл. 2), установлено, что для образцов, полученных в высокомолекулярном растворителе, преобладание тяжелых УВ не столь существенно, хотя и статистически значимо. Здесь можно отметить значительное количество парафинов и, что более интересно, большое количество кислородсодержащих соединений, чего не наблюдалось в случае растворителя этанола. Можно предположить, что при использовании декалина механизм деструкции ОВ отличается от предыдущего случая и кислород, выделенный из органической массы, взаимодействует с углеводородными радикалами и остается в составе ЖП.
Таблица 2.
Групповой состав жидких продуктов (растворитель декалин)
| Ката- лизатор |
Групповой состав, мас. % | ||||||
|---|---|---|---|---|---|---|---|
| парафины | асфальтены | карбоиды | карб. к-ты | орг. осн. | фенолы | неидент. остаток | |
| СоМо восст. | 12.01 ± 4.30 | 36.67 ± 5.84 | 18.16 ± 3.18 | 3.28 ± 1.31 | 14.61 ± 6.21 | 0.15 ± 0.07 | 15.12 ± 1.96 |
| СоМо осерн. | 8.72 ± 2.41 | 21.71 ± 4.29 | 37.76 ± 5.36 | 5.47 ± 1.87 | 1.14 ± 0.93 | 0.56 ± 0.11 | 24.64 ± 5.12 |
| FeNi восст. | 8.62 ± 1.21 | 41.06 ± 4.88 | 16.92 ± 5.11 | 1.53 ± 0.52 | 8.08 ± 1.14 | 1.43 ± 0.53 | 22.36 ± 3.18 |
| FeNi осерн. | 8.89 ± 2.18 | 24.34 ± 2.11 | 41.31 ± 7.02 | 12.71 ± 4.12 | 0.8 ± 0.09 | 0.41 ± 0.04 | 11.54 ± 1.25 |
Здесь можно отметить значительное количество парафинов и, что более интересно, большое количество кислородсодержащих соединений, чего не наблюдалось в случае растворителя этанола. Можно предположить, что при использовании декалина механизм деструкции ОВ отличается от предыдущего случая и кислород, выделенный из органической массы, взаимодействует с углеводородными радикалами и остается в составе ЖП.
Интересно влияние природы катализатора и состояния активного центра на состав жидких продуктов. Если на содержание углеводородных фракций это влияние не столь велико (за исключением увеличения содержания карбоидов при использовании осерненных катализаторов в обоих случаях и требует дополнительных исследований), то нельзя не отметить изменений в содержании кислородсодержащих соединений. Так, например, при использовании декалина для обеих каталитических систем в осерненной форме наблюдается значительное количество карбоновых кислот, а в случае восстановленных катализаторов – преобладают органические основания.
На следующем этапе отдельные фракции веществ, выделенные из ЖП гидроожижения, были проанализированы различными аналитическими методами. Для карбоидов, которые не растворяются в органических растворителях, определен элементный состав и показано, что они представляют собой смесь высокомолекулярных соединений с соотношением С/Н 11.1–10.7 и содержанием кислорода, не превышающим 9 мас. %. Другие фракции анализировали методом ХМС.
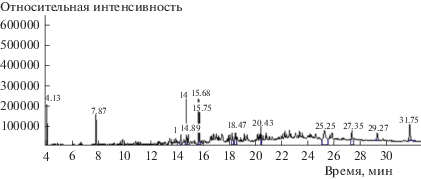
В качестве примера на рис. 3 приведена хроматограмма бензольного раствора УВ стадии (3) (в данном случае гидроожижение проводили с использованием декалина и СоМо осерненного катализатора). Несмотря на то, что на данном этапе предполагается выделение УВ, согласно данным ХМС-анализа, наиболее интенсивные пики на данной хроматограмме – замещенные фенолы (tуд = 14.74 –15.75 мин).
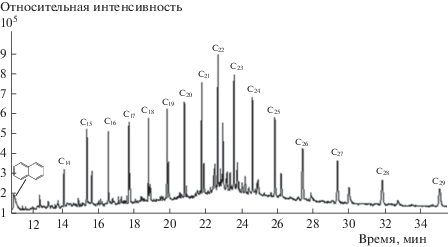
Методом ХМС достоверно удалось идентифицировать УВ от С5 до С29. При этом преобладающими являются циклопентан, тридекан, пента-, гекса-, гептадекан, эйкозан, трикозан (как линейного строения, так и их изомеры), ряд диенов. Их суммарное содержание в смеси составляет 41.59 мас.%, остальное приходится на продукты превращения декалина, растворитель, в данном случае бензол, и ряд неидентифицированных соединений с очень низким содержанием. После удаления полярных соединений методом ТФЭ удалось улучшить идентификацию индивидуальных компонентов парафиновой фракции (рис. 4) – УВ от С14 до С29, включая изомеры (преимущественно от С21 до С26).
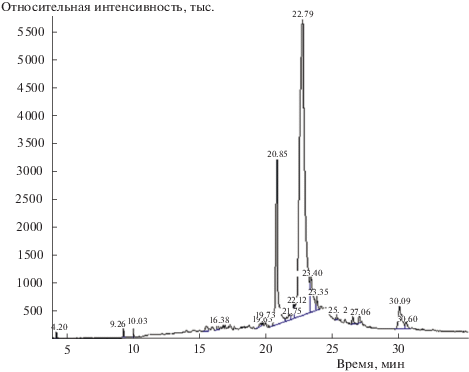
При анализе кислородсодержащих фракций (стадии 5–7, осадок растворяли в этилацетате) удалось идентифицировать ряд карбоновых кислот от С2 до С16 и их соли, гликоли, замещенные ксилолы, короткоцепочечные альдегиды, высокомолекулярные спирты (С14 –С18). Для примера на рис. 5 представлена хроматограмма органических кислот (стадия 6). Компоненты с максимальным содержанием – гексадекановая (tуд = = 20.85 мин) и олеиновая (tуд = 22.79 мин) кислоты.
В данной работе остался неясным один важный момент – ни на одном из этапов анализа нам не удалось достоверно идентифицировать и количественно определить азотсодержащие соединения, хотя в исходном сапропеле содержание азота около 13%, а по данным элементного анализа в ЖП содержится примерно 5.5% азота. Данный вопрос требует дальнейшего изучения.
Таким образом, предложен подход, позволяющий не только разделить ЖП гидроожижения сапропеля по групповому составу, но и идентифицировать значительную часть индивидуальных компонентов.
Показано, что при использовании этанола в качестве растворителя, в составе ЖП преобладают карбоиды и асфальтены, а при применении декалина наблюдается увеличение содержания парафинов и кислородсодержащих соединений. Влияние природы катализатора и состояния активного центра на состав не столь существенно, за исключением преобладания карбоидов при применении осерненных каталитических систем.
В выбранных условиях конверсия ОВ не очень глубокая и выход ЖП небольшой, что затрудняет точность разделения смеси и анализ отдельных компонентов; необходима оптимизация условий проведения процесса с целью его интенсификации. Предложенные подходы будут в дальнейшем применены к анализу продуктов гидроожижения сапропелей (с большей конверсией ОВ) для более точного и детального определения их компонентного состава.
Физико-химические исследования исходных материалов и опытных образцов проведены с использованием приборной базы Омского регионального центра коллективного пользования СО РАН, г. Омск. Авторы выражают благодарность сотруднику лаборатории аналитических и физико-химических методов исследования ИППУ СО РАН Е.Н. Кудря за проведение хромато-масс-спектрометрии.
Работа выполнена в рамках государственного задания ИППУ СО РАН в соответствии с Программой фундаментальных научных исследований государственных академий наук на 2013–2020 годы по направлению V.46, проект № V.46.4.4, этап 2 (номер госрегистрации в системе ЕГИСУ НИОКТР AAAA-A17-117021450098-2).
Список литературы
Добрецов В.Б. Сапропели России: освоение, использование, экология. СПб.: ГИОРД, 2005. 200 с.
Гонцов А.А. Минеральное сырье. Сапропели. М.: ЗАО “Геоинформмарк”, 1997. 20 с.
Кирейчева Л.В. Сапропели: состав, свойства, применение. М.: Изд-во “РОМА”, 1998. 120 с.
Кривонос О.И., Терехова Е.Н., Плаксин Г.В., Лавренов А.В. // Химия и технология топлив и масел. 2016. № 1. С. 3.
Казаков Е.И., Покровская Л.С., Любимова З.В. // Химия твердого топлива. 1973. № 5. С. 33.
Sunggyu Lee, Shah Y.T. Biofuels and Bioenergy: Processes and Technologies. Taylor & Francis Group. 2012. 341 p.
Trautmann M., Lang S., Traa Y. // Fuel. 2015. V. 151. P. 102.
Zhiping L., Lijuan G., Hengfu Sh., Weilai Chen, Zhicai Wang, Shibiao Ren. // Fuel Proces. Technol. 2011. V. 92. P. 2055.
Шарыпов В.И., Кузнецов Б.Н., Береговцова Н.Г., Васильева Н.Ю., Соколенко В.А., Павленко Н.И., Старцев А.Н., Пармон В.Н. // Химия в интересах устойчивого развития. 2006. Т. 14. № 1. С. 73.
Кузнецов Б.Н., Тарабанько В.Е., Черняк М.Ю., Береговцова Н.Г., Шарыпов В.И., Милошенко Т.П., Плаксин Г.В. // Химия растительного сырья. 2004. № 1. С. 35.
Шарыпов В.И., Береговцова Н.Г., Барышников С.В., Таран О.П., Страховенко В.Д., Кузнецов Б.Н. // Химия растительного сырья. 2013. Т. 4. С. 213.
Тутурина В.В., Семенова З.В., Евстафьев С.Н. // Химия твердого топлива. 1981. № 1. С. 105.
Мусина Г.Н. // Наука и мир. 2014. Т. 2. № 11 (15). С. 12.
Kleinert M., Barth T. // Energy & Fuels. 2008. № 22. P. 1371.
Вершинин В.И., Перцев Н.В., Планирование и математическая обработка результатов химического эксперимента. Изд-во ОмГУ, 2005. 216 с.
Казаков Е.И. Методика изучения сапропелевых отложений. М., 1953. 49 с.
Дополнительные материалы отсутствуют.
Инструменты
Нефтехимия